一种新冠病毒sars-cov-2的双特异性抗体及应用
技术领域
1.本发明属于抗体研究技术领域,具体涉及一种新冠病毒sars-cov-2的双特异性抗体及应用。
背景技术:
2.噬菌体抗体库技术(phage antibody library)是近年发展的一项分子生物学新技术,近年来越来越多的学者利用这项技术获得目标抗体以应用于医疗制药及安全检测等多个领域。噬菌体抗体库技术的发展和应用,为抗体技术领域带来了巨大的变化,极大地推动了各种性能优良基因工程抗体的开发和应用。获得大容量的抗体库是筛选获得特异性抗体的前提条件。
3.新冠病毒被世界卫生组织命名为严重急性呼吸系统综合征冠状病毒2型(sars-cov-2)。新冠病毒为β属的新型冠状病毒,有包膜,颗粒呈圆形或椭圆形,常为多形性,直径为60-140nm。全基因组比对发现新型冠状病毒与严重急性呼吸系统综合征病毒(sars-cov)同源性达到70%,序列差异主要体现在与宿主细胞作用的关键spike基因(编码s-蛋白)。
4.严重急性呼吸系统综合征冠状病毒2型(sars-cov-2)变异的出现威胁到现有疫苗和治疗性抗体的有效性,并强调需要额外的基于抗体的工具,通过靶向刺突蛋白的多个位点可有效的中和变异毒株。我们从covid-19患者的单个核细胞(pbmc)中分离出了多个针对sars-cov-2的单克隆抗体。双特异性抗体是一种人工制备的可以同时结合两种不同抗原或同一抗原不同位点的特殊抗体。将靶向sars-cov-2病毒上两个位点的天然抗体连接在一起,制备一种同时靶向两个独立的病毒位点的双特异性抗体,可体现了单个分子中鸡尾酒的优势,并更有效的针对这种病毒变体导致的治疗抵抗,阻断新冠病毒感染人体细胞, 从而解决这个问题。
技术实现要素:
5.本发明通过结合非重叠的特异性设计了双特异性抗体,提供了一种可有效抑制sars-cov-2感染的双特异性抗体,能够在制备诊断或治疗新型冠状病毒引起的疾病的试剂或药物中应用。
6.为实现上述目的,本发明采用的技术方案为:一种新冠病毒sars-cov-2的双特异性抗体,包括第一重链和第二重链,所述第一重链的可变区氨基酸序列为seq id no:1,所述第二重链的可变区氨基酸序列为seq id no:3。
7.进一步,所述新冠病毒sars-cov-2的双特异性抗体还包括第一轻链和第二轻链,所述第一轻链的可变区氨基酸序列为seq id no:2,所述第二轻链的可变区氨基酸序列为seq id no:4。
8.进一步,所述新冠病毒sars-cov-2的双特异性抗体的第一重链的可变区识别s蛋白rbd结构域氨基酸位点ser447、glu484、val445、gly446、lys444中的一种,第二重链的可
变区识别s蛋白rbd结构域氨基酸位点thr333、leu335、glu340、thr345、asn440中的一种。
9.进一步,所述新冠病毒sars-cov-2的双特异性抗体能够与新冠病毒sars-cov-2s蛋白特异性结合。
10.一种新冠病毒sars-cov-2的双特异性抗体在制备诊断或治疗新型冠状病毒引起的疾病的试剂或药物中的应用。
11.与现有技术相比,本发明的有益效果为:本发明通过结合非重叠的特异性设计了双特异性抗体,提供了一种可有效抑制sars-cov-2感染的双特异性抗体,亲和力高,能够与新冠病毒sars-cov-2s蛋白特异性结合,能够在制备诊断或治疗新型冠状病毒引起的疾病的试剂或药物中应用。
附图说明
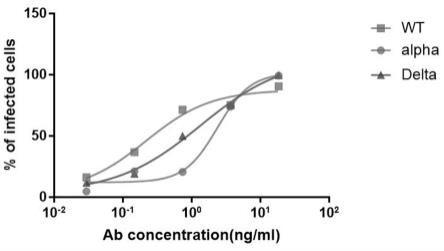
12.图1为本发明新冠病毒sars-cov-2的特异性中和抗体的抑制曲线。
具体实施方式
13.下面结合附图和具体的实施例对本发明的技术方案及效果做进一步描述,但本发明的保护范围并不限于此。
14.实施例1一种新冠病毒sars-cov-2的双特异性抗体,包括第一重链和第二重链,所述第一重链的可变区氨基酸序列为seq id no:1,evqlvqsggglvqpggslrlscaasgitvnsnymswvrqapgkglewvsiiysggstyytdsvkgrftisrdnskntlylqmnslraedtavyycarsygdyyfdywgqgtlvtvss;所述第二重链的可变区氨基酸序列为seq id no:3,qitlkesggglvqtgrslrlscaasgftfddyamhwvrqapgkglewvsgsswnsgtigyadsvkgrftisrdnaknslylqmnslraedtalyycakdirqkyydistgyykygeqdygmdvwgqgtlvtvss。
15.进一步,所述新冠病毒sars-cov-2的双特异性抗体还包括第一轻链和第二轻链,所述第一轻链的可变区氨基酸序列为seq id no:2,diqmtqspsslsasvgdrvtitcqasqdirnylnwyqqkpgrapdllifdasdletgvpsrfsgsgsgtdftftisslqpedigtyycqqygnlpltfgggtkveik;所述第二轻链的可变区氨基酸序列为seq id no:4,qavltqpasvsgspgqsitisctgtssdvgaynyvswyqhhpgkapelmiydvtkrpaglpnrfsgsksgntasltisglqaedeasyycssyttsstvifgggtkltvl。
16.所述新冠病毒sars-cov-2的双特异性抗体fab第一重链氨基酸序列为seq id no:5,evqlvqsggglvqpggslrlscaasgitvnsnymswvrqapgkglewvsiiysggstyytdsvkgrftisrdnskntlylqmnslraedtavyycarsygdyyfdywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkt;fab第一轻链氨基酸序列为seq id no:6,diqmtqspsslsasvgdrvtitcqasqdirnylnwyqqkpgrapdllifdasdletgvpsrfsgsgsg
tdftftisslqpedigtyycqqygnlpltfgggtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec;fab第二重链氨基酸序列为seq id no:7,qitlkesggglvqtgrslrlscaasgftfddyamhwvrqapgkglewvsgsswnsgtigyadsvkgrftisrdnaknslylqmnslraedtalyycakdirqkyydistgyykygeqdygmdvwgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkt;fab第二轻链氨基酸序列为seq id no:8,qavltqpasvsgspgqsitisctgtssdvgaynyvswyqhhpgkapelmiydvtkrpaglpnrfsgsksgntasltisglqaedeasyycssyttsstvifgggtkltvlgqpkaapsvtlfppsseelqankatlvclisdfypgavtvawkadsspvkagvetttpskqsnnkyaassylsltpeqwkshrsyscqvthegstvektvaptecs。
17.进一步,所述新冠病毒sars-cov-2的双特异性抗体的第一重链的可变区识别s蛋白rbd结构域氨基酸位点ser447、glu484、val445、gly446、lys444中的一种,第二重链的可变区识别s蛋白rbd结构域氨基酸位点thr333、leu335、glu340、thr345、asn440中的一种。
18.一种新冠病毒sars-cov-2的双特异性抗体在制备诊断或治疗新型冠状病毒引起的疾病的试剂或药物中的应用。
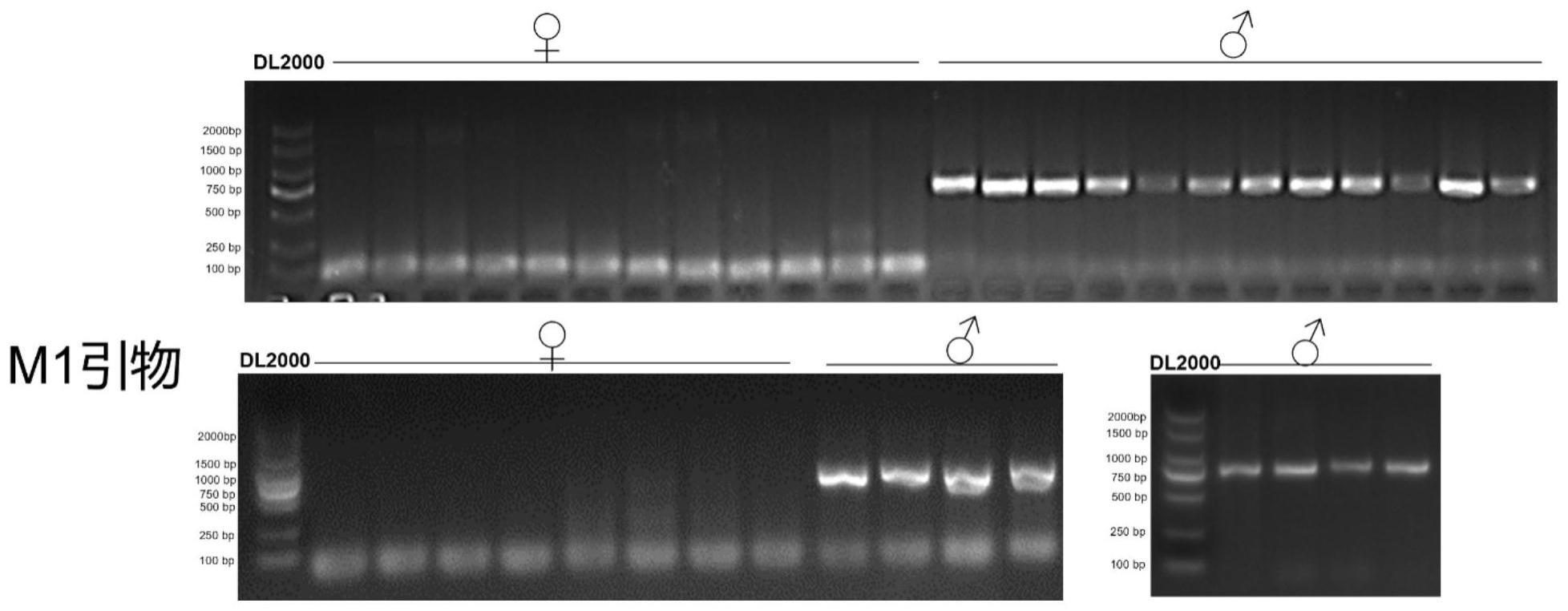
19.实施例2本发明新冠病毒sars-cov-2的双特异性抗体的制备方法包括以下步骤:1、获取免疫材料总rna/mrna从新型冠状病毒感染康复者的外周血淋巴细胞提取总rna,并且进一步从rna分离mrna(takara cat#z652n/636592,具体实验步骤参见产品说明书)。
20.2、设计合成引物针对人全套抗体的引物均按照v-base网站(http://vbase.mrc-cpe.cam.ac.uk/)中提供的人全套抗体基因序列信息设计人全套抗体的引物,引物由金唯智公司合成。引物在h2o中溶解为 100 pmol/μl,并保存于
ꢀ‑
20℃。
21.3、cdna第一链的合成及全套igg1轻链全长基因和重链可变区基因的扩增通过两步法扩增组件抗体基因库:1、以获得的mrna为模板,用promega的mmlv进行逆转录合成 cdna (按照promega公司产品的说明书进行,其中引物为thermocat#n8080127、逆转录酶为 promega cat# m1701);2、以第一步获得的cdna为模板,利用2中设计的引物,通过pcr(takara cat# rr900a,按照公司产品的说明书进行)扩增组件抗体的klc, llc和vh基因库。凝胶电泳纯化回收后(利用莱枫的凝胶回收试剂盒,按照《分子克隆实验指南》中的记载操作)分别获得pcr产物——klc片段、llc片段和vh片段。
22.4、构建fab噬菌体展示文库通过t4连接酶连接目的片段与载体,构建fab噬菌体展示文库。根据在带有氨苄青霉素抗性的lb平皿上长出的细菌克隆数,计算所构建的fab噬菌体表面展示噬菌体文库原始库容量为1.44
×
108。从抗体fab噬菌体文库中随机挑选10个单克隆进行序列测定,结果表明有6个不同的轻重链基因编码序列组合,多样性为60%,即8.64
×
107。
23.5、特异性抗体筛选用生物素标记的sars-cov-2 s1抗原结合亲和素标记磁珠吸附的液相筛选法筛选
抗原特异性fab。四轮液相筛选抗原浓度分别为10ug/ml、1ug/ml、1ug/ml、1ug/ml。仅第一轮筛选洗脱收集的噬菌体,经扩增后用于第二轮筛选。第二、三轮筛选洗脱收集的噬菌体均不经扩增直接用于后续筛选过程。
24.三、四轮筛选洗脱收集的噬菌体,侵染tg1细菌,铺氨苄青霉素平皿,37℃培养过夜。次日,从每个抗原特异性平皿挑单克隆培养扩增,并加iptg(终浓度为1nm)诱导过夜。通过elisa分析培养液中的抗原特异性fab。elisa读数大于最低elisa读数两倍的克隆记为阳性克隆。挑合适个数的阳性克隆进行测序分析,获得elisa读数较高的独特的氨基酸序列。
25.6、通过中和试验筛选获得sars-cov-2 特异性中和抗体将待测抗体样品和阳性对照抗体(金斯瑞)与hrp-rbd预孵育,使中和抗体与hrp-rbd结合。然后将混合物添加到预包被有hace2蛋白的捕获板中。未结合的hrp-rbd以及与非中和抗体结合的hrp-rbd将被捕获在平板上,而与中和抗体结合的hrp-rbd-中和抗体复合物在上清中并在洗涤过程中洗弃。洗涤步骤结束后,加入tmb溶液,使其变为蓝色。加入停止溶液,反应淬灭,颜色变黄色。在450nm处读板,样品的吸光度与抗sars-cov-2 中和抗体的滴度成反比。
26.最终获得2个sars-cov-2 特异性中和抗体。以临界值(cut-off):信号值抑制率=20%计算,抗体s82信号值抑制率为71.4%,ec50为0.03ug/ml;抗体s126信号值抑制率为58%,ec50为0.02ug/ml。
27.7、双特异性抗体表达以包含单克隆抗体的质粒为模板,用相应的限制性内切酶酶切获得抗体的轻链和重链可变区分子片段,通过常规分子生物学方法,添加n端信号肽和c端6
×
his tag,并将分子片段插入哺乳动物表达载体pcdna3.1( )中。双特异性抗体分子是通过转染expi 293f
™
细胞制备产生,转染6天后,收细胞上清,并通过hiload superdex柱纯化回收抗体。所有抗体都进行了质量控制和表征分析,评估稳定性和可重复性。
28.8、假病毒中和试验验证中和活性构建带有荧光素酶(luc)或绿色荧光蛋白(gfp)报告基因,过表达ace2的质粒,稳定转染293t细胞株。将4倍连续稀释的抗体与sars-cov-2假病毒在37℃下孵育1小时。该混合物随后与293t细胞共孵育48h;用pbs洗涤两次后,裂解细胞。使用荧光素酶检测系统测量裂解液中的荧光素酶活性。
29.本发明新冠病毒sars-cov-2的双特异性中和抗体的抑制曲线如图1所示。结果示,双特异性抗体针对新型冠状病毒wt, 变异毒株alpha和delta的半抑制浓度(ic50)分别为 0.4505 ng/ml、0.1822 ng/ml和0.2349 ng/ml。
30.尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。