1.本发明涉及优化单克隆抗体的序列以增强其生物物理特性的方法,该生物物理特性包括针对优化的制造的热力学稳定性、体内行为和更长的保质期。
背景技术:
2.抗体是由免疫系统产生的保护性应答,通常在暴露于抗原后触发。尽管在抗原暴露后的初级应答中产生的抗体具有较低的亲和力,但已知亲和力可通过称为体细胞免疫球蛋白(ig)超突变的过程得到改善(neuberger,m.s.&milstein,c.somatic hypermutation.current opinion in immunology 7,248-254(1995))。该过程涉及免疫球蛋白基因片段的几轮重组;可变(v)、多样性(d)和连接(j)以及导致抗体对抗原具有非常强的亲和力和高选择性的抗体的互补决定区(cdr)中突变集合的积累(sun,s.b.等人,mutational analysis of 48g7 reveals that somatic hypermutation affects both antibody stability and binding affinity,journal of the american chemical society 135,9980-9983(2013);作者根据重复数据撤回)。虽然这些积累的突变中的大多数存在于cdr中并且对于与抗原的高亲和力相互作用至关重要,但是一些其他突变遍布于可变区中并且不参与直接抗原结合并且因此对抗体亲和力没有贡献(wang,f.等人,somatic hypermutation maintains antibody thermodynamic stability during affinity maturation.proceedings of the national academy of sciences of the united states of america 110,4261-4266(2013);作者根据重复数据撤回)。cdr(通常也称为超变区)是形成抗体抗原识别位点的重链和轻链两者的可变区中的环。它们的构象由环的长度和组成限定。框架(fr)区是排列为两个β-折叠的反平行β-链,这两个β-折叠负责维持可变结构域的结构完整性并充当cdr的结构支架。fr对于结构多样性、vl/vh取向很重要,并且也可以直接参与抗原结合(sela-culang,i.等人,the structural basis of antibody-antigen recognition.frontiers in immunology 4(2013))。在亲和力成熟期间发生在cdr中的亲和力突变可能对抗体稳定性产生有害影响。最近已经证明,位于整个可变区的中性体细胞超突变通常补偿由亲和力突变引起的对抗体稳定性的不利影响(sun,s.b.等人,mutational analysis of 48g7 reveals that somatic hypermutation affects both antibody stability and binding affinity.journal of the american chemical society 135,9980-9983(2013))。抗体支架的亲和力与稳定性之间的这种强烈协调也已经在定向进化研究中得到证明,其中在cdr内或框架区中的亲和力成熟过程期间获得的突变可以是功能性的并且同时是不稳定的(houlihan,g.,gatti-lafranconi,p.,lowe,d.&hollfelder,f.directed evolution of anti-her2 darpins by snap display reveals stability/function trade-offs in the selection process.protein engineering,design &selection:peds 28,269-279(2015);julian,m.c.等人,co-evolution of affinity and stability of grafted amyloid-motif domain antibodies.protein engineering,design&selection:peds 28,339-350(2015))。
3.抗体和相关产品是增长最快的一类治疗剂。治疗性抗体必须表现出有利的药学特性,包括高热稳定性和低聚集倾向,以便促进制造和储存,以及延长血清半衰期。只有具有有利的生物物理特性(包括构象和胶体稳定性)的功能活性分子才可以成为药物。(jain,t.等人,biophysical properties of the clinical-stage antibody landscape.proceedings of the national academy of sciences of the united states of america 114,944-949(2017))。抗体的构象稳定性例如由较高的热稳定性和较低的聚集倾向决定。热稳定性从抗体表达、纯化、配制和保质期开始,在药物发现中起着关键作用(goswami,s.,wang,w.,arakawa,t.&ohtake,s.developments and challenges for mab-based therapeutics.antibodies 2,452-500(2013))。高通量自动筛选测定对于确定构象稳定性和在开发早期对数百个命中进行排序至关重要。增强的热稳定性是获得最佳药代动力学和药效学特性以及更长的保质期和储存的关键(thiagarajan,g.,semple,a.,james,j.k.,cheung,j.k.&shameem,m.a comparison of biophysical characterization techniques in predicting monoclonal antibody stability.mabs 8,1088-1097(2016))。已经一致地观察到,体外亲和力成熟的抗体比它们的亲本抗体热稳定性低。通常需要通过将cdr移植到稳定框架上、哺乳动物细胞展示和体外体细胞超突变(shm)的组合来进一步优化,以改善抗体的稳定性(mcconnell,a.d.等人,a general approach to antibody thermostabilization.mabs 6,1274-1282(2014))。
4.预防不良副作用对于患者的安全和生物治疗候选药物的成功至关重要。最重要的是在抗体候选药物的最早开发阶段评估预期的免疫原性并消除潜在的副作用。由于fda要求进行严格的临床前风险评估,因此开发了不同的方法来评估和降低预期的免疫原性。
5.抗体工程技术是发现和开发生物治疗药物的关键。将从非人物种发现的抗体人源化以克服和降低免疫原性的风险。来自非人物种的抗体的人源化已成功应用于优化mab的临床开发。人源化抗体占目前fda批准的89种抗体的约43%(即38种mab)。完全人抗体越来越普遍,并且在临床上mab比例越来越大。它们源自经人源化体液免疫系统遗传工程化的转基因动物,诸如和迄今为止,已经批准了21种从转基因动物获得的完全人mab,这相当于所有市售mab的24%。从转基因动物获得的一些抗体序列在框架区和cdr区中含有体细胞超突变。体细胞超突变可能会导致人框架区中出现异常或低频残基,并影响生物治疗药物的稳定性和免疫原性。
6.产生具有长保质期和低免疫原性的稳定抗体仍然具有挑战性,并且通常是一个漫长而痛苦的过程。
技术实现要素:
7.在某些实施方案中,本发明提供了一种设计优化抗体的方法,该方法包括:
8.a)识别用于优化的抗体;
9.b)识别所述抗体vh和/或vl中的一个或多个异常或低频残基;
10.c)将所述抗体vh和/或vl序列与最接近的人和非人种系序列进行比对;
11.d)识别所述抗体vh、vl或两者中的一个或多个体细胞超突变位点;
12.e)识别通常在所述体细胞超突变位点中的位点处观察到的一个或多个种系残基;
13.f)设计并工程化在所述体细胞超突变位点中的位点处含有所述种系残基的变体
或变体库;
14.g)评估所述变体或变体库的特性;以及
15.h)选择一个或多个优化变体,
16.其中所述一个或多个优化变体具有改善的生物物理特性、降低的免疫原性风险或两者。
17.在其他某些实施方案中,本发明提供了一种设计优化抗体的方法,该方法包括:
18.a)识别用于优化的抗体;
19.b)识别所述抗体vh和/或vl中的一个或多个异常或低频残基;
20.c)将所述抗体vh和/或vl序列与最接近的人和非人种系序列进行比对;
21.d)识别所述抗体vh、vl或两者中的一个或多个体细胞超突变位点;
22.e)识别通常在所述体细胞超突变位点中的位点处观察到的一个或多个种系残基;
23.f)设计并工程化在所述体细胞超突变位点中的位点处含有所述种系残基的变体或变体库;
24.g)克隆并生产所述变体或变体库;
25.h)评估所述变体或变体库的生物物理特性;
26.i)评估所述变体或变体库的免疫原性风险;以及
27..j)选择一个或多个优化变体,
28.其中所述一个或多个最佳优化变体具有改善的生物物理特性、降低的免疫原性风险或两者。
29.在某些实施方案中,异常或低频残基的识别例如通过基于计算机的软件(诸如但不限于abysis)来完成。
30.在某些实施方案中,生物物理评估通过例如分析超速离心、热稳定性、解折叠自由能或分析尺寸排阻来完成。
31.在某些实施方案中,免疫原性风险评估例如在计算机上进行,诸如通过评分。
32.在某些实施方案中,氨基酸替换可以发生在例如四个fr中的任何一个或多个fr中。在这方面,氨基酸替换可以发生在重链或轻链的fr1、fr2、fr3和/或fr4中。在其他某些实施方案中,一个或多个氨基酸残基可以用种系残基替换,只要氨基酸替换改善优化抗体的生物物理特性。
33.在一些其他实施方案中,氨基酸替换可以发生在例如cdr中的任何一个或多个cdr中。在这方面,氨基酸替换可以发生在重链或轻链的cdr1、cdr2和/或cdr3中。在其他某些实施方案中,一个或多个氨基酸残基可以用种系残基替换,只要氨基酸替换改善优化抗体的生物物理特性。
34.在其他实施方案中,本发明不限于包含抗体重链多肽或轻链多肽的分离的抗原结合剂。实际上,由体细胞超突变产生的框架的任何氨基酸残基可以任何组合被种系氨基酸残基替换,只要抗原结合剂的稳定性由于氨基酸替换而增强或改善,而不伴随生物活性的丧失。
附图说明
35.图1a示出了tmeb675与人种系序列的vh序列比对以及异常或低频残基的识别。在框架区内观察到vh中的三个体细胞超突变(shm)(r14p、p20l、h81q)。
36.图1b示出了tmeb675与人种系序列的vk序列比对以及异常或低频残基的识别。在框架区中观察到一个体细胞超突变(shm)(a1d),并且在cdr3中观察到一个体细胞超突变(a91p)。
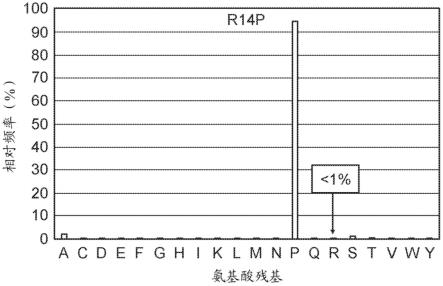
37.图2a示出了使用abysis门户对tmeb675 vh的位置14处的shm精氨酸(r)的相对频率的评估。
38.图2b示出了使用abysis门户对tmeb675 vh的位置20处的shm脯氨酸(p)的相对频率的评估。
39.图2c示出了使用abysis门户对tmeb675 vh的位置81处的shm组氨酸(h)的相对频率的评估。
40.图2d示出了使用abysis门户对tmeb675 vl的位置1处的shm丙氨酸(a)的相对频率的评估。
41.图2e示出了使用abysis门户对tmeb675vl的位置91处的shm丙氨酸(a)的相对频率的评估。
42.图3示出了tmeb675的分子同源性模型。在框架区中发现的shm残基在棒形表示中标记并突出显示。
43.图4示出了tmeb675和tmeb762两者通过分析超速离心的归一化g(s*)沉降速度运行。由sedanal v697进行全局拟合分析,并将数据全局拟合至两个物种,非相互作用模型。
44.图5示出了使用差示扫描荧光法(dsf)的tmeb675和tmeb762的固有特性表征。将350/330nm比率的一阶导数强度对温度(℃)作图。
45.图6示出了使用差示扫描量热法(dsc)的tmeb675和tmeb762的固有特性表征。将热容量cp(cal/mol/℃)对温度(℃)作图。
46.图7示出了使用通过荧光强度比率350/330nm的变化监测的gdncl等温化学变性的tmeb675的固有特性表征。
47.图8示出了使用通过荧光强度比率350/330nm的变化监测的gdncl等温化学变性的tmeb762的固有特性表征。
48.图9示出了tmeb762和tmeb675在一个月内的储存(4℃)和加速(40℃)稳定性。将时间零与1个月之间的聚集体水平变化对天数作图。
49.图10示出了tmeb762和tmeb675的非特异性结合数据,其通过将相对结合应答单位对不同表面作图而由表面等离子体共振法测定。
50.图11示出了优化算法工作流程。
51.图12示出了psmw56、人种系ighv4-39*01和psmw57的重链(vh)的序列比对。位置68处的罕见的体细胞超突变(苏氨酸变为异亮氨酸)以粗体突出显示。psmw57是psmw56的工程化变体。ile68种系化为苏氨酸。
52.图13示出了位置68处的异常或低频框架残基(ile)。将该残基再工程化为thr残基。thr的选择基于种系残基(ighv4-39*01)。
53.图14示出了使用差示扫描荧光法(dsf)的psmw56和psmw57的固有特性表征。与亲
本变体psmw56相比,工程化变体psmw57示出显著改善的tm和tagg。
54.图15a示出了dl3b355重链与人种系(ighv3-13*05)和工程化变体dl3b355-1、dl3b355-2和dl3b355-3的序列比对。hcdr1、hcdr2和hcdr3序列用下划线标出。位置85处的罕见的体细胞超突变(组氨酸)以粗体突出显示。
55.图15b示出了dl3b355轻链与人种系(igkv1-5*03)和工程化变体dl3b355-1、dl3b355-2和dl3b355-3的序列比对。lcdr1、lcdr2和lcdr3序列用下划线标出。位置84处的罕见的体细胞超突变(glu)以粗体突出显示。
56.图16a示出了在dl3b355的重链位置85处的异常或低频框架残基。将该残基再工程化以与相应的种系残基(天冬酰胺)匹配。
57.图16b示出了在dl3b355的轻链位置84处的异常或低频框架残基。将该残基再工程化以与相应的种系残基(甘氨酸)匹配。
58.图17示出了使用差示扫描荧光法(dsf)的dl3b355和dll3变体的固有特性表征。与亲本克隆相比,所有三个工程化的dl3b355变体都示出改善的热稳定性(tm和tagg)。
具体实施方式
59.当结合附图阅读时,将更好地理解前述发明内容以及以下对本技术的实施方案的详细描述。但是,应当理解,本专利申请不限于附图中示出的精确实施方案。
60.本说明书中包括的对文件、行为、材料、装置、文章等的讨论旨在为本发明提供上下文。这样的讨论并不承认任何或所有这些内容构成现有技术的一部分或限制任何公开或要求保护的发明。
61.除非另有明确说明,否则在整个说明书中,抗体恒定区的氨基酸残基根据eu索引编号,如kabat等人,sequences of proteins of immunological interest,第5版,public health service,national institutes of health,bethesda,md.(1991)中描述的。
62.应当了解,本文所用的术语只是为了描述具体实施方案的目的,并非旨在进行限制。除非另有定义,否则本文使用的所有技术和科学术语的含义与本发明所属领域的普通技术人员通常所理解的含义相同。虽然与本文所述的那些方法和材料相似或等效的任意方法和材料都可以用于检验本发明的实践中,然而本文中描述示例性材料和方法。在描述和要求保护本发明时,将使用以下术语。
63.如本说明书和所附权利要求中所用,除非内容另有明确说明,否则单数形式
″
一个
″
、
″
一种
″
和
″
所述
″
包括复数指代。因此,例如,对
″
一个细胞
″
的提及包括两个或更多个细胞的组合等等。
64.过渡术语
″
包括
″
、
″
基本上由......组成
″
和
″
由......组成
″
旨在暗示它们在专利用语中的公认含义;即,(i)
″
包括
″
与
″
包含
″
、
″
含有
″
或
″
其特征在于
″
同义,并且是包括端值在内或末端开放的,并且不排除附加的、未列出的要素或方法步骤;(ii)
″
由......组成
″
排除权利要求书未指定的任何要素、步骤或成分;以及(iii)
″
基本上由......组成
″
将权利要求的范围限制于指定的材料或步骤
″
以及本质上不影响受权利要求书保护的发明的基本及新颖特征的材料或步骤
″
。还提供了以短语
″
包括
″
(或其等同形式)描述的实施方案,如以
″
由......组成
″
和
″
基本上由......组成
″
独立描述的那些实施方案。
65.如本文所用,多个列举的要素之间的连接术语
″
和/或
″
被理解为涵盖单个选项和
组合选项两者。例如,在两个要素由
″
和/或
″
连接的情况下,第一种选项是指在没有第二个要素的情况下适用第一个要素。第二种选项是指在没有第一个要素的情况下适用第二个要素。第三种选项是指适合一起使用第一要素和第二要素。这些选项中的任一种均被理解为落在含义内,并且因此满足如本文所用的术语
″
和/或
″
的要求。多于一种选项的并行适用性也被理解为落在含义内,并且因此满足术语
″
和/或
″
的要求。
66.还应当理解,当提及本发明的部件的尺寸或特征时,本文使用的术语
″
约
″
、
″
大约
″
、
″
大致
″
、
″
基本上
″
和类似的术语表示所描述的尺寸/特征不是严格的边界或参数,并且不排除在功能上相同或相似的微小变化,如本领域普通技术人员所理解的。至少,包括数值参数的这种参考将包括使用本领域已接受的数学和工业原理(例如,舍入、测量或其他系统误差、制造公差等)的变化,不会改变最低有效数字。
67.除非另有说明,否则任何数值,诸如本文所述的浓度或浓度范围,应理解为在所有情况下均由术语
″
约
″
修饰。
″
约
″
是指处于如本领域的普通技术人员所确定的特定值的可接受误差范围之内,其将部分取决于所述值是如何测量或测定的,即所述测量系统的限制。在特定测定、结果或实施方案的上下文中,除非实施例或说明书其他地方内另有明确说明,否则
″
约
″
意指在根据本领域惯例的一个标准偏差之内、或多至10%的范围(无论哪个更大)。因此,数值通常包括所述值的
±
10%。例如,1mg/ml的浓度包括0.9mg/ml至1.1mg/ml。同样,1%至10%(w/v)的浓度范围包括0.9%(w/v)至11%(w/v)。除非上下文另有明确指示,否则如本文所用,使用的数值范围明确地包括所有可能的子范围、该范围之内的所有单个数值,包括此类范围之内的整数和该范围之内的分数。
68.除非另有说明,否则在一系列要素之前的术语
″
至少
″
应理解为指代系列中的每个要素。本领域的技术人员将会认识到、或仅使用常规实验就能够确定本文所述发明的具体实施方案的多种等同物。此类等同物旨在由本发明所涵盖。
69.″
抗原
″
是指能够介导免疫应答的任何分子(例如蛋白质、肽、多糖、糖蛋白、糖脂、核酸、其部分或它们的组合)。示例性免疫应答包括抗体产生和免疫细胞诸如t细胞、b细胞或nk细胞的活化。
70.″
抗原结合片段
″
或
″
抗原结合结构域
″
是指蛋白质的结合抗原的部分。抗原结合片段可以是合成的、可酶促获得的或经遗传工程化的多肽,并且包括免疫球蛋白的结合抗原的部分,诸如vh、vl、vh和vl、fab、fab
′
、f(ab
′
)2、fd和fv片段,由一个vh结构域或一个vl结构域组成的结构域抗体(dab),驼峰化vh结构域,vhh结构域,由模拟抗体的cdr诸如fr3-cdr3-fr4部分、hcdr1、hcdr2和/或hcdr3以及lcdr1、lcdr2和/或lcdr3的氨基酸残基组成的最小识别单元,结合抗原的替代性支架,以及包含抗原结合片段的多特异性蛋白质。抗原结合片段(诸如vh和vl)可经由合成接头连接在一起以形成各种类型的单抗体设计,其中在vh和vl结构域由单独的单链表达的那些情况下,vh/vl结构域可在分子内或分子间配对,以形成单价抗原结合结构域,诸如单链fv(scfv)或双价抗体。抗原结合片段也可以缀合至其它抗体、蛋白质、抗原结合片段或替代性支架缀合,所述支架可以是单特异性或多特异性的以工程化双特异性和多特异性蛋白质。
71.″
抗体
″
广义上是指并包括免疫球蛋白分子,具体包括单克隆抗体(包括鼠科动物单克隆抗体、人单克隆抗体、人源化单克隆抗体和嵌合单克隆抗体),抗原结合片段,多特异性抗体(诸如双特异性抗体、三特异性抗体、四特异性抗体等),二聚、四聚或多聚抗体,单链
抗体、结构域抗体,以及包含具有所需特异性的抗原结合位点的免疫球蛋白分子的任何其他经修饰构型。
″
全长抗体
″
包含由二硫键互连的两条重链(hc)与两条轻链(lc)以及它们的多聚体(例如igm)。每条重链由重链可变区(vh)和重链恒定区(由结构域ch1、铰链、ch2和ch3构成)构成。每条轻链由轻链可变区(vl)和轻链恒定区(cl)构成。vh区和vl区可进一步细分为超变区,该超变区称为互补决定区(cdr)并间插有框架区(fr)。各个vh和vl由三个cdr和四个fr片段构成,并按以下顺序从氨基端至羧基端排列:fr1、cdr1、fr2、cdr2、fr3、cdr3和fr4。免疫球蛋白可根据重链恒定结构域氨基酸序列被指定为五种主要种类,即iga、igd、ige、igg和igm。iga和igg进一步亚分类为同种型iga1、iga2、igg1、igg2、igg3和igg4。基于其恒定域的氨基酸序列,可将任何脊椎物种的抗体轻链指定为两种完全不同的类型即κ和λ中的一种。
72.″
生物活性
″
是指例如抗原的结合亲和力、中和或抑制。
73.″
互补决定区
″
(cdr)是结合抗原的抗体区。vh中存在三个cdr(hcdr1、hcdr2、hcdr3)并且vl中存在三个cdr(lcdr1、lcdr2、lcdr3)。cdr可以使用各种描绘诸如kabat(wu等人,(1970)j exp med 132(2):211-250)、(kabat等人,1991,j immunol 147(5):1709-19)、chothia(chothia等人,(1987)j.mol.biol.196(4):901-17)、imgt(lefranc等人,(2003)dev comp immunol 27(1):55-77)和abm(martin和thornton,(1996)j mol biol 263(5):800-815)来定义。描述了各种描绘和可变区编号之间的对应关系(参见例如lefranc等人,(2003)dev comp immunol27(1):55-77;honegger和pluckthun,j mol biol(2001)309(3):657-670;国际免疫遗传学(imgt)数据库;web资源,http://www_imgt_org)。可用程序(诸如ucl business plc的abysis)可用于描绘cdr。除非说明书中另有明确地说明,否则如本文所用,术语
″
cdr
″
、
″
hcdr1
″
、
″
hcdr2
″
、
″
hcdr3
″
、
″
lcdr1
″
、
″
lcdr2
″
和
″
lcdr3
″
包括由任何上述方法(kabat、chothia、imgt或abm)定义的cdr。
74.″
框架区
″
或
″
fr
″
是充当cdr的支架的抗体区。框架区负责支持抗原与抗体的结合。框架残基包括与抗原接触的残基,该残基是抗体结合位点的一部分,并且在序列上位于靠近cdr的位置或当在折叠的三维结构中时位于靠近cdr的位置。框架残基还包括不与抗原接触但通过辅助对cdr的结构支持而间接影响结合的残基。fr可以使用各种描绘诸如kabat、chothia、imgt和abm(martin和thornton,(1996)j mol biol 263:800-815)来定义。可用程序(诸如ucl business plc的abysis)可用于描绘fr。术语
″
fr1
″
、
″
fr2
″
、
″
fr3
″
、
″
fr4
″
包括由上述任何方法定义的fr。术语
″
hcfr
″
表示重链框架区fr1、fr2、fr3或fr4。术语
″
lcfr
″
表示轻链框架区fr1、fr2、fr3或fr4。
75.″
免疫球蛋白
″
可根据重链恒定结构域氨基酸序列分为五个主要种类,即iga、igd、ige、igg和igm。iga和igg进一步亚分类为同种型iga1、iga2、igg1、igg2、igg3和igg4。基于其恒定域的氨基酸序列,可将任何脊椎物种的抗体轻链指定为两种完全不同的类型即κ和λ中的一种。
76.″
人抗体
″
是指当施用于人受试者时被优化以具有最小限度的免疫应答的抗体。人抗体的可变区源自人免疫球蛋白序列。如果人抗体包含恒定区或恒定区的一部分,则该恒定区也源自人免疫球蛋白序列。如果人抗体的可变区由使用人种系免疫球蛋白或重排免疫球蛋白基因的系统获得,则该人抗体包含
″
源自
″
人起源序列的重链可变区和轻链可变区。此类示例性系统为在噬菌体上展示的人免疫球蛋白基因库,以及转基因非人动物,诸如携
带人免疫球蛋白基因座的小鼠或大鼠。由于用于获得人抗体和人免疫球蛋白基因座的系统之间的差异,体细胞突变的引入或有意将取代引入框架或cdr中或两者,因此
″
人抗体
″
与在人中表达的免疫球蛋白相比通常包含氨基酸差异。通常,
″
人抗体
″
的氨基酸序列与由人种系免疫球蛋白基因或重排免疫球蛋白基因编码的氨基酸序列具有至少约80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%的同一性。在一些情况下,
″
人抗体
″
可以包含由人框架序列分析得出的共有框架序列(例如,如knappik等人,(2000)j mol biol 296:57-86中所述),或结合到展示在噬菌体上的人免疫球蛋白基因库中的合成hcdr3(例如,如shi等人,(2010)j mol biol 397:385-96和国际专利公开wo2009/085462中所述的)。
″
人抗体
″
的定义中不包括至少一个cdr源自非人物种的抗体。
77.″
人源化抗体
″
是指其中至少一个cdr来源于非人物种并且至少一个框架来源于人免疫球蛋白序列的抗体。人源化抗体在框架中可包含取代,使得该框架可能不是表达的人免疫球蛋白或人免疫球蛋白种系基因序列的精确拷贝。
78.″
分离的
″
是指已经与分子(诸如本公开的scfv或包含本公开的scfv的异源蛋白)产生于其中的系统(诸如重组细胞)中的其他组分基本上分离和/或从其他组分中纯化出来的分子的同源群体,以及已经受至少一个纯化或分离步骤的蛋白质。
″
分离的
″
是指基本上不合其他细胞材料和/或化学物质的分子,并且涵盖分离至更高纯度(诸如80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%纯度)的分子。
79.″
变体
″
、
″
突变体
″
或
″
改变的
″
是指因一处或多处修饰(例如,一个或多个取代、插入或缺失)而不同于参考多肽或参考多核苷酸的多肽或多核苷酸。更具体地,本发明涉及变体多肽,其中该变体具有这样的氨基酸序列,当与种系免疫球蛋白序列比对时包含对应于fr1、fr2、fr3、fr4、cdr1、cdr2或cdr3中的任何氨基酸的氨基酸残基的至少一个取代,并且其中取代位点是先导抗体中识别的smh位点。变体多肽与参考多肽相比可以具有改善的特性,特别是在与稳定性相关的特性方面。改善的稳定性可以通过示出改善的热稳定性、增加的解折叠能、更低的聚集、改善的储存稳定性或改善的非特异性结合特性的变体来证明。改善的特性通常是与变体抗体在制造中的用途相关的特性。在本发明的一些实施方案中,修饰位点通过与种系抗体的序列比对来识别。在一个具体的实施方案中,序列比对用软件abysis来完成(swindells,m.b.等人,abysis:integrated antibody sequence and structure-management,analysis,and prediction.j mol biol 429,356-364(2017))。在一些实施方案中,修饰取代、插入或缺失通过抗体工程技术来完成。
80.″
tm
″
或
″
中点温度
″
是热解折叠曲线的温度中点。它是指50%的氨基酸序列处于其天然构象而另外50%变性的温度。热解折叠曲线通常绘制为温度的函数。tm用于测量蛋白质稳定性。通常,tm越高表示蛋白质越稳定。tm可以使用本领域技术人员熟知的方法容易地测定,诸如圆二色光谱法、差示扫描量热法、差示扫描荧光法(基于内在染料和外在染料两者)、uv光谱法、ft-ir和等温量热法(itc)。
81.″
tagg
″
是指蛋白质通过二聚化或寡聚化开始聚集的温度。聚集温度检测聚集的开始,即蛋白质将示出聚集倾向的温度。tagg可通过差示扫描量热法(dsc)、差示扫描荧光法(dsf)或通过圆二色性(cd)测定。这些技术可以检测蛋白质构象的微小变化,并因此检测聚
集的起始点。tagg值可以低于或高于tm。在tagg低于tm的情况下,蛋白质首先二聚化和/或寡聚化,并且然后在高于tagg的温度下稍后开始解折叠。在tagg高于tm的情况下,蛋白质首先开始解折叠,并且然后在高于tm的温度下聚集。这两个事件都是常见的并且取决于氨基酸组成和蛋白质构象。
82.化学变性是热变性的完美互补方法,用于测量蛋白质的固有稳定性,即使在较低温度(4℃至40℃,储存和生理温度)下也无需从较高温度外推稳定性值。温度外推非常容易出错,因为蛋白质的温度依赖性稳定性是三个重要参数的函数,诸如δh(解折叠的焓)、δs(解折叠的熵)和δcp(解折叠的热容量变化)。
83.″
δgu″
是指
″
解折叠的吉布斯自由能
″
,其在确定蛋白质在较低温度下的固有稳定性中起着关键作用。δgu通过化学变性测量。δgu的测定用于稳定性优化和聚集最小化。δgu越高的蛋白质,其天然构象越稳定。即使在较低温度下存在少量变性蛋白质也可引发聚集、化学降解并因此丧失结合和功能。因此,关键是确定治疗候选药物的解折叠自由能,以了解其天然构象的稳定性。化学变性可以在变性剂诸如氯化胍和/或脲的存在下通过诸如紫外、荧光和圆二色光谱法的技术测量。三个参数(δgu、c
50
和m)通过从化学变性收集的数据的非线性最小二乘拟合确定,其中m是δgu作为变性剂浓度的函数的变化率,并且c
50
是50%的蛋白质分子处于天然折叠状态和50%处于解折叠变性状态时的变性剂浓度。δgu和c
50
两者的增加表示蛋白质的固有稳定性的增加。在观察到两个解折叠转变的情况下,δgu1和δgu2将分别指第一解折叠转变和第二解折叠转变。
84.″
改善的稳定性
″
是指抗体变体对高温或低温、免疫球蛋白聚集和抗体制造期间测试的其他应激的耐受性增加。具有改善的稳定性的本公开的抗体是当与仅在一个或多个体细胞超突变位点不同的相同抗体进行比较时单体含量增加、熔点(tm)升高、tagg升高、解折叠自由能(δgu1、δgu1、c
50
)升高或聚集水平减少的抗体。单体含量的升高可以是2%或更多。升高的tm可以是1℃或更多,诸如1℃、2℃、3℃、4℃、5℃、6℃、7℃、8℃、9℃、10℃、11℃、12℃、13℃、14℃、15℃、16℃、17℃、18℃、19℃、20℃、21℃、22℃、23℃、24℃或25℃的升高。升高的tagg可以是1℃或更多,诸如1℃、2℃、3℃、4℃、5℃、6℃、7℃、8℃、9℃、10℃、11℃、12℃、13℃、14℃、15℃、16℃、17℃、18℃、19℃、20℃、21℃、22℃、23℃、24℃或25℃的升高。升高的δgu1(第一解折叠转变)或δgu2(第二解折叠转变)可以增加4kj/mol或更多。c
50
的增加可以是0.1m或更多。聚集的减少可以是1%或更多。
85.″
表面暴露的
″
是指氨基酸残基至少部分暴露于蛋白质表面并且可接触溶剂,诸如可被氘化。基于一级序列或蛋白质来预测残基的表面可及性的算法是本领域熟知的。另选地,可从蛋白质的晶体结构识别表面暴露的残基。
86.″
体细胞超突变
″
或
″
shm
″
是指多核苷酸序列的突变,其可由细胞机制的作用引发或与其相关,免疫系统通过这种作用来适应新的外来元素,如在类别转换期间所见。作为亲和力成熟过程的主要组成部分,shm使用于识别外来元素诸如抗原的b细胞受体多样化,并允许免疫系统在生物体的生命周期期间调整其对新威胁的应答。体细胞超突变影响免疫球蛋白基因的可变区。本发明提供了一种增加抗体稳定性的方法,该方法包括通过与种系抗体的序列比对来识别抗体框架区或cdr区中的体细胞超突变的步骤。该方法还包括评估存在于shm位点处的氨基酸残基的频率并将该氨基酸残基突变为相应的种系氨基酸的步骤。
87.″
种系抗体
″
是由未经历导致特定抗体表达的基因重排和突变的成熟过程的非淋
巴细胞编码的抗体序列。由本发明的各个实施方案提供的优点之一源于这样的认识,种系抗体基因比成熟抗体基因更可能保留动物物种中个体特有的必需氨基酸序列结构,因此更可能具有增强的稳定性。
88.在本发明的一些实施方案中,使用人抗体基因库,特别是人种系抗体基因库来识别给定抗体中由免疫活动引起的体细胞超突变。例如,人重链和轻链可变结构域基因的种系dna和编码的蛋白质序列可以在the international immunogenetics informationweb resources,http://www_imgt_org处找到。
89.本发明的另一个实施方案是抗体分子库,其中每个抗体分子包含vh结构域和vl结构域,该vh结构域由一组vh互补决定区hcdr1、hcdr2和hcdr3以及框架区fr1、fr2、fr3和fr4组成,该vl结构域由一组vl互补决定区lcdr1、lcdr2和lcdr3以及框架区fr1、fr2、fr3和fr4组成,并且其中已经经历shm的框架的一个或多个残基已经突变为种系残基。
90.在一些情况下,抗体的vh和vl框架区包含相对于人基因的种系氨基酸序列的一个或多个氨基酸取代、缺失和/或插入。在一些情况下,抗体的vh和vl框架区包含相对于种系氨基酸序列的1、2、3、4、5、6、7、8、9或10个氨基酸取代。在一些情况下,这些取代、缺失和/或插入中的一个或多个处于重链和轻链的框架区中。在一些情况下,这些取代、缺失和/或插入中的一个或多个处于重链和轻链的cdr中。在一些情况下,取代可代表相对于参考抗体中的氨基酸在此类位置处的保守或非保守氨基酸取代。
91.在一些情况下,重链的可变结构域包含来自种系氨基酸序列的1、2、3、4、5、6、7、8、9或10个取代、缺失和/或插入。在一些情况下,与种系氨基酸序列相比,取代是非保守取代。在一些情况下,取代、缺失和/或插入在重链的框架区中。在一些情况下,氨基酸取代、缺失和/或插入在重链的cdr区中。
92.在一些情况下,轻链的可变结构域包含来自种系氨基酸序列的1、2、3、4、5、6、7、8、9或10个取代、缺失和/或插入。在一些情况下,与种系氨基酸序列相比,取代是非保守取代。在一些情况下,取代、缺失和/或插入在轻链的框架区中。在一些情况下,氨基酸取代、缺失和/或插入在轻链的cdr区中。
93.在另一方面,对框架区进行突变,使得所得框架区具有相应种系基因的氨基酸序列。可以在框架区或cdr区中进行突变以增加抗体的热稳定性并改善保质期。框架区中的突变还可以改变或降低抗体的免疫原性。单个抗体可以在可变结构域或恒定结构域的任何一个或多个cdr或框架区中具有突变。
94.术语
″
种系化
″
是将在抗体vh或vl序列中发现的一个或多个氨基酸逆转为种系序列的相应氨基酸的过程。在一些示例中,种系化涉及用来自最接近匹配种系序列的等效残基替换异常或低频残基。具有与人vh3家族成员同源的氨基酸序列的vh或vl结构域的种系化通常涉及在该位置处发现为异常或低频残基或罕见残基的残基的替换/取代。异常或低频残基可能是体细胞超突变的结果。
95.本文所述的种系化的一般原理同样适用于本发明的该实施方案。例如,在vh和vl结构域中含有异常或低频残基的先导选择的克隆可以通过应用库方法在它们的框架区(fr)中进行种系化。在与最接近的人种系(对于vh和vl)和其他人种系进行比对后,识别fr中待改变的残基并选择人残基。虽然种系化可能涉及用来自最接近匹配的人种系的等效残
基替换体细胞超突变残基,但这不是必需的,并且也可以使用来自其他人种系的残基。
96.种系化过程的总体目标是产生一种分子,其中vh和vl结构域在引入人类受试者时表现出最小的免疫原性和改善的稳定性,同时保持由亲本vh和vl结构域形成的抗原结合位点的特异性和亲和力。
97.″
异常残基
″
是指在抗体的可变区中发现的氨基酸残基,其频率与在种系抗体中发现的氨基酸残基的频率相比小于1%。
98.″
低频残基
″
是指在抗体的可变区中发现的氨基酸残基,其频率与在种系抗体中发现的氨基酸残基的频率相比较低。频率可以是1%、2%、3%、4%、5%、6%、7%、8%、9%或10%的频率。
99.术语
″
kd″
是指
″
平衡解离常数
″
,并且是指在平衡滴定测量中获得的值,或通过解离速率常数(k
off
)除以缔合速率常数(k
on
)获得的值。
″
ka″
是指亲合常数。缔合速率常数、解离速率常数和平衡解离常数用于表示抗体对抗原的结合亲和力。用于测定缔合速率常数和解离速率常数的方法是本领域熟知的。使用基于荧光的技术提供了高灵敏度和在平衡状态下检查生理缓冲液中的样品的能力。可以使用其他实验方法和仪器,诸如(生物分子相互作用分析)测定。
100.除非另有明确说明,否则在整个说明书中,抗体恒定区中的氨基酸残基根据如kabat等人(1991,j immunol 147(5):1709-19)中描述的eu索引编号。
101.本文使用如表1中所示的常规单字母和三字母氨基酸代码。
102.表1.
103.氨基酸三字母代码单字母代码丙氨酸alaa精氨酸argr天冬酰胺asnn天冬氨酸aspd半胱氨酸cysc谷氨酸glue谷氨酰胺glnq甘氨酸glyg组氨酸hish异亮氨酸ilei亮氨酸leul赖氨酸lysk甲硫氨酸metm苯丙氨酸phef脯氨酸prop丝氨酸sers苏氨酸thrt色氨酸trpw酪氨酸tyry
缬氨酸valv
104.改善抗体稳定性的方法
105.本发明提供了一种改善抗体的方法,该方法包括以下步骤中的一个或多个或所有步骤:识别用于优化的抗体,识别抗体vh或vl或vh和vl中的一个或多个异常或低频残基;将抗体vh和vl序列与最接近的人或非人种系序列进行比对;识别vh和vl的框架中的体细胞超突变位点;识别通常在体细胞超突变位点处观察到的一个或多个种系残基;设计并工程化在体细胞超突变位点处含有一个或多个种系突变的变体或变体库;克隆并生产工程化变体;以及评估工程化变体的生物物理特性,评估工程化变体的免疫原性风险并选择一个或多个最佳变体。
106.在本发明的某些实施方案中,异常或低频残基的识别通过基于计算机的软件来完成。在具体的实施方案中,基于计算机的软件是软件abysis。可用于识别异常或低频残基的框架序列可从包括种系抗体基因序列的公共数据库或公开的参考文献中获得。例如,人重链和轻链可变结构域基因的种系dna和编码的蛋白质序列可以在处找到。
107.含有衍生自种系序列的框架区的抗体是指从使用人种系免疫球蛋白基因的系统,诸如从转基因小鼠、大鼠或鸡或从噬菌体展示库获得的抗体。由于例如天然存在的体细胞突变或有意取代,这种抗体与其来源的序列相比可能含有氨基酸差异。在某些实施方案中,先导抗体的异常或低频残基是框架区、cdr1、cdr2或cdr3中的体细胞超突变。
108.可以被替换以改善稳定性的异常或低频残基可以是由软件abysis计算的具有最低频率的残基(swindells,m.b.等人,abysis:integrated antibody sequence and structure-management,analysis,and prediction.j mol biol 429,356-364(2017))。在本发明的某个实施方案中,将被种系残基取代的异常残基的频率小于1%。将被种系残基取代的低频残基的频率为1%、2%、3%、4%、5%、6%、7%、8%、9%或10%。
109.本发明提供了一种设计变体抗体的方法,其中vh、vl或vh和vl两者任选地在抗体的框架区中包含一个、两个、三个、四个、五个、六个、七个、八个、九个、十个、十一个、十二个、十三个、十四个或十五个氨基酸取代。任选地,取代可以在cdr1、cdr2或cdr3内,但不应影响抗体的结合。在本发明的上下文中,取代是在观察到异常或低频残基的位点处的种系取代。可能的取代位点在抗体的框架区内。示例性取代可以是种系取代。
110.该方法还包括评估原始先导抗体和工程化变体的稳定性的步骤。在本发明的上下文中,可以使用本领域已知的任何合适的测定法来测量抗体的稳定性,诸如例如但不限于测量解折叠自由能、热稳定性、单体和其他更高阶聚集体的定量尺寸分布、储存和非特异性结合。测量蛋白质稳定性的方法包括但不限于分析超速离心法、差示扫描量热法、分析尺寸排阻法、差示扫描荧光法。预测稳定性的方法可以包括分子建模。在本发明的上下文中也可以使用其他测量体内和体外蛋白质稳定性的方法。抗体的稳定性可以根据转变中点值tm、聚集温度tagg、解折叠自由能δgu和c
50
、聚集状态的变化或与非特异性表面的结合来测量。如本文所用,术语
″
稳定性
″
是指抗体在经受高温或低温、免疫球蛋白聚集和抗体制造中测试的其他应激时保持其结构构象和/或其活性和/或亲和力的能力。具有改善的稳定性的抗体变体是指抗体变体对高温或低温、免疫球蛋白聚集和抗体制造期间测试的其他应激的耐受性增加。
111.在一些实施方案中,分析超速离心评估还包括将工程化变体的分析超速离心沉降
速度(auc-sv)与所述先导抗体的auc-sv进行比较。优选地,本发明识别抗体框架区中的异常或低频残基并用种系残基取代异常或低频残基的方法提供了具有改善的auc-sv值的抗体变体。例如,变体抗体将表现出>95%的单体(例如95%、96%、97%、98%、99%或100%的单体)。具有改善的auc-sv值的抗体将示出单体含量增加2%或更多。
112.在一些实施方案中,热稳定性评估还包括将每个所述工程化变体的热解折叠曲线的tm与所述先导抗体的热解折叠曲线的tm进行比较。优选地,本发明识别抗体框架区中的异常或低频残基并用种系残基取代异常或低频残基的方法提供了具有增加的tm值的抗体变体。如本发明所述,一个或多个突变对变体抗体的热稳定性的影响通过测量从热解折叠曲线外推的tm值的变化来确定。增加变体抗体的稳定性的有利突变预计会增加tm。例如,当与原始先导抗体tm进行比较时,变体抗体将表现出1℃或更多的δtm增加(诸如1℃、2℃、3℃、4℃、5℃、6℃、7℃、8℃、9℃、10℃、11℃、12℃、13℃、14℃、15℃、16℃、17℃、18℃、19℃、20℃、21℃、22℃、23℃、24℃或25℃的δtm)。
113.在一些实施方案中,热稳定性评估还包括将每个所述工程化变体的tagg值与所述先导抗体的tagg值进行比较。优选地,本发明识别抗体框架区中的异常或低频残基并用种系残基取代异常或低频残基的方法提供了具有增加的tagg值的抗体变体。增加变体抗体的稳定性的有利突变预计会增加tagg。例如,当与原始先导抗体tagg进行比较时,变体抗体将表现出1℃-25℃的δtagg(例如1℃、2℃、3℃、4℃、5℃、6℃、7℃、8℃、9℃、10℃、11℃、12℃、13℃、14℃、15℃、16℃、17℃、18℃、19℃、20℃、21℃、22℃、23℃、24℃或25℃的δtagg)。
114.在一个实施方案中,解折叠自由能还包括将每个工程化变体的δgu1、agu2、c
50
与先导抗体的δgu1、δgu2、c
50
进行比较。优选地,本发明识别抗体框架区中的异常或低频残基并用种系残基取代异常或低频残基的方法提供了具有增加的δgu1、δgu2、c50值的抗体变体。增加变体抗体的稳定性的有利突变可增加变体抗体的δgu1、δgu2或c
50
值。例如,当与原始先导抗体δgu1或δgu2进行比较时,变体抗体将表现出4kj/mol或更多的δgu1或δgu2增加。当与先导抗体进行比较时,变体抗体还可以表现出0.1m或更多的c
50
增加。
115.在一个实施方案中,所述工程化变体的储存稳定性在4℃或40℃下在2周和4周时测量并与所述先导抗体的储存稳定性进行比较。在具体的实施方案中,储存稳定性通过观察在时间零与1个月之间聚集水平的变化来测量。优选地,本发明识别抗体框架区中的异常或低频残基并用种系残基取代异常或低频残基的方法提供了具有减少的聚集的抗体变体。例如,当与原始先导抗体聚集水平进行比较时,变体抗体将表现出1%-5%的δ%聚集(例如1%、2%、3%、4%或5%的δ%聚集)减少。
116.在另一个实施方案中,产生稳定抗体的方法包括评估工程化变体的免疫原性风险。
117.在本发明的某些实施方案中,免疫原性风险评估在计算机上测量。在具体的实施方案中,在计算机上的免疫原性风险评估通过epivax评分来测量。在某些实施方案中,变体抗体的免疫原性风险等于或低于原始先导抗体的免疫原性风险。
118.在某些实施方案中,工程化变体在抗体的人框架区、cdr1、cdr2或cdr3中产生。氨基酸替换可以通过本领域已知的任何合适的方法进行。
119.在一些实施方案中,要求保护的发明的方法包括测量先导抗体和抗体变体的亲和
力,并将抗体变体的亲和力与先导抗体的亲和力进行比较。先导抗体和抗体变体的亲和力可以使用任何合适的方法通过实验确定。一种示例性方法采用本领域技术人员已知的proteon xpr36、biacore 3000、octet、kinexa仪器、elisa或竞争结合测定法。如果在不同条件(例如,渗透压、ph)下测量,则所测量的抗体亲和力可变化。因此,亲和力和其他结合参数(例如kd、k
on
和k
off
)的测量通常用标准化条件和标准化缓冲液(诸如本文所述的缓冲液)进行。本领域技术人员将理解,例如使用biacore 3000或proteon进行亲和力测量的内部误差(测量为标准偏差,sd)通常可在典型检出限内的测量值的5%-33%内。因此,当提及kd值时,术语
″
约
″
反映测定中的典型标准偏差。
120.本发明的方法还包括选择表现出增强的稳定性但保留与先导分子相似的亲和力的变体抗体。在一些实施方案中,变体抗体的亲和力在功能上相同或相似,如本领域普通技术人员所理解的。在其他实施方案中,变体抗体的亲和力可以比原始先导抗体的亲和力更紧密。至少,包括数值参数的这种参考将包括使用本领域已接受的数学和工业原理(例如,舍入、测量或其他系统误差、制造公差等)的变化,不会改变最低有效数字。
121.实施例1
122.下面的实施例描述了通过在抗体框架中识别的shm位点的种系化来优化抗前列腺靶抗体tmeb675。尽管抗体符合高亲和力抗体的功能标准特征,但其示出较差的固有特性。tmeb675的再工程化产生了一组变体,基于其功能和有利的生物物理特性从这些变体中选择tmeb762。
123.发现、工程化和种系优化
124.单克隆抗体(tmeb675)是通过用重组人tmeff2在转基因平台中对omnirat进行免疫而发现的。是一个治疗性人抗体平台,可生产高度多样化的完全人抗体库。含有嵌合人/大鼠igh基因座(包含22个人vh,所有与大鼠ch基因座连接的天然构型的人d和jh片段)以及完全人igl基因座(与jκ-cκ连接的12个vκ和与jλ-cλ连接的16个vλ)(osbom,m.j.等人,high-affinity igg antibodies develop naturally in ig-knockout rats carrying germline human igh/igkappa/iglambda loci bearing the rat ch region.j immunol 190,1481-1490(2013))。因此,大鼠表现出大鼠免疫球蛋白的表达降低,并且响应于免疫,引入的人重链和轻链转基因经历类别转换和体细胞突变以产生具有完全人可变区的高亲和力嵌合人/大鼠igg单克隆抗体。wo14/093908中描述了的制备和用途以及由这些大鼠携带的基因组修饰。在89天免疫方案后,从大鼠收获淋巴结并用于产生杂交瘤。通过elisa筛选杂交瘤上清液与重组人tmeff2的结合。
125.基于筛选结果,对若干杂交瘤克隆进行测序、表达和功能表征。tmeb675示出所需的重组蛋白亲和力和细胞结合属性(表2),并被选择用于进一步研究。
126.表2:本表中提供了通过spr进行亲和力测量的参数。包括缔合常数ka(m-1
s-1
)、解离常数kd(s-1
)和平衡常数kd(m)。
[0127][0128]
abysis工具允许搜索抗体重链和轻链序列内的
″
异常残基
″
(swindells,m.b.等
人,abysis:integrated antibody sequence and structure-management,analysis,and prediction.j mol biol 429,356-364(2017))。由抗体序列数据库中小于1%的阈值定义的异常残基提供了关于某些位置的关键功能的提示。由抗体序列数据库中1%-10%阈值定义的低频异常残基提供了关于某些位置的关键功能的提示。
[0129]
tmeb675的可变重链和轻链区与人种系序列的vh和vl使用abysis门户进行的序列比对表明框架区内有几个体细胞超突变(shm)。在vh中观察到三个体细胞超突变(r14p、p20l、h81q),而在vk中观察到两个shm(a1d、a91p)(图1a、图1b、图2a-图2d)。在abysis分析中,分别在人重链框架(hcfr)的位置14、20和81处发现的精氨酸、脯氨酸和组氨酸氨基酸残基以及在人轻链框架的位置1处发现的丙氨酸残基被评分为低频,表明这些是异常或低频残基(图2a-图2e)。tmeb675的hcfr的位置14处的精氨酸和位置20处的脯氨酸是低频残基(<1%,表3、表4和表5)。
[0130]
与在位置14处最常见的脯氨酸残基(脯氨酸残基频率95.029%)相比,在该位置处发现的shm精氨酸很罕见(频率0.151%)。(表3和表4,图2a)。与最常见的亮氨酸残基(频率73.024%)相比,在重链位置20处发现的shm脯氨酸的频率也较低(频率0.088%)。(表3和表5,图2b)。与通常在位置81处发现的最常见的谷氨酰胺残基(频率57.576%)相比,在该位置处发现第三个shm组氨酸的频率也相对罕见(频率1.604%)(表3和表6,图2c)。表3示出了位置14、20和81处的人重链种系序列和典型组成。表4、表5和表6分别示出了位置14、20和81处的abysis数据库重链序列和残基的组成。表7和表8分别示出了位置1和91处的abysis数据库轻链序列和残基的组成。
[0131]
表3:位置14、20和81处的人重链(ighv)种系序列和残基的组成。
[0132]
[0133]
[0134]
[0135]
[0136]
[0137]
[0138]
[0139]
[0140][0141]
表4:位置14处的abysis数据库重链序列和残基的组成。
[0142]
#chothiah14所有#氨基酸不相同的计数相对频率(%)a14261.97c30.004d360.05e120.017f380.052g170.023h440.061i300.041k100.014l4050.559m50.007n50.007p6880395.03q220.03
r1090.151s8491.173t3910.54v910.126w40.006y120.017
[0143]
表5:位置20处的abysis数据库重链序列和残基的组成。
[0144]
#chothiah20所有#氨基酸不相同的计数相对频率(%)a1270.161c10.001d20.003e00f1220.155g40.005h140.018i865811k80.01l5749873.02m22722.886n00p690.088q40.005r100.013s220.028t250.032v981312.46w20.003y400.051
[0145]
表6:位置81处的abysis数据库重链序列和残基的组成。
[0146]
#chothiah81所有#氨基酸不相同的计数相对频率(%)a1240.147c20.002d23002.72e1295715.322f140.017g1360.161h13561.604
i2000.237k1043912.345l4120.487m4940.584n9131.08p240.028q4868757.576r17982.126s7640.903t37044.38v970.115w50.006y910.108
[0147]
在轻链中发现了两个shm。在lcfr的位置1处发现了shm,并在该位置处产生了丙氨酸(图1b,表7)。天冬氨酸是在该位置处最常见的残基(频率37.355%),而ala在该位置处相对罕见(频率6.099%)(表7,图2d)。在lccdr的位置91处也发现了shm,在该位置处产生了丙氨酸残基。在位置91处的脯氨酸是在该位置处最常见的残基(50.996%),而ala相对罕见(频率2.332%)(表8,图2e)。
[0148]
表7:位置1处的abysis数据库轻链序列和残基的组成。
[0149]
#chothial1所有#氨基酸不相同的计数相对频率(%)a14746.099c30.012d902837.355e426817.66f310.128g1350.559h540.223i390.161k580.24l430.178m420.174n3451.428p420.174q654427.077r390.161s17757.344t460.19v430.178
w40.017y1350.559
[0150]
表8:位置91处的abysis数据库轻链序列和残基的组成。
[0151]
#chothial91所有#氨基酸不相同的计数相对频率(%)a6602.332c130.046d4271.509e660.233f1250.442g16445.809h4571.615i2851.007k1660.587l343812.148m620.219n11914.208p1443250.996q1190.42r3191.127s305310.788t9603.392v3271.155w760.269y4501.59
[0152]
为了评估shm对与靶蛋白结合的潜在影响,通过hxms测定结合表位。hdx-ms将四个区确定为互补位定义区。这些区分布在抗体的重链中的三个位置和轻链中的一个区,在观察到体细胞超突变的框架外(数据未示出)。因此,预计这些位点的种系化不会影响结合亲和力和功能。
[0153]
表达在重链shm位点或轻链shm位点中或在组合的重链和轻链shm位点中具有突变的种系变体并测试其功能活性和固有特性两者。采用图11所示的工作流程来识别shm并工程化具有改善的分子属性的抗体。构建的二元变体库描述于表9中。如下所述测试每个变体的功能和生物物理特性。
[0154]
表9:二元变体库。
[0155][0156]
生物物理评估
[0157]
用于评估生物物理特性的方法
[0158]
差示扫描荧光法(dsf)
[0159]
使用自动化prometheus仪器通过nanodsf测定抗体变体的热稳定性。通过将样品从384孔样品板装载到24孔毛细管中来进行测量。对每个样品执行重复运行。典型igg样品的热扫描范围为20℃至95℃,速率为1.0℃/分钟。将330nm和350nm发射波长处的固有色氨酸和酪氨酸荧光以及比率f350nm/f330nm比率与温度作图以生成解折叠曲线。
[0160]
nanodsf仪器的背反射光学器件发射波长不被蛋白质吸收的近uv光。聚集的蛋白质将散射光,而非散射光将到达检测器。背反射光的减少是聚集的直接量度,并以mau(衰减单位)对温度作图。
[0161]
在ph 7.4的磷酸盐缓冲盐水中以0.5mg/ml测量抗体变体的热解折叠参数(tm和tagg)。
[0162]
通过在室温下将纯化的mab在0m至6m的不同浓度的gdncl中温育过夜来进行化学变性实验。第二天在25℃下使用nanodsf测量固有荧光。在gdncl的每个浓度下对f350nm/f330nm比率作图以生成解折叠曲线,该解折叠曲线通过二态或三态解折叠方程拟合以获得解折叠自由能(δgu)和50%分子以解折叠形式存在时的变性剂浓度(c
1/2
,也称为c
50
)。
[0163]
差示扫描量热法(dsc)
[0164]
通过毛细管vp-dsc微量热计(microcal inc.northampton,ma)表征热稳定性。在25℃至120℃下以1.0mg/ml的蛋白质浓度和1℃/min的扫描速率执行温度扫描。从蛋白质扫描中减去缓冲液参考扫描,并在热力学分析之前对蛋白质浓度进行标准化。使用非二态模型拟合dsc曲线以获得焓和表观转变温度(tm)值。
[0165]
非特异性结合
[0166]
通过生物传感器技术(biacore 8k)测定先导分子与不相关表面的非特异性结合。将浓度为1μm的抗体变体通过涂覆有不相关蛋白质的spr表面。预测显示与不相关表面显著
结合的抗体具有较差的体内特性和制造挑战。不相关表面包括带负电荷和带正电荷的蛋白质、疏水蛋白质和人igg。
[0167]
分析超速离心
[0168]
使用beckman optima auc仪器通过分析超速离心测量溶液中单体和其他更高阶蛋白质聚集体的定量尺寸分布。将样品装载到配备有1.2cmbeckman中心件(额定为50k rpm)和石英窗的离心池中。将池装配并扭转至1301bs。将离心池置于an-50(8孔)或an-60(4孔)转子中并置于auc室内。在开始运行之前,将auc仪器的温度设置为20.5℃至少一小时。以40k rpm、250次扫描计数(250次扫描)、90秒扫描收集频率、10μm数据分辨率和280nm波长执行运行。使用直接边界拟合软件sedanal分析数据。
[0169]
短期稳定性(4℃,40℃)
[0170]
通过分析尺寸排阻色谱法(sec-hplc)测试浓缩的mab以测量单体的百分比。然后将mab在4℃和40℃下温育4周。定期抽取等分试样,并通过sec-hplc检查完整性。
[0171]
分子建模
[0172]
使用moe建模软件(ccg,montreal)使用其标准抗体建模方案生成分子同源性模型。种系化突变被识别并在棒形表示中突出显示。分子图在计算机图形程序pymol中生成。
[0173]
生物物理评估的结果
[0174]
shm残基的再工程化导致发现具有更好的生物物理属性的优化变体。在所测试的11个变体中,含有三个重链再工程化种系突变r14p、p20l和h81q以及两个轻链种系突变a1d和a91p的tmeb762具有最佳的生物物理特性。残基根据kabat进行编号。为了更好地理解shm的作用和热稳定的结构基础,将五个种系突变作图到两个fv的分子模型上(moe,ccg,montreal)(图3)。在五个种系突变中,a1d和h82h表面暴露,并且因此对结构域稳定性几乎没有贡献。vh r14p可能对结构有影响,并且因此可能对结构域稳定性有轻微影响。根据分子建模,vh p20l和vl a95p突变可能是两个主要的结构决定因素。p20l位于β链的中间,其侧链包埋在vh核心中。脯氨酸在典型的β链结构中不是有利的残基。在该位置处的leu将恢复有利的残基,并且亮氨酸侧链将很好地填充在核心中。在这类vl中位置95处的氨基酸残基通常处于使稳定性最大化的顺式构象。先前报道了在该位置处的非pro突变对稳定性和结构的影响(luo,j.等人,coevolution of antibody stability and vkappa cdr-l3 canonical structure.j mol biol 402,708-719(2010))。在该位置处的ala可能扭曲局部规范结构或被迫形成非常不利的非pro顺式肽键。两者都会对稳定性产生负面影响。总体而言,种系突变的基本原理得到了很好的支持。
[0175]
生物物理表征
[0176]
分析超速离心(auc)
[0177]
微量工艺和产品相关杂质的存在对安全性构成主要威胁并增加免疫原性相关风险。对高质量分子进行生物物理表征对于真正确定其固有特性至关重要。auc是一种测量溶液中单体和其他更高阶蛋白质聚集体的定量尺寸分布的强大技术(berkowitz,s.a.role of analytical ultracentrifugation in assessing the aggregation of protein biopharmaceuticals.aaps j 8,e590-605(2006))。具体地,基于沉降速度(sv)的分析以无偏的方式独特地测量任何缓冲液中蛋白质的流体动力学大小和形状。图4示出了tmeb762(黑线)和tmeb675(灰线)两者的分析超速离心沉降速度(auc-sv)运行。基于sv-auc分析,
tmeb675和tmeb762两者在纯化后表现出>95%的单体并且因此是用于进一步生物物理表征的良好起始材料。
[0178]
热稳定性
[0179]
构象稳定性和胶体稳定性两者充分证明了可制造性参数,这些可制造性参数预测稳定性、保质期和成功的药物开发。同时评估两个参数是长期稳定性测定的非常有效的方法。温度是剖析分子的结构稳定性的广泛使用的变性方法之一。基于色氨酸的荧光发射用于使用prometheus nt.48仪器监测两种mab在pbs中的热解折叠。高荧光灵敏度检测使得能够监测由于不同子结构域解折叠引起的mab构象变化。同时,荧光检测可以通过使用背反射光强度技术监测温度诱导的聚集来检测胶体稳定性的变化。同样地,差示扫描量热法是用于确定在较高温度下的基于结构域的稳定性的工业金标准热熔融工具。图5提供了通过nano dsf测定的tmeb675和tmeb762的热解折叠曲线图。数据示出tmeb762更稳定。tmeb762的解折叠在高于tmeb675的温度(约59℃)下开始,而fab解折叠在接近75℃下发生(表10)。该抗体非常稳定,并且在低于该温度下没有示出聚集迹象(tagg)。图6示出了通过dsc测定的tmeb675和tmeb762的热解折叠曲线图。
[0180]
表10:由dsc(解折叠开始和fab结构域解折叠tm)和dsf(tagg)测定的热稳定性参数。
[0181]
mabt开始-dsc(℃)tm(fab)-dsctagg-dsf(℃)tmeb67552.961.861.5tmeb76259.375.575.7
[0182]
解折叠自由能
[0183]
无疑,热变性实验是最常见的稳定性测定工具之一,其可作为用于早期分级排序分子的高通量。然而,现有的挑战是基于较高的温度数据精确地计算较低温度下的固有稳定性。该计算容易出错,因为热熔融由于聚集而通常是不可逆的,这妨碍了在较低温度下可靠的稳定性参数的外推(freire,e.,schon,a.,hutchins,b.m.&brown,r.k.chemical denaturation as a tool in the formulation optimization of biologics.drug discov today 18,1007-1013(2013))。此外,先导候选药物的稳定性通常仅在25℃或37℃下进行测量。在单一温度下的等温化学变性(icd)是一种经过验证的可靠热力学分析,以提供蛋白质在任何溶剂中的固有稳定性(svilenov,h.,markoja,u.&winter,g.isothermal chemical denaturation as a complementary tool to overcome limitations of thermal differential scanning fluorimetry in predicting physical stability of protein formulations.eur j pharm biopharm 125,106-113(2018))。在icd实验中,在测量构象变化之前,将mab以给定浓度在递增浓度的变性化学品中温育最少12-16小时。f350/f330荧光比率的变化用于确定在变性化学品的每个测量浓度下解折叠蛋白质的分数。由拟合曲线计算的解折叠吉布斯自由能(δgu)是mab在特定温度下的固有构象稳定性的指标。该拟合的另一个重要参数是c50,其表示50%抗体解折叠时变性剂的浓度。图7和图8提供了在25℃下测量的tmeb675和tmeb762的icd解折叠曲线。有趣的是注意到tmeb675表现出δgu为24.3kj/mol的单一转变,而tmeb762示出三种解折叠状态,典型的是表现良好的mab,第一转变δgu为63.5kj/mol,而第二转变δgu为37.3kj/mol。tmeb762的第一转变的解折叠自由能增加大约三倍,这清楚地表明tmeb762本质上比tmeb675更稳定,这可能是由于其种系优
化的fab结构域(表11)。
[0184]
表11:来自icd实验的固有稳定性参数。δgu1、δgu2、c
50
是在nano dsf实验中生成的gdncl诱导变性曲线的2态和3态拟合的计算参数。
[0185][0186]
储存稳定性评估
[0187]
加速热应力是行业广泛使用的强制降解测定,以产生足够的降解产物并在缩短的时间内了解抗体的降解机制。它被用作长期货架稳定性的直接预测。通过分析尺寸排阻色谱法(asec)监测tmeb675和tmeb762在pbs中的降解,研究了它们的长期储存(4℃)和加速储存(40℃)两者一个月。asec色谱图(数据未示出)示出抗体通过聚集随时间推移降解而不片段化。对两种mab在时间零、2周和4周之间聚集体水平的变化作图(图9)。tmeb762在4℃下具有<0.3%的聚集体并且在40℃下加速储存一个月时具有<1%的聚集体。然而,tmeb675在4℃和40℃下一个月后分别示出0.5%和3%的聚集增加。与各个文献一致,较高的热稳定性与较低的聚集倾向相关(brader,m.l.等人,examination of thermal unfolding and aggregation profiles of a series of developable therapeutic monoclonal antibodies.mol pharm 12,1005-1017(2015).;he,f.等人,detection of igg aggregation by a high throughput method based on extrinsic fluorescence.jpharm sci 99,2598-2608(2010))。
[0188]
非特异性结合
[0189]
先导候选药物的序列优化有时可能会导致它们的物理特性诸如疏水性、电荷异质性、折叠、溶解性和溶剂可及性意外改变。这些固有特性的改变将对可开发性和药代动力学行为具有重大影响。mab的更快清除可归因于体内与其他不相关蛋白质的非特异性相互作用。这些简单的物理特性可以通过非特异性结合测定来测量(dostalek,m.,prueksaritanont,t.&kelley,r.f.pharmacokinetic de-risking tools for selection of monoclonal antibody lead candidates.mabs 9,756-766(2017))。这里我们使用基于表面等离子体共振(spr)的非特异性结合测定来确定tmeb675和tmeb762两者与疏水、带电和igg表面的非特异性结合特性。基于收集的许多早期和晚期候选药物(包括市售抗体)的实验数据,我们提出了针对非特异性结合测试的候选药物的相对结合应答的标准(此处未揭示)。在每个实验中运行适当的对照抗体(阳性和阴性)以进行验证。将tmeb675和tmeb762的相对应答单位对与不同表面的结合作图。从每个数据集中减去对对照葡聚糖表面流动池的结合应答。即使在1μm浓度下,tmeb762和tmeb675也没有示出与测试的任何带电表面的非特异性结合(图10)。与任何不相关表面的非特异性结合可能是开发这些对体内行为具有潜在担忧的mab的重大挑战。
[0190]
生物物理评估示出,框架残基的种系化安全且有利地增强了tmeb762的热稳定性并降低了聚集倾向而不显著改变抗体的构象。
[0191]
免疫原性风险评估
[0192]
与tmeb675相比,tmeb762示出降低的免疫原性风险,这通过人种系序列同一性%
的改善来指示。此外,在计算机上的免疫原性风险评估评分也显著改善(表12)。epivax筛选免疫原性并依靠一组免疫信息工具来预测肽和蛋白质的免疫原性。
[0193]
表12:tmeb675和工程化变体tmeb762的免疫原性风险评估。
[0194][0195]
结合亲和力
[0196]
测量tmeb762的结合亲和力并与tmeb675进行比较,并总结于表13中。
[0197]
表13:本表中提供了通过spr进行亲和力测量的参数。包括缔合常数ka(m-1
s-1
)、解离常数kd(s-1
)和平衡常数kd(m)。
[0198][0199]
结论
[0200]
在测试的11个变体中,tmeb762具有最理想的功能和生物物理特性。tmeb675的种系化导致构象更稳定的tmeb762,其具有非常低的聚集倾向(<1%)并符合fda/ema批准和临床阶段的mab候选药物的质量属性。
[0201]
实施例2
[0202]
实施例1中描述的工作流程用于优化其他不同结构和功能的抗体。实施例2描述了通过在抗体框架中识别的shm位点的种系化来优化抗前列腺靶抗体psmw56。
[0203]
发现、工程化和种系优化
[0204]
单克隆抗体(psmw56)是通过用重组人psma蛋白质在转基因平台中对omnirat进行免疫而发现的。在89天免疫方案后,从大鼠收获淋巴结并用于产生杂交瘤。通过elisa筛选杂交瘤上清液与重组抗原的结合。基于筛选结果,对若干杂交瘤克隆进行测序、表达和功能表征。变体psmw56示出所需的重组蛋白亲和力(表14),并被选择用于进一步研究。尽管抗体符合高亲和力抗体的功能标准特征,但其示出较差的热稳定性。
[0205]
表14:通过spr测定的平衡常数kd(m)的亲和力测量的参数。
[0206][0207]
抗psma抗体的工程化
[0208]
psmw56的可变重链区与人种系序列的vh使用abysis门户进行的序列比对表明框架区内有几个体细胞超突变(shm)。在vh中观察到一个体细胞超突变(ile68)(图12和图13)。苏氨酸是在位置68处发现的常见氨基酸残基。在位置68处发现的ile的shm频率(3%)
低于在该位置处最常见的thr残基(thr残基频率85%)。表15示出了位置68处abysis数据库重链序列和残基的组成。通过在亲本克隆psmw56上用thr替换ile68来生成工程化变体psmw57。
[0209]
表15:抗psma的位置68处的abysis数据库重链序列和残基的组成。
[0210]
#chothiah68所有#氨基酸不相同的计数相对频率(%)a12601c1<1d42<1e153<1f100<1g34<1h25<1i22193k244<1l48<1m47<1n252<1p30<1q175<1r108<1s82159t7430285v468<1w0<1y85<1
[0211]
抗psma抗体变体的生物物理评估-热稳定性
[0212]
表达具有重链i68t突变的种系变体(psmw57)并测试其热稳定性。如图14所示,当与psmw56进行比较时,工程化的抗psma变体(psmw57)示出热稳定性(tm和tagg两者)的显著增加,这表明图11中描述的工作流程适用于其他抗体。
[0213]
实施例3
[0214]
为了进一步证明图11的工作流程广泛适用于其他抗体,应用该工作流程来优化抗前列腺癌抗体dl3b355。下面的实施例描述了通过在抗体框架中识别的shm位点的种系化来优化dl3b355。
[0215]
发现、工程化和种系优化
[0216]
抗dll3单克隆抗体是通过用重组人dll3免疫alivamab小鼠而发现的,该alivamab小鼠是一个产生具有人独特型的多种抗体库的转基因完全人抗体平台。通过elisa筛选杂交瘤上清液与重组抗原的结合。
[0217]
基于筛选结果,对若干杂交瘤克隆进行测序、表达和功能表征。dl3b355示出所需
的重组蛋白亲和力(表16),并被选择用于进一步研究。
[0218]
表16:通过spr测定平衡常数kd(m)的亲和力测量的参数。
[0219][0220]
如实施例1中所述,使用abysis工具搜索抗体重链和轻链序列内的
″
异常残基
″
。由抗体序列数据库中1%阈值定义的异常残基提供了关于某些位置的关键功能的提示。
[0221]
抗dll3抗体的工程化
[0222]
dl3b355的可变重链和轻链区与人种系序列的vh和vl使用abysis门户进行的序列比对表明框架区内有几个体细胞超突变(shm)。在vh中观察到一个体细胞超突变(his85)(图15a和图16b)。在重链中,天冬酰胺是在位置85处发现的常见氨基酸残基。与在位置85处最常见的asn残基(asn残基频率52%,表17)相比,在该位置处发现的his的shm频率罕见(<1%)。在vl中观察到一个体细胞超突变(glu84)(图15b和图16b)。在重链中,甘氨酸是在位置84处发现的常见氨基酸残基。与在位置84处最常见的gly残基(gly残基频率93%,表18)相比,在该位置处发现的glu的shm频率罕见(<1%)。如表19所示生成了dl3b355的三个工程化变体。
[0223]
表17:抗dll3的位置85处的abysis数据库重链序列和残基的组成。
[0224]
#chothiah85所有#氨基酸不相同的计数相对频率(%)a2700.319c160.019d16001.892e4350.514f8721.031g7100.84h1750.207i1520.18k14611.728l540.064m430.051n4465052.801p150.018q3230.382r7130.843s3046236.023t19252.276v5170.611w50.006y1120.132
[0225]
表18:抗dll3的位置84处的abysis数据库轻链序列和残基的组成。
[0226]
#chothial84所有#氨基酸不相同的计数相对频率(%)a6122c3<1d318<1e266<1f7<1g3376593h43<1i1<1k17<1l5<1m6<1n179<1p2<1q14<1r346<1s7002t59<1v58<1w10<1y37<1
[0227]
表19:抗dll3的工程化变体库。
[0228]
#名称重链轻链1dl3b355-变体1h85n-2dl3b355-变体2h85ne84g3dl3b355-变体3-e84g
[0229]
dll3抗体变体的生物物理评估-热稳定性
[0230]
测量每个工程化抗dll3变体的热稳定性参数以确定种系突变是否对生物物理属性具有积极作用。通过dsf和dsc测量解折叠的开始和fab结构域解折叠tm。如图17所示,工程化的抗dll3变体示出热稳定性(tm和tagg两者)的显著增加。
[0231]
本说明书中所引用的所有出版物,包括但不限于专利和专利申请均以引用方式并入本文,如同在本文中完整给出。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
