1.本发明涉及一种用于制备硫代烷基嘧啶的方法和由其得到的化合物。
背景技术:
2.wo 2015/108779中描述了制备作为除草剂的某些嘧啶氧基苯衍生物的方法。用于制备嘧啶衍生物的方法披露于organic synthesis[有机合成]2003,80,200-206;organic process research and development[有机工艺研究与开发]2005,9,141-148和eur.j.org.chem.[欧洲有机化学杂志]2014,7426-7432中。虽然前面的参考文献中披露的方法可以提供所期望的化合物,但寻求持续改进,特别是在开发以商业规模提供材料的方法方面。因此,持续需要更低成本、更有效、更灵活或更方便操作的新方法。
技术实现要素:
[0003]
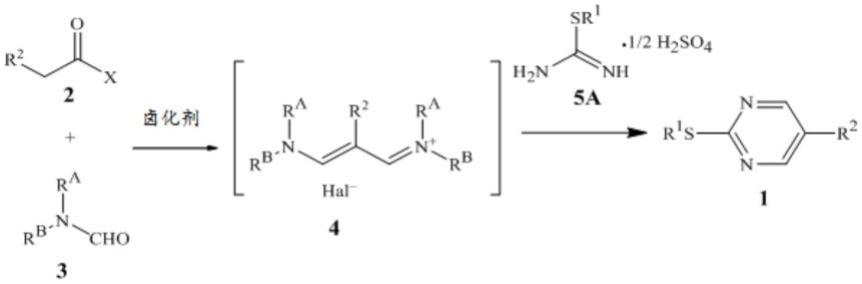
本发明涉及一种用于制备具有式1的化合物的方法
[0004][0005]
其中
[0006]
r1是c
1-c4烷基;并且
[0007]
r2是卤素、c
1-c4烷基或c
1-c4卤代烷基;
[0008]
该方法包括处理具有式2的化合物
[0009][0010]
其中
[0011]
r2是卤素、c
1-c4烷基或c
1-c4卤代烷基;并且
[0012]
x是cl或oh
[0013]
该处理是在卤化剂和具有式3的化合物的存在下
[0014][0015]
其中
[0016]
ra和rb各自独立地是c
1-c4烷基;或者
[0017]
ra和rb合在一起是-(ch2)
4-、-(ch2)
5-或-ch2ch2och2ch
2-以提供具有式4的中间体
[0018][0019]
其中
[0020]
r2是卤素、c
1-c4烷基或c
1-c4卤代烷基;并且
[0021]
ra和rb各自独立地是c
1-c4烷基;或者
[0022]
ra和rb合在一起是-(ch2)
4-、-(ch2)
5-或-ch2ch2och2ch
2-;并且
[0023]
hal-是氯离子或溴离子;以及
[0024]
在碱的存在下用具有式5的化合物的酸式盐处理该具有式4的中间体
[0025][0026]
其中r1是c
1-c4烷基。
[0027]
本发明还提供了一种用于制备具有式8的化合物的方法
[0028][0029]
其中
[0030]
r2是卤素、c
1-c4烷基或c
1-c4卤代烷基;
[0031]
每个r3独立地是卤素、氰基、氨基、c
1-c4烷基、c
2-c4烯基、c
2-c4炔基、c
1-c4烷氧基、c
2-c4烷氧基羰基、c
2-c4烷基羰基氧基、c
2-c4烷氧基烷基或c
1-c4卤代烷基;
[0032]
每个r4独立地是卤素、氰基、c
1-c4烷基、c
1-c4烷氧基、c
1-c4卤代烷基、c
1-c4卤代烷氧基或scf3;
[0033]
m是0、1、2或3;并且
[0034]
r是0、1或2;
[0035]
该方法包括处理具有式2的化合物
[0036][0037]
其中
[0038]
r2是卤素、c
1-c4烷基或c
1-c4卤代烷基;并且
[0039]
x是cl或oh
[0040]
该处理是在卤化剂和具有式3的化合物的存在下
[0041][0042]
其中
[0043]
ra和rb各自独立地是c
1-c4烷基;或者
[0044]
ra和rb合在一起是-(ch2)
4-、-(ch2)
5-或-ch2ch2och2ch
2-[0045]
以提供具有式4的中间体
[0046][0047]
其中
[0048]
r2是卤素、c
1-c4烷基或c
1-c4卤代烷基;并且
[0049]
ra和rb各自独立地是c
1-c4烷基;或者
[0050]
ra和rb合在一起是-(ch2)
4-、-(ch2)
5-或-ch2ch2och2ch
2-;并且
[0051]
hal-是氯离子或溴离子;
[0052]
用具有式5的化合物的酸式盐处理该具有式4的中间体
[0053][0054]
其中r1是c
1-c4烷基;
[0055]
该处理是在碱的存在下以制备具有式1的化合物
[0056]
[0057]
其中
[0058]
r1是c
1-c4烷基;
[0059]
r2是卤素、c
1-c4烷基或c
1-c4卤代烷基;
[0060]
用氧化剂处理该具有式1的化合物以提供具有式6的化合物
[0061][0062]
其中
[0063]
r1是c
1-c4烷基;并且
[0064]
r2是卤素、c
1-c4烷基或c
1-c4卤代烷基;以及
[0065]
在第二种碱的存在下用具有式7的化合物处理该具有式6的化合物
[0066][0067]
其中
[0068]
每个r3独立地是卤素、氰基、氨基、c
1-c4烷基、c
2-c4烯基、c
2-c4炔基、c
1-c4烷氧基、c
2-c4烷氧基羰基、c
2-c4烷基羰基氧基、c
2-c4烷氧基烷基或c
1-c4卤代烷基;
[0069]
每个r4独立地是卤素、氰基、c
1-c4烷基、c
1-c4烷氧基、c
1-c4卤代烷基、c
1-c4卤代烷氧基或scf3;
[0070]
m是0、1、2或3;并且
[0071]
r是0、1或2。
具体实施方式
[0072]
如本文所使用的,术语“包含(comprises)”、“包含(comprising)”、“包括(includes)”、“包括(including)”、“具有(has)”、“具有(having)”、“含有(contains)”、“含有(containing)”、“特征为(characterized by)”或其任何其他变体,旨在涵盖非排他性包括,受到明确指出的任何限制。例如,包含一系列要素的组合物、混合物、工艺或方法不一定仅限于那些要素,而是可以包括未明确列出的其他要素或此类组合物、混合物、工艺或方法固有的其他要素。
[0073]
连接短语“由
……
组成”排除任何未指出的要素、步骤或成分。如果在权利要求中,则此短语将使权利要求为封闭式,不包括除所述那些外的材料,但与其通常相关的杂质除外。当短语“由
……
组成”出现在权利要求主体的子句中而非紧接前序部分时,该短语仅仅限制该子句中阐述的要素;整体上,该权利要求并不排除其他要素。
[0074]
连接词“基本上由
……
组成”用于定义组合物、工艺或方法,其包括除字面上所披
露的那些之外的材料、步骤、特征、组分或要素,前提是这些另外的材料、步骤、特征、组分或要素不会实质性地影响所要求保护的发明的基本和新颖特征。术语“基本上由
……
组成”居于“包含”和“由
……
组成”中间。
[0075]
当申请人已经用开放式术语如“包含”定义了本发明或其一部分时,则应易于理解(除非另外指明),说明书应被解释为还使用术语“基本上由
……
组成”或“由
……
组成”描述本发明。
[0076]
此外,除非明确相反地指出,否则“或”是指包含性的或而非排他性的或。例如,条件a或b由以下中任一个满足:a为真(或存在)且b为假(或不存在)、a为假(或不存在)且b为真(或存在)以及a和b皆为真(或存在)。
[0077]
另外,在本发明的要素或组分之前的不定冠词“一个/一种(a和an)”旨在关于该要素或组分的实例(即,出现)数量是非限制性的。因此,“一个/一种(a或an)”应被理解为包括一个/一种或至少一个/一种,并且要素或组分的单数单词形式也包括复数,除非数字显然意指单数。
[0078]
如本文所使用的,术语“合适的”表示如此描述的实体适合于在所示的情况或环境中使用。如本文所使用的,术语“处理(treatment)”、“处理(treating)”等表示使用化学、化学工艺或工艺条件(例如加热)来改变其他材料或化合物的现有条件。
[0079]
如本文所使用的,术语“中间体”是指化学工艺中的化合物或化学实体,其在提供起始材料后且在制备最终产物前的步骤中制备。在一些情况下,中间体在化学工艺过程中没有被分离,而是原位转化为后续的化合物。本文中可以使用一组包围中间体的化学结构的括号来表示在将中间体转化为后续的化合物之前中间体没有被分离;例如“[中间体]”。
[0080]
如本文所使用的,术语“伸缩性(telescopic)”是指其中在工艺中形成的至少一种中间体化合物在工艺的后续步骤中进行处理而未将其分离的工艺。例如,化合物可以只在一个反应器中进行连续的化学反应。
[0081]
如本文所使用的,“碱金属”是指周期表第1族的元素,包括锂、钠、钾和铯,优选钠或钾,或其阳离子,如当与阴离子抗衡离子结合使用以定义化合物时。
[0082]
在以上详述中,术语“烷基”,单独使用或在复合词如“烷硫基”或“卤代烷基”中使用,包括直链或支链的烷基,如甲基、乙基、正丙基、异丙基、或不同的丁基、戊基、或己基异构体。“烯基”包括直链或支链的烯烃,如乙烯基、1-丙烯基、2-丙烯基和不同的丁烯基、戊烯基和己烯基异构体。“烯基”还包括多烯,如1,2-丙二烯基和2,4-己二烯基。“炔基”包括直链或支链的炔烃,如乙炔基、1-丙炔基、2-丙炔基和不同的丁炔基、戊炔基和己炔基异构体。
[0083]“烷氧基”包括例如甲氧基、乙氧基、正丙氧基、异丙氧基和不同的丁氧基、戊氧基和己氧基异构体。“烷氧基烷基”表示烷基上的烷氧基取代。“烷氧基烷基”的实例包括ch3och2、ch3och2ch2、ch3ch2och2、ch3ch2ch2och2和ch3ch2och2ch2。“烷硫基”包括支链或直链的烷硫基部分,如甲硫基、乙硫基和不同的丙硫基、丁硫基、戊硫基和己硫基异构体。
[0084]
术语“卤素”,单独地或在复合词如“卤代烷基”中,或者当在描述如“被卤素取代的烷基”中使用时,包括氟、氯、溴或碘。此外,当在复合词如“卤代烷基”中使用时,或者当在描述如“被卤素取代的烷基”中使用时,所述烷基可以是被卤素原子(其可以是相同的或不同的)部分地或完全地取代的。“卤代烷基”或“被卤素取代的烷基”的实例包括chf2、f3c、clch2、cf3ch2和cf3ccl2。
[0085]
术语“卤代烷氧基”等类似于术语“卤代烷基”所定义。“卤代烷氧基”的实例包括cf3o-、ccl3ch2o-、hcf2ch2ch2o-和cf3ch2o-。“烷基羰基”表示键合到c(=o)部分上的直链或支链的烷基部分。“烷基羰基”的实例包括ch3c(=o)-、ch3ch2ch2c(=o)-和(ch3)2chc(=o)-。“烷氧基羰基”的实例包括ch3oc(=o)-、ch3ch2oc(=o)-、ch3ch2ch2oc(=o)-、(ch3)2choc(=o)-和不同的丁氧基-或戊氧基羰基异构体。“烷基羰基氧基”表示键合到c(=o)o-部分上的直链或支链的烷基部分。“烷基羰基氧基”的实例包括ch3c(=o)o-、ch3ch2ch2c(=o)o-和(ch3)2chc(=o)o-。
[0086]
在取代基中的碳原子的总数用“c
i-c
j”前缀表示,其中例如i和j是从1至4的数。例如,c
1-c4烷基磺酰基表示甲基磺酰基至丁基磺酰基;c2烷氧基烷基表示ch3och
2-;c3烷氧基烷基表示例如ch3ch(och3)-、ch3och2ch
2-或ch3ch2och
2-;并且c4烷氧基烷基表示被含有总共四个碳原子的烷氧基取代的烷基的各种异构体,实例包括ch3ch2ch2och
2-和ch3ch2och2ch
2-。
[0087]
当化合物被带有下标(其表示所述取代基的数目可以超过1)的取代基取代时,所述取代基(当它们超过1时)独立地选自所定义的取代基的组,(例如,(r3)m,m是0、1、2或3)。当基团含有可以是氢的取代基,例如(当m=0时),则当该取代基为氢时,认为这等同于所述基团是未被取代的。当显示出可变基团任选地附接到一个位置,例如(r3)m其中m可以是0时,则氢可以位于该位置,即使在可变基团定义中没有提及。当基团上的一个或多个位置被称为是“没有被取代的”或“未被取代的”时,则附接氢原子以占据任何自由价。
[0088]
术语“任选地”当在本文中使用时意指任选的条件可以存在或可以不存在。例如,当反应任选地在溶剂的存在下进行时,该溶剂可以存在或可以不存在。
[0089]
术语“任选地取代的”是指这样的基团,其为未被取代的或具有至少一个不消除由未被取代的类似物所具有的化学或生物活性的非氢取代基。如本文所使用的,除非另外指明,否则将应用下列定义。术语“任选地被
……
取代的”与短语“未被取代的或被
……
取代的”或与术语“(未)被
……
取代的”可互换使用。除非另外指明,否则任选地取代的基团可在基团的每个可取代的位置处具有取代基,并且每个取代彼此独立。
[0090]
本发明的实施例包括以下。
[0091]
实施例a1.如在发明内容中所述的用于制备具有式1的化合物的方法。
[0092]
实施例a2.如实施例a1所述的方法,其中r1是c
1-c2烷基。
[0093]
实施例a3.如实施例a2所述的方法,其中r1是甲基。
[0094]
实施例a4.如实施例a1至a3中任一项所述的方法,其中该酸式盐是半硫酸盐。
[0095]
实施例a5.如实施例a1至a4中任一项所述的方法,其中r2是卤素。
[0096]
实施例a6.如实施例a5所述的方法,其中r2是氯。
[0097]
实施例a7.如实施例a1至a6中任一项所述的方法,其中x是cl。
[0098]
实施例a8.如实施例a1至a6中任一项所述的方法,其中x是oh。
[0099]
实施例a9.如实施例a1至a8中任一项所述的方法,其中该卤化剂是pocl3。
[0100]
实施例a9a.如实施例a1至a8中任一项所述的方法,其中该卤化剂是维尔斯迈尔-哈克试剂(vilsmeier-haack reagent)。
[0101]
实施例a10.如实施例a1至a9中任一项所述的方法,其中ra和rb各自独立地是c
1-c4烷基。
[0102]
实施例a11.如实施例a10所述的方法,其中ra和rb各自独立地是c
1-c2烷基。
[0103]
实施例a12.如实施例a11所述的方法,其中ra和rb各自是甲基。
[0104]
实施例a13.如实施例a1至a12中任一项所述的方法,其中该碱选自碱金属醇化物、碱金属乙酸盐、碱金属氢氧化物和叔胺。
[0105]
实施例a14.如实施例a1至a13中任一项所述的方法,其中该处理是在合适的溶剂中进行。
[0106]
实施例b1.如实施例a1至a14中任一项所述的方法,其进一步包括制备具有式6的化合物
[0107][0108]
其中
[0109]
r1是c
1-c4烷基;并且
[0110]
r2是卤素、c
1-c4烷基或c
1-c4卤代烷基
[0111]
该制备是通过用氧化剂处理具有式1的化合物。
[0112]
实施例b2.如实施例b1所述的方法,其中r1是c
1-c2烷基。
[0113]
实施例b3.如实施例b2所述的方法,其中r1是甲基。
[0114]
实施例b4.如实施例b1至b3中任一项所述的方法,其中r2是卤素。
[0115]
实施例b5.如实施例b4所述的方法,其中r2是氯。
[0116]
实施例b6.如实施例b1至b5中任一项所述的方法,其中该氧化剂选自间氯过氧苯甲酸、高碘酸钠、高锰酸钾、过氧一硫酸钾和过氧化氢。
[0117]
实施例b7.如实施例b6所述的方法,其中该氧化剂选自间氯过氧苯甲酸、过氧一硫酸钾和过氧化氢。
[0118]
实施例b8.如实施例b7所述的方法,其中该氧化剂是间氯过氧苯甲酸。
[0119]
实施例c1.如实施例a1至a14和b1至b8中任一项所述的方法,其进一步包括制备具有式8的化合物
[0120][0121]
其中
[0122]
r2是卤素、c
1-c4烷基或c
1-c4卤代烷基;
[0123]
每个r3独立地是卤素、氰基、氨基、c
1-c4烷基、c
2-c4烯基、c
2-c4炔基、c
1-c4烷氧基、c
2-c4烷氧基羰基、c
2-c4烷基羰基氧基、c
2-c4烷氧基烷基或c
1-c4卤代烷基;
[0124]
每个r4独立地是卤素、氰基、c
1-c4烷基、c
1-c4烷氧基、c
1-c4卤代烷基、c
1-c4卤代烷氧基或scf3;
[0125]
m是0、1、2或3;并且
[0126]
r是0、1或2;
[0127]
该制备是通过处理该具有式6的化合物
[0128][0129]
其中
[0130]
r1是c
1-c4烷基;并且
[0131]
r2是卤素、c
1-c4烷基或c
1-c4卤代烷基
[0132]
该处理是在第二种碱的存在下用具有式7的化合物
[0133][0134]
其中
[0135]
每个r3独立地是卤素、氰基、氨基、c
1-c4烷基、c
2-c4烯基、c
2-c4炔基、c
1-c4烷氧基、c
2-c4烷氧基羰基、c
2-c4烷基羰基氧基、c
2-c4烷氧基烷基或c
1-c4卤代烷基;
[0136]
每个r4独立地是卤素、氰基、c
1-c4烷基、c
1-c4烷氧基、c
1-c4卤代烷基、c
1-c4卤代烷氧基或scf3;
[0137]
m是0、1、2或3;并且
[0138]
r是0、1或2。
[0139]
实施例c2.如实施例c1所述的方法,其中r2是卤素。
[0140]
实施例c3.如实施例c2所述的方法,其中r2是氯。
[0141]
实施例c4.如实施例c1至c3中任一项所述的方法,其中m是0。
[0142]
实施例c5.如实施例c1至c3中任一项所述的方法,其中每个r3独立地是卤素、氰基、c
1-c4烷基或c
1-c4卤代烷基。
[0143]
实施例c6.如实施例c5所述的方法,其中每个r3独立地是卤素或氰基。
[0144]
实施例c7.如实施例c6所述的方法,其中每个r3独立地是氰基。
[0145]
实施例c8.如实施例c6所述的方法,其中每个r3独立地是氯。
[0146]
实施例c9.如实施例c6所述的方法,其中每个r3独立地是溴。
[0147]
实施例c10.如实施例c1至c3和c5至c9中任一项所述的方法,其中m是1或2并且r3在3位或4位或者在3位和4位附接至式7或式8的其余部分。
[0148]
实施例c11.如实施例c10所述的方法,其中m是1。
[0149]
实施例c12.如实施例c11所述的方法,其中r3在3位附接至式7或式8的其余部分。
[0150]
实施例c13.如实施例c11所述的方法,其中r3在4位附接至式7或式8的其余部分。
氯-2-[3-氯-2-[3-(二氟甲基)-5-异噁唑基]-苯氧基]-嘧啶;cas号1801862-02-1)。
[0180]
实施例c29.如实施例c1至c28中任一项所述的方法,其中该具有式8的化合物是使用具有式6的化合物(通过如实施例b1至b8中任一项所述的方法制备)和具有式1的化合物(如实施例a1至a14中任一项所述制备)制备的。
[0181]
实施例d1.经由具有式5a的化合物的酸式盐制备发明内容的具有式8的化合物的方法
[0182][0183]
其中r1是c
1-c4烷基。
[0184]
实施例d2.如实施例d1所述的方法,其中r1是c
1-c2烷基。
[0185]
实施例d3.如实施例d2所述的方法,其中r1是甲基。
[0186]
实施例d4.如实施例d1至d3中任一项所述的方法,其中该酸式盐是半硫酸盐。
[0187]
实施例d5.如实施例d1至d4中任一项所述的方法,其中r2是卤素。
[0188]
实施例d6.如实施例d6所述的方法,其中r2是氯。
[0189]
实施例d7.如实施例d1至d6中任一项所述的方法,其中x是cl。
[0190]
实施例d8.如实施例d1至d6中任一项所述的方法,其中x是oh。
[0191]
实施例d9.如实施例d1至d8中任一项所述的方法,其中该卤化剂是pocl3。
[0192]
实施例a9a.如实施例a1至a8中任一项所述的方法,其中该卤化剂是维尔斯迈尔-哈克试剂。
[0193]
实施例d10.如实施例d1至d9中任一项所述的方法,其中ra和rb各自独立地是c
1-c4烷基。
[0194]
实施例d11.如实施例d10所述的方法,其中ra和rb各自独立地是c
1-c2烷基。
[0195]
实施例d12.如实施例d11所述的方法,其中ra和rb各自是甲基。
[0196]
实施例d13.如实施例d1至d12中任一项所述的方法,其中该碱选自碱金属醇化物、碱金属乙酸盐、碱金属氢氧化物和叔胺。
[0197]
实施例d14.如实施例d1至d13中任一项所述的方法,其中该处理是在合适的溶剂中进行。
[0198]
实施例d15.如实施例d1至d14中任一项所述的方法,其中该氧化剂选自间氯过氧苯甲酸、高碘酸钠、高锰酸钾、过氧一硫酸钾和过氧化氢。
[0199]
实施例d16.如实施例d15所述的方法,其中该氧化剂选自间氯过氧苯甲酸、过氧一硫酸钾和过氧化氢。
[0200]
实施例d17.如实施例d16所述的方法,其中该氧化剂是间氯过氧苯甲酸。
[0201]
实施例d18.如实施例d1至d17中任一项所述的方法,其中m是0。
[0202]
实施例d19.如实施例d1至d17中任一项所述的方法,其中每个r3独立地是卤素、氰基、c
1-c4烷基或c
1-c4卤代烷基。
[0203]
实施例d20.如实施例d19所述的方法,其中每个r3独立地是卤素或氰基。
[0204]
实施例d21.如实施例d20所述的方法,其中每个r3独立地是氰基。
[0205]
实施例d22.如实施例d20所述的方法,其中每个r3独立地是氯。
[0206]
实施例d23.如实施例d20所述的方法,其中每个r3独立地是溴。
[0207]
实施例d24.如实施例d1至d17和d19至d23中任一项所述的方法,其中m是1或2并且r3在3位或4位或者在3位和4位附接至式7或式8的其余部分。
[0208]
实施例d25.如实施例d24所述的方法,其中m是1。
[0209]
实施例d26.如实施例d25所述的方法,其中r3在3位附接至式7或式8的其余部分。
[0210]
实施例d27.如实施例d25所述的方法,其中r3在4位附接至式7或式8的其余部分。
[0211]
实施例d28.如实施例d1至d27中任一项所述的方法,其中每个r4独立地是卤素、氰基、c
1-c4烷基、c
1-c4卤代烷基或c
1-c4卤代烷氧基。
[0212]
实施例d29.如实施例d28所述的方法,其中每个r4是卤素或c
1-c4卤代烷基。
[0213]
实施例d30.如实施例d29所述的方法,其中每个r4是c
1-c4卤代烷基。
[0214]
实施例d31.如实施例d310所述的方法,其中每个r4是c
1-c4氟烷基。
[0215]
实施例d32.如实施例d31所述的方法,其中每个r4是c1氟烷基。
[0216]
实施例d33.如实施例d1至d32中任一项所述的方法,其中r是0或1。
[0217]
实施例d34.如实施例d33所述的方法,其中r是1。
[0218]
实施例d35.如实施例d35所述的方法,其中r4在3'位被取代。
[0219]
实施例d36.如实施例d1至d35中任一项所述的方法,其中该第二种碱选自碱金属醇化物、碱金属乙酸盐、碱金属氢氧化物和叔胺。
[0220]
实施例d37.如实施例d36所述的方法,其中该第二种碱是碱金属碳酸盐。
[0221]
实施例d38.如实施例d37所述的方法,其中该第二种碱是碳酸钾。
[0222]
实施例d39.如实施例d1所述的方法,其中该具有式8的化合物选自由以下组成的组
[0223]
2-[2-(3-溴-5-异噁唑基)苯氧基]-5-氯嘧啶,
[0224]
5-氯-2-[2-[3-(二氟甲基)-5-异噁唑基]苯氧基]嘧啶,
[0225]
5-氯-2-[2-[3-(三氟甲基)-5-异噁唑基]苯氧基]嘧啶,
[0226]
5-氯-2-[2-[3-(二氟甲基)-5-异噁唑基]-3-氟苯氧基]嘧啶,
[0227]
5-溴-2-[2-[3-(二氟甲基)-5-异噁唑基]-3-氟苯氧基]嘧啶,
[0228]
5-氯-2-[2-[3-(三氟甲基)-5-异噁唑基]-3-氯苯氧基]嘧啶,
[0229]
5-氯-2-[2-[3-(三氟甲基)-5-异噁唑基]-3-氟苯氧基]嘧啶,
[0230]
5-氯-2-[2-[3-(二氟甲基)-5-异噁唑基]-3-氯苯氧基]嘧啶,
[0231]
5-溴-2-[2-[3-(二氟甲基)-5-异噁唑基]-3-氯苯氧基]嘧啶,
[0232]
5-溴-2-[2-[3-(三氟甲基)-5-异噁唑基]-3-氯苯氧基]嘧啶,和
[0233]
5-氯-2-[2-[3-(二氟甲基)-5-异噁唑基]-3-溴苯氧基]嘧啶。
[0234]
实施例d40.如实施例d39所述的方法,其中该具有式8的化合物是具有式8a的化合物
[0235][0236]
即5-氯-2-[2-[3-(二氟甲基)-5-异噁唑基]-3-氯苯氧基]嘧啶(可替代地称为5-氯-2-[3-氯-2-[3-(二氟甲基)-5-异噁唑基]-苯氧基]-嘧啶;cas号1801862-02-1)。
[0237]
本发明的实施例(包括上述实施例a1至a14、b1至b8、c1至c29和d1至d40以及本文所述的任何其他实施例)可以以任何方式组合,并且实施例中的变量的描述不仅涉及具有式8的化合物,而且还涉及可用于制备具有式8的化合物的具有式1至7的起始化合物和中间体化合物。
[0238]
优选的实施例包括:
[0239]
实施例p1.如发明内容或实施例a1至a14、b1至b8、c1至c29和d1至d40中任一项所述的方法,其中
[0240]
r1是c
1-c2烷基;并且
[0241]
每个ra和rb是甲基。
[0242]
实施例p2.如实施例p1所述的方法,其中r1是甲基并且r2是卤素。
[0243]
实施例p3.如实施例p2所述的方法,其中r2是氯。
[0244]
实施例p4.如实施例p1所述的方法,其中x是cl。
[0245]
实施例p5.如实施例c1至c29中任一项、实施例d1至d49或实施例p1至p4中任一项所述的方法,其中
[0246]
m是0或1;
[0247]
r是0或1;
[0248]
r2是卤素;
[0249]
r3是卤素、氰基、c
1-c4烷基或c
1-c4卤代烷基,其中当m是1时,r3在3位附接至式7和式8的其余部分;并且
[0250]
r4是c
1-c4卤代烷基,其中当r是1时,r4在3'位被取代。
[0251]
实施例p6.如实施例p5所述的方法,其中r2和r3二者都是氯。
[0252]
实施例p7.如实施例p1至p5中任一项所述的方法,其中r4是c1氟烷基。
[0253]
在以下方案中,除非另外指明,否则以下具有式1至8的化合物中的x、ra、rb、r1、r2、r3、r4、m和r的定义是如以上在发明内容和具体实施方式中所定义的。
[0254]
本文所述的方法提供了可用于制备具有式8的除草化合物的具有式1和6的经取代的嘧啶的有效且稳健的合成。
[0255]
如方案1所示,可以以伸缩性方式制备具有式1的化合物,其包括任选地在合适的溶剂中,用卤化剂处理具有式2的化合物和具有式3的化合物,以得到具有式4的中间体,以及在碱的存在下用具有式5的化合物的酸式盐处理具有式4的中间体而未将其分离。合适的
卤化剂包括pocl3、pobr3、socl2、sobr2、(cocl)2或cocl2,优选pocl3、socl2、(cocl)2或cocl2。当使用溴化剂时,式4中的hal-是溴离子并且当使用氯化剂时,式4中的hal-是氯离子。三氯氧磷,pocl3,是更优选的卤化剂。可替代地,卤化剂可通过使cocl2与n,n-二甲基甲酰胺反应预先制备,以作为维尔斯迈尔-哈克试剂。合适的溶剂包括n,n-二甲基甲酰胺、二氯乙烷、甲苯、或乙腈。用于此反应的合适的碱包括碱金属醇化物,如甲醇钠和异丙醇钠;或碱金属乙酸盐,如乙酸钠和乙酸钾;碱金属氢氧化物,如氢氧化钠;或叔胺,如三乙胺和二异丙基乙胺。n,n-二甲基甲酰胺是优选的具有式3的化合物。在一些实施例中,尤其是当具有式3的化合物是n,n-二甲基甲酰胺时,可使用过量的具有式3的化合物代替额外的溶剂。具有式2的化合物和卤化剂可以以任何顺序顺序地或同时地添加到具有式3的化合物中。优选的酸式盐是方案1中所示的具有式5a的半硫酸盐。
[0256]
方案1
[0257][0258]
如方案2所示,具有式6的烷基磺酰基嘧啶化合物可通过在合适的溶剂或溶剂混合物(如水、二氯甲烷、甲醇、乙腈、乙酸、或乙酸乙酯)中,用氧化剂(如间氯过氧苯甲酸、高碘酸钠、高锰酸钾、过氧一硫酸钾或过氧化氢)氧化具有式1的化合物制备。
[0259]
方案2
[0260][0261]
如方案3所示,本发明还涉及一种用于制备具有式8的化合物的方法,其是通过通常在碱和溶剂的存在下将具有式6的嘧啶(如以上在方案1和2中所述制备)与具有式7的苯酚偶联。合适的溶剂包括乙腈、甲苯、异丙醇、四氢呋喃、二甲基亚砜或n,n-二甲基甲酰胺。用于反应的合适的碱包括碱金属氢化物,如氢化钠;或碱金属醇化物,如异丙醇钠和叔丁醇钾;或碱金属氢氧化物,如氢氧化钾和氢氧化钠;或碱金属碳酸盐,如碳酸钾和碳酸铯;或碱,如双(三甲基甲硅烷基)氨基锂、双(三甲基甲硅烷基)氨基钠和二异丙基氨基锂;或叔胺,如三乙胺和二异丙基乙胺。优选地,具有式8的化合物可通过亲核取代通过在合适的溶剂(如乙腈或n,n-二甲基甲酰胺)中,在碱(如碳酸钾或碳酸铯)的存在下,在范围从20℃至110℃或从50℃至110℃的温度下,将具有式6的化合物与具有式7的化合物加热制备。
[0262]
方案3
[0263][0264]
具有式7的化合物可以如wo 2015/108779中所述制备。
[0265]
如方案4所示,具有式7的化合物可通过用合适的去保护剂将具有式9的化合物(其中r
p
是ch3或-c(=o)ch3)去保护制备。合适的甲氧基(即当r
p
是ch3时)去保护剂(如乙酸中的bbr3、alcl3和hbr)可在从-80℃至120℃的温度下在溶剂(如甲苯、二氯甲烷和二氯乙烷)的存在下使用。合适的乙酰氧基(即当r
p
是-c(=o)ch3时)去保护剂包括甲醇中的碳酸钾或含水甲醇中的乙酸铵,可在室温下使用,如das,等人,tetrahedron[四面体]2003,59,1049-1054和所引用的方法中讨论的。可替代地,具有式9的化合物可与甲醇中的强酸性离子交换树脂如15(用磺酸部分官能化的微孔苯乙烯二乙烯基苯基质,从密歇根州米德兰陶氏化学公司(dow chemical,midland michigan)可获得)结合(如das,等人tet.lett.[四面体通讯]2003,44,5465-5468中所讨论)或与乙醇中的乙酸钠结合(如narender,t.,等人synthetic communications[合成通讯]2009,39(11),1949-1956中所讨论),以获得具有式7的化合物。适合用于制备具有式7的化合物的其他有用的酚保护基团可在greene,t.w.;wuts,p.g.m.protective groups in organic synthesis[有机合成中的保护基团],第4版;威利出版社(wiley):霍博肯,新泽西州,1991中找到。
[0266]
方案4
[0267][0268]
具有式9的中间体化合物可以如方案5一般所示由具有式10的中间体化合物通过本领域技术人员已知的多种方法制备。
[0269]
方案5
[0270][0271]
具有式9的化合物可以通过使用铃木(suzuki)条件或施蒂勒(stille)条件将具有式10的前体(其中j是br、cl、i或三氟甲磺酸酯)与含有硼酸盐或三烷基锡基团的异噁唑杂环偶联获得。铃木偶联通常是在pd(0)或pd(ii)盐、合适的配体和碱的存在下进行。用于此转化的合适的碱包括碳酸钾或碳酸铯,而pd(ii)盐(如pd(oac)2或pdcl2)可以与配体(如三苯基膦或1,1'-双(二苯基膦基)二茂铁(dppf))结合使用。铃木偶联的条件详尽记录在文献中(参见例如angewandte chemie international edition[应用化学国际版]2006,45,3484和tetrahedron letters[四面体通讯]2002,58(14),2885)。硼杂环中间体是可商购的或可以通过文献中已知的方法从相应的卤化物或三氟甲磺酸盐制备(参见例如pct专利公开wo 2007/043278,美国专利号8,080,566,organic letters[有机化学通讯]2011,13(6),1366和organic letters[有机化学通讯]2012,14(2),600)。施蒂勒偶联通常可在pd(0)或pd(ii)盐、配体和cu(i)盐(如碘化铜(i))的存在下进行。反应可在范围从环境温度至溶剂的回流温度的温度下在溶剂(如二噁烷、1,2-二甲氧基乙烷或甲苯)中进行。关于施蒂勒偶联中使用的条件和试剂,参见chemical reviews[化学综述]2007,107(1),133-173。
[0272]
可替代地,具有式10的化合物(其中j是硼酸盐或三烷基锡基团)可以使用铃木或施蒂勒方法与卤素取代的异噁唑基杂环(即异噁唑-x)其中x是卤素偶联,以提供具有式9的化合物。熟练的化学人员将意识到,在涉及具有式10的化合物和异噁唑-x的反应中谨慎地选择基团x和j,可以利用“metal-catalyzed cross-coupling reactions[金属催化的交叉偶联反应]”,编辑a.de meijere和f.diederich,威利-vch出版社(wiley-vch),魏因海姆(weinheim),2004,第1和2卷中所述的各种交叉偶联程序如熊田偶联(kumada coupling)、桧山偶联(hiyama coupling)或根岸偶联(negishi coupling)合成具有式7的化合物。
[0273]
当式10中的j是烯、炔、肟、腈或酮时,可以使用katritsky,advances in heterocyclic chemistry[杂环化学进展],第1-104卷,爱思唯尔(elsevier)中所述的方法制备各种杂环。在产生区域异构混合物的情况下,可以使用本领域已知的常规分离技术分离所期望的产物。
[0274]
值得注意地,如方案6所示,具有式7a的化合物可通过以下制备:在碱的存在下用具有式12的酰化剂lg(c=o)r4(其中lg是氯、烷氧基或-o(c=o)r4)处理具有式11的2-羟苯乙酮,以制备具有式13的4h-1-苯并吡喃-4-酮
[0275]
其中
[0276]
每个r3独立地是卤素、氰基、氨基、c
1-c4烷基、c
2-c4烯基、c
2-c4炔基、c
1-c4烷氧基、c
2-c4烷氧基羰基、c
2-c4烷基羰基氧基、c
2-c4烷氧基烷基或c
1-c4卤代烷基;其中每个r3在5位或6位附接至具有式13的4h-1-苯并吡喃-4-酮的其余部分;并且
[0277]
r4是氰基、c
1-c4烷基、或c
1-c4卤代烷基;
[0278]
用羟胺盐处理具有式13的4h-1-苯并吡喃-4-酮;以及用酸处理所得的具有式14的1-(2-羟苯基)-丁烷-1,3-二酮3-肟。在一些情况下,可以处理具有式14的化合物以提供异噁唑的环化,以便形成具有式7a的化合物而无需从反应混合物中分离。
[0279]
方案6
[0280][0281]
可替代地,具有式13的化合物可以如方案7中所示制备。用甲基氯化镁处理具有式15的腈接着水解提供具有式16的邻卤代苯乙酮。值得注意地,x1是氯。在一些情况下,具有式16的化合物可以是可商购的。在碱的存在下用具有式12的酰化剂lg(c=o)r4(其中lg是氯、烷氧基或-o(c=o)r4)处理具有式16的化合物提供具有式17的化合物,其可随邻位卤素的置换而环化,以提供具有式13的化合物。在一些实施例中,具有式17的化合物在具有式16的化合物的酰化条件下环化成具有式13的化合物,或通过加热具有式17的化合物,例如在约100℃至200℃、或约120℃至约180℃、或约140℃至约160℃的温度下。在此类实施例的任一个中,无需分离具有式17的化合物。
[0282]
方案7
[0283][0284]
类似地,如方案8所示,具有式7a的化合物可由具有式18的2-甲氧基苯乙酮通过在碱的存在下用具有式12的酰化剂lg(c=o)r4(其中lg是烷氧基或-o(c=o)r4)处理以制备具有式19的二酮化合物来制备。可以用羟胺盐处理具有式19的化合物以提供具有式21的化合
物,其可以如关于方案4所述去保护以提供具有式7a的化合物。
[0285]
方案8
[0286][0287]
应认识到,以上对于制备具有式1-21的化合物所描述的一些试剂和反应条件可能不与中间体中存在的某些官能团相容。在这些情况下,将保护/去保护序列或官能团相互转化结合到合成中将有助于获得所期望的产物。保护基团的使用和选择对于化学合成领域的技术人员来说将是显而易见的(参见,例如greene,t.w.;wuts,p.g.m.protective groups in organic synthesis[有机合成中的保护基团],第2版;威利出版社:纽约,1991)。本领域技术人员将认识到,在一些情况下,在按照任何单独方案中描绘的引入给定试剂后,可能必需进行没有详细描述的额外常规合成步骤以完成具有式1-18的化合物的合成。本领域技术人员还将认识到,可能必需以与制备具有式1-21的化合物所呈现的具体序列所暗含的不同的顺序来进行以上方案中示出的步骤的组合。本领域技术人员还将认识到,本文所述的具有式1-21的化合物和中间体可经受各种亲电反应、亲核反应、自由基反应、有机金属反应、氧化反应和还原反应以添加取代基或改性现有的取代基。
[0288]
无需进一步详细阐述,据信本领域技术人员使用先前描述可以最大程度地利用本发明。因此,以下实例应被解释为仅是说明性的,并且无论如何不以任何方式限制本披露。以下实例中的步骤示出了在整体合成转化中每个步骤的程序,并且用于每个步骤的起始材料并不必须由其程序描述于其他实例或步骤中的具体制备试验来制备。百分比是按重量计。缩写“h”代表“小时(hour或hours)”;“hplc”意指高效液相色谱法。1h nmr谱以四甲基硅烷的低场处的ppm来报告;s是单峰,d是双峰,dd是双二重峰,t是三重峰并且m是多重峰。
[0289]
合成实例1
[0290]
5-氯-2-(甲硫基)-嘧啶(cas号38275-42-2)的制备
[0291]
向配备有顶置式搅拌器、热电偶、再循环加热和冷却浴、氮气入口和洗涤器的100ml夹套反应器中添加41ml的n,n-二甲基甲酰胺,并将反应器加热至50℃。滴加氯乙酰氯(10g,88.5mmol),并将反应混合物在50℃下维持1h。然后将所得的混合物加热至70℃接着滴加三氯氧磷(13.6g,88.5mmol)以使温度维持在70℃与75℃之间。将反应在70℃下维持4h,并且然后冷却至50℃。将s-甲异硫脲半硫酸盐(12.3g,88.5mmol)添加到反应混合物中,接着添加固体甲醇钠(23.9g,443mmol)。将所得的混合物加热至60℃持续2h,并且然后冷却至40℃。将水(60ml)滴加到反应器中,并将所得的浆料缓慢冷却至20℃并搅拌2h。然后将固
体通过过滤收集,用水(20ml)洗涤,并在环境温度下干燥,以提供标题化合物即具有式1的化合物(8.5g,基于氯乙酰氯的产率为60%)。1h nmr(400mhz,dmso-d6)δ8.76(s,2h),2.53(s,3h)。m.p.=61.6℃。
[0292]
合成实例2
[0293]
5-氯-2-(甲硫基)-嘧啶(cas号38275-42-2)的替代制备
[0294]
向配备有顶置式搅拌器、热电偶、再循环加热和冷却浴、氮气入口和洗涤器的100ml夹套反应器中添加37ml的n,n-二甲基甲酰胺,接着滴加三氯氧磷(12.2g,79.7mmol),同时将温度维持在低于30℃。将反应混合物搅拌1h后,将其加热至70℃。滴加氯乙酰氯(9g,79.7mmol),并将反应混合物在70℃下维持4h。在冷却至环境温度后,将s-甲异硫脲半硫酸盐(11.1g,79.7mmol)添加到反应混合物中,接着添加固体乙酸钠(32.7g,398mmol)。将所得的混合物加热至60℃持续2h,并且然后冷却至40℃。将水(54ml)滴加到反应器中,并将所得的浆料缓慢冷却至20℃并搅拌2h。然后将固体通过过滤收集,用水(20ml)洗涤,并在环境温度下干燥,以提供7.6g的标题化合物即具有式1的化合物(90.8wt%,基于氯乙酰氯的产率为55%)。
[0295]
合成实例3
[0296]
5-氯-2-(甲硫基)-嘧啶(cas号38275-42-2)的替代制备
[0297]
向配备有顶置式搅拌器、热电偶、再循环加热和冷却浴、氮气入口和洗涤器的100ml夹套反应器中添加12.3g维尔斯迈尔-哈克试剂(92.9mmol)和30ml的n,n-二甲基甲酰胺。然后将所得的浆料加热至50℃。滴加10g氯乙酰氯(88.5mmol),以使反应温度维持在50℃与52℃之间,并将反应混合物在50℃下维持过夜。将所得的溶液冷却至环境温度并移至加料漏斗中。将17.6g三乙胺(177mmol)和30ml的n,n-二甲基甲酰胺添加到反应器中,并将混合物冷却至10℃。然后滴加加料漏斗中的溶液,同时使温度维持在低于25℃,并一次性添加13.3g的s-甲异硫脲半硫酸盐(97.4mmol)。然后将所得的反应混合物加热至70℃持续4h,并且冷却至20℃。将水(100ml)滴加到反应器中,并将所得的浆料搅拌2h。然后将固体通过过滤收集,用水洗涤(30ml x 2次),并在室温下干燥,以提供10.1g的标题产物(99.3wt%,基于氯乙酰氯的产率为72%)。1h nmr(400mhz,dmso-d6)δ8.76(s,2h),2.52(s,3h)。m.p.=61.6℃。
[0298]
合成实例4
[0299]
5-氯-2-(甲磺酰基)-嘧啶(cas号38275-47-7)的制备
[0300]
在环境温度下,向配备有顶置式搅拌器、热电偶、再循环加热和冷却浴和氮气入口的100ml夹套反应器中添加5-氯-2-(甲硫基)-嘧啶(即合成实例1、2或3的产物;5g,31.1mmol)和钨酸钠二水合物(0.52g,1.6mmol),接着添加水(15ml)和乙酸乙酯(15ml)。将所得的混合物加热至60℃,并且然后滴加50%含水过氧化氢(5.3g,77.7mmol)以使反应温度维持在60℃与65℃之间。在2h后,通过hplc确定反应完成。将反应混合物冷却至环境温度,并用亚硫酸氢钠淬灭反应混合物中过量的过氧化氢。然后将有机层分离,并用15ml的乙酸乙酯萃取水层。将合并的有机层浓缩以得到粗产物。从甲苯和庚烷中结晶提供5.6g的标题化合物即具有式6的化合物(基于5-氯-2-(甲硫基)-嘧啶的产率为93%)。1h nmr(400mhz,dmso-d6)δ9.24(s,2h),3.42(s,3h)。m.p.=122℃。
[0301]
合成实例5
[0302]
5-氯-2-[2-[3-(二氟甲基)-5-异噁唑基]-3-氯苯氧基]嘧啶(可替代地称为5-氯-2-[3-氯-2-[3-(二氟甲基)-5-异噁唑基]-苯氧基]-嘧啶;cas号1801862-02-1)的制备步骤a:5-氯-2-(二氟甲基)-4h-1-苯并吡喃-4-酮的制备
[0303]
在25℃下,向配备有顶置式搅拌器、蒸馏头和氮气入口的250-ml圆底烧瓶中添加甲醇钠(10.8g,200mmol)和n,n-二甲基乙酰胺(50ml)。将2,6-二氯苯乙酮(35g,181mmol)和二氟乙酸乙酯(27g,218mmol)在n,n-二甲基乙酰胺(20ml)中的预混合溶液滴加到甲醇钠浆料中,以使反应温度维持在25℃与35℃之间。在35℃下1h后,在减压下通过蒸馏去除反应产生的甲醇和乙醇。向单独的配备有顶置式搅拌器、回流冷凝器和氮气入口的1-l圆底烧瓶中添加n,n-二甲基乙酰胺(80ml),将其加热至150℃。在2.5h内将反应混合物添加到热n,n-二甲基乙酰胺中,同时使温度维持在150℃。通过hplc分析判断完成后,将反应混合物冷却至50℃。将水(200ml)缓慢添加到反应器中,并将所得的浆料缓慢冷却至20℃并搅拌1h。然后将固体通过过滤收集,用水(100ml)洗涤并在环境温度下干燥,以提供38g的粗产物。用活性炭处理粗产物以去除有色杂质并从甲苯中再结晶以得到呈淡黄色固体的标题化合物(31.7g)(基于2,6-二氯苯乙酮的产率为76%)。1h nmrδ7.79(t,1h),7.70(dd,1h),7.76(dd,1h),7.15-6.89(t,1h),6.68(s,1h)。m.p.=113℃。
[0304]
步骤b:3-氯-2-[3-(二氟甲基)-5-异噁唑基]-苯酚的制备
[0305]
在环境温度下,向配备有顶置式搅拌器和温度探针的500ml夹套反应器中添加5-氯-2-(二氟甲基)-4h-1-苯并吡喃-4-酮(即步骤a的产物,合成实例5;50g,217mmol)、羟胺氯化氢盐(18.1g,260mmol)和甲醇(150ml)。一次性将固体乙酸钠(21.3g,260mmol)添加到反应混合物中,并将所得的浆料搅拌过夜。然后,缓慢添加浓氯化氢溶液(34g,325mmol),并将所得的浆料搅拌1h。通过hplc判断完成后,将水(220ml)添加到反应器中,并将浆料在环境温度下搅拌2h。然后将固体通过过滤收集,用水中的10%甲醇(150ml)洗涤并在环境温度下干燥,以提供49.1g的标题化合物(93wt%,基于5-氯-2-(二氟甲基)-4h-1-苯并吡喃-4-酮的产率为91%)。1h nmrδ10.7(s,1h),7.48-7.22(t,1h),7.40(t,1h),7.09(d,1h),7.05(s,1h),7.01(d,1h)。m.p.=139.7℃。
[0306]
步骤c.5-氯-2-[2-[3-(二氟甲基)-5-异噁唑基]-3-氯苯氧基]-嘧啶(可替代地称为5-氯-2-[3-氯-2-[3-(二氟甲基)-5-异噁唑基]-苯氧基]-嘧啶;cas号1801862-02-1)的制备
[0307]
向配备有加热/冷却再循环浴、氮气入口、温度探针和顶置式搅拌器的100ml吹氮玻璃夹套反应器中添加3-氯-2-[3-(二氟甲基)-5-异噁唑基]-苯酚(即合成实例5,步骤b的产物;4.02g,96.5wt%,15.8mmol)、5-氯-2-甲磺酰基-嘧啶(即合成实例4的产物;3.44g,97.0wt%,17.3mmol)、碳酸钾(3.27g,23.7mmol)和异丙醇(12.1g)。将所得的浆料加热至65℃持续1h,并通过hplc分析判断完成后,在5分钟内添加水(12.1g)。将反应混合物冷却至54℃,使两个液相分离,并移除水相。在将有机溶液冷却至0℃时,从异丙醇中结晶出固体。将固体通过过滤收集,用预先冷却的异丙醇/水混合物(4/1v/v,3.5g)洗涤,并在60℃下在真空下干燥以提供标题化合物即具有式8的化合物(4.62g,99.4wt%,81.2%产率)。1h nmr(400mhz,cdcl3)δ8.44(s,2h),7.47-7.55(m,2h),7.22(dd,1h),6.61-6.87(t,1h),6.70(s,1h)。m.p.=66.5℃。
[0308]
通过本文所述的程序和本领域已知的方法,可以使用所述的方法制备以下化合
物。以下缩写用于随后的表中:i意指异,me意指甲基(ch3),et意指乙基(ch2ch3),pr意指丙基,i-pr意指异丙基,并且bu意指丁基。
[0309]
表1
[0310][0311][0312][0313]
表2
[0314]
[0315][0316]
表3
[0317][0318]
其中
[0319]
m是0(即r3不存在)
[0320][0321]
下表中的每一个以与上表3相同的方式构成,除了表3的标题行(即“m是0(即r3不存在))用以下所示的相应标题行替代外。例如,表4中的第一个条目是具有式8的化合物,其中m是1,r3是3-f,r2是f并且r4是f。表4的其余部分以相同方式构成,并且因此表5至61的其余部分以相同方式构成。
[0322]
[0323]
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。