用于治疗肥胖症的使用胰高血糖素和glp-1共激动剂的组合疗法
1.对以电子方式提交的序列表的引用
2.与本技术一起提交的ascii文本文件的以电子方式提交的序列表内容(名称:sequencelisting_st25.txt;大小:1,763字节;以及创建日期:2019年12月2日)通过引用以其全文并入本文。
背景技术:
3.肥胖症和糖尿病的发病率在流行病比例中不断上升。糖尿病的特征在于由于胰岛素产生缺陷、胰岛素作用缺陷或两者兼有而导致的高水平血糖。2型糖尿病(t2dm)约占所有已确诊糖尿病病例的90%至95%,且随着体重的增加,患2型糖尿病的风险也会增加。肥胖症患者的2型糖尿病患病率是正常体重成人的三至七倍,而体重指数(bmi)大于35kg/m2的人群中患病可能性高20倍。然而,体重减轻可以改善、控制或治愈2型糖尿病。
4.胰高血糖素和glp-1两者,充当它们各自的受体处的激动剂,已经显示出对减轻体重有效。正在销售或处于开发中的用于治疗肥胖症的某些glp-1类似物包括,例如,利拉鲁肽(liraglutide)(来自诺和诺德公司(novo nordisk)的和艾塞那肽(exenatide)(来自礼来公司/艾米林生物制药公司(eli lilly/amylin)的。胰高血糖素/glp-1激动肽也已在wo 2014/091316中披露。
5.虽然一些疗法可用于控制血糖,但目前没有疗法能实现显著的体重减轻,这仍然是患者的显著未满足需求。50%患者在10年内从用于葡萄糖控制的口服单一疗法(通常使用二甲双胍)进展到开始胰岛素治疗,通常在开始胰岛素治疗前进行多次口服组合疗法。胰岛素的使用加剧了体重增加,在开始胰岛素疗法后的第一年里,体重增加可达6kg。这种体重增加可导致胰岛素抗性增加,而这与高血压、血脂异常和主要的不良心血管事件的风险增加有关。关于降低胰岛素抗性,显著的体重减轻(>5%)是降低胰岛素抗性的最佳干预,尽管这目前只能通过集中的饮食和生活方式干预和/或减肥手术可靠地实现。
6.达格列净和二甲双胍的组合作为二联疗法已在t2dm受试者中进行了广泛研究,并显示出有利的收益-风险曲线。然而,在52周内对hba1c和体重的作用是适中的(hba1c从基线的7.7%下降0.52%,且体重减轻约3kg)。在较长时间段内,更大的作用对疾病改良而言可能是最佳的。
7.因此,仍然需要避免副作用的、有效的方法,以在人类患者中改善血糖控制、减轻体重和治疗2型糖尿病(t2dm)。
技术实现要素:
8.本文提供了在人类患者中改善血糖控制、减轻体重和治疗2型糖尿病(t2dm)的方法,该方法包括施用glp-1/胰高血糖素激动肽、达格列净和二甲双胍。
9.本文提供了一种在有需要的人类患者中改善血糖控制的方法,该方法包括向该患者施用足以改善血糖控制的量的:(i)可妥度肽(cotadutide)(seq id no:4);(ii)达格列
净;和(iii)二甲双胍。
10.本文提供了一种在有需要的人类患者中减轻体重的方法,该方法包括向该患者施用足以减轻体重的量的:(i)可妥度肽(seq id no:4);(ii)达格列净;和(iii)二甲双胍。
11.本文提供了一种在有需要的人类患者中治疗2型糖尿病(t2dm)的方法,该方法包括向该患者施用足以治疗t2dm的量的:(i)可妥度肽(seq id no:4);(ii)达格列净;和(iii)二甲双胍。
12.在一些方面,将该可妥度肽以每天至少20μg的初始剂量施用,并且其后以第二较高剂量施用。在一些方面,该可妥度肽在施用该第二剂量后以第三剂量施用,其中该第三剂量高于该第二剂量,任选地,其中该第三剂量不超过每天600μg,或其中该第三剂量不超过每天300μg。在一些方面,将该初始剂量施用约7天至约14天。
13.在一些方面,将该可妥度肽以每天100μg的初始剂量施用7天,以每天200μg的第二剂量施用接下来7天,并且随后以每天300μg的剂量施用。在一些方面,将该可妥度肽通过注射施用,任选地其中该施用是皮下施用。
14.在一些方面,将该达格列净以每天5mg或10mg的剂量施用,任选地以每天10mg的剂量施用。在一些方面,将该达格列净通过口服施用。
15.在一些方面,将该二甲双胍以每天500mg至2550mg、500mg至2000mg、500mg至1000mg或500mg至850mg的剂量施用。在一些方面,将该二甲双胍通过口服施用。
16.在一些方面,该施用减少了该患者的混合餐耐量试验(mmtt)血浆葡萄糖曲线下面积(auc)
0-4小时
。在一些方面,该施用使该患者的mmtt血浆葡萄糖auc
0-4小时
减少至少25mg-hr/dl、至少50mg-hr/dl、至少75mg-hr/dl、至少100mg-hr/dl或至少150mg-hr/dl。在一些方面,该施用使该患者的mmtt血浆葡萄糖auc
0-4小时
百分比减少至少5%、至少10%、至少15%或至少20%。
17.在一些方面,该施用减少该患者的持续葡萄糖监测(cgm)葡萄糖auc
0-24
。在一些方面,该施用使该患者的cgm葡萄糖auc
0-24
减少至少200mg-hr/dl、至少250mg-hr/dl、至少300mg-hr/dl、至少350mg-hr/dl、至少400mg-hr/dl、至少450mg-hr/dl、至少500mg-hr/dl、至少550mg-hr/dl、至少600mg-hr/dl或至少650mg-hr/dl。
18.在一些方面,该施用减少该患者的24小时cgm平均葡萄糖。在一些方面,该施用使该患者的24小时cgm平均葡萄糖减少至少10mg/dl、至少15mg/dl、至少20mg/dl或至少25mg/dl。
19.在一些方面,该施用使该患者的cgm葡萄糖的标准偏差(sd)减少至少5mg/dl。
20.在一些方面,该施用使该患者的cgm平均葡萄糖波动幅度(mage)减少至少10mg/dl、至少15mg/dl、至少20mg/dl或至少25mg/dl。
21.在一些方面,该施用减少该患者的空腹血浆葡萄糖(fpg)。在一些方面,该施用使该患者的fpg减少至少5mg/dl、至少10mg/dl、至少15mg/dl、至少20mg/dl、至少25mg/dl或至少30mg/dl。
22.在一些方面,该施用使该患者的血红蛋白a1c(hba1c)减少至少0.5%或至少1%。
23.在一些方面,该施用使该患者的体重减轻至少2kg或至少3kg。
24.在一些方面,该减少发生在从初始施用该可妥度肽开始的28天。
25.在一些方面,该施用使该患者达到正常血糖水平。
26.在一些方面,该施用防止该患者出现高血糖水平。
27.在一些方面,该施用改善该患者的血糖控制。
28.在一些方面,该施用减轻该患者的体重。
29.在一些方面,该施用治疗该患者的t2dm。
30.在一些方面,该施用持续至少四周。
31.在一些方面,该施用是饮食和运动的辅助。
32.在一些方面,该患者具有≥25kg/m2至≤40kg/m2的体重指数(bmi)。在一些方面,该患者具有≥7.0%至≤10.0%的血红蛋白a1c(hba1c)。在一些方面,该患者患有t2dm。
附图说明
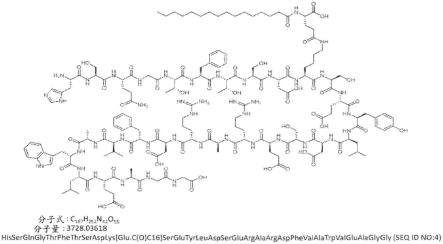
33.图1示出了可妥度肽的化学结构、化学式(c
167h252n42o55
)和分子量(3728.09)(medi0382;seq id no:4)。
34.图2提供了在接受达格列净和二甲双胍二联疗法的患者中可妥度肽(“medi0382”)研究的流程图(参见实例1)。
具体实施方式
35.i.定义
36.贯穿本披露,术语“一个/种(a或an)”实体是指一个/种或多个/种该实体;例如,“多核苷酸”应理解为代表一种或多种多核苷酸。因此,术语“一个/种(a或an)”、“一个/种或多个/种”和“至少一个/种”本文可互换地使用。
37.此外,当在文中使用时“和/或”被理解为这两个指定的特征或组分中每一者与或不与另一者一起被具体披露。因此,如在本文中的短语例如“a和/或b”中所使用的术语“和/或”旨在包括“a和b”、“a或b”、“a”(单独)和“b”(单独)。同样,术语“和/或”如在词组如“a、b和/或c”中使用时是旨在涵盖以下方面中的每一者:a、b、和c;a、b或c;a或c;a或b;b或c;a和c;a和b;b和c;a(单独);b(单独);和c(单独)。
38.应当理解,无论在什么情况下本文用语言“包含”描述方面时,也提供了用“由......组成”和/或“主要由......组成”描述的其他类似方面。“含有”特定氨基酸序列的肽是指含有氨基酸序列的肽,其中该肽可以含有或不含有另外的氨基酸或其他对氨基酸序列的修饰。由特定氨基酸序列“组成”的肽是指仅含有氨基酸序列且不含另外的氨基酸或其他对氨基酸序列的修饰的肽。“包含”由特定氨基酸序列“组成”的氨基酸序列的肽是指含有氨基酸序列且不含另外的氨基酸的肽;然而,肽可以包含其他对氨基酸序列的修饰(例如,酰基部分或棕榈酰基部分)。
39.除非另外定义,否则本文使用的所有技术和科学术语具有如本披露所属领域的普通技术人员通常理解的相同含义。例如,concise dictionary of biomedicine and molecular biology[简明生物医学和分子生物学词典],juo,pei-show,第2版,2002,crc press[crc出版社];dictionary of cell and molecular biology[细胞和分子生物学词典],第3版,1999,academic press[学术出版社];以及oxford dictionary of biochemistry and molecular biology[生物化学和分子生物学牛津词典],修订版,2000,oxford university press[牛津大学出版社]为技术人员提供在本披露中使用的许多术语
的通用词典注释。
[0040]
单位、前缀和符号是以它们的国际单位系统(syst
è
me international de unites)(si)接受的形式表示。数值范围包括限定该范围的数字。除非另外说明,否则氨基酸序列是以氨基至羧基取向从左向右书写。本文提供的小标题不是本披露的不同方面的限制,可以通过作为一个整体参考本说明书来获得这些方面。因此,通过以其全文参考说明书,更充分地定义了紧接着在下文中定义的术语。
[0041]
如本文使用的,术语“多肽”旨在涵盖单数“多肽”以及复数“多肽”,并且包含两个或更多个氨基酸的任何链或多个链。因此,如本文使用的,“肽”、“肽亚单位”、“蛋白质”、“氨基酸链”、“氨基酸序列”、或用来指代两个或更多个氨基酸的链或多个链的任何其他术语,都被包括定义“多肽”中,尽管这些术语的每一者都可具有更具体的含义。术语“多肽”可以用来替代任何这些术语或者与其可互换地使用。该术语进一步包括已经历翻译后或合成后修饰的多肽,这些修饰例如,棕榈酰基基团的缀合、糖基化、乙酰化、磷酸化、酰胺化、通过已知保护/阻断基团进行的衍生、蛋白水解裂解或通过非天然存在的氨基酸进行的修饰。
[0042]
更具体地说,如本文使用的术语“肽”涵盖全长肽以及其片段、变体或衍生物,例如,glp-1/胰高血糖素激动肽(例如,在长度上为29、30或31个氨基酸)。如本文披露的“肽”,例如glp-1/胰高血糖素激动肽,可以是包含用来增加半衰期的另外的成分(例如像fc结构域或白蛋白结构域)的融合多肽的一部分。如本文描述的肽还可以许多不同的途径衍生。本文描述的肽可以包含修饰,包括例如棕榈酰基基团的缀合。
[0043]
本文使用的术语“可妥度肽”和“medi0382”是指具有图1所示结构的肽。
[0044]
术语“分离的”是指肽或核酸通常将根据本披露的状态。分离的肽和分离的核酸将不含或基本上不含在天然状态下与其相关联的材料,如在其天然环境下,或在这种制备是通过在体外或在体内实施的重组dna技术时在其制备环境(例如细胞培养物)中与其一起存在的其他肽或核酸。肽和核酸可以用稀释剂或佐剂配制,并且仍然为了实用目的可以被分离-例如如果这些肽用于包被微量滴定板用于免疫测定,则这些蛋白质通常将与明胶或其他载体混合,或者当用于诊断或治疗时将与药学上可接受的载体或稀释剂混合。
[0045]“重组”肽是指经由重组dna技术产生的肽。如同已经通过任何适合的技术分离、分级或部分纯化或基本上纯化的天然或重组多肽一样,出于本披露的目的,在宿主细胞中表达的重组产生的肽也被视为分离的。
[0046]
当提及glp-1/胰高血糖素激动肽时,术语“片段”、“类似物”、“衍生物”或“变体”包括保留至少某种期望的活性(例如,结合到胰高血糖素和/或glp-1受体上)的任何肽。本文提供的glp-1/胰高血糖素激动肽的片段包括在表达、纯化、和/或施用至受试者期间展现出所希望的特性的蛋白水解片段、缺失片段。
[0047]
如本文使用的,术语“变体”是指由于氨基酸取代、缺失、插入、和/或修饰而不同于所列举肽的肽。变体可以使用本领域已知的诱变技术来产生。变体还可以,或可替代地,含有其他修饰-例如肽可以是缀合或偶联的,例如融合到异源氨基酸序列或其他部分上,例如用于增加半衰期、溶解度、或稳定性。缀合或偶联到本文提供的肽上的部分的实例包括,但不限于,白蛋白、免疫球蛋白fc区、聚乙二醇(peg)等。该肽还可以与便于该肽的合成、纯化或鉴定或增强该多肽结合到固相支持物上的接头或其他序列(例如,6-his)缀合或产生偶联。
[0048]
术语“组合物”或“药物组合物”是指如下组合物,这些组合物含有本文提供的glp-1/胰高血糖素激动肽连同例如药学上可接受的、用于向对治疗有需要的受试者(例如,需要改善血糖控制、减轻体重、和/或治疗t2dm的人类受试者)施用的载体、赋形剂、或稀释剂。
[0049]
术语“药学上可接受的”是指如下组合物,这些组合物在合理的医学判断范围内适合于与人以及动物的组织接触而没有过度的毒性或与合理的利益/风险比相当的其他并发症。
[0050]“有效量”是本文提供的试剂(例如,glp-1/胰高血糖素激动肽、达格列净和/或二甲双胍)的量,该量以单剂量或作为一系列剂量的一部分施用至受试者对于治疗(例如改善血糖控制、减轻体重和/或治疗t2dm)是有效的。
[0051]
如本文使用的,术语“受试者”和“患者”可互换地使用。该受试者可以是动物。在本披露的一些方面,该受试者是哺乳动物,例如非人类动物(例如,牛、猪、马、猫、狗、大鼠、小鼠、猴或其他灵长类等)。在本披露的一些方面,该受试者是食蟹猴。在本披露的一些方面,该受试者是人类。
[0052]
如本文使用的,“有需要的受试者”或“有需要的患者”是指希望治疗的个体,例如,需要改善血糖控制、减轻体重和/或治疗t2dm的受试者。
[0053]
术语如“治疗(treating,treatment或to treat)”是指治愈和/或停止已确诊的病理病症或障碍的进展的治疗性措施。术语如“预防”是指预防和/或减缓所靶向的病理病症或障碍发展的防治性或预防性措施。因此,需要治疗的那些包括已患有疾病或病症的那些。需要预防的那些包括容易患上疾病或病症的那些以及有待预防疾病或病症的那些。
[0054]
与一种或多种另外的治疗剂“组合”施用包括以任何顺序同时(并行)或连续施用。
[0055]
术语,如“降低严重程度”是指减慢或减轻已确诊的病理病症或障碍的症状的治疗性措施。
[0056]
如本文使用的,“glp-1/胰高血糖素激动肽”是嵌合肽,其展现出相对于天然胰高血糖素的至少约1%、5%、10%、20%、30%、40%、50%、60%、70%、80%、90%、95%、或更高的在胰高血糖素受体上的活性,并且还展现出相对于天然glp-1的至少约1%、5%、10%、20%、30%、40%、50%、60%、70%、80%、90%、95%、或更高的在glp-1受体上的活性。
[0057]
如本文使用的术语“天然胰高血糖素”是指包含seq id no:1序列的天然存在的胰高血糖素,例如人胰高血糖素。术语“天然glp-1”是指天然存在的glp-1,例如人glp-1,并且是涵盖例如glp-1(7-36)酰胺(seq id no:2)、glp-1(7-37)酸(seq id no:3)或者这两种化合物的混合物的通用术语。如本文使用的,在没有任何进一步指定的情况下,对“胰高血糖素”或“glp-1”的一般参考旨在分别表示天然的人胰高血糖素或天然的人glp-1。除非另外指出,“胰高血糖素”是指人胰高血糖素,并且“glp-1”是指人glp-1。
[0058]
ii.glp-1/胰高血糖素激动肽
[0059]
本文提供了结合到胰高血糖素受体上且结合到glp-1受体上的肽。例如可妥度肽(g933;medi0382)的示例性肽在wo 2014/091316和wo 2017/153575(其各自通过引用以其全文并入本文)中提供。在本文提供的一些方面,该肽是可妥度肽,即具有hsqgtftsdx
10
seyldserardfvawleagg-酸序列的30个氨基酸的线性肽,其中x
10
=具有通过γ谷氨酸接头与ε氮缀合的棕榈酰基基团的赖氨酸(即k(ge-棕榈酰基))(seq id no:4)(参见图1)。在一些方面,本文提供的肽是胰高血糖素和glp-1活性的共激动剂。此类肽在本文中称为glp-1/胰高
血糖素激动肽。如本文提供的glp-1/胰高血糖素激动肽具有有利比率的glp-1和胰高血糖素活性,以便促进体重减轻、预防体重增加、或者维持所希望的体重,并且具有优化的溶解度、可配制性、和稳定性。在一些方面,如本文提供的glp-1/胰高血糖素激动肽对人glp1和人胰高血糖素受体具有活性。在一些方面,如披露的glp-1/胰高血糖素激动肽对胰高血糖素和glp-1受体具有所希望的效价,并且具有所希望的促进体重减轻的相对效价。
[0060]
可妥度肽具有在位置12的谷氨酸残基,并且对胰高血糖素受体和glp-1受体两者都保持稳健的活性。相应的残基在毒蜥外泌肽(exendin)-4(艾塞那肽(exenatide))和胰高血糖素中是赖氨酸,而在glp-1中是丝氨酸。虽然这个残基被认为不与该受体接触,但是在电荷上从正到负的变化可改变邻近的环境。此外,可妥度肽具有在位置27处的谷氨酸残基。在毒蜥外泌肽4中的残基27是赖氨酸并且在glp1(缬氨酸)和胰高血糖素(甲硫氨酸)中是不带电的疏水残基。毒蜥外泌肽4的赖氨酸与glp1受体在残基glu127和glu24处发生静电相互作用(c.r.underwood等人,j biol chem[生物化学杂志]285 723-730(2010);s.runge等人,j biol chem[生物化学杂志]283 11340-11347(2008))。虽然当在位置27处的电荷被改变为负的时候可预期到glp1r效价的损失,但是这种改变与可妥度肽中的glp1r活性相容。
[0061]
可妥度肽被棕榈酰化以通过与血清白蛋白结合来延长其半衰期,从而降低其肾脏清除倾向。
[0062]
可替代地或另外,本文披露的glp-1/胰高血糖素激动肽可与异源部分结合,例如以延长半衰期。该异源部分是蛋白质、肽、蛋白质结构域、接头、有机聚合物、无机聚合物、聚乙二醇(peg)、生物素、白蛋白、人血清白蛋白(hsa)、hsa fcrn结合部分、抗体、抗体的结构域、抗体片段、单链抗体、结构域抗体、白蛋白结合结构域、酶、配体、受体、结合肽、非fniii支架、表位标签(epitope tag)、重组多肽聚合物、细胞因子、或此类部分的两种或更多种的组合。
[0063]
可妥度肽可以滴定剂量(例如,以初始剂量,然后以第二较高剂量,并且任选地其后以第三较高剂量)施用。该初始剂量和任选地该第二剂量可以施用约7天至约14天。该初始剂量可以是至少每天20μg。该最高剂量(例如,该第二剂量或该第三剂量)可以是不超过每天600μg的剂量。该最高剂量(例如,该第二剂量或该第三剂量)可以是不超过每天300μg的剂量。
[0064]
iii.制造glp-1/胰高血糖素激动肽的方法
[0065]
可通过任何适合的方法制造本文提供的用于使用的glp-1/胰高血糖素激动肽。例如,在本文提供的一些方面,通过本领域普通技术人员熟知的方法,例如通过如merrifield描述的固相合成(1963,j.am.chem.soc.[美国化学学会杂志]85:2149-2154),化学合成本文提供的用于使用的glp-1/胰高血糖素激动肽。可以例如,通过使用自动合成仪,使用标准试剂完成固相肽合成,如wo 2014/091316(其通过引用以其全文并入本文)的实例1中所解释的。
[0066]
可替代地,可以使用如本领域普通技术人员熟知的合宜的载体/宿主细胞组合以重组方式产生本文提供的用于使用的glp-1/胰高血糖素激动肽。用于以重组方式产生glp-1/胰高血糖素激动肽的许多种方法是可得的。通常,将编码glp-1/胰高血糖素激动肽的多核苷酸序列插入适当的表达媒介物,例如,含有用于该插入的编码序列的转录和翻译的必需元件的载体。将编码glp-1/胰高血糖素激动肽的核酸插入载体的正确阅读框中。然后将
该表达载体转染到适合的表达该glp-1/胰高血糖素激动肽的宿主细胞中。适合的宿主细胞包括但不限于细菌、酵母、或哺乳动物细胞。许多种可商购的宿主-表达载体系统可以用来表达本文描述的glp-1/胰高血糖素激动肽。
[0067]
iv.达格列净
[0068]
达格列净是一种钠-葡萄糖协同转运2(sglt2)抑制剂。化学上描述为d-葡萄糖醇,1,5-酐-1-c-[4-氯代-3-[(4乙氧基苯基)甲基]苯基]-,(1s)-与(2s)-1,2-丙二醇,水合物(1∶1∶1)混合。达格列净已被批准作为饮食和运动的辅助而用于在改善患有t2dm的成人的血糖控制中使用。
[0069]
可商购的达格列净是可商购的达格列净是片剂含有5mg或10mg的达格列净。片剂含有以下非活性成分:微晶纤维素、无水乳糖、交聚维酮、二氧化硅和硬脂酸镁。片剂还含有薄膜包衣,该薄膜包衣含有聚乙烯醇、二氧化钛、聚乙二醇、滑石和黄色氧化铁。
[0070]
达格列净可通过口服施用,例如作为口服片剂施用。达格列净可以与或不与食物一起在早上施用。
[0071]
v.二甲双胍
[0072]
如本文使用的,术语“二甲双胍”和“盐酸二甲双胍”可互换地使用,以指代n,n-二甲基亚氨基二碳酰亚胺二酰胺盐酸盐。二甲双胍已被批准用于在管理t2dm中使用。
[0073]
二甲双胍作为片剂和xr延缓释放片剂是可商购的。片剂含有500mg、850mg或1000mg的二甲双胍。每个片剂含有非活性成分聚维酮和硬脂酸镁。此外,500mg和850mg片剂的包衣含有羟丙甲纤维素,而1000mg片剂的包衣含有羟丙甲纤维素和聚乙二醇。xr延缓释放片剂含有500mg或750mg的二甲双胍。xr 500mg片剂含有非活性成分羧甲基纤维素钠、羟丙甲纤维素、微晶纤维素和硬脂酸镁。xr 750mg片剂含有非活性成分羧甲基纤维素钠、羟丙甲纤维素和硬脂酸镁。
[0074]
二甲双胍可通过口服施用,例如作为口服片剂施用。
[0075]
二甲双胍可以每天500mg至2550mg的剂量施用。二甲双胍可以每天500mg至2000mg的剂量施用。二甲双胍可以每天500mg至1000mg的剂量施用。二甲双胍可以每天500mg至850mg的剂量施用。
[0076]
vi.药物组合物和试剂盒
[0077]
如本文提供的,glp-1/胰高血糖素激动肽(例如,可妥度肽)可与达格列净和二甲双胍组合用于在有需要的人类患者中改善血糖控制、减轻体重和/或治疗t2dm。
[0078]
glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍可以在分开的药物组合物中施用。
[0079]
在一些方面,试剂盒提供了glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍。在某些方面,试剂盒包含glp-1/胰高血糖素激动肽(例如,可妥度肽)和将该
glp-1/胰高血糖素激动肽(例如,可妥度肽)与达格列净和二甲双胍一起施用的说明书。在一些方面,试剂盒包含glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净,以及将该glp-1/胰高血糖素激动肽(例如,可妥度肽)和达格列净与二甲双胍一起施用的说明书。在一些方面,试剂盒包含glp-1/胰高血糖素激动肽(例如,可妥度肽)、二甲双胍,以及将该glp-1/胰高血糖素激动肽(例如,可妥度肽)和二甲双胍与达格列净一起施用的说明书。在一些方面,试剂盒包含达格列净、二甲双胍,以及将该达格列净和二甲双胍与glp-1/胰高血糖素激动肽(例如,可妥度肽)一起施用的说明书。
[0080]
可以将包含glp-1/胰高血糖素激动肽(例如,可妥度肽)的药物组合物配制用于注射。可以将包含glp-1/胰高血糖素激动肽(例如,可妥度肽)的药物组合物配制用于皮下施用。
[0081]
包含glp-1/胰高血糖素激动肽(例如,可妥度肽)的药物组合物可以包含约100mg、约200mg或约300mg的glp-1/胰高血糖素激动肽(例如,可妥度肽)。
[0082]
可以将包含达格列净的药物组合物配制用于口服施用。包含达格列净的药物组合物可以是用于口服施用的片剂。
[0083]
包含达格列净的药物组合物可包含约5mg或约10mg的达格列净。
[0084]
可以将包含二甲双胍的药物组合物配制用于口服施用。包含二甲双胍的药物组合物可以是用于口服施用的片剂。
[0085]
包含二甲双胍的药物组合物可包含约500mg、约750mg、约850mg或约1000mg的二甲双胍。
[0086]
vii.使用方法
[0087]
如本文提供的,glp-1/胰高血糖素激动肽(例如,可妥度肽)可与达格列净和二甲双胍组合用于在有需要的人类患者中改善血糖控制、减轻体重和/或治疗t2dm。
[0088]
如本文提供的在有需要的人类受试者中改善血糖控制的方法,该方法可以包括向该受试者施用glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍。本披露还提供了glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍(任选地在分开的药物组合物中),用于在有需要的人类受试者中改善血糖控制。本披露还提供了glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍(任选地在分开的药物组合物中),用于在制造如下药物中使用,该药物用于在有需要的人类受试者中改善血糖控制。用于改善血糖控制的glp-1/胰高血糖素激动肽(例如,可妥度肽)可以20-600μg或100-300μg的剂量施用或用于施用,任选地其中该施用为通过注射施用(例如,皮下施用)。用于改善血糖控制的glp-1/胰高血糖素激动肽(例如,可妥度肽)可以每天施用或用于施用(例如,以20-600μg或100-300μg的日剂量),任选地其中该施用为通过注射施用(例如,皮下施用)。用于改善血糖控制的glp-1/胰高血糖素激动肽(例如,可妥度肽)可以滴定剂量(例如,以100μg的初始剂量,然后200μg的第二剂量,然后300μg的第三剂量)施用或用于施用。该初始剂量可以施用约7天。该第二剂量可以施用约7天。用于改善血糖控制的达格列净可以10mg的剂量施用或用于施用,任选地其中该施用为口服(例如,通过口服片剂)。用于改善血糖控制的二甲双胍可以例如每天500mg至2550mg的剂量施用或用于施用,任选地其中该施用为口服(例如,通过口服片剂)。该施用可以是饮食和运动的辅助。
[0089]
如本文提供的在有需要的人类受试者中减轻体重的方法,该方法可以包括向该受
试者施用glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍。本披露还提供了glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍(任选地在分开的药物组合物中),用于在有需要的人类受试者中减轻体重。本披露还提供了glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍(任选地在分开的药物组合物中),用于在制造如下药物中使用,该药物用于在有需要的人类受试者中减轻体重。用于减轻体重的glp-1/胰高血糖素激动肽(例如,可妥度肽)可以20-600μg或100-300μg的剂量施用或用于施用,任选地其中该施用为通过注射施用(例如,皮下施用)。用于减轻体重的glp-1/胰高血糖素激动肽(例如,可妥度肽)可以每天施用或用于施用(例如,以20-600μg或100-300μg的日剂量),任选地其中该施用为通过注射施用(例如,皮下施用)。用于减轻体重的glp-1/胰高血糖素激动肽(例如,可妥度肽)可以滴定剂量(例如,以100μg的初始剂量,然后200μg的第二剂量,然后300μg的第三剂量)施用或用于施用。该初始剂量可以施用约7天。该第二剂量可以施用约7天。用于减轻体重的达格列净可以10mg的剂量施用或用于施用,任选地其中该施用为口服(例如,通过口服片剂)。用于减轻体重的二甲双胍可以例如每天500mg至2550mg的剂量施用或用于施用,任选地其中该施用为口服(例如,通过口服片剂)。该施用可以是饮食和运动的辅助。
[0090]
如本文提供的在有需要的人类受试者中治疗t2dm的方法,该方法可以包括向该受试者施用glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍。本披露还提供了glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍(任选地在分开的药物组合物中),用于在有需要的人类受试者中治疗t2dm。本披露还提供了glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍(任选地在分开的药物组合物中),用于在制造如下药物中使用,该药物用于在有需要的人类受试者中治疗t2dm。用于治疗t2dm的glp-1/胰高血糖素激动肽(例如,可妥度肽)可以20-600μg或100-300μg的剂量施用或用于施用,任选地其中该施用为通过注射施用(例如,皮下施用)。用于治疗t2dm的glp-1/胰高血糖素激动肽(例如,可妥度肽)可以每天施用或用于施用(例如,以20-600μg或100-300μg的日剂量),任选地其中该施用为通过注射施用(例如,皮下施用)。用于治疗t2dm的glp-1/胰高血糖素激动肽(例如,可妥度肽)可以滴定剂量(例如,以100μg的初始剂量,然后200μg的第二剂量,然后300μg的第三剂量)施用或用于施用。该初始剂量可以施用约7天。该第二剂量可以施用约7天。用于治疗t2dm的达格列净可以10mg的剂量施用或用于施用,任选地其中该施用为口服(例如,通过口服片剂)。用于治疗t2dm的二甲双胍可以例如每天500mg至2550mg的剂量施用或用于施用,任选地其中该施用为口服(例如,通过口服片剂)。该施用可以是饮食和运动的辅助。
[0091]
在本文提供的一些方面,glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍可以减少患者的混合餐耐量试验(mmtt)血浆葡萄糖曲线下面积(auc)
0-4小时
。在一些方面,mmtt血浆葡萄糖auc
0-4小时
可减少至少25mg-hr/dl、至少50mg-hr/dl、至少75mg-hr/dl、至少100mg-hr/dl、或至少150mg-hr/dl。在一些方面,mmtt血浆葡萄糖auc
0-4小时
可减少25-200mg-hr/dl、50-200mg-hr/dl、75-200mg-hr/dl、100-200mg-hr/dl、或150-200mg-hr/dl。在一些方面,mmtt血浆葡萄糖auc
0-4小时
百分比可减少至少5%、至少10%、至少15%、或至少20%。该减少可发生于例如首次施用glp-1/胰高血糖素激动肽(例如,可妥度肽)后的28天内。
[0092]
在本文提供的一些方面,glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍可以减少患者的持续葡萄糖监测(cgm)葡萄糖auc
0-24
。在一些方面,cgm葡萄糖auc
0-24
可减少至少200mg-hr/dl、至少250mg-hr/dl、至少300mg-hr/dl、至少350mg-hr/dl、至少400mg-hr/dl、至少450mg-hr/dl、至少500mg-hr/dl、至少550mg-hr/dl、至少600mg-hr/dl、或至少650mg-hr/dl。在一些方面,cgm葡萄糖auc
0-24
可减少200-750mg-hr/dl、250-750mg-hr/dl、300-750mg-hr/dl、350-750mg-hr/dl、400-750mg-hr/dl、450-750mg-hr/dl、500-750mg-hr/dl、550-750mg-hr/dl、600-750mg-hr/dl、或650-750mg-hr/dl。该减少可发生于例如首次施用glp-1/胰高血糖素激动肽(例如,可妥度肽)后的28天内。
[0093]
在本文提供的一些方面,glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍可以减少患者的24小时cgm平均葡萄糖。在一些方面,24小时cgm平均葡萄糖可减少至少10mg/dl、至少15mg/dl、至少20mg/dl、或至少25mg/dl。在一些方面,24小时cgm平均葡萄糖可减少10-35mg/dl、15-35mg/dl、20-35mg/dl、或25-35mg/dl。该减少可发生于例如首次施用glp-1/胰高血糖素激动肽(例如,可妥度肽)后的28天内。
[0094]
在本文提供的一些方面,glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍可将患者的cgm葡萄糖的标准偏差(sd)减少至少5mg/dl。在本文提供的一些方面,glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍可将患者的cgm葡萄糖的标准偏差(sd)减少5-15mg/dl。该减少可发生于例如首次施用glp-1/胰高血糖素激动肽(例如,可妥度肽)后的28天内。
[0095]
在本文提供的一些方面,glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍可将患者的cgm平均葡萄糖波动幅度(mage)减少至少10mg/dl、至少15mg/dl、至少20mg/dl或至少25mg/dl。在本文提供的一些方面,glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍可将患者的cgm mage减少10-35mg/dl、15-35mg/dl、20-35mg/dl、或25-35mg/dl。该减少可发生于例如首次施用glp-1/胰高血糖素激动肽(例如,可妥度肽)后的28天内。
[0096]
在本文提供的一些方面,glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍可减少患者空腹血浆葡萄糖(fpg)。在一些方面,fpg可减少至少5mg/dl、至少10mg/dl、至少15mg/dl、至少20mg/dl、至少25mg/dl、或至少30mg/dl。在一些方面,fpg可减少5-50mg/dl、10-50mg/dl、15-50mg/dl、20-50mg/dl、25-50mg/dl、或30-50mg/dl。该减少可发生于例如首次施用glp-1/胰高血糖素激动肽(例如,可妥度肽)后的28天内。
[0097]
在本文提供的一些方面,glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍可将患者的血红蛋白a1c(hba1c)减少至少0.5%或至少1%。在本文提供的一些方面,glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍可将患者的hbalc减少0.5%-2%或1%-2%。该减少可发生于例如首次施用glp-1/胰高血糖素激动肽(例如,可妥度肽)后的28天内。
[0098]
在本文提供的一些方面,glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍可将患者的体重减轻至少2kg或至少3kg。在本文提供的一些方面,glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍可将患者的体重减轻2-10kg或3-10kg。该减少可发生于例如首次施用glp-1/胰高血糖素激动肽(例如,可妥度肽)后的28天内。
[0099]
在本文提供的一些方面,glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和
二甲双胍可使患者达到正常血糖水平。在本文提供的一些方面,glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍可防止患者出现高血糖水平。
[0100]
如本文提供的,以上任何方面讨论的人类受试者均患有2型糖尿病。
[0101]
如本文提供的,以上任何方面讨论的人类受试者均具有25至40kg/m2的体重指数(bmi)。
[0102]
如本文提供的,以上任何方面讨论的人类受试者均具有≥7.0%至≤10.0%的血红蛋白alc(hba1c)。
[0103]
在一些方面,本文提供的人类受试者在施用glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍的组合之前,正在接受二甲双胍的治疗。在一些方面,本文提供的人类受试者在施用glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍的组合之前,正在接受二甲双胍mtd>1g的治疗。
[0104]
在一些方面,本文提供的人类受试者在施用glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍的组合之前,正在接受达格列净和二甲双胍的治疗。在一些方面,本文提供的人类受试者在施用glp-1/胰高血糖素激动肽(例如,可妥度肽)、达格列净和二甲双胍的组合之前,正在接受10mg达格列净和二甲双胍mtd>1g的治疗。
[0105]
实例
[0106]
实例1:可妥度肽结合达格列净和二甲双胍二联疗法
[0107]
进行了一项2a期随机化、安慰剂对照、双重束缚的研究,以证明可妥度肽在用达格列净和二甲双胍二联疗法治疗的患有2型糖尿病(t2dm)的超重/肥胖受试者中的功效和安全性。
[0108]
(a)受试者
[0109]
共有128名受试者同意参加本研究。本研究纳入了用二甲双胍单一疗法或用二甲双胍和达格列净二联疗法治疗的t2dm受试者。根据以下纳入和排除标准筛选受试者。
[0110]
纳入标准:
[0111]
·
筛选时年龄≥18岁的男性和女性受试者;
[0112]
·
筛选时体重指数(bmi)介于25kg/m2和40kg/m2(包括端值)之间;
[0113]
·
筛选时hba1c范围介于7.0%和10.0%(包括端值)之间;
[0114]
·
确诊为t2dm,且在筛选前至少8周用二甲双胍单一疗法(mtd>1g)治疗或在筛选前至少3个月用稳定口服剂量的达格列净10mg和二甲双胍(mtd>1g)治疗。
[0115]
排除标准:
[0116]
·
在筛选期(第1次就诊)开始之前或研究开始期(第4次就诊)之前已接受以下药物治疗中任一种的任何受试者:
[0117]
o在筛选时(第1次就诊)同时使用获准用于控制体重或食欲的任何药物产品、或草药或非处方(otc)制剂;
[0118]
o在筛选时(第1次就诊)的最近30天内或药物的5个半衰期内(以较最长者为准),同时或先前使用获准用于体重减轻的药物(例如,奥利司他、安非他酮-纳曲酮、苯丁胺-托吡酯、苯丁胺、氯卡色林);
[0119]
o在研究开始(第4次就诊)前的最近72小时内,同时使用剂量大于150mg(每日一次)的阿司匹林(乙酰水杨酸);
[0120]
o在研究开始(第4次就诊)前的最近72小时内,同时使用总日剂量大于3000mg的对乙酰氨基酚(醋氨酚)或含对乙酰氨基酚的制剂;
[0121]
o在研究开始(第4次就诊)前的最近72小时内,同时使用总日剂量大于1000mg的抗坏血酸(维生素c)补充剂;或
[0122]
o在研究开始(第4次就诊)前的最近72小时内,同时使用鸦片剂、多潘立酮、甲氧氯普胺或其他已知改变胃排空的药物;
[0123]
·
诊断为1型糖尿病、青年人中的成年型糖尿病或成人晚发自身免疫性糖尿病,或存在抗谷氨酸脱羧酶、抗胰岛细胞或抗胰岛素抗体;
[0124]
·
在筛选或随机化时有急性失代偿性血糖控制症状(例如,口渴、多尿、体重减轻),有糖尿病酮症酸中毒(dka)病史,或在筛选前90天内有高渗性非酮症昏迷或接受每日皮下(sc)胰岛素治疗;
[0125]
·
随机化前空腹高血糖(>250mg/dl>13.9mmol/l);
[0126]
·
c-肽水平<正常下限;
[0127]
·
接受过急性或慢性胰腺炎或胰腺切除术;
[0128]
·
筛选时高甘油三酯血症(>400mg/dl);
[0129]
·
可能影响胃排空或可以影响对安全性和耐受性数据的解释的重大炎症性肠病、胃轻瘫或其他严重疾病,或影响上消化道的手术(包括减肥手术和程序);
[0130]
·
重大肝病(未伴随门静脉高压或肝硬化的非酒精性脂肪性肝炎或非酒精性脂肪肝病除外)和/或筛选时具有以下结果中任一种的受试者:天冬氨酸转氨酶(ast)≥3倍正常上限(uln),丙氨酸转氨酶(alt)≥3倍uln,或总胆红素(tbl)≥2倍uln;
[0131]
·
筛选时,肾功能受损定义为估算肾小球滤过率(egfr)≤60ml/min/1.73m2(使用同位素稀释质谱法-可追溯的mdrd研究方程式根据肾脏疾病饮食改良[mdrd]的egfr(国际单位制[si]));
[0132]
·
筛选前1个月内,使用袢利尿剂;
[0133]
·
高血压控制不佳,定义如下:收缩bp>160mmhg,仰卧休息10分钟后舒张bp或≥100mmhg,并在筛选(所有受试者的第1次就诊)时通过重复测量进行确认;
[0134]
·
筛选前3个月内有不稳定型心绞痛、心肌梗塞、短暂性脑缺血发作或卒中,或在过去6个月内接受了经皮冠状动脉介入治疗或冠状动脉搭桥术的受试者或在筛选时应当接受这些程序的受试者;
[0135]
·
严重充血性心力衰竭(纽约心脏病学会iii级和iv级);
[0136]
·
筛选时基础降钙素水平>50ng/l,或有甲状腺髓样癌或多发性内分泌肿瘤病史或家族病史;
[0137]
·
筛选时有血红蛋白病、溶血性贫血或慢性贫血(男性血红蛋白浓度<11.5g/dl(115g/l),而女性血红蛋白浓度<10.5g/dl(105g/l)),或已知会干扰hba1c测量结果解释的任何其他病症;
[0138]
·
筛选前5年内有肿瘤病病史,经充分治疗的基底细胞皮肤癌、鳞状细胞皮肤癌或原位宫颈癌除外;
[0139]
·
血清乙型肝炎表面抗原、丙型肝炎抗体和人类免疫缺陷病毒抗体的任何阳性结果;
[0140]
·
接受二联疗法的受试者在筛选(第1次就诊)前一个月或接受单一疗法的受试者在导入期(第2次就诊)前一个月患有最近病毒感染或需要使用抗生素的疾病;以及
[0141]
·
筛选前6个月内有复发的(至少2次)泌尿道和/或生殖道感染(包括霉菌感染,例如鹅口疮)病史。
[0142]
在同意参加的128名受试者中,有79名受试者被认为是筛选失败,而有49名受试者被随机化(25名受试者分至可妥度肽组,并且24名受试者分至安慰剂组)。
[0143]
共有47名受试者(95.9%)完成本研究,且共有46名受试者(93.9%)按计划完成治疗。三名受试者(6.1%,全部在可妥度肽治疗组)中断治疗:2名受试者(4.1%)由于不良事件(ae)中断,1名受试者(2.0%)因其退出而中断。
[0144]
接受研究产品的所有49名受试者均被纳入意向治疗(itt)群体、接受治疗(as-treated)群体和免疫原性群体。共有25名接受可妥度肽的受试者具有可评估的给药后pk数据,并被纳入可妥度肽pk群体中。共有49名受试者被纳入达格列净群体,并且48名受试者被纳入酮pk群体。分析群体分组如下:
[0145]
·
意向治疗(itt)群体=接受根据其随机化治疗组分析的任何研究产品(可妥度肽或安慰剂)的随机化受试者。
[0146]
·
接受治疗群体=接受根据其实际接受的治疗分析的任何研究产品(可妥度肽或安慰剂)的受试者。
[0147]
·
可妥度肽药物代谢动力学(pk)群体=接受了至少1剂量的研究产品(可妥度肽或安慰剂)并获取了至少1份高于定量下限的可妥度肽pk样品的受试者。
[0148]
·
达格列净pk群体=接受了至少1剂量的研究产品(达格列净或安慰剂),并获取了至少1份达格列净的高于定量下限的达格列净pk样品的受试者。
[0149]
·
酮pk群体=接受了至少1剂量的研究产品(可妥度肽或达格列净或安慰剂),并获取了至少1份高于定量下限的酮pk样品的受试者。
[0150]
·
免疫原性群体=接受治疗群体(可妥度肽和安慰剂)中具有至少一份用于免疫原性试验的血清样品的受试者。
[0151]
分析群体汇总于表1中。无受试者被排除在任何分析群体之外。
[0152]
表1:分析群体
[0153]
群体安慰剂可妥度肽总计itt群体242549接受治疗群体242549免疫原性群体242549可妥度肽pk群体02525达格列净pk群体242549酮pk群体242448
[0154]
各治疗组之间的人口统计学特征和基线疾病特征通常保持平衡。(参见表2)接受治疗群体的平均年龄为59.7岁(范围:41至74岁),且大多数受试者为男性。平均体重为95.86kg,且在基线时,可妥度肽组的受试者体重低于安慰剂组的受试者(分别为92.24kg和99.63kg);平均总bmi为33.279kg/m2,且各组之间相似。平均身高为169.43cm。t2dm的平均持续时间为8.28年,并且可妥度肽组与安慰剂组相比,疾病持续时间更长(分别为9.16年和
7.36年)。基线时平均hba1c总体为7.69%(范围:6.5%至10.1%),且超过一半的受试者在基线时接受二甲双胍单一疗法(57.1%)。
[0155]
表2:受试者人口统计学特征和基线疾病特征(接受治疗群体)
[0156]
[0157]
[0158][0159]ahba1c=糖化血红蛋白;max=最大值;min=最小值;sd=标准偏差
[0160]b注意:在双盲治疗期间,受试者接受二甲双胍和达格列净背景二联疗法。
[0161]
(b)研究设计
[0162]
图2中提供了所提出研究的流程图。筛选期后,用二甲双胍单一疗法治疗的受试者仅进入4周的导入期,在此期间向受试者每天口服施用10mg达格列净。已用二甲双胍和达格列净二联疗法治疗过的纳入的受试者在整个研究中继续接受这种二联疗法(10mg达格列净和二甲双胍(最大耐受剂量(mtd)≥1g))。
[0163]
在导入期(针对接受二甲双胍单一疗法且空腹血浆葡萄糖(fpg)≥7.0mmol/l(126mg/dl)的受试者)或筛选期(针对接受二甲双胍和达格列净二联疗法的受试者)后,将受试者随机化为以下为期4周的治疗期中的治疗组:
[0164]
·
每天早上皮下(sc)施用一次可妥度肽(滴定量从100μg持续7天增加到200μg持续7天,再增加到300μg持续14天),持续28天(n=23);或
[0165]
·
每天早上sc施用一次安慰剂,持续28天(n=23)。
[0166]
给药可妥度肽或安慰剂的第一天被认为是第1天。在每次给药的当天,均如上所述施用研究产品(可妥度肽或安慰剂)。在需要禁食进行额外评估的研究日,在适用评估前大约2.5小时服用研究产品。对于居家治疗施用,应在每天早上醒来后在早餐前,在可行的范围内尽快使用载药注射器通过sc注射自我施用每日一次剂量。
[0167]
混合餐耐量试验
[0168]
在第-2天和第27天,受试者进入此单元。在第-1天和第28天,最少10小时禁食后,在受试者饮用标准化混合餐之前,立即采集葡萄糖代谢组(葡萄糖、胰岛素、c-肽、胰高血糖素和活性glp-1)的血液样品(t=“0分钟”)。然后受试者食用了一罐ensure plus,其为含有脂肪、碳水化合物和蛋白质组分的营养补充剂,组成标准混合餐耐量试验(mmtt)。餐后,获取定时连续的血液样品用于测量葡萄糖和与葡萄糖代谢相关的参数(在此期间无额外食物摄取)。在第-1天和第28天进行mmtt。
[0169]
食用标准餐后,在t=“0分钟”(餐前)和15、30、45、60、90、120、180和240分钟(
±
5分钟)时获取葡萄糖代谢组的血液样品。在第-1天和第28天施用标准餐后(t=“0分钟”)的第6、8、12和24小时(
±
30分钟),对胰高血糖素、胰岛素、c-肽和葡萄糖进行了额外采样。
[0170]
葡萄糖auc
0-4h
从基线(第-1天)到28天治疗结束(第28天)的变化和百分比变化由mmtt测量确定。此外,活性glp-1、胰高血糖素、胰岛素和c-肽auc
0-4h
从基线(第-1天)到第28天的变化也由mmtt测量。
[0171]
持续葡萄糖监测
[0172]
使用了持续葡萄糖监测(cgm)装置测量研究期间的间质葡萄糖水平。受试者持续
佩戴cgm传感器,直到更换传感器为止(每7至14天)。如果受试者在整个研究过程中无法忍受佩戴cgm传感器,则将传感器移除;但是受试者不论是否进行连续cgm都应留在研究中。
[0173]
血糖仪测量毛细血管血糖/酮读数
[0174]
在研究开始时,两个治疗组的每位受试者均获得了标准化血糖仪、葡萄糖和酮的测试条以及日记。在研究期间,鼓励受试者进行手指点刺试验(finger-prick test),如果他们感到不适,尤其是如果他们认为症状可能是由于低血糖引起的,则他们不需要定期测试。如果研究者或现场工作人员认为受试者可能正在经历低血糖或高血糖症,则用标准化血糖仪测试毛细血管血糖。毛细血管血糖水平<3mmol/l(54mg/dl)视为不良事件(ae),无论受试者是否有症状。
[0175]
在研究过程期间,受试者每天使用酮手指点刺试验条和提供的酮监测仪测试他们的血酮水平(早餐前)。要求受试者在纸质日记中记录酮值,该日记由研究工作人员提供并在门诊就诊时(即,当受试者把该纸质日记带回家时)检查。临床工作人员提供关于如何使用酮监测仪的培训。
[0176]
体重
[0177]
在筛选期间、在导入期开始时(第-28天)以及在第1天(给药前)和第29天早餐之前,测量体重。受试者应当脱下他们的鞋并且去除笨重衣物。使用校准的秤。
[0178]
确定从基线(第1天)到第29天的体重(kg)变化和百分比变化。还确定了从基线(第1天)到第29天体重减轻≥5%的受试者的比例。
[0179]
药物代谢动力学评估
[0180]
收集血液以评估可妥度肽和达格列净在血浆中的药物代谢动力学(pk)。使用单独的经过验证的液相色谱法-串联质谱法测量血浆中可妥度肽和达格列净的pk。pk的血液样品(可妥度肽和达格列净)采集如下:
[0181]
可妥度肽:
[0182]
·
第7、14和28天:给药前;给药后0.5、1和2小时(
±
15分钟);和给药后4、6、8和12(
±
30分钟);
[0183]
·
第8和15天:给药前;以及
[0184]
·
第29天:第28天给药时间后24小时
[0185]
达格列净:
[0186]
·
第-1、7、14和28天:给药前;给药后0.5、1和2小时(
±
15分钟);和给药后4、6、8和12小时(
±
30分钟);
[0187]
·
第1、8和15天:给药前;以及
[0188]
·
第29天:第28天给药时间后24小时
[0189]
免疫学评估和不良事件
[0190]
收集血液样品以评估抗药物抗体(ada)对可妥度肽的反应。使用经过验证的免疫测定评估血清样品的ada。收集自知情同意之日起整个治疗期并且包括随访期的不良事件(ae)和严重不良事件(sae)。按严重程度和与研究产品的关系对ae和sae进行分级,并且评估sae与方案程序的关系。
[0191]
(c)结果
[0192]
观察到可妥度肽组与安慰剂组相比,具有临床上有意义和统计学上显著的结果。
[0193]
mmtt血浆葡萄糖auc
0-4h
的变化
[0194]
评估了从基线评价到第28天评价的混合餐耐量试验(mmtt)血浆葡萄糖auc
0-4h
的变化。观察到可妥度肽组与安慰剂组相比,mmtt血浆葡萄糖auc
0-4h
从基线到第28天的减少在统计学上显著更大(ls平均差:-143.09mg-hr/dl;p<0.0001)(表3)。
[0195]
还评估了从基线评估到第28天评估的mmtt血浆葡萄糖auc
0-4h
的百分比变化。观察到可妥度肽组与安慰剂组相比,mmtt血浆葡萄糖auc
0-4h
从基线到第28天的减少在统计学上显著更大(ls平均差:-22.17%;p<0.0001)(表3)。
[0196]
表3:mmtt后从基线到第28天的血浆葡萄糖auc
0-4h
的变化和百分比变化(itt群体)
[0197]
[0198][0199]
ancova=协方差分析;auc
0-4h
=从时间0到4小时的浓度-时间曲线下面积;ci=置信区间;itt=意向治疗;ls=最小二乘;max=最大值;min=最小值;mmtt=混合餐耐量试
验;sd=标准偏差
[0200]
注意:在双盲治疗期间,受试者接受二甲双胍和达格列净背景二联疗法。
[0201]a来自以治疗效果和基线值为协变量的ancova的ls均值、其相关的95%ci和p值。
[0202]
由cgm测量的24小时葡萄糖控制
[0203]
受试者接受持续葡萄糖监测(cgm),共进行28天,其中每7至14天更换一次传感器。在第7(100μg)、14(200μg)和28(300μg)天,测量了cgm葡萄糖auc
0-24h
和24小时内平均葡萄糖从基线到每个给药水平结束的变化。通过测量24小时内cgm葡萄糖值的标准偏差(sd)、变异系数(cv)和平均葡萄糖波动幅度(mage)的变化,评估了葡萄糖水平的可变性。
[0204]
观察到可妥度肽组与安慰剂组相比,在第7天(分别为-832.66和49.14mg-hr/dl)和在第14天(分别为-666.05和57.30mg-hr/dl)的cgm葡萄糖auc
0-24h
相对于基线的平均减少在数值上更大。在第28天,观察到可妥度肽组与安慰剂组相比,cgm葡萄糖auc
0-24h
相对于基线的减少在统计学上显著更大(ls平均差:-806.61mg-hr/dl;p=0.0001)(表4)。
[0205]
表4:从基线到每个给药水平结束的cgm葡萄糖auc0-24h变化(itt群体)
[0206]
[0207][0208]
ancova=协方差分析;auc
0-24h
=从时间0到4小时的浓度-时间曲线下面积;cgm=持续葡萄糖监测;ci=置信区间;itt=意向治疗;locf=末次观察推进法;ls=最小二乘;max=最大值;min=最小值;sd=标准偏差
[0209]
注意:在双盲治疗期间,受试者接受二甲双胍和达格列净背景二联疗法。
[0210]a来自以治疗效果和基线值为协变量的ancova的ls均值、其相关的95%ci和p值。
[0211]
观察到可妥度肽组与安慰剂组相比,在第7天(分别为-34.74和2.59mg/dl)和在第14天(分别为-28.34和2.83mg/dl)的24小时内cgm平均葡萄糖相对于基线的平均减少在数值上更大。在第28天,观察到可妥度肽组与安慰剂组相比,cgm平均葡萄糖相对于基线的减少在统计学上显著更大(ls平均差:-34.06mg/dl;p=0.0001)。
[0212]
观察到可妥度肽组与安慰剂组相比,在第7天(分别为-7.21和-3.01mg/dl)和在第
14天(分别为-7.52和1.38mg/dl)的24小时内cgm葡萄糖的sd相对于基线的平均减少在数值上更大。在第28天,观察到可妥度肽组与安慰剂组相比,cgm葡萄糖的sd相对于基线的减少在统计学上显著更大(ls平均差:-8.45mg/dl;p=0.0029)(表5)。
[0213]
表5:从基线到每个给药水平结束的cgm葡萄糖24小时内sd变化(itt群体)
[0214]
[0215][0216]
ancova=协方差分析;auc
0-24h
=从时间0到24小时的浓度-时间曲线下面积;cgm=持续葡萄糖监测;ci=置信区间;itt=意向治疗;locf=末次观察推进法;ls=最小二乘;max=最大值;min=最小值;sd=标准偏差
[0217]
注意:在双盲治疗期间,受试者接受二甲双胍和达格列净背景二联疗法。
[0218]a来自根据基线值调整的协方差分析的ls均值、其相关的ci和p值。
[0219]
从基线到第7天、第14天或第28天的24小时内cgm葡萄糖的cv在各组之间无显著性差异(第28天的ls平均差:-2.41%;p=0.2429)。
[0220]
观察到可妥度肽组与安慰剂组相比,在第7天(分别为-25.74和-13.46mg/dl)和在第14天(分别为-26.59和18.05mg/dl)的cgm葡萄糖的mage相对于基线的平均减少在数值上更大。在第28天,观察到可妥度肽组与安慰剂组相比,cgm葡萄糖的mage相对于基线的减少在统计学上显著更大(ls平均差:-24.83mg/dl;p=0.0011)。
[0221]
在每个给药水平结束时,评估处于正常血糖、高血糖、低血糖和临床显著低血糖范围内的24小时cgm葡萄糖读数百分比相对于基线的变化。
[0222]
血糖正常范围定义为血浆葡萄糖≥70mg/dl(≥3.9mmol/l)且≤180mg/dl(≤10.0mmol/l)。对于血糖正常范围内的cgm葡萄糖读数的平均基线百分比,可妥度肽组为82.94%,且安慰剂组为84.77%。观察到可妥度肽组与安慰剂组相比,在第7天(分别为7.12%和-5.61%)和在第14天(分别为5.31%和-2.79%)的血糖正常范围内的cgm葡萄糖读数百分比相对于基线的平均增加在数值上更大。在第28天,观察到可妥度肽组与安慰剂组相比,血糖正常范围内的24小时cgm葡萄糖读数百分比相对于基线无显著性差异(ls平均差:8.78%;p=0.0828)。
[0223]
高血糖范围定义为血浆葡萄糖>180mg/dl(>10.0mmol/l)。对于高血糖范围内的cgm葡萄糖读数的平均基线百分比,可妥度肽组为14.11%,且安慰剂组为12.24%。观察到可妥度肽组与安慰剂组相比,在第7天(分别为-13.99%和3.62%)和在第14天(分别为-9.81%和0.36%)的高血糖范围内的cgm葡萄糖读数百分比相对于基线的平均减少在数值上更大。在第28天,观察到可妥度肽组与安慰剂组相比,高血糖范围内的cgm葡萄糖读数百分比相对于基线的减少在统计学上显著更大(ls平均差:-12.83%;p=0.0088)。
[0224]
低血糖范围定义为血浆葡萄糖<70mg/dl(<3.9mmol/l)。对于低血糖范围内的cgm葡萄糖读数的平均基线百分比,可妥度肽组为2.61%,且安慰剂组为2.67%。观察到可妥度肽组与安慰剂组相比,在第7天(分别为6.08%和1.17%)的低血糖范围内的cgm葡萄糖读数平均百分比相对于基线的增加在数值上更大,而各组在第14天(分别为3.44%和2.00%)相对于基线的变化相似。在第28天,观察到可妥度肽组与安慰剂组相比,低血糖范围内的24小时cgm葡萄糖读数百分比相对于基线无显著性差异(ls平均差:3.35%;p=0.2204)。
[0225]
临床显著低血糖范围定义为血浆葡萄糖<54mg/dl(3.0mmol/l)。两组的临床显著低血糖范围内的cgm血糖读数平均基线百分比都很低(可妥度肽组为0.58%,且安慰剂组为0.39%)。在第7天、第14天或第28天,在各组中观察到,临床显著低血糖范围内的24小时cgm血糖读数的百分比相对于基线无显著性差异(第28天ls平均差:1.03%;p=0.3692)。
[0226]
此外,对7天的cgm平均葡萄糖进行了事后分析,以进一步评价可妥度肽在每个剂量水平下对葡萄糖控制的作用。针对每个7天给药间隔(第1天至第7天[100μg剂量]、第8天至第14天[200μg剂量]、第15天至第21天和第22天至第28天[均300μg剂量]),七天cgm平均葡萄糖数据汇总如下。在每个剂量水平下,观察到可妥度肽组与安慰剂组相比,7天内cgm平均葡萄糖值的减少在统计学上显著更大(表6)。
[0227]
表6:在每个给药水平下的7天cgm平均葡萄糖的变化(itt群体)
[0228]
[0229][0230]
cgm=持续葡萄糖监测;ci=置信区间;itt=意向治疗;max=最大值;min=最小值;sd=标准偏差
[0231]
注意:在双盲治疗期间,受试者接受二甲双胍和达格列净背景二联疗法。
[0232]a2-样品t试验的p值。
[0233]
fpg的变化
[0234]
评估空腹血浆葡萄糖(fpg)从基线到第28天的变化。观察到可妥度肽组与安慰剂组相比,fpg从基线到第28天的减少在统计学上显著更大(ls平均差:-37.73mg/dl;p<0.0001)(表7)。
[0235]
表7:空腹血浆葡萄糖从基线到第28天的变化(itt群体)
[0236][0237]
ancova=协方差分析;ci=置信区间;itt=意向治疗;locf=末次观察推进法;ls=最小二乘;max=最大值;min=最小值;sd=标准偏差
[0238]
注意:在双盲治疗期间,受试者接受二甲双胍和达格列净背景二联疗法。
[0239]a来自以治疗效果和基线值为协变量的ancova的ls均值、其相关的95%ci和p值。
[0240]
hba1c的变化
[0241]
评估血红蛋白a1c(糖化血红蛋白;hba1c)从基线到第28天的变化。观察到可妥度肽组与安慰剂组相比,hba1c从基线到第28天的减少在统计学上显著更大(ls平均差:-0.58%;<0.0001)(表8)。
[0242]
表8:血红蛋白a1c从基线到第28天的变化(itt群体)
[0243][0244]
ancova=协方差分析;ci=置信区间;itt=意向治疗;ls=最小二乘;max=最大值;min=最小值;sd=标准偏差
[0245]
注意:在双盲治疗期间,受试者接受二甲双胍和达格列净背景二联疗法。
[0246]a来自以治疗效果和基线值为协变量的ancova的ls均值、其相关的95%ci和p值。
[0247]
体重的变化
[0248]
评估从基线到第29天的体重变化和百分比变化。观察到可妥度肽组与安慰剂组相比,体重(ls平均差:-2.13kg;p=0.0002)和体重百分比(ls平均差:-2.26%;p=0.0002)从基线到第29天的减少在统计学上显著更大(表9)。
[0249]
表9:从基线到第29天的体重变化和百分比变化(itt群体)
[0250][0251][0252]
ancova=协方差分析;ci=置信区间;itt=意向治疗;locf=末次观察推进法;ls=最小二乘
[0253]
注意:在双盲治疗期间,受试者接受二甲双胍和达格列净背景二联疗法。
[0254]a来自以治疗效果和基线值为协变量的ancova的ls均值、其相关的95%ci和p值。
[0255]
还评估了从基线到第29天体重减轻≥5%的受试者的比例。从基线到第29天,安慰剂组中没有受试者达到体重减轻≥5%,而可妥度肽组中有3名受试者(12.5%)达到。
[0256]
mmtt期间的胰腺和肠促胰岛素激素变化
[0257]
评估胰岛素和c-肽auc
004h
从基线到第28天的变化。基线时,可妥度肽组与安慰剂
组相比,平均胰岛素auc
0-4h
较高(分别为91.768和78.472hr.mu/l)。可妥度肽组和安慰剂组在第28天的ls平均胰岛素auc
0-4h
相对于基线无显著性差异(分别为-0.08和2.78hr.mu/l;ls平均差:-2.86hr.mu/l;p=0.7760)。基线时,可妥度肽组和安慰剂组的平均c-肽auc
0-4h
相似(分别为11.278和10.605hr.μg/l)。可妥度肽组和安慰剂组在第28天的ls平均c-肽auc
0-4h
相对于基线无显著性差异(分别为0.32和-0.29hr.μg/l;ls平均差:0.61hr.mu/l;p=0.4345)。
[0258]
评估了从基线到第28天的胰高血糖素auc
0-4h
变化,并且可妥度肽组和安慰剂组在第28天的ls平均胰高血糖素auc
0-4h
相对于基线无显著性差异(分别为-12.52和-23.84hr.pg/l;ls平均差:11.32hr.pg/l;p=0.7687)。
[0259]
评估了从基线到第28天的glp-1(活性形式)auc
0-4h
变化,并且可妥度肽组和安慰剂组在第28天的ls平均glp-1 auc
0-4h
相对于基线无显著性差异(分别为-131.67和-130.93hr.ng/l;ls平均差:-0.73hr.ng/l;p=0.9946)。
[0260]
酮体和ffa水平
[0261]
评估了空腹游离脂肪酸(ffa)从基线到每个剂量水平结束的变化。治疗组之间从基线到第7天(100μg)、第14天(200μg)或第28天(300μg)的空腹ffa变化相似(第28天ls平均差:-0.04meq/l;p=0.5322)。
[0262]
葡萄糖尿排泄
[0263]
评估了从基线到第28天的24小时葡萄糖尿排泄的变化。基线时,可妥度肽组的受试者相比于安慰剂组的受试者有较少的尿葡萄糖排泄(分别为4552.85和9107.06mg/24hr)。在第28天,可妥度肽组与安慰剂组相比,ls平均葡萄糖尿排泄相对于基线的减少更少(分别为-643.46和-1564.72mg/24h);然而,各组之间的差异无统计学意义(ls平均差:921.26mg/24h;p=0.4128)。
[0264]
药物代谢动力学参数
[0265]
评估了c
max
、t
max
、t
1/2 cl/f、auc
0-inf
、auc
0-最后
和auc
τ
的端点,以评价(在用达格列净、二甲双胍和可妥度肽治疗的受试者中)可妥度肽和达格列净的pk曲线、以及评价(在用达格列净、二甲双胍和安慰剂治疗的受试者中)达格列净的pk曲线。
[0266]
从观察到的数据中识别c
max
和相应的t
max
。末端相的对数线性回归得出了末端速率常数(λz)。通过对数线性梯形法则计算给药间隔期间血浆浓度时间-曲线下面积(auc
τ
)。曲线下面积到无穷大(auc
0-inf
)计算为auc(
0-t
)和ct/z的总和,其中ct是从最后一个可量化时间点的对数线性回归分析获得的观察到的血浆浓度,并且z是末端相速率常数。清除率(cl/f)由剂量/auc
0-inf
确定,并且末端半衰期(t
1/2
)计算为0.693/λz。
[0267]
单独的达格列净的平均pk参数与文献中报道的相似(达格列净新药上市申请(dapagliflozin new drug application submission)202293.fda.2013年7月11日):对于10mg/天/os(口服;po)的剂量,c
max
为120ng/ml,t
max
为1小时,auc
inf
为516至506ng.hr/ml,半衰期为15小时,并且表观清除率为约20l/hr。在本研究中,两个治疗组中表观清除率均是达格列净略高(在25l/hr范围内)。
[0268]
达格列净的最大血浆浓度受到可妥度肽存在的影响:在第-1天观察到平均c
max
为116.7ng/ml,在第7天和第14天分别降低至84.4ng/ml和61.1ng/ml,然后在第28天再次上升至94.2ng/ml。在接受达格列净和安慰剂的组中观察到了相似的效果,其中在第-1天观察到
平均c
max
为110.1ng/ml,在第7天和第14天分别降低至92.0ng/ml和95.6ng/ml,然后在第28天再次上升至112.2ng/ml。在第-1天和第28天之间的不同情况下,观察到c
max
的可变性相似(两种疗法(用可妥度肽和不用可妥度肽)的c
max
的cv%在35%至55%之间)。这种影响可能是由可妥度肽对胃排空的作用引起的。
[0269]
在所有情况下,就治疗组(其中达格列净与可妥度肽共同施用)中的auc
inf
而言,达格列净的总暴露都略高,尽管这早在第-1天就观察到了(尚未共同施用可妥度肽时)。达格列净c
谷
血浆浓度的分析还证实了达格列净与可妥度肽共同施用的给药前浓度有最小增加;然而,计算了2个治疗组之间达格列净的相似累积率,表明可妥度肽的存在不会导致总日暴露发生重大变化。
[0270]
在所有4种情况下,两个治疗组的表观清除率(大约25l/hr)与文献数据(20l/hr)相比都略高,并且因此t
1/2
降低(约8小时,相比于15小时),因此其与达格列净与可妥度肽的共同施用不可能相关。
[0271]
在达格列净的存在下,可妥度肽的pk符合该化合物的历史数据:在测试的剂量范围内观察到线性c
max
(100、200和300μg的剂量下平均c
max
分别为5.2ng/ml、10.1ng/ml和17.2ng/ml)和auc
inf
(100、200和300μg的剂量下平均auc
inf
分别为106.4ng.hr/ml、196.7ng.hr/ml和314.6ng.hr/ml)。各剂量下表观清除率和半衰期也一致(cl/f为1.1至1.3l/hr,并且t
1/2
为8.8-9.1小时)且符合历史数据。
[0272]
在所有情况下,β-羟基丁酸酯的血浆水平在两种治疗中相似。在第-1天和第28天之间,酮平均最大浓度(c
max
)在单独用达格列净治疗的受试者中观察到为0.29至0.35mmol/l,相比于在用达格列净与可妥度肽组合治疗的受试者中观察到为0.31至0.39mmol/l。类似地,在第-1天和第28天之间,通过auc
τ
测量的平均日暴露在单独用达格列净治疗的受试者中在4.58至5.32mmol.hr/l的范围内,相比于在用达格列净与可妥度肽组合治疗的受试者中观察到在4.95至5.44mmol.hr/l的范围内。
[0273]
可妥度肽给药前血浆浓度分析(c
谷
)表明在第7、14和28天平均浓度分别上升为1.9、3.5和5.2ng/ml,与剂量滴定100、200和300μg剂量一致,并且从历史数据总体上证实了该肽的pk线性。
[0274]
总体来说,单独的10mg/天po达格列净的pk结果符合文献结果,而100至300μg/天可妥度肽的pk结果符合历史数据。可妥度肽临床pk不受达格列净存在的影响,并且观察到对达格列净口服吸收的影响很小,这可能与glp-1药理学驱动的胃排空延迟有关。
[0275]
免疫原性
[0276]
评估了ada和滴度的发展(在任何测试呈阳性的受试者中),以评价滴定多至300μg剂量的可妥度肽的免疫原性概况。基线时,安慰剂组中无受试者而可妥度肽组中有3名受试者(12.0%)测试呈ada阳性。基线时测试呈阳性的这些受试者在基线后均无ada阳性。安慰剂组中有一名受试者(4.2%)而可妥度肽组中有3名受试者(12.5%)基线后呈ada阳性。没有受试者接受过增强ada的治疗,其定义为药物施用期间基线ada滴度增强到4倍或更高水平。
[0277]
就诊时,在第29天,安慰剂组无受试者而可妥度肽组有1名受试者(4.2%)呈ada阳性。在研究结束时,安慰剂组中有一名受试者(4.2%)而可妥度肽组中有2名受试者(8.3%)呈ada阳性。
[0278]
安全性
[0279]
总体来说,可妥度肽组和安慰剂组的治疗紧急不良事件(teae)的发生率相似(分别为52.0%和58.3%)。两名受试者(均在可妥度肽组)报告teae,这导致停用研究产品(由于腹痛和呕吐事件)。所有teae在严重程度上均为轻度(1级)或中度(2级)。
[0280]
研究产品相关的teae(由研究者判断)在可妥度肽组比安慰剂组更为频繁(分别为40.0%和16.7%)。与可妥度肽治疗相关的大多数teae均在胃肠道障碍的soc中。
[0281]
达格列净相关的teae的发生率(由研究者判断)在可妥度肽组和安慰剂组均较低且无明显不同(分别为4.0%和8.3%)。
[0282]
在施用可妥度肽后,在血液学、血清化学或尿检实验室值方面没有临床上有意义的趋势。施用可妥度肽后未观察到血压(bp)方面有意义的变化;然而,观察到可妥度肽组与安慰剂组相比心率增加。除了心率,在定量或定性心电图(ecg)参数方面均未观察到临床上有意义的趋势。
[0283]
结论
[0284]
观察到可妥度肽组与安慰剂组相比,mmtt血浆葡萄糖auc
0-4h
从基线到第28天的变化和百分比变化的减少在统计学上显著更大。
[0285]
从第7天开始一直持续到第28天,观察到可妥度肽组(每周滴定多至300μg剂量水平)与安慰剂组相比,cgm葡萄糖auc
0-24h
和24小时内平均葡萄糖的减少。如通过24小时内cgm葡萄糖值的sd和mage所评估的,在所有剂量水平下均观察到血糖可变性改善;观察到各组之间的cgm葡萄糖的cv无显著性差异。
[0286]
血糖正常范围内的cgm葡萄糖读数百分比在两个治疗组中均在基线时较高,如针对接受达格列净和二甲双胍双重背景治疗的受试者所预期的。在每个给药水平结束时,观察到可妥度肽组与安慰剂组相比,血糖正常范围内的cgm葡萄糖读数百分比相对于基线的增加在数值上更大。在28天给药结束时,观察到可妥度肽组与安慰剂组相比,高血糖范围内的cgm葡萄糖读数百分比的减少在统计学上显著更大。在任何剂量水平下,观察到低血糖范围内或临床显著低血糖范围内的cgm葡萄糖读数百分比无显著性差异。
[0287]
在每个剂量水平下,观察到可妥度肽组与安慰剂组相比,7天内cgm平均葡萄糖值的减少在统计学上显著更大。
[0288]
观察到可妥度肽组与安慰剂组相比,从基线到28天治疗结束,fpg和hba1c的减少在统计学上显著更大。
[0289]
观察到可妥度肽组与安慰剂组相比,从基线到29天治疗结束,体重的减少在统计学上显著更大。从基线到第29天,安慰剂组中没有受试者达到体重减轻≥5%,而可妥度肽组中有3名受试者(12.5%)达到。
[0290]
在28天治疗结束时,在mmtt期间,可妥度肽组和安慰剂组在胰腺和肠促胰岛素激素变化(包括胰岛素、c-肽、胰高血糖素和glp-1(活性形式))上无显著性差异。
[0291]
在可妥度肽组和安慰剂组观察到从基线到每个给药水平结束的空腹ffa变化相似。可妥度肽组和安慰剂组在β-羟基丁酸酯水平(酮体)上无显著性差异。
[0292]
28天治疗后,各组之间在24小时尿葡萄糖排泄上无统计学显著性差异。
[0293]
***
[0294]
本披露范围不受所描述的具体实施例的限制,这些实施例意欲作为本披露的单独
方面的简单说明,并且在功能上等效的任何组合物或方法均处于本披露的范围内。事实上,除了本文示出和描述的那些修改以外,本披露的各种修改通过前述说明书和附图对于本领域技术人员来说将变得清楚。此类修改旨在落入所附权利要求书的范围内。
[0295]
本说明书提到的所有公开和专利申请均通过引用并入本文,其引用程度就如同每个单独公开或专利申请特定地并且单独地指示通过引用并入本文一样。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。