一种干酪乳杆菌lc-12发酵溶胞产物的制备方法及其应用
技术领域
1.本发明涉及微生物发酵技术领域,特别涉及一种干酪乳杆菌发酵溶胞产物的制备方法及其应用。
背景技术:
2.乳酸杆菌是一类广泛应用于食品发酵技术领域和肠道健康维护的微生物,多具有人体肠道内较强的定殖能力和维护菌群平衡的效果;同时在乳制品发酵和植物基发酵等产品中可提供发酵风味和口感,并起到促进营养吸收和帮助消化的功能。
3.目前干酪乳杆菌多备用于牛乳、豆乳、干酪等乳制品的发酵剂或辅助发酵剂。随着植物基发酵饮品的兴起,干酪乳杆菌在花生乳、山药乳及核桃乳的发酵产品开发过程中也被广泛应用,使新品获得良好的风味。
4.近年来,对于包括乳酸杆菌在内的多种益生菌及其功能特性已研究的比较成熟,除食品行业外还应用在了医药领域及护肤领域。如专利申请cn103582486a中针对源自嗜酸乳杆菌、段度感觉和乳双歧杆菌的组合物具有较高的抗氧化活性,可应用于医药、食品领域。专利申请cn103937716a公开了一种具有显著体外抗氧化能力和抑制致病菌能力,并且能显著降低慢性酒精肝损伤大鼠模型血脂和血清内毒素水平的发酵乳杆菌grx07,该菌株能够缓解肝脏炎症反应,上调肝脏抗氧化特异蛋白nrf2表达量,降低干细胞凋亡率,下调肝脏炎性因子的表达,对慢性酒精肝损伤具有良好的缓解作用。专利申请cn111973546a公开了一种抗氧化益生菌面膜及其制备方法,所述活性成分包括植物乳杆菌24-7的发酵产物,具有良好的保湿、修复、预防衰老的功效。sz
ö
ll
˝ osi[ ]研究中证明,灭活型长双歧杆菌ncc2705和长双歧杆菌ncc3001(热处理)、长双歧杆菌bl/81和超声处理的长双歧杆菌bl/84裂解物促进人角质形成细胞(nheks)的分化标志物(角蛋白krt1、krt10和转谷氨酰胺酶tgm1)。此外,在融合后的nhek中,经长双歧杆菌非复制株和提取物处理后,抗菌肽(如β-防御素-1和bdef)以及参与伤口愈合的分子(如组织蛋白酶b、d和h)的表达显著增加。这些结果得到了mrna转录本水平的证实。
[0005]
许多化妆品中已开发出通过添加发酵产物来改善皮肤问题进行调控。gueniche将双歧杆菌的提取液作为化妆品的功效成分达到了缓解皮肤敏感性的效果,同时增加了皮肤对物理化学刺激的耐受性。在理肤泉的产品研发中,发现透明颤菌(vitreoscilla filliformis)发酵溶胞物可以刺激β防御素的产生及toll受体影响人先天免疫反应,从而缓解了皮肤的干燥和敏感症状,恢复了皮肤屏障机能和皮肤表面生物的多样性,最终改善了脂溢性皮炎和湿疹性皮炎。
[0006]
发明专利cn112375722b中公开了一种分离自新疆伊犁州健康婴儿粪便样本的可改善过敏的干酪乳杆菌lc-12及其产品、应用,菌种保藏编号为cgmccno .21372,保藏日期为2020年12月14日,菌种命名为lc-12,保藏单位为中国普通微生物菌种保藏管理中心。该菌株具有降低特异性ige的表达水平、提高特异性igg2a的表达水平、提高白介素10的表达水平的功能。权利要求包括所述的干酪乳杆菌lc-12(lactobacillus casei)制得的产品,
其特征在于,所述的产品包括内服制剂和/或外用制剂,且制剂中均含有所述的干酪乳杆菌lc-12粉剂,并要求所述制剂中干酪乳杆菌lc-12粉剂的活菌数﹥50亿/g。专利中实施例表现出通过活菌悬液灌胃方式处理后可降低过敏源在小鼠体内特异性ige的表达水平、提高过敏源在小鼠体内特异性igg2a的表达水平、提高小鼠机体内il-10的表达水平。该专利公开了干酪乳杆菌lc-12活菌在抗过敏方面的应用,其具有改善过敏性症状的功效。现有技术中未发现干酪乳杆菌lc-12在皮肤抗炎方面的研究。
技术实现要素:
[0007]
本发明要解决的技术问题是,提供一种具有皮肤抗炎功效的干酪乳杆菌lc-12发酵溶胞产物的制备方法及其应用。
[0008]
为解决上述技术问题,本发明采用以下技术方案:一种干酪乳杆菌lc-12发酵溶胞产物的制备方法,其特征在于采用以下步骤:a、将干酪乳杆菌lc-12接种到mrs培养基中进行培养,培养条件为:30-42℃,80-180 rpm/min转速摇床,培养20-80小时,得到种子液;所述mrs培养基由以下原料组分组成:酪蛋白酶消化物10.0g、柠檬酸三铵2.0g、牛肉膏粉10.0g、硫酸镁(mgso4
·
7h2o)0.2g、酵母膏粉4.0g、硫酸锰(mnso4 ·
4h2o) 0.05g、乙酸钠5.0g、磷酸氢二钾2.0g、葡萄糖20.0g、吐温80 1.08g;所述mrs培养基的ph值为5.5-5.9;所述干酪乳杆菌lc-12的保藏号为:cgmccno .21372,保藏单位为中国普通微生物菌种保藏管理中心; b、将步骤a所得种子液接种到mrs培养基中,在30-42℃环境,80-180 rpm/min转速下进行摇床扩培,得发酵液;c、将步骤b所得发酵液在3500-8000rpm转速,4℃环境下离心处理20min,过滤得干酪乳杆菌菌体;d、将步骤c所得干酪乳杆菌菌体用磷酸缓冲液进行洗涤,然后离心,反复洗涤2-5次,得洁净干酪乳杆菌菌体;所述磷酸缓冲液的摩尔浓度为0.01-0.05mol/l,ph 为6.5-7.5;e、将步骤d所得洁净干酪乳杆菌菌体与磷酸缓冲液按质量比1:1混合后,超声处理20-40min,得到破壁菌体混合物;将所述破壁菌体混合物进行离心处理,得上清液,即为干酪乳杆菌lc-12发酵溶胞产物。
[0009]
所述干酪乳杆菌lc-12发酵溶胞产物具有皮肤抗炎功效的应用。
[0010]
所述干酪乳杆菌lc-12发酵溶胞产物作为皮肤抗炎活性成分在化妆品中的应用,添加量为质量百分比0.078-5%。
[0011]
所述干酪乳杆菌lc-12发酵溶胞产物作为皮肤抗炎活性成分在化妆品中的应用,添加量为质量百分比0.2-5%。
[0012]
所述干酪乳杆菌lc-12发酵溶胞产物作为皮肤抗炎活性成分在化妆品中的应用,添加量为质量百分比2.5%。
[0013]
实施例1制备的干酪乳杆菌lc12发酵产物溶胞物具有抗炎功效评价实验,实验方法如下:1、材料试剂:磷酸盐缓冲液(pbs)、fbs、dmem高糖培养基、脂多糖(lps)、cck-8试剂
(abbkine)、no检测试剂盒(碧云天)。
[0014]
主要仪器:二氧化碳培养箱(panasonic)、二级生物安全柜(nuaire)、多功能酶标仪(spark)。
[0015]
样品来源:实施例1制备的干酪乳杆菌lc-12发酵溶胞产物。
[0016]
2、试验方法:2.1样品毒性浓度筛选2.1.1复苏细胞:将冻存raw264.7细胞解冻后接种于含fbs体积分数为10%的dmem培养基中,保证细胞状态和代数。5%体积浓度co2条件下培养箱中培养24h,用dmem培养基将raw细胞从培养瓶上冲洗下来,重悬细胞,进行计数,调节细胞浓度为细胞以13000个/孔,100μl/孔接种于96孔细胞培养板中,将96孔板置于37℃,5%体积浓度co2条件下培养箱中培养24h。
[0017]
2.1.2按不同浓度梯度稀释样品,每种待测样品配制4个浓度,将样品加入到细胞接种板中,同时设置:阳性对照:raw264.7细胞 1mg/mlsds;空白对照:raw264.7细胞 10�s的dmem培养基;试剂空白对照:无细胞,只加100μldmem培养基;然后将细胞培养板置于37℃,5%co2条件下培养箱中孵育24h。
[0018]
2.1.3培养结束,弃去培养液,向板内各孔中加入10μlcck-8溶液(包括试剂空白对照孔),轻轻震荡混匀,然后置于37℃,5%co2条件下培养箱中孵育1-2h。注意尽量不要在孔中引入气泡,在测定前需要将孔内气泡排净,避免干扰od读数。
[0019]
2.1.4孵育结束后,用酶标仪测96孔板各孔在450nm的吸光度值。
[0020]
2.1.5计算公式:细胞存活率(%)=(待测样品od-试剂空白od)/(空白组od-试剂空白od)
×
100%样品毒性浓度筛选实验结果如表1所示。在1.25-5%质量浓度范围内细胞存活率在90%以上,表面不具有细胞毒性,该浓度范围内可以应用于化妆品中或其他皮肤用产品中。
[0021]
2.2raw264.7细胞no含量测定2.2.1复苏细胞,将冻存细胞解冻后接种于含fbs体积分数为10%的dmem培养基中,保证细胞状态和代数。5%体积浓度co2条件下培养箱中培养24h,用dmem培养基将raw细胞从培养瓶上冲洗下来,重悬细胞,进行计数,调节细胞浓度为细胞以13000个/孔,100μl/孔接种于96孔细胞培养板中,将96孔板置于37℃,5%体积浓度co2条件下培养箱中培养24h。
[0022]
2.2.2筛选细胞毒性存活率大于90%的样品浓度,将样品加入到细胞接种板中,同时设置:空白对照:完全培养基 raw264.7细胞;阳性对照:完全培养基 raw264.7细胞 1μg/mllps 200μg/ml地塞米松;lps组:完全培养基 raw264.7细胞 1μg/mllps(终浓度);2.2.3细胞培养24h后,弃掉培养基,每孔加入200μl培养基,再加入2μllps溶液(100μg/ml),使其在体系中的终浓度为1μg/ml,混匀后将96孔板置于37℃,5%co2条
件下培养箱中培养24 h。
[0023]
2.2.4孵育24 h后,将 96 孔中细胞培养液每孔吸出50 μl到新的 96 孔板中,再先后加入 no 检测试剂盒中griess reagent
ꢀⅰ
溶液50 μl、griess reagent
ꢀⅱ
溶液50 μl,轻轻震荡混匀,用酶标仪测 96 孔板各孔在540 nm的吸光度值。
[0024]
2.2.5 计算公式:no抑制率(%)=1-((待测样品od-空白od)/(lps组od-空白od)
×
100%)2.3.统计分析所有试验按照平行设计原则,至少重复 2-3 次,实验数据以均数标准差(mean
±
sd)表示,使用 excel 统计软件进行数据分析。
[0025]
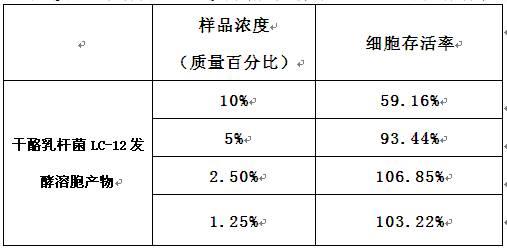
3.试验结果3.1注射液样品raw264.7细胞毒性筛选将实施例1制备的干酪乳杆菌lc-12发酵溶胞产物用纯净水分别稀释至质量百分浓度为10%、5%、2.50%和1.25%,选取不同浓度干酪乳杆菌lc-12发酵溶胞产物进行毒性筛选,筛选出最适浓度进行no含量检测。
[0026]
表1.不同浓度干酪乳杆菌lc-12发酵溶胞产物对raw264.7细胞存活率的影响实验结果显示,质量浓度为2.50%的干酪乳杆菌lc-12发酵溶胞产物细胞毒性最小,故选择质量浓度为2.50%的干酪乳杆菌lc-12发酵溶胞产物进行细胞no释放检测。
[0027]
3.2注射液样品raw264.7细胞no释放检测细菌脂多糖(lps)是格兰氏阴性菌细胞壁的主要组成成分之一,是诱导炎症反应的主要物质之一,no在免疫调节和炎症介导中起重要作用,利用lps诱导raw264.7小鼠巨噬细胞产生no是常用的的体外皮肤炎症检验模型。本实验采用质量浓度为2.50%的干酪乳杆菌lc-12发酵溶胞产物稀释液与100 μg/ml含量的地塞米松进行对比测试,实验结果如表2所示。
[0028]
表2.干酪乳杆菌lc-12发酵溶胞产物对raw264.7小鼠巨噬细胞no释放的影响
由于上述实验中使用的干酪乳杆菌lc12发酵溶胞产物浓度较高,为了验证该原料在no释放抑制率的抗炎效果方面有无浓度依赖性,故选取6个低浓度重复试验,结果如表3所示:表3.不同浓度干酪乳杆菌lc12发酵产物溶胞物样品对raw264.7小鼠巨噬细胞no释放的影响由表3可知,不同浓度干酪乳杆菌lc12发酵产物溶胞物样品对raw264.7小鼠巨噬细胞no释放的影响实验中,随着样品质量浓度的降低,其抑制效果同样呈下降趋势,在0.078125%浓度下仍有一定的no抑制率效果,说明其具有较好的抗炎作用,可以起到舒缓肌肤的功效。
[0029]
综上所述,本发明制备的干酪乳杆菌lc-12发酵溶胞产物,在1.25-5%质量浓度范围内细胞存活率在90%以上,该浓度范围内可以应用于化妆品中或其他类皮肤制剂中。不同质量浓度的干酪乳杆菌lc-12发酵溶胞产物对于抗炎的效果随着浓度的降低而降低,no抑制率在49.08%-8.10%之间,2.5%质量浓度时抗炎效果最好。质量浓度在0.078125%时,no抑制率为8.10%,仍然具有一定的抗炎效果。所以应用到化妆品中起抗炎功效的的质量浓度优选为2.5%。干酪乳杆菌lc-12发酵溶胞产物添加到化妆品中可以通过抗炎的作用起到舒缓肌肤的功效。
具体实施方式
[0030]
实施例1:一种干酪乳杆菌lc-12发酵溶胞产物的制备方法,其特征在于采用以下步骤:a、将干酪乳杆菌lc-12接种到mrs培养基中进行培养,培养条件为:30℃,80 rpm/min转速摇床,培养28小时,得到种子液,所述mrs培养基由以下原料组分组成:酪蛋白酶消化物10.0g、柠檬酸三铵2.0g、牛肉膏粉10.0g、硫酸镁(mgso4·
7h2o)0.2g、酵母膏粉4.0g、硫
酸锰(mnso
4 ·
4h2o) 0.05g、乙酸钠5.0g、磷酸氢二钾2.0g、葡萄糖20.0g、吐温80 1.08g;所述种子培养基的ph值为5.5;所述干酪乳杆菌lc-12的保藏号为:cgmccno .21372,保藏单位为中国普通微生物菌种保藏管理中心; b、将步骤a所得种子液接种到mrs培养基中,在30℃环境,80 rpm/min转速下进行摇床扩培,得发酵液;c、将步骤b所得发酵液在3500rpm转速,4℃环境下离心处理20min,过滤得干酪乳杆菌菌体;d、将步骤c所得干酪乳杆菌菌体用磷酸缓冲液进行洗涤,然后离心,反复洗涤2次,得洁净干酪乳杆菌菌体;所述磷酸缓冲液的摩尔浓度为0.01mol/l,ph 为6.5;e、将步骤d所得洁净干酪乳杆菌菌体与磷酸缓冲液按质量比1:1混合后,超声处理20min,得到破壁菌体混合物;将所述破壁菌体混合物进行离心处理,得上清液,即为为干酪乳杆菌lc-12发酵溶胞产物。
[0031]
实施例2:一种干酪乳杆菌lc-12发酵溶胞产物的制备方法,其特征在于采用以下步骤:a、将干酪乳杆菌lc-12接种到mrs培养基中进行培养,培养条件为:30-42℃,80-180 rpm/min转速摇床,培养52小时,得到种子液,所述mrs培养基由以下原料组分组成:酪蛋白酶消化物10.0g、柠檬酸三铵2.0g、牛肉膏粉10.0g、硫酸镁(mgso4·
7h2o)0.2g、酵母膏粉4.0g、硫酸锰(mnso
4 ·
4h2o) 0.05g、乙酸钠5.0g、磷酸氢二钾2.0g、葡萄糖20.0g、吐温80 1.08g;所述种子培养基的ph值为5.7;所述干酪乳杆菌lc-12的保藏号为:cgmccno .21372,保藏单位为中国普通微生物菌种保藏管理中心; b、将步骤a所得种子液接种到mrs培养基中,在35℃环境,100 rpm/min转速下进行摇床扩培,得发酵液;c、将步骤b所得发酵液在5000rpm转速,4℃环境下离心处理20min,过滤得干酪乳杆菌菌体;d、将步骤c所得干酪乳杆菌菌体用磷酸缓冲液进行洗涤,然后离心,反复洗涤3次,得洁净干酪乳杆菌菌体;所述磷酸缓冲液的摩尔浓度为0.02mol/l,ph 为7.0;e、将步骤d所得洁净干酪乳杆菌菌体与磷酸缓冲液按质量比1:1混合后,超声处理30min,得到破壁菌体混合物;将所述破壁菌体混合物进行离心处理,得上清液,即为为干酪乳杆菌lc-12发酵溶胞产物。
[0032]
实施例3:一种干酪乳杆菌lc-12发酵溶胞产物的制备方法,其特征在于采用以下步骤:a、将干酪乳杆菌lc-12接种到mrs培养基中进行培养,培养条件为:42℃,180 rpm/min转速摇床,培养80小时,得到种子液,所述mrs培养基由以下原料组分组成:酪蛋白酶消化物10.0g、柠檬酸三铵2.0g、牛肉膏粉10.0g、硫酸镁(mgso4·
7h2o)0.2g、酵母膏粉4.0g、硫酸锰(mnso
4 ·
4h2o) 0.05g、乙酸钠5.0g、磷酸氢二钾2.0g、葡萄糖20.0g、吐温80 1.08g;所述种子培养基的ph值为5.9;所述干酪乳杆菌lc-12的保藏号为:cgmccno .21372,保藏单位为中国普通微生物菌种保藏管理中心; b、将步骤a所得种子液接种到mrs培养基中,在42℃环境,180 rpm/min转速下进行摇床扩培,得发酵液;
c、将步骤b所得发酵液在8000rpm转速,4℃环境下离心处理20min,过滤得干酪乳杆菌菌体;d、将步骤c所得干酪乳杆菌菌体用磷酸缓冲液进行洗涤,然后离心,反复洗涤5次,得洁净干酪乳杆菌菌体;所述磷酸缓冲液的摩尔浓度为0.05mol/l,ph 为6.5-7.5;e、将步骤d所得洁净干酪乳杆菌菌体与磷酸缓冲液按质量比1:1混合后,超声处理40min,得到破壁菌体混合物;将所述破壁菌体混合物进行离心处理,得上清液,即为为干酪乳杆菌lc-12发酵溶胞产物。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。