用于癌症治疗的新型白介素-2变体
1.相关专利申请
2.本技术要求于2019年12月13日提交的美国临时申请第62/947,806号和于2019年6月14日提交的美国临时申请第62/861,651号的权益,所述临时申请的每一项通过引用以其整体并入本文。
背景技术:
3.白介素2(il-2)是首次描述的针对t细胞的生长因子。自其发现以来,il-2已被显示出在体外促进t细胞的增殖和存活(smith,k a.(1988)science.240,1169-76)以及在t病毒感染(blattman,j n等人,(2003)nat med 9,540-7)或疫苗(fishman,m.等人,(2008)j immunother.31,72-80,kudo-saito,c.等人,(2007)cancer immunol immunother.56,1897-910;lin,c t.等人,(2007)immunol lett.114,86-93)的情况中加强免疫应答的能力。
4.il-2已被用于癌症治疗。重组的人类il-2是一种用于转移性黑素瘤和肾癌的有效的免疫疗法,约10%的患者有持久的响应。然而,短半衰期和严重毒性限制了il-2的最佳给药。此外,il-2还以较高的亲和力与其异源三聚体受体il-2rαβγ结合,优先扩增表达高组成型水平il-2rα的免疫抑制性调节性t细胞(treg)。treg的扩增代表了il-2对癌症免疫疗法的不期望的影响。因此,使用il-2的癌症的成功的免疫疗法必须解决两个根本的重要问题:1)如何限制副作用,同时在需要处是有活性的;以及2)如何在限制treg刺激的同时优先活化效应t细胞。
5.最近发现,il-2可以被修饰以选择性地刺激细胞毒性效应t细胞。各种方法已经导致产生具有改进的和选择性的免疫刺激能力的il-2变体。这些il-2变体中的一些被设计成增加该分子主要通过高亲和力受体(α链、β链和γ链)而不是通过中等亲和力受体(β链和γ链)进行信号传导的能力。基本理念是促进在t细胞中的信号传导而不是在nk细胞中的信号传导,在nk细胞中的信号传导被认为是观察到的毒性作用的原因。以下发明都在该系列工作内:美国专利第7,186,804号,美国专利第7,105,653号,美国专利第6,955,807号,美国专利第5,229,109号,美国专利申请20050142106。重要的是应注意,这些发明都不涉及在体内比天然il-2具有更大治疗功效的il-2变体。
6.总之,il-2是一种高度多效性细胞因子,与不同细胞群体的生物活性密切相关。这一特性使il-2成为免疫应答调节中的重要节点,使il-2成为治疗和复杂免疫调节的吸引人的靶。此外,可以制备受体亚基偏倚的il-2变体以实现il-2介导的选择性免疫调节,以优先扩增和活化teff细胞来攻击癌细胞同时降低treg细胞的扩增和活化。
7.发明的公开内容
8.在一方面,本发明涉及il-2突变变体的产生,该il-2突变变体特征在于是il-2活性的选择性激动剂,具有降低或消除的与il-2rα的结合能力。特别地,这些变体将提供克服在天然il-2治疗中观察到的局限的方法,该局限源于天然il-2的已被证明的在体内扩增天然调节性t细胞的能力。本发明涉及除了若干个被突变的氨基酸以外,与人类il-2共有其一
级序列的多肽。引入的突变大幅降低了这些多肽刺激treg细胞的能力,并给予il-2更大的功效。此外,引入的突变预期减少cd25介导的vls和cd25介导的吸收效应(sink effect)。本发明涉及除了一个至若干个被突变的氨基酸以外,与人类il-2共有其一级序列的多肽。本发明还包括这些突变变体单独或与疫苗、或免疫检查点抑制剂、或肿瘤相关抗原(taa)靶向生物制品组合、或作为双功能融合构建体的一部分,用于治疗其中不期望调节性t细胞(treg)活性的疾病诸如癌症或感染的治疗用途。
9.在一方面,本发明涉及il-2突变变体的产生,该il-2突变变体特征在于是il-2活性的选择性激动剂,除了降低或消除的与il-2rα的结合能力之外,通过降低il-2rβγ相互作用具有最佳调节的整体效力。引入的突变防止了对途径的过度活化,降低了不期望的“命中靶(on-target)”“未命中组织(off-tissue)”毒性,减少了潜在的吸收,降低了与淋巴细胞过度刺激相关的活化诱导的细胞衰竭,减轻了受体介导的il-2内化,并且因此延长了体内半衰期,并导致缓慢和持久的药效学以改进生物分布、生物利用度、功能和抗肿瘤功效。本发明人还提出,使用与il-2rα的结合降低或消除和il-2rβγ活性减弱的il-2变体将促进在细胞因子和表现出明显不同的效力和分子量的抗体臂之间建立化学计量平衡,以允许最佳给药和维持每个臂的功能。本发明涉及除了一个至若干个被突变的氨基酸以外,与人类il-2共有其一级序列的多肽。本发明还包括这些突变变体单独或与疫苗、或免疫检查点抑制剂、或肿瘤相关抗原(taa)靶向生物制品组合、或作为双功能融合构建体的一部分用于治疗疾病诸如癌症或感染的治疗用途。
10.在一方面,本发明涉及il-2突变变体的产生,该il-2突变变体特征在于是il-2活性的选择性激动剂,除了降低或消除的与il-2rα的结合能力之外,具有降低的il-2rβγ相互作用。引入的突变提供了延长且持久的药效学和潜在地药代动力学。此外,引入的突变降低了细胞衰竭和活化诱导的细胞死亡,并增强了持久的淋巴细胞响应性。因此,引入的突变允许较少频率的给药方案,并提供临床上的给药便利。商品成本也预期降低。本发明涉及除了一个至若干个被突变的氨基酸以外,与人类il-2共有其一级序列的多肽。本发明还包括这些突变变体单独或与疫苗、或免疫检查点抑制剂、或肿瘤相关抗原(taa)靶向生物制品组合、或作为双功能融合构建体的一部分用于治疗疾病诸如癌症或感染的治疗用途。
11.在一方面,本发明涉及il-2突变变体的产生,该il-2突变变体特征在于是il-2活性的选择性激动剂,具有消除的与il-2rα的结合和野生型对应物无法匹敌的未预料到的高级别的增强的效应t细胞和nk细胞响应。cd25结合消除性突变被预期降低向cd25或cd25 细胞的吸收(sink),并因此增加对il-2rβγ的可用性。富集的受体占用引发强烈的细胞毒性细胞响应和强烈的肿瘤杀伤功效。本发明涉及除了一个至若干个被突变的氨基酸以外,与人类il-2共有其一级序列的多肽。本发明还包括这些突变变体单独或与疫苗、或免疫检查点抑制剂、或肿瘤相关抗原(taa)靶向生物制品组合、或作为双功能融合构建体的一部分用于治疗疾病诸如癌症或感染的治疗用途。
12.在本发明的一方面,引入的突变降低了与il-2rα(cd25)的结合能力,但保留了低水平的treg响应。残余的免疫调节性treg提供免疫平衡,以改进全身耐受性,并确保免疫平衡不会过度偏向细胞毒性效应细胞。精细调节的treg响应设置为不遭受肿瘤杀伤功效,但足够强以维持外周耐受性。本发明涉及除了一个至若干个被突变的氨基酸以外,与人类il-2共有其一级序列的多肽。本发明还包括这些突变变体单独或与疫苗、或免疫检查点抑制
剂、或肿瘤相关抗原(taa)靶向生物制品组合、或作为双功能融合构建体的一部分用于治疗疾病诸如癌症或感染的治疗用途。
13.在一方面,本发明涉及il-2突变变体的产生,该il-2突变变体具有降低的聚集、增加的表达、改进的可制造性和可开发性,伴随包括以下的属性的组合:例如,大幅降低的刺激treg细胞的能力、降低的受体过度活化、降低的不期望的“命中靶”“未命中组织”毒性以及延长的药效学,以改进生物分布、生物利用度、功能和抗肿瘤功效。本发明涉及除了一个至若干个被突变的氨基酸以外,与人类il-2共有其一级序列的多肽。本发明还包括这些突变变体单独或与疫苗、或免疫检查点抑制剂、或肿瘤相关抗原(taa)靶向生物制品组合、或作为双功能融合构建体的一部分用于治疗疾病诸如癌症或感染的治疗用途。
14.在一方面,本发明涉及il-2突变变体的产生,该il-2突变变体特征在于严重毒性(诸如在肾癌和黑素瘤的临床治疗中与高剂量il-2相关的血管渗漏综合征(vls))的降低。特别地,引入的突变大幅降低了与il-2rα(cd25)的结合能力;因此,削弱了与cd25 肺内皮细胞结合,并预期防止内皮细胞损伤和显著降低vls。本发明涉及除了一个至若干个被突变的氨基酸以外,与人类il-2共有其一级序列的多肽。本发明还包括这些突变变体单独或与疫苗、或免疫检查点调节剂、或肿瘤相关抗原(taa)靶向生物制品组合、或作为双功能融合构建体的一部分用于治疗疾病诸如癌症或感染以改进安全谱的治疗用途。
15.本发明允许当前在癌症治疗中基于il-2的免疫调节的策略的实质性改进。特别地,用本文描述的突变变体替换天然il-2,将导致不会优先于细胞毒性效应细胞刺激treg细胞,降低不期望的“命中靶”“未命中组织”毒性,使与过度刺激相关的细胞衰竭最小化,并改进药效学和潜在的药代动力学。预期突变会削弱与cd25 肺内皮细胞的结合,并且因此降低vls。在各种实施方案中,il-2变体(或突变体)包含源自如seq id no:3中列出的成熟的人类il-2多肽序列的il-2变体(或突变体)的序列。在各种实施方案中,il-2变体发挥il-2激动剂的作用。在各种实施方案中,il-2变体发挥il-2拮抗剂的作用。在各种实施方案中,il-2变体包含seq id no:31-66,或seq id no:111-120,或seq id no:47的氨基酸9-133、10-133和11-113。
16.在另一方面,本发明的il-2变体与至少一种异源蛋白附接。在各种实施方案中,il-2变体与至少一种赋予融合分子延长的半衰期的多肽融合。这样的多肽包括igg fc或结合新生fc受体的其他多肽、人类血清白蛋白或结合具有延长的血清半衰期的蛋白的多肽。在各种实施方案中,il-2变体与igg fc分子融合。在各种实施方案中,fc结构域是人类igg fc结构域。在各种实施方案中,fc结构域源自seq id no:6中列出的人类igg1重链恒定结构域序列。在各种实施方案中,fc结构域为具有seq id no:7中列出的氨基酸序列的fc结构域。在各种实施方案中,fc结构域为具有seq id no:8中列出的氨基酸序列的fc结构域。在各种实施方案中,fc结构域源自人类igg2重链恒定结构域序列。在各种实施方案中,fc结构域源自人类igg4重链恒定结构域序列。
17.在各种实施方案中,il-2变体可以与igg fc区的n末端或c末端连接。
18.术语“fc”是指包含完整抗体的非抗原结合片段的序列的分子或序列,无论是单体形式还是多聚体形式。天然fc的原始免疫球蛋白来源优选地为人类来源,并且可以是本领域公开的任何免疫球蛋白。天然fc由单体多肽组成,单体多肽可以通过共价(即二硫键)和非共价缔合连接成二聚体或多聚体形式。天然fc分子的单体亚基之间的分子间二硫键的数
目取决于类别(例如igg、iga、ige)或亚类(例如igg1、igg2、igg3、iga1、igga2)而在从1至4的范围内。天然fc的一种实例是由木瓜蛋白酶消化igg产生的二硫键合的二聚体(参见ellison等人(1982),nucleic acids res.10:4071-9)。如本文使用的术语“天然fc”是单体、二聚体和多聚体形式的总称。fc结构域包含蛋白a、蛋白g、各种fc受体和补体蛋白的结合位点。
19.在各种实施方案中,术语“fc变体”是指从天然fc修饰、但仍然包含补救受体fcrn的结合位点的分子或序列。国际申请wo 97/34631(1997年9月25日公布)和wo 96/32458描述了示例性的fc变体以及与补救受体的相互作用,并特此通过引用并入。此外,天然fc包含可被去除的位点,因为它们提供本发明的融合分子不需要的结构特征或生物活性。因此,在各种实施方案中,术语“fc变体”包括缺乏一个或更多个天然fc位点或残基的分子或序列,所述天然fc位点或残基影响或参与(1)二硫键形成,(2)与所选宿主细胞的不相容性,(3)在所选宿主细胞中表达时的n末端异质性,(4)糖基化,(5)与补体的相互作用,(6)与补救受体以外的fc受体的结合,或(7)抗体依赖性细胞毒性(adcc)。
20.术语“fc结构域”包括如上文定义的天然fc和fc变体分子和序列。如同fc变体和天然fc,术语“fc结构域”包括单体或多聚体形式的分子,无论是从完整抗体消化的还是通过重组基因表达或通过其他方式产生的。在各种实施方案中,“fc结构域”是指两个fc结构域单体(seq id no:6)的二聚体,其通常包括全部或部分的铰链区。在各种实施方案中,fc结构域可以被突变以缺乏效应子功能。在各种实施方案中,fc结构域中的每个fc结构域单体包含ch2抗体恒定结构域中的氨基酸取代,以降低fc结构域和fcγ受体之间的相互作用或结合。在各种实施方案中,fc结构域的每个亚基包含三个氨基酸取代,这三个氨基酸取代降低与活化性fc受体的结合和/或效应子功能,其中所述氨基酸取代是l234a、l235a和g237a(seq id no:7)。在各种实施方案中,fc结构域的每个亚基包含三个氨基酸取代,这三个氨基酸取代降低与活化性fc受体的结合和/或效应子功能,其中所述氨基酸取代是l234a、l235a和p329g。
21.在各种实施方案中,fc结构域可以被突变以进一步延长体内半衰期。在各种实施方案中,fc结构域的每个亚基包含美国专利公布第7,658,921号中公开的增强与人类fcrn的结合的三个氨基酸取代m252y、s254t和t256e。在各种实施方案中,fc结构域的每个亚基包含美国专利公布第7,371,826号中公开的氨基酸取代n434a(seq id no:8)。在各种实施方案中,fc结构域的每个亚基包含美国专利公布第8,546,543号中公开的增强与人类fcrn的结合的氨基酸取代m428l或n434s。在各种实施方案中,半衰期延长突变可以与降低与活化性fc受体的结合和/或效应子功能的氨基酸取代组合。
22.在各种实施方案中,il-2变体fc-融合蛋白将是单体的,即,仅包含单个il-2突变蛋白分子。在这样的实施方案中,融合蛋白共表达为异源二聚体fc(例如具有seq id no:9中列出的序列的knob-fc)与il-2变体和匹配的异源二聚体fc(例如具有seq id no:10中列出的序列的hole-fc)连接。当两个含fc的多肽的异源二聚体形成时,所得的蛋白仅包含单价il-2变体。在各种实施方案中,用于制备单价il-2fc融合蛋白的异源二聚体fc结构域是具有降低/消除的效应子功能和延长的半衰期的knob fc结构域(seq id no:134)和具有降低/消除的效应子功能和延长的半衰期的hole-fc结构域(seq id no:135)。
23.在各种实施方案中,本发明的il-2变体可以附接至赋予融合分子延长的半衰期的
抗体,诸如抗匙孔血蓝蛋白(klh)抗体。这样的抗体识别外来抗原,赋予较长的半衰期,但在人体中不具有生物功能或损害。igg类别可以是igg、iga、ige或亚类(例如,igg1、igg2、igg3、iga1、iga2)。
24.在各种实施方案中,本发明的il-2变体构建体包含结合癌症组织中富含的分子(诸如肿瘤相关抗原(taa))的抗体、抗体片段、蛋白或肽形式的靶向部分。
25.taa可以是针对其需要免疫应答的任何分子、大分子、分子组合等。taa可以是包含多于一个多肽亚基的蛋白。例如,蛋白可以为二聚体、三聚体或更高级多聚体。在各种实施方案中,蛋白的两个或更多个亚基可以以共价键诸如例如二硫键连接。在各种实施方案中,蛋白的亚基可以以非共价相互作用保持在一起。因此,taa可以是技术人员希望针对其诱导免疫应答的任何肽、多肽、蛋白、核酸、脂质、碳水化合物或有机小分子或其任何组合。在各种实施方案中,taa为包含以下的肽:约5个、约6个、约7个、约8个、约9个、约10个、约11个、约12个、约13个、约14个、约15个、约16个、约17个、约18个、约19个、约20个、约25个、约30个、约35个、约40个、约45个、约50个、约55个、约60个、约65个、约70个、约75个、约80个、约85个、约90个、约95个、约100个、约150个、约200个、约250个、约300个、约400个、约500个、约600个、约700个、约800个、约900或约1000个氨基酸。在各种实施方案中,肽、多肽或蛋白是通常通过注射向受试者施用的分子。
26.在各种实施方案中,肿瘤特异性抗体或结合蛋白用作靶向部分,以将il-2变体引导至病变部位,诸如肿瘤部位,在该部位它们可以刺激更佳的抗肿瘤免疫应答,同时避免游离细胞因子治疗的全身性毒性。对于il-2全激动剂(il-2full agonist),il-2
–
il-2r相互作用,而不是抗体-抗原靶向,可以决定免疫细胞因子在典型抗体剂量定位至il-2受体表达细胞而不是肿瘤细胞。在各种实施方案中,在抗体融合蛋白中使用具有降低/消除的与il-2rα的结合和减弱的效力的il-2变体有助于在il-2和靶向抗体之间建立化学计量平衡,以实现最佳剂量,在该剂量抗体可以实现足够的靶位占据,同时il-2部分不会引起途径的过度活化。在il-2抗体融合蛋白中使用具有降低/消除的与il-2rα的结合和减弱的效力的il-2变体并经由抗体进一步增强肿瘤靶向,使外周活化和aicd最小化、减轻抗原吸收并经由抗体臂促进肿瘤靶向。
27.在各种实施方案中,本发明的il-2变体可以附接至靶向/双功能部分,该靶向/双功能部分为靶向免疫检查点调节剂的抗体、抗体片段、蛋白或肽。
28.已经报道了在各种免疫细胞上表达的许多免疫检查点蛋白抗原,包括例如,sirp(在巨噬细胞、单核细胞、树突细胞上表达)、cd47(在肿瘤细胞和其他细胞类型上高表达)、vista(在单核细胞、树突细胞、b细胞、t细胞上表达)、cd152(由活化的cd8 t细胞、cd4 t细胞和调节性t细胞表达)、cd279(在肿瘤浸润性淋巴细胞上表达,由活化的t细胞(cd4和cd8两者)、调节性t细胞、活化的b细胞、活化的nk细胞、无变应性t细胞、单核细胞、树突细胞表达)、cd274(在t细胞、b细胞、树突细胞、巨噬细胞、血管内皮细胞、胰岛细胞上表达)和cd223(由活化的t细胞、调节性t细胞、无变应性t细胞、nk细胞、nkt细胞和浆细胞样树突细胞表达)(参见,例如,pardoll,d.,nature reviews cancer,12:252-264,2012)。结合被确定为免疫检查点蛋白的抗原的抗体是本领域技术人员已知的。例如,本领域已经描述了各种抗cd276抗体(参见,例如,美国专利公布第20120294796号(johnson等人)及其中引用的参考文献);本领域已经描述了各种抗cd272抗体(参见,例如,美国专利公布第20140017255号
(mataraza等人)及其中引用的参考文献);本领域已经描述了各种抗cd152/ctla-4抗体(参见,例如,美国专利公布第20130136749号(korman等人)及其中引用的参考文献);本领域已经描述了各种抗lag-3/cd223抗体(参见,例如,美国专利公布第20110150892号(thudium等人)及其中引用的参考文献);本领域已经描述了各种抗cd279(pd-1)抗体(参见例如,美国专利第7,488,802号(collins等人)及其中引用的参考文献);本领域已经描述了各种抗cd274(pd-l1)抗体(参见例如,美国专利公布第20130122014号(korman等人)及其中引用的参考文献);本领域已经描述了各种抗tim-3抗体(参见,例如,美国专利公布第20140044728号(takayanagi等人)及其中引用的参考文献);并且本领域已经描述了各种抗b7-h4抗体(参见,例如,美国专利公布第20110085970号(terrett等人)及其中引用的参考文献);并且本领域已经描述了各种抗tigit抗体(参见,例如,美国专利公布第20180169239a1号(grogan)及其中引用的参考文献)。这些参考文献中的每一篇关于其中教导的特定抗体和序列通过引用以其整体特此并入。
29.在各种实施方案中,il-2变体可以与表现出与存在于免疫细胞表面的免疫检查点蛋白抗原结合的抗体、抗体片段、或蛋白或肽融合。在各种实施方案中,免疫检查点蛋白抗原选自由以下组成的组但不限于cd279(pd-1)、cd274(pdl-1)、cd276、cd272、cd152、cd223(lag-3)、cd40、sirpα、cd47、ox-40、gitr、icos、cd27、4-1bb、tim-3、b7-h3、b7-h4、tigit和vista。
30.在各种实施方案中,抗体是拮抗性fap抗体或抗体片段。在各种实施方案中,抗体是包含seq id no:136和137中列出的可变结构域序列的人源化拮抗性fap抗体。在各种实施方案中,异源蛋白是针对免疫检查点调节剂的抗体或抗体片段。在各种实施方案中,抗体是拮抗性pd-1抗体或抗体片段。在各种实施方案中,抗体是包含以下中列出的可变结构域序列的拮抗性pd-1抗体:seq id no:138和139,seq id no:140和141,seq id no:142和143,seq id no:144和145,或seq id no:146和147。在各种实施方案中,抗体是包含seq id no:148和149中列出的可变结构域序列的拮抗性人类pd-l1抗体。在各种实施方案中,抗体是包含seq id no:150和151中列出的可变结构域序列的拮抗性ctla-4抗体。在各种实施方案中,异源蛋白通过接头和/或铰链接头肽附接至il-2变体。接头或铰链接头可以是相对地不含二级结构的在5个、10个、15个、20个、30个、40个或更多个氨基酸之间的人工序列。
31.在各种实施方案中,异源蛋白通过在10个、15个、20个、30个、40个或更多个氨基酸之间的刚性接头肽附接至il-2变体,所述刚性接头肽展示出α-螺旋构象并用作蛋白结构域之间的刚性间隔物。
32.在另一方面,il-2变体可以以美国专利第4,640,835号、第4,496,689号、第4,301,144号、第4,670,417号、第4,791,192号或第4,179,337号中阐述的方式连接至各种非蛋白质聚合物,包括但不限于各种多元醇,诸如聚乙二醇、聚丙二醇或聚氧化烯。在各种实施方案中,可以在il-2变体内的不同位置进行氨基酸取代,以促进聚合物诸如peg的添加。在各种实施方案中,这样的peg化的蛋白可以比非peg化的蛋白具有增加的半衰期和/或降低的免疫原性。
33.在各种实施方案中,il-2变体可以在n末端或c末端处非共价或共价地连接至结合新生fcγ/受体的igg fc或其他多肽、人类血清白蛋白、或结合具有延长的血清半衰期的蛋白的多肽或各种非蛋白质聚合物。
0531和p-0689共有相同的野生型il-2中的改进可开发性的氨基酸取代s125i。p-0531包含与同源二聚体fc融合的二价il-2变体,而p-0689包含与knob-into-hole异源二聚体fc融合的单价il-2。
43.图4描绘了在elisa中各种突变对il-2变体fc融合体与il-2rα结合强度的影响。(4a)il-2变体fc融合体含有对t41的氨基酸取代;(4b)il-2变体fc融合体含有对y107的氨基酸取代;(4c和4d)il-2变体fc融合体含有对r38的氨基酸取代。
44.图5描绘了在elisa中il-2e68取代对il-2变体fc融合体与il-2rα结合强度的影响。
45.图6描绘了在elisa中il-2e62取代对il-2变体fc融合体与il-2rα结合强度的影响。
46.图7描绘了在elisa中各种il-2p65取代对il-2变体fc融合体与il-2rα结合强度的影响。(7a-7b)il-2p65取代导致与il-2rα的结合增强;(7c)il-2p65取代导致与il-2rα的结合降低;(7d)il-2p65取代导致与il-2rα的结合完全丧失。
47.图8描绘了在elisa中il-2氨基酸取代组合对与il-2rα结合强度的影响。(8a)il-2f42a取代对与il-2rα结合强度的影响;(8b)f42a和破坏cd25的取代e62f的组合导致与il-2rα的结合完全丧失;(8c)f42a和破坏cd25的取代p65h的组合导致与il-2rα的结合完全丧失。
48.图9描绘了在人类pbmc测定中,与野生型融合蛋白(p-0531)和基准蛋白(p-0551)相比,il-2变体fc融合蛋白对cd4 treg细胞中stat5磷酸化的剂量依赖性诱导的不同作用。该组il-2变体含有导致与il-2rα结合增强、降低或消除的cd25干扰突变。
49.图10描绘了与野生型il-2融合蛋白p-0531和基准蛋白p-0551相比,在elisa中一组il-2变体fc融合蛋白与il-2rβγ结合的完全保留。该组il-2变体含有导致与il-2rα结合增强、降低或消除的cd25干扰突变。
50.图11描绘了在诱导人类pbmc中cd8 t细胞(11a)和nk细胞(11b)上的ki67表达方面表现出相当的活性的一组il-2变体fc融合蛋白。该组il-2变体含有导致与il-2rα结合增强、降低或消除的cd25干扰突变。野生型il-2融合蛋白p-0531和基准蛋白p-0511被包括在内用于比较。
51.图12描绘了il-2化合价对诱导人类pbmc中cd8 t细胞上的ki67表达的活性的影响。p-0531和p-0689是野生型il-2fc融合蛋白的二价和单价对应物。p-0635和p-0704是il-2p65r fc融合体的二价和单价等同物。
52.图13描绘了与其野生型对应物相比,各种调节il-2rβ/γc的氨基酸取代或n末端缺失对诱导cd4 t细胞上pstat5表达的活性的影响。(13a)在位置d20处具有氨基酸取代的il-2突变体;(13b-13c)在位置l19处具有氨基酸取代的il-2突变体;(13d)il-2q126e突变;和(13e)具有n末端氨基酸缺失的il-2突变体。
53.图14描绘了破坏il-2rβ或γc的氨基酸取代对elisa中与il-2rβγ结合强度的影响(14a)以及对诱导人类pbmc中cd8 t细胞上ki67表达的活性的影响(14b)。p-0689是单价野生型il-2fc融合蛋白,并且p-0704是单价il-2p65r fc融合体,它们不再能够与il-2rα结合,但保留对二聚体il-2rβγ受体的完全亲和力和功能活性。
54.图15描绘了在诱导人类pbmc中cd8 t细胞(15a)、nk细胞(15b)和cd4 t细胞(15c)
上的ki67表达方面,各种破坏il-2rβ的氨基酸变化对il-2变体fc融合体活性的影响。p-0704和基准分子(p-0551的单体形式)被包括在内用于比较。
55.图16描绘了在balb/c小鼠中单次注射后p-0704对外周血中treg细胞(16a)、cd8 t细胞(16b)和nk细胞(16c)的扩增的时间依赖性作用。p-0704是单价il-2p65r fc融合体;p-0689(单价野生型il-2fc融合蛋白)被包括在内用于比较。在第3天和第5天收集血液,用于通过facs分析进行淋巴细胞表型分析。
56.图17描绘了在人类pbmc测定中融合形式对cd4 treg细胞(17a)、cd8 t细胞(17b)和nk细胞(17c)上stat5磷酸化的剂量依赖性诱导的影响。p-0704是单价il-2p65r fc融合体,并且p-0803是含有相同il-2部分的抗体融合体。
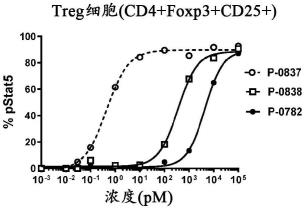
57.图18描绘了在人类pbmc测定中,与野生型融合蛋白(p-0837)相比,il-2变体抗体融合蛋白对cd4 treg细胞(18a)、cd8 t细胞(18b)和nk细胞(18c)上stat5磷酸化的剂量依赖性诱导的不同作用。p-0838含有显著降低与il-2rα结合能力的il-2p65q突变,并且p-0782具有与il-2rα结合被消除的il-2p65r部分。
58.图19描绘了调节il-2rβ的氨基酸变化对il-2变体抗体融合体在人类pbmc中在刺激cd8 t细胞(19a)和nk细胞(19b)上的stat5磷酸化以及诱导cd8 t细胞(19c)和nk细胞(19d)上的ki67表达方面的活性的影响。所有三种化合物都在il-2部分中包含p65r突变,并且p-0786和p-0783分别含有另外的破坏il-2rβ的突变l19q和l19h。
59.图20描绘了在人类pbmc测定中,在刺激cd4 treg细胞(20a)、cd8 t细胞(20b)和nk细胞(20c)上的stat5磷酸化以及诱导cd8 t细胞(20d)和nk细胞(20e)上的ki67表达方面,调节il-2rβ的氨基酸变化对il-2变体抗体融合体的活性的影响。所有三种化合物p-0838、p-0790和p-0787都在il-2部分中包含p65q突变,并且p-0790和p-0787分别含有另外的调节il-2rβ的突变l19q和l19h。p-0837是野生型il-2融合对应物。
60.图21描绘了在ctll-2细胞增殖方面,调节il-2rβ的氨基酸变化对il-2变体抗体融合体的活性的影响。p-0782、p-0783和p-0786全部在il-2部分中包含p65r突变;p-0786和p-0783分别含有另外的调节il-2rβ的突变l19q和l19h。p-0837是野生型il-2融合对应物。
61.图22描绘了在elisa中il-2变体的融合对与抗体臂的直接结合(22a)和配体竞争性抑制(22b)的极小影响,以及类似地,通过facs分析进行分析,il-2变体人类pd-1抗体il-2显示出与亲本抗体相似的与细胞表面表达的pd1的结合(图22c)。p-0795是人类pd-1拮抗剂抗体,p-0803、p-0880和p-0885具有与p-0795重链c末端共价连接的单体il-2p65r变体。p-0803和p-0885共有相同的il-2p65r/s125i取代,但具有不同的接头(分别为(g3s)2和(g4s)3)。与p-0880相比p-0885含有一个另外的l19q突变。p-0704和p-0859分别是p-0880和p-0885的fc融合对应物。
62.图23描绘了il-2变体抗体融合蛋白对人类pbmc中cd4 treg细胞(23a和23b)、cd8 t细胞(23c和23d)和nk细胞(23e和23f)上stat5磷酸化的剂量依赖性诱导的不同作用。p-0803和p-0804是分别含有p65r和l19h/p65r突变的il-2变体人类pd-1抗体融合蛋白。p-0782是il-2 p65r替代小鼠pd-1抗体融合体(il-2p65r surrogate mouse pd-1antibody fusion),并且与p-0782相比,p-0783含有另外的l19h突变。
63.图24描绘了蛋白a纯化后il-2变体人类pd-1抗体融合蛋白p-0840(24a)、p-0841(24b)、p-0803(24c)和p-0880(24d)的尺寸排阻色谱图。
64.图25描绘了在人类pbmc测定中,il-2变体抗体融合蛋白的接头长度对cd8 t细胞(25a和25b)和nk细胞(25c和25d)上stat5磷酸化的剂量依赖性诱导的影响。p-0840和p-0841两者都是il-2l19q/p65q变体人类pd-1抗体融合蛋白;p-0840包含(g3s)2接头,而p-0841具有(g4s)3接头。同样地,p-0803和p-0880是il-2p65r变体人类pd-1抗体融合蛋白;p-0803包含(g3s)2接头,而p-0880具有(g4s)3接头。
65.图26描绘了在人类pbmc中,在刺激cd8 t细胞(26a)和nk细胞(26b)上的stat5磷酸化以及诱导cd8 t细胞(26c)和nk细胞(26d)上的ki67表达方面,调节il-2rβ的氨基酸变化对il-2变体人类pd-1抗体融合体的活性的影响。所有三种化合物p-0880、p-0885和p-0882都在il-2部分中包含p65r突变,而p-0885和p-0882分别含有另外的调节il-2rβ的突变l19q和l19h。p-0849是野生型il-2融合对应物。所有化合物都具有连接pd-1抗体重链和il-2的(g4s)3接头。
66.图27描绘了在c57bl6小鼠中单次注射后,il-2变体替代小鼠pd-1抗体融合蛋白p-0782、p-0838、p-0781(基准)和p-0837对cd8 t细胞(27a)和nk细胞(27b)上ki67表达的时间依赖性作用,以及对cd8细胞(27c)和nk细胞(27d)细胞扩增的时间依赖性作用。细胞扩增以细胞数量相对于基线的变化倍数来表示。p-0782在il-2部分中包含p65r突变,p-0838含有p65q突变,p-0781含有消除了与il-2rα的结合的基准il-2变体,并且p-0837是野生型il-2融合对应物。
67.图28描绘了在c57bl6小鼠中单次注射后,il-2变体替代小鼠pd-1抗体融合蛋白p-0786对cd8 t细胞(28a)和nk细胞(28b)上ki67表达的时间依赖性和剂量依赖性作用,以及对cd8 t细胞(28c)和nk细胞(28d)的细胞扩增的时间依赖性和剂量依赖性作用。细胞扩增以细胞数量相对于基线的变化倍数来表示。p-0786包含l19q/p65r突变,该突变导致与il-2rα的结合被消除以及整体效力降低。p-0837(野生型il-2融合对应物)被包括在内用于比较。
68.图29描绘了在c57bl6小鼠中单次注射后,il-2变体替代小鼠pd-1抗体融合蛋白p-0783对cd8 t细胞(29a)和nk细胞(29b)上ki67表达的时间依赖性和剂量依赖性作用,以及对cd8细胞(29c)和nk细胞(29d)的细胞扩增的时间依赖性和剂量依赖性作用。细胞扩增以细胞数量相对于基线的变化倍数来表示。p-0783包含l19h/p65r突变,该突变导致与il-2rα的结合被消除以及整体效力降低。p-0837(野生型il-2融合对应物)被包括在内用于比较。
69.图30描绘了用il-2变体替代小鼠pd-1抗体融合蛋白p-0782、p-0786和p-0783处理的c57bl/6小鼠的体重变化。所有化合物在il-2部分中都包含p65r突变,p-0781含有消除了与il-2rα的结合的基准il-2变体,并且p-0786和p-0783分别含有另外的破坏il-2rβ的突变l19q和l19h。数据表示为平均值
±
sem。
70.图31描绘了在皮下b16f10鼠黑素瘤肿瘤模型中,按照q7d重复给药方案,il-2变体替代小鼠pd-1抗体融合蛋白的抗肿瘤功效(31a)和体重变化(31b)。所有三种抗体融合蛋白都含有il-2p65q突变,以削弱与il-2rα的结合;p-0790和p-0787分别包含另外的l19q和l19h突变,以进一步调节整体效力。数据表示为平均值
±
sem。
71.图32描绘了在皮下b16f10鼠黑素瘤肿瘤模型中,按照q7d重复给药方案,两种不同剂量的p-0787的抗肿瘤功效(32a)和体重变化(32b)。p-0787是包含l19h/p65q突变的il-2变体替代小鼠pd-1抗体融合蛋白。数据表示为平均值
±
sem。
72.图33描绘了在皮下b16f10鼠黑素瘤肿瘤模型中,按照q7d重复给药方案,il-2变体替代小鼠pd-1抗体融合蛋白p-0782和p-0786的抗肿瘤功效。p-0722(替代小鼠pd-1抗体)被包括在内用于比较。p-0782和p-0786两者都包含消除il-2rα结合的突变p65r,而p-0786含有另外的l19q突变以调节整体效力。数据表示为平均值
±
sem。
73.图34描绘了在小鼠b16f10肺转移模型中p-0790对肺转移结节的剂量依赖性抑制。(34a)平均肺结节计数;(34b)来自每组的代表性动物的肺部图片。p-0790是il-2l19q/p65q替代小鼠pd-1抗体融合蛋白,其具有显著受损的与il-2rα的结合和受调节的整体效力。数据表示为平均值
±
sem。通过单因素anova随后tukey事后检验进行统计分析。*p《0.05。
74.用于进行本公开内容的方式
75.本发明涉及除了一个至若干个被突变的氨基酸以外,与人类il-2共有一级序列的多肽。il-2变体包含大幅降低这些多肽刺激treg细胞的能力并使其在肿瘤治疗中更有效的突变。还包括这些突变变体单独使用或与疫苗、或taa靶向生物制品、或免疫检查点阻断剂组合使用、或用作双功能分子构建体中的构建模块,用于治疗其中不期望调节性t细胞(treg)活性的疾病诸如癌症或感染的治疗用途。在另一方面,本发明涉及包含所公开的多肽的药物组合物。最后,本发明涉及所公开的多肽和药物组合物的治疗用途,这是由于它们选择性调节免疫系统对癌症和其他感染性疾病的作用。
76.定义
77.术语“多肽”、“肽”和“蛋白”在本文中可互换使用,以指氨基酸残基的聚合物。在各种实施方案中,“肽”、“多肽”和“蛋白”是其α碳通过肽键连接的氨基酸链。因此链的一个末尾(氨基末端)处的末端氨基酸具有游离氨基基团,而链的另一个末尾(羧基末端)处的末端氨基酸具有游离羧基基团。如本文使用的,术语“氨基末端”(缩写为n末端)是指在肽的氨基末端处的氨基酸上的游离α-氨基基团,或指在肽中的任何其他位置处的氨基酸的α-氨基基团(参与肽键时的氨基基团)。类似地,术语“羧基末端”是指肽的羧基末端上的游离羧基基团,或肽中任何其他位置处的氨基酸的羧基基团。肽还包括基本上任何多氨基酸,包括但不限于肽模拟物(peptide mimetic),诸如通过醚键而非酰胺键连接的氨基酸。
78.本公开内容的多肽包括已经以任何方式和出于任何原因被修饰的多肽,例如,以:(1)降低对蛋白水解的敏感性,(2)降低对氧化的敏感性,(3)改变形成蛋白复合物的结合亲和力,(4)改变结合亲和力,和(5)赋予或改变其他物理化学特性或功能特性。
79.如本文使用的氨基酸“取代”是指用不同的氨基酸替换多肽中亲本多肽序列的特定位置处的一个氨基酸。氨基酸取代可以使用本领域熟知的遗传方法或化学方法来产生。例如,单氨基酸取代或多氨基酸取代(例如,保守氨基酸取代)可以在天然存在的序列中进行(例如,在形成分子间接触的结构域以外的多肽部分中)。“保守氨基酸取代”是指多肽中的氨基酸被功能上相似的氨基酸取代。以下六组各自包含互相为保守取代的氨基酸:
80.1)丙氨酸(a)、丝氨酸(s)和苏氨酸(t)
81.2)天冬氨酸(d)和谷氨酸(e)
82.3)天冬酰胺(n)和谷氨酰胺(q)
83.4)精氨酸(r)和赖氨酸(k)
84.5)异亮氨酸(i)、亮氨酸(l)、甲硫氨酸(m)和缬氨酸(v)
85.6)苯丙氨酸(f)、酪氨酸(y)和色氨酸(w)
[0086]“非保守氨基酸取代”是指这些类别之一的成员取代为来自另一类别的成员。在进行这样的改变时,根据各种实施方案,可以考虑氨基酸的亲水指数(hydropathic index)。基于氨基酸的疏水性和电荷特征,每种氨基酸已经被指定了亲水指数。它们是:异亮氨酸( 4.5);缬氨酸( 4.2);亮氨酸( 3.8);苯丙氨酸( 2.8);半胱氨酸/胱氨酸( 2.5);甲硫氨酸( 1.9);丙氨酸( 1.8);甘氨酸(-0.4);苏氨酸(-0.7);丝氨酸(-0.8);色氨酸(-0.9);酪氨酸(-1.3);脯氨酸(-1.6);组氨酸(-3.2);谷氨酸(-3.5);谷氨酰胺(-3.5);天冬氨酸(-3.5);天冬酰胺(-3.5);赖氨酸(-3.9)和精氨酸(-4.5)。
[0087]
本领域理解亲水氨基酸指数在赋予蛋白相互作用的生物功能中的重要性(参见例如,kyte等人,1982,j.mol.biol.157:105-131)。已知,某些氨基酸可以被具有相似亲水指数或评分的其他氨基酸取代,并且仍保持相似的生物活性。在基于亲水指数进行改变时,在各种实施方案中,包括了其亲水指数在
±
2内的氨基酸的取代。在各种实施方案中,包括在
±
1内的那些,并且在各种实施方案中,包括在
±
0.5内的那些。
[0088]
本领域还理解,可以基于亲水性有效地进行相似氨基酸的取代,特别是当从而产生的生物功能蛋白或肽被意图用于在免疫学实施方案中使用时,如本文所公开的。在各种实施方案中,蛋白的最大局部平均亲水性(如由其相邻氨基酸的亲水性决定的)与其免疫原性和抗原性,即,与蛋白的生物学特性相关。
[0089]
以下亲水性值(hydrophilicity values)被指定至这些氨基酸残基:精氨酸( 3.0);赖氨酸( 3.0);天冬氨酸( 3.0. -.1);谷氨酸( 3.0. -.1);丝氨酸( 0.3);天冬酰胺( 0.2);谷氨酰胺( 0.2);甘氨酸(0);苏氨酸(-0.4);脯氨酸(-0.5. -.1);丙氨酸(-0.5);组氨酸(-0.5);半胱氨酸(-1.0);甲硫氨酸(-1.3);缬氨酸(-1.5);亮氨酸(-1.8);异亮氨酸(-1.8);酪氨酸(-2.3);苯丙氨酸(-2.5)和色氨酸(-3.4)。在基于相似亲水性值进行改变时,在各种实施方案中,包括其亲水性值在
±
2内的氨基酸的取代,在各种实施方案中,包括在
±
1内的那些,并且在各种实施方案中,包括在
±
0.5内的那些。
[0090]
示例性的氨基酸取代在表1中列出。
[0091]
表1
[0092][0093]
技术人员将能够使用公知技术确定如本文列出的合适的多肽变体。在各种实施方案中,本领域技术人员可以通过靶向被认为对于活性不重要的区域来鉴定分子中可以被改变而不破坏活性的适合区域。在其他实施方案中,技术人员可以鉴定在相似多肽间保守的分子的残基和部分。在另外的实施方案中,即使可能对生物活性或对结构重要的区域也可以经历保守氨基酸取代,而不破坏生物活性或不会不利地影响多肽结构。
[0094]
此外,本领域技术人员可以回顾鉴定相似多肽中对活性或结构重要的残基的结构-功能研究。鉴于这样的比较,技术人员可以预测对应于相似多肽中对活性或结构重要的氨基酸残基的多肽中的氨基酸残基的重要性。本领域技术人员可以选择对这样预测的重要氨基酸残基进行化学上相似的氨基酸取代。
[0095]
本领域技术人员还可以分析相似多肽中与该结构相关的三维结构和氨基酸序列。鉴于这样的信息,本领域技术人员可以预测多肽的氨基酸残基在其三维结构方面的排列。在各种实施方案中,本领域技术人员可以选择不对预测在多肽表面上的氨基酸残基进行根本改变(radical changes),因为此类残基可能参与与其他分子的重要相互作用。此外,本领域技术人员可以产生在每个期望的氨基酸残基处包含单个氨基酸取代的测试变体。然后可以使用本领域技术人员已知的活性测定来筛选变体。这些变体可以用于收集关于合适变体的信息。例如,如果人们发现,特定氨基酸残基的改变导致破坏的、不期望地减少的或不合适的活性,则可以避免具有这样的改变的变体。换句话说,基于从这样的常规实验收集的
信息,本领域技术人员可以容易地确定应避免在该处单独的或与其他突变组合的进一步取代的氨基酸。
[0096]
如本文使用的术语“多肽片段”和“截短的多肽”是指与对应的全长蛋白相比具有氨基末端缺失和/或羧基末端缺失的多肽。在各种实施方案中,片段的长度可以是例如,至少5个、至少10个、至少25个、至少50个、至少100个、至少150个、至少200个、至少250个、至少300个、至少350个、至少400个、至少450个、至少500个、至少600个、至少700个、至少800个、至少900个或至少1000个氨基酸。在各种实施方案中,片段的长度还可以是例如,最多1000个、最多900个、最多800个、最多700个、最多600个、最多500个、最多450个、最多400个、最多350个、最多300个、最多250个、最多200个、最多150个、最多100个、最多50个、最多25个、最多10个或最多5个氨基酸。片段还可以在其任一个或两个末端处包含一个或更多个另外的氨基酸,例如,来自不同的天然存在的蛋白的氨基酸的序列(例如,fc或亮氨酸拉链结构域)或人工氨基酸序列(例如,人工接头序列)。
[0097]
本文使用的术语“多肽变体”、“杂合多肽(hybrid polypeptide)”和“多肽突变体”是指包含这样的氨基酸序列的多肽,其中相对于另一个多肽序列,一个或更多个氨基酸残基被插入到该氨基酸序列中、从该氨基酸序列中缺失和/或被取代到该氨基酸序列中。在各种实施方案中,待被插入、缺失或取代的氨基酸残基的数目可以是例如,至少1个、至少2个、至少3个、至少4个、至少5个、至少10个、至少25个、至少50个、至少75个、至少100个、至少125个、至少150个、至少175个、至少200个、至少225个、至少250个、至少275个、至少300个、至少350个、至少400个、至少450个或至少500个氨基酸的长度。本公开内容的杂合体包括融合蛋白。
[0098]
多肽的“衍生物”是已经被化学修饰的多肽,所述化学修饰例如,缀合至另一个化学部分(诸如例如,聚乙二醇、白蛋白(例如,人类血清白蛋白))、磷酸化和糖基化。
[0099]
术语“%序列同一性”与术语“%同一性”在本文中可互换使用并且指当使用序列比对程序比对时,在两个或更多个肽序列之间的氨基酸序列同一性的水平或在两个或更多个核苷酸序列之间的核苷酸序列同一性的水平。例如,如本文使用的,通过定义的算法确定的80%同一性与80%序列同一性意指相同的意思,并且意指给定序列与另一长度的另一序列至少80%相同。在各种实施方案中,%同一性选自例如,与给定序列至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%或更大的序列同一性。在各种实施方案中,%同一性在例如约60%至约70%、约70%至约80%、约80%至约85%、约85%至约90%、约90%至约95%或约95%至约99%的范围内。
[0100]
术语“%序列同源性”与术语“%同源性”在本文中可互换使用并且指当使用序列比对程序比对时,在两个或更多个肽序列之间的氨基酸序列同源性的水平或在两个或更多个核苷酸序列之间的核苷酸序列同源性的水平。例如,如本文使用的,通过定义的算法确定的80%同源性与80%序列同源性意指相同的意思,并且因此给定序列的同源物具有相对于给定序列的长度大于80%的序列同源性。在各种实施方案中,%同源性选自例如,与给定序列至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%或更大的序列同源性。在各种实施方案中,%同源性在例如约60%至约70%、约70%至约80%、约80%至约85%、约85%至约90%、约90%至约95%或约95%至约99%的范围内。
[0101]
可以用于确定两个序列之间的同一性的示例性计算机程序包括但不限于在互联网在ncbi的网站上公开地可得的一套blast程序,例如blastn、blastx和tblastx、blastp和tblastn。另参见altschul等人,j.mol.biol.215:403-10,1990(特别参考公布的默认设置,即参数w=4、t=17)和altschul等人,nucleic acids res.,25:3389-3402,1997。当相对于genbank蛋白序列和其他公开数据库中的氨基酸序列评价给定氨基酸序列时,通常使用blastp程序进行序列检索。blastx程序优选用于针对在genbank蛋白序列和其他公开数据库中的氨基酸序列检索在所有阅读框中已经被翻译的核酸序列。使用开放空位(gap)罚分为11.0和延伸空位罚分为1.0的默认参数并且使用blosum-62矩阵运行blastp和blastx两者。
[0102]
除了计算序列同一性百分比以外,blast算法还进行两个序列之间的相似性的统计分析(参见例如,karlin &altschul,proc.nat'l.acad.sci.usa,90:5873-5787,1993)。由blast算法提供的相似性的一个量度是最小总概率(p(n)),所述最小总概率提供在两个核苷酸序列或氨基酸序列之间的匹配偶然发生的概率的指示。例如,如果在测试核酸与参考核酸的比较中,最小总概率为例如小于约0.1、小于约0.01或小于约0.001,则该核酸被认为与参考序列相似。
[0103]
如本文使用的术语“修饰”是指对肽骨架(例如氨基酸序列)的任何操作或对多肽的翻译后修饰(例如糖基化)。
[0104]
如本文使用的术语“knob-into-hole修饰”是指两个免疫球蛋白重链的ch3结构域之间的界面内的修饰。在一种实施方案中,“knob-into-hole修饰”包含一条抗体重链中的氨基酸取代t366w和任选的氨基酸取代s354c,以及另一条抗体重链中的氨基酸取代t366s、l368a、y407v和任选的y349c。knob-into-hole技术在例如美国专利第5,731,168号;美国专利第7,695,936号;ridgway等人,prot eng 9,617-621(1996)和carter,j immunol meth 248,7-15(2001)中描述。
[0105]
如本文使用的术语“融合蛋白”是指包含两个或更多个最初编码不同蛋白的基因的融合多肽分子,其中融合蛋白的组分通过肽键直接彼此连接或通过肽接头彼此连接。如本文使用的术语“融合”是指通过肽键直接连接的组分或经由一个或更多个肽接头连接的组分。
[0106]“接头”是指共价地或通过离子键、范德华力或氢键连接两个其他分子的分子,例如在5'末端处与一个互补序列杂交并且在3'末端处与另一个互补序列杂交从而连接两个非互补序列的核酸分子。“可裂解的接头”是指可以被降解或以其他方式切断以使通过该可裂解的接头连接的两个组分分开的接头。可裂解的接头通常被酶,通常是肽酶、蛋白酶、核酸酶、脂肪酶等裂解。可裂解的接头还可以通过环境因素,诸如例如温度、ph、盐浓度等的改变来裂解。
[0107]
如本文使用的术语“肽接头”是指包含一个或更多个氨基酸,通常为约2个-20个氨基酸的肽。肽接头是本领域已知的或在本文中被描述。合适的非免疫原性接头肽包括,例如,(g4s)n、(sg4)n或g4(sg4)n肽接头。“n”通常是1和10之间,通常2和4之间的数字。
[0108]“药物组合物”是指适于在动物中药物使用的组合物。药物组合物包含药理学有效量的活性剂和药学上可接受的载体。“药理学有效量”是指有效产生预期药理学结果的剂的量。“药学上可接受的载体”是指任何标准的药物载体、媒介物、缓冲剂和赋形剂,诸如磷酸
盐缓冲盐水溶液、5%右旋糖的水性溶液,和乳液,诸如油/水乳液或水/油乳液,和各种类型的润湿剂和/或佐剂。合适的药学载体和制剂在remington's pharmaceutical sciences,第21版2005,mack publishing co,easton中描述。“药学上可接受的盐”是可以被配制成用于药学用途的化合物的盐,包括例如金属盐(钠、钾、镁、钙等)和氨的盐或有机胺的盐。
[0109]
如本文使用的,“治疗(treatment)”(及其语法变化形式诸如“治疗(treat)”或“治疗(treating)”)是指试图改变被治疗的个体的疾病的自然过程的临床干预,并且临床干预可以用于预防来进行或者在临床病理过程期间进行。期望的治疗效果包括但不限于,防止疾病的发生或复发、减轻症状、减轻疾病的任何直接或间接病理后果、防止转移、降低疾病进展速度、改善或缓和疾病状态以及缓解或改善预后。如本文使用的,“减轻”疾病、紊乱或状况意指降低疾病、紊乱或状况的症状的严重性和/或发生频率。另外,本文中述及“治疗”包括述及治愈性、缓解性和预防性治疗。
[0110]
如本文使用的术语“有效量”或“治疗有效量”是指足以治疗特定紊乱、状况或疾病,诸如改善、缓和、减轻和/或延迟其一种或更多种症状的化合物或组合物的量。述及癌症或其他不需要的细胞增殖,有效量包括足以实现以下的量:(i)降低癌细胞的数目;(ii)降低肿瘤尺寸;(iii)在一定程度抑制、延缓、减缓并且优选地停止癌细胞浸润到外周器官中;(iv)抑制(即,在一定程度减缓并且优选地停止)肿瘤转移;(v)抑制肿瘤生长;(vi)预防或延迟肿瘤的发生和/或复发;和/或(vii)在一定程度减轻一种或更多种与癌症相关的症状。有效量可以以一次或更多次施用来施用。
[0111]
措辞“施用”或“引起施用(cause to be administered)”是指由医学专业人员(例如医师)或控制患者的医疗护理的人员采取的控制和/或允许向患者施用所讨论的剂/化合物的行动。引起施用可以包括诊断和/或确定合适的治疗方案,和/或为患者开特定的剂/化合物的处方。这样的开处方可以包括例如起草处方形式、注释医疗记录等。当本文中描述施用时也设想了“引起施用”。
[0112]
术语“患者”、“个体”和“受试者”可以互换地使用,并且指哺乳动物,优选人类或非人类灵长类动物,但也指家养哺乳动物(例如犬科动物或猫科动物)、实验室哺乳动物(例如小鼠、大鼠、兔、仓鼠、豚鼠)和农业哺乳动物(例如马科动物、牛科动物、猪、绵羊(ovine))。在各种实施方案中,患者可以是在医院、精神病护理机构如门诊或其他临床环境中的医师或其他卫生工作者的护理下的人类(例如,成年男性、成年女性、青少年男性、青少年女性、男性儿童、女性儿童)。在各种实施方案中,患者可以是免疫功能低下的患者或免疫系统减弱的患者,包括但不限于患有原发性免疫缺陷、aids的患者;服用某些免疫抑制药物的癌症患者和移植患者;以及患有影响免疫系统的遗传性疾病(例如,先天性无丙种球蛋白血症、先天性iga缺乏症)的患者。在各种实施方案中,患者患有免疫原性癌症,包括但不限于膀胱癌、肺癌、黑素瘤和报道具有高突变率的其他癌症(lawrence等人,nature,499(7457):214-218,2013)。
[0113]
术语“免疫疗法”是指包括但不限于以下的癌症治疗:使用针对特定肿瘤抗原的消耗性抗体的治疗;使用抗体-药物缀合物的治疗;使用针对共刺激性或共抑制性分子(免疫检查点)(诸如ctla-4、pd-1、ox-40、cd137、gitr、lag3、tim-3、sirp、cd47和vista)的激动性抗体、拮抗性抗体或阻断性抗体的治疗;使用双特异性t细胞结合抗体诸如博纳吐单抗的治疗;涉及施用生物响应调节剂(诸如il-2、il-12、il-15、il-21、gm-csf、ifn-α、
ifn-β和ifn-γ)的治疗;使用治疗性疫苗诸如sipuleucel-t的治疗;使用树突细胞疫苗或肿瘤抗原肽疫苗的治疗;使用嵌合抗原受体(car)-t细胞的治疗;使用car-nk细胞的治疗;使用肿瘤浸润性淋巴细胞(til)的治疗;使用过继转移的抗肿瘤t细胞(离体扩增的和/或tcr转基因的)的治疗;使用tall-104细胞的治疗;和使用免疫刺激剂(诸如toll样受体(tlr)激动剂cpg和咪喹莫特)的治疗。
[0114]“耐受性或难治性癌症”是指不响应于先前的抗癌疗法的肿瘤细胞或癌症,所述先前的抗癌疗法包括例如化学疗法、手术、放射疗法、干细胞移植和免疫疗法。肿瘤细胞可以在治疗的开始时是耐受性或难治性的,或者它们可以在治疗期间变成耐受性或难治性的。难治性肿瘤细胞包括在治疗的开始时不响应的肿瘤,或最初持续短的时间段响应治疗但不能响应治疗的肿瘤。难治性肿瘤细胞还包括响应于使用抗癌疗法的治疗但不能响应于随后几轮疗法的肿瘤。为了本发明的目的,难治性肿瘤细胞还包括通过使用抗癌疗法的治疗表现出被抑制但在治疗停止后长达5年,有时长达10年或更长时间而复发的肿瘤。抗癌疗法可以使用单独的化学治疗剂、单独的放射、单独的靶向疗法、单独的手术或其组合。为了便于描述而非限制,应理解,难治性肿瘤细胞与耐受性肿瘤是可互换的。
[0115]
如本文使用的术语“fc结构域”或“fc区”用于定义免疫球蛋白重链的c末端区域,其包含至少一部分恒定区。该术语包括天然序列fc区和变体fc区。igg fc区包含igg ch2和igg ch3结构域。本文中的ch3区可以是天然序列ch3结构域或变体ch3结构域(例如,在其一条链中具有引入的“突起(protuberance)”(“knob”)并且在其另一条链中具有相应的引入的“空腔(cavity)”(“hole”)的ch3结构域;参见美国专利第5,821,333号,通过引用明确并入本文)。这样的变体ch3结构域可以用于促进如本文描述的两个不同的免疫球蛋白重链的异源二聚体化。除非本文中另外规定,否则fc区或恒定区中氨基酸残基的编号根据eu编号系统。
[0116]
如本文使用的术语“效应子功能”是指可归因于免疫球蛋白的fc区的那些生物活性,所述fc区随免疫球蛋白亚型而不同。免疫球蛋白效应子功能的实例包括:c1q结合和补体依赖性细胞毒性(cdc)、fc受体结合、抗体依赖性细胞介导的细胞毒性(adcc)、抗体依赖性细胞吞噬作用(adcp)、细胞因子分泌、免疫复合物介导的抗原呈递细胞的抗原摄取、细胞表面受体(例如b细胞受体)的下调和b细胞活化。效应子功能也可以指由效应免疫细胞诸如cd8细胞和nk细胞引发的类似免疫应答。
[0117]
如本文使用的术语“调节性t细胞”或“treg细胞”意指可以抑制其他t细胞(效应t细胞)的响应的专门类型的cd4 t细胞。treg细胞的特征在于cd4、il-2受体(cd25)的α亚基和转录因子叉头盒p3(foxp3)的表达(sakaguchi,annu rev immunol 22,531-62(2004)),并在诱导和维持对抗原(包括由肿瘤表达的抗原)的外周自身耐受性中起关键作用。
[0118]
如本文使用的术语“常规cd4 t细胞”意指调节性t细胞之外的cd4 t细胞。常规cd4 t细胞表达cd3和cd4。在幼稚和未受刺激的条件下,它们不表达il-2受体的α亚基(cd25),但表达il-2受体的βγ亚基。
[0119]
术语“cd8 t细胞”是一类特征在于表达cd3和cd8的细胞毒性t淋巴细胞。cd8 t细胞主要表达il-2受体的βγ亚基,并在杀伤癌细胞、被病毒感染的细胞或以其他方式受损的细胞中发挥关键作用。
[0120]
术语“nk细胞”是一类对先天免疫系统至关重要的细胞毒性淋巴细胞。nk细胞主要
表达il-2受体的βγ亚基,并提供针对病毒感染的细胞和肿瘤形成的快速应答。
[0121]
如本文使用的,“特异性结合”意指对抗原的结合是选择性的,并且可以与不需要的或非特异性的相互作用区分开。免疫球蛋白结合特定抗原的能力可以通过酶联免疫吸附测定(elisa)或本领域技术人员熟悉的其他技术例如表面等离子体共振(spr)技术来测量。
[0122]
如本文使用的术语“亲和力”或“结合亲和力”是指分子(例如抗体)的单个结合位点与其结合配偶体(例如抗原)之间的非共价相互作用的总和的强度。分子x对其配偶体y的亲和力一般可以通过解离常数(kd)来呈现,解离常数是解离速率常数和结合速率常数(分别为koff和kon)的比率。用于测量亲和力的一种特殊方法是表面等离子体共振(spr)。
[0123]
如本文使用的,术语“降低的结合”是指各自相互作用的亲和力的降低,如例如通过spr测量的。相反,“增加的结合”是指各自相互作用的结合亲和力的增加。
[0124]
如本文使用的术语“聚合物”通常包括但不限于均聚物;共聚物,诸如例如嵌段、接枝、无规和交替共聚物;和三元共聚物;以及它们的混合物和变化形式(modifications)。此外,除非另外明确限定,否则术语“聚合物”应包括材料的所有可能的几何构型。这些构型包括但不限于全同立构、间同立构和无规对称。
[0125]“聚乙二醇”或“peg”意指聚亚烷基二醇化合物或其衍生物,带有或不带有偶联剂或衍生化,所述衍生化带有偶联部分或活化部分(例如带有醛、羟基琥珀酰亚胺基、酰肼、硫醇、三氟甲磺酸酯、tresylate、氮丙啶、环氧乙烷、邻二硫吡啶(orthopyridyl disulphide)、乙烯基砜、碘乙酰胺或马来酰亚胺部分)。在各种实施方案中,peg包括基本上线性的、直链peg、支链peg或树枝状peg。peg是一种公知的水溶性聚合物,可商购获得或可根据本领域公知的方法通过乙二醇的开环聚合制备(sandler和karo,polymer synthesis,academic press,new york,vol.3,第138-161页)。
[0126]“多核苷酸”是指包含核苷酸单元的聚合物。多核苷酸包括天然存在的核酸,诸如脱氧核糖核酸(“dna”)和核糖核酸(“rna”)以及核酸类似物。核酸类似物包括包含以下的那些:非天然存在的碱基,以天然存在的磷酸二酯键以外的连接与其他核苷酸衔接(engage)的核苷酸,或包含通过除了磷酸二酯键以外的连接来附接的碱基的核苷酸。因此,核苷酸类似物包括例如并且不限于,硫代磷酸酯、二硫代磷酸酯、磷酸三酯(phosphorotriester)、氨基磷酸酯(phosphoramidate)、有机磷酸酯(organophosphate)、甲基膦酸酯、手性甲基膦酸酯、2-o-甲基核糖核苷酸、肽核酸(pna)等。这样的多核苷酸可以例如使用自动化的dna合成仪来合成。术语“核酸”通常是指大的多核苷酸。术语“寡核苷酸”通常是指短的多核苷酸,通常不大于约50个核苷酸。将理解的是,当核苷酸序列由dna序列(即,a、t、g、c)表示时,这还包括其中“u”代替“t”的rna序列(即,a、u、g、c)。
[0127]
本文使用常规符号描述多核苷酸序列:单链多核苷酸序列的左手末端为5'-末端;双链多核苷酸序列的左手方向被称作5'-方向。向新生rna转录物5'至3'添加核苷酸的方向被称作转录方向。具有与mrna相同的序列的dna链被称作“编码链”;在具有与从该dna转录的mrna相同的序列的dna链上并且位于rna转录物的5'-末端的5'的序列被称作“上游序列”;在具有与rna相同的序列的dna链上并且在编码rna转录物的3'-末端的3'的序列被称作“下游序列”。
[0128]“互补的”是指两个多核苷酸的相互作用表面的拓扑相容性或匹配在一起。因此,这两个分子可以被描述为互补的,并且更进一步地,接触表面特征是彼此互补的。如果第一
多核苷酸的核苷酸序列与第二多核苷酸的多核苷酸结合配偶体的核苷酸序列基本上相同,或者如果第一多核苷酸可以与第二多核苷酸在严格杂交条件下杂交,则第一多核苷酸与第二多核苷酸是互补的。
[0129]“与...特异性杂交”或“特异性杂交”或“与...选择性杂交”是指当特定核苷酸序列存在于复杂混合物(例如,总细胞)dna或rna中时,在严格条件下核酸分子优先与该序列的结合、双链体化或杂交。术语“严格条件”是指这样的条件,在该条件下探针将优先与其靶子序列杂交,并且在较小程度上与其它序列杂交或根本不与其他序列杂交。在核酸杂交实验诸如dna杂交和rna杂交的背景下,“严格杂交”和“严格杂交洗涤条件”为序列依赖性的,并且在不同的环境参数下是不同的。对核酸杂交的广泛指导可见于:tijssen,1993,laboratory techniques in biochemistry and molecular biology
‑‑
hybridization with nucleic acid probes,第i部分,第2章,“overview of principles of hybridization and the strategy of nucleic acid probe assays”,elsevier,n.y.;sambrook等人,2001,molecular cloning:a laboratory manual,cold spring harbor laboratory,第3增补版,ny;以及ausubel等人,编著,现行版,current protocols in molecular biology,greene publishing associates and wiley interscience,ny。
[0130]
通常,高度严格的杂交和洗涤条件被选择为比在定义的离子强度和ph的特定序列的热解链点(tm)低约5℃。tm为50%的靶序列与完全匹配的探针杂交的温度(在定义的离子强度和ph条件下)。非常严格的条件被选择为等于特定探针的tm。用于在dna印迹或rna印迹中的滤器上进行具有多于约100个互补残基的互补核酸的杂交的严格杂交条件的实例为在42℃,50%福尔马林与1mg肝素,过夜进行杂交。高度严格的洗涤条件的实例为在72℃,0.15m nacl,持续约15分钟。严格洗涤条件的实例为在65℃,0.2x ssc洗涤,持续15分钟。参见sambrook等人对于ssc缓冲液的描述。可以进行低严格洗涤以去除背景探针信号,然后进行高严格洗涤。对于例如多于约100个核苷酸的双链体的示例性中度严格洗涤为在45℃,1x ssc,持续15分钟。对于例如多于约100个核苷酸的双链体的示例性低严格洗涤为在40℃,4-6x ssc,持续15分钟。通常,在特定杂交测定中,与对不相关探针观察到的信噪比相比2x(或更高)的信噪比指示检测到特异性杂交。
[0131]“引物”是指能够与指定的多核苷酸模板特异性杂交并提供用于合成互补多核苷酸的起始点的多核苷酸。当多核苷酸引物被置于诱导合成的条件下(即,在核苷酸、互补多核苷酸模板和用于聚合的剂诸如dna聚合酶的存在下)时,这样的合成发生。引物通常是单链的,但可以是双链的。引物通常为脱氧核糖核酸,但许多合成的和天然存在的引物可用于许多应用。引物与模板互补,引物被设计成与模板杂交以用作合成起始的位点,但不需要反映模板的精确序列。在这样的情况下,引物与模板的特异性杂交取决于杂交条件的严格度。引物可以用例如显色性、放射性或荧光性的部分标记并用作可检测的部分。
[0132]
当用于述及多核苷酸使用时,“探针”是指能够与另一多核苷酸的指定序列特异性杂交的多核苷酸。探针与靶互补多核苷酸特异性杂交,但不需要反映模板的精确互补序列。在这样的情况下,探针与靶的特异性杂交取决于杂交条件的严格度。探针可以用例如显色性、放射性或荧光性的部分标记并用作可检测的部分。在其中探针提供用于合成互补多核苷酸的起始点的情况下,探针也可以是引物。
[0133]“载体”是可以被用于将与其连接的另一核酸引入到细胞中的多核苷酸。一种类型
的载体是“质粒”,其是指可以将另外的核酸区段连接到其中的线性或环状双链dna分子。另一种类型的载体是病毒载体(例如,复制缺陷型逆转录病毒、腺病毒和腺相关病毒),其中另外的dna区段可以被引入到病毒基因组中。某些载体能够在引入了它们的宿主细胞中自主复制(例如,包含细菌复制起点的细菌载体和附加型哺乳动物载体(episomal mammalian vector))。其他载体(例如,非附加型哺乳动物载体)在引入到宿主细胞中后被整合到宿主细胞的基因组中,并且从而与宿主基因组一起复制。“表达载体”是可以指导选择的多核苷酸的表达的一种类型的载体。
[0134]“调控序列”是影响与其可操作地连接的核酸的表达(例如,表达的水平、时机或位置)的核酸。调控序列可以例如直接对被调控的核酸发挥其作用,或通过一种或更多种其他分子(例如,与调控序列和/或核酸结合的多肽)的作用发挥其作用。调控序列的实例包括启动子、增强子和其他表达控制元件(例如多腺苷酸化信号)。调控序列的另外的实例描述于例如goeddel,1990,gene expression technology:methods in enzymology 185,academic press,san diego;california.和baron等人,1995,nucleic acids res.23:3605-06中。如果调控序列影响核苷酸序列的表达(例如,表达的水平、时机或位置),则核苷酸序列与调控序列“可操作地连接”。
[0135]“宿主细胞”是可以被用于表达本公开内容的多核苷酸的细胞。宿主细胞可以是原核生物,例如大肠杆菌(e.coli),或者宿主细胞可以是真核生物,例如单细胞真核生物(例如,酵母或其他真菌)、植物细胞(例如,烟草或番茄植物细胞)、动物细胞(例如,人类细胞、猴细胞、仓鼠细胞、大鼠细胞、小鼠细胞或昆虫细胞)或杂交瘤。通常,宿主细胞是可以用编码多肽的核酸转化或转染的培养的细胞,所述核酸然后可以在宿主细胞中被表达。措辞“重组宿主细胞”可以被用于表示已经用待表达的核酸转化或转染的宿主细胞。宿主细胞还可以是包含核酸但不以期望的水平表达该核酸的细胞,除非调控序列被引入到宿主细胞中,使得调控序列变成与该核酸可操作地连接。应理解,术语宿主细胞不仅指特定的受试者细胞,而且还指这样的细胞的后代或潜在后代。因为某些修饰可以由于例如突变或环境影响而在随后世代中发生,这样的后代实际上可能与亲本细胞不相同,但仍然被包括在如本文使用的该术语的范围内。
[0136]
术语“分离的分子”(其中分子是例如多肽或多核苷酸)是这样的分子:该分子凭借其起源或衍生的来源(1)不与在其天然状态中伴随其的、天然地缔合的组分缔合,(2)基本上不含来自相同物种的其他分子,(3)由来自不同物种的细胞表达,或(4)不存在于自然界中。因此,化学合成的或在与其天然起源的细胞不同的细胞系统中表达的分子将是与其天然缔合的组分“分离”的。也可以通过使用本领域熟知的纯化技术分离使分子基本上不含天然缔合的组分。分子纯度或均一性可以通过本领域熟知的许多手段来测定。例如,多肽样品的纯度可以使用本领域熟知的技术使用聚丙烯酰胺凝胶电泳和对凝胶染色以使多肽可视化来测定。为了某些目的,可以通过使用hplc或本领域熟知的用于纯化的其他手段来提供更高的分辨率。
[0137]
当样品的至少约60%至75%表现为单一种类的多肽时,蛋白或多肽是“基本上纯的”、“基本上均一的”或“基本上纯化的”。多肽或蛋白可以是单体的或多聚体的。基本上纯的多肽或蛋白将通常包含约50%、60%、70%、80%或90%w/w的蛋白样品,更通常约95%并且优选地将超过99%纯。蛋白纯度或均一性可以通过本领域熟知的许多手段来指示,所述
手段诸如蛋白样品的聚丙烯酰胺凝胶电泳,随后用本领域熟知的染色剂对凝胶进行染色后使单个多肽条带可视化。为了某些目的,可以通过使用hplc或本领域熟知的用于纯化的其他手段来提供更高的分辨率。
[0138]
如本文使用的术语“标记”或“标记的”是指在抗体中掺入另一种分子。在一种实施方案中,标记物是可检测的标志物,例如掺入放射性标记的氨基酸或附接至可以通过标记的亲和素检测的生物素基部分的多肽(例如,包含荧光标志物的链霉亲和素或可以通过光学方法或量热法检测的酶活性)。在另一种实施方案中,标记物或标志物可以是治疗性的,例如药物缀合物或毒素。标记多肽和糖蛋白的各种方法是本领域中已知的并且可以被使用。用于多肽的标记物的实例包括但不限于以下:放射性同位素或放射性核素(例如3h、
14
c、
15
n、
35
s、
90
y、
99
tc、
111
in、
125
i、
131
i);荧光标记物(例如fitc、罗丹明、镧系元素荧光团);酶标记物(例如辣根过氧化物酶、β-半乳糖苷酶、萤光素酶、碱性磷酸酶);化学发光标志物;生物素基基团;由第二报告物识别的预定的多肽表位(例如亮氨酸拉链配对序列、第二抗体的结合位点、金属结合结构域、表位标签);磁性剂(magnetic agent),诸如钆螯合物;毒素诸如百日咳毒素、紫杉醇、细胞松弛素b、短杆菌肽d、溴化乙锭、吐根碱、丝裂霉素、依托泊苷、替尼泊苷、长春新碱、长春花碱、秋水仙碱、多柔比星、柔红霉素、二羟基蒽二酮(dihydroxy anthracin dione)、米托蒽醌、光神霉素、放线菌素d、1-去氢睾酮、糖皮质激素、普鲁卡因、丁卡因、利多卡因、普萘洛尔(propranolol)和嘌呤霉素及其类似物或同系物。在各种实施方案中,标记物通过各种长度的间隔臂(spacer arm)附接,以降低潜在的空间位阻。
[0139]
如本文使用的术语“异源”是指非天然的或在自然界不存在的组合或状态,所述组合或状态例如可以通过用源自另一来源的组分或状态替换现有的天然组分或状态来实现。类似地,在除了其中蛋白天然地表达的生物体之外的生物体中的蛋白表达构成异源表达系统和异源蛋白。
[0140]
应理解,本文描述的本公开内容的方面和实施方案包括“由这些方面和实施方案组成”和/或“主要由这些方面和实施方案组成”。
[0141]
本文中述及“约”值或参数包括(并且描述)针对该值或参数本身的变化。例如,述及“约x”的描述包括对“x”的描述。
[0142]
除非上下文另外明确规定,否则如本文和所附的权利要求中使用的单数形式“一”、“或”和“该”包括复数指代物。应理解,本文描述的本公开内容的方面和变化形式包括“由这些方面和变化形式组成”和/或“主要由这些方面和变化形式组成”。
[0143]
il-2
[0144]
白介素-2(il-2)是一种经典的th1细胞因子,由t细胞通过t细胞抗原受体和共刺激分子cd28活化后产生。il-2的调节通过作用于il-2启动子以产生新的基因转录的信号传导途径和转录因子的活化而发生,但也涉及对il-2mrna的稳定性的调节。il-2结合多链受体,包括通过jak-stat途径介导信号传导的高度调节的α链及β和γ链。il-2向t细胞、b细胞和nk细胞递送活化、生长和分化信号。il-2在介导活化诱导的t细胞的细胞死亡中也很重要,这一功能为终止免疫应答提供了关键机制。一种商业上可获得的未糖基化的人类重组il-2产品阿地白介素(可从prometheus laboratories inc.,san diego calif.以商标为的des-丙氨酰基-1,丝氨酸-125人类白介素-2获得),已被批准用于向罹患转移性肾细胞癌和转移性黑素瘤的患者施用。il-2还被建议用于在罹患或感染丙型肝炎
病毒(hcv)、人类免疫缺陷病毒(hiv)、急性髓性白血病、非霍奇金淋巴瘤、皮肤t细胞淋巴瘤、幼年类风湿性关节炎、特应性皮炎、乳腺癌和膀胱癌的患者中施用。不幸的是,短半衰期和严重毒性限制了il-2的最佳给药。
[0145]
如本文使用的,术语“天然il-2”和“天然白介素-2”在蛋白或多肽的上下文中是指任何天然存在的哺乳动物白介素-2氨基酸序列,包括未成熟形式或前体形式和成熟形式。各个物种的天然哺乳动物白介素-2的氨基酸序列的genbank登录号的非限制性实例包括np_032392.1(小家鼠(mus musculus),未成熟形式)、np_001040595.1(猕猴(macaca mulatta),未成熟形式)、np_000577.2(人类,前体形式)、caa01199.1(人类,未成熟形式)、aad48509.1(人类,未成熟形式)和aab20900.1(人类)。在本发明的各种实施方案中,天然il-2是天然存在的哺乳动物il-2的未成熟或前体形式。在其他实施方案中,天然il-2是天然存在的哺乳动物il-2的成熟形式。在各种实施方案中,天然il-2是天然存在的人类il-2的前体形式。在各种实施方案中,天然il-2是天然存在的人类il-2的成熟形式。在各种实施方案中,基于il-2的结构域d2源自seq id no:1中列出的人类il-2前体序列的氨基酸序列:
[0146]
myrmqllscialslalvtnsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfcqsiistlt(seq id no:1)。
[0147]
在各种实施方案中,基于il-2的结构域d2包含seq id no:3中列出的在位置125处包含半胱氨酸至丝氨酸的取代的人类il-2成熟形式野生型序列的氨基酸序列,但是与天然存在的il-2相比,不改变il-2受体结合:
[0148]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfsqsiistlt(seq id no:3)。
[0149]
il-2变体
[0150]
本发明涉及除了一个至若干个被突变的氨基酸以外,与人类il-2共有一级序列的多肽。一组il-2变体包含大幅降低这些多肽刺激treg细胞的能力并使它们在肿瘤的治疗中更有效的突变。还包括这些突变变体单独使用或与疫苗、或taa靶向生物制品、或免疫检查点阻断剂组合使用、或用作双功能分子构建体中的构建模块,用于治疗其中不期望调节性t细胞(treg)活性的疾病诸如癌症或感染的治疗用途。在另一方面,本发明涉及包含所公开的多肽的药物组合物。最后,本发明涉及所公开的多肽和药物组合物的治疗用途,这是由于它们对免疫系统对疾病如自身免疫性紊乱和炎性紊乱或癌症和各种感染性疾病的选择性调节作用。
[0151]
本发明涉及长度为100个至500个氨基酸的多肽,优选大小为140个残基,其表观分子量为至少15kd。这些多肽与天然il-2保持多于90%的高序列同一性。在它们的序列的一个区域中,这些多肽被突变,引入与天然il-2中相同位置的氨基酸残基不同的氨基酸残基。
[0152]
本发明的多肽可被称为免疫调节多肽、il-2类似物或il-2变体以及其他名称。这些多肽是基于il-2受体复合物的3d结构(可在pdb公共数据库中获得)设计的,主要在与il-2受体亚基α相互作用的氨基酸对应的il-2位置引入突变。
[0153]
在各种实施方案中,il-2变体(或突变体)包含源自如seq id no:3中列出的成熟的人类il-2多肽序列的序列。在各种实施方案中,il-2变体包含与天然(或野生型)il-2蛋
白不同的氨基酸序列。在各种实施方案中,il-2变体与il-2受体多肽相互作用,并且起il-2激动剂或拮抗剂的作用。在各种实施方案中,具有激动剂活性的il-2变体具有超级激动剂活性。在各种实施方案中,il-2变体可以起il-2激动剂或拮抗剂的作用,与其与il-2rα的缔合无关。il-2激动剂通过与野生型il-2相比生物活性相当或增加来例示。il-2拮抗剂通过与野生型il-2相比生物活性降低或通过抑制il-2介导的响应的能力来例示。在各种实施方案中,与天然il-2序列相比,il-2变体的序列具有至少一个氨基酸变化,例如取代或缺失,这样的变化导致il-2激动剂或拮抗剂活性。在各种实施方案中,il-2变体具有seq id no:31-66中列出的氨基酸序列,其具有降低/消除的与il-2rα的结合,以选择性地活化效应t细胞(teff)并使之增殖。在各种实施方案中,il-2变体具有seq id no:111-120中列出的氨基酸序列,其除了包含导致降低/消除的与il-2rα结合的突变之外,还包含调节il-2rβ或γc的突变,以选择性地活化具有减弱的效力的效应t细胞并使之增殖,从而降低il-2rβ或γc相关的毒性,减弱细胞衰竭并改进持久的药效学。在各种实施方案中,il-2变体具有以下中的氨基酸序列:seq id no:189(氨基酸462-586)、seq id no:190(氨基酸462-585)和seq id no:191(氨基酸462-584),其除了包含导致降低/消除的与il-2rα结合的突变之外,还包含n末端缺失,以选择性地活化具有减弱的效力的效应t细胞并使之增殖。在各种实施方案中,具有seq id no:31-66、111-120中列出的氨基酸序列和seq id no:47的氨基酸9-133、10-133和11-133的il-2变体还包含s125i氨基酸取代,以改进il-2和相应融合蛋白的可开发性谱。
[0154]
在表2中提供了在与il-2rα的界面处具有引入的氨基酸取代的示例性il-2变体。
[0155]
表2
[0156]
包含对与受体亚基α相互作用的氨基酸的突变的il-2变体或融合构建体。所有变体都包含改进可开发性的取代(s125i)。
[0157]
[0158][0159]
本发明的主要方面是相对于野生型il-2改进il-2对表达il-2rβγ(而不是il-2rα)的细胞超过表达il-2rαβγ的细胞的选择性,以用于癌症治疗。本发明人使用的一种方法是通过将破坏cd25的突变引入细胞因子组分中来产生高选择性的il-2-fc融合蛋白。破坏cd25的突变的选择是基于对il-2/il-2r共晶体结构(pdb代码2b51)的检查。在与il-2受体α亚基的界面处对一个或两个相关残基引入了多于一个氨基酸取代(包括r38、t41、f42、f44、e62、p65、e68和y107),旨在降低或消除与il-2rα的结合。这些构建体还含有s125i突变,用于显著改进可开发性。另外,il-2变体与il-2rα 肺内皮细胞结合的削弱预期防止内皮细胞损伤并显著降低vls。此外,cd25结合的削弱也预期降低cd25抗原吸收,并富集对表达il-2rβγ的细胞的细胞因子占据,并且因此增强体内响应和肿瘤杀伤功效。
[0160]
由于所有被靶向的il-2残基(r38、t41、f42、f44、e62、p65、e68和y107)都在与il-2rα的界面处,并与多于一个il-2rα残基形成氢键/盐桥或疏水相互作用(mathias rickert
等人,(2005)science 308,1477-80),因此推断表中列出的il-2变体和相似物预期破坏与il-2rα的相互作用,并产生具有降低或消除的与il-2rα结合的il-2变体。然而,发现不同位点处的突变和同一位点处的不同取代可以导致影响il-2rα结合的巨大差异,这是根据基于结构的诱变方法无法预测的,并且有些是特别意想不到的(参见实施例4和实施例5)。
[0161]
此外,据推断,为了最佳活性,可以进一步引入调节il-2rβγ的取代以减弱整体效力。il-2rβγ调节效力的激动剂可以防止细胞毒性淋巴细胞的过度活化,并使“命中靶”但“未命中组织”毒性最小化。另外,过度刺激诱导的细胞衰竭和凋亡可以被最小化。此外,细胞因子信号传导分子结合亲和力的减弱可以降低受体介导的内化,减少不需要的靶吸收,并导致持续的受体活化和持久的药效学和药代动力学;因此,调节il-2rβγ的取代可以潜在地降低毒性,并改进药代动力学和药效学以及治疗指数。
[0162]
在表3中提供了具有氨基酸取代(包含对具有降低/消除的与il-2rα结合的il-2变体的破坏il-2rβ或γc的突变)的示例性il-2变体:
[0163]
表3
[0164]
将破坏il-2rβ或γc的取代引入具有降低/消除的与il-2rα结合的il-2变体。所有变体都包含改进可开发性的取代(s125i)。
[0165][0166][0167]
本发明还包括对上文提及的il-2变体类别并且特别是表2和表3中描述的那些的另外修饰,包括对上文提及的il-2变体的8个、9个或10个n末端残基的缺失,以便以各种水平的减弱的效力选择性地活化效应t细胞并使之增殖。任何另外的组合突变都符合本发明的精神和范围,无论是改变它们对il-2受体的特定组分的亲和力,还是改进它们的体内药效学:增加半衰期或降低它们被t细胞内化。这些另外的突变可以通过用生物信息学工具合理设计获得,或者通过使用不同性质的组合分子文库(噬菌体文库、酵母或细菌中的基因表达文库)获得。在另一方面,本发明涉及一种融合蛋白,该融合蛋白包含与载体蛋白偶联的上文描述的任何免疫调节性多肽。载体蛋白可以是白蛋白或人类免疫球蛋白的fc区。
[0168]
在各种实施方案中,使用各种长度和组成的接头将具有seq id no:170中列出的氨基酸序列的il-2rαsushi连接在il-2和fc结构域之间。fc结构域可以在n末端或c末端。具有seq id no:171-172中列出的氨基酸序列的il-2-il-2rαsushi-fc融合蛋白预期具有降低的与il-2rα的结合,以选择性地活化效应t细胞并使之增殖。
[0169]
在各种实施方案中,il-2和il-2rαsushi形成非共价复合。il-2被融合到hole-fc
链(seq id no:10)的n末端或c末端,并且il-2rαsushi被融合到knob-fc链(seq id no:9)的n末端或c末端。非共价c末端il-2-il-2rαsushi-fc融合蛋白具有seq id no:173-174中列出的氨基酸序列。
[0170]
表4
[0171]
il-2和il-2rαsushi共价连接或非共价复合为fc融合蛋白
[0172][0173][0174]
fc结构域
[0175]
igg类的免疫球蛋白是人类血液中最丰富的蛋白之一。它们的循环半衰期可长达21天。已经报道了将igg的fc区与另一种蛋白(诸如各种细胞因子和受体)的结构域组合的融合蛋白(参见例如,capon等人,nature,337:525-531,1989;chamow等人,trends biotechnol.,14:52-60,1996);美国专利第5,116,964号和第5,541,087号)。原型融合蛋白是通过igg fc的铰链区中的半胱氨酸残基连接的同源二聚体蛋白,产生类似于igg分子、没有重链可变区和ch1结构域以及轻链的分子。包含fc结构域的融合蛋白的二聚体性质在提供与其他分子的更高级相互作用(即二价或双特异性结合)方面可能是有利的。由于结构同源性,fc融合蛋白表现出与具有相似同种型的人类igg相当的体内药代动力学谱。
[0176]
术语“fc”是指包含完整抗体的非抗原结合片段的序列的分子或序列,无论是单体形式还是多聚体形式。天然fc的原始免疫球蛋白来源优选地为人类来源,并且可以是任何免疫球蛋白,尽管igg1和igg2是优选的。天然fc由单体多肽组成,单体多肽可以通过共价(即二硫键)和非共价缔合连接成二聚体或多聚体形式。天然fc分子的单体亚基之间的分子间二硫键的数目取决于类别(例如igg、iga、ige)或亚类(例如igg1、igg2、igg3、iga1、igga2)而在从1至4的范围内。天然fc的一种实例是由木瓜蛋白酶消化igg产生的二硫键合的二聚体(参见ellison等人(1982),nucleic acids res.10:4071-9)。如本文使用的术语“天然fc”是单体、二聚体和多聚体形式的总称。fc结构域包含蛋白a、蛋白g、各种fc受体和补体蛋白的结合位点。
[0177]
在各种实施方案中,术语“fc变体”是指从天然fc修饰、但仍然包含补救受体fcrn的结合位点的分子或序列。国际申请wo 97/34631(1997年9月25日公布)和wo 96/32478描述了示例性的fc变体以及与补救受体的相互作用,并特此通过引用并入。此外,天然fc包含可被去除的位点,因为它们提供本发明的融合分子不需要的结构特征或生物活性。因此,在各种实施方案中,术语“fc变体”包括缺乏一个或更多个天然fc位点或残基的分子或序列,所述天然fc位点或残基影响或参与(1)二硫键形成,(2)与所选宿主细胞的不相容性,(3)在所选宿主细胞中表达时的n末端异质性,(4)糖基化,(5)与补体的相互作用,(6)与补救受体以外的fc受体的结合,或(7)抗体依赖性细胞毒性(adcc)。
[0178]
术语“fc结构域”包括如上文定义的天然fc和fc变体分子和序列。如同fc变体和天
然fc,术语“fc结构域”包括单体或多聚体形式的分子,无论是从完整抗体消化的还是通过重组基因表达或通过其他方式产生的。在各种实施方案中,“fc结构域”是指两个fc结构域单体(seq id no:6)的二聚体,其通常包括全部或部分的铰链区。在各种实施方案中,fc结构域可以被突变以缺乏效应子功能。在各种实施方案中,fc结构域中的每个fc结构域单体包含ch2抗体恒定结构域中的氨基酸取代,以降低fc结构域和fcγ受体之间的相互作用或结合。在各种实施方案中,fc结构域的每个亚基包含三个氨基酸取代,这三个氨基酸取代降低与活化性fc受体的结合和/或效应子功能,其中所述氨基酸取代是l234a、l235a和g237a(seq id no:7)。
[0179]
在各种实施方案中,fc结构域中的两个fc结构域单体中的每一个包含促进两个单体异源二聚体化的氨基酸取代。在各种其他实施方案中,fc结构域单体的异源二聚体化可以通过在两个fc结构域单体中引入不同但相容的取代诸如“knob-into-hole”残基对来促进。“knob-into-hole”技术也公开于美国专利公布第8,216,805号中。在又另一种实施方案中,一个fc结构域单体包含knob突变t366w,并且另一个fc结构域单体包含hole突变t366s、l358a和y407v。在各种实施方案中,引入形成稳定化的二硫桥的两个cys残基(s354c在“knob”侧,并且y349c在“hole”侧)(seq id no:9和10)。异源二聚体fc的使用可以产生单价il-2变体。
[0180]
在各种实施方案中,用于制备二聚体il-2变体fc融合体的fc结构域序列是seq id no:7中列出的人类igg1-fc结构域序列:
[0181]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seq id no:7)
[0182]
其中seq id no:7含有消除fcγr和c1q结合的氨基酸取代(加下划线)。
[0183]
在各种实施方案中,用于制备二聚体il-2fc融合蛋白的fc结构域序列是seq id no:8中列出的igg1-fc结构域序列:
[0184]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhahytqkslslspg(seq id no:106)
[0185]
其中seq id no:8含有消除fcγr和c1q结合的氨基酸取代(加下划线)和延长半衰期的氨基酸取代(粗体)。
[0186]
在各种实施方案中,用于制备单体il-2变体fc融合体的异源二聚体fc结构域序列是seq id no:9中列出的knob-fc结构域序列:
[0187]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seq id no:9)
[0188]
其中seq id no:9含有消除fcγr和c1q结合的氨基酸取代(加下划线)。
[0189]
在各种实施方案中,用于制备il-2变体的异源二聚体fc结构域序列是seq id no:
10中列出的hole-fc结构域序列:
[0190]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppcreemtknqvslscavkgfypsdiavewesngqpennykttppvldsdgsfflvskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seq id no:10)
[0191]
其中seq id no:10含有消除fcγr和c1q结合的氨基酸取代(加下划线)。
[0192]
在各种实施方案中,用于制备单体il-2变体fc融合蛋白的异源二聚体fc结构域是具有降低/消除的效应子功能和延长的半衰期的knob-fc结构域并有seq id no:134中列出的氨基酸序列:
[0193]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhahytqkslslspg(seq id no:134)
[0194]
其中seq id no:134含有消除fcγr和c1q结合的氨基酸取代(加下划线)和延长半衰期的氨基酸取代(粗体)。
[0195]
在各种实施方案中,用于制备单体il-2变体fc融合蛋白的异源二聚体fc结构域是具有降低/消除的效应子功能和延长的半衰期的hole-fc结构域并有seq id no:135中列出的氨基酸序列:
[0196]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppcreemtknqvslscavkgfypsdiavewesngqpennykttppvldsdgsfflvskltvdksrwqqgnvfscsvmhealhahytqkslslspg(seq id no:135)
[0197]
其中seq id no:135含有消除fcγr和c1q结合的氨基酸取代(加下划线)和延长半衰期的氨基酸取代(粗体)。
[0198]
作为靶向部分的抗体
[0199]
在各种实施方案中,本发明的il-2变体构建体包含结合癌症组织中富含的分子(诸如肿瘤相关抗原(taa))的抗体、抗体片段、蛋白或肽形式的靶向部分。
[0200]
taa可以是针对其需要免疫应答的任何分子、大分子、分子组合等。taa可以是包含多于一个多肽亚基的蛋白。taa可以是包含多于一个多肽亚基的蛋白。例如,蛋白可以为二聚体、三聚体或更高级多聚体。在各种实施方案中,蛋白的两个或更多个亚基可以以共价键诸如例如二硫键连接。在各种实施方案中,蛋白的亚基可以以非共价相互作用保持在一起。因此,taa可以是技术人员希望针对其诱导免疫应答的任何肽、多肽、蛋白、核酸、脂质、碳水化合物或有机小分子或其任何组合。在各种实施方案中,taa为包含以下的肽:约5个、约6个、约7个、约8个、约9个、约10个、约11个、约12个、约13个、约14个、约15个、约16个、约17个、约18个、约19个、约20个、约25个、约30个、约35个、约40个、约45个、约50个、约55个、约60个、约65个、约70个、约75个、约80个、约85个、约90个、约95个、约100个、约150个、约200个、约250个、约300个、约400个、约500个、约600个、约700个、约800个、约900或约1000个氨基酸。在各种实施方案中,肽、多肽或蛋白是通常通过注射向受试者施用的分子。在各种实施方案中,在施用后,肿瘤特异性抗体或结合蛋白用作靶向部分,以将il-2变体引导至病变部位,
诸如癌症部位,在该部位,活性结构域可以被释放并与其在病变细胞上的同源受体相互作用。
[0201]
任何前述标志物都可以用作用于本发明il-2变体的taa靶。在各种实施方案中,设想用于本公开内容的il-2变体构建体和方法的一种或更多种taa、taa变体或taa突变体选自或源自表5中提供的列表。
[0202]
表5
[0203]
[0204]
[0205][0206]
在各种实施方案中,本发明的il-2变体可以附接至靶向/双功能部分,该靶向/双功能部分为靶向免疫检查点调节剂的抗体、抗体片段、蛋白或肽。
[0207]
已经报道了在各种免疫细胞上表达的许多免疫检查点蛋白抗原,包括例如,sirp(在巨噬细胞、单核细胞、树突细胞上表达)、cd47(在肿瘤细胞和其他细胞类型上高表达),vista(在单核细胞、树突细胞、b细胞、t细胞上表达)、cd152(由活化的cd8 t细胞、cd4 t细胞和调节性t细胞表达)、cd279(在肿瘤浸润性淋巴细胞上表达,由活化的t细胞(cd4和cd8两者)、调节性t细胞、活化的b细胞、活化的nk细胞、无变应性t细胞、单核细胞、树突细胞表达)、cd274(在t细胞、b细胞、树突细胞、巨噬细胞、血管内皮细胞、胰岛细胞上表达)和cd223(由活化的t细胞、调节性t细胞、无变应性t细胞、nk细胞、nkt细胞和浆细胞样树突细胞表达)(参见,例如,pardoll,d.,nature reviews cancer,12:252-264,2012)。结合被确定为免疫检查点蛋白的抗原的抗体是本领域技术人员已知的。例如,本领域已经描述了各种抗cd276抗体(参见,例如,美国专利公布第20120294796号(johnson等人)及其中引用的参考文献);本领域已经描述了各种抗cd272抗体(参见,例如,美国专利公布第20140017255号(mataraza等人)及其中引用的参考文献);本领域已经描述了各种抗cd152/ctla-4抗体(参见,例如,美国专利公布第20130136749号(korman等人)及其中引用的参考文献);本领域已经描述了各种抗lag-3/cd223抗体(参见,例如,美国专利公布第20110150892号(thudium等人)及其中引用的参考文献);本领域已经描述了各种抗cd279(pd-1)抗体(参见例如,美国专利第7,488,802号(collins等人)及其中引用的参考文献);本领域已经描述了各种抗cd274(pd-l1)抗体(参见例如,美国专利公布第20130122014号(korman等人)及其中引用的参考文献);本领域已经描述了各种抗tim-3抗体(参见,例如,美国专利公布第20140044728号(takayanagi等人)及其中引用的参考文献);并且本领域已经描述了各种抗b7-h4抗体(参见,例如,美国专利公布第20110085970号(terrett等人)及其中引用的参考文献)。这些参考文献中的每一篇关于其中教导的特定抗体和序列通过引用以其整体特此并入。
[0208]
在各种实施方案中,il-2融合配偶体可以是表现出与存在于免疫细胞表面的免疫检查点蛋白抗原结合的抗体、抗体片段、或蛋白或肽。在各种实施方案中,免疫检查点蛋白抗原选自由以下组成的组但不限于pd1(cd279)、pdl-1(cd274)、cd276、cd272、cd152(ctla-4)、cd223、cd279、cd274、cd40、sirpα、cd47、ox-40、gitr、icos、cd27、4-1bb、tim-3、b7-h3、b7-h4、tigit和vista。
[0209]
在各种实施方案中,抗体是拮抗性fap抗体或抗体片段。在各种实施方案中,抗体是包含seq id no:136和137中列出的可变结构域序列的人源化拮抗性fap抗体。在各种实施方案中,异源蛋白是针对免疫检查点调节剂的抗体或抗体片段。在各种实施方案中,抗体是拮抗性人类tigit抗体。在各种实施方案中,抗体是拮抗性pd-1抗体或抗体片段。在各种实施方案中,抗体是包含以下中列出的可变结构域序列的拮抗性pd-1抗体:seq id no:138和139,seq id no:140和141,seq id no:142和143,seq id no:144和145,或seq id no:146和147。在各种实施方案中,抗体是包含seq id no:148和149中列出的可变结构域序列的拮抗性人类pd-l1抗体。在各种实施方案中,抗体是包含seq id no:150和151中列出的可变结构域序列的拮抗性人类ctla-4抗体。在各种实施方案中,示例性双功能il-2pd1抗体融合蛋白在表12中列出。
[0210]
双功能il-2变体pd-1抗体融合蛋白
[0211]
在各种实施方案中,绕开肿瘤微环境中的免疫抑制效应的免疫检查点阻断性抗体或增强现有应答的免疫刺激性抗体被用于构建il-2抗体融合蛋白。在浸润于肿瘤微环境中的经历肿瘤抗原的衰竭的t细胞上,负免疫检查点的表达水平特别地增加。在各种实施方案中,将il-2变体拴系到靶向免疫检查点的抗体,预期将il-2导向衰竭的t细胞,并使肿瘤微环境在免疫学上变热(immunologically hot)。在各种实施方案中,双功能il-2变体检查点抑制剂抗体融合蛋白可以优先将il-2以顺式递送至表达检查点抑制剂的细胞,诸如浸润于肿瘤微环境中的经历肿瘤抗原的衰竭的t细胞,以促进选择性信号传导并增强期望的肿瘤部位处的活性。在各种实施方案中,双功能il-2变体检查点抑制剂抗体融合蛋白通过去除负调节和重振t细胞功能以及扩增teff细胞数量提供协同作用,以进一步增强免疫系统的抗肿瘤活性。
[0212]
在各种实施方案中,双功能il-2变体检查点抑制剂抗体融合蛋白降低il-2的全身性暴露和脱靶毒性。在各种实施方案中,使用具有降低/消除的与il-2rα的结合和减弱/调节的il-2rβγ活性两者的il-2变体有助于在细胞因子il-2活性和抗体活性之间建立化学计量平衡。减弱的il-2活性变体和在衰竭的teff细胞处具有足够抗体靶向或顺式活化将允许最佳给药并维持每个臂的功能。此外,与抗体融合的减弱的il-2活性变体预期经由针对肿瘤和/或免疫细胞位点的抗体靶向部分使外周活化最小化、降低t细胞aicd、减轻抗原吸收并促进肿瘤杀伤。
[0213]
在各种实施方案中,本发明的il-2变体可以附接至检查点抑制剂,所述检查点抑制剂是靶向免疫检查点调节剂的抗体、抗体片段、蛋白或肽。在各种实施方案中,免疫检查点抑制剂是拮抗剂pd-1抗体。在各种实施方案中,pd-1抗体包含以下中列出的可变结构域序列:seq id no:138和139,seq id no:140和141,seq id no:142和143,seq id no:144和145,或seq id no:146和147。在各种实施方案中,示例性双功能il-2pd1抗体融合蛋白在表12中列出。
[0214]
接头
[0215]
在各种实施方案中,异源蛋白通过接头和/或铰链接头肽附接至il-2变体。接头或铰链接头可以是相对地不含二级结构或展示出α螺旋构象的在5个、10个、15个、20个、30个、40个或更多个氨基酸之间的人工序列。
[0216]
肽接头在蛋白结构域之间提供共价连接和另外的结构和/或空间柔性。如本领域
已知的,肽接头含有柔性氨基酸残基,诸如甘氨酸和丝氨酸。在各种实施方案中,肽接头可以包含1-100个氨基酸。在各种实施方案中,间隔物可以包含基序gggsgggs(seq id no:18)。在其他实施方案中,接头可以包含基序ggggs(seq id no:21)n,其中n是1至10的整数。在其他实施方案中,接头还可以包含除甘氨酸和丝氨酸之外的氨基酸。在另一种实施方案中,接头可以包含其他蛋白基序,包括但不限于α-螺旋构象的序列,诸如aeaaakeaaakeaaaka(seq id no:16)。在各种实施方案中,可以调节接头长度和组成以优化活性或可开发性,包括但不限于表达水平和聚集倾向。在另一种实施方案中,肽接头可以是简单的化学键,例如酰胺键(例如通过peg的化学缀合)。
[0217]
在表6中提供了示例性的肽接头:
[0218]
表6
[0219]
接头序列seq id no:gggsgggsgggs11gggs12gssggsggsggsg13gssgt14ggggsggggsgggs15aeaaakeaaakeaaaka16ggggsggggsggggsggggs17gggsgggs18gsgst19ggss20ggggs21ggsg22sggg23gsgs24gsgsgs25gsgsgsgs26gsgsgsgsgs27gsgsgsgsgsgs28ggggsggggs29ggggsggggsggggs30
[0220]
多核苷酸
[0221]
在另一方面,本公开内容提供了分离的核酸分子,该分离的核酸分子包含编码本公开内容的il-2、il-2变体、il-2融合蛋白或il-2变体融合蛋白的多核苷酸。主题核酸可以是单链的或双链的。这样的核酸可以是dna或rna分子。dna包括例如cdna、基因组dna、合成的dna、通过pcr扩增的dna及其组合。编码il-2多肽的基因组dna获取自基因组文库,该基因组文库对许多物种是可得的。合成的dna从化学合成重叠的寡核苷酸片段然后组装片段以重构编码区和侧翼序列的部分或全部而可获得。可以从指导mrna的高水平合成的原核表达载体,诸如使用t7启动子和rna聚合酶的载体获得rna。cdna获取自从分离自表达il-2的各
种组织的mrna制备的文库。本公开内容的dna分子包括全长基因以及多核苷酸及其片段。全长基因还可以包含编码n末端信号序列的序列。此类核酸可以例如在用于制备新型il-2变体的方法中使用。
[0222]
在各种实施方案中,分离的核酸分子包含本文描述的多核苷酸,并且还包含编码本文描述的至少一种异源蛋白的多核苷酸。在各种实施方案中,核酸分子还包含编码本文描述的接头或铰链接头的多核苷酸。
[0223]
在各种实施方案中,本公开内容的重组核酸可以可操作地连接至表达构建体中的一种或更多种调控核苷酸序列。调控序列是本领域所认知的并且被选择以指导il-2变体的表达。相应地,术语调控序列包括启动子、增强子和其他表达控制元件。在goeddel;gene expression technology:methods in enzymology,academic press,san diego,calif.(1990)中描述了示例性的调控序列。通常,所述一种或更多种调控核苷酸序列可以包括但不限于启动子序列、前导或信号序列、核糖体结合位点、转录起始和终止序列、翻译起始和终止序列、以及增强子或激活序列。本公开内容设想了本领域已知的组成型或诱导型启动子。启动子可以是天然存在的启动子或者组合多于一个启动子的元件的杂合启动子。表达构建体可以存在于细胞中的附加体诸如质粒上,或者表达构建体可以插入染色体中。在各种实施方案中,表达载体包含选择性标志物基因以允许选择转化的宿主细胞。选择性标志物基因是本领域熟知的并且将随着使用的宿主细胞变化。
[0224]
在本公开内容的另一方面,主题核酸在表达载体中提供,所述表达载体包含编码il-2变体并可操作地连接到至少一个调控序列的核苷酸序列。术语“表达载体”是指用于从多核苷酸序列表达多肽的质粒、噬菌体、病毒或载体。适于在宿主细胞中表达的载体是容易地可得的并利用标准重组dna技术将核酸分子插入到载体中。此类载体可以包括各种各样的表达控制序列,当被可操作地连接至dna序列时,所述表达控制序列控制该dna序列的表达,并可以在这些载体中使用以表达编码il-2变体的dna序列。此类有用的表达控制序列包括,例如,sv40的早期启动子和晚期启动子、tet启动子、腺病毒或巨细胞病毒介导的早期启动子、rsv启动子、lac系统、trp系统、tac或trc系统、其表达由t7 rna聚合酶指导的t7启动子、λ噬菌体的主要操纵子和启动子区域、fd外壳蛋白的控制区域、3-磷酸甘油酸激酶或其他糖酵解酶的启动子、酸性磷酸酶例如phos的启动子、酵母a-交配因子的启动子、杆状病毒系统的多角体启动子和已知控制原核细胞或真核细胞或它们的病毒的基因表达的其他序列及其各种组合。应理解,表达载体的设计可能取决于诸如待转化的宿主细胞的选择和/或期望表达的蛋白的类型的因素。此外,还应考虑载体的拷贝数、控制该拷贝数的能力、以及载体编码的任何其他蛋白诸如抗生素标志物的表达。适用于表达il-2的示例性表达载体是包含il-2多核苷酸的pdsra(描述于wo 90/14363,通过引用并入本文)及其衍生物,以及本领域已知的或下文描述的任何另外的合适的载体。
[0225]
本公开内容的重组核酸可以通过将克隆的基因或其一部分连接到适于在原核细胞、真核细胞(酵母、鸟类、昆虫或哺乳动物)或两者中表达的载体中来产生。用于产生重组il-2多肽的表达载体包括质粒和其他载体。例如,合适的载体包括以下类型的质粒:用于在原核细胞诸如大肠杆菌中表达的pbr322衍生的质粒、pembl衍生的质粒、pex衍生的质粒、pbtac衍生的质粒和puc衍生的质粒。
[0226]
一些哺乳动物表达载体包含利于载体在细菌中增殖的原核序列以及在真核细胞
中表达的一种或更多种真核转录单元两者。pcdnai/amp、pcdnai/neo、prc/cmv、psv2gpt、psv2neo、psv2-dhfr、ptk2、prsvneo、pmsg、psvt7、pko-neo和phyg衍生的载体为适于转染真核细胞的哺乳动物表达载体的实例。这些载体中的一些被来自细菌质粒诸如pbr322的序列修饰,以利于在原核细胞和真核细胞两者中复制和药物抗性选择。可选地,病毒诸如牛乳头瘤病毒的衍生物(bpv-1)或epstein-barr病毒的衍生物(phebo、prep衍生的和p205)可以用于蛋白在真核细胞中的瞬时表达。其他病毒(包括逆转录病毒)表达系统的实例可见于下文基因疗法递送系统的描述中。在质粒的制备方面和宿主生物体的转化方面所采用的各种方法是本领域熟知的。对于适于原核细胞和真核细胞两者的其他表达系统以及一般的重组程序,参见sambrook、fritsch和maniatis的molecular cloning a laboratory manual,第2版(cold spring harbor laboratory press,1989)第16和17章。在一些情形下,可能期望通过使用杆状病毒表达系统来表达重组多肽。此类杆状病毒表达系统的实例包括pvl衍生的载体(诸如pvl1392、pvl1393和pvl941)、pacuw衍生的载体(诸如pacuw1)以及pbluebac衍生的载体(诸如含有b-gal的pbluebac iii)。
[0227]
在各种实施方案中,载体将被设计成用于在cho细胞中产生主题il-2变体,诸如pcmv-script载体(stratagene,la jolla,calif.)、pcdna4载体(invitrogen,carlsbad,calif.)和pci-neo载体(promega,madison,wis.)。将明显的是,主题基因构建体可以被用于引起主题il-2变体在增殖于培养基中的细胞中表达,例如以产生用于纯化的蛋白,包括融合蛋白或变体蛋白。
[0228]
本公开内容还涉及用重组基因转染的宿主细胞,所述重组基因包含编码一种或更多种主题il-2变体的氨基酸序列的核苷酸序列。宿主细胞可以是原核细胞或真核细胞。例如,本公开内容的il-2变体可以在细菌细胞诸如大肠杆菌、昆虫细胞(例如,使用杆状病毒表达系统)、酵母或哺乳动物细胞中表达。其他合适的宿主细胞是本领域技术人员已知的。
[0229]
相应地,本公开内容还涉及产生主题il-2变体的方法。例如,可以在允许发生il-2变体的表达的适当条件下培养用编码il-2变体的表达载体转染的宿主细胞。il-2变体可以从含有il-2变体的细胞分泌和从含有il-2变体的细胞和培养基的混合物分离。可选地,il-2变体可以保留在细胞质中或保留在膜级分中,并收获、裂解细胞和分离蛋白。细胞培养物包括宿主细胞、培养基和其他副产物。用于细胞培养的合适培养基是本领域熟知的。
[0230]
本公开内容的多肽和蛋白可以根据本领域技术人员熟知的蛋白纯化技术来纯化。这些技术在一个层面上涉及蛋白质级分和非蛋白质级分的粗分级。将肽或多肽与其他蛋白分离后,可以利用色谱技术和电泳技术进一步纯化感兴趣的肽或多肽,以实现部分或完全纯化(或纯化至均一)。如本文使用的术语“分离的多肽”或“纯化的多肽”意图指可与其他组分分离的组合物,其中多肽被纯化至相对于其天然可获得状态的任何程度。因此纯化的多肽还指脱离其可能天然存在的环境的多肽。通常,“纯化的”将指已经经历分级以去除各种其他组分的多肽组合物,并且多肽该组合物基本上保留了其表达的生物活性。当使用术语“基本上纯化的”时,该指定将指这样的肽或多肽组合物,其中多肽或肽形成组合物的大部分组分,诸如构成组合物中的蛋白的约50%、约60%、约70%、约80%、约85%或约90%或更多。
[0231]
适用于纯化的各种技术将是本领域技术人员熟知的。这些技术包括,例如,用硫酸铵、peg、抗体(免疫沉淀)等沉淀或通过热变性沉淀,然后离心;色谱,诸如亲和色谱(蛋白a
柱)、离子交换色谱、凝胶过滤色谱、反相色谱、羟基磷灰石色谱、疏水相互作用色谱;等电聚焦;凝胶电泳;以及这些技术的组合。如本领域一般已知的,认为进行各种纯化步骤的顺序可以改变,或者某些步骤可以省略,并且仍得到用于制备基本上纯化的多肽的合适方法。
[0232]
药物组合物
[0233]
在另一方面,本公开内容提供了药物组合物,所述药物组合物包含与药学上可接受的载体混合的il-2变体或il-2变体融合蛋白。此类药学上可接受的载体是本领域普通技术人员所熟知并理解的,并且已被广泛描述(参见例如,remington's pharmaceutical sciences,第18版,a.r.gennaro编著,mack publishing company,1990)。可以包括药学上可接受的载体以用于改变、保持或维持,例如,ph、摩尔渗透压浓度、黏度、澄清度、颜色、等渗性、气味、无菌性、稳定性、溶解或释放速率、组合物的吸收或渗透的目的。这样的药物组合物可以影响多肽的物理状态、稳定性、体内释放速率以及体内清除速率。合适的药学上可接受的载体包括但不限于,氨基酸(诸如甘氨酸、谷氨酰胺、天冬酰胺、精氨酸或赖氨酸);抗菌剂;抗氧化剂(诸如抗坏血酸、亚硫酸钠或亚硫酸氢钠);缓冲剂(诸如硼酸盐、碳酸氢盐、tris-hcl、柠檬酸盐、磷酸盐、其他有机酸);填充剂(bulking agents)(诸如甘露醇或甘氨酸);螯合剂(诸如乙二胺四乙酸(edta));复合剂(complexing agent)(诸如咖啡因、聚乙烯吡咯烷酮、β-环糊精或羟丙基-β-环糊精);填料;单糖;二糖和其他碳水化合物(诸如葡萄糖、甘露糖或糊精);蛋白(诸如血清白蛋白、明胶或免疫球蛋白);着色剂;调味剂和稀释剂;乳化剂;亲水性聚合物(诸如聚乙烯吡咯烷酮);低分子量多肽;盐形成抗衡离子(诸如钠);防腐剂(诸如苯扎氯铵、苯甲酸、水杨酸、硫柳汞、苯乙醇、对羟基苯甲酸甲酯、对羟基苯甲酸丙酯、氯己定、山梨酸或过氧化氢);溶剂(诸如甘油、丙二醇或聚乙二醇);糖醇(诸如甘露醇或山梨醇);悬浮剂;表面活性剂或润湿剂(诸如普朗尼克、peg、山梨醇酐酯(sorbitan esters)、聚山梨醇酯诸如聚山梨醇酯20、聚山梨醇酯80、曲拉通(triton)、氨丁三醇、卵磷脂、胆固醇、tyloxapal);稳定性增强剂(蔗糖或山梨醇);张度增强剂(诸如碱金属卤化物(优选氯化钠或氯化钾)、甘露醇和山梨醇);递送媒介物;稀释剂;赋形剂和/或药物佐剂(pharmaceutical adjuvants)。
[0234]
药物组合物中的主要媒介物或载体实质上可以是水性的或非水性的。例如,合适的媒介物或载体可以是可能补充有用于肠胃外施用的组合物中常见的其他材料的注射用水、生理盐水溶液或人工脑脊液。中性缓冲盐水或与血清白蛋白混合的盐水是另外的示例性媒介物。其他的示例性药物组合物包含约ph 7.0-8.5的tris缓冲液或约ph 4.0-5.5的乙酸盐缓冲液,其还可以包含山梨醇或山梨醇的合适替代物。在本公开内容的一种实施方案中,可以通过将选择的具有期望程度的纯度的组合物与任选的制剂用剂(formulation agent)(remington's pharmaceutical sciences,同上)混合来制备组合物以便以冻干的块状物或水性溶液形式储存。另外,可以使用合适的赋形剂诸如蔗糖将治疗组合物配制为冻干物。最佳的药物组合物将取决于例如意图的施用途径、递送形式和期望的剂量由本领域普通技术人员确定。
[0235]
当设想肠胃外施用时,治疗性药物组合物可以呈在药学上可接受的媒介物中包含期望的il-2多肽或il-2多肽融合蛋白的无致热原、肠胃外可接受的水性溶液的形式。用于肠胃外注射的特别合适的媒介物是无菌蒸馏水,其中多肽被配制为合适储存的无菌、等渗溶液。在各种实施方案中,适于可注射施用的药物制剂可以在水性溶液,优选地在生理上相
容的缓冲液诸如hanks溶液、ringer溶液或生理缓冲盐水中配制。水性注射悬浮液可以包含增加悬浮液黏度的物质,诸如羧甲基纤维素钠、山梨醇或右旋糖酐。此外,活性化合物的悬浮液可以被制备为合适的油性注射悬浮液。任选地,悬浮液还可以包含合适的稳定剂或增加化合物的溶解度并允许制备高度浓缩的溶液的剂。
[0236]
在各种实施方案中,可以使用胶体分散系统将治疗性药物组合物配制为用于靶向递送。胶体分散系统包括大分子复合体、纳米胶囊、微球、珠和基于脂质的系统,基于脂质的系统包括水包油乳液、胶束、混合的胶束和脂质体。在脂质体产生中有用的脂质的实例包括磷脂酰化合物,诸如磷脂酰甘油、磷脂酰胆碱、磷酯酰丝氨酸、磷脂酰乙醇胺、鞘脂、脑苷脂和神经节苷脂。示例性磷脂包括卵磷脂、二棕榈酰磷脂酰胆碱和二硬脂酰磷脂酰胆碱。脂质体的靶向还可以基于例如器官特异性、细胞特异性和细胞器特异性并且是本领域已知的。
[0237]
在各种实施方案中,设想了药物组合物的口服施用。以该形式施用的药物组合物可以使用或不使用固体剂型诸如片剂和胶囊的复合中通常使用的那些载体配制。在用于口服施用的固体剂型(胶囊、片剂、丸剂、糖衣丸、粉末、颗粒等)中,本公开内容的一种或更多种治疗化合物可以与一种或更多种药学上可接受的载体诸如柠檬酸钠或磷酸氢钙(dicalcium phosphate)和/或以下中的任一种混合:(1)填料或增量剂(extender),诸如淀粉、乳糖、蔗糖、葡萄糖、甘露醇和/或硅酸;(2)粘合剂,诸如例如羧甲基纤维素、藻酸盐(alginate)、明胶、聚乙烯吡咯烷酮、蔗糖和/或阿拉伯树胶;(3)保湿剂,诸如甘油;(4)崩解剂,诸如琼脂-琼脂、碳酸钙、马铃薯或木薯淀粉、藻酸、某些硅酸盐和碳酸钠;(5)溶液阻滞剂,诸如石蜡;(6)吸收加速剂,诸如季铵化合物;(7)润湿剂,诸如例如鲸蜡醇和单硬脂酸甘油酯;(8)吸收剂,诸如高岭土和膨润土;(9)润滑剂,诸如滑石、硬脂酸钙、硬脂酸镁、固体聚乙二醇、月桂基硫酸钠及其混合物;以及(10)着色剂。在胶囊、片剂和丸剂的情况下,药物组合物还可以包含缓冲剂。相似类型的固体组合物还可以用作使用诸如乳糖(lactose)或乳糖(milk sugar)以及高分子量聚乙二醇等的赋形剂软填充和硬填充的明胶胶囊中的填料。用于口服施用的液体剂型包括药学上可接受的乳液、微乳液、溶液、悬浮液、糖浆剂和酏剂。除了活性成分之外,液体剂型可以包含本领域中常用的惰性稀释剂,诸如水或其他的溶剂、增溶剂和乳化剂诸如乙醇、异丙醇、碳酸乙酯、乙酸乙酯、苄醇、苯甲酸苄酯、丙二醇、1,3-丁二醇、油(特别地,棉籽油、花生油、玉米油、胚芽油、橄榄油、蓖麻油和芝麻油)、甘油、四氢糠醇、聚乙二醇和脱水山梨醇的脂肪酸酯及其混合物。除惰性稀释剂之外,口服组合物还可以包含辅料(adjuvants),诸如润湿剂、乳化剂和悬浮剂、增甜剂、调味剂、着色剂、增香剂和防腐剂。
[0238]
在各种实施方案中,设想了将药物组合物局部施用(topical administration)至皮肤或施用至黏膜。局部制剂还可以包含已知作为皮肤或角质层渗透增强剂有效的各种各样的剂中的一种或更多种。这些剂的实例是2-吡咯烷酮、n-甲基-2-吡咯烷酮、二甲基乙酰胺、二甲基甲酰胺、丙二醇、甲醇或异丙醇、二甲基亚砜和氮酮。还可以包含另外的剂以使制剂在化妆品上可接受。这些剂的实例是脂肪、蜡、油、染料、芳香剂、防腐剂、稳定剂和表面活性剂。还可以包含角质软化剂(keratolytic agent),诸如本领域已知的那些角质软化剂。实例是水杨酸和硫磺。用于局部或经皮施用的剂型包括粉末、喷雾剂、软膏剂(ointments)、糊剂、霜剂(creams)、洗剂、凝胶、溶液、贴剂和吸入剂。可以在无菌条件下将活性化合物与药学上可接受的载体以及与可能需要的任何防腐剂、缓冲剂或喷射剂混合。除了本公开内
容的主题化合物(例如il-2变体)之外,软膏剂、糊剂、霜剂和凝胶可以包含赋形剂,诸如动物和植物脂肪、油、蜡、石蜡、淀粉、黄芪胶、纤维素衍生物、聚乙二醇、硅酮、膨润土、硅酸、滑石和氧化锌或其混合物。
[0239]
本文中设想的用于使用的另外的药物组合物包括在持续递送或控制递送的制剂中包含多肽的制剂。在各种实施方案中,药物组合物可以被配制于纳米颗粒中、配制为缓释水凝胶或掺入溶瘤病毒中。这样的纳米颗粒方法包括,例如,包封在包含作为药物载体的具有疏水主链和亲水支链的聚合物的纳米颗粒中,包封在微米颗粒中,以乳剂插入到脂质体中,以及与其他分子缀合。纳米颗粒的实例包括用壳聚糖和卡波姆包衣的粘膜粘附性纳米颗粒(takeuchi等人,adv.drug deliv.rev.47(1):39-54,2001)以及包含带电荷的组合聚酯、聚(2-磺丁基-乙烯醇)和聚(d,l-乳酸-共-羟基乙酸)的纳米颗粒(jung等人,eur.j.pharm.biopharm.50(1):147-160,2000)。基于白蛋白的纳米颗粒组合物已被开发为用于递送疏水性药物诸如紫杉烷的药物递送系统。参见,例如,美国专利第5,916,596号、第6,506,405号、第6,749,868号、第6,537,579号、第7,820,788号和第7,923,536号。(白蛋白稳定的紫杉醇纳米颗粒制剂)于2005年在美国获得批准,并随后在其他多个国家获得批准,用于治疗转移性乳腺癌。
[0240]
用于配制各种其他持续递送或控制递送工具诸如脂质体运载体、生物可侵蚀的微粒或多孔珠和贮库型注射剂的技术也是本领域技术人员已知的。
[0241]
待被治疗上使用的药物组合物的有效量将取决于例如治疗背景和治疗目标。本领域技术人员将理解,用于治疗的适当剂量水平将因此部分地取决于所递送的分子、多肽所用于的适应症、施用途径、以及患者的尺寸(体重、体表或器官尺寸)和状况(年龄和总体健康)而变化。相应地,临床医师可以调整剂量并改变施用途径以获得最佳治疗效果。典型的剂量可以取决于上文提及的因素而在从约0.001mg/kg至最多约100mg/kg或更多的范围内。多肽组合物可以优选地注射或静脉内施用。长效药物组合物可以取决于特定制剂的半衰期和清除速率每三天至每四天一次、每周一次或每两周一次施用。给药频率将取决于使用的制剂中的多肽的药代动力学参数。通常,施用组合物直至达到实现期望的效果的剂量。因此组合物可以作为单剂量或作为随时间的多剂量(以相同或不同的浓度/剂量)或作为持续的输注施用。常规地进行适当剂量的进一步改进。适当的剂量可以通过使用适当的剂量-响应数据来确定。
[0242]
药物组合物的施用途径根据已知方法,例如口服;通过静脉内、腹膜内、脑内(实质内)、脑室内、肌内、眼内、动脉内、门静脉内、病灶内途径,髓内、鞘内、心室内、经皮、皮下或腹膜内或瘤内注射;以及鼻内、肠内、局部、舌下、尿道、阴道或直肠方式;通过持续释放系统或通过植入装置。当期望时,组合物可以通过团注(bolus)注射施用,或通过输注持续施用,或通过植入装置施用。可选地或另外,组合物可以经由期望的分子已经吸附或包封至其上的膜、海绵状物或另一种适当的材料的植入局部施用。当使用植入装置时,可以将该装置植入到任何合适的组织或器官中,并且期望的分子的递送可以经由扩散施用、缓释团注或持续施用。
[0243]
治疗用途
[0244]
在一方面,本公开内容提供了用于治疗受试者的癌细胞的方法,该方法包括向所述受试者施用在药学上可接受的载体中的治疗有效量(作为单一疗法或在组合疗法方案
中)的本公开内容的il-2变体或il-2变体融合蛋白,其中这样的施用抑制癌细胞的生长和/或增殖。特别地,本公开内容的il-2变体或il-2变体融合蛋白在治疗以癌症为特征的紊乱中是有用的。这样的紊乱包括但不限于实体瘤,诸如乳腺癌、呼吸道癌、脑癌、生殖器官的癌症、消化道的癌症、尿道的癌症、眼癌、肝癌、皮肤癌、头颈癌、甲状腺癌、甲状旁腺癌以及它们的远端转移,淋巴瘤,肉瘤,多发性骨髓瘤和白血病。乳腺癌的实例包括但不限于侵袭性导管癌、侵袭性小叶癌、原位导管癌和原位小叶癌。呼吸道的癌症的实例包括但不限于小细胞肺癌和非小细胞肺癌,以及支气管腺瘤和胸膜肺母细胞瘤(pleuropulmonary blastoma)。脑癌的实例包括但不限于脑干和下丘脑胶质瘤、小脑和大脑星形细胞瘤、髓母细胞瘤、室管膜瘤,以及神经外胚层和松果体肿瘤。男性/雄性生殖器官的肿瘤包括但不限于前列腺癌和睾丸癌。女性/雌性生殖器官的肿瘤包括但不限于子宫内膜癌、宫颈癌、卵巢癌、阴道癌和外阴癌,以及子宫的肉瘤。消化道的肿瘤包括但不限于肛门癌、结肠癌、结肠直肠癌、食管癌、胆囊癌、胃癌、胰腺癌、直肠癌、小肠癌和唾液腺癌。尿道的肿瘤包括但不限于膀胱癌、阴茎癌、肾癌、肾盂癌、输尿管癌和尿道癌。眼癌包括但不限于眼内黑素瘤和视网膜母细胞瘤。肝癌的实例包括但不限于肝细胞癌(具有或不具有纤维板层变体的肝细胞癌)、胆管癌(肝内胆管癌)和混合性肝细胞胆管癌。皮肤癌包括但不限于鳞状细胞癌、卡波济氏肉瘤(kaposi's sarcoma)、恶性黑素瘤、梅克尔细胞癌(merkel cell skin cancer)和非黑素瘤皮肤癌。头颈癌包括但不限于鼻咽癌以及唇和口腔癌。淋巴瘤包括但不限于aids相关淋巴瘤、非霍奇金淋巴瘤、皮肤t细胞淋巴瘤、霍奇金病和中枢神经系统淋巴瘤。肉瘤包括但不限于软组织肉瘤、骨肉瘤、恶性纤维组织细胞瘤、淋巴肉瘤和横纹肌肉瘤。白血病包括但不限于急性髓性白血病、急性淋巴母细胞白血病、各种淋巴细胞白血病、各种髓细胞性白血病和毛细胞白血病。在各种实施方案中,癌症将是具有tgf-β家族成员(诸如激活蛋白a、肌生成抑制蛋白、tgf-β和gdf15)的高表达的癌症,例如胰腺癌、胃癌、卵巢癌、结肠直肠癌、黑素瘤白血病、肺癌、前列腺癌、脑癌、膀胱癌和头颈癌。
[0245]“治疗有效量”或“治疗有效剂量”是指将使被治疗的紊乱的一种或更多种症状减轻至一定程度的被施用的治疗剂的量。
[0246]
治疗有效剂量可以通过确定ec
50
从细胞培养物测定初始地评估。然后,可以在动物模型中配制剂量以实现包括如在细胞培养物中确定的ec
50
的循环血浆浓度范围。此类信息可以被用于更精确地确定在人类中有用的剂量。血浆中的水平可以例如通过hplc测量。确切的组合物、施用途径和剂量可以由个体医师鉴于受试者的状况来选择。
[0247]
可以调整剂量方案以提供最佳的期望的响应(例如,治疗响应或预防响应)。例如,可以施用单次团注,可以随时间施用若干分次剂量(多个或重复或维持)并且剂量可以根据治疗情境的迫切需要所指示的按比例减少或增加。为了便于施用和剂量的一致性,配制呈剂量单位形式的肠胃外组合物是特别有益的。如本文使用的剂量单位形式是指适合作为用于待治疗的哺乳动物受试者的单一剂量的物理分散的单位;每一个单位包含与需要的药物载体一起的被计算产生期望的治疗作用的预定的量的活性化合物。本公开内容的剂量单位形式的规格将主要由抗体的独特特征和待实现的特定治疗作用或预防作用决定。
[0248]
因此,技术人员将理解,基于本文提供的公开内容,根据治疗领域熟知的方法调整剂量和给药方案。即,最大可耐受剂量可以被容易地确定,并且向受试者提供可检测的治疗益处的有效量也可以被确定,向受试者提供可检测的治疗益处而施用每种剂的时间要求同
样可以被确定。因此,尽管在本文中例举了某些剂量和施用方案,这些实例绝非限制在实践本公开内容时可以向受试者提供的剂量和施用方案。
[0249]
应注意,剂量值可以随着待减轻的状况的类型和严重性而变化,并且可以包括单个剂量或多于一个剂量。还应理解,对于任何特定受试者,应根据个体需要和施用组合物或监督组合物的施用的人士的专业判断随时间调整具体剂量方案,并且本文列出的剂量范围仅是示例性的并且不意图限制所要求保护的组合物的范围或实践。另外,本公开内容的组合物的剂量方案可以基于多个因素,包括疾病的类型、受试者的年龄、体重、性别、医学状况、状况的严重性、施用途径和使用的特定抗体。因此,剂量方案可以广泛变化,但可以使用标准方法常规地确定。例如,剂量可以基于药代动力学或药效学参数调整,所述参数可以包括临床作用诸如毒性作用和/或实验值。因此,本公开内容包括如技术人员确定的受试者内的剂量递增(intra-subject dose-escalation)。确定适当的剂量和方案是相关技术领域熟知的并且将被理解为一旦提供本文所公开的教导,则由技术人员掌握。
[0250]
本公开内容的il-2变体或il-2变体融合蛋白的治疗有效量或预防有效量的示例性、非限制性每日给药范围可以为0.001至100mg/kg体重、0.001至90mg/kg体重、0.001至80mg/kg体重、0.001至70mg/kg体重、0.001至60mg/kg体重、0.001至50mg/kg体重、0.001至40mg/kg体重、0.001至30mg/kg体重、0.001至20mg/kg体重、0.001至10mg/kg体重、0.001至5mg/kg体重、0.001至4mg/kg体重、0.001至3mg/kg体重、0.001至2mg/kg体重、0.001至1mg/kg体重、0.010至50mg/kg体重、0.010至40mg/kg体重、0.010至30mg/kg体重、0.010至20mg/kg体重、0.010至10mg/kg体重、0.010至5mg/kg体重、0.010至4mg/kg体重、0.010至3mg/kg体重、0.010至2mg/kg体重、0.010至1mg/kg体重、0.1至50mg/kg体重、0.1至40mg/kg体重、0.1至30mg/kg体重、0.1至20mg/kg体重、0.1至10mg/kg体重、0.1至5mg/kg体重、0.1至4mg/kg体重、0.1至3mg/kg体重、0.1至2mg/kg体重、0.1至1mg/kg体重、1至50mg/kg体重、1至40mg/kg体重、1至30mg/kg体重、1至20mg/kg体重、1至10mg/kg体重、1至5mg/kg体重、1至4mg/kg体重、1至3mg/kg体重、1至2mg/kg体重或1至1mg/kg体重。应注意,剂量值可以随着待被缓解的状况的类型和严重性变化。还应理解,对于任何特定受试者,应根据个体需要和施用组合物或监督组合物的施用的人士的专业判断随时间调整具体剂量方案,并且本文列出的剂量范围仅是示例性的并且不意图限制所要求保护的组合物的范围或实践。
[0251]
本公开内容的药物组合物的毒性和治疗指数可以在细胞培养物或实验动物中通过标准制药学程序确定,例如,确定ld
50
(对群体的50%致死的剂量)和ed
50
(对群体的50%治疗有效的剂量)。毒性剂量和治疗有效剂量之间的剂量比是治疗指数,并且治疗指数可以表示为比率ld
50
/ed
50
。表现出大治疗指数的组合物通常是优选的。
[0252]
il-2变体或il-2变体融合蛋白药物组合物的施用的给药频率取决于疗法的性质和被治疗的特定疾病。受试者可以以规律间隔治疗,诸如每周两次、每周地或每月地,直到实现期望的治疗结果。示例性给药频率包括但不限于:无间断地每周一次;每2周一次;每3周一次;无间断地每周一次,持续2周,然后每月一次;无间断地每周一次,持续3周,然后每月一次;每月一次;每两个月一次;每3个月一次;每4个月一次;每5个月一次;或每6个月一次,或每年一次。
[0253]
组合疗法
[0254]
如本文使用的,提及本公开内容的il-2变体或il-2变体融合蛋白和一种或更多种
其他治疗剂时,术语“共施用(co-administration)”、“共施用(co-administered)”和“与...组合(in combination with)”意图意指,并且的确是指并且包括以下:本公开内容的il-2变体或il-2变体融合蛋白和一种或更多种治疗剂的此类组合同时施用至需要治疗的受试者,其中这样的组分被一起配制成单一剂型,所述单一剂型在基本上相同的时间将所述组分释放至所述受试者;本公开内容的il-2变体或il-2变体融合蛋白和一种或更多种治疗剂的此类组合基本上同时施用至需要治疗的受试者,其中这样的组分彼此分开配制成单独的剂型,所述单独的剂型在基本上相同的时间被所述受试者服用,届时所述组分基本上在相同的时间释放至所述受试者;本公开内容的il-2变体或il-2变体融合蛋白和一种或更多种治疗剂的此类组合顺序施用至需要治疗的受试者,其中这样的组分彼此分开配制成单独的剂型,所述单独的剂型被所述受试者在连续的时间服用,每次施用之间具有显著的时间间隔,届时所述组分在基本上不同的时间释放至所述受试者;以及,本公开内容的il-2变体或il-2变体融合蛋白和一种或更多种治疗剂的此类组合顺序施用至需要治疗的受试者,其中这样的组分一起配制成单一剂型,所述单一剂型以受控方式释放所述组分,届时所述组分在相同和/或不同的时间同时、连续和/或重叠地释放至所述受试者,其中每个部分可以通过相同或不同的途径施用。
[0255]
在另一方面,本公开内容提供了一种用于治疗受试者的癌症或癌症转移的方法,该方法包括施用与第二疗法组合的治疗有效量的本发明的药物组合物,所述第二疗法包括但不限于免疫疗法、细胞毒性化学疗法、小分子激酶抑制剂靶向疗法、手术、放射疗法和干细胞移植。例如,这样的方法可以被用于预防性癌症预防、预防手术后癌症复发和转移,以及作为其他常规癌症疗法的辅助手段。本公开内容认识到,常规癌症疗法(例如,化学疗法、放射疗法、光疗法、免疫疗法和手术)的有效性可以通过本文描述的组合方法的使用来增强。
[0256]
大量的常规化合物已经被证明具有抗赘生物活性。这些化合物已经被用作化学疗法中的药剂以缩小实体瘤、预防转移和进一步生长、或减少白血病或骨髓恶性肿瘤中的恶性t细胞的数目。尽管化学疗法在治疗各种类型的恶性肿瘤中是有效的,但许多抗赘生物化合物诱导不期望的副作用。已经显示出,当将两种或更多种不同的治疗组合时,治疗可以协同地工作,并且允许降低每种治疗的剂量,从而降低每种化合物在较高的剂量产生的有害副作用。在其他情况下,对于治疗是难治性的恶性肿瘤可以响应于两种或更多种不同治疗的组合疗法。
[0257]
在各种实施方案中,第二抗癌剂,诸如化学治疗剂将被施用至患者。示例性化学治疗剂的列表包括但不限于,柔红霉素、更生霉素(dactinomycin)、多柔比星、博莱霉素、丝裂霉素、氮芥、苯丁酸氮芥、美法仑、环磷酰胺、6-巯基嘌呤、6-硫鸟嘌呤、苯达莫司汀、阿糖胞苷(ca)、5-氟尿嘧啶(5-fu)、氟尿苷(5-fudr)、氨甲蝶呤(mtx)、秋水仙碱、长春新碱、长春花碱、依托泊苷、替尼泊苷、顺铂、卡铂、奥沙利铂、喷司他丁、克拉屈滨、阿糖胞苷、吉西他滨、普拉曲沙、米托蒽醌、己烯雌酚(des)、氟达拉滨(fluradabine)、异环磷酰胺、羟基脲紫杉烷(hydroxyureataxanes)(诸如紫杉醇和多西他赛(doxetaxel))和/或蒽环类抗生素,以及剂的组合,诸如但不限于da-epoch、chop、cvp或folfox。在各种实施方案中,这样的化疗剂的剂量包括但不限于约10mg/m2、20mg/m2、30mg/m2、40mg/m2、50mg/m2、60mg/m2、75mg/m2、80mg/m2、90mg/m2、100mg/m2、120mg/m2、150mg/m2、175mg/m2、200mg/m2、210mg/m2、220mg/m2、230mg/
m2、240mg/m2、250mg/m2、260mg/m2和300mg/m2中的任一种。
[0258]
在各种实施方案中,本公开内容的组合治疗方法还可以包括向受试者施用治疗有效量的免疫疗法,所述免疫疗法包括但不限于,使用针对特定肿瘤抗原的消耗性抗体的治疗;使用抗体-药物缀合物的治疗;使用针对共刺激性或共抑制性分子(免疫检查点)(诸如ctla-4、pd-1、ox-40、cd137、gitr、lag3、tim-3、sirp、cd47、cd40、tigit和vista)的激动性抗体、拮抗性抗体或阻断性抗体的治疗;使用双特异性t细胞结合抗体诸如博纳吐单抗的治疗;涉及施用生物响应调节剂(诸如il-12、il-15、il-21、gm-csf、ifn-α、ifn-β和ifn-γ)的治疗;使用治疗性疫苗诸如sipuleucel-t的治疗;使用树突细胞疫苗或肿瘤抗原肽疫苗的治疗;使用嵌合抗原受体(car)-t细胞的治疗;使用car-nk细胞的治疗;使用肿瘤浸润性淋巴细胞(til)的治疗;使用过继转移的抗肿瘤t细胞(离体扩增的和/或tcr转基因的)的治疗;使用tall-104细胞的治疗;和使用免疫刺激剂(诸如toll样受体(tlr)激动剂cpg和咪喹莫特)的治疗;其中组合疗法提供了增加的对肿瘤细胞的效应细胞杀伤,即,当被共施用时,il-2变体和免疫疗法之间存在协同作用。
[0259]
在各种实施方案中,组合疗法包括同时施用在同一药物组合物中或在单独的药物组合物中的il-2变体和第二剂组合物。在各种实施方案中,顺序施用il-2变体组合物和第二剂组合物,即,在施用第二剂组合物之前或之后施用il-2变体组合物。在各种实施方案中,il-2变体组合物和第二剂组合物的施用是同时的,即,il-2变体组合物和第二剂组合物的施用时间段彼此重叠。在各种实施方案中,il-2变体组合物和第二剂组合物的施用是非同时的。例如,在各种实施方案中,终止il-2变体组合物的施用,然后施用第二剂组合物。在各种实施方案中,终止施用第二剂组合物,然后施用il-2变体组合物。
[0260]
提供以下实施例以更充分地说明本公开内容,但不应解释为限制本公开内容的范围。
[0261]
实施例1
[0262]
il-2fc融合构建体的构建和产生
[0263]
对所有基因进行密码子优化以便在哺乳动物细胞中表达,合成这些基因并亚克隆到接受者哺乳动物表达载体(genscript)中。蛋白表达由cmv启动子驱动,并且合成的sv40聚腺苷酸(polya)信号序列存在于cds的3'端。在构建体的n末端处工程化有前导序列,以确保合适的信号传导和加工以便分泌。
[0264]
构建体通过使用聚乙烯亚胺(pei,25,000mw线性,polysciences)用哺乳动物表达载体共转染悬浮生长的hek293-f细胞来产生。如果有两种或更多种表达载体,则载体以1:1的比转染。对于转染,将hek293细胞在无血清freestyle
tm 293表达培养基(thermofisher)中培养。对于在1000ml摇瓶(工作体积330ml)中的产生,将hek293细胞以0.8
×
106个细胞/ml的密度接种,24小时后进行转染。将总共330μg的dna表达载体与16.7ml opti-mem培养基(thermofisher)混合。在添加稀释于16.7ml opti-mem培养基中的0.33mg pei后,将混合物涡旋15sec,并随后在室温孵育10min。然后将dna/pei溶液添加至细胞,并在37℃在具有8%的co2的培养箱中孵育。在第4天将丁酸钠(millipore sigma)以2mm的最终浓度添加至细胞,以帮助维持蛋白表达。培养6天后,收集上清液用于通过以2200rpm离心20min进行纯化。将溶液无菌过滤(0.22μm过滤器,corning)。使用蛋白a亲和色谱从细胞培养物上清液纯化所分泌的蛋白。
[0265]
可选地,按照制造商的说明书,在expicho细胞(thermofisher)中产生构建体。
[0266]
对于亲和色谱,将每种上清液加载到用25ml磷酸盐缓冲盐水ph 7.2(thermofisher)平衡的hitrap mabselectsure柱(cv=5ml,ge healthcare)上。通过用5倍柱体积的pbs ph 7.2洗涤来去除未结合的蛋白,并用25mm柠檬酸钠、25mm氯化钠,ph 3.2洗脱目标蛋白。蛋白溶液通过添加3%的1m tris ph 10.2来中和。离子交换色谱术或混合模式色谱术,包括但不限于captommc(ge healthcare)、陶瓷羟基磷灰石或陶瓷氟磷灰石(bio-rad),也根据需要被用于对蛋白a材料进行精制。靶蛋白用ultra-15浓缩器10kda nmwc(merck millipore ltd.)浓缩。
[0267]
在具有还原剂和不存在还原剂的情况下,通过sds-page和用考马斯亮蓝(coomassie)(imperialr stain)染色来分析所纯化的构建体的纯度和分子量。根据制造商的说明使用预制凝胶系统(4%-12%或8%-16%bis-tris,thermofisher)。纯化的蛋白样品的蛋白浓度通过测量280nm处的uv吸光度(nanodrop分光光度计,thermofisher)除以基于氨基酸序列计算的摩尔消光系数来确定。构建体的聚集体含量在agilent 1200高效液相色谱(hplc)系统上进行分析。在25℃,使用150mm磷酸钠ph 7.0作为流动相,将样品注射到advancebio尺寸排阻柱(4.6x150mm,2.7μm,lc柱,agilent)上。
[0268]
蛋白a纯化的示例性il-2变体fc融合构建体p-0635和p-0704的sds-page和尺寸排阻色谱分析在图1中示出。p-0635(seq id no:85;图1a)和p-0704(seq id no:96和10;图1b)共有il-2中相同的氨基酸取代p65r。p-0635包含与同源二聚体fc融合的二价il-2变体,而p-0704包含与knob-into-hole异源二聚体fc融合的单价il-2变体。sds-page分析展示,两种分子都表现出高蛋白纯度,并且在还原性条件下运行的样品(泳道2)显示出对p-0635的同源二聚体fc链和p-0704的异源二聚体fc链的预期mw。尺寸排阻色谱分析显示,在最初的蛋白a捕获步骤后,两种分子都表现出低聚集倾向并且聚集少于5%。
[0269]
实施例2
[0270]
il-2中的单个氨基酸取代导致融合体化合物的可开发性的普遍改进
[0271]
当应用于il-2时,寻找产生具有期望的生物学特性的变体蛋白的突变组合的工程化方法遇到了重大挑战。本领域已知,天然存在的il-2蛋白倾向于非常不稳定并且易于聚集。这在我们的实验中得到了展示,野生型il-2fc融合蛋白(p-0250)以低水平表达(在hek-293f细胞中瞬时表达为约3mg/l),具有高聚集倾向,通过图2a中描绘的sec色谱图例示。工程化努力陷入困境,因为旨在实现期望的生物活性的il-2的氨基酸取代通常导致突变蛋白甚至更不稳定。当前工作早期阶段的il-2变体有很大一部分以极低水平表达,并且一些变体明显更容易聚集,通过图2b中描绘的p-0318(il-2d20i/n88i fc融合体)的sec色谱图例示。这对于治疗剂的制备和储存是有问题的。
[0272]
还观察到,在具有不同突变位点的构建体或共有相同突变位点但残基取代不同的突变体之间,il-2变体fc融合体的表达谱和聚集倾向显著不同。该观察结果由p-0317(il-2d20i/n88r fc融合体)和p-0318(il-2d20i/n88i fc融合体)例示。两种变体融合体在残基20和88处共有相同的突变位点,并且仅相差一个氨基酸,并且以相似的低水平表达。如在图2b中可以观察到的,p-0318非常易于聚集,并且含有65%的高分子量物质,这使得预期的峰
在色谱图中为次要物质,并用箭头标记。相比之下,p-0317相对纯净,具有7.5%的聚集体(图2c)。可以推断,n88r突变可以降低所得融合蛋白的聚集倾向。然而,il-2具有n88r单突变或d20t/n88r双重突变所产生的融合蛋白p-0254和p-0324,分别具有30%-40%聚集体的聚集倾向。因此,单个氨基酸取代对蛋白稳定性的贡献表现为取决于背景。
[0273]
对il-2的氨基酸取代通常导致较不稳定的蛋白的事实因不同残基取代对蛋白稳定性的不可预测的贡献而更加复杂。因此,非常希望找到能够普遍增强蛋白可开发性(包括改进的稳定性、更高的表达水平和更低的聚集倾向)的残基取代。
[0274]
在位置125处的氨基酸取代最初旨在调节il-2选择性,因为该残基紧邻q126,q126对γc相互作用是必需的。天然存在的il-2在位置125处含有非配对的半胱氨酸,该半胱氨酸在proleukin中被丝氨酸替换。在位置125处含有丙氨酸取代的il-2也被广泛使用。由于在位置125处对半胱氨酸的丝氨酸或丙氨酸取代保留了全部生物活性,因此在位置125处引入了包括glu、lys、try、his和ile的大体积(bulky)带电残基或疏水残基,旨在干扰q126与γc的相互作用,从而实现改变的生物活性。除了含有ile125的融合分子(p-0531)外,所有的所得融合分子都表达水平太低而无法表征。当与其s125对应物(p-0250)相比时,p-0531以显著更高的水平表达(29.5mg/l对比3.1mg/l滴度),具有大幅降低的聚集倾向(0.7%对比25.7%聚集)。可开发性尤其是对产物纯度的令人印象深刻的改进,促使我们评价是否可以在不同的突变背景中重现位置125处异亮氨酸取代的这种提高。
[0275]
因此将s125i取代引入到许多il-2变体fc融合分子中。在il-2的氨基酸位置125处含有ile取代(125i)的构建体使用与其ser-125对应物相同的载体并以相同的培养条件进行表达,并使用mabselectsure进行纯化。在表7中总结了表达水平(mg/l)和通过sec色谱术以示例性分子的聚集%评估的纯度。表7同一行中的两种分子共有相同的其他氨基酸取代,并且差异仅在于残基125处为丝氨酸或异亮氨酸。野生型il-2fc融合体的s125i等同物p-0531(seq id no:68)的sec谱在图2d中进一步示出。从表7清楚的是,在位置125处的异亮氨酸取代导致表达水平提高到4至11倍,并且聚集倾向一致地低。
[0276]
表7s125i取代使各种il-2融合蛋白的聚集降低并且表达增加
[0277][0278][0279]
从本发明明显的是,在位置125处的异亮氨导致il-2融合构建体可开发性的普遍改进。这一发现尤其有价值,因为改变临界稳定的野生型il-2通常导致甚至更不稳定的突变蛋白的事实妨碍了为了获得期望的生物学特性的il-2的工程化。il-2工程化的固有挑战可以通过在位置125处用异亮氨酸单个氨基酸取代来缓解。
[0280]
实施例3
[0281]
设计il-2构建体以改进对效应t细胞和nk细胞的选择性
[0282]
本发明的主要方面是相对于野生型il-2改进il-2对表达il-2rβγ(而不是il-2rα)的细胞超过表达il-2rαβγ的细胞的选择性,以用于癌症治疗。本发明人使用的一种方法是通过将破坏cd25的突变引入细胞因子组分中来产生高选择性的il-2-fc融合蛋白。破坏cd25的突变的选择是基于对il-2/il-2r共晶体结构(pdb代码2b51)的检查。在与il-2受体α亚基的界面处对一个或两个相关残基引入了多于一个氨基酸取代(包括r38、t41、f42、f44、e62、p65、e68和y107),旨在降低或消除与il-2rα的结合。这些构建体还含有s125i突变,用于显著改进可开发性。另外,il-2变体与il-2rα 肺内皮细胞结合的削弱预期防止内皮细胞损伤并显著降低vls。此外,cd25结合的削弱也预期降低cd25抗原吸收,并富集对表达il-2rβγ的细胞的细胞因子占据,并且因此增强体内响应和肿瘤杀伤功效。
[0283]
表3总结了表达为c末端与fc同源二聚体或fc异源二聚体融合的一组il-2突变蛋白。一组含有对与il-2受体α亚基的界面处残基的一个或两个氨基酸取代的il-2变体(seq id no:31-66)经由“gggsgggs”接头(seq id no:18)融合到fc同源二聚体的c末端成为二价il-2融合体(seq id no:69-95)或融合到fc异源二聚体的c末端成为单价il-2融合体(seq id no:96-106)。
[0284]
实施例4
[0285]
在与il-2rα的界面处引入的il-2突变对与受体亚基α结合的影响
[0286]
一组il-2突变蛋白被表达为与fc同源二聚体或fc异源二聚体的c末端融合体,并在酶联免疫吸附测定(elisa)中筛选与il-2rα的结合。简言之,将il-2rα-ecd(seq id no:5)以0.1μg/孔包被到nunc maxisorp 96孔微孔板的孔上。在4℃孵育过夜并用superblock(thermofisher)封闭后,以100μl/孔向每个孔添加从100nm开始的3倍系列稀释的il-2fc融合蛋白。在室温孵育1小时后,将100μl/孔的山羊抗人类igg fc-hrp(1:5000稀释于稀释剂中)添加到每个孔中,并在室温孵育1小时。每个步骤后,将孔彻底抽吸,并用pbs/0.05%tween-20洗涤三次。最后,向每个孔添加100μl tmb底物;将板在室温在黑暗中显影(develop)10分钟,并添加100μl/孔的停止溶液(2n硫酸,ricca chemical)。确定450nm处的吸光度,并使用prism软件(graphpad)拟合曲线。
[0287]
首先,测试野生型il-2fc融合蛋白p-0531和p-0689的s125i等同物的cd25结合。p-0531包含与fc同源二聚体融合的二价il-2部分(seq id no:68),并且p-0689(seq id no:107 10)是p-0531的单价对应物。如图3所示,p-0531和p-0689之间结合ec
50
的2倍差异(分别为0.21nm和0.51nm)与il-2化合价差异一致。
[0288]
由于所有靶向的il-2残基r38、t41、f42、f44、e62、p65、e68和y107都位于与il-2rα的界面处,并与多于一个il-2rα残基形成氢键/盐桥或疏水相互作用(mathias rickert等人,(2005)science 308,1477-80),因此推断,这些位点处的氨基酸取代预期会破坏与il-2rα的相互作用,并产生具有降低或消除的与il-2rα结合的il-2变体。然而,结合数据揭示,不同il-2突变对il-2rα结合的影响差异明显。
[0289]
如图4所示,在位置t41(在图4a中由p-0603、p-0604和p-0605例示)或y107(在图4b中由p-0610、p-0611和p-0612例示)处含有各种取代的il-2同源二聚体fc融合体完全保留了与il-2rα的结合强度。数据表明,残基t41和y107可能在功能上并不重要,尽管它们在il-2rα的界面处并与多种il-2rα残基相互作用。
[0290]
残基r38被认为是il-2/il-2rα相互作用的能量热点,参与关键氢键;多项工程化
努力(例如,keith m.heaton等人,(1993)cancer res.53.2597-2602,和peisheng hu等人,(2003)blood 101:4853-4861)显示在r38处的各种取代导致与il-2rα的相互作用破坏。因此,相当意想不到的是,观察到由p-0602(r38a)、p-0614(r38f)和p-0615(r38g)例示的各种突变没有导致或仅导致与il-2rα结合强度的极小降低(最多3倍)。在图4c-4d中示出了结合数据。
[0291]
同样地,残基e68参与与il-2rα界面残基的多于一个氢键,但是e68处的各种氨基酸特性的取代(由e68a(p-0628)、e68f(p-0629)、e68h(p-0630)和e68l(p-0631)例示)都没有导致与il-2rα结合的任何降低。感兴趣的是,p-0629和p-0630实际上展示出与il-2rα的结合分别增强了3倍和14倍(图5)。
[0292]
总之,il-2残基t41、r38、e68和y107的替换通常不会破坏il-2rα相互作用,并且所得的il-2同源二聚体fc融合体保留了完全或接近完全的与il-2rα的结合。在表8中总结了针对p-0531的elisa结合ec
50
归一化的各种il-2突变蛋白的elisa结合ec
50
。
[0293]
表8
[0294]
其替换通常不会破坏il-2rα相互作用并且所得的il-2变体保留与il-2rα的完全结合的il-2残基
[0295][0296]
相比之下,残基e62处的氨基酸取代(由p-0624(e62a)、p-0625(e62f)、p-0626(e62h)和p-0627(e62l)例示)全都导致与il-2rα的结合降低,表明e62确实是il-2/il-2rα相互作用的能量热点。如图6中展示的,虽然e62h和e62l取代仅导致与il-2rα结合的2-3倍的略微降低,但e62a和e62f突变似乎在与该il-2r亚基的相互作用中产生巨大破坏,导致与il-2rα的结合分别降低60倍和150倍。另外,文献中充分记载了il-2f42a突变(p-0613)破坏与受体α的相互作用,这展示于图8a中,其中与il-2rα的结合降低15倍。
[0297]
总之,f42和e62是这样的il-2残基,其替换通常会破坏il-2rα相互作用,并且所得的il-2变体展示出与il-2rα的结合降低。各种il-2突变蛋白的elisa结合ec
50
针对p-0531的elisa结合ec
50
进行标准化,并在表9中示出。
[0298]
表9
[0299]
其替换通常会破坏il-2rα相互作用并且所得的il-2变体具有降低的与il-2rα的结合的il-2残基
[0300][0301]
实施例5
[0302]
残基p65处的氨基酸取代对与受体亚基α的结合产生意想不到的多方面的(manifold)影响
[0303]
il-2残基p65与若干关键的il-2rα界面残基(包括r36和l42)发生范德华相互作用,但不与il-2rα形成盐桥或氢键。因此推测p65取代可能仅导致与该il-2r亚基相互作用的略微破坏,并可能对与il-2rα的结合引起轻微影响。然而,p65取代对il-2rα相互作用的影响与假设形成了鲜明对比,并且意想不到地是多方面的,包括完全保留/增强、降低或完全消除与il-2rα的结合。
[0304]
在p65处引入了多于一种取代,由p65g、p65e、p65a、p65h、p65n、p65q、p65r、p65k例示,并且所得的il-2突变蛋白表达为与fc同源二聚体或fc异源二聚体的c末端融合体。这组il-2突变蛋白随后在与cd25结合的elisa中被筛选。在图7中示出了结合数据,并在表10总结了针对p-0531或p-0689的elisa结合ec
50
进行归一化以匹配每种构建体的化合价的il-2突变蛋白的elisa结合ec
50
。
[0305]
表10p65的取代导致对il-2rα结合的意想不到的多方面的影响
[0306][0307]
如图7a和图7b中所示,p65g(p-0608)、p65e(p-0633)、p65a(p-0706)突变似乎没有在与il-2rα亚基的相互作用中产生任何破坏;相反,当与它们的野生型对应物相比时,与il-2rα的结合强度分别增强了18倍、10倍和10倍。
[0308]
另一组il-2突变蛋白fc融合体p-0634、p-0708和p-0709含有p65突变,该p65突变导致il-2与il-2rα亚基的相互作用显著破坏。如图7c中所示和表9中总结的,p65n(p-0708)导致与il-2rα结合的8.6倍的略微降低,而p65h(p-0634)和p65h(p-0709)取代导致更明显
的影响,这分别由il-2rα结合降低23倍和43倍所展示。
[0309]
另一类il-2p65取代p65r和p65k似乎对il-2和il-r2rα相互作用产生巨大破坏,并消除了p-0635、p-0704和p-0707与il-2rα的结合(图7d)。p-0635和p-0704是包含p65r取代的il-2fc融合体的二价和一价对应物,并且p-0707含有p65k氨基酸替换。图7d示出,所有三种il-2突变蛋白fc融合体在il-2rα浓度高达100nm时显示出极小信号,与含有三重的破坏cd25的突变f42a/y45a/l72g的基准分子相当,该基准分子表现为消除结合(christian klein等人oncoimmunology(2017),6:3,e1277306)。
[0310]
如图7a-7c以及表9和表10中总结的,残基p65的取代导致对il-2rα结合的意想不到的多方面的影响。重要的是,它的取代可以完全保留/增强、降低或完全消除所得的il-2变体与il-2rα的结合。如本领域技术人员将理解的,由单个氨基酸的变化导致的这种水平的活性变化不能够通过基于结构的诱变方法来预测。现有技术也没有预期或教导il-2rα结合的完全消除,因为p65的突变仅改变了范德华相互作用表面的有限的部分。
[0311]
实施例6
[0312]
调节il-2与受体亚基α结合的氨基酸取代组合
[0313]
如本领域技术人员将理解的,本发明中公开的突变可以任选地和独立地以任何方式组合,以最佳地调节il-2与受体亚基α的结合。在此,我们通过组合两个破坏il-2rα的氨基酸取代展示了不能够与il-2rα结合的il-2化合物的设计。
[0314]
p-0613含有f42a突变,其导致与il-2rα的结合降低了15倍(图8a),p-0625和p-0634含有e62f和p65h取代,分别具有降低150倍和23倍的与il-2rα的结合。p-0702中的f42a和e62f双突变组合以及p-0703中的f42a和p65h双突变组合两者都导致消除的与il-2rα的结合(图8b和图8c)。如预期的,包含f42/e62a双氨基酸改变的p-0766和f42a/e62h双取代的p-0767不能够与il-2rα结合(数据未示出)。
[0315]
除了作为设计具有消除的与il-2rα结合的il-2突变蛋白的有效方法,氨基酸组合也可用于调节结合活性水平。在此示出的一种实例是p-0765,它组合了一个破坏cd25的突变f42a和一个增强cd25的取代p65a,并且与它的野生型对应物p-0689相比,与il-2rα的结合强度有6.8倍的略微降低(数据未示出),这与单个突变的组合一致。在表11中总结了针对p-0689的elisa结合ec
50
归一化的il-2突变蛋白的elisa结合ec
50
。
[0316]
表11cd25界面处的氨基酸取代的组合对与il-2rα的结合的影响
[0317][0318]
总之,氨基酸取代组合是调节il-2与受体亚基α结合的多用途方法。它可以通过组合两个破坏cd25的残基实现il-2rα结合的完全消除,或者它可以用于以不同的减弱水平来调节il-2rα结合。
[0319]
实施例7
[0320]
在离体功能测定中,il-2rα结合强度的调节与刺激treg细胞的il-2效力相关
[0321]
随后检测了一组il-2变体fc融合蛋白与野生型融合蛋白p-0531和基准分子p-0551(seq id no:95)相比差异性刺激cd4 treg细胞中stat5磷酸化的能力。已知在il-2结合跨膜il-2受体后,stat5参与下游信号级联。在facs分析中,使用新鲜的人类外周血单个核细胞(pbmc)测量淋巴细胞亚群中stat5的磷酸化,并且使用叉头转录因子foxp3来鉴定treg群体。
[0322]
在4℃使纯化的pbmc在无血清macs缓冲液中饥饿1小时。然后在37℃将2
×
105个pbmc用测试化合物的系列稀释液处理30min。通过用1
×
foxp3固定/透化工作溶液孵育30分钟并用1
×
透化缓冲液洗涤,用foxp3/转录因子染色缓冲液组(ebio)固定和透化细胞。将细胞另外用cytofix缓冲液固定,并用perm缓冲液iii(bd biosciences)透化,并且然后洗涤。在通过添加人类trustain fcx(1:50稀释)封闭fc受体后,以制造商推荐的浓度用抗cd25-pe抗体、抗foxp3-apc抗体、抗pstat5-fitc抗体和抗cd4-percp-cy5.5抗体的混合物将细胞在室温染色45分钟。通过离心收集细胞,洗涤,重悬于facs缓冲液中,并通过流式细胞术进行分析。将treg细胞亚群的流式细胞术数据门控为cd4 /foxp3 /cd25
高
组。数据表示为门控的群体中pstat5阳性细胞的百分比。
[0323]
这组il-2变体fc融合体含有赋予以下的氨基酸取代:增强与il-2rα的结合(p-0608)、降低与il-2rα的结合(p-0626、p-0634和p-0624)或消除与il-2rα的结合(p-0635)。此外,p-0626、p-0634和p-0624展示出il-2rα结合强度的不同水平的减弱;p-0626、p-0634和p-0624的结合降低分别为2.6倍、23倍和60倍。il-2rα结合调节的趋势和水平以各种il-2变体fc融合体刺激cd4 treg细胞中stat5磷酸化的不同效力来反映(图9)。在刺激treg stat5磷酸化方面,与il-2rα结合增强的p-0608相应地展示出比p-0531更高的效力趋势。p-0626、p-0624和p-0634全都显示出降低的pstat5效力,与它们的较低的il-2rα结合强度一致。它们保留的尽管较低的与il-2rα的结合仍然导致比消除了与il-2rα结合的p-0635和基准p-0551更有效的treg活化。p-0635和p-0551具有相当的右移5个对数的在treg细胞中诱导pstat5的效力,并且这种低水平的treg信号传导可能是由treg细胞上表达的il-rβγ的活化导致的。因此,在cd8 t细胞和nk细胞也被活化时的浓度,突变体预期实现期望的活化treg的特性。令人惊讶地观察到il-2rα结合的完全消除导致treg效力降低超过5个对数(图9)。
[0324]
实施例8
[0325]
在il-2rα界面处引入的il-2突变对与il-2rβγ相互作用的影响
[0326]
为了研究在il-2rα界面处引入的il-2突变是否将影响il-2与il-2rβγ的相互作用,在实施例7的同一组il-2变体fc融合蛋白的elisa中评估了与il-2rβγ的结合。
[0327]
简言之,将包含与fc hole链(seq id no:10)的n末端融合的il-2rβecd(seq id no:109)和与fc knob链(seq id no:9)的n末端融合的γcecd(seq id no:110)的重组il-2rβγ异源二聚体以2μg/孔包被到nunc maxisorp 96孔微孔板的孔上。在4℃孵育过夜并用1%bsa封闭后,以100μl/孔向每个孔添加从10nm开始的3倍系列稀释的il-2fc融合蛋白。在室温孵育1小时后,将100μl/孔的生物素小鼠抗人类il-2克隆b33-2(bd biosiences)以0.5μg/ml添加到每个孔中,并在室温孵育1小时。随后,向每个孔中添加100μl/孔的链霉亲和
素-hrp(1∶5000稀释于稀释剂中)并在室温孵育40min。每个步骤后,将孔彻底抽吸,并用pbs/0.05%tween-20洗涤三次。最后,向每个孔添加100μl tmb底物;将板在室温在黑暗中显影10分钟,并添加100μl/孔的停止溶液(2n硫酸,ricca chemical)。确定450nm处的吸光度,并使用prism软件(graphpad)拟合曲线。
[0328]
如图10所示,与野生型il-2融合体p-0531相比,包含赋予增强、降低或消除的与il-2rα结合的突变的示例性的il-2变体fc融合体全都展示出未改变的与il-2rβγ的结合。数据证实,在il-2rα界面处引入的测试il-2突变确实仅干扰了cd25结合,而不影响与il-2rβγ的相互作用。
[0329]
通过流式细胞术进一步表征了该组示例性il-2变体fc融合蛋白诱导人类cd8 t细胞和nk细胞上的ki67表达。新鲜分离的nk细胞和cd8 t细胞不表达cd25或表达非常低的cd25表达,并且il-2r信号传导主要经由中等亲和力受体亚基βγ介导。ki67是作为细胞增殖标志物的核蛋白。
[0330]
简言之,通过ficoll-hypaque离心法从健康供体的血沉棕黄层分离人类pbmc。将纯化的人类pbmc用系列稀释的il-2变体fc融合化合物处理,并在37℃孵育5天。在第5天,将细胞用facs缓冲液(1%fbs/pbs)洗涤一次,并首先用fc阻断剂和表面标志物抗体、抗人类cd56-fitc抗体、抗人类cd8-apc抗体染色。孵育30分钟并洗涤后,用200μl/孔的1
×
foxp3固定和透化工作溶液将细胞沉淀物(cell pellet)完全重悬,并在室温在黑暗中孵育30分钟。离心后,向每个孔中添加200μl的1
×
透化缓冲液进行另一次洗涤。将细胞沉淀重悬于含有抗人类ki67-pe抗体(1:25稀释)的透化缓冲液中。在室温孵育30分钟后,收集细胞并洗涤,重悬于facs缓冲液中,并通过流式细胞术分析。数据表示为门控的群体中ki-67阳性细胞的百分比。
[0331]
与p-0531和p-0551相比,响应于il-2变体fc融合蛋白的cd8 t细胞和nk细胞上ki-67表达的剂量依赖性增加在图11a和图11b中示出。干扰cd25的突变的引入导致fc融合构建体具有与野生型il-2二价融合蛋白p-0531相当的效力。
[0332]
此外,表征了p-0689和p-0704(分别为p-0531和p-0635的单价对应物)对人类cd8 t细胞上ki-67的表达的诱导。如图11c中示出的,p-0689(野生型il-2)和含有消除与il-2rα结合的p65r突变的p-0704显示出等同效力的cd8 t细胞上ki-67表达的剂量依赖性增加。组合的离体功能数据进一步证实,在il-2rα界面处引入的il-2突变对与il-2rβγ的相互作用具有极小影响或没有影响。此外,p-0531和p-0689之间以及p-0635和p-0704之间的效力差异与它们各自的il-2化合价差异一致。
[0333]
实施例9
[0334]
将破坏il-2rβ或γc的取代引入具有降低的与il-2rα结合的il-2变体用于整体效力减弱
[0335]
全il-2激动剂可能导致途径过度活化和不期望的“命中靶”“未命中组织”毒性。对于il-2rβγ选择性全激动剂来说可能尤其如此;由于增强的选择性和降低的cd25吸收,il-2rβγ选择性全激动剂可以增强cd4 、cd8 效应t细胞和nk细胞的明显的体内响应。因此,可能观察到急性毒性伴随体重明显下降。此外,过度刺激诱导的细胞衰竭或死亡可能引起重复给药后体内响应丧失。推断较低的总体效力可以防止途径过度活化,并降低不需要的靶吸收;因此,可以潜在地降低毒性并改进药代动力学和药效学。为了最佳活性,用于减弱整
体效力的调节il-2rβγ的取代因此被引入到具有降低/消除的与il-2rα结合的il-2变体。减弱的与il-2rβγ的结合亲和力也将降低受体介导的il-2内化,从而导致比野生型il-2缓慢但持续的受体活化和持久的药效学。
[0336]
破坏il-2rβ或γc的突变的选择是基于对il-2/il-2r共晶体结构(pdb代码2b51)的检查。在与il-2rβ或γc发生直接接触的界面处或其附近的残基的替换可以导致与il-2rβγ的结合降低,并从而调节活化途径的整体效力。例如,d20参与与il-2rβ界面处的受体亚基侧链的广泛的氢键网络。类似地,n88是il-2/il-2rβ相互作用的能量热点,参与与受体链的关键氢键。q126是γc相互作用必需的,然而,能量热点处的氨基酸取代可能导致活性实质性减少,呈现次优效力,这由图13a中d20位置处的各种突变(d20e、d20t、d20n、d20q、d20s)例示。在p-0250(seq id:67)中将所有突变引入il-2并表达为il-2变体fc融合蛋白。如图13a所示,d20处的大多数突变导致刺激仅表达il-2rβγ亚基的cd4 tconv细胞中pstat5表达的活性大幅减少或消除。类似地,位置n88处的突变也导致cd4 tconv细胞活化的活性大部分消除(数据未示出)。
[0337]
因此在位置l19(该残基仅与il-2rβ发生范德华相互作用)处引入氨基酸取代,并且所得的突变体仅调节而非消除il-2的功能活性。图13b和图13c示出,在位置19处含有各种突变的il-2变体展示出一系列水平的诱导cd4 tconv细胞上stat5磷酸化的效力。与野生型相比,l19y、l19r、l19q突变导致轻度活性降低,而l19n和l19h中度降低活性。对于l19d,这样的活性显著受损。通过突变位置l19实现的不同水平的效力降低有助于活性精细调节,以得到降低毒性并改进体内药代动力学和药效学的最佳效力。
[0338]
此外,在q126(该残基对γc相互作用是必需的)处含有氨基酸改变的il-2变体被类似地制备。在图13d中展示了il-2q126e fc融合蛋白诱导cd4 tconv细胞上stat5磷酸化的功能活性。与其野生型对应物相比,q126e导致活性略微降低。
[0339]
另外,由于il-2的n末端处的氨基酸主要参与与il-2rβγ的相互作用,因此n末端氨基酸缺失被认为是调节整体效力的不同方法。因此,构建了基于含有l19h/s125i/q126e的il-2变体的n末端缺失突变体(5个、7个、9个或11个n末端氨基酸缺失),并在人类pbmc测定中进行测定。作为亲本分子,il-2l19h/s125i/q126e变体保留了与il-2rα的完全结合,但与il-2rβγ的结合减少,因此其只能在treg细胞中进行可靠测定,这仍然能够剖析突变对整体效力的影响。包含11-aa缺失的fc il-2变体没有产生足够的材料用于表征。如图13e中描绘的,虽然5-aa缺失和7-aa缺失完全保留了效力,但9-aa缺失导致了25倍的活性损失(18pm对比0.74pm)。因此预期,不同效力的各种il-2变体可以通过n末端处7个、8个、9个或10个氨基酸的氨基酸缺失来进一步调节,以获得期望的活性谱。
[0340]
破坏il-2rβ的突变l19h、l19q、l19y和破坏γc的突变q126e被引入p-0704,分别产生p-0731、p-0759、p-0761和p-0732。p-0704包含导致与il-2rα的结合完全丧失的p65r氨基酸取代。与p-0704相比,p-0731、p-0759、p-0761和p-0732在elisa中评估了与il-2rβγ的结合,并通过流式细胞术评估了对人类cd8 t细胞、cd4 t细胞和nk细胞上ki-67表达的诱导。
[0341]
如图14a所示,与p-0689和p-0704相比,示例性的il-2变体fc融合体全都显示出不同水平的降低的与il-2rβγ的结合。由于il-2与受体亚基β或γ的结合弱且解离速率高,因此无法通过elisa可靠地评估每种单独亚基的结合活性(数据未示出)。然而,与il-2rβγ异源二聚体结合的降低被预期是归因于氨基酸改变破坏了与相应β或γ受体亚基的相互作
用。
[0342]
评估了由p-0731中破坏il-2rβ的取代l19h和p-0732中破坏γc的突变q126e引起的诱导人类pbmc中人类cd8 t细胞上ki67表达的活性的效力降低。野生型il-2单体fc融合的s125i等同物p-0689和失去与il-2rα的结合但完全保留对二聚体il-2rβγ受体的亲和力和功能活性的p-0704,被包括在内用于比较。如图14b中展示的,所有单体il-2fc融合蛋白以剂量依赖性方式诱导ki-67阳性cd8 t细胞百分比增加;与p-0704相比,p-0731表现出约30倍的效力降低。p-0732表现出最低的效力,与p-0704相比具有减弱大于100倍的ec
50
。
[0343]
在图15a、图15b和图15c中分别示出了p-0731、p-0759和p-0761对人类cd8 t细胞、nk细胞和cd4 t细胞增殖的剂量依赖性增加。il-2变体fc融合蛋白p-0731、p-0759和p-0761除了全都含有p-0704中的消除il-2rα结合的取代p65r外,在位置l19处全都含有破坏il-2rβ的突变。与p-0704相比,所有变体在人类cd8 t细胞、nk细胞和cd4 t细胞增殖中都显示出预期的效力降低。p-0759(l19q)和p-0761(l19y)显示出3-5倍的效力略微降低,而p-0731中的l19h突变导致更强烈的30倍效力降低。通过l19q和l19h取代的效力减弱水平在所有评估的细胞亚群中遵循相同的趋势,并且与诱导cd4 tconv细胞上pstat5表达的活性降低水平(图13b和图13c)和结合重组il-2rβγ蛋白的减弱水平(图14a)一致。与p-0704相比,基准分子在诱导细胞增殖方面表现出相当但稍低的效力。
[0344]
总之,除了在il-2中引入破坏cd25的取代以抑制免疫抑制性treg的不期望的扩增外,还可以进一步引入破坏il-2rβγ的取代或n末端缺失来减弱整体效力,以获得最佳活性。较低的效力可以防止途径的过度活化,并降低不需要的靶吸收;因此,可以潜在地降低毒性并改进药代动力学和药效学。
[0345]
实施例10
[0346]
在小鼠中单次注射后il-2变体fc融合蛋白的药效学作用
[0347]
在balb/c小鼠中在单次注射后进行了用p-0704(seq id no:96和10)处理后不同淋巴细胞亚群的细胞扩增的时间进程,p-0704是与il-2rα的结合被消除的c末端单价il-2变体fc融合蛋白。随着时间的推移,监测对外周血淋巴细胞扩增的效应。此外,还将p-0704的免疫药效学谱与野生型il-2对应物p-0689(seq id no:107和10)的免疫药效学谱进行了比较。
[0348]
在研究之前,从charles river实验室接收七周龄的雌性balb/c小鼠,并在机构内适应至少7天。媒介物和以0.6mg/kg单剂量的p-0704和p-0689在第0天腹膜内(i.p.)施用至小鼠。注射后第3天和第5天抽取血液样品。每组包括4只小鼠。
[0349]
肝素处理的全血用于免疫表型分析。使用bd pharm裂解缓冲液裂解红细胞后,通过台盼蓝死细胞排除对总存活单核血细胞计数,并继续进行ki67细胞内染色。用200μl/孔的1
×
foxp3固定/透化工作溶液完全重悬细胞沉淀物,并在室温在黑暗中孵育30分钟。离心后,向每个孔中添加200μl的1
×
透化缓冲液进行另一次洗涤。用纯化的抗小鼠cd16/cd32抗体(1:50稀释)阻断fc受体后,用apc-cy7 cd3、bv510 cd4、fitc foxp3、pe ki67、apc cd335和percpcy 5.5cd8(1:50稀释)对细胞进行染色。孵育30分钟后,收集细胞并洗涤,重悬于facs缓冲液中,并通过流式细胞术分析。
[0350]
如图16a所示,p-0689中的野生型il-2导致treg细胞的强扩增(细胞数量增加6倍)在第3天达到峰值,这被认为是治疗癌症所不期望的,而p-0704在第3天没有treg扩增并且
在第5天仅极小地扩增treg细胞。相比之下,p-0704在第3天增加了cd8 t细胞在总cd3 淋巴细胞群体中的百分比,并在第5天使cd8群体从19%(基线)继续增强到67%(图16b)。相反,通过p-0689的cd8 t细胞扩增极小(图16b)。对于nk细胞,通过p-0704,在第3天观察到5.4倍细胞数量增加,并且细胞继续扩增并导致在第5天的64倍的细胞增加。p-0689在第3天使nk细胞数量增加了7.8倍,但该作用快速减弱并在第5天返回到基线(图16c)。
[0351]
总之,p-0704展示出几乎消除的treg扩增,并明显增强了cd8细胞和nk细胞扩增,这与p-0689的细胞扩增谱截然不同。该观察与il-2rα亚基结合能力以及随后treg细胞响应性的巨大差异一致。另外,作为il-2rβγ选择性全激动剂,p-0704可以增强cd8 效应t细胞和nk细胞的明显的体内响应,这是由于增强的选择性和降低的cd25吸收。
[0352]
实施例11
[0353]
il-2-抗体融合蛋白的构建、表达和纯化
[0354]
在本实施例中,制备并评估了各种il-2-抗体融合蛋白。将il-2变体栓系到靶向免疫检查点的抗体,预期将il-2导向衰竭的t细胞,并使肿瘤微环境在免疫学上变热。该策略还降低了il-2的全身性暴露和脱靶毒性。免疫检查点抑制剂与il-2变体的双功能融合蛋白也预期通过除去负调节和在功能和数量上重振t细胞来提供协同作用。免疫检查点阻断性抗体-细胞因子融合蛋白预期进一步增强免疫系统对抗肿瘤的活性。本发明人提出,使用具有降低或消除的与il-2rα的结合和减弱的il-2rβγ活性的il-2变体将有助于在细胞因子和表现出明显不同效力和分子量的抗体臂之间建立化学计量平衡,以允许最佳给药和维持每个臂的功能。此外,细胞因子活性减弱预期使外周活化最小化、减轻抗原吸收并促进经由抗体臂的肿瘤靶向。
[0355]
对于在细胞毒性t细胞或其他还表达il-2rβγ的淋巴细胞亚群上表达的检查点抑制剂靶,诸如pd-1,预期il-2pd-1抗体融合蛋白可以优先将il-2变体以顺式递送至pd-1 细胞,诸如肿瘤微环境中活化和衰竭的cd8 t细胞,以促进选择性信号传导。
[0356]
按照这一概念,构建了各种il-2-抗体融合蛋白。
[0357]
为了制备il-2-抗体融合蛋白,将上文列出的抗体的重链的ch1-ch2-ch3(基于eu编号的抗体残基118-447)结构域替换为seq id no:162中列出的igg1序列,该igg1序列包含l234a、l235a、g237a突变,以消除与fcγr和c1q的结合,但保留fcrn结合或pk。il-2变体肽经由具有表6中列出的序列的肽接头融合到fc结构域的c末端。可选地,为了表达单价il-2变体,上文列出的抗体的重链的ch1-ch2-ch3结构域被seq id no:163-164中列出的异源二聚体链替换。il-2变体肽经由具有表6中列出的序列的肽接头融合到使用knob-into-holes技术工程化的含有knob的异源二聚体重链的c末端。半衰期延长突变,例如n434a,可以进一步引入同源二聚体或异源二聚体fc链中。在表12中列出了示例性il-2pd-1拮抗剂抗体融合蛋白。另外,p-0844是包含seq id no:182-184的基准il-2变体pd-1拮抗剂抗体融合蛋白。
[0358]
表12示例性的il-2变体拮抗剂pd-1抗体融合蛋白
[0359]
[0360][0361]
按照实施例1中详述的相同程序进行基因合成、表达载体构建、以及蛋白产生、纯化和表征。
[0362]
类似地产生鼠替代pd-1il-2变体融合蛋白以用于免疫活性小鼠的体内肿瘤模型。替代抗小鼠pd-1抗体包含seq id no:185-187,其携带用于除去效应子功能和用于异源二聚化的fc突变;il-2变体经由(g4s)3接头(seq id no:15)融合到抗小鼠pd-1hc链2(seq id no:186)的c末端。表13列出了每种示例性鼠替代pd1-il-2变体融合蛋白中的il-2变体:
[0363]
表13示例性的鼠替代pd-1il-2变体融合蛋白
[0364][0365]
实施例12
[0366]
在离体功能测定中il-2变体抗体融合蛋白完全保留了il-2效力和活性谱
[0367]
本研究中的替代小鼠pd-1拮抗剂抗体(seq id no:185-187)不与人类抗原交叉反应;因此,它在人类细胞中被用作非功能性抗体,以评估抗体融合形式对il-2变体刺激淋巴细胞亚群并使之增殖的效力和活性谱的影响。
[0368]
抗体融合形式的影响由p-0782与它的fc融合对应物p-0704的比较来例示。p-0782和p-0704两者都包含单体il-2p65r变体,其经由柔性(g3s)2接头(seq id no:18)连接到异源二聚体fc结构域的c末端。il-2中的p65r取代消除了与il-2rα的结合(图7d)。如图17a-17c中描绘的,p-0782和p-0704在诱导cd4 treg细胞(图17a)、cd8 t细胞(图17b)和nk细胞(图17c)中的剂量依赖性stat5磷酸化方面是同等有效的。数据证实,与抗体融合的il-2部分与其相应的fc融合蛋白中一样完全保留了它的活性。
[0369]
此外,比较了三种il-2变体小鼠pd1抗体融合蛋白p-0837、p-0838和p-0782刺激人类pbmc中pstat5的活性。p-0838和p-0782中的il-2突变分别为p65q和p65r。p-0837包含野生型il-2部分(seq id no:4)。与野生型相比,p65q使il-2rα结合强度降低了43倍(表10),并且p65r消除了与il-2rα的结合。证实了前面实施例中的il-2fc融合分子的发现,图18a-18c展示了在il-2rα界面处引入的il-2突变确实仅干扰cd25,而不影响与il-2rβγ的相互作用。由于人类pbmc中幼稚cd8 t细胞和nk细胞不表达cd25或表达非常低水平的cd25,所有这三种分子在对这两个淋巴细胞亚群上pstat5表达的剂量依赖性刺激中显示出相同的效力(图18b和图18c)。相反,treg细胞组成性地表达高水平的cd25,并且因此p-0838和p-0782在刺激treg细胞中pstat5表达方面显示出比野生型对应物p-0837明显降低的响应(图18a);对于p-0837、p-0838和p-0782,ec
50
分别为0.45pm、0.36nm(比p-0837弱800倍)和4.5nm(比p-0837弱10,000倍)。cd25结合降低的突变体p-0838和cd25结合消除的突变体p-0782两者在刺激cd8细胞和nk细胞方面保留了与野生型对应物相似的效力。另外,消除p-0782中的il-2rα结合导致treg/cd8的ec
50
比为约1,表明相对于细胞毒性效应细胞对treg细胞没有优先刺激(treg细胞的ec
50
为4.5nm对比cd8 t细胞的ec
50
为4.6nm)。p-0838中存在的尽管显著减弱的il-2rα结合导致treg细胞比cd8 t细胞的pstat5响应性增强约13倍(treg为0.36nm对比cd8 t细胞为4.6nm)。
[0370]
在il-2抗体融合形式的离体功能测定中,还评估了除了与il-2rα结合降低外,具有破坏il-2rβ的突变l19q或l19h的效力减弱的il-2变体。与p-0782相比,p-0786包含一个另外的l19q取代,并且p-0783含有l19h。p-0782、p-0786和p-0783的fc对应物分别是p-0704、p-0759和p-0731。
[0371]
在图19a和图19b中分别示出了由p-0782、p-0786和p-0783以剂量依赖性方式诱导人类cd8 t细胞和nk细胞上的stat5磷酸化;在图19c和图19d中分别描述了相同淋巴细胞亚群增殖的剂量依赖性增加。与p-0782相比,p-0786在诱导cd8 t细胞(图19a)和nk细胞(图19b)上的stat5磷酸化方面显示出2-3倍的效力略微降低,而p-0783中的l19h突变导致更强烈的20-30倍效力降低(图19a和图19b)。对于cd8 t细胞(图19c)和nk细胞(图19d)上ki67的剂量依赖性增加,观察到类似水平的效力减弱。抗体融合蛋白p-0782、p-0786和p-0783的效力减弱水平分别遵循与它们对应的fc融合蛋白p-0704、p-0759和p-0731相同的趋势(图15a和图15b)。
[0372]
在il-2抗体融合形式中p65q突变的背景下,也评估了通过破坏il-2rβ的突变的效力减弱。l19q和l19h被引入p-0838以分别制备p-0790和p-0787。图20a、图20b和图20c显示了它们刺激treg细胞、cd8 t细胞和nk细胞上stat5磷酸化的活性。图20d和图20e示出了cd8 t细胞和nk细胞上增殖标志物ki67的剂量依赖性增加。效力减弱的水平遵循与基于消除il-rα的取代p65r的ab融合体观察到的相同的趋势。
[0373]
进一步评估了p-0782、p-0786和p-0783以及p-0837的ctll-2增殖活性,p-0837包含s125i等同野生型il-2。ctll-2细胞是表达α、β和γ受体亚基的c57bl/6小鼠来源的细胞毒性t细胞。简言之,收获ctll2细胞,洗涤,并重悬于不含il-2的培养基(rpmi1640,10%fcs,2mm谷氨酰胺)中,并孵育两小时(il-2饥饿)。饥饿后,将50μl以50,000个/ml重悬于不含il-2的新鲜培养基中的ctll-2细胞转移至96孔u形底板。将50μl系列稀释的il-2抗体融合体添加到孔中,以使最终体积为100μl/孔。将样品孵育2天,并按照制造商的说明书,使用
0841具有(g4s)3接头(seq id no:15)。如图24a和图24b中所示,蛋白a纯化的由expicho瞬时表达产生的p-0841比由相同产生和纯化过程产生的p-0840显示出显著更少的低分子量杂质(3%对比16%)。对于p-0803和p-0880(seq id no:177、175和141)观察到类似的杂质含量差异(11%对比2.7%;图24c和图24d),它们的接头分别是(g3s)2和(g4s)3,并且其他序列相同。
[0384]
虽然p-0841和p-0880中稍长的接头与它们各自的含较短接头的对应物相比导致改进的纯度,但对il-2部分的生物活性的影响极小或略微增强,由细胞毒性淋巴细胞上的pstat5刺激效力例示(图25)。由于对融合蛋白的可开发性谱的有利影响,因此较长的接头比较短的接头更优选,而不会引起其它负面影响。
[0385]
构建了一些具有经由(g4s)3接头融合到含knob的异源二聚体重链的c末端的il-2变体的p-0795融合蛋白p-0880、p-0882(seq id no:176、175和141)和p-0885(seq id no:179、175和141)。如图22c中所示,与单独的hpd1抗体相比,在具有较长接头的il-2变体hupd-1抗体融合蛋白中,与细胞表面表达的pd-1的结合没有改变。在离体功能测定中进一步测试了它们,以研究il-2在cd8 t细胞和nk细胞中刺激pstat5和诱导ki67表达方面的效力(图26)。这三种构建体都包含消除il-2rα的突变p65r,而p-0882和p-0885分别含有另外的l19h和l19q突变,以调节整体效力。野生型il-2对应物p-0849被包括在测定中用于比较。在表14中总结了离体功能活性。与p-0880相比,通过p-0885和p-0882的效力减弱水平在评估的细胞亚群中遵循相同的趋势,并且与观察到的p-0759和p-0731对比p-0704(各自的fc融合蛋白;图15a和图15b),以及p-0786和p-0783对比p-0782(各自的小鼠pd1抗体融合蛋白;图19)的降低的水平一致。如预期的,野生型il-2融合体显示出与p-0880相当的对cd8 t细胞和nk细胞的活性。
[0386]
表14
[0387]
il-2变体人类pd-1抗体融合蛋白的活性
[0388][0389]
实施例14
[0390]
il-2变体替代小鼠pd-1抗体融合蛋白在c57bl6小鼠中的药效学作用
[0391]
在c57bl6小鼠中单次注射后评估il-2变体小鼠pd-1抗体融合蛋白的药效学作用。在研究之前,从charles river实验室接收7周龄的雌性c57bl6小鼠,并在机构内适应至少7天。媒介物和单次给药的每种il-2小鼠pd-1抗体融合蛋白在时间0时腹膜内施用至小鼠。注射后第3天、第5天、第7天和第10天抽取血液样品。每组包括5只小鼠。肝素处理的全血用于实施例10中描述的免疫表型分析。
[0392]
p-0782包含消除il-2rα结合的il-2p65r部分,p-0838包含降低il-2rα结合的il-2p65q部分,而p-0837含有野生型il-2。p-0781,含有与il-2rα结合完全丧失的基准il-2变体(seq id no:188)的对应小鼠pd-1抗体融合蛋白,被包括在内用于比较。
[0393]
在以2mg/kg单次注射后,对于cd8细胞和nk细胞测试的所有化合物,cd8细胞和nk
细胞上的ki67刺激达到最大水平(图27a-27b)。对于每种化合物,cd8 t细胞上的峰值ki67表达信号达到最大水平并在第3天达到峰值。对于p-0782、p-0838和基准p-0781,信号持续到第7天,并在第10天减弱。相比之下,对于野生型p-0837,ki67信号以加快的速率减弱(图27a)。对于测试的所有化合物,在nk细胞上观察到相似的ki67诱导(图27b)。
[0394]
引人注目的是,cd8细胞和nk细胞扩增在测试的化合物之间显示出巨大的差异。具有消除il-2rα结合的突变的p-0782显示出cd8 t细胞(图27c)和nk细胞(图27d)的强烈扩增。两个淋巴细胞亚群的扩增在第3天开始,持续并在第7天达到峰值,其中cd8 t细胞增加了68倍并且nk细胞数量增加了182倍。含有il-2rα结合能力降低的突变的p-0838显示出与wt抗体融合体相似或稍强的cd8细胞和nk细胞扩增。对于基准p-0781,与p-0780和p-0838相比,两个淋巴细胞亚群的扩增都是中等的。形成鲜明对比的是,野生型p-0837对两个淋巴细胞亚群的细胞扩增在第5天达到峰值,伴随显著降低的最大信号(cd8 t细胞增加3.9倍并且nk细胞增加6.8倍;图27c和图27d)。
[0395]
可能的是,消除cd25结合的突变可以提供降低cd25吸收效应的优势,并因此增加il-2rβγ的可用性。富集的受体占据引发强烈的细胞毒性细胞扩增。具有残留的cd25结合活性的突变体可能仍然具有吸收效应,从而导致与野生型相似的对cd8细胞和nk细胞的活性。总之,与p-0838和p-0837相比,p-0782显示出截然不同的细胞扩增谱。与测试的任何化合物相比,p-0782展示出cd8 t细胞和nk细胞两者的明显的增殖和扩增,并且高于基准化合物p-0781。作为il-2rβγ选择性全激动剂,由于增强的选择性和降低的cd25吸收,因此p-0782和p-0781可以增强cd8 效应t细胞和nk细胞的明显的体内响应。尽管与野生型相比,p-0838没有显示出强的cd8细胞和nk细胞扩增,但引入的降低与il-2rα(cd25)结合能力的突变预期在降低vls方面提供益处。此外,残留的免疫调节性treg响应可以提供免疫平衡,以提高全身耐受性,并确保免疫平衡不会过度偏向细胞毒性效应细胞。treg响应可以精细调节,以免于遭受肿瘤杀伤功效,但足够强以维持外周耐受性。
[0396]
还测试了带有il-2变体的双功能pd1抗体融合蛋白的药效学,所述il-2变体除了含有消除与il-2rα的结合能力的突变之外,还含有降低il-2rβγ相互作用的突变。p-0786和p-0783两者都是p-0782的il-2效力减弱的对应物,分别引入了不同的调节il-2rβ的突变l19q和l19h。图19c和图19d显示了这三种化合物在刺激ki67表达方面的体外效力差异。在图28和图29中示出了p-0786和p-0783在两种不同剂量水平对cd8 细胞和nk细胞的增殖和扩增的作用。如图28a中所示,较低效力的化合物p-0786在第5天诱导了cd8 t细胞上的峰值ki67信号,而不是对野生型p-0837观察到的第3天。p-0783和p-0837两者使nk细胞上的ki67增加最大化(图28b),这与nk细胞比cd8 t细胞对il-2更有响应性的概念一致。
[0397]
与野生型融合体相比,减弱的il-2变体的pd1抗体融合体的药效学作用明显改进。图28c和图28d展示了与野生型相比,p-0786对细胞扩增的明显延长和增强的剂量响应效应。cd8 t细胞和nk细胞扩增的增加被延迟但持续且持久。来自2mg/kg剂量组的响应在第7天达到峰值,并且在第10天没有返回到基线,而来自5mg/kg剂量组的响应急剧且连续增加,在给药后第10天没有达到峰值。相反,野生型融合体组的cd8细胞和nk细胞扩增是边缘性的,在第5天达到峰值,并在第7天返回到基线(图28c和图28d)。
[0398]
包含甚至更弱的il-2激动剂的p-0783显示出与p-0786相似的延迟但持续且持久的以剂量依赖性方式诱导cd8 细胞和nk细胞的ki67表达(图29a和图29b)和扩增(图29c和
图29d)的效应。对于每种化合物,细胞数量达到峰值的日期和细胞数量增加的变化倍数总结于表15中。
[0399]
表15处理后相对于基线的峰值外周细胞数量和变化倍数
[0400][0401]
此外,如图30中展示的,效力水平和相应的细胞毒性淋巴细胞扩增与由小鼠体重减轻反映的毒性相关。作为il-2rβγ选择性全激动剂,p-0782引起cd8 t细胞和nk细胞两者数量的明显增加,并导致最大的体重减轻;减弱的激动剂p-0786和p-0783在体内显示出改进的耐受性。在耐受性方面p-0783比p-0786稍有优势,这与p-0783是比p-0786更弱的激动剂的事实一致。
[0402]
总之,p-0782在使cd8 t细胞和nk细胞增殖和扩增方面展示出强大的药效学作用。p-0786和p-0783显示出较弱但更持续的信号。这三种化合物的效力排序在离体和体内之间大体上一致。此外,与完全激动剂p-0782相比,效力减弱的化合物p-0786和p-0783在体内显示出改进的药效学和耐受性。
[0403]
实施例15
[0404]
pd1抗体il-2变体融合蛋白在同基因(syngeneic)小鼠肿瘤模型中的体内功效
[0405]
在皮下b16f10黑素瘤小鼠肿瘤模型中测试了il-2变体小鼠pd-1抗体融合蛋白的抗肿瘤功效。雌性c57bl/6小鼠(7周)在4-7天适应后按体重随机分到处理组中(n=10/组)。第3代的b16f10细胞(5
×
105个细胞/小鼠)在第-1天皮下(s.c.)接种到小鼠的右肋腹。小鼠在第0天、第7天和第14天三次腹膜内(i.p.)施用测试化合物(q7d)。密切监测所有小鼠并每周三次测量体重。使用标准卡尺每周三次测量肿瘤,肿瘤尺寸通过标准公式长度
×
(宽度)w2×
0.5以mm3计算。当肿瘤尺寸超过限值1500mm3时,对小鼠实施安乐死。
[0406]
三种抗体融合蛋白p-0838、p-0790和p-0787以3mg/kg和两次q7d剂量给药。所有三种融合蛋白都含有il-2p65q突变以削弱与il-2rα的结合;p-0790和p-0787分别包含另外的l19q和l19h突变以进一步降低il-2rβγ活性,从而调节整体效力。如图31a中展示的,所有化合物都显示出强的单剂抗肿瘤功效,其中p-0787、p-0790和p-0838的肿瘤生长抑制分别为78%、64%和57%。肿瘤抑制功效的水平与从p-0838到p-0790和到p-0787的体外效力减弱相关。
[0407]
类似于在图30中观察到的,图31b描绘了全il-2激动剂p-0838具有最早和最高的毒性,如由最大体重减轻反映的;并且减弱的激动剂p-0790和p-0787在体内显示出改进的耐受性。在耐受性方面p-0787比p-0790具有一些优势,这与p-0783是比p-0786更弱的激动剂的事实一致。总体上,数据支持il-2rβγ选择性且减弱的突变体展示出良好的肿瘤杀伤功效和改进的耐受性。
[0408]
对于p-0787,进一步研究了剂量对体内肿瘤抑制和耐受性的作用。如在图32a中观察到的,随着剂量从3mg/kg增加到5mg/kg,p-0787显示出相似的有效抗肿瘤效果。剂量升高
并没有产生明显的体重减轻(图32b),表明弱激动剂有助于高剂量和增加耐受性。
[0409]
对于p-0782和p-0786以1.5mg/kg和2次q7d剂量给药,也观察到强的肿瘤生长抑制(图33)。在b16f10同基因模型中,替代小鼠pd-1抗体p-0722没有显示出抗肿瘤效果,而p-0782和p-0786显示出相当的较强的肿瘤生长抑制,尽管p-0786是p-0782的减弱的对应物。
[0410]
最后,在小鼠b16f10肺转移模型中测试了il-2变体抗体融合蛋白p-0790。简言之,将3
×
105个小鼠黑素瘤细胞静脉内注射到雌性b57bl6小鼠(10-12周龄)中。在次日(第1天)经由腹膜内注射开始三次q7d处理。处理组(n=5只/组)包括以0.3mg/kg、1mg/kg和3mg/kg的p-0790和以3mg/kg的相应的抗体p-0722。媒介物(pbs)被包括在内作为阴性对照。在第24天,所有小鼠都被处死用于组织收获。对肺肿瘤结节进行计数,并且抗转移效果由处理组和媒介物对照之间不同数量的肿瘤结节来表示。
[0411]
p-0790是il-2l19q/p65q pd-1抗体融合蛋白,具有显著削弱的与il-2rα的结合和调节整体效力。类似地,替代小鼠pd-1抗体p-0722在抑制b16f10肿瘤细胞转移方面是无效的,而观察到p-0790对肺转移结节的剂量依赖性抑制。图34a示出了平均肺结节计数,并且图34b展示了来自每组代表性动物的肺部图片。数据表示为平均值
±
sem。
[0412]
总之,各种il-2变体小鼠pd-1抗体融合蛋白展示出强的单剂抗肿瘤作用。减弱的il-2激动剂显示出有效的肿瘤生长抑制和改进的耐受性,这允许更高的剂量以用于提高功效。
[0413]
实施例16
[0414]
选择的il-2变体pd-1抗体融合蛋白在食蟹猴中的药效学/药代动力学和安全性评价
[0415]
将评价所选择的il-2变体pd-1抗体融合蛋白在食蟹猴中的pk/pd特性和安全性。未经药物的食蟹猴将适应和训练2-3周,并随机分为每组一只猴,其后是给药前基线周。在第 1天,一个组将接受静脉内施用媒介物(pbs),并且其他组将用不同的测试化合物进行静脉内给药。
[0416]
在第-3天、第2天、第4天、第6天、第8天、第10天、第12天、第15天采集血液。从猴全血分离外周血单个核细胞(pbmc),并用于外周血treg、非调节性cd4 t细胞、cd8 t细胞、cd8 t中枢记忆细胞、cd8 效应记忆细胞、cd8 t幼稚细胞和nk细胞的facs免疫表型分析,以确定药效学。还将通过测量cd25和ki67来监测细胞活化和增殖。还将全血用于全血细胞计数(cbc),分为5部分:中性粒细胞、淋巴细胞、单核细胞、嗜酸性粒细胞和嗜碱性粒细胞。
[0417]
所选择的il-2变体pd-1抗体融合蛋白的pk特性将在食蟹猴血浆样品中通过使用小鼠抗人类il-2ab(bd pharmingen)包被96孔板以捕获融合蛋白来测量全长完整分子来评估。小鼠抗人类il-2-生物素(机构内)将用于检测,并且随后将定量测试化合物的血浆浓度。除了在第-3天、第2天、第3天、第4天、第5天、第6天、第8天、第10天、第15天采集的血浆样品之外,并且在施用选择的il-2变体pd-1抗体融合蛋白后的第1天在10分钟、1小时、4小时和8小时采集另外四份血浆样品。
[0418]
来自第-7天、第8天、第15天的血浆样品还将用于评价以下临床化学参数:天冬氨酸氨基转移酶、丙氨酸氨基转移酶、碱性磷酸酶、γ谷氨酰基转移酶、白蛋白、总胆红素、肌酐、血尿素氮和c反应蛋白。
[0419]
此外,在整个研究期间,将每周监测每只动物的体重。体温和血压将在第-1天(给
药前)和药物施用后6小时、24小时、96小时和168小时进行监测。
[0420]
本文公开的和要求保护的所有物品和方法均可鉴于本公开内容被制备和执行而无需过度实验。尽管已根据优选的实施方案描述本公开内容的物品和方法,但对于本领域技术人员将明显是,变化形式可被应用到所述物品和方法而不偏离本公开内容的精神和范围。对于本领域技术人员明显的是,所有这样的变化和等效物,无论是现存的或以后开发的,都被认为是在由所附权利要求限定的本公开内容的精神和范围之内。说明书中提及的所有专利、专利申请和出版物指示本公开内容所属领域的普通技术人员的水平。为了所有目的,所有专利、专利申请和出版物通过引用以其整体并入本文,并且其程度如同每个单独出版物单独地且具体地被指示为了任何和所有目的通过引用以其整体并入本文。本文例证地表述的本公开内容可在本文未具体地公开的任何一个或更多个要素不存在的条件下被合适地实践。因此,应理解,尽管本公开内容已通过优选的实施方案和任选的特征被具体地公开,但是本领域技术人员可寻求本文公开的概念的改变和变化形式,并且认为此类改变和变化形式在由所附的权利要求限定的本公开内容的范围内。
[0421]
序列表
[0422]
在所附的序列表中列出的核酸序列和氨基酸序列按37c.f.r.1.822中规定的使用核苷酸碱基的标准字母缩写和氨基酸的单字母编码示出。
[0423]
seq id no:1是人类il-2前体氨基酸序列。
[0424]
seq id no:2是人类il-2成熟形式天然存在的氨基酸序列。
[0425]
seq id no:3是人类il-2成熟形式野生型氨基酸序列。
[0426]
seq id no:4是包含用于改进融合蛋白可开发性谱的s125i取代的人类il-2成熟形式氨基酸序列。
[0427]
seq id no:5是人类il-2rα细胞外结构域氨基酸序列。
[0428]
seq id no:6是人类igg1-fc氨基酸序列。
[0429]
seq id no:7是具有降低/消除的效应子功能的人类igg1-fc序列。
[0430]
seq id no:8是具有降低/消除的效应子功能和延长的半衰期的人类igg1-fc序列。
[0431]
seq id no:9是具有降低/消除的效应子功能的knob-fc氨基酸序列。
[0432]
seq id no:10是具有降低/消除的效应子功能的hole-fc氨基酸序列。
[0433]
seq id no:11-30是各种肽接头序列的氨基酸序列。
[0434]
seq id no:31-66是在与il-2受体α亚基的界面处具有引入的氨基酸取代的各种il-2变体的氨基酸序列。
[0435]
seq id no:67-107是各种il-2变体fc融合蛋白的氨基酸序列。
[0436]
seq id no:108是基准il-2变体fc融合蛋白的氨基酸序列。
[0437]
seq id no:109是人类il-2rβ细胞外结构域氨基酸序列。
[0438]
seq id no:110是人类γc细胞外结构域氨基酸序列。
[0439]
seq id no:111-120是各种il-2变体的氨基酸序列。
[0440]
seq id no:121-133是各种il-2变体fc融合蛋白的氨基酸序列。
[0441]
seq id no:134是具有降低/消除的效应子功能和延长的半衰期的knob-fc氨基酸序列。
[0442]
seq id no:135是具有降低/消除的效应子功能和延长的半衰期的hole-fc氨基酸序列。
[0443]
seq id no:136-137是人源化抗fap抗体的重链和轻链的氨基酸序列。
[0444]
seq id no:138-139是人类pd-1拮抗剂抗体的重链和轻链的氨基酸序列。
[0445]
seq id no:140-141是pd-1拮抗剂抗体的重链和轻链的氨基酸序列。
[0446]
seq id no:142-143是pd-1拮抗剂抗体的重链和轻链的氨基酸序列。
[0447]
seq id no:144-145是pd-1拮抗剂抗体的重链和轻链的氨基酸序列。
[0448]
seq id no:146-147是pd-1拮抗剂抗体的重链和轻链的氨基酸序列。
[0449]
seq id no:148-149是pd-l1拮抗剂抗体的重链和轻链的氨基酸序列。
[0450]
seq id no:150-151是ctla-4拮抗剂抗体的重链和轻链的氨基酸序列。
[0451]
seq id no:152-153是cd40激动剂抗体的重链和轻链的氨基酸序列。
[0452]
seq id no:154-155是纤连蛋白拮抗剂抗体的重链和轻链的氨基酸序列。
[0453]
seq id no:156-157是cd20拮抗剂抗体的重链和轻链的氨基酸序列。
[0454]
seq id no:158-159是her-2/neu拮抗剂抗体的重链和轻链的氨基酸序列。
[0455]
seq id no:160-161是egfr拮抗剂抗体的重链和轻链的氨基酸序列。
[0456]
seq id no:162是具有降低/消除的fc效应子功能的人类igg1ch1ch2ch3结构域序列的氨基酸序列。
[0457]
seq id no:163是具有降低/消除的fc效应子功能的人类igg1
[0458]
ch1ch2ch3结构域knob链序列的氨基酸序列。
[0459]
seq id no:164是具有降低/消除的fc效应子功能的人类igg1
[0460]
ch1ch2ch3结构域hole链序列的氨基酸序列。
[0461]
seq id no:165-169是各种il-2变体抗体融合蛋白的氨基酸序列。
[0462]
seq id no:170是人类il-2受体αsushi结构域氨基酸序列。
[0463]
seq id no:171-174是il-2和il-2rsushi fc融合蛋白的氨基酸序列。
[0464]
seq id no:175-181是各种il-2变体人类pd-1拮抗剂抗体融合蛋白的knob链的氨基酸序列。
[0465]
seq id no:182-184是基准il-2变体抗体融合蛋白的氨基酸序列。
[0466]
seq id no:185-187是具有异源二聚体重链的替代抗小鼠pd-1抗体的氨基酸序列。
[0467]
seq id no:188是基准il-2变体的氨基酸序列。
[0468]
seq id no:189-191是各种il-2变体人类pd-1拮抗剂抗体融合蛋白的knob链的氨基酸序列。
[0469]
序列表
[0470]
人类il-2前体序列
[0471]
myrmqllscialslalvtnsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfcqsiistlt(seq id no:1)
[0472]
人类il-2成熟形式天然存在的序列
[0473]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkplee
vlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfcqsiistlt(seq id no:2)
[0474]
人类il-2成熟形式野生型序列
[0475]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfsqsiistlt(seq id no:3)
[0476]
人类il-2s125i变体序列
[0477]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:4)
[0478]
人类il-2rα(cd25)细胞外结构域序列
[0479]
elcdddppeiphatfkamaykegtmlnceckrgfrriksgslymlctgnsshsswdnqcqctssatrnttkqvtpqpeeqkerkttemqspmqpvdqaslpghcrepppweneateriyhfvvgqmvyyqcvqgyralhrgpaesvckmthgktrwtqpqlictgemetsqfpgeekpqaspegrpesetsclvtttdfqiqtemaatmetsiftteyq(seq id no:5)
[0480]
人类igg1-fc
[0481]
dkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seq id no:6)
[0482]
具有降低/消除的效应子功能的人类igg1-fc
[0483]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seq id no:7)
[0484]
具有降低/消除的效应子功能和延长的半衰期的人类igg1-fc
[0485]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhahytqkslslspg(seq id no:8)
[0486]
具有降低/消除的效应子功能的人类igg knob-fc
[0487]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seq id no:9)
[0488]
具有降低/消除的效应子功能的人类igg hole-fc
[0489]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppcreemtknqvslscavkgfypsdiavewesngqpennykttppvldsdgsfflvskltvdksrwqqgnvfscsvmhealhnhytqks
lslspg(seq id no:10)
[0490]
肽接头序列gggsgggsgggs(seq id no:11)
[0491]
肽接头序列gggs(seq id no:12)
[0492]
肽接头序列gssggsggsggsg(seq id no:13)
[0493]
肽接头序列gssgt(seq id no:14)
[0494]
肽接头序列ggggsggggsggggs(seq id no:15)
[0495]
肽接头序列aeaaakeaaakeaaaka(seq id no:16)
[0496]
肽接头序列ggggsggggsggggsggggs(seq id no:17)
[0497]
肽接头序列gggsgggs(seq id no:18)
[0498]
肽接头序列gsgst(seq id no:19)
[0499]
肽接头序列ggss(seq id no:20)
[0500]
肽接头序列ggggs(seq id no:21)
[0501]
肽接头序列ggsg(seq id no:22)
[0502]
肽接头序列sggg(seq id no:23)
[0503]
肽接头序列gsgs(seq id no:24)
[0504]
肽接头序列gsgsgs(seq id no:25)
[0505]
肽接头序列gsgsgsgs(seq id no:26)
[0506]
肽接头序列gsgsgsgsgs(seq id no:27)
[0507]
肽接头序列gsgsgsgsgsgs(seq id no:28)
[0508]
肽接头序列ggggsggggs(seq id no:29)
[0509]
肽接头序列gsgsgsgsgsgsggs(seq id no:30)
[0510]
il-2f42a/s125i变体序列
[0511]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltakfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:31)
[0512]
il-2r38f/s125i变体序列
[0513]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:32)
[0514]
il-2r38g/s125i变体序列
[0515]
aptssstkktqlqlehllldlqmilnginnyknpkltgmltakfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:33)
[0516]
il-2r38a/s125i变体序列
[0517]
aptssstkktqlqlehllldlqmilnginnyknpkltamltfkfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:34)
[0518]
il-2t41a/s125i变体序列
[0519]
aptssstkktqlqlehllldlqmilnginnyknpkltrmlafkfympkkatelkhlqcleeelkplee
vlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:35)
[0520]
il-2t41g/s125i变体序列
[0521]
aptssstkktqlqlehllldlqmilnginnyknpkltrmlgfkfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:36)
[0522]
il-2t41v/s125i变体序列
[0523]
aptssstkktqlqlehllldlqmilnginnyknpkltrmlvfkfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:37)
[0524]
il-2f44g/s125i变体序列
[0525]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkgympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:38)
[0526]
il-2f44v/s125i变体序列
[0527]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkvympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:39)
[0528]
il-2e62a/s125i变体序列
[0529]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleealkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:40)
[0530]
il-2e62f/s125i变体序列
[0531]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeflkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:41)
[0532]
il-2e62h/s125i变体序列
[0533]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleehlkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:42)
[0534]
il-2e62l/s125i变体序列
[0535]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleellkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:43)
[0536]
il-2p65g/s125i变体序列
[0537]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkgleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:44)
[0538]
il-2p65e/s125i变体序列
[0539]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkeleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:45)
[0540]
il-2p65h/s125i变体序列
[0541]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkhleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:46)
[0542]
il-2p65r/s125i变体序列
[0543]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:47)
[0544]
il-2p65a/s125i变体序列
[0545]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkaleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:48)
[0546]
il-2p65k/s125i变体序列
[0547]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkkleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:49)
[0548]
il-2p65n/s125i变体序列
[0549]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelknleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:50)
[0550]
il-2p65q/s125i变体序列
[0551]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkqleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:51)
[0552]
il-2e68a/s125i变体序列
[0553]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkpleavlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:52)
[0554]
il-2e68f/s125i变体序列
[0555]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkplefvlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:53)
[0556]
il-2e68h/s125i变体序列
[0557]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkplehvlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:54)
[0558]
il-2e68l/s125i变体序列
[0559]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkplelvlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:55)
[0560]
il-2e68p/s125i变体序列
[0561]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkplepvlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:56)
[0562]
il-2y107g/s125i变体序列
[0563]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkvympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmcegadetativeflnrwitfiqsiistlt(seq id no:57)
[0564]
il-2y107h/s125i变体序列
[0565]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkvympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmcehadetativeflnrwitfiqsiistlt(seq id no:58)
[0566]
il-2y107l/s125i变体序列
[0567]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkvympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceladetativeflnrwitfiqsiistlt(seq id no:59)
[0568]
il-2y107v/s125i变体序列
[0569]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkvympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmcevadetativeflnrwitfiqsiistlt(seq id no:60)
[0570]
il-2f42a/e62f/s125i变体序列
[0571]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltakfympkkatelkhlqcleeflkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:61)
[0572]
il-2f42a/e62a/s125i变体序列
[0573]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltakfympkkatelkhlqcleealkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:62)
[0574]
il-2f42a/e62h/s125i变体序列
[0575]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltakfympkkatelkhlqcleehlkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:63)
[0576]
il-2f42a/p65h/s125i变体序列
[0577]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltakfympkkatelkhlqcleeelkhleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:
64)
[0578]
il-2f42a/p65r/s125i变体序列
[0579]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltakfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:65)
[0580]
il-2f42a/p65a/s125i变体序列
[0581]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltakfympkkatelkhlqcleeelkaleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:66)
[0582]
p-0250
[0583]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfsqsiistlt(seq id no:67)
[0584]
p-0531
[0585]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:68)
[0586]
p-0613
[0587]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltakfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:69)
[0588]
p-0614
[0589]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltfmltfkfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:70)
[0590]
p-0615
[0591]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnak
id no:76)
[0602]
p-0607
[0603]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkvympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:77)
[0604]
p-0624
[0605]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleealkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:78)
[0606]
p-0625
[0607]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeflkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:79)
[0608]
p-0626
[0609]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleehlkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:80)
[0610]
p-0627
[0611]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleellkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:81)
[0612]
p-0608
[0613]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvs
ltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkgleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:82)
[0614]
p-0633
[0615]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkeleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:83)
[0616]
p-0634
[0617]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkhleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:84)
[0618]
p-0635
[0619]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:85)
[0620]
p-0628
[0621]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkpleavlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:86)
[0622]
p-0629
[0623]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkplefvlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:87)
[0624]
p-0630
[0625]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkplehvlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:88)
[0626]
p-0631
[0627]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkplelvlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:89)
[0628]
p-0632
[0629]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkplepvlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:90)
[0630]
p-0609
[0631]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkvympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmcegadetativeflnrwitfiqsiistlt(seq id no:91)
[0632]
p-0610
[0633]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkvympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmcehadetativeflnrwitfiqsiistlt(seq id no:92)
[0634]
p-0611
[0635]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqks
lslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkvympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceladetativeflnrwitfiqsiistlt(seq id no:93)
[0636]
p-0612
[0637]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkvympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmcevadetativeflnrwitfiqsiistlt(seq id no:94)
[0638]
p-0551
[0639]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltakfampkkatelkhlqcleeelkpleevlngaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:95)
[0640]
p-0704knob链
[0641]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:96)
[0642]
p-0706knob链
[0643]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkaleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:97)
[0644]
p-0707knob链
[0645]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkkleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:98)
[0646]
p-0708knob链
[0647]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelknleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:99)
[0648]
p-0709knob链
[0649]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkqleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:100)
[0650]
p-0702knob链
[0651]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltakfympkkatelkhlqcleeflkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:101)
[0652]
p-0766knob链
[0653]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltakfympkkatelkhlqcleealkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:102)
[0654]
p-0767knob链
[0655]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltakfympkkatelkhlqcleehlkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:103)
[0656]
p-0703knob链
[0657]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltakfympkkatelkhlqcleee
lkhleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:104)
[0658]
p-0705knob链
[0659]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltakfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:105)
[0660]
p-0765knob链
[0661]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltakfympkkatelkhlqcleeelkaleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:106)
[0662]
p-0689knob链
[0663]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:107)
[0664]
基准knob链
[0665]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltakfampkkatelkhlqcleeelkpleevlngaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:108)
[0666]
人类il-2rβ(cd122)细胞外结构域序列
[0667]
avngtsqftcfynsraniscvwsqdgalqdtscqvhawpdrrrwnqtcellpvsqaswacnlilgapdsqklttvdivtlrvlcregvrwrvmaiqdfkpfenlrlmapislqvvhvethrcnisweisqashyferhlefeartlspghtweeaplltlkqkqewicletltpdtqyefqvrvkplqgefttwspwsqplafrtkpaalgkdt(seq id no:109)
[0668]
人类共用亚基gammaγc(cd132)细胞外结构域序列
[0669]
lnttiltpngnedttadfflttmptdslsvstlplpevqcfvfnveymnctwnsssepqptnltlhywyknsdndkvqkcshylfseeitsgcqlqkkeihlyqtfvvqlqdpreprrqatqmlklqnlvipwapenltlhklsesqlelnwnnrflnhclehlvqyrtdwdhswteqsvdyrhkfslpsvdgqkrytfrvrsrfnplcgsaqhwsewsh
pihwgsntskenpflfalea(seq id no:110)
[0670]
il-2l19h/p65r/s125i变体序列
[0671]
aptssstkktqlqlehllhdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:111)
[0672]
il-2l19q/p65r/s125i变体序列
[0673]
aptssstkktqlqlehllqdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:112)
[0674]
il-2l19y/p65r/s125i变体序列
[0675]
aptssstkktqlqlehllydlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:113)
[0676]
il-2l19h/p65q/s125i变体序列
[0677]
aptssstkktqlqlehllhdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkqleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:114)
[0678]
il-2l19h/p65h/s125i变体序列
[0679]
aptssstkktqlqlehllhdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkhleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:115)
[0680]
il-2l19h/p65n/s125i变体序列
[0681]
aptssstkktqlqlehllhdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelknleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:116)
[0682]
il-2l19q/p65q/s125i变体序列
[0683]
aptssstkktqlqlehllqdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkqleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:117)
[0684]
il-2l19q/p65h/s125i变体序列
[0685]
aptssstkktqlqlehllqdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkhleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:118)
[0686]
il-2l19q/p65n/s125i变体序列
[0687]
aptssstkktqlqlehllqdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelknleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:119)
[0688]
il-2p65r/s125i/q126e变体序列
[0689]
aptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrlee
vlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiesiistlt(seq id no:120)
[0690]
p-0731knob链
[0691]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllhdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:121)
[0692]
p-0759knob链
[0693]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllqdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:122)
[0694]
p-0761knob链
[0695]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllydlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:123)
[0696]
p-0811knob链
[0697]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllhdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkqleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:124)
[0698]
p-0812knob链
[0699]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllhdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkhleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:125)
[0700]
p-0813knob链
[0701]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnak
id no:131)
[0712]
p-0760
[0713]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllqdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:132)
[0714]
p-0762
[0715]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllydlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:133)
[0716]
具有延长的体内半衰期的knob-fc
[0717]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhahytqkslslspg(seq id no:134)
[0718]
具有延长的体内半衰期的hole-fc
[0719]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppcreemtknqvslscavkgfypsdiavewesngqpennykttppvldsdgsfflvskltvdksrwqqgnvfscsvmhealhahytqkslslspg(seq id no:135)
[0720]
人源化抗fap抗体重链
[0721]
qvqlvqsgaevkkpgasvkvsckasgytfteniihwvrqapgqglewmgwfhpgsgsikyaqkfqgrvtmtadkststvymelsslrsedtavyycarhggtgrgamdywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seq id no:136)
[0722]
人源化抗fap抗体κ轻链
[0723]
diqmtqspsslsasvgdrvtitcrasrsistsaysymhwyqqkpgkapklliylasnlesgvpsrfsgsgsgtdftltisslqpedfatyycqhsrelpytfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec(seq id no:137)
[0724]
人类pd-1拮抗剂抗体重链
[0725]
evqlvqsgaevkkpgasvkvsckasgyrftsygiswvrqapgqglewmgwisayngntnyaqklqgrvtmttdtstntaymelrslrsddtavyycardadyssgsgywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seq id no:138)
[0726]
人类pd-1拮抗剂抗体lλ
[0727]
syeltqppsvsvspgqtaritcsgdalpkqyaywyqqkpgqapvmviykdterpsgiperfsgsssgtkvtltisgvqaedeadyycqsadnsityrvfgggtkvtvlgqpkaapsvtlfppsseelqankatlvclisdfypgavtvawkadsspvkagvetttpskqsnnkyaassylsltpeqwkshrsyscqvthegstvektvaptecs(seq id no:139)
[0728]
人源化pd-1拮抗剂抗体-hc
[0729]
evqlvesggglvkpggslrlscaasgftfssydmswvrqapgkglewvatisgggsytyypdsvkgrftisrdnaknslylqmnslraedtavyycaspdssgvaywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seq id no:140)
[0730]
人源化pd-1拮抗剂抗体-lκ
[0731]
divmtqsplslpvtpgepasitckasqdvetvvawylqkpgqsprlliywastrhtgvpdrfsgsgsgtdftlkisrveaedvgvyycqqysrypwtfgqgtkleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec(seq id no:141)
[0732]
人源化pd-1拮抗剂抗体-hc
[0733]
qgqlvqsgaevkkpgasvkvsckasgytftdyemhwvrqapgqglewmgviesetggtaynqkfkgrakitadkststaymelsslrsedtavyyctregittvattyywyfdvwgqgttvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk(seq id no:142)
[0734]
人源化pd-1拮抗剂抗体-lκ
[0735]
dvvmtqsplslpvtlgqpasiscrssqsivhsngntylewylqkpgqspqlliykvsnrfsgvpdrfsgsgsgtdftlkisrveaedvgvyycfqgshvpltfgqgtkleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec(seq id no:143)
[0736]
人源化pd-1拮抗剂抗体-hc
[0737]
qvqlvqsgvevkkpgasvkvsckasgytftnyymywvrqapgqglewmgginpsnggtnfnekfknrvtlttdsstttaymelkslqfddtavyycarrdyrfdmgfdywgqgttvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk(seq id no:144)
[0738]
人源化pd-1拮抗剂抗体-lκ
[0739]
eivltqspatlslspgeratlscraskgvstsgysylhwyqqkpgqaprlliylasylesgvparfsgsgsgtdftltisslepedfavyycqhsrdlpltfgggtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec(seq id no:145)
[0740]
human pd-1拮抗剂抗体-hc
[0741]
qvqlvesgggvvqpgrslrldckasgitfsnsgmhwvrqapgkglewvaviwydgskryyadsvkgrftisrdnskntlflqmnslraedtavyycatnddywgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtktytcnvdhkpsntkvdkrveskygppcppcpapeflggpsvflfppkpkdtlmisrtpevtcvvvdvsqedpevqfnwyvdgvevhnaktkpreeqfnstyrvvsvltvlhqdwlngkeykckvsnkglpssiektiskakgqprepqvytlppsqeemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflysrltvdksrwqegnvfscsvmhealhnhytqkslslslgk(seq id no:146)
[0742]
人类pd-1拮抗剂抗体-lκ
[0743]
eivltqspatlslspgeratlscrasqsvssylawyqqkpgqaprlliydasnratgiparfsgsgsgtdftltisslepedfavyycqqssnwprtfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec seq id no:147)
[0744]
人源化pd-l1拮抗剂抗体-hc
[0745]
evqlvesggglvqpggslrlscaasgftfsdswihwvrqapgkglewvawispyggstyyadsvkgrftisadtskntaylqmnslraedtavyycarrhwpggfdywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqyastyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk(seq id no:148)
[0746]
人源化pd-l1拮抗剂抗体-lκ
[0747]
diqmtqspsslsasvgdrvtitcrasqdvstavawyqqkpgkapklliysasflysgvpsrfsgsgsgtdftltisslqpedfatyycqqylyhpatfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec(seq id no:149)
[0748]
人类ctla-4拮抗剂抗体-hc
[0749]
qvqlvesgggvvqpgrslrlscaasgftfssytmhwvrqapgkglewvtfisydgnnkyyadsvkgrftisrdnskntlylqmnslraedtaiyycartgwlgpfdywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkrvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk(seq id no:150)
[0750]
人类ctla-4拮抗剂抗体-lκ
[0751]
eivltqspgtlslspgeratlscrasqsvgssylawyqqkpgqaprlliygafsratgipdrfsgsgsgtdftltisrlepedfavyycqqygsspwtfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec(seq id no:151)
[0752]
人类cd40激动剂抗体-hc
[0753]
qvqlvqsgaevkkpgasvkvsckasgytftgyymhwvrqapgqglewmgwinpdsggtnyaqkfqgrvtmtrdtsistaymelnrlrsddtavyycardqplgyctngvcsyfdywgqgtlvtvssastkgpsvfplapcsrstsestaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssnfgtqtytcnvdhkpsntkvdktverkccvecppcpappvagpsvflfppkpkdtlmisrtpevtcvvvdvshedpevqfnwyvdgvevhnaktkpreeqfnstfrvvsvltvvhqdwlngkeykckvsnkglpapiektisktkgqprepqvytlppsreemtknqvsltclvkgfypsdisvewesngqpennykttppmldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk(seq id no:152)
[0754]
人类cd40激动剂抗体-lκ
[0755]
diqmtqspssvsasvgdrvtitcrasqgiyswlawyqqkpgkapnlliytastlqsgvpsrfsgsgsgtdftltisslqpedfatyycqqanifpltfgggtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec(seq id no:153)
[0756]
人源化抗纤连蛋白抗体-hc
[0757]
evqllesggglvqpggslrlscaasgftfssfsmswvrqapgkglewvssisgssgttyyadsvkgrftisrdskntlylqmnslraedtavyycakpfpyfdywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkrvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk(seq id no:154)
[0758]
人源化抗纤连蛋白抗体-lκ
[0759]
eivltqspgtlslspgeratlscrasqsvsssflawyqqkpgqaprlliyyassratgipdrfsgsgsgtdftltisrlepedfavyycqqtgripptfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec(seq id no:155)
[0760]
嵌合抗cd20抗体-hc
[0761]
qvqlqqpgaelvkpgasvkmsckasgytftsynmhwvkqtpgrglewigaiypgngdtsynqkfkgkatltadkssstaymqlssltsedsavyycarstyyggdwyfnvwgagttvtvsaastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkaepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk(seq id no:156)嵌合抗cd20抗体-lκ
[0762]
qivlsqspailsaspgekvtmtcrasssvsyihwfqqkpgsspkpwiyatsnlasgvpvrfsgsgsgtsysltisrveaedaatyycqqwtsnpptfgggtkleikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec(seq id no:157)
[0763]
人源化抗her2抗体-hc
[0764]
evqlvesggglvqpggslrlscaasgfnikdtyihwvrqapgkglewvariyptngytryadsvkgrftisadtskntaylqmnslraedtavyycsrwggdgfyamdywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsreemtknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk(seq id no:158)
[0765]
人源化抗her2抗体-lκ
[0766]
diqmtqspsslsasvgdrvtitcrasqdvntavawyqqkpgkapklliysasflysgvpsrfsgsrsgtdftltisslqpedfatyycqqhyttpptfgqgtkveikrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec(seq id no:159)
[0767]
嵌合抗egfr抗体-hc
[0768]
qvqlkqsgpglvqpsqslsitctvsgfsltnygvhwvrqspgkglewlgviwsggntdyntpftsrlsinkdnsksqvffkmnslqsndtaiyycaraltyydyefaywgqgtlvtvsaastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapellggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgk(seq id no:160)
[0769]
嵌合抗egfr抗体-lκ
[0770]
dilltqspvilsvspgervsfscrasqsigtnihwyqqrtngsprllikyasesisgipsrfsgsgsgtdftlsinsvesediadyycqqnnnwpttfgagtklelkrtvaapsvfifppsdeqlksgtasvvcllnnfypreakvqwkvdnalqsgnsqesvteqdskdstyslsstltlskadyekhkvyacevthqglsspvtksfnrgec(seq id no:161)
[0771]
具有降低/消除的效应子功能的人类igg1 ch1-ch2-ch3结构域
[0772]
astkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssv
vtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seq id no:162)
[0773]
具有降低/消除的效应子功能的人类igg1 ch1-ch2-ch3结构域knob链
[0774]
astkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seq id no:163)
[0775]
具有降低/消除的效应子功能的人类igg1 ch1-ch2-ch3结构域hole链
[0776]
astkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppcreemtknqvslscavkgfypsdiavewesngqpennykttppvldsdgsfflvskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seq id no:164)
[0777]
人源化pd-1拮抗剂抗体-hc-il-2变体
[0778]
evqlvesggglvkpggslrlscaasgftfssydmswvrqapgkglewvatisgggsytyypdsvkgrftisrdnaknslylqmnslraedtavyycaspdssgvaywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhahytqkslslspggggsgggsaptssstkktqlqlehllhdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:165)
[0779]
人源化pd-1拮抗剂抗体-hc-il-2变体knob链
[0780]
evqlvesggglvkpggslrlscaasgftfssydmswvrqapgkglewvatisgggsytyypdsvkgrftisrdnaknslylqmnslraedtavyycaspdssgvaywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:166)
[0781]
人源化pd-1拮抗剂抗体-hc-il-2变体knob链
[0782]
evqlvesggglvkpggslrlscaasgftfssydmswvrqapgkglewvatisgggsytyypdsvkgrftisrdnaknslylqmnslraedtavyycaspdssgvaywgqgtlvtvssastkgpsvfplapsskstsggtaalgc
lvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkqleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:167)
[0783]
人源化pd-1拮抗剂抗体-hc-il-2变体knob链
[0784]
evqlvesggglvkpggslrlscaasgftfssydmswvrqapgkglewvatisgggsytyypdsvkgrftisrdnaknslylqmnslraedtavyycaspdssgvaywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvctlppsreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspggggsgggsaptssstkktqlqlehllqdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkqleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:168)
[0785]
人源化pd-1拮抗剂抗体-igg1-hc hole链
[0786]
evqlvesggglvkpggslrlscaasgftfssydmswvrqapgkglewvatisgggsytyypdsvkgrftisrdnaknslylqmnslraedtavyycaspdssgvaywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppcreemtknqvslscavkgfypsdiavewesngqpennykttppvldsdgsfflvskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seq id no:169)
[0787]
人类il-2rαsushi结构域序列
[0788]
elcdddppeiphatfkamaykegtmlnceckrgfrriksgslymlctgnsshsswdnqcqctssatrnttkqvtpqpeeqkerkttemqspmqpvdqaslpghcrepppweneateriyhfvvgqmvyyqcvqgyralhrgpaesvckmthgktrwtqpqlictg(seq id no:170)
[0789]
p-0327
[0790]
dkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppsrdeltknqvsltclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgggggsggggsggggselcdddppeiphatfkamaykegtmlnceckrgfrriksgslymlctgnsshsswdnqcqctssatrnttkqvtpqpeeqkerkttemqspmqpvdqaslpghcrepppweneateriyhfvvgqmvyyqcvqgyralhrgpaesvckmthgktrwtqpqlictgggggsggggsggggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkpleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfsqsiistlt(seq id no:171)
[0791]
p-0422
no:176)
[0801]
人源化pd-1拮抗剂抗体-hc-il-2变体knob链
[0802]
evqlvesggglvkpggslrlscaasgftfssydmswvrqapgkglewvatisgggsytyypdsvkgrftisrdnaknslylqmnslraedtavyycaspdssgvaywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppcreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgggggsggggsggggsaptssstkktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:177)
[0803]
人源化pd-1拮抗剂抗体-hc-il-2变体knob链
[0804]
evqlvesggglvkpggslrlscaasgftfssydmswvrqapgkglewvatisgggsytyypdsvkgrftisrdnaknslylqmnslraedtavyycaspdssgvaywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppcreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgggggsggggsggggsaptssstkktqlqlehllqdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkqleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:178)
[0805]
人源化pd-1拮抗剂抗体-hc-il-2变体knob链
[0806]
evqlvesggglvkpggslrlscaasgftfssydmswvrqapgkglewvatisgggsytyypdsvkgrftisrdnaknslylqmnslraedtavyycaspdssgvaywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppcreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgggggsggggsggggsaptssstkktqlqlehllqdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:179)
[0807]
人源化pd-1拮抗剂抗体-hc-il-2变体knob链
[0808]
evqlvesggglvkpggslrlscaasgftfssydmswvrqapgkglewvatisgggsytyypdsvkgrftisrdnaknslylqmnslraedtavyycaspdssgvaywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppcreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgggggsggggsggggsaptssstkktqlqlehllhdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeel
kqleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:180)
[0809]
人源化pd-1拮抗剂抗体-hc-il-2变体knob链
[0810]
evqlvesggglvkpggslrlscaasgftfssydmswvrqapgkglewvatisgggsytyypdsvkgrftisrdnaknslylqmnslraedtavyycaspdssgvaywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppcreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgggggsggggsggggsaptssstkktqlqlehllqdlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelknleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:181)
[0811]
基准pd-1拮抗剂抗体-hc-hole链
[0812]
evqllesggglvqpggslrlscaasgfsfssytmswvrqapgkglewvatisgggrdiyypdsvkgrftisrdnskntlylqmnslraedtavyycvlltgrvyfaldswgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaaggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalgapiektiskakgqprepqvctlppsrdeltknqvslscavkgfypsdiavewesngqpennykttppvldsdgsfflvskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seq id no:182)
[0813]
基准pd-1拮抗剂抗体-hc-基准il-2变体knob链
[0814]
evqllesggglvqpggslrlscaasgfsfssytmswvrqapgkglewvatisgggrdiyypdsvkgrftisrdnskntlylqmnslraedtavyycvlltgrvyfaldswgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaaggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalgapiektiskakgqprepqvytlppcrdeltknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgggggsggggsggggsapassstkktqlqlehllldlqmilnginnyknpkltrmltakfampkkatelkhlqcleeelkpleevlngaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfaqsiistlt(seq id no:183)
[0815]
基准pd-1拮抗剂抗体-lλ
[0816]
evqllesggglvqpggslrlscaasgfsfssytmswvrqapgkglewvatisgggrdiyypdsvkgrftisrdnskntlylqmnslraedtavyycvlltgrvyfaldswgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaaggpsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalgapiektiskakgqprepqvctlppsrdeltknqvslscavkgfypsdiavewesngqpennykttppvldsdgsfflvskltvdksrwqqgnvfscsvmhealhnhytqkslslspg(seq id no:184)
[0817]
替代小鼠pd-1拮抗剂抗体hc链1
[0818]
evqlqesgpglvkpsqslsltcsvtgysitssyrwnwirkfpgnrlewmgyinsagisnynpslkrrisitrdtsknqfflqvnsvttedaatyycarsdnmgttpftywgqgtlvtvssakttppsvyplapgsaaqtnsmvtlgclvkgyfpepvtvtwnsgslssgvhtfpavlqsdlytlsssvtvpsstwpsqtvtcnvahpasstkvdkkivprdcgckpcictvpevssvfifppkpkdvltitltpkvtcvvvaiskddpevqfswfvddvevhtaqtkpreeqinstfrsvselpimhqdwlngkefkcrvnsaafgapiektisktkgrpkapqvytipppkkqmakdkvsltcmitnffpeditvewqwngqpaenykntqpimktdgsyfvysklnvqksnweagntftcsvlheglhnhhtekslshspg(seq id no:185)
[0819]
替代小鼠pd-1拮抗剂抗体hc链2
[0820]
evqlqesgpglvkpsqslsltcsvtgysitssyrwnwirkfpgnrlewmgyinsagisnynpslkrrisitrdtsknqfflqvnsvttedaatyycarsdnmgttpftywgqgtlvtvssakttppsvyplapgsaaqtnsmvtlgclvkgyfpepvtvtwnsgslssgvhtfpavlqsdlytlsssvtvpsstwpsqtvtcnvahpasstkvdkkivprdcgckpcictvpevssvfifppkpkdvltitltpkvtcvvvaiskddpevqfswfvddvevhtaqtkpreeqinstfrsvselpimhqdwlngkefkcrvnsaafgapiektisktkgrpkapqvytipppkeqmakdkvsltcmitnffpeditvewqwngqpaenydntqpimdtdgsyfvysdlnvqksnweagntftcsvlheglhnhhtekslshspg(seq id no:186)
[0821]
替代小鼠pd-1拮抗剂抗体lc
[0822]
divmtqgtlpnpvpsgesvsitcrssksllysdgktylnwylqrpgqspqlliywmstrasgvsdrfsgsgsgtdftlkisgveaedvgiyycqqglefptfgggtklelkrtdaaptvsifppsseqltsggasvvcflnnfyprdinvkwkidgserqngvlnswtdqdskdstysmsstltltkdeyerhnsytceathktstspivksfnrnec(seq id no:187)
[0823]
基准il-2变体
[0824]
apassstkktqlqlehllldlqmilnginnyknpkltrmltakfampkkatelkhlqcleeelkpleevlngaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfaqsiistlt(seq id no:188)
[0825]
人源化pd-1拮抗剂抗体-hc-il-2变体knob链
[0826]
evqlvesggglvkpggslrlscaasgftfssydmswvrqapgkglewvatisgggsytyypdsvkgrftisrdnaknslylqmnslraedtavyycaspdssgvaywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppcreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgggggsggggsggggsktqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:189)
[0827]
人源化pd-1拮抗剂抗体-hc-il-2变体knob链
[0828]
evqlvesggglvkpggslrlscaasgftfssydmswvrqapgkglewvatisgggsytyypdsvkgrftisrdnaknslylqmnslraedtavyycaspdssgvaywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppcreemtknqvslwclvkgf
ypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgggggsggggsggggstqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:190)
[0829]
人源化pd-1拮抗剂抗体-hc-il-2变体knob链
[0830]
evqlvesggglvkpggslrlscaasgftfssydmswvrqapgkglewvatisgggsytyypdsvkgrftisrdnaknslylqmnslraedtavyycaspdssgvaywgqgtlvtvssastkgpsvfplapsskstsggtaalgclvkdyfpepvtvswnsgaltsgvhtfpavlqssglyslssvvtvpssslgtqtyicnvnhkpsntkvdkkvepkscdkthtcppcpapeaagapsvflfppkpkdtlmisrtpevtcvvvdvshedpevkfnwyvdgvevhnaktkpreeqynstyrvvsvltvlhqdwlngkeykckvsnkalpapiektiskakgqprepqvytlppcreemtknqvslwclvkgfypsdiavewesngqpennykttppvldsdgsfflyskltvdksrwqqgnvfscsvmhealhnhytqkslslspgggggsggggsggggsqlqlehllldlqmilnginnyknpkltrmltfkfympkkatelkhlqcleeelkrleevlnlaqsknfhlrprdlisninvivlelkgsettfmceyadetativeflnrwitfiqsiistlt(seq id no:191)。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
