1.本发明属于药物化学技术领域,具体涉及一种苯并噻唑类化合物,其药物组合物、制备方法和应用。
背景技术:
2.乙型肝炎病毒(hbv)是引起乙型肝炎(简称乙肝)的病原体。hbv感染是全球性的公共卫生问题,持续性hbv感染会导致肝硬化甚至肝癌。随着基因工程疫苗的生产和投入,乙肝疫苗的普及率逐年上升,乙肝的感染率呈下降趋势。在我国,由于乙肝病毒携带者的基数较大,因此,乙肝的防治在当前甚至未来几十年仍然是我国公共卫生的重点。
3.核苷类似物和i型干扰素这些逆转录酶抑制剂虽然可以有效降低hbv dna水平,在患者中控制乙肝病毒水平,但是由于其作用靶点为rna逆转录为dna的过程,对于hbeag和hbsag的清除无直接作用。因此核苷类似物单药治疗发生hbeag和hbsag血清学转化的概率极低,并不能真正治愈乙肝,患者需要长期甚至终身服用药物。i型干扰素的治疗疗程长、费用高,患者持久应答率也仅为10-47%,上述非特异性的抗病毒疗法的治疗策略,对乙肝患者的治疗效果不理想。
4.乙型肝炎疫苗是用于预防乙型肝炎的有效手段,常规重组乙型肝炎疫苗主要用于特异性预防新生儿和易感人群的hbv感染。新生儿乙肝疫苗免疫接种有效地预防了新发hbv感染。其中以天然结构的乙肝表面抗原(hbsag)为靶抗原。但是,这一手段仅能在未经感染的健康人体内诱导产生抗体,发挥预防效果,是一种预防性疫苗。
5.慢性hbv感染的持续状态主要是由于机体对乙肝病毒抗原的免疫耐受。而免疫预防性乙肝疫苗对已患有慢性hbv感染者无效,也无任何治疗效果。慢性hbv感染患者如不做任何治疗,据统计将有25-40%的感染者会进展为失代偿性肝硬化或者肝癌。因此,目前全世界许多学者尝试通过诱导慢性hbv感染者产生针对hbv病毒抗原的特异性免疫应答反应,通过调动机体本身的特异性免疫力,清除慢性hbv感染性肝细胞的治疗性疫苗,现有的治疗性乙肝疫苗具有某些优点,但也存在着一些问题。如dna疫苗能诱导强烈的细胞免疫和体液免疫应答,可打破特异性细胞毒t淋巴细胞(ctl)耐受,但其安全性(包括环境安全性和人体安全性)和标准化问题尚待深入研究。多表位基因疫苗或多表位多肽疫苗为多价疫苗研究提供了新的思路,但是由于mhc分子的限制性,其仅局限于表达某些特定mhc分子的患者,并且还需要克服表位疫苗免疫原性弱的固有缺点。抗原抗体复合物治疗性疫苗由于采用的是常规的铝盐佐剂,其免疫原性也具有一定的局限性。
6.目前市场上主要通过使用干扰素或者核苷类似物进行抗病毒治疗。其中核苷类似物通过抑制hbv复制过程中的逆转录酶活性从而抑制hbv产生。逆转录酶抑制剂虽然可以使患者控制乙肝病毒水平,但是成本较高,且缺乏靶向性,逆转录酶抑制剂在服用后大多通过肾脏排出,只有极少部分被肝脏器官吸收,治疗效果较差。
技术实现要素:
7.为改善上述技术问题,本发明提供了一种式(i)所示的化合物、其消旋体、立体异构体、互变异构体、同位素标记物、溶剂化物、多晶型物或它们药学上可接受的盐;
[0008][0009]
其中,r1选自h、无取代或任选被一个、两个或更多个ra取代的c
1-12
烷基、c
1-12
烷氧基;
[0010]
r2选自无取代或任选被一个、两个或更多个rb取代的c
1-12
烷基、c
6-14
芳基、5-14元杂芳基;
[0011]
r3选自无取代或任选被一个、两个或更多个rc取代的c
1-12
烷基、c
1-12
烷氧基、3-12元杂环基、5-14元杂芳基;
[0012]
每个ra、rb、rc相同或不同,彼此独立地选自卤素、c
1-12
烷基、c
1-12
烷氧基、c
6-14
芳基、5-14元杂芳基、3-12元杂环基。
[0013]
根据本发明的实施方案,r1可以选自h、c
1-6
烷氧基;
[0014]
r2可以选自c
6-10
芳基-c
1-6
烷基、c
1-6
烷基-c
6-10
芳基;
[0015]
r3可以选自卤代c
1-6
烷氧基、3-8元杂环基、5-10元杂芳基。
[0016]
根据本发明的实施方案,r1可以选自h、c
1-3
烷氧基;
[0017]
r2可以选自c
6-8
芳基-c
1-3
烷基、c
1-3
烷基-c
6-8
芳基;
[0018]
r3可以选自卤代c
1-3
烷氧基、3-6元杂环基、5-6元杂芳基。
[0019]
根据本发明的实施方案,r1可以选自h、甲氧基;
[0020]
r2可以选自苯甲基、4-异丙基苯基;
[0021]
r3可以选自呋喃基、cf3ch2o-。
[0022]
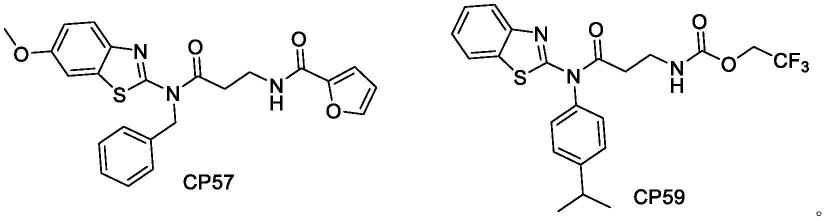
根据本发明的实施方案,式(i)所示化合物选自以下结构:
[0023][0024]
本发明还提供一种药物组合物,其包含治疗有效量的式(i)所示的化合物、其消旋体、立体异构体、互变异构体、同位素标记物、溶剂化物、多晶型物或它们药学上可接受的盐中的至少一种。
[0025]
根据本发明的实施方案,所述药物组合物经配制而通过选自以下的途径给药:口服、注射、直肠、经鼻、经肺、局部、口腔和舌下、阴道、肠胃外、皮下、肌肉内、静脉内、皮内、鞘内和硬膜外。
[0026]
根据本发明的实施方案,所述药物组合物优选以口服方式给药。
[0027]
所述口服剂型没有特别限定,可以采用本领域熟知的任意口服剂型,优选包括片剂、胶囊、混悬剂或者口服溶液等本领域已知的口服剂型。作为口服剂型时,使用的剂量标准例如为500-1500mg/天,优选用量为700-1200mg/天,优选800-1000mg/天,最优选为1000mg/天。
[0028]
根据本发明的药物组合物的用药时间可以视病情程度而定,优选至少为1个月,例如可以为1、2、3、4、5或6个月,最长可能因病情需要而终身服药。
[0029]
根据本发明的实施方案,所述药物组合物还可以包含药学上可接受的辅料,其选自包括但不限于下列辅料中的至少一种:填充剂、崩解剂、粘合剂、润滑剂、表面活性剂、矫味剂、湿润剂、ph调节剂、增溶剂或助溶剂、渗透压调节剂。本领域技术人员根据具体剂型的需要,可以容易地确定如何选择相应的辅料及其相应用量。
[0030]
根据本发明的实施方案,所述药物组合物还可以进一步含有一种或多种额外的治疗剂。本发明还提供所述式(i)所示的化合物、其消旋体、立体异构体、互变异构体、同位素标记物、溶剂化物、多晶型物或它们药学上可接受的盐中的至少一种,以及所述药物组合物在制备药物中的应用。
[0031]
根据本发明的实施方案,所述药物为治疗或预防病毒性肝炎药物。
[0032]
根据本发明的实施方案,所述病毒性肝炎包括乙型肝炎或丁型肝炎。
[0033]
本发明还提供所述式(i)所示的化合物、其消旋体、立体异构体、互变异构体、同位素标记物、溶剂化物、多晶型物或它们药学上可接受的盐,以及所述药物组合物在预防和/或治疗病毒性肝炎中的用途。
[0034]
本发明还提供一种预防或治疗病毒性肝炎的方法,包括给予患者预防或治疗有效量的式(i)所示的化合物、其消旋体、立体异构体、互变异构体、同位素标记物、溶剂化物、多晶型物或它们药学上可接受的盐中的至少一种,或者给予患者预防或治疗有效量的上述药物组合物。
[0035]
根据本发明的实施方案,所述病毒性肝炎包括乙型肝炎或丁型肝炎。
[0036]
在一些实施方案中,所述患者哺乳动物,优选是人。
[0037]
有益效果
[0038]
式(i)所示的化合物对乙型肝炎表面抗原(hbsag)和乙肝e抗原(hbeag)具有明显的抑制作用,在细胞试验和动物试验中具备降低乙型肝炎病毒(hbv)载量、hbsag和/或hbeag水平的能力,因而有望达到清除乙肝病毒的效果,由此达到乙型肝炎的治愈。
附图说明
[0039]
图1为测试例1中本发明化合物的细胞活性图。
[0040]
图2为测试例1中本发明化合物的hbeag抑制率图。
[0041]
图3为测试例1中本发明化合物的hbsag抑制率图。
[0042]
术语定义与说明
[0043]
除非另有说明,本技术说明书和权利要求书中记载的基团和术语定义,包括其作为实例的定义、示例性的定义、优选的定义、表格中记载的定义、实施例中具体化合物的定义等,可以彼此之间任意组合和结合。这样的组合和结合后的基团定义及化合物结构,应当被理解为本技术说明书和/或权利要求书记载的范围内。
[0044]
除非另有说明,本说明书和权利要求书记载的数值范围相当于至少记载了其中每一个具体的整数数值。例如,数值范围“1-12”相当于记载了数值范围“1-12”中的每一个整数数值即1、2、3、4、5、6、7、8、9、10、11、12。此外,当某些数值范围被定义为“数”时,应当理解为记载了该范围的两个端点、该范围内的每一个整数以及该范围内的每一个小数。例如,“0~10的数”应当理解为不仅记载了0、1、2、3、4、5、6、7、8、9和10的每一个整数,还至少记载了其中每一个整数分别与0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9的和。
[0045]
应当理解,本文在描述一个、两个或更多个中,“更多个”应当是指大于2,例如大于等于3的整数,例如3、4、5、6、7、8、9或10。
[0046]
术语“卤素”表示氟、氯、溴和碘。
[0047]
术语“c
1-12
烷基”应理解为表示具有1~12个碳原子的直链或支链饱和一价烃基。例如,“c
1-10
烷基”表示具有1、2、3、4、5、6、7、8、9或10个碳原子的直链和支链烷基,“c
1-8
烷基”表示具有1、2、3、4、5、6、7、或8个碳原子的直链和支链烷基,“c
1-6
烷基”表示具有1、2、3、4、5或6个碳原子的直链和支链烷基。所述烷基是例如甲基、乙基、丙基、丁基、戊基、己基、异丙基、异丁基、仲丁基、叔丁基、异戊基、2-甲基丁基、1-甲基丁基、1-乙基丙基、1,2-二甲基丙基、新戊基、1,1-二甲基丙基、4-甲基戊基、3-甲基戊基、2-甲基戊基、1-甲基戊基、2-乙基丁基、1-乙基丁基、3,3-二甲基丁基、2,2-二甲基丁基、1,1-二甲基丁基、2,3-二甲基丁基、1,3-二甲基丁基或1,2-二甲基丁基等或它们的异构体。
[0048]
术语“3-12元杂环基”是指饱和的或不饱和的非芳族的环或环系,例如,其是4-、5-、6-或7-元的单环、7-、8-、9-、10-、11-或12-元的二环(如稠环、桥环、螺环)或者三环环系,并且含有至少一个,例如1、2、3、4、5个或更多个选自o、s和n的杂原子,其中n和s还可以任选被氧化成各种氧化状态,以形成氮氧化物、-s(o)-或-s(o)
2-的状态。优选地,所述杂环基可以选自“3-10元杂环基”。术语“3-10元杂环基”意指饱和的或不饱和的非芳族的环或环系,并且含有至少一个选自o、s和n的杂原子。所述杂环基可以通过所述碳原子中的任一个或氮原子(如果存在的话)与分子的其余部分连接。所述杂环基可以包括稠合的或桥连的环以及螺环的环。特别地,所述杂环基可以包括但不限于:4元环,如氮杂环丁烷基、氧杂环丁烷基;5元环,如四氢呋喃基、二氧杂环戊烯基、吡咯烷基、咪唑烷基、吡唑烷基、吡咯啉基;或6元环,如四氢吡喃基、哌啶基、吗啉基、二噻烷基、硫代吗啉基、哌嗪基或三噻烷基;或7元环,如二氮杂环庚烷基。任选地,所述杂环基可以是苯并稠合的。所述杂环基可以是双环的,例如但不限于5,5元环,如六氢环戊并[c]吡咯-2(1h)-基环,或者5,6元双环,如六氢吡咯并[1,2-a]吡嗪-2(1h)-基环。杂环基可以是部分不饱和的,即它可以包含一个或多个双键,例如但不限于二氢呋喃基、二氢吡喃基、2,5-二氢-1h-吡咯基、4h-[1,3,4]噻二嗪基、1,2,3,5-四氢噁唑基或4h-[1,4]噻嗪基,或者,它可以是苯并稠合的,例如但不限于二氢异喹啉基。所述3-12元杂环基与其它基团相连构成本发明的化合物时,可以为3-12元杂环基上的碳原子与其它基团相连,也可以为3-12元杂环基环上杂环原子与其它基团相连。例如当3-12元杂环基选自哌嗪基时,可以为哌嗪基上的氮原子与其它基团相连。或当3-12元杂环基选自哌啶基时,可以为哌啶基环上的氮原子和其对位上的碳原子与其它基团相连。
[0049]
术语“c
6-14
芳基”应理解为优选表示具有6、7、8、9、10、11、12、13或14个碳原子的一价芳香性或部分芳香性的单环、双环或三环烃环(“c
6-14
芳基”),特别是具有6个碳原子的环(“c6芳基”),例如苯基;或联苯基,或者是具有9个碳原子的环(“c9芳基”),例如茚满基或茚
基,或者是具有10个碳原子的环(“c
10
芳基”),例如四氢化萘基、二氢萘基或萘基,或者是具有13个碳原子的环(“c
13
芳基”),例如芴基,或者是具有14个碳原子的环(“c
14
芳基”),例如蒽基。当所述c
6-14
芳基被取代时,其可以为单取代或者多取代。并且,对其取代位点没有限制,例如可以为邻位、对位或间位取代。
[0050]
术语“5-14元杂芳基”应理解为包括这样的一价单环、双环或三环芳族环系:其具有5、6、7、8、9、10、11、12、13或14个环原子,特别是5或6或9或10个碳原子,且其包含1-5个,优选1-3各独立选自n、o和s的杂原子并且,另外在每一种情况下可为苯并稠合的。“杂芳基”还指其中杂芳族环与一个或多个芳基、脂环族或杂环基环稠合的基团,其中所述连接的根基或点在杂芳族环上。当所述5-14元杂芳基与其它基团相连构成本发明的化合物时,可以为5-14元杂芳基环上的碳原子与其它基团相连,也可以为5-14元杂芳基环上的杂原子与其它基团相连。当所述5-14元杂芳基被取代时,其可以为单取代或者多取代。并且,对其取代位点没有限制,例如可以为杂芳基环上与碳原子相连的氢被取代,或者杂芳基环上与杂原子相连的氢被取代。
[0051]
术语“螺环”是指两个环共用1个成环原子的环系。
[0052]
术语“稠环”是指两个环共用2个成环原子的环系。
[0053]
术语“桥环”是指两个环共用3个以上成环原子的环系。
[0054]
除非另有说明,杂环基、杂芳基或亚杂芳基包括其所有可能的异构形式,例如其位置异构体。因此,对于一些说明性的非限制性实例,可以包括在其1-、2-、3-、4-、5-、6-、7-、8-、9-、10-、11-、12-位等(如果存在)中的1、2个或更多个位置上取代或与其他基团键合的形式,包括吡啶-2-基、亚吡啶-2-基、吡啶-3-基、亚吡啶-3-基、吡啶-4-基和亚吡啶-4-基;噻吩基或亚噻吩基包括噻吩-2-基、亚噻吩-2-基、噻吩-3-基和亚噻吩-3-基;吡唑-1-基、吡唑-3-基、吡唑-4-基、吡唑-5-基。
[0055]
在本文中,术语“药学上可接受的盐”是指由药学上可接受的无毒的酸(包括无机或有机酸)制成的盐。本发明的化合物可以是单盐、二盐或三盐,取决于在化合物的游离碱形式中存在的酸性官能团的数目。作为实例,所述酸包括乙酸、三氟乙酸、苯磺酸、苯甲酸、樟脑磺酸、柠檬酸、乙烷磺酸、富马酸、葡萄糖、谷氨酸、氢溴酸、盐酸、羟乙磺酸、乳酸、马来酸、苹果酸、杏仁酸、甲烷磺酸、粘酸、硝酸、扑酸、泛酸、磷酸、琥珀酸、硫酸、草酸、酒石酸、对甲苯磺酸等。
[0056]
病毒性肝炎
[0057]
病毒性肝炎的病原学分型,目前已被公认的有甲、乙、丙、丁、戊五种肝炎病毒,分别写作hav、hbv、hcv、hdv、hev,除乙型肝炎病毒为dna病毒外,其余均为rna病毒。
[0058]
乙型肝炎是由乙型肝炎病毒引起的以肝脏病变为主的一种传染病。临床上以食欲减退、恶心、上腹部不适、肝区痛、乏力为主要表现。部分患者可有黄疸发热和肝大伴有肝功能损害。有些患者可慢性化,甚至发展成肝硬化,少数可发展为肝癌。
[0059]
乙型病毒性肝炎的病原为乙型肝炎病毒(hbv),其为一种dna病毒,其基因组是双链、环形、不完全闭合dna。病毒最外层是病毒的外膜或衣膜,其内层为核心部分,核蛋白即是核心抗原(hbcag),不能在血清中检出。hbsag阳性者的血清在电子显微镜下可见3种颗粒,直径为22nm的圆形和丝状颗粒,还有较少的直径为42埃的球形颗粒,又称为dane氏颗粒,是完整的hbv颗粒。
[0060]
乙型肝炎的标志检测如下所述:
①
hbsag与抗-hbs:hbsag阳性示hbv目前处于感染阶段,抗-hbs为免疫保护性抗体阳性示已产生对hbv的免疫力。慢性hbsag携带者的诊断依据为无任何临床症状和体征、肝功能正常,hbsag持续阳性6个月以上者。
②
hbeag与抗-hbe:hbeag阳性为hbv活跃复制及传染性强的指标,被检血清从hbeag阳性转变为抗-hbe阳性表示疾病有缓解感染性减弱。
③
hbcag与抗-hbc:hbcag阳性提示存在完整的hbv颗粒直接反应,hbv活跃复制由于检测方法复杂临床少用。抗-hbc为hbv感染的标志,抗-hbc igm阳性提示处于感染早期,体内有病毒复制。在慢性轻度乙型肝炎和hbsag携带者中hbsag、hbeag和抗-hbc三项均阳性具有高度传染性指标难以阴转。
[0061]
在本文中,“对此有需要的个体”包括感染/携带乙型肝炎病毒或丁型肝炎病毒的个体,尤其是患有急性、慢性、重型肝炎或肝炎后肝硬化的患者,乙型肝炎表面抗原的携带者,和感染丁型肝炎的患者等。
[0062]
在本文中,“治疗有效量”或“有效量”是指在剂量下有效并且持续所需时间周期以实现期望的治疗结果的量。药物组合物的治疗有效量将取决于疾病或症状的特性和特定的药物,且可以通过本领域技术人员已知的标准临床技术确定。
[0063]
治疗结果可以包括减轻症状、延长存活、提高移动性等。治疗结果不必然是“(完全)治愈”。治疗结果也可以是预防性的。
[0064]
本技术的药物或药物组合物通过适合于待治疗疾病的任何途径给药。合适的途径包括口服、直肠、鼻、肺、局部(包括口腔和舌下)、阴道和肠胃外(包括皮下、肌肉内、静脉内、皮内、鞘内和硬膜外)等。将会理解,优选途径可根据例如接受者的状况而变化。根据本发明的药物或药物组合物的一个优点在于,它们是口服生物可利用的并且可以口服给药。
[0065]
在一个优选实施方式中,所述药物组合物经配制通过选自以下的途径给药:口服、直肠、经鼻、经肺、局部、口腔和舌下、阴道、肠胃外、皮下、肌肉内、静脉内、皮内、鞘内和硬膜外。
[0066]
在一个优选实施方式中,所述组合物经配制通过口服给药,优选为片剂或胶囊的形式。
[0067]
根据本发明的药物组合物可以用常规载体和赋形剂(其将根据通常的实践选择)配制。片剂将含有赋形剂、助流剂、填充剂、粘合剂等。水性制剂以无菌形式制备,并且当用于通过非口服给药递送时,通常是等渗的。所有制剂将任选地含有赋形剂,例如“handbook of pharmaceutical excipients”(1986)中所述的赋形剂。赋形剂包括抗坏血酸和其它抗氧化剂,螯合剂如edta,碳水化合物如葡聚糖,羟基烷基纤维素,羟基烷基甲基纤维素,硬脂酸等。制剂的ph范围为约3至约11,但通常为约7至10。在一些实施方式中,制剂的ph范围为约2至约5,但通常为约3至4。
[0068]
制剂包括适用于前述给药途径的制剂。制剂可以方便地以单位剂型存在,并且可以通过药学领域熟知的任何方法制备。技术和制剂通常在remington’spharmaceutical sciences(mack publishing co.,easton,pa)中找到。这样的方法包括使活性成分与由一种或多种辅助成分构成的载体结合的步骤。通常,通过将活性成分与液体载体或细分的固体载体或两者均匀地和紧密地结合在一起,然后根据需要使产品成形,来制备制剂。
[0069]
适用于口服给药的本技术的制剂可以作为以下形式存在:各自含有预定量活性成分的离散单元,如胶囊剂或片剂;粉末或颗粒;水性或非水性液体中的溶液或混悬液;或者
水包油液体乳剂或油包水液体乳剂。
[0070]
片剂通过任选地与一种或多种辅助成分一起压制或模制而制成。压制片剂可以通过以下来制备:在合适的机器中压制自由流动形式如粉末或颗粒的活性成分,其任选地与粘合剂、润滑剂、惰性稀释剂、防腐剂、表面活性剂或分散剂混合。模制片剂可以通过在合适的机器中模制经惰性液体稀释剂润湿的粉末状活性成分的混合物而制备。片剂可任选地包衣或刻痕,并任选地配制,以便从该片剂提供活性成分的缓释或控释。
[0071]
用于口服使用的制剂也可以呈现为硬明胶胶囊,其中活性成分与惰性固体稀释剂例如磷酸钙或高岭土混合,或呈现为软明胶胶囊,其中活性成分与水或油介质例如花生油、液体石蜡或橄榄油混合。
具体实施方式
[0072]
下文将结合具体实施例对本发明的技术方案做更进一步的详细说明。应当理解,下列实施例仅为示例性地说明和解释本发明,而不应被解释为对本发明保护范围的限制。凡基于本发明上述内容所实现的技术均涵盖在本发明旨在保护的范围内。
[0073]
除非另有说明,以下实施例中使用的原料和试剂均为市售商品,或者可以通过已知方法制备。
[0074]
实施例1化合物cp57的制备
[0075]
按照以下路线制备得到化合物cp57
[0076][0077]
实施例2化合物cp59的制备
[0078]
按照以下路线制备得到化合物cp59
[0079][0080]
测试例1体外抗hbv活性实验
[0081]
1.实验方案
[0082]
铺细胞和化合物处理
[0083]
第0天,将hepg2.2.15铺种到96孔板中(6
×
104个细胞/孔)。
[0084]
第1天,加含化合物的培养基。受试化合物稀释3个单药浓度(表1),测试化合物测试3个浓度,对照化合物etv共8个浓度,3倍稀释,三复孔。细胞在5%co2和37℃的条件下培养3天。
[0085]
第4天,更换一次含化合物的新鲜培养基。
[0086]
第7天,收集上清,将收集的细胞上清用elisa法检测hbeag和hbsag。同时,celltiter-glo检测细胞活力,收集细胞冷冻保存(备用)。
[0087]
表2.受试化合物测试浓度(μm)
[0088][0089]
样品检测
[0090]
elisa法检测细胞培养上清中hbeag和hbsag的含量:
[0091]
方法参照试剂盒说明书,方法简述如下:分别取50μl的标准品,样品和对照品加入到检测板中,然后每孔加入50μl酶结合物,37℃孵育60分钟,用洗液洗板后吸干,然后加入50μl预混发光底物,室温避光孵育10分钟,最后酶标仪测定发光值。
[0092]
celltiter-glo细胞活力检测:
[0093]
参照celltiter-glo试剂盒说明书测定细胞活力,方法简述如下:收集细胞培养上清之后,每孔加入celltiter-glo(培养基1:1稀释),室温孵育10分钟,酶标仪测定发光值。
[0094]
数据分析
[0095]
hbeag抑制率(%)=(1-样品的hbeag值/dmso对照组hbeag值)
×
100%
[0096]
hbsag抑制率(%)=(1-样品的hbsag值/dmso对照组hbsag值)
×
100%
[0097]
细胞活性(%)=((化合物组样品的值
–
空白对照组平均值)/(dmso组平均值
–
空白对照组平均值)
×
100%
[0098]
应用graphpad prism软件(four parameter logistic equations)计算ec
50
值。
[0099]
本发明化合物(cp57)的活性见下表1:
[0100]
表1
[0101][0102][0103]
由表1可知,本发明的化合物细胞毒性低,且对hbsag和hbeag均具有较高的抑制率,是用于治疗病毒性肝炎的潜在药物。
[0104]
以上,对本发明的实施方式进行了说明。但是,本发明不限定于上述实施方式。凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。