作为抗癌症剂的n-酰化组氨酸二肽
1.相关申请的交叉引用
2.本技术要求于2019年10月16日提交的美国临时专利申请号62/916,001的优先权权益,其全部内容通过援引并入本文中。
3.联邦资助的研究
4.本发明在美国国立卫生研究院(national institutes of health)授予的合同gm062480和hg007735的政府支持下完成。政府对本发明享有一定的权利。
技术领域
5.本公开涉及用于治疗癌症,特别是乳腺癌症的n-酰化组氨酸二肽及其衍生物。
技术背景
6.尽管乳腺癌症的高存活率,但它仍然是影响女性的最常见癌症。仅在美国,2019年估计有271,270例新乳腺癌症病例,并且同年估计有42,260例死于该疾病。乳腺癌症的治疗取决于诸如肿瘤期、尺寸和患者偏好的因素而不同。虽然大多数的治疗涉及保乳手术或乳腺切除术伴随放射疗法,但在大约35%的早期(i和ii)癌症中,治疗将包括药物疗法(靶向的和/或非靶向的)。在iii期和iv期乳腺癌症中,至少58%以药物疗法组合手术和/或放射疗法来治疗。需要表现出更高的疗效和/或更低的毒性的用于治疗乳腺癌症的小分子疗法。
技术实现要素:
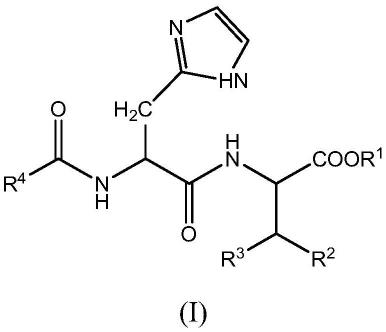
7.在一个方面,本公开涉及式i的a化合物:
[0008][0009]
其中,
[0010]
r1是h或(c
1-c6)烷基;
[0011]
r2是(c
1-c
10
)烃基;
[0012]
r3是(c
1-c6)烷基;
[0013]
r4选自(c
14-c
20
)烃基;经卤素、羟基、巯基、(c
1-c6)酰基、(c
1-c6)烷氧基、(c
1-c6)卤代烷氧基、氨基、(c
1-c6)烷基氨基、二(c
1-c6)烷基氨基和(c
1-c6)烷基硫基中的一种或多种取代的(c
14-c
20
)烃基;(c
10-c
20
)氧杂烷基;(c
10-c
20
)硫杂烷基和(c
10-c
20
)氮杂烷基。
[0014]
在另一方面中,本公开涉及包括药学上可接受的载体和式i化合物的药物组合物。
[0015]
在另一方面,本公开涉及治疗乳腺癌症的方法,所述方法包括向需要治疗的哺乳动物施用治疗有效量的式i的化合物。
[0016]
在另一方面,本公开涉及式i的化合物,用于治疗乳腺癌症的用途。
[0017]
在另一方面,本公开涉及式i化合物在制备用于治疗乳腺癌症的药物中的用途。
附图说明
[0018]
当参考附图阅读以下详细描述时,将更好地理解本公开的这些和其他特征、方面和优点,其中:
[0019]
图1:mbc017与mda-mb-231细胞的剂量响应曲线。在37℃下,将化合物mbc017与mda-mb-231三阴性人乳腺癌症细胞在指示浓度下孵育3天,之后基于cell titer blue荧光进行细胞生存力测定。归一化的细胞生存力数据是三个生物复制的平均值,其以百分比表示,并且标准误差由每个平均数据点的误差棒表示(空白方块)。化合物浓度在x轴上以对数比例表示,单位为μm。如在nature scientific reports,article number:14701,(2015)中所述,使用名为drfit的自由软件分析数据。将drfit用于将绘制的数据点拟合至希尔方程(红色曲线),并生成ic50值(μm),显示在图表上。这些数据不足以计算出准确的ic50值。
[0020]
图2:mbc0171与mda-mb-231细胞的剂量响应曲线。在37℃下,将化合物mbc0171与mda-mb-231三阴性人乳腺癌症细胞在指示浓度下孵育3天,之后基于cell titer blue荧光进行细胞生存力测定。归一化的细胞生存力数据是三个生物复制的平均值,其以百分比表示,并且标准误差由每个平均数据点的误差棒表示(空白方块)。化合物浓度在x轴上以对数比例表示,单位为μm。如在nature scientific reports,article number:14701,(2015)中所述,使用名为drfit的自由软件分析数据。将drfit用于将绘制的数据点拟合至希尔方程(红色曲线),并生成ic50值(μm),显示在图表上。
[0021]
图3:mbc0172与mda-mb-231细胞的剂量响应曲线。在37℃下,将化合物mbc0172与mda-mb-231三阴性人乳腺癌症细胞在指示浓度下孵育3天,之后基于cell titer blue荧光进行细胞生存力测定。归一化的细胞生存力数据是三个生物复制的平均值,其以百分比表示,并且标准误差由每个平均数据点的误差棒表示(空白方块)。化合物浓度在x轴上以对数比例表示,单位为μm。如在nature scientific reports,article number:14701,(2015)中所述,使用名为drfit的自由软件分析数据。将drfit用于将绘制的数据点拟合至希尔方程(红色曲线),并生成ic50值(μm),显示在图表上。
[0022]
图4:mbc0174与mda-mb-231细胞的剂量响应曲线。在37℃下,将化合物mbc0174与mda-mb-231三阴性人乳腺癌症细胞在指示浓度下孵育3天,之后基于cell titer blue荧光进行细胞生存力测定。归一化的细胞生存力数据是三个生物复制的平均值,其以百分比表示,并且标准误差由每个平均数据点的误差棒表示(空白方块)。化合物浓度在x轴上以对数比例表示,单位为μm。如在nature scientific reports,article number:14701,(2015)中所述,使用名为drfit的自由软件分析数据。将drfit用于将绘制的数据点拟合至希尔方程(红色曲线),并生成ic50值(μm),显示在图表上。
[0023]
图5:mbc0179与mda-mb-231细胞的剂量响应曲线。在37℃下,将化合物mbc0179与mda-mb-231三阴性人乳腺癌症细胞在指示浓度下孵育3天,之后基于cell titer blue荧光
进行细胞生存力测定。归一化的细胞生存力数据是三个生物复制的平均值,其以百分比表示,并且标准误差由每个平均数据点的误差棒表示(空白方块)。化合物浓度在x轴上以对数比例表示,单位为μm。如在nature scientific reports,article number:14701,(2015)中所述,使用名为drfit的自由软件分析数据。将drfit用于将绘制的数据点拟合至希尔方程(红色曲线),并生成ic50值(μm),显示在图表上。
[0024]
图6:mbc0179与htert-hme1细胞在megm培养基中的剂量响应曲线。在37℃下,将化合物mbc0179与htert-hme1健康人乳房上皮细胞在指示浓度下,于富含生长因子的megm培养基中孵育3天,之后基于cell titer blue荧光进行细胞生存力测定。归一化的细胞生存力数据是三个生物复制的平均值,其以百分比表示,并且标准误差由每个平均数据点的误差棒表示(空白方块)。化合物浓度在x轴上以对数比例表示,单位为μm。如在nature scientific reports,article number:14701,(2015)中所述,使用名为drfit的自由软件分析数据。将drfit用于将绘制的数据点拟合至希尔方程(红色曲线),并生成ic50值(μm),显示在图表上。
[0025]
图7:mbc0179与mda-mb-231细胞在megm培养基中的剂量响应曲线。在37℃下,将化合物mbc0179与mda-mb-231三阴性人乳腺癌症细胞在指示浓度下,于富含生长因子的megm培养基中孵育3天,之后基于cell titer blue荧光进行细胞生存力测定。归一化的细胞生存力数据是三个生物复制的平均值,其以百分比表示,并且标准误差由每个平均数据点的误差棒表示(空白方块)。化合物浓度在x轴上以对数比例表示,单位为μm。如在nature scientific reports,article number:14701,(2015)中所述,使用名为drfit的自由软件分析数据。将drfit用于将绘制的数据点拟合至希尔方程(红色曲线),并生成ic50值(μm),显示在图表上。
[0026]
图8:mbc0179与mcf7细胞的剂量响应曲线。在37℃下,将化合物mbc0179与mcf7雌激素受体阳性的人乳腺癌症细胞在指示浓度下孵育3天,之后基于cell titer blue荧光进行细胞生存力测定。归一化的细胞生存力数据是三个生物复制的平均值,其以百分比表示,并且标准误差由每个平均数据点的误差棒表示(空白方块)。化合物浓度在x轴上以对数比例表示,单位为μm。如在nature scientific reports,article number:14701,(2015)中所述,使用名为drfit的自由软件分析数据。将drfit用于将绘制的数据点拟合至希尔方程(红色曲线),并生成ic50值(μm),显示在图表上。
[0027]
图9:mbc0179与mda-mb-468细胞的剂量响应曲线。在37℃下,将化合物mbc0179与mda-mb-468三阴性人乳腺癌症细胞在指示浓度下孵育3天,之后基于cell titer blue荧光进行细胞生存力测定。归一化的细胞生存力数据是三个生物复制的平均值,其以百分比表示,并且标准误差由每个平均数据点的误差棒表示(空白方块)。化合物浓度在x轴上以对数比例表示,单位为μm。如在nature scientific reports,article number:14701,(2015)中所述,使用名为drfit的自由软件分析数据。将drfit用于将绘制的数据点拟合至希尔方程(红色曲线),并生成ic50值(μm),显示在图表上。
[0028]
图10:mbc0179与zr-75-30细胞的剂量响应曲线。在37℃下,将化合物mbc0179与zr-75-30人乳腺癌症细胞在指示浓度下孵育3天,之后基于cell titer blue荧光进行细胞生存力测定。归一化的细胞生存力数据是三个生物复制的平均值,其以百分比表示,并且标准误差由每个平均数据点的误差棒表示(空白方块)。化合物浓度在x轴上以对数比例表示,
单位为μm。如在nature scientific reports,article number:14701,(2015)中所述,使用名为drfit的自由软件分析数据。将drfit用于将绘制的数据点拟合至希尔方程(红色曲线),并生成ic50值(μm),显示在图表上。
[0029]
图11:mbc0179与k-562细胞的剂量响应曲线。在37℃下,将化合物mbc0179与k-562人慢性髓细胞性白血细胞,非粘附细胞系,在指示浓度下孵育3天,之后基于cell titer blue荧光进行细胞生存力测定。归一化的细胞生存力数据是三个生物复制的平均值,其以百分比表示,并且标准误差由每个平均数据点的误差棒表示(空白方块)。化合物浓度在x轴上以对数比例表示,单位为μm。如在nature scientific reports,article number:14701,(2015)中所述,使用名为drfit的自由软件分析数据。将drfit用于将绘制的数据点拟合至希尔方程(红色曲线),并生成ic50值(μm),显示在图表上。
[0030]
图12:mbc0179与hepg2细胞的剂量响应曲线。在37℃下,将化合物mbc0179与hepg2人肝癌细胞在指示浓度下孵育3天,之后基于cell titer blue荧光进行细胞生存力测定。归一化的细胞生存力数据是三个生物复制的平均值,其以百分比表示,并且标准误差由每个平均数据点的误差棒表示(空白方块)。化合物浓度在x轴上以对数比例表示,单位为μm。如在nature scientific reports,article number:14701,(2015)中所述,使用名为drfit的自由软件分析数据。将drfit用于将绘制的数据点拟合至希尔方程(红色曲线),并生成ic50值(μm),显示在图表上。
[0031]
图13:mbc0179与a549细胞的剂量响应曲线。在37℃下,将化合物mbc0179与a549人肺癌症细胞在指示浓度下孵育3天,之后基于cell titer blue荧光进行细胞生存力测定。归一化的细胞生存力数据是三个生物复制的平均值,其以百分比表示,并且标准误差由每个平均数据点的误差棒表示(空白方块)。化合物浓度在x轴上以对数比例表示,单位为μm。如在nature scientific reports,article number:14701,(2015)中所述,使用名为drfit的自由软件分析数据。将drfit用于将绘制的数据点拟合至希尔方程(红色曲线),并生成ic50值(μm),显示在图表上。
[0032]
图14:mbc0179与ovcar-3细胞的剂量响应曲线。在37℃下,将化合物mbc0179与ovcar-3人卵巢癌症细胞在指示浓度下孵育3天,之后基于cell titer blue荧光进行细胞生存力测定。归一化的细胞生存力数据是三个生物复制的平均值,其以百分比表示,并且标准误差由每个平均数据点的误差棒表示(空白方块)。化合物浓度在x轴上以对数比例表示,单位为μm。如在nature scientific reports,article number:14701,(2015)中所述,使用名为drfit的自由软件分析数据。将drfit用于将绘制的数据点拟合至希尔方程(红色曲线),并生成ic50值(μm),显示在图表上。
[0033]
图15:mbc0179与sk-n-sh细胞的剂量响应曲线。在37℃下,将化合物mbc0179与sk-n-sh人神经母细胞瘤在指示浓度下孵育3天,之后基于cell titer blue荧光进行细胞生存力测定。归一化的细胞生存力数据是三个生物复制的平均值,其以百分比表示,并且标准误差由每个平均数据点的误差棒表示(空白方块)。化合物浓度在x轴上以对数比例表示,单位为μm。如在nature scientific reports,article number:14701,(2015)中所述,使用名为drfit的自由软件分析数据。将drfit用于将绘制的数据点拟合至希尔方程(红色曲线),并生成ic50值(μm),显示在图表上。
[0034]
图16:mbc0179与4t1细胞的剂量响应曲线。在37℃下,将化合物mbc0179与4t1小鼠
三阴性乳腺癌症细胞在指示浓度下孵育3天,之后基于cell titer blue荧光进行细胞生存力测定。归一化的细胞生存力数据是三个生物复制的平均值,其以百分比表示,并且标准误差由每个平均数据点的误差棒表示(空白方块)。化合物浓度在x轴上以对数比例表示,单位为μm。如在nature scientific reports,article number:14701,(2015)中所述,使用名为drfit的自由软件分析数据。将drfit用于将绘制的数据点拟合至希尔方程(红色曲线),并生成ic50值(μm),显示在图表上。
[0035]
图17:用mbc0179研究4t1小鼠乳腺癌症肺转移。植入一周后,仅将化合物mbc0179(在7%w/v聚氧乙烯蓖麻油el/10%v/v乙醇/90%v/v生理盐水负载体中)或负载体静脉内施用至携带4t1鼠乳腺癌症细胞系衍生的乳腺肿瘤的三组六只balb/c小鼠(8周龄)。在使用负载体(蓝色条)、10mg/kg(红色条)或15mg/kg(绿色条)的mbc0179,每周两次给药,持续四周后,根据iacuc指南对小鼠进行人道安乐死,并切除肺用于4t1集落形成测定,以提供4t1肺转移的测量。绘制集落计数,计算平均值和标准误差(误差棒)。进行统计显著性的双尾t检验来比较负载体组和15mg/kg mbc0179治疗组,在图表上用p值表示。此外,基于每组的平均集落计数,对负载体组进行归一化,计算负载体组和15mg/kg mbc0179治疗组之间肺源性4t1集落的降低百分比,如图表所示。
具体实施方式
[0036]
本文所述的化合物抑制肿瘤生长。可用于本文所述方法的化合物落入式i的类:
[0037][0038]
在这些化合物中,r1可以是h或(c
1-c6)烷基。在一些实施方式中,r1是氢;在一些实施方式中,r1是甲基或乙基。
[0039]
r2是(c
1-c
10
)烃基,并且r3是(c
1-c6)烷基。在一些实施方式中,r2是乙基并且r3是甲基。在一些实施方式中,r2和r3都是甲基。
[0040]
r4选自(c
14-c
20
)烃基;经卤素、羟基、巯基、(c
1-c6)酰基、(c
1-c6)烷氧基、(c
1-c6)卤代烷氧基、氨基、(c
1-c6)烷基氨基、二(c
1-c6)烷基氨基和(c
1-c6)烷基硫基中的一种或多种取代的(c
14-c
20
)烃基;(c
10-c
20
)氧杂烷基;(c
10-c
20
)硫杂烷基和(c
10-c
20
)氮杂烷基。在一些实施方式中,r4是(c
14-c
20
)脂肪烃。在一些实施方式中,r4是氟化(c
14-c
20
)脂肪烃。在一些实施方式中,r4是直链(c
14-c
20
)烷基。在一些实施方式中,r1是h并且r4是(c
14-c
20
)烷基。
[0041]
所公开的化合物在当r1是烷基时是碱性的,在当r1是氢时是两性的。术语“药学上可接受的盐”是指由药学上可接受的无毒酸或碱(包括无机酸和碱以及有机酸和碱)制备的盐。当本公开的化合物是碱性时,盐可以由药学上可接受的无毒酸制备。本发明化合物的合
适的药学上可接受的酸加成盐包括乙酸、己二酸、藻酸、抗坏血酸、天冬氨酸、苯磺酸(苯磺酸盐)、苯甲酸、硼酸、丁酸、樟脑酸、樟脑磺酸、碳酸、柠檬酸、乙二磺酸、乙磺酸、乙二胺四乙酸、甲酸、富马酸、葡庚糖酸、葡萄糖酸、谷氨酸、氢溴酸、盐酸、氢碘酸、羟基萘甲酸、羟乙磺酸、乳酸、乳糖酸、十二烷基磺酸、马来酸、苹果酸、苦杏仁酸、甲磺酸、粘酸、萘磺酸(naphthylenesulfonic)、硝酸、油酸、双羟萘酸、泛酸、磷酸、特戊酸、多聚半乳糖醛酸、水杨酸、硬脂酸、琥珀酸、硫酸、鞣酸、酒石酸、特拉克酸(teoclatic)、对甲苯磺酸盐等的酸加成盐。当r1不是烷基时,除了内盐之外,本发明化合物的合适的药学上可接受的碱加成盐包括但不限于由铝、钙、锂、镁、钾、钠和锌制成的金属盐或者由赖氨酸、精氨酸、n,n'-二苄基乙二胺、氯普鲁卡因、胆碱、二乙醇胺、乙二胺、葡甲胺(n-甲基葡糖胺)和普鲁卡因制成的有机盐。其他药学上可接受的盐在适当时包括与具有1到20个碳原子的烷基连接的羧酸根、磺酸根和膦酸根阴离子和无毒的铵阳离子。尽管药学上可接受的反荷离子将优选用于制备药物制剂和用于治疗方法的用途,但其它阴离子作为合成中间体是完全可接受的。因此,当这类盐是化学中间体时,该阴离子可能是药学上不期望的。
[0042]
在整个说明书中,术语和取代基保留它们的定义。
[0043]
烃是指仅包含氢和碳的支架。它包括烷基、环烷基、多环烷基、烯基、炔基、芳基及其组合。实施例包括苯基、苄基、苯乙基、环己基甲基、樟脑基、9-十六烯基、6-十八烯基、9-十八烯基、9-二十烯基和13-二十二烯基。
[0044]
烷氧基(alkoxy)或烷氧基(alkoxyl)是指通过氧与母体结构连接的具有1至6个碳原子的直链、支链、环状构型的基团及其组合。实例包括甲氧基、乙氧基、丙氧基、异丙氧基、环丙氧基、环己氧基等。
[0045]
氧杂烷基是指其中一个或多个碳(及其相关的氢)被氧替代的烷基残基。实例包括3,6,9-三氧杂癸基等。术语氧杂烷基旨在如本领域所理解的[参见naming and indexing of chemicalsubstances for chemical abstracts,出版于american chemical society,196,但不受127(a)限制],即它是指其中氧经由单键与其相邻原子键合(形成醚键)的化合物;它不是指双键氧,如羰基基团中存在。类似地,硫杂烷基和氮杂烷基是指其中一个或多个碳分别被硫或氮替代的烷基残基。
[0046]
酰基是指通过羰基官能团连接到母体结构的具有1、2、3、4和5个碳原子的直链、支链、环状构型、饱和、不饱和和芳香族基团及其组合。实施例包括甲酰基、乙酰基、苯甲酰基、丙酰基、异丁酰基等。
[0047]
芳基和杂芳基意指包含选自o、n或s的0-3个杂原子的5-元或6-元芳香族或杂芳香族环;包含选自o、n或s的0-3个杂原子的双环9-元或10-元芳香族或杂芳香族环体系;或者包含选自o、n或s的0-3个杂原子的三环13-元或14-元芳香族或杂芳香族环体系。
[0048]
如本文所用,术语“任选取代的”可以与“未取代的或取代的”互换使用。术语“取代的”是指特定基团中的一个或多个氢原子经特定的基团替代。例如,取代的(c
14-c
20
)烃基是指(c
14-c
20
)烃基残基,其中,一个或多个h原子经卤素、羟基、巯基、(c
1-c6)酰基、(c
1-c6)烷氧基、(c
1-c6)卤代烷氧基、氨基、(c
1-c6)烷基氨基、二(c
1-c6)烷基氨基或(c
1-c6)烷基硫基替代。这种取代的烃基残基的实例是蓖麻油基(即,12-羟基-9-十八烯基)。尽管在“任选取代的”残基的大多数情况下,1、2或3个氢原子经特定的基团替代,但在氟代烃残基的情况下,超过3个氢原子可以被氟替代;事实上,所有可用的氢原子都可以被氟替代,例如全氟丙基。
[0049]
本文所述的化合物包含至少两个不对称中心,并且因此引起对映异构体、非对映异构体和其它立体异构形式,其根据绝对立体化学可以定义为(r)-或(s)-。本公开意在包括所有此类可能的异构体,以及它们的外消旋和光学的纯形式。二肽的(s,s)非对映异构体是优选的,即二肽包括两个l-氨基酸。光学活性(r)-和(s)-异构体可以使用手性合成子或手性试剂制备,或使用常规技术拆分。当本文所述化合物包含烯属双键或其他几何不对称中心时,并且除非另有说明,否则该化合物旨在包括e和z几何异构体两者。同样,所有互变异构形式也旨在包括在内。
[0050]
在一些实例中,式i化合物的部分可以包括氨基酸。氨基酸可以作为不同的立体异构体存在,相关领域的技术人员通常称之为d-和l-异构体。氨基酸的l-异构体是由活细胞产生并结合到蛋白中的那些。在一些式i化合物中,其部分地包括一个或两个氨基酸,各自独立地或两个氨基酸组分可以全部或主要以l-异构体(大于90%w/v)存在,或全部或主要以d-异构体存在。在其他实例中,每种各自独立地或两个种氨基酸组分可以以大致相等的比例的l-和d-异构体存在。在一些实例中,一种异构体主要呈l-型或d-型,而另一种异构体作为两种异构体的混合物存在。在其他实例中,两种氨基酸组分都呈d-或l-型,而在另一个实例中,一种可以呈d-型,而另一种呈l-型。不限于特定的作用机制或者化合物的有效性程度或持续时间,然而细胞中天然存在的多肽主要由l-构型的氨基酸组成,如本文所公开的,包括一种或多种d-型氨基酸组分的式i化合物可能比具有不是呈d-型氨基酸组分的化合物对肽酶作用更具抗性,并且因此,在向细胞或生物施用时表现出延长的或增强的生理功效。
[0051]
如本文所用,并且如本领域技术人员所理解的,除非明确进一步限定,否则所叙述的“化合物”旨在包括该化合物的盐。在特定的实施方式中,术语“式i化合物”是指药学上可接受的盐。
[0052]
将认识到,本公开的化合物可以以放射性标记的形式存在,即,化合物可以包含一个或多个原子,该原子包含的原子质量或质量数不同于通常在自然界中发现的原子质量或质量数。替代地,单一结构的多个分子可以包括至少一个原子,该原子的同位素比率不同于自然界中发现的同位素比率。氢、碳、磷、氟、氯和碘的放射性同位素包括,例如,2h、3h、
11
c、
13
c、
14
c、
15
n、
35
s、
18
f、
36
cl、
123
i、
125
i、
131
i和
133
i。包含那些放射性同位素和/或其他原子的其他放射性同位素的化合物在本公开的范围内。特别优选包含3h、
14
c和碘放射性同位素的化合物,因为它们易于制备和检测。包含同位素
11
c、
13
n、
15
o和
18
f的化合物非常适用于正电子发射断层显像。本公开的放射性标记的式i和ii化合物通常可以通过本领域技术人员熟知的方法制备。方便起见,这种放射性标记的化合物可以通过实施实例和方案中公开的程序,通过容易获得的放射性标记的试剂取代非放射性标记的试剂来制备。
[0053]
尽管该公开易于以许多不同形式的实施方式,但是示出了本公开的优选实施方式。然而,应当理解的是,本公开被认为是本公开的原理的范例,并且不旨在将本公开限制于所示的实施方式。
[0054]
在进一步的组合物方面中,本公开涉及药学上可接受的载体和式i的化合物。这种药物组合物可以另外包括其他抗肿瘤剂和赋形剂。由于它们旨在用于治疗癌症,并且不是用于形成表面活性剂或络合物,因此它们通常不含络合金属,诸如铜。优选的载体是水性的,并且不含不溶于水的溶剂。一种或多种载体必须是“可接受的”,意为与制剂的其它成分相容,并且对其接受者无害。可以将组合物配制用于口服、局部或肠胃外施用。例如,它们可
以通过静脉内、动脉内、皮下以及直接进入cns——鞘内或脑室内给予。
[0055]
制剂包括适于口服、肠胃外(包括皮下、皮内、肌内、静脉内和关节内)、直肠和局部(包括皮肤、口腔、舌下和眼内)施用的制剂。化合物优选口服或通过注射(静脉内或皮下)施用。向患者施用的化合物的精确量将由主治医师负责。然而,所采用的剂量将取决于许多因素,包括患者的年龄和性别、待治疗的确切疾患及其严重性。此外,施用途径可以取决于病症及其严重性而改变。方便起见,制剂可以以单位剂型存在,并且可以通过药学领域公知的任何方法制备。通常,制剂是通过将活性成分与液体载体或细分的固体载体或两者均匀且紧密地结合来制备,并且然后,如果需要,将产品成型为所期望的制剂。
[0056]
适用于口服施用的本公开的制剂可以作为以下项存在:作为离散单位诸如胶囊、扁囊剂或片剂,各自包含预定量的活性成分;作为粉末或颗粒;作为在水性液体或非水性液体中的溶液或混悬剂;或者作为水包油液体乳剂或油包水液体乳剂。活性成分也可以作为丸剂、冲剂或糊剂存在。
[0057]
片剂可以任选地与一种或多种辅助成分,通过压制或模塑制成。压制片剂可以通过以下制备:在合适的机器中压制呈自由流动形式的活性成分诸如粉末或颗粒,任选与粘结剂、润滑剂、惰性稀释剂、润滑、表面活性或分散的剂混合。模制片剂可以通过在合适的机器中模制用惰性液体稀释剂润湿的粉末化合物的混合物来制备。片剂可以任选地被包覆或刻痕,并且可以被配制以提供其中活性成分的缓释、迟释或控释。
[0058]
肠胃外施用的制剂包括水性和非水性无菌注射溶液,其可以包含抗氧化剂、缓冲剂、抑菌剂以及使制剂与预期接受者的血液等渗的溶质。肠胃外施用的制剂还包括水性和非水性无菌混悬剂,其可以包括助悬剂和增稠剂。制剂可以存在于单位剂量或多剂量容器中,例如密封的安瓿和小瓶,并且可以在储存在仅需要在使用前立即添加无菌液体载体(例如盐水、磷酸盐缓冲盐水(pbs)等)的冷冻干燥(冻干)条件下。即时注射溶液和混悬剂可以由前述种类的无菌粉末、颗粒和片剂制备。优选的单位剂量制剂是包含有效剂量的活性成分或其适当部分的那些制剂。
[0059]
应当理解的是,除了上面特别提到的成分之外,关于所讨论的制剂类型,本公开的制剂可以包括本领域常规的其它剂,例如适用于口服施用的那些制剂可以包括调味剂。
[0060]
如本文所用,术语“治疗(treatment)”或“治疗(treating)”、或“减轻”或“改善”是指获得有益的或期望的结果的方法,该结果包括但不限于治疗益处和/或预防益处。治疗益处意指正在治疗的潜在疾患的改善。此外,经改善与潜在疾患相关的一种或多种生理症状来实现治疗益处,使得在患者中观察到改进,尽管患者可能仍受该潜在疾患折磨。在其他实例中,可以将式i化合物向动物或人受试者,或者向样品(诸如细胞培养物或其他体外系统)施用用于治疗以外的目的。其他实例包括式i化合物,用于治疗乳腺癌症的用途。还有另一实施例包括式i化合物在制备用于治疗乳腺癌症的药物中的用途。在一些实例中,为了治疗或其它目的,可以施用单一的式i化合物,或两种或更多种式i化合物的任意组合。
[0061]
化合物可以通过本领域公知的方法合成。例如,在美国公开申请2012/0308646第[0179]段及其后段落中所述的合成中,组氨酸可以取代丙氨酸。以类似的方式,可以利用具有
–
chr2r3侧链的其它氨基酸合成式i的其它化合物。
[0062]
已测试的式i化合物的一些实例包括表1中确定的那些,如下:给出了每种测试分子的完整化学名称,每行中都有相应的化合物和肽名称id。在显示用于计算ic50值的剂量
响应数据的图号旁边,显示每种化合物所针对的测试细胞系和所得ic50值(μm)。在“细胞系”列中,所有细胞均示出为在dmem或rpmi培养基中测试,以括号指示,并如正文所述。然而,在一些情况下,使用megm培养基对mbc0179肽与htert-hme1和mda-mb-231细胞比较,以使由于在富含生长因子的megm培养基中孵育的差异最小化,并促进真正的比较。在mbc017的情况下,该化合物确实降低了细胞生存力,但不足以能够准确计算ic50,并且示出为未计算(nc)。
[0063]
表1:cell titer blue体外细胞生存力测定的结果总结。
[0064]
[0065][0066]
测定和测试结果
[0067]
采用可商购的体外细胞生存力试剂(cell titer blue)以确定几种化合物(1-5)针对多种癌症和健康组织来源的细胞系的抗癌症有效性。细胞系总结在表2中,如下:所有细胞系和关于每个细胞系来源和特征的信息均购自atcc(www.atcc.org)。通用名称和atcc产品id示出在第一(最左)列。从左侧开始,第二和第三列描述了从中分离出每种细胞系的生物和组织。第四和第五列显示每种细胞系的细胞类型和疾病状态(例如,正常与癌)。第六列提供了使用体外细胞生存力测定针对每种细胞系测试的化合物的总结。每种化合物的肽名id在括号中示出,编号为1至5。
[0068]
表2:测试细胞系的描述。
[0069]
[0070][0071][0072]
cell titer blue试剂(可从promega,inc.获得)是包含刃天青的缓冲溶液,刃天青是通过代谢活性细胞转化为试卤灵(一种可检测的荧光产物)的化合物。因此试卤灵产物
的荧光强度用作活细胞数量的比例量度,允许待监测的癌症或其他细胞系内细胞生存力的变化,以响应细胞毒性或细胞抑制剂的添加。各种人乳房组织来源的细胞系被广泛用于研究针对体外抗乳腺癌症的潜在治疗剂的作用。人乳腺癌症细胞系可以基于激素受体状态,即雌激素、孕酮和人表皮生长因子阳性或阴性,细分为多组。可以将健康人乳房组织来源的细胞系,htert-hme1用于体外测定治疗剂对健康人乳房组织的作用。此外,高度转移性和侵袭性的鼠(小鼠)乳腺癌症细胞系4t1已被广泛用于监测从小鼠乳腺脂肪垫(fat pad)到肺部的乳腺癌症转移,以便在体内动物模型中系统地研究抗癌症疗剂的抗转移有效性。肺转移可以方便地通过成熟的集落形成测定来量化。代表除乳腺癌症以外的各种癌症的其它人类组织来源的模型细胞系可以用于体外评估抗癌化合物的潜力。这些包括k-562(慢性髓细胞性白血病)、hepg2(肝细胞癌)、ovcar-3(卵巢腺癌)、sk-n-sh(神经母细胞瘤)和a549(肺癌)。使用cell titer blue生存力测定,针对人和鼠来源两者的一系列癌症细胞系加上一种健康人的乳房细胞系,体外测定了几种化合物(表1,图1-16)。进行了小鼠4t1转移研究,以确定一种化合物mbc0179的抗转移性潜力(图17)。
[0073]
试剂和设备
[0074]
二甲亚砜(dmso)、cremophor el、亚甲蓝、100x倍抗生素/抗真菌溶液、胶原酶(iv型)、dna酶i和6-硫鸟嘌呤可从millipore-sigma获得。肽(化合物1-5,表1)如上所述由bio basic,inc.(ontario,canada)合成。将肽溶解在dmso中至10mm,然后稀释到适当的培养基中。根据生产商的说明书使用cell titer blue reagent(promega,inc.)。使用560nm激发和583nm发射下的enspire荧光读板仪(perkinelmer)测量试卤灵荧光。
[0075]
细胞系与培养
[0076]
所有细胞系均从美国典型培养物保藏中心(american type culture collection)atcc(www.atcc.org,详细参见表2)获得。培养基和培养基补充物可从thermofisher scientific获得。除非另有说明,否则细胞在补充有10%(v/v)胎牛血清(fbs)和1%(v/v)抗生素/抗真菌溶液(100单位/ml青霉素、100μg/ml链霉素和0.025μg/ml两性霉素b)的dmem(dulbecco改良eagle培养基)培养基中以单层生长。htert-hme1(并且对于一个实验,mda-mb-231)细胞在补充有10%(v/v)fbs和1%(v/v)抗生素/抗真菌溶液的megm(乳腺上皮细胞生长培养基)培养基(lonza)中生长。4t1和ovcar-3细胞在补充有10%(v/v)fbs和1%(v/v)抗生素/抗真菌溶液的rpmi(roswell park memory institute)1640培养基中生长。k-562细胞(非粘附细胞系)在补充有10%(v/v)fbs和1%(v/v)抗生素/抗真菌溶液的dmem中悬浮生长并测定。将细胞以4000个细胞/孔接种在96孔平底细胞培养观察板(每孔100μl培养基)中,并且在药物或负载体孵育之前,允许细胞在37℃下继续生长24小时。
[0077]
生存力测定
[0078]
接种后生长24小时(第0天)之后,将培养基更换为相同组合物加上负载体(1%v/v dmso)或在1%v/v dmso中的肽(药物)的培养基,以不同浓度添加(如图和图例中所示)。允许药物或负载体在37℃下继续孵育72小时,之后进行cell titer blue测定。在每个孔中加入10%v/v的cell titer blue试剂,并且将板在37℃下孵育2小时,之后进行荧光测量。所有实验数据是三次生物重复的产物,各自进行三份法(三次技术重复)。从包含负载体或药物与细胞的每个孔中减去平均基线试卤灵荧光(培养基无细胞)。然后将校正的荧光信号归
一化至负载体处理的孔中,并表示为归一化细胞生存力的百分比。绘制数据,曲线拟合于希尔方程,并且使用drfit软件计算ic
50
值(如nature scientific reports 5,article number:14701,2015中所述),合并所有3次生物重复的平均值和标准误差(图1-16)。
[0079]
4t1小鼠乳腺癌症转移研究
[0080]
将250000个4t1细胞植入8周龄的balb/c雌性小鼠(3组,每组n=6,负载体加2个药物治疗组)的第4腹股沟乳腺脂肪垫中。细胞植入一周后,每周两次通过静脉内施用给予10mg/kg(治疗,组2)和15mg/kg(治疗,组3)的mbc0179的剂量在载体(7%w/v cremophor el和10%乙醇的生理盐水)中或仅载体(对照,组1)。每周三次对所有动物称重,并使用卡尺测量肿瘤。植入后五周,根据iacuc指南,所有动物通过过度暴露于二氧化碳而被人道地安乐死,并切除肺用于集落形成测定。取出小鼠的双肺,用dulbecco磷酸盐缓冲盐水(dpbs)(vwr)洗涤,用剪刀切碎成小块,通过用宽口移液管反复吸取进一步破碎,并在包含4mg/ml胶原酶iv型和2.5u/ml dnase i的5ml dpbs中于37℃在搅拌下消化2小时。将样品通过40μm细胞滤器过滤并以1000rpm旋转5分钟,用10ml的dpbs洗涤,再次旋转,并最终重悬于补充有10%(v/v)fbs、1%(v/v)抗生素/抗真菌溶液和60μm 6-硫鸟嘌呤的5ml的dmem中(由于4t1细胞对6-硫鸟嘌呤的抗性,其内含物确保仅计数4t1集落)。对于每个处理组的肺(来自一只动物),将5ml的浓缩细胞转移至6孔细胞培养板的第一个孔中,并且然后用每孔中补充有10%(v/v)fbs、1%(v/v)抗生素/抗真菌溶液和60μm 6-硫鸟嘌呤的5ml的dmem连续稀释1/10到剩余5个孔的每个孔中。将该板在37℃下培养2周,之后取出培养基并用5ml的dpbs洗涤每个孔两次。然后在室温下添加1ml的甲醇固定细胞20分钟。除去甲醇,并用1ml的亚甲蓝染色溶液(水中0.03%w/v)孵育细胞10分钟。然后通过将该板浸入水中除去背景亚甲蓝,以显示蓝色染色的4t1集落,随后计数。考虑到每个孔的原始稀释因子,计算了每组肺的4t1集落总数。然后对每个治疗组或对照组中所有受试者的这些计数取平均值,并计算标准误差并绘制值(图17)。最后,使用双尾t检验评估了对照组和治疗组之间变化的统计显著性。
[0081]
结果
[0082]
表1(和图1)中总结,在孵育3天后,相对于负载体,n-[n-(1-氧代十六烷基)-l-组氨酰基]-l-缬氨酸(1)或mbc017以剂量依赖性方式降低了存活的mda-mb-231三阴性(密封蛋白-低亚型)人乳腺癌症细胞的部分。观察到用125μm的mbc017的生存力几乎有40%降低,然而这种降低不足以精确计算ic
50
值。mbc017的衍生物,即mbc0171、mbc0172、mbc0174和mbc0179也证明了针对mda-mb-231细胞的抗癌症有效性,获得的ic
50
值分别为6730μm、13.1μm、62.1μm和14.7μm(表1,图2-5)。用化合物mbc0179测试了htert-hme1,一种正常生长在补充生长因子的megm培养基中的人正常乳房上皮细胞系,结果为ic
50
(270μm,表1,图6)相对于在相同培养基中与mda-mb-231细胞孵育的mbc0179的ic
50
(8.88μm,表1,图7)显著增加。这些数据表明,与正常乳房上皮细胞相比,mbc0179对乳房上皮癌症细胞的生长具有选择性抑制。针对其他人乳腺癌症细胞系,即mcf7(er
,lumina亚型)、mda-mb-468(三阴性,基底亚型)和zr-75-30(er her2 ,lumina亚型)进一步测试了mbc0179,得出细胞生存力的剂量依赖性降低,并且结果为ic
50
值分别为355μm(图8)、15.7μm(图9)和9.7μm(图10)。这些数据强烈表明mbc0179可能对宽范围的乳腺癌症分子亚型有效。此外,用代表慢性髓细胞性白血病(k562,图11,ic
50
=6.11μm)、肝癌症(hepg2,图12,ic
50
=24.9μm)、肺癌症(a549,图13,ic
50
=10.5μm)、卵巢癌症(ovcar-3,图14,ic
50
=9.22μm)和神经母细胞瘤(sk-n-sh,图15,ic
50
=35μm)的几种模型人癌症细胞系测定mbc0179的细胞生存力降低。这些数据证明了广泛的抗癌症有效性,表明mbc0179可能是癌症不可知的(agnostic)。最后,为了在进行4t1体内小鼠乳腺癌症转移研究之前获得抗转移潜力的初步指征,用高转移性小鼠三阴性乳腺癌症细胞系4t1的剂量依赖性生存力实验完成了化合物mbc0179有效性的体外评估。图16中的剂量响应数据强烈表明该药物将是有效的(ic
50
=25.5μm),并且因此开启了体内研究(结果描述如下)。
[0083]
在小鼠中,4t1乳腺癌症细胞主要从乳腺脂肪垫转移至肺,并且由于4t1细胞对6-硫鸟嘌呤的抗性,已广泛采用集落生成测定来测量4t1肺转移。从三个研究组(负载体治疗组、10mg/kg mbc0179治疗组和15mg/kg mbc0179治疗组)收集数据,每组由六只雌性balb/c小鼠组成,每周两次给药。绘制了各组的平均4t1集落计数(图17),并在负载体和15mg/kg mbc0179治疗组之间观察到肺转移在统计学上显著的境地(p=0.03,双尾t-检验)。此外,这两组之间肺转移的降低百分比为74.4%(图17)。总体而言,肺转移呈剂量依赖性降低,表明mbc0179可以在体内预防乳腺癌症转移,并且在人中可能具有类似的治疗益处。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。