1.本发明是关于母乳低聚糖的新应用,具体地说,是关于母乳低聚糖在制备可调控倡导免疫的婴幼儿配方食品中的应用,以及所制备得到的婴幼儿配方食品。
背景技术:
2.母乳喂养是人类社会生存和可持续发展的重要根基,没有母乳喂养就没有人类本身。即使到了科学发展的今天,母乳喂养也是其他任何人工喂养方式都无法比拟的。在婴儿方面,母乳喂养除了提供新生儿和婴儿全面均衡的营养成分外,还富含抵抗感染性疾病(如胃肠道感染)的活性成分。通常,由于各种原因,很多母亲常选用婴幼儿配方食品喂养宝宝。作为母乳替代品,婴幼儿配方食品目前仍无法达到母乳的水平,营养及功能性成分远不及母乳。因此,无限贴近母乳是未来婴幼儿配方食品行业发展的终极目标。
3.目前,市售婴幼儿配方食品多以乳基奶粉产品为主。已有研究表明,母乳蛋白质、脂肪酸、碳水化合物等与其他哺乳动物乳汁差异较大。多年来,基于国内外母乳研发不断深入,婴幼儿奶粉产业上游原料发展取得突破,已开发出多种母乳成分替代原料。如1,3-二油酸-2棕榈酸甘油三酯(opo)、乳铁蛋白、α-乳清蛋白、β-酪蛋白、乳脂肪球膜等,基本可实现脂肪与蛋白质母乳化。
4.母乳低聚糖(human milk oligosaccharides,简称hmos)属于母乳中除乳糖和脂肪外,含量第三丰富的物质。其总含量在泌乳期的各个阶段有变化,在成熟乳中大约是12-14g/l,而初乳中大约是20-24g/l。每一种母乳低聚糖的结构在还原端都有一个乳糖,大部分以聚乳糖胺作为结构主链,并在链端含有岩藻糖、唾液酸或二者均有。母乳低聚糖主要由三大类组成:岩藻糖基类低聚糖,以2
’‑
岩藻糖基低聚糖和3
’‑
岩藻糖基低聚糖为代表性物质;唾液酸基类低聚糖,以3
’‑
唾液酸基乳糖和6
’‑
唾液酸基乳糖为代表性物质;不含岩藻糖基或唾液酸基的核心糖链结构形成的低聚糖,以乳糖-n-四糖和乳糖-n-新四糖为代表性物质。hmos的存在与含量存在个体差异,并与哺乳母亲的路易斯分泌型组成有关。由于婴幼儿配方粉的原料通常是牛乳,而牛乳中通常不含或含有很少这类低聚糖物质,hmos便成为了婴幼儿配方粉想要更加接近母乳成分所必须跨越的一道鸿沟。
5.人体的免疫机能分为先天免疫和适应性免疫。先天免疫是天生的,基于个人的遗传基因构成。吞噬类细胞在先天免疫中负责攻击、吞噬并摧毁外来微生物。适应性免疫是在生命期间获得的,直接针对特定的致病微生物或其他外来物质。在适应性免疫中,外来物质(主要是蛋白质),可能作为抗原来触发免疫反应。t淋巴细胞是适应性免疫中一类很重要的细胞,它们在胸腺成熟,能直接攻击外来细胞,产生细胞介导免疫。而作为单核细胞的后代,巨噬细胞对t细胞的功能非常重要,它们能吞噬并处理外来抗原;当t细胞在巨噬细胞表面接触到抗原与身体自身的蛋白质在一起时,会被激活。
6.肠道中存在大量的巨噬细胞,这些细胞对于维持微生态平衡可能有重要的作用。这些巨噬细胞可分为两个亚群,分别是耐受型(tolerant)巨噬细胞和发炎型(inflammatory)巨噬细胞。耐受型是内环境稳态中主要的一种亚型,它们更迭速度低,主要
位于cd4 t细胞附近的粘膜下层。发炎型巨噬细胞不存在于内环境稳态中,但当有感染发生,并伴随依赖于ccr-2的单核细胞迁移时,这种细胞会被快速招募。它们迭代速度很快,能产生tnf-α和许多其他的促炎症因子。通常将未分化的巨噬细胞表示成m0,发炎型或传统激活的巨噬细胞表示为m1,耐受型或选择性激活的巨噬细胞表示为m2。
7.小肠上皮细胞形成了对致病菌的第一道抵御防线。致病菌吸附在小肠上皮细胞,或随之侵入,都会给上皮细胞提供信号,并进一步激发其产生细胞因子或趋化因子。这些是可溶性调节物质,能吸引免疫系统的细胞,或激活免疫细胞并启动免疫应答。适宜的免疫应答可保护机体免受感染。
8.目前在婴幼儿配方食品等领域,需要有调控肠道中的免疫细胞并可缓解婴幼儿肠道不适及提升自身免疫能力的解决方案。
技术实现要素:
9.本发明的一个目的在于提供一种母乳低聚糖的新应用,具体是其在制备具有可调控调控巨噬细胞以调控肠道免疫的母乳化婴幼儿配方食品中的应用。
10.本发明的另一个目的在于提供一种母乳化婴幼儿配方食品。
11.本发明的另一个目的在于提供一种母乳化婴幼儿配方食品的应用。
12.本发明发现一些母乳低聚糖具有显著调控巨噬细胞的响应的功效,具体表现在可改变巨噬细胞的基因表型,促进巨噬细胞释放一系列趋化因子,调控巨噬细胞向m1型分化,从而可吸引其他免疫细胞共同抵御感染,以此激活系统的免疫活性。这些功效将使得母乳低聚糖添加到婴幼儿配方食品中,可给免疫系统尚在发育的婴幼儿提供更多的保护。
13.具体而言,本发明提供了母乳低聚糖在制备具有调控巨噬细胞以调控肠道免疫功效的婴幼儿配方食品中的应用。
14.本发明还提供了一种具有调控巨噬细胞以调控肠道免疫功效的婴幼儿配方食品,其中含有母乳低聚糖。
15.已知母乳低聚糖包括岩藻糖基乳糖、唾液酸基乳糖,以及不带岩藻糖基或唾液酸基的母乳寡糖基本糖链结构(典型的代表物质包括乳糖-n-四糖及其同分异构体乳糖-n-新四糖)。
16.其中2
’‑
岩藻糖基乳糖(2
’‑
fucosyllactose,2
’‑
fl或2-fl或2fl),为岩藻糖与乳糖形成的三糖结构,是岩藻糖基类低聚糖的代表性物质。市售该物质通常为经微生物发酵法制备,与人乳中发现的寡糖具有相同结构。
17.3-岩藻糖基乳糖(3-fucosyllactose,3
’‑
fl或3-fl或3fl),为岩藻糖与乳糖形成的三糖结构,与2
’‑
岩藻糖基乳糖互为同分异构体。是岩藻糖基类低聚糖的代表性物质。该物质经微生物发酵法制备,与人乳中发现的寡糖具有相同结构。
18.乳糖-n-四糖(lacto-n-tetraose,lnt),为乳糖与四糖形成的六糖结构,是以核心糖链为基础结构,且不含岩藻糖基或唾液酸基的低聚糖的代表性物质。该物质经微生物发酵法制备,与人乳中发现的寡糖具有相同结构。
[0019]3’‑
唾液酸基乳糖(3
’‑
sialyllactose,3
’‑
sl或3-sl或3sl),为唾液酸与乳糖形成的三糖结构,是唾液酸基类低聚糖的代表性物质。该物质经微生物发酵法制备,与人乳中发现的寡糖具有相同结构。
[0020]6’‑
唾液酸基乳糖(6
’‑
sialyllactose,6
’‑
sl或6-sl或6sl),为唾液酸与乳糖形成的三糖结构,是唾液酸基类低聚糖的代表性物质。该物质经微生物发酵法制备,与人乳中发现的寡糖具有相同结构。
[0021]
根据本发明的具体实施方案,本发明的具有调控巨噬细胞以调控肠道免疫功效的婴幼儿配方食品,其中含有母乳低聚糖70.9-1363.7mg/100g,或以计奶液计含有母乳低聚糖0.1-1.8g/l。优选地,本发明的婴幼儿配方食品中含有母乳低聚糖70.9-1060.7mg/100g,或以计奶液计含有母乳低聚糖0.1-1.4g/l;更优选含有母乳低聚糖70.9-681.9mg/100g,或以计奶液计含有母乳低聚糖0.1-0.9g/l。
[0022]
根据本发明的具体实施方案,本发明的具有调控巨噬细胞以调控肠道免疫功效的婴幼儿配方食品,为婴幼儿配方粉,其中含有母乳低聚糖70.9-606.1mg/100g,并且,该婴幼儿配方食品中含有:蛋白质8.5-20g/100g,脂肪13.5-30g/100g,碳水化合物40-71g/100g。
[0023]
根据本发明的具体实施方案,本发明的具有调控巨噬细胞以调控肠道免疫功效的婴幼儿配方食品,所述母乳低聚糖包括唾液酸基类低聚糖。优选地,所述唾液酸基类低聚糖包括3-sl和/或6-sl。更优选地,3-sl、6-sl在婴幼儿配方食品中的含量单独地或总和均不低于70.9mg/100g。具体而言,母乳低聚糖3-sl在婴幼儿配方食品中的应用量为70.9-606.1mg/100g粉,换算成奶液为0.1-0.8g/l,优选为70.9-454.6mg/100g粉,换算成奶液为0.1-0.6g/l,更优选为70.9-227.3mg/100g粉,换算成奶液为0.1-0.3g/l。6-sl在婴幼儿配方食品中的应用量为70.9-757.6mg/100g粉,换算成奶液为0.1-1.0g/l,优选为70.9-606.1mg/100g粉,换算成奶液为0.1-0.8g/l,更优选为70.9-454.6mg/100g粉,换算成奶液为0.1-0.6g/l。
[0024]
根据本发明的具体实施方案,本发明的具有调控巨噬细胞以调控肠道免疫功效的婴幼儿配方食品中,所述调控巨噬细胞包括:改变巨噬细胞的基因表型,促进巨噬细胞释放趋化因子,和/或调控巨噬细胞向m1型分化。
[0025]
在本发明的一些具体实施方案中,本发明的食品中的母乳低聚糖是用于改变巨噬细胞的基因表型和/或促进巨噬细胞释放趋化因子以提升巨噬细胞的免疫活性。
[0026]
根据本发明的具体实施方案,本发明的食品中的母乳低聚糖是用于调控受试者肠道内的巨噬细胞。
[0027]
在本发明的一些具体实施方案中,本发明的食品中的母乳低聚糖是用于促进巨噬细胞释放趋化因子ccl17、cxcl9、cxcl10、cxcl11、cxcl1、cxcl5、cxcl8、ccl3、ccl4、ccl5、ccl20中的一种或多种。
[0028]
在本发明的一些具体实施方案中,本发明的食品中的母乳低聚糖是用于促进巨噬细胞释放趋化因子cxcl9、cxcl10、cxcl11中的一种或多种。
[0029]
在本发明的一些具体实施方案中,本发明的食品中的母乳低聚糖是用于促进巨噬细胞释放趋化因子cxcl1、cxcl5、cxcl8、ccl3、ccl4、ccl5、ccl20中的一种或多种。
[0030]
根据本发明的具体实施方案,本发明的具有调控巨噬细胞以调控肠道免疫功效的婴幼儿配方食品,提供其中蛋白质的主要原料包括以下重量份的原料中的一种或多种:全脂奶粉140-260份,乳清蛋白粉25-120份,生乳700-3000份,脱脂奶粉120-240份,大豆浓缩蛋白20-120份。
[0031]
本发明所述婴幼儿配方食品中蛋白质可由上原料搭配使用,且不限以上种类。
[0032]
以上乳原料为多种哺乳动物来源,如牛乳及牛乳制品;羊乳及羊乳制品等。且不限于以上原料种类。
[0033]
根据本发明的具体实施方案,本发明的具有调控巨噬细胞以调控肠道免疫功效的婴幼儿配方食品,提供其中脂肪的主要原料包括以下重量份的原料中的一种或多种:玉米油20-50份,大豆油40-65份,葵花籽油0-100份,1,3-二油酸-2-棕榈酸甘油三酯0-115份,椰子油5-50份,低芥酸菜籽油30-85份。
[0034]
本发明所述婴幼儿配方食品中脂肪可由上原料搭配使用,且不限以上种类。
[0035]
根据本发明的具体实施方案,本发明的具有调控巨噬细胞以调控肠道免疫功效的婴幼儿配方食品,提供其中碳水化合物的主要原料包括以下重量份的原料中的一种或多种:乳糖80-450份,麦芽糊精50-200份,固体玉米糖浆50-200份,白砂糖25-200份。
[0036]
本发明所述婴幼儿配方奶粉中碳水化合物可由上原料搭配使用。
[0037]
本发明的具有调控巨噬细胞以调控肠道免疫功效的婴幼儿配方食品中,还可包括婴幼儿配方食品中常用的其他营养添加剂租房,例如,其原料中还可添加4-20份的维生素、矿物质类营养素。此外,配方中还可以添加部分可选择性成分,包括膳食纤维(低聚果糖、低聚半乳糖、多聚果糖等)、肌醇、牛磺酸、左旋肉碱、二十二碳六烯酸、二十碳四烯酸、叶黄素、乳铁蛋白等。这些营养素类原料的来源、含量及使用量,应符合婴幼儿配方食品及相关国家标准。
[0038]
根据本发明的具体实施方案,本发明的具有调控巨噬细胞以调控肠道免疫功效的婴幼儿配方食品,其中维生素成分包括维生素a、维生素d、维生素e、维生素k1、维生素b1、维生素b2、维生素b6、维生素b12、烟酸、叶酸、泛酸、维生素c、胆碱和生物素中的一种或多种。矿物质成分包括钠、钾、钙、磷、铜、铁、锌、锰、碘、硒、镁、钾及它们的衍生物中的一种或多种。
[0039]
在本发明的一些具体实施方案中,所述婴幼儿配方食品为适用0~6月婴儿食用的婴儿配方食品。优选地,每100g婴儿配方食品(适用0~6月婴儿食用)中维生素、矿物质含量为:
[0040]
项目含量/100g维生素a/(μgre)308~462维生素d/(μg)10.32~15.48维生素e/(mgα-te)5.6~8.4维生素k1/(μg)56~84维生素b1/(μg)440~660维生素b2/(μg)480~720维生素b6/(μg)336~504维生素b12/(μg)2.08~3.12烟酸/(μg)3200~4800叶酸/(μg)62.4~93.6泛酸/(μg)2280~3420维生素c/(mg)52~78生物素/(μg)12.8~19.2
胆碱/(mg)104~156钠/(mg)144~216钾/(mg)372~558铜/(μg)308~462镁/(mg)25.6~38.4铁/(mg)3.8~5.7锌/(mg)3.016~4.524锰/(μg)40~60钙/(mg)280~420磷/(mg)176~264碘/(μg)78.4~117.6氯/(mg)260~390硒/(μg)15.6~23.4
[0041]
优选地,每100g婴儿配方食品(适用0~6月婴儿食用)中可选择性成分含量为:
[0042][0043][0044]
在本发明的一些具体实施方案中,所述婴幼儿配方食品为适用7~12月龄较大婴儿食用的婴儿配方食品。优选地,每100g婴儿配方食品(适用7~12月龄较大婴儿食用)中维生素、矿物质含量为:
[0045]
项目含量/100g维生素a/(μgre)296~444维生素d/(μg)9.92~14.88维生素e/(mgα-te)5.6~8.4维生素k1/(μg)32~48维生素b1/(μg)560~840维生素b2/(μg)768~1152维生素b6/(μg)320~480维生素b12/(μg)2.08~3.12
烟酸/(μg)3280~4920叶酸/(μg)52~78泛酸/(μg)2520~3780维生素c/(mg)52~78生物素/(μg)12~18胆碱/(mg)99.2~148.8钠/(mg)96~144钾/(mg)372~558铜/(μg)222.4~333.6镁/(mg)24.8~37.2铁/(mg)4.944~7.416锌/(mg)2.48~3.72锰/(μg)40~60钙/(mg)344~516磷/(mg)229.6~344.4碘/(μg)74.4~111.6氯/(mg)320~480
[0046]
优选地,每100g较大婴儿配方食品(适用于7~12月龄较大婴儿食用)中可选择性成分含量为:
[0047][0048][0049]
在本发明的一些具体实施方案中,所述婴幼儿配方食品为适用12~36月龄幼儿食用的幼儿配方食品。优选地,每100g幼儿配方食品(适用12~36月龄幼儿食用)中维生素、矿物质含量为:
[0050][0051][0052]
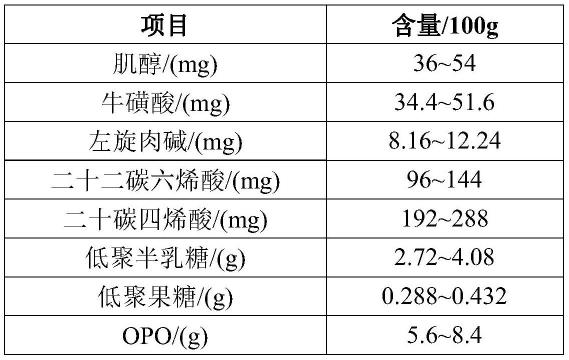
优选地,每100g幼儿配方食品(适用于12~36月龄幼儿食用)中可选择性成分含量为:
[0053]
项目含量/100g胆碱/(mg)96~144肌醇/(mg)26.4~39.6牛磺酸/(mg)32~48左旋肉碱/(mg)6.56~9.84二十二碳六烯酸/(mg)96~144二十碳四烯酸/(mg)96~144低聚半乳糖/(g)2.72~4.08低聚果糖/(g)0.288~0.432opo/(g)4.8~7.2
核苷酸/(mg)28~42
[0054]
另一方面,本发明还提供了一种制备所述的婴幼儿配方食品的方法,该方法采用湿法或干法生产工艺,将母乳低聚糖与配方中的其他原料混合,制备所述婴幼儿配方食品。具体地,湿法工艺通常包括:配料,均质,浓缩杀菌,喷雾干燥,得到成品;其中hmo可在配料时一起混料,也可以在其他物料成粉后再混料添加。干法生产工艺通常包括:配料,预热,均质,浓缩杀菌,喷雾干燥,干混添加(包括添加hmo),得到成品。
[0055]
另一方面,本发明还提供了所述的婴幼儿配方食品在制备具有调控巨噬细胞以调控肠道免疫功效的婴幼儿配方粉中的应用。其中,所述调控巨噬细胞包括:改变巨噬细胞的基因表型,促进巨噬细胞释放趋化因子,和/或调控巨噬细胞向m1型分化。
[0056]
在本发明的一些具体实施方案中,本发明证实了母乳低聚糖不影响单核细胞趋化因子ccl2。母乳低聚糖3-sl和6-sl可支持释放cxcl8、ccl5、ccl3、cxcl5、ccl20、cxcl1与ccl4等趋化因子。这些趋化因子可支持吸引更多的免疫细胞,比如可能包括单核细胞等。
[0057]
从而,本发明可通过婴幼儿配方食品中添加母乳低聚糖,能调控巨噬细胞的响应,支持巨噬细胞的发展,让免疫细胞在某些特定活动上更活跃,或吸引更多的免疫细胞,呈现出激活状态,来中和致病菌,从而可以调控肠道免疫,给受试者特别是给免疫系统尚在发育的婴幼儿提供更多的保护。
附图说明
[0058]
图1显示母乳低聚糖各单体对受试巨噬细胞用7-aad染色实验结果。
[0059]
图2显示主成分分析展示的m1和m2型巨噬细胞特有的基因表型标记物分子。
[0060]
图3显示母乳低聚糖与巨噬细胞共培养后,部分hmo影响了巨噬细胞的表型。
[0061]
图4显示母乳低聚糖与巨噬细胞共培养后,产生的趋化因子ccl2的情况。
[0062]
图5显示母乳低聚糖与巨噬细胞共培养后,产生的趋化因子ccl11的情况。
[0063]
图6显示母乳低聚糖与巨噬细胞共培养后,产生的代表典型m2型巨噬细胞的趋化因子ccl17的情况。
[0064]
图7显示母乳低聚糖与巨噬细胞共培养后,产生的代表典型m1型巨噬细胞的趋化因子cxcl9的情况。
[0065]
图8显示母乳低聚糖与巨噬细胞共培养后,产生的代表典型m1型巨噬细胞的趋化因子cxcl10的情况。
[0066]
图9显示母乳低聚糖与巨噬细胞共培养后,产生的代表典型m1型巨噬细胞的趋化因子cxcl11的情况。
[0067]
图10显示母乳低聚糖与巨噬细胞共培养后,产生的趋化因子cxcl1的情况。
[0068]
图11显示母乳低聚糖与巨噬细胞共培养后,产生的趋化因子cxcl5的情况。
[0069]
图12显示母乳低聚糖与巨噬细胞共培养后,产生的趋化因子cxcl8的情况。
[0070]
图13显示母乳低聚糖与巨噬细胞共培养后,产生的趋化因子ccl3的情况。
[0071]
图14显示母乳低聚糖与巨噬细胞共培养后,产生的趋化因子ccl4的情况。
[0072]
图15显示母乳低聚糖与巨噬细胞共培养后,产生的趋化因子ccl5的情况。
[0073]
图16显示母乳低聚糖与巨噬细胞共培养后,产生的趋化因子ccl20的情况。
具体实施方式
[0074]
为了对本发明的技术特征、目的和有益效果有更加清楚的理解,现结合具体实施例及对本发明的技术方案进行以下详细说明,应理解这些实例仅用于说明本发明而不用于限制本发明的范围。实施例中,各原始试剂材料均可商购获得,未注明具体条件的实验方法为所属领域熟知的常规方法和常规条件,或按照仪器制造商所建议的条件。
[0075]
实施例1
[0076]
本实施例提供一种粉状婴幼儿配方食品,其中总蛋白质含量为11.1g/100g粉,脂肪含量为28.0g/100g粉;碳水化合物含量为53.0g/100g粉;母乳低聚糖含量70.9mg/100g粉。
[0077]
本实施例的婴幼儿配方食品由以下重量份的原料复配实现:
[0078]
生牛乳1000份,乳糖327份,葵花籽油137份,大豆油56份,玉米油31份,脱盐乳清粉(d90)171份,乳清蛋白粉26份,乳清蛋白粉(wpc80)24份,酪蛋白21.5份,母乳低聚糖(3-sl)0.78份。
[0079]
本实施例的婴幼儿配方食品采用湿法工艺制备而成,主要包括:配料(包括添加hmo),均质,浓缩杀菌,喷雾干燥,得到成品。
[0080]
实施例2
[0081]
本实施例提供一种粉状婴幼儿配方食品,其中总蛋白质含量为8.5g/100g粉,脂肪含量为13.5g/100g粉;碳水化合物含量为75g/100g粉;母乳低聚糖含量606.1mg/100g粉。
[0082]
本实施例的婴幼儿配方食品由以下重量份的原料复配实现:
[0083]
全脂奶粉140份、乳清蛋白粉25份、脱脂奶粉120份;
[0084]
玉米油20份、大豆油40份、椰子油10份、低芥酸菜籽油30份;
[0085]
乳糖450份、麦芽糊精200份、固体玉米糖浆100份;
[0086]
母乳低聚糖(3-sl)6.73份。
[0087]
本实施例的婴幼儿配方食品采用干法生产工艺制备而成,主要包括:配料,预热,均质,浓缩杀菌,喷雾干燥,干混添加hmo,得到成品。
[0088]
实施例3
[0089]
本实施例提供一种粉状婴幼儿配方食品,其中总蛋白质含量为20g/100g粉,脂肪含量为30g/100g粉;碳水化合物含量为40g/100g粉;母乳低聚糖含量227.3mg/100g粉。
[0090]
本实施例的婴幼儿配方食品由以下重量份的原料复配实现:
[0091]
生牛乳1000份,脱脂奶粉240份,乳清蛋白粉25份;
[0092]
玉米油50份,大豆油65份,葵花籽油70份,椰子油50份和(或)低芥酸菜籽油70份;
[0093]
母乳低聚糖(6-sl)2.52份。
[0094]
本实施例的婴幼儿配方食品采用湿法工艺制备而成,主要包括:配料(包括添加hmo),均质,浓缩杀菌,喷雾干燥,得到成品。
[0095]
母乳低聚糖功效实验
[0096]
实验方法
[0097]
对单核细胞与巨噬细胞的采集与培养参照tang等人(2017,j.func.foods)及govers等人(2020,food funct.)所述。从三个健康的捐献者的血液中分离并获取原单核细胞,在单核细胞与m-csf培养七天后,可得到原单核细胞m0。此后用对照的培养液或hmo进行
激活:如果与tnfα和infγ培养24小时,可得到m1型的巨噬细胞;如果与il-4培养24小时,可以得到m2型巨噬细胞;本发明的实验组是将原单核细胞m0与hmo培养共24小时,得到的巨噬细胞记为“m(ndp)”,进行基因转录的测定,以分析巨噬细胞的表型变化(看是否向更成熟的m1和m2表型转变)。本发明中同时分析了巨噬细胞产生的趋化因子,并进行迁移测试。
[0098]
具体血样采集与培养的实验条件如下所述:
[0099]
使用生产商推荐的操作方法,采用quadromacs系统和cd14 microbeads磁珠分选试剂盒(miltenyi biotec,莱顿,荷兰),从健康的捐献者血样中获得血沉棕黄层(从全血样离心分离获取的含白细胞和血小板的部分)。采集血样前,获得了捐献者的书面同意。在添加了10%胎牛血清(fbs,hyclone,埃因霍温,荷兰),1%mem非必需氨基酸(gibco布雷斯维克,荷兰),1%丙酮酸钠(lonza,布雷达,荷兰),1%青霉素/链霉素(sigma,圣路易斯,密苏里州,美国)和50ng/ml mcsf(r&d systems,明尼安那波利斯,明尼苏达州,美国)的rpmi 1640
–
glutamax培养基(gibco,布雷斯维克,荷兰)中,以1
×
106细胞/2ml/孔的浓度在24孔板培养7天后,单核细胞分化为巨噬细胞。在培养3天和5天后,一半培养基被替换为含有100ng/ml mcsf的培养基。在第7天,将培养基替换为不添加任何其他物质的培养基,则巨噬细胞极化为m0;将培养基替换为含有20ng/ml tnf-α和20ng/ml inf-γ(r&d systems,明尼安那波利斯,明尼苏达州,美国)的培养基,则巨噬细胞极化为m1;将培养基替换为含有20ng/ml il-4(r&d systems,明尼安那波利斯,明尼苏达州,美国)的培养基,则巨噬细胞极化为m2;另外将受试物质hmo以0.1mg/ml的浓度添加,与巨噬细胞在不含有mcsf培养基条件下,培养24小时。
[0100]
脂多糖检测
[0101]
分析hmo产生的脂多糖(lps)含量,当产生的脂多糖满足促使巨噬细胞响应的检测限以下,则可用于后续实验。
[0102]
对脂多糖lps的检测参考govers等人(2016,bioact.carbohydr.diet.fibre.)所述。为测定脂多糖,使用了0.1mg/ml浓度。一个内毒素单元对应着0.1到0.2pg lps,取决于lps的种类,并估计为可反映0.2pg lps。
[0103]
巨噬细胞存活率测试
[0104]
为了检测激活后巨噬细胞的活性,用不含有钙/镁的pbs冲洗巨噬细胞。用edta-胰蛋白酶解离巨噬细胞,离心并用含有钙/镁的pbs冲洗。用培养基处理过的巨噬细胞被分到两个试管(1个作为不染色的对照),所有细胞重新悬混于含有5微升7-aad(染色剂)的pbs中,孵育10分钟,用流式细胞仪检测。
[0105]
当细胞死亡后,或正在经历凋亡时,细胞膜表面会有孔,7-aad可以通过这些孔进入到细胞内并连接到dna上。将巨噬细胞暴露于添加了hmo的环境中,收获细胞并加入7-aad。用流式细胞仪洗去并测量产生的荧光信号。所有细胞都有一定程度的背景荧光产生,因此与没有染色的对照相比,即使没有任何受试物质引起的激发,都会有些微增加的荧光信号。所以微量的阳性染色并不是一个负面的信号,而仅仅是细胞本身产生的背景荧光。如果受试物质导致了细胞死亡,那么百分比将会在20-100%的区间。
[0106]
基因表达与炎症因子测试
[0107]
分离原单核细胞,使其向m0分化。之后将细胞与不同的hmo单体一起培养。分析细胞活性,分析培养基中趋化因子的产生。将rna提取后,进行cdna的合成,使用qpcr进行检
测,采用m1、m2和m(ndp)的特定序列来分析基因表达。采用已建立的m1的标记物和m2的标记物的倍数变化来表征受试物质是否可引起巨噬细胞向m1或m2的表型分化。
[0108]
巨噬细胞基因转录的测量通过以下步骤完成:使用trizol、rneasy和dnase qiagen试剂盒,获取rna,如tang等人(2017,j.funct.foods)所述。用通常被认为是m1型表达的基因(ido1,lamp3,gch1,cxcl11,以及gbp5)以及m2型表达的基因(cd209,chdh,dcir,il-17rb,以及mgl)标记物,使用q-pcr来检测基因表达,对基因标记物的选取同样如tang等人(2017,j.funct.foods)(参考基因actb,rplp0)所述。
[0109]
使用multi-plex试剂盒(legendplex人促炎症趋化因子试剂组),在被激活的巨噬细胞的上清液测定分泌的细胞因子含量。
[0110]
数据分析
[0111]
对于数据结果进行双样本双侧t检验(two tailed,paired t-test)。两个组若有显著性差异,且p《0.05,则用星号*表示。
[0112]
各母乳低聚糖对lps产生的实验结果
[0113]
当脂多糖浓度在20pg/ml以上时,巨噬细胞会有强烈的反应。因此该检测的目的是控制巨噬细胞与hmo共培养时,产生的脂多糖,减少对后续测试的影响。检测结果参见表1。当峰值在50%到200%之间时,是经过验证可信的峰值区间。可见,当hmo的浓度在0.1mg/ml时,产生的脂多糖浓度是低于阈值的。
[0114]
表1
[0115]
hmolps(pg/0.1mg)spike(%)2-fl0.81193-fl10.91273-sl15.9996-sl18.4144lnt15.2120
[0116]
各母乳低聚糖对巨噬细胞7-aad染色实验结果
[0117]
实验前准备步骤及具体实验方法请见前述段落。
[0118]
若受试物质会引起细胞死亡,那么在流式细胞仪产生的图像上,会在较高的峰右边产生一个一定高度的峰,并可由此算出死亡的细胞占的百分比。
[0119]
检测结果参见图1所示,受试物质引起的第二个峰是极其微小的,肉眼几乎看不见。同时也算出被各种hmo单体激发的巨噬细胞,其产生的死亡细胞的百分比基本上不超过1%(表2)。因此可以认为与hmo共培养不会杀死巨噬细胞,巨噬细胞生长状况是较好的。
[0120]
表2
[0121]
%medium(m0)m1m22-fl3-fl3-sl6-sllnthd961.060.750.570.510.610.960.370.67hd972.380.470.80.690.680.370.711.04hd980.440.50.90.750.870.570.570.99
[0122]
各母乳低聚糖对于巨噬细胞基因表型影响的测试
[0123]
本实施例检测了各母乳低聚糖对于巨噬细胞基因表型影响。测试结果参见图2和图3。如图2所示,根据在先研究确定了m1和m2型巨噬细胞特有的基因表型及其标记物分子。
将不同的hmo单体与巨噬细胞共培养后,发现3-sl和6-sl能影响巨噬细胞的基因表型,使其分别更偏向于m1和m2的表型(图3),而其他三种受试的hmo(2
’‑
fl、3-fl和lnt)并无此作用。
[0124]
各母乳低聚糖与巨噬细胞共培养产生的趋化因子测试
[0125]
本实施例检测了各母乳低聚糖与巨噬细胞共培养产生的趋化因子的表达情况。各趋化因子据现有技术报道的主要功效参见表3。
[0126]
表3
[0127][0128]
测试结果参见图4至图16。
[0129]
ccl2是一个重要的单核细胞趋化因子,对单核细胞和嗜碱性粒细胞有趋化性,但对嗜中性粒细胞和嗜酸性粒细胞没有趋化性。如图4所示,受试的母乳低聚糖单体并不会影响ccl2这个趋化因子的释放。
[0130]
ccl11参与过敏应答,是嗜酸性粒细胞的趋化因子。如图5所示,对于ccl11趋化因子,hmo只导致了很低的释放,影响非常微小。
[0131]
ccl17是典型的m2巨噬细胞亚群的标记物分子,其是t细胞的趋化因子,不是单核细胞或粒细胞的趋化因子。如图6所示,在所有受试的hmo但体重,只有3-sl和6-sl一定程度地影响了ccl17的释放。
[0132]
cxcl9、cxcl10和cxcl11是典型的m1巨噬细胞亚群标记物分子,如图7至图9所示,所有受试hmo中,只有3-sl和6-sl影响了它们的释放,且以cxcl10和cxcl11更为显著。但与m1亚群巨噬细胞的释放量比起来,这两种hmo刺激巨噬细胞后所产生的这些趋化因子含量相对较低。
[0133]
如图10至图16所示,3-sl和6-sl在与巨噬细胞共培养后,显著地影响了其他一系列趋化因子的释放,包括cxcl1、cxcl5、cxcl8、ccl3、ccl4、ccl5、ccl20等。
[0134]
从以上实验结果可以得出,单核细胞趋化因子ccl2不会受到hmo的影响。3-sl和6-sl可支持释放cxcl8,ccl5,ccl3,cxcl5,ccl20,cxcl1与ccl4等。这些趋化因子可支持吸引更多的免疫细胞,比如可能包括单核细胞等。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。