1.本发明涉及一类5-脂肪杂环基-3-羟基吡啶-2-甲酰基甘氨酸类化合物、制备方法、药物组合物和应用,尤其涉及一类可有效抑制脯胺酰羟化酶2的5-脂肪杂环基-3-羟基吡啶-2-甲酰基甘氨酸类化合物、制备方法、药物组合物和应用。
背景技术:
2.慢性肾病(chronic kidney disease,ckd)是一类进行性、不可逆的以患者的gfr小于60ml/min/1.73m2为最主要特征,伴有不同类型并发症的慢性疾病。贫血是慢性肾病较为严重的并发症,故由慢性肾病所诱发的贫血又名肾性贫血。肾性贫血的诱因是患有慢性肾病病人内源性的红细胞生成素(erythropoietin,epo)分泌不足和长期处于炎症状态所导致的功能性铁缺乏。epo是人体红细胞生成通路中最为重要的激素,其主要功能为促进原成红细胞向成熟的红细胞分化并抑制前者在这过程之中的凋亡,提高机体血液中的红细胞数目,从而增强机体对缺氧的耐受。epo在人体内主要由肾脏的epo生成间质细胞分泌,然而由于疾病,慢性肾病患者的epo生成细胞转变为肌成纤维细胞,丧失了分泌该种激素的能力。此外,患者长期的炎症反应会诱导肝脏分泌铁调素,铁调素会降解与铁代谢相关的膜铁转运蛋白、转铁素等蛋白,导致机体发生功能铁缺乏。
3.肾性贫血的治疗主要围绕提高患者红细胞数目、促进患者epo分泌和改善患者铁代谢稳态展开。其对应的治疗策略大致上可分为输血治疗与药物治疗。输血治疗可直接提高患者的血红蛋白水平,而药物治疗主要关注促进患者的epo分泌或补充患者缺乏的内源性epo并改善患者的铁代谢。治疗肾性贫血的药物可大致分为大分子重组促红细胞生成素(recombinant human erythropoietin,rhuepo)和小分子脯氨酸羟化酶2抑制剂、转录因子gata抑制剂、造血干细胞磷酸酶抑制剂等。
4.尽管使用外源性的rhuepo可以有效地发挥内源性epo的作用,促进患者红细胞生成。然而,该类药物给药方式的限制所导致的患者的低顺应性以及长期服用药物所导致的严重的心血管不良事件的风险在一定程度上限制了其使用。此外,单独使用rhuepo无法纠正患者的铁缺乏状态,患者需要额外补充铁剂。因此,寻找具有新机制的治疗药物,以在纠正患者内源性epo生成不足的情况下改善患者的铁代谢,成为了一个迫切的需求。
技术实现要素:
5.发明目的:针对现有化合物疗效受限、顺应性差、易发生不良反应等不足,本发明旨在提供一类针对脯胺酰羟化酶2蛋白靶点的高效、低毒的5-脂肪杂环基-3-羟基吡啶-2-甲酰基甘氨酸类化合物、制备方法、药物组合物和应用。
6.技术方案:作为本发明涉及的第一方面,本发明的5-脂肪杂环基-3-羟基吡啶-2-甲酰基甘氨酸类化合物具有式(i)的结构,所述化合物包含其药学上可接受的盐:
[0007][0008]
其中:
[0009]
a选自含有一个氮原子的5~7元饱和或者不饱和的脂肪杂环,所述脂肪杂环的碳原子与吡啶环相连;
[0010]
为单键或双键;
[0011]
ar选自5~6元单环芳基或杂芳基或者含有8~10个环原子的双环芳基或杂芳基,其中,所述杂芳基含有1~4个氮、氧或硫原子;
[0012]
l选自单键或含有1~3个亚甲基、氮、氧、砜基、羰基或脲基的连接链;
[0013]
r1选自氢、甲基或氯原子;
[0014]
r2选自一个或多个c
1-c3烷基、c
1-c3烷氧基、c
1-c3烷氨基、c
1-c3酰胺基、c
1-c3卤代烷基、卤素、氰基、羟基或氨基取代的ar。
[0015]
优选,所述化合物结构中:
[0016]
所述结构中:
[0017]
a选自
[0018]
l选自单键l选自单键
[0019][0020]
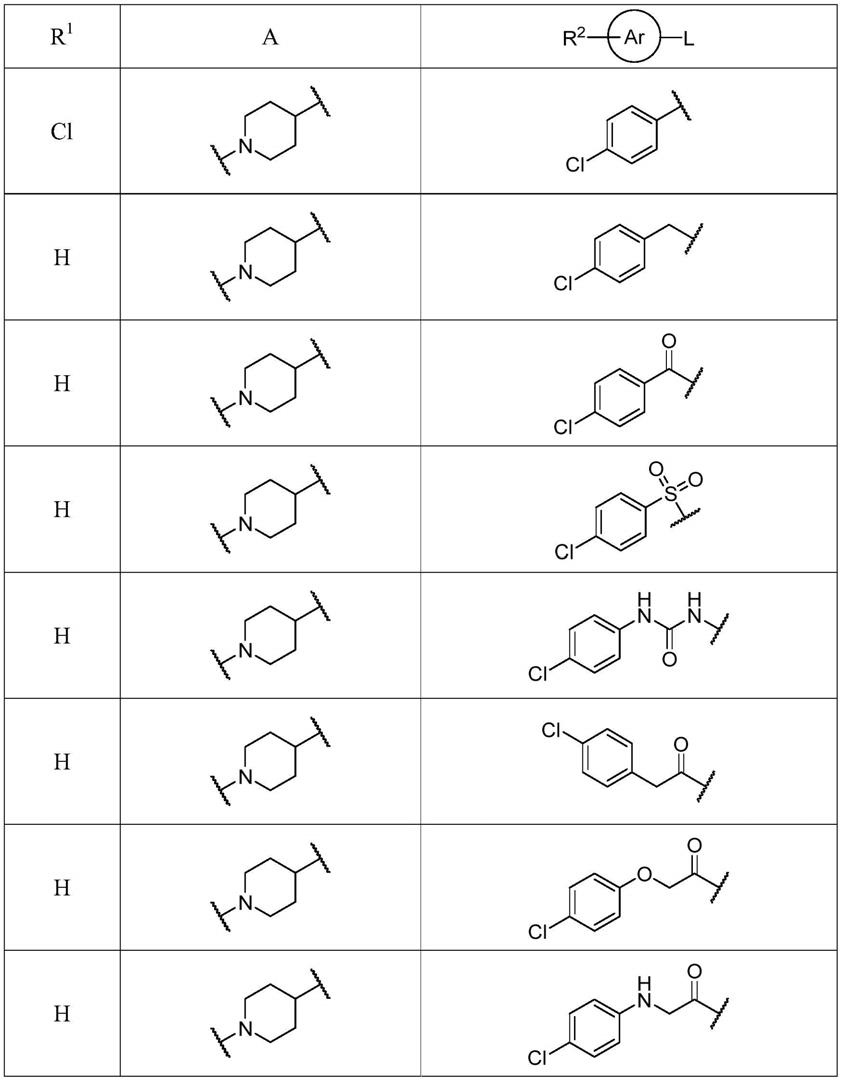
更具体地,上述5-脂肪杂环基-3-羟基吡啶-2-甲酰基甘氨酸类化合物选自以下任一化合物:
[0021]
[0022]
[0023]
[0024]
[0025]
。
[0026]
上述5-脂肪杂环基-3-羟基吡啶-2-甲酰基甘氨酸类化合物的药学上可接受的盐为所述化合物与酸或碱形成的盐,所述酸为盐酸、氢溴酸、硫酸、磷酸、甲磺酸、苯磺酸、对甲苯磺酸、萘磺酸、柠檬酸、苹果酸、酒石酸、乳酸、丙酮酸、乙酸、马来酸、琥珀酸、富马酸、水杨酸、苯基乙酸或杏仁酸;所述碱为含有碱性金属阳离子、碱土金属阳离子或铵阳离子盐的无机碱,胆碱、二乙醇胺或吗啉。
[0027]
作为本发明涉及的第二方面,上述5-脂肪杂环基-3-羟基吡啶-2-甲酰基甘氨酸类化合物的制备方法为:
[0028]
化合物(ii)经偶联、脱保护、取代、脱保护、水解反应得到化合物(i);
[0029][0030]
具体地,化合物(ii)与带有保护基的杂环硼酸酯片段在碱和催化剂的条件下偶联,其中碱选自碳酸铯、磷酸钾、碳酸钾、碳酸钠等,催化剂可选自1,1-双二苯基膦二茂铁二氯化钯、双三苯基膦二氯化钯、四(三苯基膦)钯等。优选1,1-双二苯基膦二茂铁二氯化钯和碳酸铯的组合。中间体(iii)在三氟乙酸条件下脱去叔丁氧羰基保护基得中间体(iv);中间体(iv)与带有不同连接链的片段反应得中间体(v);中间体(v)在四氯化钛、钯/碳条件下脱去苄基保护基或还原双键得中间体(vi);中间体(vi)经酯水解得通式(i)化合物。
[0031]
其中,a、ar、r1、r2的定义如前所述;
[0032]
将相应的酸或碱与以上方法制备的化合物(i)成盐,即得所述化合物的药学上可接受的盐。
[0033]
作为本发明涉及的第三方面,本发明的药物组合物包含上述5-脂肪杂环基-3-羟基吡啶-2-甲酰基甘氨酸类化合物以及药学上可接受的载体。
[0034]
上述5-脂肪杂环基-3-羟基吡啶-2-甲酰基甘氨酸类化合物可以添加药学上可接受的载体制成常见的药用制剂,如片剂、胶囊、糖浆、悬浮剂或注射剂,制剂可以加入香料、甜味剂、液体/固体填料、稀释剂等常用药用辅料。
[0035]
作为本发明涉及的第四方面,上述化合物及其药物组合物可作为脯胺酰羟化酶2抑制剂药物,用于治疗贫血症或缺血性疾病;其中,贫血症选自由肾炎、肾损伤、类风湿性关节炎、风湿热、炎症性肠道疾病以及肿瘤化疗引起的贫血症;缺血性疾病选自缺血性脑卒中或心肌缺血相关疾病。
[0036]
有益效果:与现有技术相比,本发明具有如下显著优点:
[0037]
(1)该类化合物和药物组合物可有效抑制脯胺酰羟化酶2蛋白的活性,从而提高细胞内hif-2α的量,进一步促进细胞内epo基因的转录并提高血浆中的epo浓度,最终促进机
体的红细胞生成,ic
50
值最优达到纳摩尔浓度级别;
[0038]
(2)该类化合物和药物组合物应用广泛,可制备为治疗贫血症或缺血性疾病药物;所述药物在分子水平、细胞水平和动物水平均可以发挥药效,并且治疗效果更优异,无明显的细胞毒性;
[0039]
(3)化合物制备方法简便可行。
附图说明
[0040]
图1为化合物对人体肝癌细胞株hep3b的细胞毒性结果;
[0041]
图2为化合物促进hif-α下游epo基因表达结果;
[0042]
图3为化合物对体内血浆网织红细胞提升结果。
具体实施方式
[0043]
下面结合实施例对本发明的技术方案作进一步说明。
[0044]
实施例1:(5-(1-叔丁氧羰基-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯
[0045]
(3-苄氧基-5-溴-3-羟基吡啶甲酰基)甘氨酸甲酯(2g,5.27mmol)溶于40ml1,4-二氧六环中,加入n-boc-1,2,5,6-四氢吡啶-4-硼酸频哪醇酯(1.79g,5.8mmol),pd(dppf)2cl2(115mg,0.158mmol),2m cs2co3溶液(5.16g,15.82mmol)10ml,升温至100℃,氮气氛下反应1小时30分钟。反应完毕,将反应液抽滤除去钯催化剂,滤液依次使用乙酸乙酯(80ml
×
3)萃取,饱和氯化钠溶液(100ml)洗涤。合并有机相,无水硫酸钠干燥,减压蒸除溶剂,粗品采用硅胶柱层析分离纯化(石油醚:乙酸乙酯=1:1),得产物为米白色粉末(1.12g,44.1%)。mp 125.6
–
126.5℃1h nmr(400mhz,dmso-d6)δ8.80(t,j=6.0hz,1h),8.33
–
8.27(m,1h),7.68(s,1h),7.54(d,j=7.5hz,2h),7.40(t,j=7.5hz,2h),7.32(t,j=7.3hz,1h),6.41(s,1h),5.29(s,2h),4.09
–
4.00(m,4h),3.65(s,3h),3.56(d,j=5.8hz,2h),2.50(s,2h),1.44(s,9h).esi-ms:m/z 482[m h]
.
[0046]
实施例2:(5-(1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯
[0047]
(5-(n-叔丁氧羰基-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(1.2g,2.49mmol)溶于30ml二氯甲烷中,冷却至0℃,加入三氟乙酸(3.7ml,49.84mmol),氮气氛下室温反应2小时。反应完毕,加入冰水(10ml)将反应淬灭,反应液使用二氯甲烷(30ml
×
3)萃取,饱和氯化钠溶液(30ml)洗涤。合并有机相,无水硫酸钠干燥,减压蒸除溶剂,粗品使用溶剂(石油醚:乙酸乙酯=20:1)重结晶,得产物为米白色粉末(810mg,85.2%)。mp 113.7
–
114.8℃ 1
h nmr(400mhz,dmso-d6)δ8.79(t,j=6.1hz,1h),8.28(d,j=1.7hz,1h),7.62(d,j=1.8hz,1h),7.53(d,j=7.0hz,2h),7.40(t,j=7.5hz,2h),7.32(t,j=7.3hz,1h),6.47(td,j=3.5,1.8hz,1h),5.30(s,2h),4.04
–
4.00(m,2h),3.65(s,3h),3.42
–
3.40(m,2h),2.93(t,j=5.6hz,2h),2.38(dt,j=6.0,3.0hz,2h).esi-ms:m/z 382[m h]
.
[0048]
实施例3:(6-氯-5-(1-(4-氯苯基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0049]
(6-氯-5-(1-(4-氯苯基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯
[0050]
(6-氯-5-(1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(100mg,0.26mmol)溶于5ml甲苯中,加入4-氯溴苯(55mg,0.28mmol),醋酸钯(2.94mg,0.013mmol),binap(7.97mg,0.015mmol),碳酸铯(256mg,0.78mmol)100℃下反应10小时。反应完毕,抽滤除去钯催化剂,减压蒸除溶剂,粗品使用硅胶柱层析分离纯化(石油醚:乙酸乙酯=1:2),得产物为米白色粉末(47mg,36.4%)。mp 182.4
–
183.7℃.1h nmr(400mhz,chloroform-d)δ8.46(d,j=1.4hz,1h),8.31(t,j=9.8hz,1h),7.61(d,j=1.4hz,1h),7.45
–
7.21(m,8h),6.99
–
6.92(m,2h),6.36(tt,j=6.2,1.0hz,1h),5.20(t,j=1.0hz,2h),4.16(d,j=9.8hz,2h),4.07(dt,j=6.1,1.0hz,2h),3.66(s,3h),3.53(t,j=7.1hz,2h),3.21(tq,j=7.3,1.0hz,2h).
[0051]
(6-氯-5-(1-(4-氯苯基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯
[0052]
(6-氯-5-(1-(4-氯苯基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(20mg,0.041mmol)溶于5ml四氢呋喃中,加入钯/碳5mg,氢气氛下反应8小时。反应结束,抽滤除去钯/碳,减压蒸除溶剂,粗品使用硅胶柱层析分离纯化(石油醚:乙酸乙酯=2:1),得产物为淡黄色粉末(13mg,78.1%)。mp 195.6
–
196.8℃.1h nmr(400mhz,chloroform-d)δ8.33(t,j=9.7hz,1h),8.27(dd,j=1.5,0.7hz,1h),7.35(dd,j=1.4,0.6hz,1h),7.29
–
7.21(m,2h),6.95
–
6.87(m,2h),4.13(d,j=9.8hz,2h),3.72(s,3h),3.56
–
3.41(m,5h),2.98
–
2.86(m,1h),2.31
–
2.13(m,4h).
[0053]
(6-氯-5-(1-(4-氯苯基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0054]
(6-氯-5-(1-(4-氯苯基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(10mg,0.022mmol)溶于3ml四氢呋喃,加入1ml水,一水合氢氧化锂(4.7mg,0.11mmol),室温下反应30分钟。反应完毕,减压蒸除反应液中的四氢呋喃,冰浴条件下加入1mol/l稀盐酸至有固体析出,抽滤干燥,得米白色粉末(8mg,82.6%)。mp 225.6
–
227.1℃.1h nmr(400mhz,dmso-d6)δ8.36(t,j=10.2hz,1h),8.23(dd,j=1.4,0.6hz,1h),7.36(dd,j=1.4,0.6hz,1h),7.28
–
7.21(m,2h),6.95
–
6.88(m,2h),4.06(d,j=10.3hz,2h),3.68(dt,j=12.4,7.1hz,2h),3.32(dt,j=12.3,7.1hz,2h),2.97
–
2.85(m,1h),2.11(qd,j=7.1,1.9hz,4h).hrms(esi):390.1211[m h]
.
[0055]
实施例4:(5-(1-(4-氯苄基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0056]
(5-(1-(4-氯苄基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯
[0057]
(5-(1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(100mg,0.26mmol)溶于5ml乙腈中,加入4-氯溴苄(59mg,0.28mmol),碳酸钾(49mg,0.35mmol),室温下反应6小时。反应完毕,抽滤除去碳酸钾,减压蒸除溶剂得淡黄色油状粗品,不经纯化直接用于下一步反应。
[0058]
(5-(1-(4-氯苄基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯
[0059]
制备方法同实施例3,原料改用(5-(1-(4-氯苄基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(131mg,0.26mmol),得产物为淡黄色粉末(20mg,18.4%)。mp 85.6
–
86.9℃.1h nmr(400mhz,dmso-d6)δ12.13(s,1h),9.41(t,j=6.2hz,1h),8.14(s,1h),7.38(t,j=8.3hz,4h),7.30(s,1h),4.07(d,j=6.2hz,2h),3.67(s,3h),3.50(s,2h),2.91(d,j=11.0hz,2h),2.64(s,1h),2.06(t,j=11.2hz,2h),1.80
–
1.66(m,
4h).
[0060]
(5-(1-(4-氯苄基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0061]
制备方法同实施例3,原料改用(5-(1-(4-氯苄基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(16mg,0.038mmol),得米白色粉末(5.8mg,37.5%)。mp 231.4
–
234.2℃.1h nmr(400mhz,dmso-d6)δ12.24(s,1h),9.24
–
9.18(m,1h),8.13(s,1h),7.40(d,j=8.2hz,2h),7.36(d,j=8.1hz,2h),7.29(s,1h),3.95(d,j=6.1hz,2h),3.51(s,2h),2.92(d,j=11.0hz,2h),2.64(s,1h),2.08(t,j=11.2hz,2h),1.78(d,j=13.1hz,2h),1.74
–
1.67(m,2h).hrms(esi):404.1357[m h]
.
[0062]
实施例5:(5-(1-(4-氯苯甲酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0063]
(5-(1-(4-氯苯甲酰基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯
[0064]
(5-(1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(140mg,0.36mmol)溶于5ml二氯甲烷中,加入4-氯苯甲酰氯(70mg,0.40mmol),三乙胺(55mg,0.5mmol),室温下反应6小时。反应完毕,加入饱和碳酸氢钠溶液(10ml)将反应淬灭,反应液使用二氯甲烷(10ml
×
3)萃取,饱和氯化钠溶液(10ml)洗涤。合并有机相,无水硫酸钠干燥,减压蒸除溶剂,粗品使用硅胶柱层析分离纯化(石油醚:乙酸乙酯=1:4),得产物为白色粉末(120mg,63.7%)。mp197.8
–
198.6℃.1h nmr(400mhz,dmso-d6)δ8.81(t,j=6.1hz,1h),8.34
–
8.28(m,1h),7.70(s,1h),7.54(q,j=8.6hz,6h),7.40(t,j=7.5hz,2h),7.32(t,j=7.2hz,1h),6.42(d,j=88.2hz,1h),5.29(s,2h),4.32(s,1h),4.09(d,j=24.8hz,1h),4.02(d,j=6.0hz,2h),3.85(d,j=15.1hz,1h),3.65(s,3h),3.55(s,1h),2.62(s,2h).
[0065]
(5-(1-(4-氯苯甲酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯
[0066]
制备方法同实施例3,原料改用(5-(1-(4-氯苯甲酰基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(100mg,0.19mmol),得产物为白色胶状物(60mg,72.3%)。1h nmr(400mhz,chloroform-d)δ11.75(s,1h),8.38(t,j=5.7hz,1h),8.01(d,j=1.9hz,1h),7.42(d,j=3.0hz,4h),7.16(d,j=1.9hz,1h),4.90(s,1h),4.26(d,j=5.7hz,2h),3.83(s,3h),3.14(s,1h),2.87(tt,j=12.1,3.6hz,2h),1.63(s,4h).
[0067]
(5-(1-(4-氯苯甲酰基-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0068]
制备方法同实施例3,原料改用(5-(1-(4-氯苯甲酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(60mg,0.13mmol),得米白色粉末(56mg,96.5%)。mp220.0
–
220.9℃.1h nmr(400mhz,dmso-d6)δ12.80(s,1h),12.25(s,1h),9.27(t,j=6.2hz,1h),8.16(d,j=1.8hz,1h),7.54
–
7.45(m,4h),7.39(d,j=1.9hz,1h),4.63(s,1h),3.98(d,j=6.1hz,2h),3.64(s,1h),3.16(s,1h),2.95(s,1h),2.85(s,1h),1.88(s,1h),1.77
–
1.65(m,3h).hrms(esi):418.1173[m h]
.
[0069]
实施例6:(5-(1-((4-氯苯基)磺酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸(5-(1-((4-氯苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯
[0070]
(5-(1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(230mg,0.60mmol)溶于5ml二氯甲烷中,加入4-氯苯磺酰氯(140mg,0.66mmol),n,n-二异丙基乙胺(170mg,1.33mmol),室温下反应6小时。反应完毕,加入饱和碳酸氢钠溶液(10ml)将反应淬
灭,反应液使用二氯甲烷(10ml
×
3)萃取,饱和氯化钠溶液(10ml)洗涤。合并有机相,无水硫酸钠干燥,减压蒸除溶剂,粗品使用硅胶柱层析分离纯化(石油醚:乙酸乙酯=1:3),得产物为米白色粉末(220mg,65.8%)。mp 187.9
–
188.9℃.1h nmr(400mhz,dmso-d6)δ8.79(t,j=6.1hz,1h),8.22(d,j=1.7hz,1h),7.86(d,j=8.7hz,2h),7.74(d,j=8.6hz,2h),7.61(d,j=1.8hz,1h),7.52(d,j=6.8hz,2h),7.39(t,j=7.4hz,2h),7.32(t,j=7.3hz,1h),6.36
–
6.32(m,1h),5.26(s,2h),4.01(d,j=6.1hz,2h),3.77(q,j=2.9hz,2h),3.64(s,3h),3.29(t,j=5.7hz,2h),2.59(s,2h).
[0071]
(5-(1-((4-氯苯基)磺酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯
[0072]
制备方法同实施例3,原料改用(5-(1-((4-氯苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(200mg,0.35mmol),得产物为米白粉末(123mg,73.8%)。mp 207.3
–
208.6℃.1h nmr(400mhz,dmso-d6)δ12.14(s,1h),9.41(t,j=6.2hz,1h),8.08(d,j=1.8hz,1h),7.78(q,j=8.7hz,4h),7.29(d,j=1.8hz,1h),4.07(d,j=6.2hz,2h),3.79(d,j=11.3hz,2h),3.66(s,3h),2.69
–
2.61(m,1h),2.36
–
2.27(m,2h),1.86(d,j=12.6hz,2h),1.81
–
1.69(m,2h).
[0073]
(5-(1-((4-氯苯基)磺酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0074]
制备方法同实施例3,原料改用(5-(1-((4-氯苯基)磺酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(120mg,0.25mmol),得米白色粉末(102mg,87.9%)。mp 220.3
–
221.7℃.1h nmr(300mhz,dmso-d6)δ12.37(s,1h),9.09(s,1h),8.07(d,j=5.3hz,1h),7.78(q,j=9.1,8.5hz,4h),7.27(s,1h),3.82(s,2h),3.76(s,2h),2.64(s,1h),2.30(d,j=11.9hz,2h),1.80(d,j=21.7hz,4h).hrms(esi):454.0842[m h]
.
[0075]
实施例7:(5-(1-((4-氯苯基)氨基甲酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0076]
(5-1-((4-氯苯基)氨基甲酰基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯
[0077]
(5-(1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(190mg,0.49mmol)溶于5ml二氯甲烷中,加入4-硝基苯基(4-氯苯基)氨基甲酸酯(145mg,0.49mmol),三乙胺(170mg,1.33mmol),室温下反应6小时。反应完毕,将反应液抽滤,滤饼使用二氯甲烷(10ml
×
3)洗涤,干燥,得产物为白色粉末(136mg,51.8%)。mp 192.2
–
199.0℃.1h nmr(400mhz,dmso-d6)δ8.81(t,j=6.1hz,1h),8.74(s,1h),8.33(d,j=1.7hz,1h),7.70(d,j=1.8hz,1h),7.58
–
7.51(m,4h),7.43
–
7.38(m,2h),7.32(dd,j=13.3,8.1hz,3h),6.49(s,1h),5.31(s,2h),4.20(d,j=3.6hz,2h),4.03(d,j=6.0hz,2h),3.70(t,j=5.4hz,2h),3.65(s,3h),2.59(s,2h).
[0078]
(5-(1-((4-氯苯基)氨基甲酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯
[0079]
制备方法同实施例3,原料改用(5-(1-((4-氯苯基)氨基甲酰基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(127mg,0.23mmol),得产物为白色粉末(60mg,56.6%)。mp 163.8
–
164.0℃.1h nmr(400mhz,dmso-d6)δ12.14(s,1h),9.45(s,1h),8.67(s,1h),8.16(s,1h),7.53(d,j=9.9hz,2h),7.34(s,1h),7.31
–
7.23(m,2h),4.29(d,j=13.1hz,2h),4.07(d,j=6.1hz,2h),3.67(d,j=3.8hz,3h),2.87(d,j=12.7hz,3h),
1.85(d,j=12.6hz,2h),1.64(q,j=10.8,9.4hz,2h).
[0080]
(5-(1-((4-氯苯基)氨基甲酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0081]
制备方法同实施例3,原料改用(5-(1-((4-氯苯基)氨基甲酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(60mg,0.13mmol),得米白色粉末(55mg,94.8%)。mp 231.8
–
234.2℃.1h nmr(400mhz,dmso-d6)δ12.26(s,1h),9.28(t,j=6.1hz,1h),8.71(s,1h),8.16(d,j=2.3hz,1h),7.53(d,j=6.7hz,2h),7.34(d,j=2.3hz,1h),7.29(s,2h),4.30(d,j=13.0hz,2h),3.98(dd,j=6.3,2.1hz,2h),2.88(t,j=12.7hz,3h),1.84(d,j=12.8hz,2h),1.65(t,j=12.2hz,2h).hrms(esi):433.1273[m h]
.
[0082]
实施例8:(5-(1-(2-(4-氯苯基)乙酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0083]
(5-(1-(2-(4-氯苯基)乙酰基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯
[0084]
(5-(1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(100mg,0.26mmol)溶于5ml n,n-二甲基甲酰胺中,加入4-氯乙酸(51mg,0.30mmol),n,n-二异丙基乙胺(168mg,1.30mmol),tbtu(126mg,0.40mmol)室温下反应10小时。反应完毕,加入饱和氯化铵溶液(10ml)将反应淬灭,反应液使用二氯甲烷(10ml
×
3)萃取,饱和氯化钠溶液(10ml)洗涤。合并有机相,无水硫酸钠干燥,减压蒸除溶剂,粗品使用硅胶柱层析分离纯化(石油醚:乙酸乙酯=1:4),得产物为淡黄色胶状物(60mg,42.8%)。1h nmr(400mhz,chloroform-d)δ8.45(d,j=1.6hz,1h),8.29(t,j=9.7hz,1h),7.62(d,j=1.4hz,1h),7.45
–
7.25(m,10h),6.35(tt,j=6.1,1.0hz,1h),5.19(t,j=1.0hz,2h),4.16(d,j=9.8hz,2h),3.97(dt,j=6.1,1.0hz,1h),3.74(dt,j=6.3,1.0hz,1h),3.71
–
3.63(m,7h),3.11(tq,j=7.0,1.0hz,2h).
[0085]
(5-(1-(2-(4-氯苯基)乙酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯
[0086]
制备方法同实施例3,原料改用(5-(1-(2-(4-氯苯基)乙酰基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(60mg,0.11mmol),得产物为白色胶状物(40mg,79.8%)。1h nmr(400mhz,chloroform-d)δ11.74(s,1h),8.37(s,1h),7.96(s,1h),7.30
–
7.26(m,3h),7.09(s,1h),6.95
–
6.91(m,2h),4.74(q,j=5.4,3.8hz,4h),4.35(dd,j=13.4,7.3hz,1h),4.26(dd,j=5.8,2.7hz,2h),4.16(d,j=13.8hz,1h),3.83(d,j=2.6hz,3h),3.80
–
3.72(m,1h),3.21(t,j=13.0hz,1h),2.79(dt,j=40.1,13.1hz,3h).
[0087]
((5-(1-(2-(4-氯苯基)乙酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0088]
制备方法同实施例3,原料改用(5-(1-(2-(4-氯苯基)乙酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(35mg,0.078mmol),得米白色粉末(20mg,60.6%)。mp 226.5
–
228.2℃.1h nmr(400mhz,dmso-d6)δ12.80(s,1h),12.26(s,1h),9.25(t,j=6.1hz,1h),8.11(d,j=1.9hz,1h),7.38(d,j=8.4hz,2h),7.28(dd,j=5.2,3.2hz,3h),4.56(d,j=12.9hz,1h),4.09(d,j=13.5hz,1h),3.96(d,j=6.0hz,2h),3.76(d,j=6.8hz,2h),3.09(t,j=12.6hz,1h),2.89(ddd,j=12.4,8.9,3.5hz,1h),2.63(t,j=12.6hz,1h),1.80(s,2h),1.51(dq,j=8.4,6.1,4.1hz,2h).hrms(esi):431.1246[m h]
.
[0089]
实施例9:(5-(1-(2-(4-氯苯氧基)乙酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0090]
(5-(1-(2-(4-氯苯氧基)乙酰基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯
[0091]
(5-(1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(50mg,0.13mmol)溶于5ml n,n-二甲基甲酰胺中,加入2-(4-氯苯氧基)乙酸(29mg,0.15mmol),n,n-二异丙基乙胺(84mg,0.65mmol),tbtu(63mg,0.20mmol)室温下反应10小时。反应完毕,加入饱和氯化铵溶液(10ml)将反应淬灭,反应液使用二氯甲烷(10ml
×
3)萃取,饱和氯化钠溶液(10ml)洗涤。合并有机相,无水硫酸钠干燥,减压蒸除溶剂,粗品使用硅胶柱层析分离纯化(石油醚:乙酸乙酯=1:4),得产物为白色胶状物(35mg,48.6%)。1h nmr(400mhz,chloroform-d)δ8.45(d,j=1.6hz,1h),8.29(t,j=9.7hz,1h),7.62(d,j=1.4hz,1h),7.45
–
7.23(m,8h),7.05
–
6.98(m,2h),6.35(tt,j=6.2,1.0hz,1h),5.19(t,j=1.0hz,2h),4.77(s,2h),4.16(d,j=9.8hz,2h),3.96(dt,j=6.1,1.0hz,1h),3.79
–
3.69(m,3h),3.66(s,3h),3.09(tq,j=7.1,1.0hz,2h).
[0092]
(5-(1-(2-(4-氯苯氧基)乙酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯
[0093]
制备方法同实施例3,原料改用(5-(1-(2-(4-氯苯氧基)乙酰基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(25mg,0.mmol),得产物为白色胶状物(16mg,76.1%)。1h nmr(400mhz,chloroform-d)δ11.74(s,1h),8.37(s,1h),7.96(s,1h),7.30
–
7.26(m,3h),7.09(s,1h),6.95
–
6.91(m,2h),4.74(q,j=5.4,3.8hz,4h),4.35(dd,j=13.4,7.3hz,1h),4.26(dd,j=5.8,2.7hz,2h),4.16(d,j=13.8hz,1h),3.83(d,j=2.6hz,3h),3.80
–
3.72(m,1h),3.21(t,j=13.0hz,1h),2.79(dt,j=40.1,13.1hz,3h).
[0094]
((5-(1-(2-(4-氯苯氧基)乙酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0095]
制备方法同实施例3,原料改用(5-(1-(2-(4-氯苯氧基)乙酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(10mg,0.021mmol),得米白色粉末(6mg,61.8%)。mp 226.5
–
228.2℃.1h nmr(400mhz,dmso-d6)δ12.83(s,1h),12.26(s,1h),9.27(t,j=6.1hz,1h),8.14(d,j=1.4hz,1h),7.35
–
7.31(m,3h),6.97(d,j=9.0hz,2h),4.88(s,2h),4.49(d,j=12.9hz,1h),3.97(d,j=6.0hz,3h),3.15(t,j=12.8hz,1h),2.94(ddd,j=11.9,8.4,3.5hz,1h),2.68(t,j=12.5hz,1h),1.84(d,j=11.0hz,2h),1.73(d,j=12.4hz,1h),1.54(q,j=11.7,11.2hz,1h).hrms(esi):447.1193[m h]
.
[0096]
实施例10:(5-(1-(2-(4-氯苯基)甘胺酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0097]
(5-(1-(2-(4-氯苯基)甘胺酰基))-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯
[0098]
(5-(1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(80mg,0.21mmol)溶于5ml n,n-二甲基甲酰胺中,加入4-氯苯基甘氨酸(46mg,0.25mmol),n,n-二异丙基乙胺(135mg,1.05mmol),tbtu(101mg,0.31mmol)室温下反应10小时。反应完毕,加入饱和氯化铵溶液(10ml)将反应淬灭,反应液使用二氯甲烷(10ml
×
3)萃取,饱和氯化钠溶液(10ml)洗涤。合并有机相,无水硫酸钠干燥,减压蒸除溶剂,粗品使用硅胶柱层析分离纯化(石油醚:乙酸乙酯=1:4),得产物为淡黄色胶状物(30mg,26.1%)。1h nmr(400mhz,chloroform-d)δ8.45(d,j=1.6hz,1h),8.29(t,j=9.7hz,1h),7.62(d,j=1.4hz,1h),
7.45
–
7.26(m,5h),7.19
–
7.12(m,2h),6.66
–
6.59(m,2h),6.35(tt,j=6.3,1.0hz,1h),5.59(t,j=7.3hz,1h),5.19(t,j=1.0hz,2h),4.16(d,j=9.8hz,2h),3.95(dt,j=6.1,1.0hz,1h),3.86(d,j=7.3hz,2h),3.80
–
3.69(m,3h),3.66(s,3h),3.10(tq,j=7.0,1.0hz,2h).
[0099]
(5-(1-(2-(4-氯苯基)甘氨酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯
[0100]
制备方法同实施例3,原料改用(5-(1-(2-(4-氯苯基)甘氨酰基基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(25mg,0.046mmol),得产物为白色胶状物(20mg,95.7%)。1h nmr(400mhz,chloroform-d)δ11.74(s,1h),8.37(s,1h),7.96(s,1h),7.30
–
7.26(m,3h),7.09(s,1h),6.95
–
6.91(m,2h),4.74(q,j=5.4,3.8hz,4h),4.35(dd,j=13.4,7.3hz,1h),4.26(dd,j=5.8,2.7hz,2h),4.16(d,j=13.8hz,1h),3.83(d,j=2.6hz,3h),3.80
–
3.72(m,1h),3.21(t,j=13.0hz,1h),2.79(dt,j=40.1,13.1hz,3h).
[0101]
(5-(1-(2-(4-氯苯基)甘氨酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0102]
制备方法同实施例3,原料改用(5-(1-(2-(4-氯苯基)甘氨酰基基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(20mg,0.043mmol),得米白色粉末(8mg,42.1%)。mp 226.5
–
228.2℃.1h nmr(400mhz,dmso-d6)δ12.83(s,1h),12.26(s,1h),9.27(t,j=6.1hz,1h),8.14(d,j=1.4hz,1h),7.35
–
7.31(m,3h),6.97(d,j=9.0hz,2h),4.88(s,2h),4.49(d,j=12.9hz,1h),3.97(d,j=6.0hz,3h),3.15(t,j=12.8hz,1h),2.94(ddd,j=11.9,8.4,3.5hz,1h),2.68(t,j=12.5hz,1h),1.84(d,j=11.0hz,2h),1.73(d,j=12.4hz,1h),1.54(q,j=11.7,11.2hz,1h).hrms(esi):444.1206[m h]
.
[0103]
实施例11:(5-(1-((4-氨基苯基)磺酰基)-吡咯烷-3-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0104]
(5-(1-((4-氨基苯基)磺酰基)-2,5-二氢-1h-吡咯烷-3-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯
[0105]
(5-(2,5-二氢-1h-吡咯烷-3-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(80mg,0.21mmol)溶于5ml二氯甲烷中,加入4-氨基苯磺酰氯(83mg,0.43mmol),n,n-二异丙基乙胺(70mg,0.54mmol),室温下反应6小时。反应完毕,加入饱和碳酸氢钠溶液(10ml)将反应淬灭,反应液使用二氯甲烷(10ml
×
3)萃取,饱和氯化钠溶液(10ml)洗涤。合并有机相,无水硫酸钠干燥,减压蒸除溶剂,粗品使用硅胶柱层析分离纯化(石油醚:乙酸乙酯=1:3),得产物为淡黄色胶状物(60mg,52.7%)。1h nmr(400mhz,chloroform-d)δ8.48(d,j=1.4hz,1h),8.32(t,j=9.7hz,1h),7.70
–
7.61(m,3h),7.45
–
7.26(m,5h),6.71
–
6.64(m,2h),6.01(tt,j=6.3,1.0hz,1h),5.25
–
5.16(m,3h),4.91(d,j=5.7hz,1h),4.16(d,j=9.8hz,2h),4.08(t,j=0.9hz,1h),4.06
–
3.97(m,3h),3.66(s,3h).
[0106]
(5-(1-((4-氨基苯基)磺酰基)-吡咯烷-3-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯
[0107]
制备方法同实施例3,原料改用(5-(1-((4-氨基苯基)磺酰基)-2,5-二氢-1h-吡咯烷-3-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(50mg,0.095mmol),得产物为白色胶状物(35mg,84.2%)。1h nmr(400mhz,chloroform-d)δ8.30(t,j=9.8hz,1h),8.25(dd,j=1.4,0.6hz,1h),7.64
–
7.57(m,2h),7.37(dd,j=1.5,0.7hz,1h),6.71
–
6.64(m,2h),5.30(d,j=5.7hz,1h),5.11(d,j=5.7hz,1h),4.23
–
4.06(m,2h),3.94
–
3.84(m,1h),3.73
–
3.60(m,
3h),3.56
–
3.36(m,2h),3.36
–
3.25(m,1h),2.40
–
2.23(m,2h).
[0108]
(5-(1-((4-氨基苯基)磺酰基)-吡咯烷-3-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0109]
制备方法同实施例3,原料改用(5-(1-((4-氨基苯基)磺酰基)-吡咯烷-3-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(20mg,0.046mmol),得米白色粉末(18mg,93.0%)。mp 224.1
–
225.4℃.1h nmr(400mhz,dmso-d6)δ8.39(t,j=10.2hz,1h),8.24(dd,j=1.4,0.6hz,1h),7.64
–
7.56(m,2h),7.40(dd,j=1.4,0.6hz,1h),6.77
–
6.70(m,2h),5.76(d,j=5.7hz,1h),5.70(d,j=5.7hz,1h),4.13(dd,j=12.4,10.2hz,1h),4.00(dd,j=12.4,10.2hz,1h),3.86(ddd,j=11.9,6.9,0.8hz,1h),3.64
–
3.38(m,3h),3.30
–
3.19(m,1h),2.31(tdd,j=7.7,6.7,3.8hz,2h).hrms(esi):420.1104[m h]
.
[0110]
实施例12:(5-(1-((4-羟基苯基)磺酰基)-氮杂环庚烷-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0111]
(5-(1-((4-羟基苯基)磺酰基)-2,3,4,7-四氢氮杂-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯
[0112]
(5-(2,3,4,7-四氢氮杂-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(80mg,0.20mmol)溶于5ml二氯甲烷中,加入4-羟基苯磺酰氯(78mg,0.40mmol),n,n-二异丙基乙胺(65mg,0.50mmol),室温下反应6小时。反应完毕,加入饱和碳酸氢钠溶液(10ml)将反应淬灭,反应液使用二氯甲烷(10ml
×
3)萃取,饱和氯化钠溶液(10ml)洗涤。合并有机相,无水硫酸钠干燥,减压蒸除溶剂,粗品使用硅胶柱层析分离纯化(石油醚:乙酸乙酯=1:3),得产物为淡黄色胶状物(56mg,50.1%)。1h nmr(400mhz,chloroform-d)δ9.02(s,1h),8.45(d,j=1.4hz,1h),8.29(t,j=9.7hz,1h),7.64
–
7.54(m,3h),7.45
–
7.26(m,5h),6.93
–
6.86(m,2h),5.99(tt,j=6.1,1.0hz,1h),5.19(t,j=1.0hz,2h),4.16(d,j=9.8hz,2h),3.66(s,3h),3.31(dt,j=15.6,7.2hz,4h),2.90(tq,j=7.1,1.0hz,2h),2.30(tdt,j=7.2,6.2,1.0hz,2h).
[0113]
(5-(1-((4-羟基苯基)磺酰基)-氮杂环庚烷-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯
[0114]
制备方法同实施例3,原料改用(5-(1-((4-羟基苯基)磺酰基)-2,3,4,7-四氢氮杂-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(50mg,0.090mmol),得产物为白色胶状物(37mg,88.1%)。1h nmr(400mhz,chloroform-d)δ9.10(s,1h),8.38
–
8.28(m,2h),7.60
–
7.53(m,2h),7.37(dd,j=1.5,0.7hz,1h),6.93
–
6.86(m,2h),4.22
–
4.06(m,2h),3.66(s,2h),3.17(td,j=7.1,0.8hz,2h),3.15
–
3.03(m,2h),2.89
–
2.78(m,1h),2.13
–
1.95(m,2h),1.84
–
1.66(m,4h).
[0115]
(5-(1-((4-羟基苯基)磺酰基)-氮杂环庚烷-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0116]
制备方法同实施例3,原料改用(5-(1-((4-羟基苯基)磺酰基)-氮杂环庚烷-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(60mg,0.12mmol),得米白色粉末(55mg,94.1%)。mp 231.1
–
232.8℃.1h nmr(400mhz,dmso-d6)δ9.49(s,1h),8.42(t,j=10.2hz,1h),8.25(dd,j=1.5,0.7hz,1h),7.61
–
7.54(m,2h),7.40(dd,j=1.4,0.6hz,1h),6.93
–
6.86(m,2h),4.14(dd,j=12.4,10.2hz,1h),4.00(dd,j=12.4,10.2hz,1h),3.17(t,j=7.1hz,2h),3.08(t,j=6.9hz,2h),2.89
–
2.77(m,1h),2.12
–
2.01(m,1h),2.03
–
1.92(m,1h),1.87
–
1.65(m,4h).hrms(esi):468.0988[m h]
.
[0117]
实施例13:(5-(1-((4-氯苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0118]
(5-(1-((4-氯苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯
[0119]
(5-(1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(100mg,0.26mmol)溶于5ml二氯甲烷中,加入4-氯苯磺酰氯(111mg,0.52mmol),n,n-二异丙基乙胺(84.7mg,0.65mmol),室温下反应6小时。反应完毕,加入饱和碳酸氢钠溶液(10ml)将反应淬灭,反应液使用二氯甲烷(10ml
×
3)萃取,饱和氯化钠溶液(10ml)洗涤。合并有机相,无水硫酸钠干燥,减压蒸除溶剂,粗品使用硅胶柱层析分离纯化(石油醚:乙酸乙酯=1:3),得产物为米白色粉末(96mg,65.8%)。mp 187.9
–
188.9℃.1h nmr(400mhz,dmso-d6)δ8.79(t,j=6.1hz,1h),8.22(d,j=1.7hz,1h),7.86(d,j=8.7hz,2h),7.74(d,j=8.6hz,2h),7.61(d,j=1.8hz,1h),7.52(d,j=6.8hz,2h),7.39(t,j=7.4hz,2h),7.32(t,j=7.3hz,1h),6.36
–
6.32(m,1h),5.26(s,2h),4.01(d,j=6.1hz,2h),3.77(q,j=2.9hz,2h),3.64(s,3h),3.29(t,j=5.7hz,2h),2.59(s,2h).
[0120]
(5-(1-((4-氯苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯
[0121]
制备方法同实施例3,原料改用(5-(1-((4-氯苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-苄氧基-吡啶-2-甲酰基)甘氨酸甲酯(80mg,0.14mmol),得产物为米白色粉末(44.5mg,65.8%)。mp 170.6
–
171.3℃.1h nmr(400mhz,dmso-d6)δ12.17(s,1h),9.42(t,j=6.2hz,1h),8.26(d,j=1.9hz,1h),7.85(d,j=8.7hz,2h),7.73(d,j=8.6hz,2h),7.38(d,j=1.9hz,1h),6.41(s,1h),4.08(d,j=6.3hz,2h),3.76(d,j=3.4hz,2h),3.67(s,3h),3.27(d,j=5.7hz,2h),2.58(s,2h).
[0122]
(5-(1-((4-氯苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0123]
制备方法同实施例3,原料改用(5-(1-((4-氯苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(40mg,0.085mmol),得米白色粉末(36mg,92.8%)。mp 219.5
–
220.8℃.1h nmr(400mhz,dmso-d6)δ12.85(s,1h),12.28(s,1h),9.27(t,j=6.2hz,1h),8.25(s,1h),7.85(d,j=8.2hz,2h),7.73(d,j=8.3hz,2h),7.37(s,1h),6.41(s,1h),3.97(d,j=6.1hz,2h),3.75(s,2h),3.27(s,2h),2.58(s,2h).hrms(esi):452.0699[m h]
.
[0124]
实施例14:(5-(1-((4-氟苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0125]
制备方法同实施例3,原料改用(5-(1-((4-氟苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(40mg,0.089mmol),得米白色粉末(37mg,95.5%)。mp 199.1
–
200.5℃.1h nmr(400mhz,dmso-d6)δ12.26(s,1h),9.25(t,j=6.2hz,1h),8.24(d,j=1.9hz,1h),7.92(dd,j=8.6,5.2hz,2h),7.50(t,j=8.6hz,2h),7.37(d,j=1.9hz,1h),6.40(t,j=3.6hz,1h),3.98(d,j=6.1hz,2h),3.75(d,j=3.5hz,2h),3.27(s,2h),2.58(s,2h).hrms(esi):436.0979[m h]
.
[0126]
实施例15:(5-(1-((2-氟苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0127]
制备方法同实施例3,原料改用(5-(1-((2-氟苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(40mg,0.089mmol),得米白色粉末(37mg,95.5%)。mp 199.0
–
199.8℃.1h nmr(400mhz,dmso-d6)δ12.81(s,1h),12.26(s,1h),9.26(t,j=6.2hz,1h),8.25(d,j=2.0hz,1h),7.88(td,j=7.5,1.8hz,1h),7.80
–
7.74(m,1h),7.52
–
7.43(m,2h),7.37(d,j=2.0hz,1h),6.48
–
6.43(m,1h),3.98(d,j=6.1hz,2h),3.89(q,j=2.9hz,2h),3.44(t,j=5.7hz,2h),2.55(d,j=6.2hz,2h).hrms(esi):436.0975[m h]
.
[0128]
实施例16:(5-(1-((3-氟苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0129]
制备方法同实施例3,原料改用(5-(1-((3-氟苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(40mg,0.089mmol),得米白色粉末(37mg,95.5%)。mp 144.4
–
145.1℃.1h nmr(400mhz,dmso-d6)δ12.82(s,1h),12.26(s,1h),9.25(t,j=6.2hz,1h),8.24(d,j=1.9hz,1h),7.73
–
7.66(m,3h),7.64
–
7.58(m,1h),7.37(d,j=1.9hz,1h),6.40(d,j=4.3hz,1h),3.98(d,j=6.1hz,2h),3.80(d,j=3.5hz,2h),3.30(d,j=5.7hz,2h),2.57(s,2h).hrms(esi):436.0977[m h]
.
[0130]
实施例17:(5-(1-((3,5-二氟苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0131]
制备方法同实施例3,原料改用(5-(1-((3,5-二氟苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(50mg,0.106mmol),得米白色粉末(45mg,95.3%)。mp 223.6
–
224.0℃.1h nmr(400mhz,dmso-d6)δ12.81(s,1h),12.27(s,1h),9.25(t,j=6.1hz,1h),8.25(d,j=2.0hz,1h),7.71(tt,j=9.2,2.3hz,1h),7.64
–
7.57(m,2h),7.39(d,j=2.0hz,1h),6.42(s,1h),3.98(d,j=6.1hz,2h),3.84(d,j=3.7hz,2h),3.36(d,j=5.9hz,2h),2.58(s,2h).hrms(esi):453.0811[m h]
.
[0132]
实施例18:(5-(1-((4-溴苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0133]
制备方法同实施例3,原料改用(5-(1-((4-溴苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(35mg,0.068mmol),得米白色粉末(29mg,85.2%)。mp 219.7
–
221.3℃.1h nmr(400mhz,dmso-d6)δ12.79(s,1h),12.26(s,1h),9.26(t,j=6.2hz,1h),8.25(d,j=1.9hz,1h),7.87(d,j=8.7hz,2h),7.77(d,j=8.6hz,2h),7.37(d,j=1.9hz,1h),6.40(s,1h),3.98(d,j=6.2hz,2h),3.76(d,j=3.6hz,2h),3.27(d,j=5.8hz,2h),2.58(s,2h).hrms(esi):491.0168[m h]
.
[0134]
实施例19:(5-(1-((4-甲基苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0135]
制备方法同实施例3,原料改用(5-(1-((4-甲基苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(40mg,0.067mmol),得米白色粉末(32mg,82.6%)。mp 219.5
–
220.9℃.1h nmr(400mhz,dmso-d6)δ12.25(s,1h),9.26(d,j=7.9hz,1h),8.24(s,1h),7.71(d,j=7.8hz,2h),7.46(d,j=7.8hz,2h),7.36(s,1h),6.39(s,1h),
3.98(d,j=6.2hz,2h),3.70(s,2h),3.22(s,2h),2.57(s,2h),2.40(s,3h).hrms(esi):432.1223[m h]
.
[0136]
实施例20:(5-(1-((4-三氟甲基苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0137]
制备方法同实施例3,原料改用(5-(1-((4-三氟甲基苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(36mg,0.072mmol),得白色粉末(22mg,62.9%)。mp 228.0
–
229.8℃.1h nmr(400mhz,dmso-d6)δ12.27(s,1h),9.24(s,1h),8.24(d,j=1.9hz,1h),8.05(q,j=8.4hz,4h),7.35(d,j=1.9hz,1h),6.40(s,1h),3.96(d,j=5.9hz,2h),3.81(d,j=3.5hz,2h),2.58(s,2h).hrms(esi):486.0944[m h]
.
[0138]
实施例21:(5-(1-((4-甲氧基苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0139]
制备方法同实施例3,原料改用(5-(1-((4-甲氧基苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(22mg,0.047mmol),得米白色粉末(37mg,52.3%)。mp 272.7
–
273.3℃.1h nmr(400mhz,dmso-d6)δ12.45(s,1h),9.04(s,1h),8.31(d,j=1.9hz,1h),7.46(s,4h),7.40(d,j=1.9hz,1h),6.46(s,1h),4.53(s,2h),3.92(d,j=3.7hz,2h),3.79(d,j=5.3hz,2h),3.17(s,2h).hrms(esi):[m h]
.
[0140]
实施例22:(5-(1-((4-三氟甲氧基苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0141]
制备方法同实施例3,原料改用(5-(1-((4-三氟甲氧基苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(30mg,0.058mmol),得米白色粉末(27mg,92.5%)。mp 213.0
–
214.3℃.1h nmr(400mhz,dmso-d6)δ12.27(s,1h),9.24(t,j=6.1hz,1h),8.24(d,j=1.9hz,1h),7.99(d,j=8.6hz,2h),7.64(d,j=8.4hz,2h),7.35(d,j=1.9hz,1h),6.40(s,1h),3.97(d,j=6.1hz,2h),3.79(d,j=3.5hz,2h),3.29(s,2h),2.57(s,2h).hrms(esi):502.0887[m h]
.
[0142]
实施例23:(5-(1-((4-氰基苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0143]
制备方法同实施例3,原料改用(5-(1-((4-氰基苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(20mg,0.043mmol),得米白色粉末(12mg,61.9%)。mp 212.6
–
214.6℃.1h nmr(400mhz,dmso-d6)δ12.28(s,1h),9.23(t,j=6.0hz,1h),8.24(d,j=1.9hz,1h),8.17
–
8.11(m,2h),8.02(d,j=8.4hz,2h),7.37(d,j=1.9hz,1h),6.40(s,1h),3.96(d,j=6.0hz,2h),3.84
–
3.79(m,2h),2.58(s,2h).hrms(esi):443.1019[m h]
.
[0144]
实施例24:(5-(1-((4-叔丁基苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0145]
制备方法同实施例3,原料改用(5-(1-((4-叔丁基苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(70mg,0.143mmol),得米白色粉末(64mg,94.1%)。mp 210.1
–
211.2℃.1h nmr(400mhz,chloroform-d)δ11.66(s,1h),8.36(t,j=5.8hz,1h),8.08(d,j=1.9hz,1h),7.75(d,j=8.5hz,2h),7.55(d,j=8.5hz,2h),7.17(d,j=2.0hz,1h),6.16(d,j=3.3hz,1h),4.30(d,j=5.8hz,2h),3.83(d,j=3.2hz,2h),3.37
219.9-220.7℃.1h nmr(400mhz,dmso-d6)δ12.80(s,1h),12.25(s,1h),9.26(t,j=6.2hz,1h),8.69(d,j=8.6hz,1h),8.31(d,j=8.2hz,1h),8.24
–
8.20(m,2h),8.12(dd,j=8.2,1.5hz,1h),7.78
–
7.74(m,1h),7.69(ddd,j=8.2,6.1,4.9hz,2h),6.43
–
6.39(m,1h),3.97(d,j=6.1hz,2h),3.92(q,j=2.9hz,2h),3.45(t,j=5.7hz,2h).hrms(esi):468.1230[m h] .
[0156]
实施例30:(5-(1-(吡啶-3-磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0157]
制备方法同实施例3,原料改用(5-(1-((吡啶-3-磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(32mg,0.074mmol),得米白色粉末(28mg,90.4%)。mp 216.4
–
217.7℃.1h nmr(400mhz,dmso-d6)δ12.84(s,1h),12.27(s,1h),9.32
–
9.22(m,1h),9.00(d,j=8.5hz,1h),8.89(d,j=5.0hz,1h),8.25(d,j=10.7hz,2h),7.73
–
7.62(m,1h),7.37(s,1h),6.41(s,1h),3.97(t,j=7.2hz,2h),3.84(s,2h),2.57(s,2h).hrms(esi):419.1020[m h]
.
[0158]
实施例31:(5-(1-(噻吩-2-磺酰基))-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0159]
制备方法同实施例3,原料改用(5-(1-(噻吩-2-磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(15mg,0.034mmol),得米白色粉末(12mg,82.6%)。mp 234.1
–
235.4℃.1h nmr(400mhz,dmso-d6)δ12.73(s,1h),12.27(s,1h),9.33
–
9.25(m,1h),8.27(d,j=3.1hz,1h),8.07(t,j=4.0hz,1h),7.74(d,j=3.8hz,1h),7.39(d,j=3.2hz,1h),7.30(q,j=4.3hz,1h),6.43(s,1h),3.98(t,j=4.5hz,2h),3.78(s,2h),3.27
–
3.24(m,2h),2.64(s,2h).hrms(esi):424.0637[m h]
.
[0160]
实施例32:(6-甲基-5-(1-(喹啉-2-磺酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0161]
制备方法同实施例3,原料改用(6-甲基-5-(1-(喹啉-2-磺酰基)-哌啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(30mg,0.062mmol),得米白色粉末(24mg,82.4%)。mp 223.1
–
224.9℃.1h nmr(400mhz,dmso-d6)δ8.97(dd,j=7.5,1.4hz,1h),8.47
–
8.38(m,2h),8.34
–
8.23(m,2h),8.07
–
8.00(m,1h),7.69
–
7.61(m,1h),7.61
–
7.52(m,2h),5.84(tt,j=6.2,1.0hz,1h),4.07(d,j=10.2hz,2h),3.72(dt,j=6.2,1.0hz,2h),3.34(td,j=7.1,0.6hz,2h),3.14(tp,j=7.1,1.0hz,2h).hrms(esi):485.1486[m h]
.
[0162]
实施例33:(5-(1-((4-氯苄基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0163]
制备方法同实施例3,原料改用(5-(1-((4-氟苯基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(40mg,0.089mmol),得米白色粉末(37mg,95.5%)。mp 199.1
–
200.5℃.1h nmr(400mhz,dmso-d6)δ12.27(s,1h),9.24(t,j=6.1hz,1h),8.25(d,j=1.9hz,1h),7.79
–
7.74(m,2h),7.37(d,j=1.9hz,1h),7.17(d,j=8.6hz,2h),6.39(d,j=4.2hz,1h),3.97(d,j=5.9hz,2h),3.85(s,2h),3.69(q,j=3.1hz,2h),3.21(t,j=5.7hz,2h),2.58(s,2h).hrms(esi):466.0839[m h]
.
[0164]
实施例34:(5-(1-((4-氟苄基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0165]
制备方法同实施例3,原料改用(5-(1-((4-氟苄基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(35mg,0.075mmol),得米白色粉末(31mg,93.4%)。mp 204.4
–
205.6℃.1h nmr(400mhz,dmso-d6)δ12.31(s,1h),9.23(t,j=6.1hz,1h),8.31(d,j=2.0hz,1h),7.48(dd,j=8.6,5.6hz,2h),7.42(d,j=2.0hz,1h),7.22(t,j=8.9hz,2h),6.46(dt,j=3.9,2.0hz,1h),4.52(s,2h),3.95(d,j=5.9hz,2h),3.91(q,j=2.9hz,2h),3.37(s,2h).hrms(esi):450.1136[m h]
.
[0166]
实施例35:(5-(1-((4-溴苄基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0167]
制备方法同实施例3,原料改用(5-(1-((4-溴苄基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(25mg,0.047mmol),得米白色粉末(20mg,82.2%)。mp 226.1
–
227.4℃.1h nmr(400mhz,dmso-d6)δ12.29(s,1h),9.26(t,j=6.2hz,1h),8.32(d,j=1.9hz,1h),7.60(d,j=8.2hz,2h),7.42(d,j=1.9hz,1h),7.40(d,j=8.4hz,2h),6.47(d,j=3.6hz,1h),4.52(s,2h),3.98(d,j=6.1hz,2h),3.92(q,j=2.9hz,2h),3.37(s,2h).hrms(esi):512.0319[m h]
.
[0168]
实施例36:(5-(1-((4-三氟甲基苄基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0169]
制备方法同实施例3,原料改用(5-(1-((4-三氟甲基苄基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(8mg,0.015mmol),得米白色粉末(6mg,77.1%)。mp 225.8
–
226.7℃.1h nmr(400mhz,dmso-d6)δ12.30(s,1h),9.24(d,j=6.3hz,1h),8.32(d,j=1.9hz,1h),7.60(d,j=8.0hz,2h),7.42(d,j=1.9hz,1h),7.40(d,j=8.2hz,2h),6.47(s,1h),4.52(s,2h),3.96(d,j=6.0hz,2h),3.92(s,2h),3.37(s,2h).hrms(esi):500.1092[m h]
.
[0170]
实施例37:(5-(1-((4-三氟甲氧基苄基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0171]
制备方法同实施例3,原料改用(5-(1-((4-三氟甲氧基苄基)磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(39mg,0.073mmol),得米白色粉末(35mg,92.1%)。mp 255.5
–
257.2℃.1h nmr(400mhz,dmso-d6)δ12.30(s,1h),9.27
–
9.22(m,1h),8.32(d,j=1.9hz,1h),7.57(d,j=8.5hz,2h),7.42(d,j=1.9hz,1h),7.39(d,j=8.1hz,2h),6.48(s,1h),4.57(s,2h),3.96(d,j=6.7hz,4h),3.39(s,2h).hrms(esi):516.1061[m h]
[0172]
实施例38:(5-(1-(苄磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸
[0173]
制备方法同实施例3,原料改用(5-(1-(苄磺酰基)-1,2,5,6-四氢吡啶-4-基)-3-羟基-吡啶-2-甲酰基)甘氨酸甲酯(30mg,0.067mmol),得米白色粉末(28mg,96.3%)。mp 195.6
–
196.5℃.1h nmr(400mhz,dmso-d6)δ12.83(s,1h),12.28(s,1h),9.27(t,j=6.1hz,1h),8.31(d,j=1.9hz,1h),7.43(dt,j=8.0,2.9hz,3h),7.38(dd,j=5.1,2.1hz,3h),6.46(d,j=3.5hz,1h),4.51(s,2h),3.99(d,j=6.1hz,2h),3.91(q,j=3.0hz,2h),3.36(s,2h).hrms(esi):432.1234[m h]
.
[0174]
实施例39:本发明的部分药效学实验
[0175]
1、荧光偏振实验测试本发明化合物对脯胺酰羟化酶2蛋白的抑制作用
[0176]
为评价本发明化合物对脯胺酰羟化酶2蛋白的抑制作用,本发明使用荧光偏振法(fluorescence polarization)对化合物与荧光基团标记的hif-1α肽段(fitc-hif-1α556-574)竞争性结合脯胺酰羟化酶2蛋白的能力进行了测试。实验方法:测试所使用的器材为384孔黑板(型号为corining#3575),测试最终体积选择60μl。所测试的化合物和荧光标记肽段分别溶解于dmso和纯水之中备用。化合物母液使用缓冲溶液进行稀释得10个浓度梯度后每孔加入20μl化合物以及等体积的蛋白和探针,使后两者的浓度分别为250nm和3nm。室温下摇床孵育1h,使用spectra max i3x多功能酶标仪进行检测,激发波长485nm,发射波长535nm,测试结果使用graphpad prsim 8进行分析。测试中所使用的空白对照为20μl hif肽段和40μl缓冲液,阴性对照为20μl hif肽段 20μlphd2蛋白 20μl缓冲液,阳性对照为上市药物fg-4592(roxadustat)。缓冲液配方为10mm hepes,ph 7.4,150mmnacl,10μm mncl2,20μm 2-og,0.05%tween-20。
[0177]
表1实施例合物的脯胺酰羟化酶2的抑制活性
[0178][0179]
由表1可见,本发明的5-脂肪杂环基-3-羟基吡啶-2-甲酰基甘氨酸类化合物具有较强的脯胺酰羟化酶2抑制活性,大部分化合物活性优于阳性对照化合物fg-4592。进一步的,本发明化合物吡啶母核5位取代杂环的饱和度对活性有着重要影响,当脂肪杂环基饱和脂肪杂环时,相较于对应的不饱和脂肪杂环取代化合物,其对脯氨酰羟化酶2的活性发生了较为显著的下降。进一步的,本发明化合物5-脂肪杂环基-3-羟基吡啶-2-甲酰基甘氨酸类化合物的连接链的类型对化合物活性具有一定的影响,当连接链为时,本发明化合物活性相较于其他连接链活性最佳。进一步的,本发明实施例中最优的化合物35的脯氨酰羟化酶2的抑制活性达到了0.028
±
0.005μm,约为阳性参照化合物fg-4592的20倍。
[0180]
2、细胞计数法(cell counting kit-8,cck-8)测试本发明化合物对人体肝癌细胞株hep3b的细胞毒性
[0181]
为了初步评价本发明化合物的安全性,采用cck-8方法测定人体肝癌细胞株hep3b
的细胞毒性。
[0182]
实验方法:将hep3b细胞接种在96孔板中,细胞贴壁后,给药组加入相应化合物的dmso溶液,以保证每个化合物终浓度为10、100μm。空白对照组加入给药组中最高浓度的dmso。同时设置2个复孔。处理24小时后,根据试剂盒说明书将cell counting kit-8(c0037,beyotime)添加到每个孔中。在37℃条件下将96孔板避光孵育2小时,使用酶标仪检测每孔450nm波长的吸光度。计算给药组吸光度值与空白对照组吸光度的比值以确定细胞活力。
[0183]
细胞活力=(加药组吸光度-空白组吸光度/对照组吸光度-空白组吸光度)
×
100%
[0184]
cck-8法测试的实验结果表明,本发明代表性化合物在100μl高浓度下相较于阳性参照fg-4592均未展现出细胞毒性。本发明化合物在细胞水平安全性方面不劣于阳性参照fg-4592(图1)。
[0185]
3、反转录-聚合酶链式反应实验(reverse transcription-polymerase chain reaction,rt-pcr)测试本发明化合物对hif-α下游epo基因的表达的促进作用。
[0186]
为验证此类化合物能够在细胞水平上稳定hif-α从而促进epo基因的表达,本发明设计了rt-pcr实验。给予化合物后,hif-α含量增多,刺激epo基因转录,将给与化合物的细胞破碎后提取其所包含的epo的rna并对其进行定量扩增,随后进行检测。rna量的提高倍数可间接用于衡量此类化合物对epo基因表达的提升能力。
[0187]
实验方法:
[0188]
预先培养人肝癌细胞hep3b细胞,孵育给药10h后,按照rna提取试剂盒操作,提取rna。根据prime script
tm rt reagent kit with gdna eraser(perfect real time)说明书进行反转录。在qpcr反应板中依次加入7μl depc水,0.5μlsense primer,0.5μl antisense primer,2μl cdna,10μl sybr premix ex taqii,在thermo stepone&steponeplus real-time pcr systems完成扩增及定量过程。以hprt作为内参基因,使用δδc
t
方法分析epo相对表达水平。
[0189]
引物序列:hprt-forward 5
′‑
gaccagtcaacaggggacat-3
′
,
[0190]
reverse 5
′‑
aacacttcgtggggtccttttc-3
′
;
[0191]
epo-forward 5
′‑
gagcccagaaggaagccatc-3
′
,
[0192]
reverse 5
′‑
cggaaagtgtcagcagtgattg-3
′
。
[0193]
表2实施例化合物提高epo基因表达的情况
[0194][0195][0196]
由表2可见,本发明的代表性化合物的rt-pcr实验结果显示代表性化合物均能够促进细胞内epo基因的表达。进一步的,本发明实施例中最优的化合物35在不同浓度下促进
epo基因表达的能力与阳性参照化合物fg-4592相当(图2)。
[0197]
4、体内血浆网织红细胞提升活性研究
[0198]
实验方法:选用18-20g的c56bl/6小鼠,将其随机分为7组:空白对照组、化合物33的单独给药组、化合物34的单独给药组、化合物35的高剂量单独给药组、化合物36的高剂量单独给药组、化合物37的高剂量单独给药组、阳性参照fg-4592的单独给药组,每组5只小鼠。给药组分别灌胃给药相应浓度的化合物,空白对照组灌胃给药与给药组相同体积的生理盐水。每天给药一次,第三次给药后4~6小时,采用眼眶后静脉丛取血法对各组小鼠取血,血样检测网织红细胞比率。
[0199]
本发明公开了部分化合物对小鼠网织红细胞提升能力的数据(图3)。结果表明在动物水平,本发明化合物33、34、35、36、37均能够提升网织红细胞的比率。进一步地,相较于阳性参照fg-4592,本发明化合物33、34、35、36、37体现出了一定的优势。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
