1.本发明涉及光谱探针技术领域,具体是涉及一种水溶性大孔道锆卟啉结构化合物的制备方法及其应用。
背景技术:
2.氟是常见的水体污染物,过量摄入氟会导致氟中毒,损害人体的骨骼和牙齿,还可能使人体肾脏受损和甲状腺激素紊乱。
3.因此,对水体中的氟离子进行监测和管理是保障水环境安全的重要内容,提供一种准确、快速、高灵敏度的水体氟离子分析检测方法十分必要。
技术实现要素:
4.一、发明原理与目的
5.发光金属-有机骨架材料(lmofs)是mofs的一个重要分支。与其他发光探针材料相比,lmofs固有的多孔性使其具有几个关键的优势。lmofs的孔隙度限制了分析物-mof的距离,使mof和分析物之间发生密切的相互作用。通过改变孔隙的大小和亲疏水性/极性等可以选择性地控制传感相互作用。lmofs还可以将分析物富集到孔中,显著提高敏感度。目前已经有一些合成lmof检测氟离子的报道,但大多无法在水介质中稳定存在,孔径是微孔或比表面积不大导致灵敏度不高。
6.二、发明方案
7.为了解决上述问题,本发明提供了一种对废水中氟离子具有高选择性的荧光探针:采用h2-tcpp(tcpp=四(4-羧基苯基)卟啉)作为配体,高度稳定的zr6团簇作为组装节点,成功合成了zr卟啉mof——pcn-222(pcn porous coordination network,多孔配位网络)。
8.pcn-222具有很大的开放孔道、非常大的比表面积和优异的稳定性。pcn-222对f
–
选择性地表现出明显的荧光猝灭响应,具有很高的灵敏度,其实用性通过检测加标水样进一步得到了验证。
9.具体的技术方案如下:
10.s1、化合物合成
11.s11、通过超声处理将zrcl4,h
2-tcpp和苯甲酸溶解在n,n-二乙基甲酰胺中,得到溶液。
12.s12、将步骤s11中制备的溶液转移进聚四氟乙烯的高压反应釜中,并置于鼓风烘箱中加热至120℃,保持48小时。
13.s13、待步骤s12中加热后的溶液冷却至室温后,使用n,n-二甲基甲酰胺通过多次抽滤进行洗涤,之后用丙酮代替n,n-二甲基甲酰胺继续洗涤数次,最终收获固体化合物产物。
14.s2、化合物活化
15.s21、为了优化活化过程,首先将少量浓盐酸添加到dmf悬浮液中,然后将步骤s213中合成的产物在120℃的dmf中浸泡12小时。
16.s22、将步骤s21中浸泡后的产物用dmf和丙酮洗涤数次,然后将产物浸入丙酮中静置24小时。
17.s23、将步骤s22中静置后的产物在真空干燥箱中真空干燥6小时进行活化处理,最后使用除气功能在120℃下再次干燥12小时。
18.优选地,上述制备方法具体为;
19.s1、化合物合成
20.s11、通过超声处理将75-100mg zrcl4,50-70mg h
2-tcpp和2.7-3.6g苯甲酸溶解在8-12ml n,n-二乙基甲酰胺中,得到溶液;
21.s12、将步骤s11中制备的溶液转移进聚四氟乙烯的高压反应釜中,并置于鼓风烘箱中加热至120℃,保持48小时;
22.s13、待步骤s12中加热后的溶液冷却至室温后,使用n,n-二甲基甲酰胺通过2-4次抽滤进行洗涤,之后用丙酮代替n,n-二甲基甲酰胺继续洗涤2-5次,最终收获固体化合物产物;
23.s2、化合物活化
24.s21、首先将0.5-1ml浓盐酸添加到20-40ml dmf悬浮液中,然后将步骤s13中合成的产物在120℃的dmf中浸泡12小时;
25.s22、将步骤s21中浸泡后的产物用dmf和丙酮洗涤2-5次,然后将产物浸入丙酮中静置24小时;
26.s23、将步骤s22中静置后的产物在真空干燥箱中真空干燥6小时进行活化处理,最后使用除气功能在120℃下再次干燥12小时。
27.根据本发明的一个方面,本发明制备的水溶性大孔道锆卟啉结构化合物的用途是作为检测废水中离子条件下的f-的荧光探针。
28.根据本发明的一个方面,所述荧光探针检测f-的方法为:在水溶液中检测荧光光谱,通过检测421nm处的荧光强度获得f-的浓度。
29.根据本发明的一个方面,f-对所述荧光探针的荧光猝灭在1~100μm(微摩尔)范围内较为剧烈,荧光猝灭率与f
–
浓度在1~20μm(微摩尔)内有明显的线性关系,可作为定量检测f
–
的工具。
30.根据本发明的一个方面,所述荧光探针对对f
–
具有出色的选择性、很低的检出限(56nm)和极快的响应速度(《5s),同时pcn-22还具备耐水、耐酸、耐光的优异化学稳定性。
31.与现有的氟离子荧光探针相比,本发明制备的pcn-222的有益效果是:
32.(1)通过水热法成功地制备了具有荧光功能的mof——pcn-222,在390-450nm有较宽的吸收带,最大吸收波长为421nm,在650-750nm有荧光发射带,最大发射波长为680nm。
33.(2)pcn-222无需任何修饰即可对f
–
显示出荧光猝灭响应,f
–
对pcn-222的荧光猝灭在0-100μm范围内较为剧烈,荧光猝灭率与f
–
浓度在0-20μm内有明显的线性关系,可作为定量检测f
–
的工具。
34.(3)pcn-222对f
–
具有出色的选择性、很低的检出限(56nm)和极快的响应速度(《5s),同时pcn-22还具备耐水、耐酸、耐光的优异化学稳定性。
35.(4)pcn-222用于自来水和太湖水的f
–
检测没有受到明显干扰,显示出良好结果,因此该荧光探针检测方法适用于水中f
–
的常规检测。
附图说明
36.图1是本发明制备的pcn-222的扫描电子显微镜sem图像;
37.图2是本发明制备的pcn-222的ft-ir谱图和xrd谱图;
38.图3是本发明制备的pcn-222的77k时的氮气吸附-解吸等温线和相应的孔径分布图;
39.图4是本发明制备的pcn-222的水溶液的紫外可见吸收光谱和三维荧光光谱;
40.图5是本发明中f
–
浓度对pcn-222荧光发射强度的影响;
41.图6是本发明制备的pcn-222的随f
–
的浓度的变化趋势和线性关系
42.图7是本发明制备原始pcn-222与在水中浸泡24小时的pcn-222的x射线衍射(xrd)图;
43.图8是本发明制备的pcn-222溶液在连续照射激发光下的荧光发射强度;
44.图9是本发明制备的pcn-222的阴离子的荧光响应时间图;
45.图10是本发明制备的pcn-222在加入200μm f
–
后的荧光强度随时间的变化图。
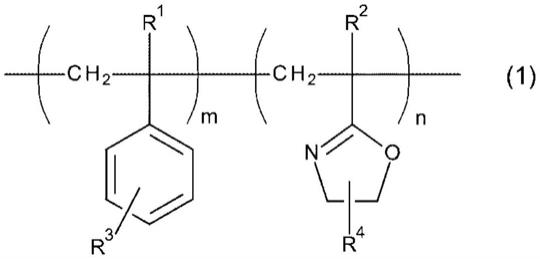
46.图11是本发明制备的pcn-222的结构示意图。
47.图2中:(a)为ft-ir谱图;(b)为xrd谱图;
48.图3中:插图为pcn-222的孔径分布图;
49.图4中:(a)为紫外可见吸收光谱;(b)为三维荧光光谱,图中的颜色灰度越深,表示荧光强度越大;
50.图5中:(λ
ex
=421nm);
51.图6中:(a)为荧光猝灭效率随f
–
浓度变化的趋势图;(b)荧光淬灭效率和f
–
浓度(0-20μm)的线性关系图,其中λ
ex
=421nm,λ
em
=680nm;
52.图8中:f
–
浓度为200μm;
53.图9中:(a)为pcn-222对低浓度(20μm)阴离子的荧光响应图;(b)为pcn-222对高浓度(200μm)阴离子的荧光响应图。
具体实施方式
54.为更进一步阐述本发明所采取的方式和取得的效果,下面将结合附图对本发明的技术方案进行清楚和完整地描述。
55.实施例一
56.本实施例主要是对本发明设计的水溶性大孔道锆卟啉结构化合物荧光探针——pcn-222的制备方法进行叙述。
57.一、实验仪器与试剂
58.本发明所用到的仪器和试剂见表1和表2。
59.表1实验仪器
[0060][0061]
表2实验试剂
[0062]
[0063][0064]
二、pcn-222的制备
[0065]
s11、通过超声处理将zrcl4(80mg),h
2-tcpp(50mg)和苯甲酸(2.7g)溶解在n,n-二乙基甲酰胺(8ml)中,得到溶液。
[0066]
s12、将步骤s11中制备的溶液转移进聚四氟乙烯的高压反应釜中,并置于鼓风烘箱中加热至120℃,保持48小时。
[0067]
s13、待步骤s12中加热后的溶液冷却至室温后,使用n,n-二甲基甲酰胺过抽滤洗涤2次,之后用丙酮代替n,n-二甲基甲酰胺继续洗涤3次,最终收获固体化合物产物。
[0068]
s2、化合物活化
[0069]
s21、为了优化活化过程,首先将0.5ml的浓盐酸添加到20ml dmf悬浮液中,然后将步骤s213中合成的产物在120℃的dmf中浸泡12小时。
[0070]
s22、将步骤s21中浸泡后的产物先用dmf洗涤2次,再用丙酮洗涤3次,最后将产物浸入丙酮中静置24小时。
[0071]
s23、将步骤s22中静置后的产物在真空干燥箱中真空干燥6小时进行活化处理,最后使用除气功能在120℃下再次干燥12小时。
[0072]
实施例二
[0073]
实施例二主要是对对实施例一记载配比外的另一种配比的制备方法进行叙述,除了以下内容外,其余部分与实施例一均相同:
[0074]
s1、化合物合成
[0075]
s11、通过超声处理将zrcl4(100mg),h
2-tcpp(60mg)和苯甲酸(3g)溶解在n,n-二乙基甲酰胺(12ml)中,得到溶液。
[0076]
s12、将步骤s11中制备的溶液转移进聚四氟乙烯的高压反应釜中,并置于鼓风烘箱中加热至120℃,保持48小时。
[0077]
s13、待步骤s12中加热后的溶液冷却至室温后,使用n,n-二甲基甲酰胺过抽滤洗涤4次,之后用丙酮代替n,n-二甲基甲酰胺继续洗涤3次,最终收获固体化合物产物。
[0078]
s2、化合物活化
[0079]
s21、为了优化活化过程,首先将1ml的浓盐酸添加到40ml dmf悬浮液中,然后将步骤s213中合成的产物在120℃的dmf中浸泡12小时。
[0080]
s22、将步骤s21中浸泡后的产物先用dmf洗涤3次,再用丙酮洗涤3次,最后将产物浸入丙酮中静置24小时。
[0081]
s23、将步骤s22中静置后的产物在真空干燥箱中真空干燥6小时进行活化处理,最后使用除气功能在120℃下再次干燥12小时。
[0082]
实验例一
[0083]
实验例一是对以上述实施例一中方法制备的pcn-222为对象进行表征的,旨在对
pcn-222的扫描电镜图、傅里叶变换红外光谱图以及xrd谱图进行说明。
[0084]
pcn-222的扫描电镜(sem)图像如图1所示,照片显示了pcn-222的立体形貌是粗细在0.5~1μm之间的棒状结构,与文献报道的pcn-222形貌一致。
[0085]
图2中(a)显示了pcn-222的傅里叶变换红外(ft-ir)光谱,其中位于1697cm-1
处的吸收峰归属于c=o的伸缩振动,1602cm-1
处的吸收峰对应于c=c的伸缩振动,1413cm-1
处的吸收峰对应于c-h和o-h的弯曲振动,1178cm-1
、1020cm-1
处的吸收峰对应于c-o的伸缩振动,700cm-1
~1000cm-1
间的吸收峰对应于c-h的弯曲振动,这些特征带均与文献报道的pcn-222的特征带一致。
[0086]
图2(b)显示了pcn-222的xrd谱图,图中中的衍射峰出现在2.4
°
、4.8
°
、7.1
°
和9.8
°
处,与文献报道的pcn-222的xrd谱图高度吻合。红外表征与xrd表征结果进一步证明了pcn-222的成功合成。
[0087]
实验例二
[0088]
实验例二是对以上述实施例一中方法制备的pcn-222为对象进行阐述的,旨在阐明pcn-222的表面积和孔径信息,为此测量了pcn-222的氮气吸附/解吸等温线和孔径分布,结果如图3所示。
[0089]
结果表明pcn-222的brunauer-emmett-teller(bet)比表面积为2080m2g-1
,表明pcn-222拥有非常大的比表面积。基于氮气吸附曲线的密度泛函理论(dft)评估表明,pcn-222具有两种类型的孔,分别为1.3nm和3.2nm(图3的插图),表明pcn-222具有一个很大的开放孔道,这与文献报道的pcn-222的孔道结构一致。以上结果都说明了pcn-222的成功合成,其结构性质也为检测性能提供了良好的支撑。
[0090]
实验例三
[0091]
实验例三是对以上述实施例一中方法制备的pcn-222为对象进行阐述的,旨在阐明pcn-222的紫外可见吸收光谱和荧光发射光谱进行说明,两个光谱的检测均在水溶液中进行。
[0092]
如图4(a)所示,在紫外可见吸收光谱的390nm至450nm之间观察到一个吸收峰,最大吸收波长为421nm(soret带),这是卟啉化合物在紫外可见光区的特征吸收峰,验证了pcn-222具有卟啉结构。
[0093]
图4(b)是pcn-222的三维荧光光谱,清晰地显示了pcn-222在650nm至750nm区间内的强荧光发射,最大发射波长为680nm;与此同时可以观察到强荧光发射区间对应的激发波长也为390nm~450nm,与吸收光谱结果相同。
[0094]
实验例四
[0095]
实验例四是对以上述实施例一中方法制备的pcn-222为对象进行阐述的,旨在确定pcn-222对f
–
的敏感性,为此研究了它们在水溶液中相互作用的荧光响应,具体见图5。
[0096]
具体的实验方法如下:
[0097]
将pcn-222溶液等量加入到10ml离心管中,每管5ml;分别向装有pcn-222溶液的离心管中加入不同浓度(0~500μm)的氟离子;混合30s后测量各离心管中pcn-222溶液的荧光发射光谱。
[0098]
如图5所示,当f
–
的浓度从0逐步增加至500μm时,pcn-222的荧光强度逐渐降低,表明f
–
淬灭了pcn-222的荧光。
[0099]
实验例五
[0100]
实验例五是对以上述实施例一中方法制备的pcn-222为对象进行阐述的,旨在阐明pcn-222随f
–
的浓度的变化趋势和线性关系,具体见图6。
[0101]
图6(a)显示了pcn-222荧光猝灭率与f
–
浓度的关系,荧光猝灭率意为已经猝灭的荧光强度与原始荧光强度的比值,表示为(1-f/f0),其中f和f0分别表示存在f
–
和不存在f
–
时的荧光强度(λ
ex
=421nm,λ
em
=680nm)。
[0102]
从图6(a)中可以看出,在0-100μm f
–
的范围内,淬灭效率急剧增加,此后增加的速率降低。更重要的是,从图6(b)可以看到,淬灭效率(1-f/f0)与f
–
浓度在0-20μm范围内具有良好的线性关系,表明pcn-222可用作定量检测f
–
浓度的荧光传感器。根据检出限计算公式(lod=3σ/斜率,σ为空白样品的标准偏差)得出的pcn-222对f
–
的检出限为56nm,远低于who要求的饮用水中f
–
的限值(~1.5mg/l),并且低于几乎所有已经报道过的mof传感器对f
–
的检出限。
[0103]
检出限低的原因可能有以下两点:第一,金属卟啉结构中存在的zr(iv)阳离子和f
–
之间的强相互作用,使得pcn-222与f
–
极易发生反应;第二,pcn-222具有很大的比表面积和孔道,f
–
能够被其富集从而产生作用。
[0104]
实验例六
[0105]
实验例六是对以上述实施例一中方法制备的pcn-222为对象进行阐述的,旨在阐明pcn-222在水中的稳定性,为此对比了未浸水与浸水24小时的pcn-222的xrd图像,具体见图7。
[0106]
具体的实验方法如下:
[0107]
将pcn-222溶液等量加入到两支10ml离心管中,每管5ml;其中一支加入200μm的氟离子,另一支加入相同体积的纯水。
[0108]
如图7所示,可以观察到浸水前后的xrd图像大致相同,说明pcn-222的主体结构基本未发生变化,该结果表明pcn-222具有优异的水稳定性。
[0109]
实验例七
[0110]
由于荧光探针是依靠荧光强度的改变来达到检测的目的,因此实验例七是对以上述实施例一中方法制备的pcn-222为对象进行阐述的,旨在阐明pcn-222在激发光下的荧光稳定性,将原始pcn-222溶液和加入f
–
后的pcn-222溶液分别在激发光下连续照射1小时,每间隔1分钟测量其荧光强度,具体结果见图8。
[0111]
具体的实验方法如下:
[0112]
使用荧光光谱仪动态检测两支离心管中的pcn-222溶液,以每分钟检测一次的频率持续检测一小时,检测过程中始终保持激发光照射。
[0113]
如图8所示,未添加f
–
的原始pcn-222溶液的荧光强度和被f
–
猝灭后的pcn-222溶液的荧光强度均在1小时内没有明显波动。这说明pcn-222具有相当的荧光稳定性,具备荧光探针的条件。综合以上结果可以发现pcn-222是同时具有水稳定性、酸稳定性、光稳定性的材料,其优异的化学稳定性的原因可能归功于pcn-222结构框架中的zr6簇,因为zr6簇被认为是mof结构中最稳定的建筑单元之一。
[0114]
实验例八
[0115]
实验例八是对以上述实施例一中方法制备的pcn-222为对象进行阐述的,旨在阐
明pcn-222对f
–
的特异性选择性,测试了部分常见离子(f
–
,k
,mg2 ,ca
2
,al
3
,cl
–
,br
–
,i-,no3–
,bro
3-,so
42-,co
32-)对pcn-222荧光强度的影响,为了让结论更有说服力,同时做了低浓度(20μm)和高浓度(200μm)两种浓度的实验,具体结果见图9。
[0116]
具体的试验方法如下:
[0117]
该实验分为低浓度组和高浓度组,旨在检测pcn-222对低浓度背景和高浓度背景下的氟离子的选择性。
[0118]
低浓度组:将pcn-222水溶液等量加入到10ml离心管中,每管5ml;分别向装有pcn-222溶液的离心管中加入相同体积相同浓度(20μm)的不同阴离子(f
–
,k
,mg2 ,ca
2
,al
3
,cl
–
,br
–
,i-,no3–
,bro
3-,so
42-,co
32-),空白对照组只加相同体积的纯水;混合30s后测量各离心管中pcn-222溶液的荧光发射光谱。共三组平行实验。
[0119]
高浓度组:将pcn-222水溶液等量加入到10ml离心管中,每管5ml;分别向装有pcn-222溶液的离心管中加入相同体积相同浓度(200μm)的不同阴离子(f
–
,k
,mg
2
,ca
2
,al
3
,cl
–
,br
–
,i-,no3–
,so
42-,bro3–
,co
32-),空白对照组只加相同体积的纯水;混合30s后测量各离心管中pcn-222溶液的荧光发射光谱。共三组平行实验。
[0120]
结果表明低浓度(图9a)和高浓度(图9b)的f
–
均显示出对pcn-222荧光强度的显着猝灭,而其他离子对荧光强度的影响很小。这说明pcn-222对f
–
具有很强的选择性,适合作为f
–
的检测探针。高选择性的原因可能是zr(iv)与f
–
之间的亲和力远高于zr(iv)与其他阴离子之间的亲和力。
[0121]
实验例九
[0122]
实验例九是对以上述实施例一中方法制备的pcn-222为对象进行阐述的,旨在阐明加入f
–
后pcn-222的荧光强度随时间的变化,具体见图10。
[0123]
如图10所示,可以很明显的看出加入f
–
不到5s,荧光强度就已经大致猝灭完全,趋于稳定。这表明该检测方法具有响应速度快的优点。
[0124]
实验例十
[0125]
实验例十是对以上述实施例一中方法制备的pcn-222为对象进行阐述的,旨在将本发明制备的pcn-222荧光探针检测法与近年来报道的f
–
的荧光检测方法进行比较,具体结果见表3。
[0126]
表3中,将文献1中记载的荧光探针编号为1,将文献2中记载的荧光探针编号为2,将文献3中记载的荧光探针编号为3,将文献4中记载的荧光探针编号为4,将文献5中记载的荧光探针编号为5,将文献6中记载的荧光探针编号为6,将文献7中记载的荧光探针编号为7,将文献8中记载的荧光探针编号为8。
[0127]
表3近年来报道的氟离子荧光检测方法
[0128][0129]
其中,文献1为2019的《selective,fast-response,and regenerable metal-organic framework for sampling excess fluoride levels in drinking water》;
[0130]
文献2为2017的《fluorescent molecule incorporated metal-organic framework for fluoride sensing in aqueous solution》;.
[0131]
文献3为2017的《silsesquioxane cages as fluoride sensors》;
[0132]
文献4为2017的《development of an inner filter effects-based upconversion nanoparticles-curcumin nanosystem for the sensitive sensing of fluoride ion》;
[0133]
文献5为2017的《boric-acid-functional lanthanide metal organic frameworks for selective ratiometric fluorescence detection of fluoride ions》;
[0134]
文献6为2016的《aie active pyridinium fused tetraphenylethene:rapid and selective fluorescent"turn-on"sensor for fluoride ion in aqueous media》;
[0135]
文献7为2016的《simple and efficient coumarin-based colorimetric and fluorescent chemosensor for f-detection:an on1-off-on2 fluorescent assay》;
[0136]
文献8为2015的《fluorescent carbon nanodots for optical detection of fluoride ion in aqueous media》。
[0137]
实验例十一
[0138]
实验例十一是对以上述实施例一中方法制备的pcn-222为对象进行阐述的,旨在验证本发明制备的pcn-222荧光探针常规分析水中氟离子的适用性,因此进一步使用实际水样进行f
–
的加标检测。
[0139]
在本实施例中,采取了自来水样品和太湖水样品两种实际水样进行分析。水样已经事先经过预处理,在处理后的水样中添加不同浓度的已知标准氟化物,然后利用pcn-222
进行荧光检测,所得的测试结果列在表4中。
[0140]
具体的实验方法如下:
[0141]
采集自来水以及太湖水的水样若干,通过0.22μm滤膜过滤以除去水中杂质。向水样中添加不同浓度(20、40、60、80、100μm)的氟离子,制备一系列包含不同浓度氟离子的水样;将水样与pcn-222分散液以1:9的比例混合(即稀释十倍,此时氟离子浓度分别为2、4、6、8、10μm);将混合液等量加入到10ml离心管中,每管5ml,测量各离心管中pcn-222溶液的荧光发射光谱。
[0142]
表4自来水样品和太湖水样品的f
–
加标检测结果
[0143][0144]
如表4所示,其中自来水样品的回收率在88.0%至103.5%的区间内,太湖水样品的回收率在93.0%至105.6%的区间内,表明利用pcn-222检测实际水样中的氟离子没有受到明显干扰。所有这些结果表明,该荧光探针检测方法具有准确性和可靠性,可用于测定水样中的f
–
。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。