一种无标记膜受体gpr84的细胞筛选模型及其应用
技术领域
1.本发明涉及无标记g蛋白偶联受体(gpcr)的细胞筛选模型构建方法及应用,具体涉及一种无标记膜受体gpr84的细胞筛选模型及其应用。
背景技术:
2.g蛋白偶联受体(g-protein-coupled receptors, gpcrs)是七次跨膜受体,其数量高达800个,是细胞信号传导中最重要的一类膜受体,在疾病的发生发展中发挥着重要的调控作用,因此是小分子药物开发中最受关注的药物靶点。目前fda批准的约34%的药物靶标为gpcrs,而且这些药物靶向的gpcrs只占总gpcrs的20%,还有大量的gpcrs,尤其是孤儿g蛋白偶联受体(orphan g-protein-coupled receptors, ogpcrs)依然未得到开发和利用。gpr84是gpcrs家族的一员,人体内gpr84主要在骨髓表达,其次在外周白细胞和肺,其它组织器官中表达量较低。gpr84一般在正常情况下表达量较低,若存在某种引起炎症反应的刺激会诱导其高表达。
3.目前受体的高通量筛选方法主要有传统的放射性配体受体结合实验法、gtpγs结合实验法、环磷酸腺苷(camp)分析法、钙流检测法、报告基因检测法、受体的内吞检测法及β-arrestin的招募检测法等。但这些方法都有一定的局限性,传统的放射性配体受体结合实验法需要洗涤和过滤,实验周期长及通量低等不足,此技术也不能区分受体的激动剂和拮抗剂;其余的gpcr检测方法主要针对某条信号通路的激活,对多条通路的激活无法区别,需要荧光蛋白标记或者额外加入指示剂,操作繁琐,而且指示剂的加入对细胞也会产生一定的损伤,影响筛选结果的可靠性。
4.采用的新型无标记细胞整合药理学技术是基于无标记的共振波导光栅(rwg)生物传感器将药物导致的细胞内成分的动态质量再分布过程转化为整体的、动态的波长位移响应信号,称为动态质量重置(dmr)信号,具有无损伤、高时空分辨、高灵敏度、高通量、能靶点-通路整合研究及操作简单、实验周期短等特点,检测过程无需标记及额外指示剂的添加,更真实的响应药物在活细胞整体水平的作用。因此,采用无标记细胞整合药理学技术构建gpr84受体无标记高通量细胞筛选模型可大大提高gpr84的内源性配体、激动剂、拮抗剂及通路调节剂的发现效率,对阐述gpr84的药理学和生理学功能具有重大意义,同时为gpr84受体密切相关的中枢神经系统疾病、内毒素血症、肥胖、2型糖尿病、血脂异常、混合谱系白血病、炎症性肠病等疾病的药物筛选提供指导。
技术实现要素:
5.本发明的目的是提供一种无标记膜受体gpr84的细胞筛选模型及其应用,以解决上述背景技术中提出的问题。
6.为了实现上述目的,借助于新型无标记细胞整合药理学技术,提供一种无标记膜受体gpr84的细胞筛选模型,用于高通量筛选gpr84受体内源性配体、激动剂、拮抗剂和通路调节剂,以及gpr84受体密切相关的中枢神经系统疾病、内毒素血症、肥胖、2型糖尿病、血脂
异常、混合谱系白血病、炎症性肠病等疾病的药物筛选。
7.本发明的技术方案为:基于无标记细胞整合药理学技术,利用稳定表达gpr84的细胞系hek293t-gi3-gpr84,借助于已知的激动剂和拮抗剂,建立gpr84受体的细胞筛选模型。根据待测样品的dmr信号谱与已知激动剂和拮抗剂的dmr特征信号谱的相似性和特异性,判断待测样品的激动活性、拮抗活性,或者对下游通路的调节影响。
8.其中,所述的无标记细胞整合药理学技术为利用共振波导光栅(rwg)生物传感器将药物导致的细胞内成分的动态再分布现象转化为整体的、动态的波长位移响应信号,此信号为波长变化的响应值(pm),通过epic光学生物传感器384微孔板实现。
9.其中,所述的gpr84受体的细胞筛选模型是在细胞兼容的具有光学生物传感功能的384微孔板中接种hek293t-gi3-gpr84细胞,接种的细胞密度为1.0 ~ 4.5
ꢀ×ꢀ
104个/孔,细胞培养液体积为40
ꢀµ
l/孔,接种后细胞培养时间为18 ~ 24 h。
10.一种无标记膜受体gpr84的细胞筛选模型的应用,待测样品具有灵敏性、饱和性及特异性的筛选步骤如下:(1)将溶解在hbss缓冲盐中的gpr84受体激动剂gtpl5846加入到接种hek293t-gi3-gpr84细胞的384微孔板中,gpr84受体激动剂gtpl5846的浓度为0.1 ~ 1000 nm,检测其dmr特征信号谱;(2)将溶解在hbss缓冲盐中的gpr84受体拮抗剂gpr84拮抗剂8加入到接种hek293t-gi3-gpr84细胞的384微孔板中,gpr84受体拮抗剂gpr84拮抗剂8的浓度为1 ~ 100000 nm,检测其dmr特征信号谱;(3)向步骤(1)和(2)分别加了gpr84受体激动剂gtpl5846和拮抗剂gpr84拮抗剂8的hek293t-gi3-gpr84细胞的384微孔板中加入具有最高响应强度对应的最低浓度的gtpl5846,检测其特征dmr信号谱;(4)获得的所有dmr特征信号谱具有浓度-响应依赖关系且具有灵敏性、饱和性及特异性。
11.一种无标记膜受体gpr84的细胞筛选模型的应用,待测样品具有激动活性的筛选步骤如下:(1)将溶解在hbss缓冲盐中的gpr84受体激动剂gtpl5846加入到接种hek293t-gi3-gpr84细胞的384微孔板中,gpr84受体激动剂gtpl5846的浓度为0.1 ~ 1000 nm,检测其dmr特征信号谱;(2)将待测样品浓度为0.01 nm ~ 100
ꢀµ
m加入到接种hek293t-gi3-gpr84细胞的微孔板中,检测其dmr信号谱;(3)关联分析步骤(1)和步骤(2)中的dmr信号谱,若步骤(2)的dmr信号谱与(1)中的dmr特征谱具有轮廓相似性;(4)将gpr84受体拮抗剂gpr84拮抗剂8(浓度为1 ~ 100000 nm)加入到接种hek293t-gi3-gpr84细胞的微孔板中,预处理5 ~ 90 min,加入与步骤(2)中相同浓度的待测样品,检测其dmr信号,若此dmr信号强度低于步骤(2)中的dmr信号强度,则判断此样品为gpr84受体的激动剂。
12.一种无标记膜受体gpr84的细胞筛选模型的应用,待测样品具有拮抗活性的筛选
步骤如下:(1)将待测样品和gtpl5846分别加入到接种hek293t-gi3-gpr84细胞的微孔板中,待测样品浓度为0.01 nm ~ 100
ꢀµ
m,gtpl5846浓度为0.1 ~ 1000 nm,检测dmr信号谱;(2)若步骤(1)中待测样品不引起dmr信号谱,向步骤(1)中加入了待测样品的细胞板中继续加入与步骤(1)中相同浓度的gtpl5846,检测dmr信号谱;若此dmr信号比步骤(1)中gtpl5846的信号弱,且其dmr信号谱图与步骤(1)中gtpl5846的dmr谱图轮廓相似,可判断待测样品是gpr84受体的拮抗剂。
13.一种无标记膜受体gpr84的细胞筛选模型的应用,待测样品对gpr84通路有调节活性的步骤如下:(1)将待测样品和gtpl5846分别加入到接种hek293t-gi3-gpr84细胞的微孔板中,待测样品浓度为0.01 nm ~ 100
ꢀµ
m,gtpl5846浓度为0.1 ~ 1000 nm,检测dmr信号谱;(2)向步骤(1)中加入了待测样品的细胞板中继续加入与步骤(1)中相同浓度的gtpl5846,检测dmr信号谱,检测时间为1 ~ 90 min;若此dmr信号比步骤(1)中gtpl5846的信号在上升期、平台期和延滞期某一个阶段不同,若步骤(1)中待测样品不具有dmr响应信号,可判断待测样品是gpr84受体下游信号通路抑制调节剂;(3)向步骤(1)中加入了待测样品的细胞板中继续加入与步骤(1)中相同浓度的gtpl5846,检测dmr信号谱,检测时间为1 ~ 90 min;若此dmr信号比步骤(1)中gtpl5846的信号在上升期、平台期和延滞期某一个阶段不同;若步骤(1)中待测样品具有dmr响应信号,将gpr84受体拮抗剂gpr84拮抗剂8加入到接种hek293t-gi3-gpr84细胞的微孔板中,gpr84受体拮抗剂gpr84拮抗剂8的浓度为1 ~ 10000 nm,预处理5 ~ 90 min,加入与步骤(1)中相同浓度的待测样品,检测其dmr信号,若此dmr信号谱与步骤(1)中的样品的dmr信号谱一致,可判断待测样品是gpr84受体下游信号通路激活调节剂。
14.其中,所述上升期为1 ~ 30 min、平台期为30 ~ 60 min和延滞期为60 ~ 90 min。
15.本发明利用建立的无标记gpr84细胞模型,可为对商品化的小分子库、自主制备的天然产物提取物、组分或化合物库及化学修饰物进行高通量筛选,获得gpr84受体的激动剂、拮抗剂和通路调节剂。此外,根据靶点与疾病的相关性,发现gpr84受体在中枢神经系统疾病、内毒素血症、肥胖、2型糖尿病、血脂异常、混合谱系白血病、炎症性肠病等疾病中发挥重要作用,也可开展相关疾病的药物筛选。
附图说明
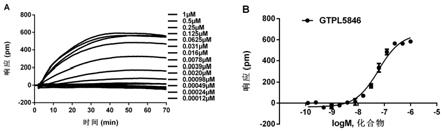
16.图1:(a)不同浓度的gtpl5846在hek293t-gi3-gpr84细胞上的dmr特征信号谱;(b)不同浓度的gtpl5846在hek293t-gi3-gpr84细胞上的浓度-响应依赖曲线。
17.图2:(a)不同浓度的gtpl5846预处理hek293t-gi3-gpr84细胞90 min后,固定浓度gtpl5846的dmr信号谱;(b)不同浓度的gtpl5846预处理hek293t-gi3-gpr84细胞90 min后,固定浓度gtpl5846的dmr信号谱对应的浓度-响应依赖曲线。
18.图3:(a)不同浓度的gpr84拮抗剂8在hek293t-gi3-gpr84细胞上的dmr特征信号谱;图4:(a)不同浓度的gpr84拮抗剂8预处理hek293t-gi3-gpr84细胞90 min后,固定浓度
gtpl5846的dmr信号谱;(b)不同浓度的gpr84拮抗剂8预处理hek293t-gi3-gpr84细胞90 min后,固定浓度gtpl5846的dmr信号谱对应的浓度-响应依赖曲线。
具体实施方式
19.现结合实例,对本发明做进一步说明。实例仅限于说明本发明,而非对本发明的限定。
20.实施例1:gpr84受体激动剂gtpl5846在hek293t-gi3-gpr84细胞上的dmr特征信号谱人胚肾细胞hek293t-gi3-gpr84细胞来源于中国科学院大连化学物理研究所,倒置显微镜购于olympus。gtpl5846(货号:hy-1276(4)和gpr84拮抗剂8(货号:hy-11256(2)购于medchemexpress公司。培养液dmem(货号:01-052-1acs)购于biological industries公司。平衡盐溶液hbss(货号:14065-056)和hepes(货号:15630-080)购于gibco公司。细胞培养板为epic光学生物传感384微孔板,购于康宁公司。检测平台为康宁第三代epic
®
成像仪,购于康宁公司,其检测信号为细胞动态质量重置(dmr)引起的波长位移。
21.将处于对数生长期的hek293t-gi3-gpr84细胞,接种于细胞兼容的384微孔板中,所用培养基为dmem,每孔的接种体积为40
ꢀµ
l,接种密度为2.5
×
104个/孔,将接种好的细胞板置于细胞培养箱中培养20 ~ 24 h,至细胞融合度达95%左右,进行活性检测。将在微孔板中的细胞培养液换成hank's平衡盐溶液(hbss,含20 mm的hepes),每孔加入体积为30 μl,加入之后,放置于epic
®
成像仪上平衡90 min;重新扫描2 min的基线,将gtpl5846加入微孔板中,每孔加入体积为10 μl,浓度为1000 nm、500 nm、250 nm、125 nm、62.5 nm、31.2 nm、15.6 nm、7.8 nm、3.9 nm、2.0 nm、1.0 nm、0.5 nm、0.2 nm和0.1 nm,平行4次,置于epic仪器上实时监测dmr信号90 min,基于细胞经gtpl5846作用的90 min内dmr最大响应值处计算gtpl5846的ec
50
值,结果见图1。实验结果表明gtpl5846激活gpr84受体产生dmr信号响应,且呈现剂量依赖,剂量响应曲线呈单相“s”型且都达到饱和响应,最高的dmr响应值达约600 pm,其ec
50
值为59.8
ꢀ±ꢀ
5.6 nm。
22.实施例2:hek293t-gi3-gpr84细胞的脱敏dmr特征信号谱将处于对数生长期的hek293t-gi3-gpr84细胞,接种于细胞兼容的384微孔板中,所用培养基为dmem,每孔的接种体积为40
ꢀµ
l,接种密度为2.5
×
104个/孔,将接种好的细胞板置于细胞培养箱中培养20 ~ 24 h,至细胞融合度达95%左右,进行活性检测。将在微孔板中的细胞培养液换成hank's平衡盐溶液(hbss,含20 mm的hepes),每孔加入体积为30 μl,加入之后,放置于epic
®
成像仪上平衡90 min;将不同浓度的gtpl5846加入微孔板中预处理hek293t-gi3-gpr84细胞90 min,每孔加入体积为10 μl,浓度为1000 nm、500 nm、250 nm、125 nm、62.5 nm、31.2 nm、15.6 nm、7.8 nm、3.9 nm、2.0 nm、1.0 nm、0.5 nm、0.2 nm和0.1 nm,平行4次;重新扫描2 min的基线,将固定浓度为125 nm的gtpl5846加入微孔板中,每孔加入体积为10 μl,平行4次,置于epic仪器上实时监测dmr信号90 min,基于细胞经gtpl5846作用的90 min内dmr最大响应值处计算ic
50
值,结果见图2。实验结果表明gtpl5846呈剂量依赖地脱敏gpr84受体,剂量响应曲线呈单相“s”型且都达到饱和响应,其的ic
50
值为43.05
ꢀ±ꢀ
7.5 nm。
23.实施例3:gpr84受体拮抗剂gpr84拮抗剂8在hek293t-gi3-gpr84细胞上的dmr特征信号谱将处于对数生长期的hek293t-gi3-gpr84细胞,接种于细胞兼容的384微孔板中,所用培养基为dmem,每孔的接种体积为40
ꢀµ
l,接种密度为2.5
×
104个/孔,将接种好的细胞板置于细胞培养箱中培养20 ~ 24 h,至细胞融合度达95%左右,进行活性检测。将在微孔板中的细胞培养液换成hank's平衡盐溶液(hbss,含20 mm的hepes),每孔加入体积为30 μl,加入之后,放置于epic
®
成像仪上平衡90 min;重新扫描2min的基线,将不同浓度的gpr84拮抗剂8加入微孔板中,每孔加入体积为10 μl,浓度为10000 nm、5000 nm、2500 nm、1250 nm、625 nm、312.5 nm、156.2 nm、78.1 nm、39.0 nm、19.5 nm、9.8 nm、4.9 nm、2.4 nm和1.2 nm,平行4次,置于epic仪器上实时监测dmr信号90 min,结果见图3。实验结果表明不同浓度的gpr84拮抗剂8的dmr响应信号接近于零。
24.实施例4:hek293t-gi3-gpr84细胞的拮抗dmr特征信号谱将处于对数生长期的hek293t-gi3-gpr84细胞,接种于细胞兼容的384微孔板中,所用培养基为dmem,每孔的接种体积为40
ꢀµ
l,接种密度为2.5
×
104个/孔,将接种好的细胞板置于细胞培养箱中培养20 ~ 24 h,至细胞融合度达95%左右,进行活性检测。将在微孔板中的细胞培养液换成hank's平衡盐溶液(hbss,含20 mm的hepes),每孔加入体积为30 μl,加入之后,放置于epic
®
成像仪上平衡90 min。将不同浓度的gpr84受体拮抗剂gpr84拮抗剂8加入微孔板中预处理细胞90 min,每孔加入体积为10 μl,浓度为10000 nm、5000 nm、2500 nm、1250 nm、625 nm、312.5 nm、156.2 nm、78.1 nm、39.0 nm、19.5 nm、9.8 nm、4.9 nm、2.4 nm和1.2 nm,平行4次;重新扫描2 min的基线,将固定浓度为125 nm的gtpl5846加入微孔板中,每孔加入体积为10 μl,平行4次,置于epic仪器上实时监测dmr信号90 min,基于细胞经gtpl5846作用的90 min内dmr最大响应值处计算ic
50
值,结果见图4。实验结果表明gpr84拮抗剂8呈剂量依赖的拮抗gpr84受体,剂量响应曲线呈单相“s”型且都达到饱和响应,其ic
50
值为192.75
ꢀ±ꢀ
36.32 nm。
25.本发明基于无标记细胞整合药理学技术,建立了gpr84无标记筛选模型,此模型具有不需要荧光标记且检测过程无需额外添加指示剂的优势,高效可靠的筛选商品化的小分子库、自主制备的天然产物提取物、组分或化合物库及化学修饰物,以获得gpr84受体的激动剂、拮抗剂和通路调节剂及gpr84受体密切相关的中枢神经系统疾病、内毒素血症、肥胖、2型糖尿病、血脂异常、混合谱系白血病、炎症性肠病等疾病的药物。
26.尽管已经示出和描述了本发的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
