1.与相关申请的交叉引用
2.本技术要求2019年6月19日在韩国知识产权局提交的韩国专利申请号10-2019-0073017的利益,其公开内容整体通过参考并入本文。
3.技术领域
4.本发明涉及一种制备含有硝基的吲哚或吲唑化合物的方法,所述化合物是用于合成制药用吲哚或吲唑化合物所必需的中间体结构。
背景技术:
5.已报道了关于具有吲哚结构作为母核的化合物的许多研究结果,代表性实例包括例如报道了所述化合物具有葡萄糖激酶活性的pct国际公开号wo2006/112549,报道了所述化合物可用作抗肿瘤剂和心血管系统产生的抑制剂的pct国际公开号wo1995/007276,以及报道了所述化合物可用作抗生素的pct国际公开号wo2004/018428。
6.其中,本发明涉及一种制备含有硝基的吲哚或吲唑化合物的方法,所述化合物作为获得对细胞坏死和坏死相关疾病表现出预防或治疗和改善作用的吲哚或吲唑化合物所必需的中间体结构。
7.常规情况下,由于在含有硝基的吲哚或吲唑化合物中间体的合成期间含有醚基的中间体从含有硝基的苯甲酸合成,因此存在着当从作为起始原料的苯甲酸进行卤化反应、乙炔中间体形成反应和环化反应时反应性低的限制,使得副反应率高,并且为了除去由所述副反应产生的副产物,每一步都必须进行柱纯化工艺例如使用硅藻土的过滤纯化。因此,存在着在进行所述柱纯化工艺时每个合成步骤不在同一个反应器中原位进行,因此工艺效率变差,并且柱纯化工艺难以规模放大,因此不能应用于大规模工艺过程的限制。
8.此外,存在着当使用含有醚基的中间体时必需进行用羧酸取代醚基的工艺,因此工艺步骤变得复杂的限制。
9.因此,迫切需要研究一种制备用于获得对细胞坏死和坏死相关疾病表现出预防或治疗和改善作用的吲哚或吲唑化合物所必需的中间体结构的工艺并且提高所述工艺的效率。
10.[现有技术文献]
[0011]
[专利文献]
[0012]
pct国际公开号wo2006/112549(2006年10月26日)
[0013]
pct国际公开号wo1995/007276(1995年3月16日)
[0014]
国际公开号wo2004/018428(2004年3月4日)
技术实现要素:
[0015]
[技术问题]
[0016]
本发明的一个方面提供了一种从含有硝基的苯甲酸化合物制备含有硝基的吲哚
或吲唑化合物的方法,所述吲哚或吲唑化合物作为获得对细胞坏死和坏死相关疾病表现出预防或治疗和改善作用的吲哚或吲唑化合物所必需的中间体结构,其中所述方法可以简化相关领域中的6个或更多个步骤的复杂工艺,提高每个中间步骤反应的反应性以提高产物得率,并用固体纯化代替柱纯化,从而适用于大规模生产工艺。
[0017]
[技术解决方案]
[0018]
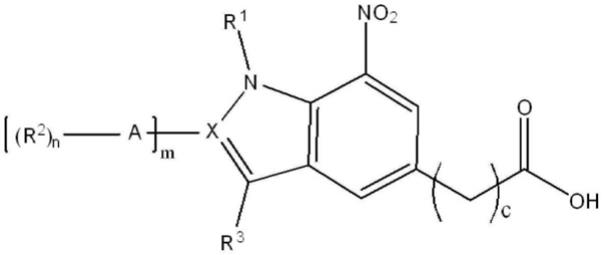
根据本发明的一个方面,提供了一种制备由式1表示的化合物的方法,所述方法包括向由式2表示的化合物添加卤素供体以制备由式3表示的化合物的步骤(步骤a),其中所述卤素供体包括选自n-碘代琥珀酰亚胺、碘化钾(ki)、碘(i2)、n-溴代琥珀酰亚胺、n-氯代琥珀酰亚胺和n-氟苯-磺酰亚胺的至少一者:
[0019]
[式1]
[0020][0021]
其中在上式1中,
[0022]
n是1至3的整数,
[0023]
m是0或1,
[0024]
b是1至3的整数,
[0025]
a表示苯基或各自含有1至3个选自n、o和s原子的杂原子的5元杂芳基或杂环并任选地被r取代,其中r表示氢或任选地被羟基或氨基取代的c
1-c
4-烷基,
[0026]
x表示c或n,前提是当x是n时m是0,而当x是c时m是1,
[0027]
r1表示氢、c
1-c
6-烷基或-(ch2)rnr8r9,其中r是2至5的整数,r8和r9各自独立地表示氢或c
1-c
3-烷基,前提是当x是n时r1是氢,
[0028]
r2表示氢、卤素或c
1-c
6-烷氧基,或表示-(ch2)
p
c(o)2r8、-(ch2)
p
or8、-(ch2)
p
nr8r9、-nhr
10
、-n(h)s(o)2r8或-nhc(o)2r
10
,或表示-(ch2)
p-杂环-r
10
,其中所述杂环组成部分是含有1或2个选自n、o和s原子的杂原子的5-6元环,其中p是0至3的整数,r8和r9如上所定义,并且r
10
表示氢、酮基、c
1-c
6-烷基羰基、c
1-c
6-烷氧基或c
1-c
6-烷基,或表示含有1或2个氮原子作为杂原子的5-6元杂环,并且
[0029]
r3表示氢、卤素、c
1-c
6-烷基或苯基,或表示-(ch2)
q-杂环,其中所述杂环组成部分是含有1或2个选自n和o原子的杂原子的5-6元环,其中q是1至3的整数,前提是当x是n时r3是氢或苯基,
[0030]
其中烷基、烷氧基、芳基、环烷基、杂环和杂芳基可以任选地被取代,并且取代基是选自羟基、c
1-c
6-烷基氨基、二(c
1-c
6-烷基)氨基、羧基、c
1-c
6-烷基、c
1-c
6-烷氧基、羧基-c
1-c
6-烷基和酮基中的一者或多者,
[0031]
[式2]
[0032][0033]
其中在上式2中,
[0034]
c是0至2的整数,并且
[0035]
[式3]
[0036][0037]
其中在上式3中,y是氟、氯、溴或碘,并且
[0038]
c与上式2中所定义的相同。
[0039]
根据本发明的另一方面,提供了一种制备由式6表示的化合物的方法,所述方法包括从由上式1表示的化合物合成由下式6表示的化合物的步骤:
[0040]
[式6]
[0041][0042]
其中在上式6中,
[0043]
r1、r2、r3、n和m与上式1中所定义的相同,
[0044]
r5表示氢、c
1-c
6-烷基、c
3-c
6-环烷基、杂环或杂环基-c
1-c
6-烷基,其中所述杂环是含有1至3个选自n和o原子的杂原子的3-8元环,前提是当x是n时r5是氢,
[0045]
r6表示-(cr8r9)u-z-d-w-r
14
,其中u是0至3的整数,z表示直接连键或选自-c(o)-和-c(o)o-,d表示直接连键、c
4-c
6-环烷基、含有1或2个n原子的5-6元杂芳基或含有1或2个选自n、o和s原子的杂原子的5-6元杂环,w表示直接连键或-nr
8-、-c(o)-、-c(o)o-、-c(o)nr
12-或-s(o)
t-,r
12
表示氢、c
1-c
3-烷基或c
6-c
10-芳基,t是1或2的整数,并且r
14
表示氢、羟基、c
1-c
6-烷基、含有1至3个选自n、o和s原子的杂原子的5-6元杂环或c
6-c
10-ar-c
1-c
6-烷基,前提是当x是n时,r6表示c
4-c
6-环烷基或含有1或2个选自n、o和s原子的杂原子的5-6元
杂环,并且
[0046]
r7表示-y'r
11
,其中y'是直接连键或表示-(cr8r9)hy"-,其中h是0至3的整数,r
11
选自氢、卤素、c
1-c
6-烷基和-(ch2)vb-r
13
,v是0至3的整数,b表示含有1或2个选自n、o和s原子的杂原子的5-6元杂环或表示c
6-c
10-芳基,r
13
表示氢、氰基、卤素、羟基、酮基、硫醇、羧基或羧基-c
1-c
6-烷基,r8和r9如权利要求1中所定义,并且y"选自-o-、-c(o)-和-c(o)o-,前提是当x是n时r7表示氢或c
1-c
6-烷基,
[0047]
其中烷基、烷氧基、芳基、环烷基、杂环和杂芳基可以任选地被取代,并且取代基是选自羟基、c
1-c
6-烷基氨基、二(c
1-c
6-烷基)氨基、羧基、c
1-c
6-烷基、c
1-c
6-烷氧基、羧基-c
1-c
6-烷基和酮基的一者或多者。
[0048]
[有利效果]
[0049]
所述制备本发明的吲哚或吲唑化合物的方法可以通过简化工艺和提高每个中间步骤的反应性来提高产物得率,并且由于与制备含有硝基的吲哚或吲唑化合物的常规方法相比通过提高靶反应的每一步的反应性来降低副产物比率,可以省略使用硅藻土的柱纯化工艺,因此可以极大改进所述工艺的效率,并且通过用固体纯化工艺代替柱纯化工艺,可以被容易地应用于大规模生产工艺。
具体实施方式
[0050]
在下文中将对本发明进行更详细描述,以帮助理解本发明。
[0051]
在本说明书和权利要求书中使用的术语或词语不应被解释为限于常规或词典的含义,而是应该在本发明人可以适合地定义所述术语的概念以便以最佳方式解释本发明的原则的基础上,被解释为与技术精神相符的含义和概念。
[0052]
在根据本发明所述的式(1)的化合物的取代基的定义中,术语“烷基”是指脂族烃基。烷基可以是不包括烯基或炔基组成部分的“饱和烷基”,或者是包括至少一个烯基或炔基组成部分的“不饱和烷基”。术语“烯基”是指含有至少一个碳-碳双键的基团,并且术语“炔基”是指含有至少一个碳-碳叁键的基团。当单独或以复合词形式例如烷氧基使用时,烷基可以是支链或直链的。
[0053]
除非另有定义,否则烷基可以具有1至20个碳原子。烷基可以是具有1至10个碳原子的中尺寸烷基。烷基可以是具有1至6个碳原子的短链烷基。典型的烷基包括但不限于甲基、乙基、丙基、异丙基、丁基、异丁基、叔丁基、戊基、己基、乙烯基、丙烯基、丁烯基等。例如,c
1-c
4-烷基在烷基链中具有1至4个碳原子,并选自甲基、乙基、丙基、异丙基、正丁基、异丁基、仲丁基和叔丁基。
[0054]
除非另有定义,否则术语“烷氧基”是指具有1至10个碳原子的烷氧基。
[0055]
除非另有定义,否则术语“环烷基”是指饱和脂族3-10元环。典型的环烷基包括但不限于环丙基、环丁基、环戊基、环己基等。
[0056]
术语“芳基”包括至少一个具有共价π电子体系的环,例如单环或稠合的多环(即共有相邻的成对碳原子的环)基团。也就是说,除非另有定义,否则芳基是指芳香族4-10元、优选地6-10元单环或多环,包括苯基、萘基等。
[0057]
除非另有定义,否则术语“杂芳基”是指芳香族3-10元环,优选为4-8元环,更优选为5-6元环,其含有1至3个选自n、o和s的杂原子,并且可以与苯环或c
3-c8环烷基稠合。单环
是氢或苯基,
[0072]
其中烷基、烷氧基、芳基、环烷基、杂环和杂芳基可以任选地被取代,并且取代基是选自羟基、c
1-c
6-烷基氨基、二(c
1-c
6-烷基)氨基、羧基、c
1-c
6-烷基、c
1-c
6-烷氧基、羧基-c
1-c
6-烷基和酮基中的一者或多者,
[0073]
[式2]
[0074][0075]
其中在上式2中,
[0076]
c是0至2的整数,并且
[0077]
[式3]
[0078][0079]
其中在化学式3中,y可以是氟、氯、溴或碘,并且
[0080]
c与上式2中所定义的相同。
[0081]
具体来说,在上式1中,上述r1可以是氢、c
1-c
6-烷基或二(c
1-c
3-烷基)氨基-c
2-c
3-烷基。
[0082]
此外,上述r2可以表示氢、卤素、羧基、羧基-c
1-c
3-烷基、c
1-c
3-烷氧基羰基、c
1-c
3-烷氧基羰基-c
1-c
3-烷基、任选地被一个酮基取代的羟基-c
1-c
3-烷基、c
1-c
3-烷氧基、-(ch2)
p
nr8r9、-nhr
10
、-n(h)s(o)2r
10
或-nhc(o)2r
10
,或者可以是-(ch2)
p-杂环-r
10
,其中杂环、p、r8、r9和r
10
如上所定义。
[0083]
此外,r3可以表示氢、甲基或卤素,或者可以表示任选地被c
1-c
3-烷氧基取代的苯基,或者可以是杂环基-c
1-c
3-亚烷基,其中所述杂环组成部分是含有1或2个选自n和o原子的杂原子并且任选地被1或2个酮基取代的5-6元环。
[0084]
此外,上述b具体来说可以是1至2,更具体来说是1。
[0085]
此外,在上式2中,c具体来说可以具有b-1的值,更具体来说是0至1,更具体来说是0。
[0086]
此外,在上式3中,y具体来说可以是溴或碘,更具体来说是碘,并且c与上式2中所定义的相同。
[0087]
此外,所述由上式1表示的化合物可以由下式(1a)或(1b)表示:
[0088]
[式1a]
[0089][0090]
[式1b]
[0091][0092]
其中在上式中,n、a、r1、r2、r3和b如权利要求1中所定义。
[0093]
例如,所述由上述式1或式1a表示的化合物可以是(7-硝基-2-苯基-1h-吲哚-5-基)甲醇,并且所述由上式2表示的化合物可以是4-氨基-3-硝基苯甲酸。
[0094]
此外,根据本发明的实施方式,步骤a)的卤素供体优选可以是n-溴代琥珀酰亚胺或n-碘代琥珀酰亚胺。
[0095]
此外,上述步骤a)可以在酸催化剂存在下进行,其中所述酸催化剂可以包括硫酸、硝酸、乙酸、三氟乙酸和盐酸中的至少一者,优选为硫酸。
[0096]
此外,上述步骤a)可以是在0-25℃的温度下,在所述酸催化剂存在下向由式2表示的化合物添加卤素供体,并在所述添加后,可以通过将温度升高到60-120℃然后将所述混合物搅拌2-10小时,来进行所述由式2表示的化合物的卤代反应。
[0097]
此外,根据本发明的实施方式,在步骤a)后可以进一步包括添加由下式4表示的化合物的步骤(步骤b):
[0098]
[式4]
[0099][0100]
其中在上式4中,
[0101]
r2、a、n和m与式1中所定义的相同,并且
[0102]
r4可以是乙炔。
[0103]
本发明的步骤b)可以是用于将卤代苯甲酸化合物与由上式4表示的乙炔化合物相连的连接反应,并且具体来说,上述步骤b)可以在金属催化剂存在下进行,其中所述金属催化剂可以含有金属例如cu(i)、pd(ii)等,并且所述金属催化剂具体来说可以是采取含有所述金属的卤化物盐形式的化合物。例如,cui和pd(pph3)2cl2可以用作金属催化剂。
[0104]
此外,上述步骤b)可以在30-100℃的温度下进行2-10小时。
[0105]
此外,根据本发明的实施方式,在步骤b)后,可以进一步包括在金属催化剂存在下
添加碱以制备由下式5表示的化合物的步骤(步骤c),其中上述步骤b)和步骤c)可以在同一反应器中进行(原位反应):
[0106]
[式5]
[0107][0108]
其中在上式5中,r1至r3、a、x、n和m与上式1中所定义的相同,并且c与上式2中所定义的相同。
[0109]
在本发明中,上述作为连接反应的步骤b)和上述作为用于形成吲哚或吲哚啉的环化反应的步骤c)可以在同一反应器中连续进行,通过由上式3表示的化合物与由式4表示的化合物的反应形成的中间体化合物在合成后可以不进行单独的分离净化或纯化过程直接与碱反应,以制备由式5表示的化合物,并且即使不进行单独的分离净化或纯化工艺,所述由式5表示的化合物也可以以高得率获得,从而极大提高了工艺的效率。
[0110]
在上述步骤c)中,所述碱可以包括例如叔丁醇钾(kobu
t
)、碳酸钾(k2co3)、1,8-二氮杂二环[5.4.0]十一碳-7-烯(dbu)、三乙胺(et3n)、二异丙基乙胺(etn(ipr)
2-)、n-甲基吗啉、甲基吡咯烷酮和n-甲基丙酰胺(nmpa)中的至少一者,并且优选为dbu。
[0111]
此外,上述步骤c)可以通过添加所述碱,然后将温度升高到50-150℃10-30小时、优选地15-20小时来进行。
[0112]
此外,根据本发明的实施方式,所述制备方法可以进一步包括在上述步骤c)后添加还原剂以制备由上式1表示的化合物的步骤(步骤d)。在这种情况下,上述步骤d)可以通过还原反应制备所述由式1表示的化合物。
[0113]
此外,所述还原剂可以是bh
3-dms(硼烷二甲基硫醚)、nabh4、二异丁基氢化铝(dibal)和氢化锂铝(lah)中的至少一者,优选为bh
3-dms(硼烷二甲基硫醚)。
[0114]
此外,在上述步骤d)中,所述还原剂可以在0-30℃、具体来说5-30℃或10-15℃的温度下添加。此外,所述由式1表示的化合物可以通过添加所述还原剂,然后将温度升高到10-80℃并搅拌2-10小时来合成。
[0115]
此外,根据本发明的另一个实施方式,本发明可以包括一种制备由式6表示的化合物的方法,所述方法包括从由上式1表示的化合物合成由下式6表示的化合物的步骤:
[0116]
[式6]
[0117][0118]
其中在上式6中,
[0119]
r1、r2、r3、n和m与上式1中所定义的相同,
[0120]
r5表示氢、c
1-c
6-烷基、c
3-c
6-环烷基、杂环或杂环基-c
1-c
6-烷基,其中所述杂环是含有1至3个选自n和o原子的杂原子的3-8元环,前提是当x是n时r5是氢,
[0121]
r6表示-(cr8r9)u-z-d-w-r
14
,其中u是0至3的整数,z表示直接连键或选自-c(o)-和-c(o)o-,d表示直接连键、c
4-c
6-环烷基、含有1或2个n原子的5-6元杂芳基或含有1或2个选自n、o和s原子的杂原子的5-6元杂环,w表示直接连键或-nr
8-、-c(o)-、-c(o)o-、-c(o)nr
12-或-s(o)
t-,r
12
表示氢、c
1-c
3-烷基或c
6-c
10-芳基,t是1或2的整数,并且r
14
表示氢、羟基、c
1-c
6-烷基、含有1至3个选自n、o和s原子的杂原子的5-6元杂环或c
6-c
10-ar-c
1-c
6-烷基,前提是当x是n时,r6表示c
4-c
6-环烷基或含有1或2个选自n、o和s原子的杂原子的5-6元杂环,并且
[0122]
r7表示-y'r
11
,其中y'是直接连键或表示-(cr8r9)hy"-,其中h是0至3的整数,r
11
选自氢、卤素、c
1-c
6-烷基和-(ch2)vb-r
13
,v是0至3的整数,b表示含有1或2个选自n、o和s原子的杂原子的5-6元杂环或表示c
6-c
10-芳基,r
13
表示氢、氰基、卤素、羟基、酮基、硫醇、羧基或羧基-c
1-c
6-烷基,r8和r9如权利要求1中所定义,并且y"选自-o-、-c(o)-和-c(o)o-,前提是当x是n时r7表示氢或c
1-c
6-烷基,
[0123]
其中烷基、烷氧基、芳基、环烷基、杂环和杂芳基可以任选地被取代,并且取代基是选自羟基、c
1-c
6-烷基氨基、二(c
1-c
6-烷基)氨基、羧基、c
1-c
6-烷基、c
1-c
6-烷氧基、羧基-c
1-c
6-烷基和酮基的一者或多者。
[0124]
此外,本发明的方法可以在合成步骤a)、步骤c)和步骤d)中的每种产物之后进一步包括纯化步骤,其中所述纯化可以通过固体纯化方法来进行。
[0125]
具体来说,根据本发明的一个实施方式,所述固体纯化可以通过在每个步骤时合成的化合物中添加水、极性有机溶剂或其混合物以形成固体,然后过滤并洗涤所述固体来进行。在这种情况下,所述极性有机溶剂具体来说可以包括醇和二氯甲烷中的至少一者,并且所述醇更具体来说可以包括甲醇、乙醇、丙醇和丁醇中的至少一者。
[0126]
此外,在将水、极性有机溶剂或其混合物添加到化合物中之前,可以通过在减压下蒸馏来获得化合物浓缩物,并且如有必要,所述方法可以进一步包括在减压下蒸馏之前将含有所述化合物的反应器冷却至室温(25
±
5℃)的步骤。
[0127]
下文中将根据实施例更详细地描述本发明。然而,下述实施例旨在说明本发明,而本发明的范围不受其限制。
[0128]
实施例
[0129]
实施例1:(7-硝基-2-苯基-1h-吲哚-5-基)甲醇的合成
[0130]
1)4-氨基-3-碘-5-硝基苯甲酸的合成
[0131]
向反应器添加可商购的4-氨基-3-硝基苯甲酸(由sinochem ningbo co.,ltd.(中国)制造)(5.0kg)、nis(n-碘代琥珀酰亚胺,9.3kg)、h2so4(0.50kg)和thf(25.0l)并在室温下搅拌,然后将反应器加热至80℃的温度并搅拌2小时。在这种情况下,当通过hplc进行的反应混合物的分析结果达到4-氨基-3-硝基苯甲酸的峰的5.0%或更小时,终止反应。
[0132]
在确认反应完成后,将反应器的温度冷却至室温,然后向通过减压蒸馏获得的浓缩溶液添加二氯甲烷(dcm,50.0l)以形成固体。将形成的固体在室温搅拌1小时或更长时间,过滤并洗涤[第1次:dcm(40.0l),第2次:h2o(30.0l),第3次:etoh/h2o=3/7,30.0l],然后在n2压力下干燥16小时,以合成4-氨基-3-碘-5-硝基苯甲酸(7.6kg,得率:89.8%,纯度:96.4%)。
[0133]
1h nmr(500mhz,dmso-d6)δ13.1(br s,1h),8.52(d,j=1.8hz,1h)8.36(d,j=1.8hz,1h),7.50(s,2h)。
[0134]
2)7-硝基-2-苯基-1h-吲哚-5-甲酸的合成
[0135]
向反应器添加上述1)的4-氨基-3-碘-5-硝基苯甲酸(7.6kg)、三乙胺(tea,7.5kg)、苯基乙炔(3.0kg)和1,4-二噁烷(76.0l)并在室温下搅拌,然后向其添加作为反应催化剂的cui[碘化亚铜(i),47.0g]和pd(pph3)2cl2(173.0g),并将反应器加热至60℃的温度。将反应混合物搅拌2小时。然后,当通过hplc分析反应混合物显示4-氨基-3-碘-5-硝基苯甲酸的峰为1.0%或更小时,终止反应。
[0136]
然后,向反应混合物添加1,8-二氮杂二环[5.4.0]十一碳-7-烯(dbu,22.5kg),并将反应器加热至110℃的温度,将反应混合物搅拌18小时,然后终止反应。在反应混合物冷却至室温后,用3n-hcl水溶液(114.0l)将ph调整到3,向其添加h2o(38.0l),将混合物搅拌2小时或更长时间,过滤并洗涤[第1次:h2o(38.0l),第2次:etoh/h2o=3/7,23.0l],然后在n2压力下干燥16小时,以合成7-硝基-2-苯基-1h-吲哚-5-甲酸(6.1kg,得率:87.4%,纯度:98.0%par)。
[0137]
1h nmr(500mhz,dmso-d6)δ11.6(s,1h),8.03(s,1h),7.96(m,3h),7.46(t,j=7.7hz,2h)7.36(d,j=7.3hz,1h),7.10(s,1h)
[0138]
3)(7-硝基-2-苯基-1h-吲哚-5-基)甲醇的合成
[0139]
向反应器添加上述2)的7-硝基-2-苯基-1h-吲哚-5-甲酸(5.8kg)和四氢呋喃(thf,61l)并在室温下搅拌,然后将反应混合物冷却至12
±
2℃,并向其缓慢地逐滴添加5m硼烷二甲基硫醚(bh
3-dms,12.3l),使其内部温度不超过40℃。在滴加完成后,将反应器加热至40℃的温度,将反应混合物搅拌2小时,然后在通过hplc分析反应混合物显示出7-硝基-2-苯基-1h-吲哚-5-甲酸的峰为1.0%或更小时,终止反应。
[0140]
在确认反应完成后,向反应混合物缓慢地逐滴添加h2o(55l),然后将混合物进行层分离以保存有机层,并将水层用乙酸乙酯(etoac,29l)萃取,与所述保存的有机层混合,并在减压下蒸馏。向得到的浓缩溶液添加乙醇/水混合溶剂(乙醇:6.1l/水:12.2l),搅拌2小时或更长时间,然后过滤。然后将得到的混合物用乙醇/水混合溶剂(etoh/h2o=1/3,9.0l)作为清洗液洗涤,然后在n2压力下干燥16小时,以合成(7-硝基-2-苯基-1h-吲哚-5-基)甲醇(4.6kg,得率:83.5%,纯度:98.4%)。
[0141]
1h nmr(500mhz,dmso-d6)δ11.6(s,1h),8.07(s,1h),8.00(m,3h),7.49(t,j=7.7hz,2h)7.40(d,j=7.3hz,1h),7.14(s,1h),5.42(t,j=6.7hz,1h),4.66(d,j=6.7hz,2h)。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。