一种基于精浆外泌体mrna表达谱术前评估无精子症的试剂盒
技术领域
1.本发明属于生物医学技术领域,具体涉及一种基于精浆外泌体mrna表达谱术前评估无精子症的试剂盒。
背景技术:
2.无精子症是最严重的一种男性不育症,可分为梗阻性无精子症(obstructive azoospermia,oa)和非梗阻性无精子症(nonobstructive azoospermia,noa)。目前临床上主要借助男科手术(复通手术、睾丸取精术等)满足无精子症患者生育需求,但实现其有效治疗的前提是准确判断无精子症的类型及其梗阻部位、取精结局等。因此,术前精准评估无精子症患者病情至关重要,有助于选择合适的手术方式,以及避免不必要的手术或二次手术。根据无精子症的规范诊疗流程,目前用于术前评估患者病情的方法主要包括精浆生化、男科超声、性激素及睾丸穿刺活检等。但现有临床方法均存在一定的局限性,主要为:首先,对于无精子症疾病分型(oa还是noa)的评估往往需要综合上述多种临床方法,难以通过单次检测实现无精子症全面且精准的病情评估,而这也明显增加患者的时间成本和经济负担。其次,具体梗阻部位的明确,对于oa患者是否手术及采取何种手术方式至关重要,然而,目前精浆生化及男科超声仅能对oa患者梗阻部位进行粗略判断,较难实现对附睾头、附睾体、附睾尾等细分部位的评估。此外,对于noa患者取精结局的评估方法,目前主要包括性激素、睾丸穿刺活检及精浆游离rna检测,例如,当患者fsh高于正常值上限时,通常认为该患者取精结局较差;睾丸穿刺活检若提示有精子,通常认为该患者取精结局较好。现有方法难以术前无创且精准预测noa取精结局的原因主要包括:性激素检测虽然技术成熟,但其检测敏感性欠佳,不易判别睾丸内是否有精的细微差异;睾丸组织样本获取为有创检查,难以推广;精浆中游离rna虽可实现无创检测,但其检测的敏感性与稳定性较差。
3.可见,上述方法难以通过单次检测实现无精子症无创、全面且精准的病情评估,易导致患者得不到最优临床处理。因此,术前精准评估无精子症患者病情至关重要,而这也正是男性不育领域亟需解决的临床问题。
4.外泌体(exosomes)是一类直径约30
‑
150nm,具有磷脂双分子层的细胞外囊泡,是细胞间信号转导的重要载体,可参与调控多种生理和病理反应。外泌体在血液、精液、尿液、乳液和唾液等人体体液中含量丰富,可携带反映亲代细胞信息的rna成分,同时具有稳定性好、可富集rna等特点,是生物学标志物的理想来源。因此,外泌体检测是目前液体活检领域的新兴方向。已有研究报道,睾丸、附睾、前列腺、精囊等生殖腺体所分泌的外泌体在精浆中含量丰富,可携带参与精子发生、精子成熟等过程的rna。基于此,本发明人以精浆外泌体中生殖腺体特异性mrna为研究对象,寻求能术前全面、无创且精准地评估无精子症患者病情的方法。
技术实现要素:
5.为了解决上述技术问题,本发明提供了一组术前评估无精子症的标志物以及试剂
盒,可用于无精子症的分型,能单次完成无精子症的术前精准评估。
6.本发明采用以下技术方案实现本发明的目的:
7.一组用于无精子症精确分型的生物分子标记物,所述分子标记为精浆外泌体mrna,所述mrna包括prm2、adam28、wfdc13、wfdc9、semg2、psa。
8.优选地,所述的prm2为睾丸特异性表达生物标志物,所述adam28为附睾头特异性表达生物标志物,所述wfdc13为附睾体特异性表达生物标志物,所述wfdc9为附睾尾特异性表达生物标志物,所述semg2为精囊特异性表达生物标志物,所述psa为前列腺特异性表达生物标志物。
9.优选地,所述prm2的ncbi id为nm_002762.4,所述adam28的ncbi id为nm_014265.6,所述wfdc9的ncbi id为nm_147198.4,所述semg2的ncbi id为nm_003008.3,所述psa的ncbi id为nm_001648.2所述wfdc13的ncbi id为nm_172005.2。
10.优选地,所述prm2的核苷酸序列如seq id no:1所示,所述adam28的核苷酸序列如seq id no:2所示、所述wfdc9的核苷酸序列如seq id no:3所示,所述semg2的核苷酸序列如seq id no:4所示,所述psa的核苷酸序列如seq id no:5所示,所述wfdc13的核苷酸序列如seq id no:6所示。
11.本发明还提供了所述分子标记为在用于评估术前无精子症试剂盒中的应用。
12.本发明还提供了一种用于评估术前无精子症试剂盒,所述试剂盒包括如权利要求1所述的mrna。
13.优选地,所述试剂盒还包括用于扩增权利要求1所述mrna的引物,所述引物序列如seq id no:7~18所示。
14.优选地,所述试剂盒还包括rna裂解液和内参基因。
15.本发明还提供了所述的试剂盒在制备评估术前无精子症制剂中的用途。
16.本发明具有以下有益效果:
17.(1)本发明的试剂盒具有无创的特点:以精液作为样本来源,实现无创。
18.(2)本发明的试剂盒具有检测全面且精准的特点:以精浆外泌体为标志物来源,聚焦至生殖腺体(睾丸、附睾头、附睾体、附睾尾、精囊、前列腺)特异性mrna,通过全面检测精浆外泌体中各部位特异性mrna表达,包括prm2、adam28、wfdc13、wfdc9、semg2及psa,以明确是否有梗阻(疾病分型,oa或者noa)以及梗阻部位;若初步判定为noa,则进一步评估其取精结局。
19.(3)本发明的试剂盒具有检测敏感且稳定的特点:基于外泌体的rna富集效应及其稳定性,同时结合精浆外泌体长链rna模板扩增及qrt
‑
pcr检测技术,对精浆中生殖腺体特异性mrna信号进行放大并获取,以实现检测的敏感性与稳定性。
附图说明
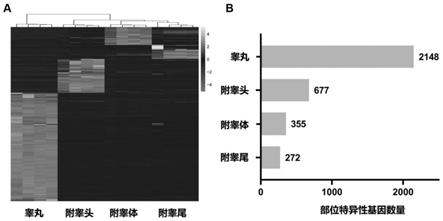
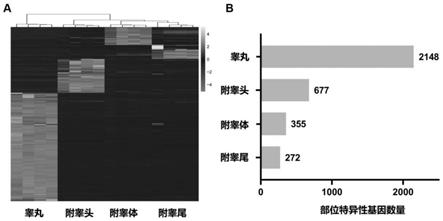
20.图1为正常年轻雄性小鼠的4个部位特异性表达的mrna热图及数量示意图(目标部位vs.其它各部位,差异倍数>4倍)
21.图2为候选标志物的初筛流程图,主要按照小鼠部位高表达、小鼠与人类物种间保守性良好、人类组织中功能重要、人类组织中特异性强等要求,在已测得的正常雄性小鼠生殖腺体节段特异性mrna中进行逐级筛选。为了克服人类生殖腺体组织,尤其是睾丸、附睾较
难获取这一问题,我们首先借助正常年轻小鼠生殖腺体组织测序,筛选出在睾丸及附睾头、附睾体、附睾尾组织表达的生殖腺体特异性mrna;其次,我们结合人类公共数据库(genecards数据库、ucsc genome browser数据库),筛选出物种间(小鼠与人)保守性良好的特异性mrna;最后,我们根据已有的数据库(string数据库、the human protein atlas数据库),进一步筛选出在人类组织中功能重要且特异性强的特异性mrna。
22.图3为雄性小鼠的睾丸及附睾头、附睾体、附睾尾中表达量分别在前25的特异性mrna示意图
23.图4为从小鼠特异性mrna中筛选出在人类组织中也有表达的mrna示意图。
24.图5为从所得mrna所对应的蛋白互作关系筛选具有重要作用的mrna的示意图
25.图6从所得mrna所对应蛋白为人睾丸特异性或附睾特异性的蛋白以筛选组织特异性好的mrna的示意图
26.图7本发明分子标记物的表达情况示意图(a为正常人精浆外泌体测序结果中的目的基因表达;b为prm2在正常人(norm.)、noa患者睾丸内有精(sperm( ))、noa患者睾丸内无精(sperm(
‑
))中的表达;c为prm2在noa患者睾丸内有精与noa患者睾丸内无精的roc曲线)
27.图8精浆外泌体生殖腺体特异性mrna表达谱示意图
28.图9本发明基于精浆外泌体mrna表达谱构建试剂盒的应用示意图
具体实施方式
29.为了更加简洁明了的展示本发明的技术方案、目的和优点,下面结合具体实施例详细说明本发明的技术方案。如无特殊说明,本发明实施例中所涉及的试剂均为市售产品,均可以通过商业渠道购买获得。
30.实施例1生物分子标志物的筛选
31.本发明生物分子标志物的筛选步骤具体如下:
32.1、首先对正常年轻雄性小鼠的4个部位(睾丸、附睾头、附睾体、附睾尾)进行了转录组测序。结果如图1所示,睾丸特异性mrna数量最多,达到2148个,附睾3个部位的特异性mrna数量依次为677个(附睾头)、355个(附睾体)、272个(附睾尾)。
33.2、从上述步骤1获得的特异性mrna中筛选出分别在睾丸、附睾头、附睾体、附睾尾中表达量靠前的25个特异性mrna。结果如图3所示,在雄性小鼠睾丸及附睾头、附睾体、附睾尾各节段中特异性高表达的mrna共100个特异性mrna(睾丸、附睾头、附睾体、附睾尾各25个,附睾共75个)。
34.3、从所述步骤2获得的100个小鼠特异性mrna中筛选出在人类组织中同样有表达的mrna,获得物种高度保守性的mrna。结果如图4所示,小鼠睾丸25个特异性mrna中有24个与人类基因序列高度保守的特异性mrna;小鼠附睾75个特异性mrna中有60个与人类基因序列高度保守的特异性mrna。数据参考自genecards数据库与ucsc genome browser数据库。
35.4、将步骤3所得mrna所对应的蛋白互作关系,以筛选具有重要作用的mrna。结果如图5所示,小鼠睾丸24个特异性mrna中有18个预测具有重要蛋白互作关系的特异性mrna;小鼠附睾60个特异性mrna中有35个预测具有重要蛋白互作关系的特异性mrna。数据参考自string数据库。
36.5、通过步骤4所得mrna所对应蛋白确定为人睾丸特异性或附睾特异性的蛋白,用
所述蛋白筛选组织特异性高的mrna。结果如图6所示,小鼠睾丸18个特异性mrna中有13个特异性mrna其所对应蛋白为人睾丸特异性;附睾35个特异性mrna中有8个特异性mrna其所对应蛋白为人附睾特异性。数据参考自the human protein atlas数据库。
37.6、为了验证上述筛选出的特异性mrna是否能作为分子标志物,我们进行了验证,具体如下:
38.在正常男性精浆外泌体(n=5)中检测了睾丸、附睾、前列腺和精囊组织中特异性mrna的表达。结果表明,有9个睾丸特异性mrna在人类精浆外泌体中有表达,这9个mrna分别为:prm2、prm1、crisp2、oaz3、akap4、odf1、tcp11、gapdhs;进一步分析发现表达量最高的prm2与精子的发生密切相关,且prm2可作为单指标即可较好地区分noa患者显微取精结局(auc=0.7811)。附睾中共有3个特异性mrna在人类精浆外泌体中有表达,分别为adam28(附睾头)、wfdc13(附睾体)、wfdc9(附睾尾)。此外,已知的精囊特异性mrna(semg2)及前列腺特异性mrna(psa)(数据参考自the human protein atlas数据库)也在精浆外泌体中检测出有较高表达。
39.基于上述结果,我们确定了用于术前评估无精子症分型的6个分子标志物,具体为:睾丸(prm2,ncbi id为nm_002762.4)、附睾头(adam28,ncbi id为nm_014265.6)、附睾体(wfdc13,ncbi id为nm_172005.2)、附睾尾(wfdc9,ncbi id为nm_147198.4)、精囊(semg2,ncbi id为nm_003008.3)及前列腺(psa,ncbi id为nm_001648.2)。
40.实施例2用于术前评估无精子症分型的分子标志物的应用
41.基于本发明筛选出的分子标志物可构建一种用于术前评估无精子症分型的试剂盒,该试剂盒包括实施例1获得的6个分子标记物。本发明试剂盒具体使用方法如下:
42.1、精浆外泌体的提取与纯化
43.取精液(>0.5ml),以4℃,12000
×
g条件下离心30min除去细胞碎片,上清液经0.22μm滤器过滤后以4℃,100000
×
g条件超速离心70min收集外泌体沉淀。沉淀经pbs重悬后再次以4℃,100000
×
g超速离心70min进行纯化,获取外泌体沉淀。
44.2、提取精浆外泌体rna并进行实时荧光定量聚合酶链式反应(qrt
‑
pcr)检测
45.经步骤1获得纯化的外泌体沉淀后,加入rna裂解液,以酚氯仿提取法获得外泌体总rna,使用nanodrop2000检测rna浓度及纯度。以500ng rna/10μl体系进行逆转录反应,得到逆转录反应液并检测其浓度。使用depc水将逆转录反应液稀释至10ng/μl,并以20μl/管分装于
‑
80℃保存。调整逆转录反应液浓度至2.5ng/μl用于qrt
‑
pcr检测。以β
‑
actin作为内参基因,每个基因检测3个副孔,并设定以下反应程序:经95℃预变性30s后,建立99个循环的模板扩增步骤,95℃处理5s;60℃处理20s。最后建立溶解曲线程序以检测产物特异性,95℃处理5s;60℃处理1min;95℃处理5s。反应结束后导出各副孔循环数,各副孔间循环数波动应保持在
±
0.3个循环。目的基因(即实施例1中的6个分子标记物)循环数均值与β
‑
actin循环数均值做差值,得到每个目的基因的delta ct值(循环阈值)。本步骤中,各目的基因的扩增引物序列如表1所示:
46.表1:精浆外泌体mrna表达谱引物序列
[0047][0048]
3、根据步骤2计算得到目的基因的delta ct值,判定精浆外泌体中6个生殖腺体特异性mrna的表达情况,结果主要包括:
[0049]
(a)当prm2的delta ct值<5时,判定为强阳性( ),当5<delta ct值<20时,判定为阳性( ),当delta ct值>20时,判定为阴性(
‑
);
[0050]
(b)当adam28的delta ct值<15时,判定为阳性( ),当delta ct值>15时,判定为阴性(
‑
);
[0051]
(c)当wfdc13的delta ct值<20时,判定为阳性( ),当delta ct值>20时,判定为阴性(
‑
);
[0052]
(d)当wfdc9的delta ct值<20时,判定为阳性( ),当delta ct值>20时,判定为阴性(
‑
);
[0053]
(e)当semg2的delta ct值<10时,判定为阳性( ),当delta ct值>10时,判定为阴性(
‑
);
[0054]
(f)当psa的delta ct值<15时,判定为阳性( ),当delta ct值>15时,判定为阴性(
‑
)。
[0055]
4、根据上述结果,构建基于精浆外泌体mrna的无精子症术前评估体系,即单次检测无精子症患者精浆外泌体中睾丸、附睾、精囊、前列腺特异性mrna的表达,依据其表达谱的变化,明确疾病分型(是否有梗阻,即oa或noa)。若判定为oa,则可进一步判定其梗阻部位;若判定为noa,则可进一步评估其取精结局(即noa无精或noa有精)。基于上述流程,获得由6个分子标志物构建的表达谱(表2),参照该分子表达谱可精准判定无精子症病情。
[0056]
表2:本发明分子标志物的表达谱
[0057][0058]
综上,通过本发明筛选出6个可在精浆外泌体中表达的特异性mrna,并依据其表达水平的高低评估无精子症患者病情,以实现单次检测精浆外泌体中生殖腺体特异性mrna表达谱术前全面、无创且精准无精子症病情的目的。
[0059]
最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的实质和范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。