1.本发明属于上转换发光和重金属离子检测技术领域,具体涉及一种对重金属离子具有荧光增强响应特性的低毒性四碘代荧光素螺环内硫酯荧光探针及其制备方法与应用。
背景技术:
2.在各种重金属中,汞离子更是被认为是毒性最强的金属离子之一。汞离子在极低浓度也会导致多种人类健康问题,包括视力丧失、严重的认知运动障碍、产前脑损伤以及对人类心脏、肾脏、胃等的损害,甚至会导致哺乳动物死亡。因此,开发高效灵敏的铜离子和汞离子化合物得到广泛研究。近年来,离子的化合物主要集中在发光性能优异的的罗丹明类化合物,但荧光素类化合物也同样拥有略逊于罗丹明发光性能的优点,因此近期也有部分基于荧光素的化合物被开发,而带卤素的荧光素由于重原子的存在,不利于荧光发光效率的提高,限制了其应用。
技术实现要素:
3.本发明的目的是提供一类四碘代荧光素螺环内硫酯类荧光探针分子及其制备方法;该类探针分子可通过上/下转换荧光快速增强响应来检测汞离子,且对细胞伤害性小,具有潜在的活体细胞应用价值。
4.为达上述发明目的,本发明采用的技术方案是:一种低毒性四碘代荧光素螺环内硫酯荧光探针,具有如下化学结构式:。
5.本发明公开了上述低毒性四碘代荧光素螺环内硫酯荧光探针作为汞离子荧光探针的应用。
6.本发明公开了上述低毒性四碘代荧光素螺环内硫酯荧光探针在生物成像中的应用;或者本发明公开了上述低毒性四碘代荧光素螺环内硫酯荧光探针在制备生物成像试剂中的应用。优选的,生物成像为细胞成像。
7.本发明公开了上述低毒性四碘代荧光素螺环内硫酯荧光探针的制备方法,以四碘代荧光素、三氯氧磷、硫化钠为原料,反应制备低毒性四碘代荧光素螺环内硫酯荧光探针。
8.本发明公开了一种汞离子检测试纸,由试纸与上述低毒性四碘代荧光素螺环内硫酯荧光探针组成;其制备方法为,将试纸浸泡所述低毒性四碘代荧光素螺环内硫酯荧光探
针的溶液后,干燥得到汞离子检测试纸。
9.本发明公开了利用上述低毒性四碘代荧光素螺环内硫酯荧光探针检测待测溶液中汞离子的方法,包括以下步骤:(1)以四碘代荧光素、三氯氧磷、硫化钠为原料,反应制备低毒性四碘代荧光素螺环内硫酯荧光探针;(2)将所述低毒性四碘代荧光素螺环内硫酯荧光探针的溶液与待测溶液混合,然后用光照射,检测荧光光谱;根据荧光光谱完成待测溶液中汞离子的检测;或者(3)将试纸浸泡所述低毒性四碘代荧光素螺环内硫酯荧光探针的溶液后,干燥得到检测试纸;将待测溶液滴在所述检测试纸上,根据颜色变化完成待测溶液中汞离子的检测。
10.本发明中,所述四碘代荧光素具有如下化学结构式:。上述技术方案中,先将四碘代荧光素与三氯氧磷反应,得到四碘代荧光素酰氯;再将四碘代荧光素酰氯与硫化钠反应,得到低毒性四碘代荧光素螺环内硫酯荧光探针。
11.优选的,四碘代荧光素、三氯氧磷、硫化钠的用量比例为1 mmol∶(0.8~1.2 ml)∶1 0mmol。
12.优选的,四碘代荧光素与三氯氧磷的反应为回流反应6~10小时;四碘代荧光素酰氯与硫化钠的反应为氮气下回流反应20~30小时。
13.优选的,四碘代荧光素与三氯氧磷反应的溶剂为二氯乙烷,反应结束旋蒸,得到的中间产物无需提纯,直接与硫化钠在氮气氛中回流反应,反应结束后,旋转蒸发除去溶剂,通过柱层析和真空干燥,得到低毒性四碘代荧光素螺环内硫酯荧光探针。
14.上述技术方案示意如下:本发明使用的是反斯托克斯发射,即“长波长激发,短波长发射”的上转换检测方法。由于以长波长光为激发的光源,可加深激发光源在介质中的穿透力,检测深度广;同时,因其所需激发能量较低,可有效地消除生物体背景荧光从而提高检测分辨率;另外,又因其所需激发能量较低,对生物活体细胞的检测杀伤力小,使其在生物成像和细胞环境检测中
具有潜在应用价值。因而,相对于斯托克斯发射的荧光(即下转换荧光)检测技术,上转换检测技术则具有更诱人的应用价值。
15.本发明中,可以采用荧光光谱检测待测溶液中的汞离子;也可以采用检测试纸肉眼观察,检测待测溶液中的汞离子。
16.上述技术方案中,采用荧光光谱检测待测溶液中的汞离子时,荧光光谱为下转换荧光光谱或者上转换荧光光谱。优选的,荧光光谱为下转换荧光光谱时,低毒性四碘代荧光素螺环内硫酯荧光探针的溶液中,低毒性四碘代荧光素螺环内硫酯荧光探针的浓度为5~15 μm;荧光光谱为上转换荧光光谱时,低毒性四碘代荧光素螺环内硫酯荧光探针的溶液中,低毒性四碘代荧光素螺环内硫酯荧光探针的浓度为0.05~10mm。进一步的,荧光光谱为下转换荧光光谱时,激发光波长为500 nm;荧光光谱为上转换荧光光谱时,激发光波长为655 nm。
17.上述技术方案中,采用检测试纸检测待测溶液中的汞离子时,低毒性四碘代荧光素螺环内硫酯荧光探针的溶液中,低毒性四碘代荧光素螺环内硫酯荧光探针的浓度为0.5
×
10
‑4~1.5
×
10
‑
4 m。颜色变化为,肉眼观察下,检测试纸的颜色由白色变为玫瑰红色时,待测溶液中含有汞离子,反之,不含汞离子。
18.本发明的技术方案具有如下技术效果和优点:本发明的探针制备方法简单,毒性很小;探针的检测体系为水/dmso(1/2, v/v)中性介质,实用性强;首次运用同一化合物实现三通道荧光检测(stokes荧光、opa
‑
uc荧光和tta
‑
uc荧光),对汞离子的传统的的stokes荧光的检测限和量程分别为8.617
×
10
‑
9 m和0~10 mm,而tta
‑
uc荧光检测限在nm级别(1.48
×
10
‑
9 m),而opa
‑
uc荧光检测量程在mm级别(0~0.5 mm),结果表明:将上述两种弱光上转换检测方法同时运用在对汞离子的检测,可实现单一化合物分子同时达到高灵敏性(nm级别)和宽检测范围(mm级别)的要求,解决了使用常规的荧光检测方法始终存在着高灵敏性和宽检测范围之间的矛盾,具有鲜明的特色和创新性;探针试纸可用于高浓度的汞离子的裸眼检测,且探针试纸遇汞均可快速变色,方便快捷;opa
‑
uc检测所用仪器为小型半导体激光器和光纤光谱仪,无需常规的大型荧光光谱仪器,因此,opa
‑
uc检测显示出更加经济和便携。从而使得上转换检测技术更具实际应用价值。
附图说明
19.图1 为四碘代荧光素螺环内硫酯的核磁氢谱(氘代dmso);图2为四碘代荧光素螺环内硫酯的质谱图;图3为四碘荧光素螺环内硫酯荧光探针的吸收光谱(探针浓度:10 μm)、下转换荧光光谱(探针浓度:10 μm)和上转换荧光光谱(探针浓度:100 μm),溶剂:dmso);图4为在不同ph值下,四碘荧光素螺环内硫酯荧光探针的荧光光谱(其中,探针浓度10 μm,水/dmso:1/2,v/v,激发波长:500 nm);图5为在不同ph值下,四碘荧光素螺环内硫酯荧光探针的最大荧光峰位强度的变化(其中,探针浓度10 μm,水/dmso:1/2,v/v,激发波长:500 nm);图6为加入16种金属阳离子后,探针的下转换荧光增强光谱(其中,阳离子浓度100 μm,探针浓度10 μm);
图7为加入16种金属阳离子后,探针的荧光响应变化柱状图(纵坐标f/f0为加入hg
2
前后探针在577nm荧光强度)(其中,阳离子浓度100 μm,探针浓度10 μm);图8为加入16种金属阳离子后,探针的上转换荧光增强光谱(其中,阳离子浓度100 μm,探针浓度100 μm);图9为加入16种金属阳离子后,探针的上转换增强响应柱状图(纵坐标ucpl/ucpl0为加入hg
2
前后探针在592 nm上转换荧光强度)(其中,阳离子浓度100 μm,探针浓度100 μm);图10为加入不同浓度的汞离子(0~10 mm),探针下转换荧光光谱(其中,探针浓度10 μm,激发波长500 nm);图11为加入不同浓度的汞离子(0~10 mm),探针的工作曲线(纵坐标f/f0为加入hg
2
前后探针在561 nm荧光强度)(其中,探针浓度10 μm,激发波长500 nm);图12为加入不同浓度的汞离子(0~0.5 mm),探针上转换荧光光谱(纵坐标ucpl/ucpl0为加入hg
2
前后探针在592 nm荧光强度)(其中,探针浓度1mm,激发波长655 nm);图13为加入不同浓度的汞离子(0~100 mm),探针的工作曲线(纵坐标ucpl/ucpl0为加入hg
2
前后探针在572 nm荧光强度)(其中,探针浓度100 μm,激发波长655 nm);图14为探针加入hg
2
后随时间变化荧光图(其中,探针浓度为10 μm,hg
2
浓度=100 μm,激发波长500 nm);图15为探针加入hg
2
后在575 nm处荧光强度的工作曲线(其中,探针浓度为10 μm,hg
2
浓度=100 μm,激发波长500 nm);图16为探针加入hg
2
后随时间变化荧光图(其中,探针浓度为100 μm,hg
2
浓度=300 μm,激发波长655 nm);图17为探针加入hg
2
后在584 nm处荧光强度的工作曲线(其中,探针浓度为300 μm,hg
2
浓度=100 μm,激发波长655 nm);图18为探针试纸条检测hg
2
的颜色变化(hg
2
浓度从左到右依次为:0,0.1,0.5,1,10,单位:mm);图19为luc
‑
1对金属离子的下转换荧光增强响应图;图20为luc
‑
5对金属离子的下转换荧光增强响应图;图21为 luc
‑
7对阳离子的的tta
‑
uc荧光选择性(luc
‑
7/dpa:10 μm/1 mm,离子:10 μm);图22为加入不同浓度汞离子后的luc
‑
7的tta
‑
uc荧光光谱及其工作曲线(luc
‑
7/dpa:10 μm/1 mm,dmso);图23为经过不同浓度luc
‑
7处理的4t1细胞的mmt分析;图24为经过luc
‑
7(10
ꢀµ
m)处理的老鼠4t1细胞加入不同浓度hg
2
后的荧光共聚成像(dapi: λ
ex = 405 nm;dye: λ
ex = 488 nm)。
具体实施方式
20.本发明公开的四碘代荧光素螺环内硫酯类荧光探针分子,对汞离子具有“上/下转换荧光”快速增强响应特性,对水环境或生物体中汞离子检测具有应用价值。
21.实验仪器及试剂
137.81, 136.36, 134.84, 130.35, 128.06, 123.72, 121.68, 117.43, 99.33 (d, j = 23.7 hz), 84.07, 81.89, 78.10。ms,计算值:[m h
] =852.63948,测试值:[m na
] = 852.64029;见附图1、附图2。
[0026]
实施例二四碘荧光素螺环内硫酯的荧光表征 探针溶液的吸收光谱和荧光光谱四碘荧光素螺环内硫酯荧光探针的吸收光谱、荧光光谱(即下转换荧光光谱)和上转换荧光光谱见图3所示。由吸收光谱(附图3)可见,探针分子的吸收峰位于~358 nm处,在545 nm处则出现非常微弱的吸收峰;这使得探针分子的粉末固体呈现淡粉红,而在dmso溶液中则为均无色溶液。
[0027]
在500 nm波长的光激发下测得探针溶液(10 mm)的下转换荧光光谱,见附图3。可见,探针的荧光峰位在563 ~569 nm处。值得注意的是,通过对比可以明显看出,在563~569 nm处的荧光峰的强度是非常弱的。
[0028]
在655 nm波长的光激发下,测得探针溶液(100 mm)的上转换荧光光谱,见附图3。可以看出,探针分子的上转换荧光强度非常之弱。
[0029]
ph值对探针的荧光光谱的影响ph为1~14的水溶液配制:分别配制0.1 m naoh水溶液和0.1 m hcl水溶液,通过ph计调整ph值,依次配制为ph为1~14的水溶液。
[0030]
然后,分别取出2 ml ph为1~14的水溶液,加入到14个比色皿中;再分别加入0.003 ml的探针溶液(10 μm)于上述14个比色皿中,用dmso定容至3 ml,得到ph为1~14的探针溶液。测试在不同ph值下,探针溶液的荧光光谱和最大荧光峰位强度的变化,见附图4、附图5。可见,在ph ≤11时,探针分子不出现荧光。由于本发明反应型的荧光探针检测为荧光增强响应;故在检测之前,探针分子不呈现荧光是一个好的优点,而且中性环境适合生物体的检测。
[0031]
实施例三汞离子检测取0.0426 g(0.001 mol)四碘荧光素螺环内硫酯于容量瓶中,加入5 ml dmso,超声振荡使其溶解,配制得到浓度为10 mm的母液,避光保存。
[0032]
下转换荧光检测溶液配制:取3 ml缓冲液/dmso(1/2,v/v)于石英比色皿中,再取出3 μl 上述母液加入石英比色皿中,超声溶解,即配得10 μm的下转换探针检测液。
[0033]
上转换荧光检测溶液配制:取3 ml缓冲液/dmso(1/3,v/v)于石英比色皿中,再取出30 μl 上述母液加入石英比色皿中,超声溶解,即配得100 μm的上转换探针检测液。
[0034]
上述缓冲液(ph=7)的配制如下:称取1.2114 g(0.01 mol)的三羟甲基氨基甲烷(tris)于100 ml去离子水中,溶解后得到三羟甲基氨基甲烷(tris)水溶液(0.1 m);再取出8.3 ml的浓盐酸(hcl,36%)稀释至1000 ml,配得hcl稀溶液(0.1 m);然后,分别取出50 ml的tris溶液和45.7 ml hcl稀溶液,用ph计微调至ph=7,定容至100 ml,即配得0.05 m的三羟甲基氨基甲烷/盐酸缓冲液(tris
‑
hcl,ph=7)。
[0035]
探针对hg
2
的下转换荧光增强响应:在17个盛有下转换探针检测液(10 μm)的比色皿中,分别加入16种金属阳离子水溶液(浓度为100 mm),它们分别是:hg
2
、cu
2
、mn
2
、nh
4
、
zn
2
、mg
2
、cd
2
、pb
2
、li
、na
、k
、ca
2
、ni
2
、co
2
、fe
2
和fe
3
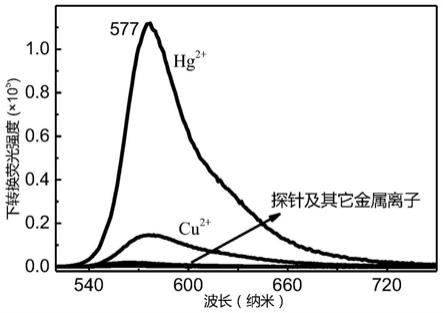
。然后测定下转换荧光光谱(激发波长500nm),见附图6、附图7所示。可见,hg
2
的加入使探针的荧光强度增强了160倍,其余金属阳离子几乎不变化。显示出探针对hg
2
具有高度的选择性荧光响应。
[0036]
探针对hg
2
的上转换荧光响应:在17个盛有上转换探针检测液(100μm)的比色皿中,分别加入16种金属阳离子水溶液(100mm),它们是:hg
2
、cu
2
、mn
2
、nh
4
、zn
2
、mg
2
、cd
2
、pb
2
、li
、na
、k
、ca
2
、ni
2
、co
2
、fe
2
和fe
3
。然后测定上转换荧光光谱(激发波长:655nm),见附图8、附图9所示。可见,除了hg
2
外,加入其他15种金属阳离子后,探针溶液在短波长处并不出现上转换荧光峰形;而hg
2
的加入使得探针溶液的上转换荧光强度增强到原来的5倍,而加入其余15种金属阳离子,探针溶液并不出现上转换荧光峰形。值得注意的是:在下转换荧光检测中起干扰作用的cu
2
,在上转换荧光检测中不再发生干扰。这说明,探针只对hg
2
具有高度的选择性上转换荧光增强响应。
[0037]
探针对hg
2
浓度的下转换荧光响应:在下转换探针检测液(10μm)中加入不同浓度的hg
2
,观察探针的下转换荧光光谱的变化(激发波长500nm),见附图10所示。可见,未加入汞离子之前,探针的荧光很弱;分别加入3ml~30mlhg
2
水溶液(1mm)于上述探针溶液中(hg
2
浓度折合为1~10μm),时,探针荧光强度不断地增强(见附图11)。由附图可见,在hg
2
浓度0~10μm范围内,其荧光强度与hg
2
浓度呈现出很好的线性关系,相关系数r2=0.99001。根据公式“检测限=3δ/k”可计算出利用荧光光谱检测hg
2
的检测限为8.617
×
10
‑9m。
[0038]
探针对hg
2
浓度的上转换荧光响应:在上转换探针检测液(1mm)溶液中加入不同浓度的hg
2
,观察探针上转换荧光光谱的变化(激发波长655nm),见附图12所示。可见,未加入汞离子之前,探针的上转换荧光很弱,分别加入3μl~30μlhg
2
水溶液(50mm)于上述探针溶液中(hg
2
浓度折合为50~500μm,探针荧光强度不断地增强(见附图13)。由附图可见,在hg
2
浓度0~500μm范围内,其上转换荧光强度与hg
2
浓度呈现出很好的线性关系,相关系数r2=0.99540。根据公式“检测限=3δ/k”可计算出利用上转换荧光光谱检测hg
2
的检测限为1.10
×
10
‑5m。
[0039]
探针对hg
2
的下转换荧光响应时间:由附图14可见,下转换探针检测液(10μm)的荧光很弱,当加入30mlhg
2
水溶液(10mm)于上述探针溶液中(hg
2
浓度折合为100μm)时,探针的荧光强度急剧增强,荧光峰位位于560nm,其变化几乎是瞬时(10秒以内)的,附图15可以更为直观的看出其随时间的变化。
[0040]
探针对hg
2
的上转换荧光响应时间:与下转换荧光情况类似,探针对于hg
2
的响应也几乎是瞬时(10秒以内)完成的(见附图16和附图17)。
[0041]
实施例四探针试纸检测hg
2
制备了hg
2
检测试纸。具体操作为:将2cm
×
1cm的试纸置于探针的溶液(探针的浓度为1
×
10
‑4m,溶剂:乙醇)中浸泡30min,取出自然晾干备用。然后,用玻璃棒蘸取不同浓度的hg
2
水溶液滴在试纸上,如附图18所示。随着hg
2
浓度的增加,试纸由无色(白色)变成玫瑰红色,且颜色依次加深,最低响应浓度为0.01mm,且效果较四溴代荧光素螺环内硫酯所制试纸更好。因此,该试纸可以对溶液中高浓度的hg
2
实现快速裸眼检测。
[0042]
迄今为止,报道的有机上转换发光(upconversion,uc)主要有双光子吸收机制(tpa
‑
uc)和三线态
‑
三线态湮灭(tta
‑
uc)机制来实现的,具有单光子吸收机制的上转换(opa
‑
uc)则是另一种独特的发光机制,鲜见报道。本发明使用的是单光子上转换(opa
‑
uc)
荧光探测技术。单光子吸收上转换(opa
‑
uc)机理是电子从基态的热活化振动
‑
转动能级(s
t
)跃迁到第一激发态(s1), 然后回落至基态并发出荧光。与上述的两种上转换(即tpa
‑
uc和tta
‑
uc)相比,opa
‑
uc的优势在于,除了具有穿透深度大和对活体伤害小等优势外;opa上转换所需的激发光源强度较小,所需上转换检测设备价格低廉便携;所需探针的浓度较小,无需隔绝氧气,空气中即可检测,因而实用性更强。
[0043]
对比例称取2.5 mmol的荧光素、3.5mmol水合肼加入100 ml三口烧瓶中,加入30 ml乙醇加热回流24小时后,旋蒸除去溶剂,加入去离子水进行重沉淀得到粗产物,分别通过水/乙醇加热挥发结晶法得到最终产物化合物luc
‑
1:ms,计算值:347.102633,测量值:347.102992;1h nmr (400 mhz, dmso
‑
d6) δ 10.05
ꢀ–ꢀ
9.49 (m, 2h), 7.86
ꢀ–ꢀ
7.73 (m, 1h), 7.49 (dd, j = 6.3, 2.9 hz, 2h), 7.07
ꢀ–ꢀ
6.93 (m, 1h), 6.60 (d, j = 2.3 hz, 2h), 6.53
ꢀ–ꢀ
6.32 (m, 4h), 4.40 (s, 2h);称取2.5 mmol四碘荧光素、3.5mmol水合肼加入100 ml三口烧瓶中,加入30 ml乙醇加热回流24小时后,旋蒸除去溶剂,加入去离子水进行重沉淀得到粗产物,分别通过水/乙醇加热挥发结晶法得到最终产物化合物luc
‑
5:ms,计算值:849.68193,测量值:850.69090;1h nmr (400 mhz, dmso
‑
d6) δ 10.34 (d, j = 393.8 hz, 2h), 7.82 (d, j = 8.6 hz, 1h), 7.54 (d, j = 8.6 hz, 1h), 7.03 (d, j = 13.1 hz, 1h), 6.78 (dd, j = 20.3, 13.2 hz, 2h), 6.63
ꢀ–ꢀ
6.34 (m, 1h), 4.63 (s, 2h);
13
c nmr (101 mhz, dmso
‑
d6) δ 165.92, 158.77, 152.79, 136.70, 129.73, 129.46, 129.16, 128.38, 123.05 (d, j = 14.8 hz), 79.41, 79.05, 78.16。
[0044]
上述对比例合成路线以及产物结构如下:探针(luc
‑
1)对金属离子的下转换荧光增强响应:在17个盛有探针溶液(10 μm,dmf/缓冲液,ph=7.0, v/v,1/2)的比色皿中,分别加入16种金属阳离子水溶液(浓度为100 mm),它们分别是:hg
2
、cu
2
、mn
2
、nh
4
、zn
2
、mg
2
、cd
2
、pb
2
、li
、na
、k
、ca
2
、ni
2
、co
2
、fe
2
和fe
3
。然后测定下转换荧光光谱(激发波长500 nm),见附图19,加入一定量的不同阳离子后,化合物luc
‑
1仅对mg
2
有微弱的响应且干扰离子较多。
[0045]
探针(luc
‑
5)对金属离子的下转换荧光增强响应:在17个盛有探针溶液(10 μm,dmf/缓冲液,ph=7.0, v/v,1/2)的比色皿中,分别加入16种金属阳离子水溶液(浓度为100 mm),它们分别是:hg
2
、cu
2
、mn
2
、nh
4
、zn
2
、mg
2
、cd
2
、pb
2
、li
、na
、k
、ca
2
、ni
2
、co
2
、fe
2
和fe
3
。然后测定下转换荧光光谱(激发波长500 nm),见附图20,加入一定量的不同阳离子后,化合物luc
‑
5对汞离子无响应。
[0046]
而在opa
‑
uc(激发波长655 nm)荧光中,对比例化合物对金属离子都未有选择性opa
‑
uc荧光增强现象。
[0047]
实施例五四碘代荧光素螺环内硫酯(luc
‑
7)在tta
‑
uc的离子探测性能 以四碘代荧光素螺环内硫酯作为敏化剂与发光剂dpa(9,10
‑
二苯基蒽)在溶液中组成双组份,产生tta
‑
uc,tta
‑
uc探测性能研究中均采用纯溶剂dmso。
[0048]
在17个盛有双组份溶液(luc
‑
7/dpa:10 μm/1 mm,dmso)的比色皿中,分别加入16种金属阳离子水溶液(浓度为10 mm),它们分别是:hg
2
、cu
2
、mn
2
、nh
4
、zn
2
、mg
2
、cd
2
、pb
2
、li
、na
、k
、ca
2
、ni
2
、co
2
、fe
2
和fe
3
,除氧后,测试其tta
‑
uc荧光光谱(激发波长655 nm)。见图21,发现在加入hg
2
后,溶液的上转换荧光明显增强,而加入其它金属离子则无明显的tta
‑
uc荧光增强,说明在tta
‑
uc光谱检测中,化合物luc
‑
7也能选择性的识别hg
2
。
[0049]
作为对比,将luc
‑
7更换为四溴代荧光素螺环内硫酯、luc
‑
1或者luc
‑
5,采用同样的双组份以及测试方法,对所有离子都没有tta
‑
uc响应。
[0050]
tta
‑
uc的灵敏度测试采用滴定法。向10 μm/1 mm的luc
‑
7/dpa的dmso溶液依次滴加1 μl的0.3 mm的汞离子水溶液,除氧后,依次测试其tta
‑
uc的荧光强度变化(见图22a)。发现依次滴加定量的汞离子后其荧光强度依次增强,由于tta
‑
uc发光过程对水及其敏感,在汞离子的浓度0~0.8 μm时,荧光强度的增加具有良好的相关性,r2为0.993332,斜率k为11.13683(见图22b),通过公式“检测限=3δ/k”可算得luc
‑
7在tta
‑
uc荧光检测通道中对hg
2
的检测限为1.48
×
10
‑
9 m,其中δ=4.53
×
10
‑1。可以看出,luc
‑
7对汞离子的tta
‑
uc的检测限极高,极为灵敏。
[0051]
实施例六生物成像 为了将化合物应用到生物细胞成像,首先通过4,5
‑
(二甲基
‑2‑
噻唑基)
‑
2,5
‑
二苯基
‑2‑
氢
‑
四唑溴化铵(mtt)测定化合物四碘代荧光素螺环内硫酯的细胞毒性,所选取的细胞为小鼠的乳腺癌细胞4t1。由图23可见,随着化合物luc
‑
7浓度的增加,细胞的成活率基本保持在较高水平(100%左右),这表明化合物的细胞毒性很小,有利于后续将其应用至细胞的生物成像中。
[0052]
细胞成像的具体步骤为:在12孔板中放置玻片,接种4t1细胞并孵育24小时;随后将细胞培养基更换为含有10 μm染料(四碘代荧光素螺环内硫酯)的培养基,共培育30分钟,用pbs洗涤两遍;再分别更换为含有0
‑
100 μm染料(hg
2
)的培养基,培育30分钟,用pbs洗涤两遍;用0.1%多聚甲醛固定细胞30分钟,用pbs洗净后使用dapi染色10分钟,再用pbs洗涤两遍;最后使用抗荧光淬灭封片剂将细胞玻片固定到载玻片上进行共聚焦荧光成像。由细胞成像照片(图24)可以看出,未加hg
2
前,化合物无明显的荧光,而在加入6.3 μm的hg
2
后,细胞中观察到明显的荧光信号,并且随着hg
2
浓度的增加,荧光逐渐增强,趋势很明显。说明四碘代荧光素螺环内硫酯在细胞成像方面表现也极为优异。
[0053]
四碘代荧光素螺环内硫酯的细胞荧光共聚成像实验结果表明:四碘代荧光素螺环内硫酯具有低毒性,且随着汞离子浓度的增加,荧光增强趋势极为明显,实现了细胞体内高灵敏的检测。兼具环境与生物体两方面应用,实用价值很高。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。