1.本发明属于药物化学技术领域,具体涉及一种治疗抗病毒药物关键中间体的制备方法。
技术背景
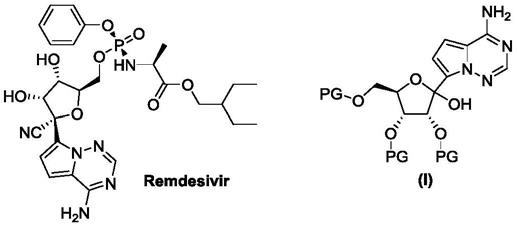
2.瑞德西韦(remdesivir)由美国吉利德(gilead)公司发现的一种核苷类抗病毒药物,其可以潜在作为广谱抗冠状病毒药物。瑞德西韦(remdesivir)和制备抗病毒药物(例如瑞德西韦)关键中间体,结构式如下:
[0003][0004]
根据gilead专利文献wo2012012776a1报道,关键中间体式(i)的合成是整个remdesivir合成路线的关键技术难点。合成路线为如下式所示:
[0005][0006]
式(ii)通过nbs进行溴代,得到式(iv),随后与式(iii)在丁基锂作为偶联剂的作用下进行低温偶联,得到中间体式(i)。
[0007]
由于该路线需要-78℃低温反应,并且丁基锂的选择性不好,产生大量副产物,反应收率很低,收率仅仅20-25%,纯化难度大,需要进行柱层析分离,所以gilead开发了改进路线在专利文献wo2016069827a1中有报道,如下式所示:
[0008][0009]
式(ii)通过nis进行碘代,得到式(v),随后与式(iii)在格式试剂作为偶联剂的作用下进行低温偶联,得到中间体式(i)。
[0010]
改进路线虽然对设备要求和能耗降低,但同样,无法解决副产物多的问题,收率仅仅 35-40%,并且此路线增加了碘的引入,增加了成本,这对于工业化生产是非常不利的。
技术实现要素:
[0011]
本发明所要解决的技术问题是克服了现有的式(i)制备方法中存在的反应步骤长、反应收率低、制备成本高、后处理过程复杂,不适合工业上大规模制备的缺陷,而提供了一种由式(ii)一步直接合成式(i)的制备方法。该方法步骤少,收率高、操作简便、成本低,适合于工业上大规模生产。
[0012][0013]
本发明提供一种核糖核苷式(i)的制备方法,该制备方法包括:在适于制备式(i)的条件下形成含有去质子化试剂、偶联剂、甲硅烷基化试剂、式(ii)化合物和式(iii)化合物的反应混合物:
[0014][0015]
其中pg独立地为羟基保护剂。当pg基团为羟基保护基时,pg可以是任何在protectivegroups in organic chemistry,peter g.m.wuts and theodora w.greene,4th ed.,2006中描述的保护基的实例。可为任何适用于羟基官能团的保护基。在一些实施方案中,代表性的羟基保护基包括但不限于硅烷、醚、酯等。在一些实施方案中,羟基保护基可为三甲基硅烷(tms)、叔丁基二甲基硅烷(tbdms)、叔丁基二苯基硅烷(tbdps)、甲基-甲氧基(mom)、四氢吡喃(thp)、叔丁基、烯丙基、苄基、乙酰基、戊酰基或苯甲酰基。在一些实施方案中,pg 基团可以为苄基(bn)。在一些实施方案中,pg基团可以为叔丁基二甲基甲硅烷基(tbs)。
[0016]
任何合适的去质子化试剂可用于制备式(i)化合物的方法中。去质子化试剂可以是钠去质子化试剂、镁基去质子化试剂、锂基去质子化试剂、钾基去质子化试剂等。例如,去质子化试剂可以是钠氢(nah)、异丙基氯化镁(iprmgcl)、异丙基氯化镁氯化锂(iprmgcl.licl)、甲基氯化镁(memgcl)、乙基氯化镁(etmgcl)、丙基氯化镁(prmgcl)、叔丁基氯化镁 (tbumgcl)、苯基氯化镁(phmgcl)、环己烷氯化镁(cyhexmgcl)、苯基溴化镁(phmgbr)、甲基溴化镁(memgbr)、乙基溴化镁(etmgbr)、丙基溴化镁(prmgbr)、环己烷溴化镁 (cyhexmgbr)、丁基锂(buli)、甲基锂(meli)、叔丁基锂(t-buli)、异丙基锂(i-prli)、苯基锂(phli)、氢化锂(lih)、乙基锂(etli)、丙基锂(prli)、环己烷锂(cyhexli)、氢化钾(kh)或其组合。在一些实施方案中,,一些去质子化试剂可以是nah、iprmgcl、memgcl 或buli或其组合。
[0017]
去质子化试剂可以任何合适的量存在。例如,去质子化试剂也可以以相比于式(ii)化合物0.1~10.0当量(mol/mol)的量存在。在一些实施例中,去质子化试剂的存在量
为相比于式(ii)化合物约1.0~3.0当量(mol/mol)。
[0018]
在制备式(i)化合物的方法中可以使用任何合适的甲硅烷基化剂。例如,甲硅烷化剂可以是氟硅烷、氯硅烷、溴硅烷、碘硅烷。在一些实施方案中,甲硅烷化剂可以是三取代的甲硅烷基氯、三取代的甲硅烷基溴、三取代的甲硅烷基碘、三取代的甲硅烷基氟。甲硅烷基部分可以具有任何合适的取代基,例如烷基、烯基、炔基、环烷基或苯基。在一些实施方案中,甲硅烷基化剂包括但不限于三甲基氯硅烷[cl-si(ch3)3,tmscl]、1,2-双(氯二甲基硅基)乙烷[cl
-ꢀ
(ch3)2sich2ch2si(ch3)
2-cl]或叔丁基二苯基甲硅烷基(tbdps)。在一些实施例中甲硅烷基化剂可以是tmscl或cl-(ch3)2sich2ch2si(ch3)
2-cl。
[0019]
甲硅烷化剂可以任何合适的量存在。例如,甲硅烷化剂也可以以相比于式(ii)化合物 0.0~10.0当量(mol/mol)的量存在。在一些实施例中,甲硅烷化剂的存在量为相比于式(ii) 化合物约1.0~2.0当量(mol/mol)。
[0020]
任何合适的偶联剂可用于制备式(i)化合物的方法中。偶联剂可以是锂偶联剂、镁偶联剂等。例如,偶联剂可以是二异丙基氨基锂(lda)、双(二异丙胺基)镁[(ipr)
2-n-mg-n-(ipr)2]、二异丙胺基溴化镁(bmda)或其组合。在一些实施方案中,偶联试剂可以是lda。在一些实施方案中,偶联试剂可以是双(二异丙胺基)镁。在一些实施方案中,偶联试剂可以是bmda。
[0021]
偶联剂可以任何合适的量存在。例如偶联剂可以以相比于式(ii)化合物0.1~10.0当量 (mol/mol)的量存在。在一些实施例中,偶联剂的存在量为相比于式(ii)化合物约1.0~2.0 当量(mol/mol)。
[0022]
任何合适的溶剂可以用于本发明的方法中。代表性的溶剂包括但不限于戊烷,不同的戊烷,己烷,不同的己烷,庚烷,不同的庚烷,石油醚,环戊烷,环己烷,苯,甲苯,乙基苯,二甲苯,二氯甲烷(dcm),三氟甲苯,卤代苯(如氯苯,氟苯,二氯苯和二氟苯),亚甲基氯,氯仿,丙酮,乙酸乙酯,二乙基醚,四氢呋喃(thf),2-甲基四氢呋喃(methf),二丁基醚,二异丙醚,甲基叔丁基醚(mtbe),二甲氧基乙烷,二噁烷(1,4-二噁烷),n-甲基吡咯烷酮(nmp),二异丙醚或其组合。在一些实施例方案中,溶剂可以是thf或me-thf。在一些实施例中溶剂可以是thf和正己烷、thf和正庚烷或thf和乙基苯或其组合。
[0023]
该方法的反应混合物可具有任意合适的温度。例如,反应混合物的温度可以为约-100℃至约100℃。在一些实施方案中,反应混合物的温度可为约-90℃至约70℃。在一些实施方案中,反应混合物的温度约-90℃至约-20℃。
[0024]
该方法的反应混合物可具有任意合适的压力。例如,反应混合物可以在大气压下。反应混合物也可以暴露于任何合适的环境,例如大气气体,或惰性气体如氮气或氩气。
[0025]
该方法在一些实施例方案中,制备式(i)的条件下形成含有去质子化试剂、偶联剂、甲硅烷基化试剂、式(ii)化合物和式(iii)化合物的反应混合物:
[0026][0027]
在一些实施例方案,pg基团可以为苄基(bn)或叔丁基二甲基甲硅烷基(tbs)。偶联剂可以是锂偶联剂、镁偶联剂,偶联剂可以是二异丙基氨基锂(lda)、双(二异丙胺基)镁 [(ipr)
2-n-mg-n-(ipr)2]、二异丙胺基溴化镁(bmda)或其组合。去质子化试剂可以是nah、 iprmgcl、memgcl或buli或其组合。甲硅烷基化剂可以是tmscl或cl-(ch3)2si ch2ch2si(ch3)
2-cl。
[0028]
本发明有益的技术效果:
[0029]
本发明提供的技术方案首先由原工艺的两步反应直接变为一步反应,省略了卤代物的合成,不仅收率提高,收率提高了25-40%,而且极大地节省了成本;其次,省去了卤素的使用,减轻了环保压力;最后,本发明提供的技术方案中反应主要副产物为式(ii),并且可以回收。
[0030]
因此,本发明所提供的技术方案克服了现有的式(i)制备方法中存在的反应步骤长、反应收率低、制备成本高、后处理过程复杂,不适合工业上大规模制备的缺陷。本发明所提供的技术方案,该方法步骤少,收率高、操作简便、成本低,产品质量好,适合于工业上大规模生产,会制得最终的药物成品,抗病毒药物(例如瑞德西韦)提供了有力的治疗保障。
具体实施方式
[0031]
下面通过实施例的方式进一步说明本发明,但并不因此将本发明限制在所述的实施例范围之中。基于本发明中的实施例,本领域技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0032]
实施例中所用的原料或试剂除特别说明之外,均市售可得。
[0033]
实施例1
[0034][0035]
氮气保护下,三口瓶中加入4-氨基吡咯并[2,1-f][1,2,4]三嗪(5g),tmscl(8.1g)和thf (150ml),混合物在25℃下搅拌1小时,然后降温至-20℃,缓慢滴加iprmgcl(57ml,1.3m 于thf溶液),滴加时保持内温≤-15℃,滴加完毕后搅拌1小时,降温至-75℃。缓慢加入lda (18.7ml,2.0m于四氢呋喃/正己烷溶液中),滴加时保持内温≤-70℃,滴加完毕后搅拌1小时,降温至-70℃。缓慢滴加糖内脂(式iii)(20.3g)的thf(25ml)溶液,滴加时保持内温≤-65℃,滴加完毕后搅拌1小时。反应完全后,用acoh淬灭,水洗,浓缩,最后通过硅胶柱
纯化,得到最终产物(式i),收率60.8%。
[0036]
实施例2
[0037][0038]
氮气保护下,三口瓶中加入4-氨基吡咯并[2,1-f][1,2,4]三嗪(10g),tmscl(12.5g)和 me-thf(300ml),混合物升温至回流搅拌1小时,然后降温至-80℃,缓慢滴加n-buli(60ml, 2.5m于正己烷溶液),滴加时保持内温≤-75℃,滴加完毕后搅拌10分钟,降温至-80℃。缓慢加入bmda(40ml,2m于正己烷溶液),滴加时保持内温≤-75℃,滴加完毕后搅拌1小时,缓慢滴加糖内脂(式iii)(31g)的thf(50ml)溶液,滴加时保持内温≤-65℃,滴加完毕后保温搅拌1小时。反应完全后,用acoh淬灭,水洗,浓缩,最后通过硅胶柱纯化,得到最终产物(式i),收率60.5%。
[0039]
实施例3
[0040][0041]
氮气保护下,三口瓶中加入4-氨基吡咯并[2,1-f][1,2,4]三嗪(50g),tmscl(81g)和thf (1200ml),混合物升温至回流搅拌1小时,然后降温至-75℃,缓慢滴加n-buli(300ml, 2.5m于正己烷溶液),滴加时保持内温≤-70℃,滴加完毕后搅拌10分钟,降温至-75℃。缓慢加入lda(190ml,2.0m于四氢呋喃/正己烷溶液中),滴加时保持内温≤-70℃,滴加完毕后搅拌1小时,降温至-70℃。缓慢滴加糖内脂(式iii)(170g)的thf(250ml)溶液,滴加时保持内温≤-65℃,滴加完毕后搅拌1小时。反应完全后,用acoh淬灭,水洗,浓缩,最后通过适当溶剂重结晶,得到最终产物(式i),收率63.7%。
[0042]
实施例4
[0043][0044]
氮气保护下,三口瓶中加入4-氨基吡咯并[2,1-f][1,2,4]三嗪(5g),tmscl(8.1g)和thf (500ml),混合物升温至回流搅拌1小时,然后降温至-90℃,缓慢滴加n-buli(15ml,2.5m 于正己烷溶液),滴加时保持内温≤-80℃,滴加完毕后搅拌10分钟,降温至-85℃。缓慢加入 lda(18.7ml,2.0m于四氢呋喃/正己烷溶液中),滴加时保持内温≤-80℃,滴加完毕后搅拌 1小时,降温至-85℃。缓慢滴加糖内脂(式iii)(20.3g)的thf(25ml)溶液,滴加时保持内温≤-80℃,滴加完毕后搅拌1小时。反应完全后,用acoh淬灭,水洗,浓缩,最后通过硅胶柱纯化,得到最终产物(式i),收率51.4%。
[0045]
实施例5
[0046][0047]
氮气保护下,三口瓶中加入4-氨基吡咯并[2,1-f][1,2,4]三嗪(20g),1,2-双(氯二甲基硅基) 乙烷(40g)和thf(2l),然后降温至-80℃,缓慢滴加n-buli(120ml,2.5m于正己烷溶液),滴加时保持内温≤-75℃,滴加完毕后搅拌10分钟,降温至-80℃。缓慢加入lda(75ml, 2.0m于四氢呋喃/正己烷溶液中),滴加时保持内温≤-70℃,滴加完毕后搅拌1小时,降温至
ꢀ-
70℃。缓慢滴加糖内脂(式iii)(65g)的thf(100ml)溶液,滴加时保持内温≤-65℃,滴加完毕后保温搅拌1小时。反应完全后,用acoh淬灭,水洗,浓缩,最后通过合适溶剂重结晶,得到最终产物(式i),收率58.2%。
[0048]
实施例6
[0049][0050]
氮气保护下,三口瓶中加入4-氨基吡咯并[2,1-f][1,2,4]三嗪(5g),tmscl(8.1g)和thf (500ml),混合物升温至回流搅拌1小时,然后降温至-10℃,缓慢滴加memgcl(15ml, 3m于thf溶液),滴加时保持内温≤-5℃,滴加完毕后搅拌10分钟,降温至-85℃。缓慢加入双(二异丙胺基)镁(110ml,0.7m于thf),滴加时保持内温≤-80℃,滴加完毕后搅拌1小时,降温至-85℃。缓慢滴加糖内脂(式iii)(17g)的thf(25ml)溶液,滴加时保持内温≤-80℃,滴加完毕后搅拌1小时。反应完全后,用acoh淬灭,水洗,浓缩,最后通过硅胶柱纯化,得到最终产物(式i),收率58%。
[0051]
实施例7
[0052][0053]
氮气保护下,三口瓶中加入4-氨基吡咯并[2,1-f][1,2,4]三嗪(5g),1,2-双(氯二甲基硅基) 乙烷(10g)和thf(250ml),混合物在25℃搅拌1小时,然后降温至0℃,加入60%nah (3.7g),加入完毕后搅拌10分钟,降温至-65℃。缓慢加入lda(18.7ml,2.0m于四氢呋喃/正己烷溶液中),滴加时保持内温≤-60℃,滴加完毕后搅拌1小时,升温至-30℃。缓慢滴加糖内脂(式iii)(20.3g)的thf(25ml)溶液,滴加时保持内温≤-25℃,滴加完毕后,升温至-20℃,保温搅拌1小时。反应完全后,用acoh淬灭,水洗,浓缩,最后通过合适溶剂重结晶
纯化,得到最终产物(式i),收率59%。
[0054]
实施例8
[0055][0056]
氮气保护下,三口瓶中加入4-氨基吡咯并[2,1-f][1,2,4]三嗪(5g),tmscl(10g)和thf (150ml),混合物升温至回流搅拌1小时,然后降温至-90℃,缓慢滴加n-buli(45ml,2.5m 于正己烷溶液),滴加时保持内温≤-80℃,滴加完毕后搅拌10分钟,降温至-85℃。缓慢加入 lda(18.7ml,2.0m于四氢呋喃/正己烷溶液中),滴加时保持内温≤-80℃,滴加完毕后搅拌 1小时,降温至-85℃。缓慢滴加糖内脂(式iii)(18.3g)的thf(25ml)溶液,滴加时保持内温≤-80℃,滴加完毕后搅拌1小时。反应完全后用acoh淬灭,水洗,浓缩,最后通过硅胶柱纯化,得到最终产物(式i),收率58%。
[0057]
实施例9
[0058][0059]
氮气保护下,三口瓶中加入4-氨基吡咯并[2,1-f][1,2,4]三嗪(5g),tmscl(8.1g)和thf (500ml),混合物升温至回流搅拌1小时,然后降温至-70℃,缓慢滴加n-buli(15ml,2.5m 于正己烷溶液),滴加时保持内温≤-65℃,滴加完毕后搅拌10分钟,升温至-40℃。在-40℃下,依次将上述制备溶液和lda(18.7ml,2.0m于四氢呋喃/正己烷溶液中)泵入管式反应器,两者反应后,将糖内脂(式iii)(20.3g)的thf(25ml)溶液泵入管式反应器中。将反应混合物收集在冰水中淬灭,加入乙酸乙酯萃取,有机层洗涤,浓缩,最后通过合适溶剂重结晶纯化,得到最终产物(式i),收率65%。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。