tnfaip3非编码序列突变检测试剂在制备预测t细胞淋巴瘤预后试剂盒中的应用
技术领域
1.本发明属于生物医学领域,特别涉及tnfaip3非编码序列突变检测试剂在制备预测t细胞淋巴瘤预后试剂盒中的应用。
背景技术:
2.t细胞淋巴瘤(t
‑
cell lymphoma,tcl)起源于淋巴母细胞或成熟t细胞。这种疾病仅占非霍奇金淋巴瘤的10
‑
15%,可进一步细分为许多相对罕见的亚型。与b细胞淋巴瘤患者相比,tcl患者的预后往往较差。目前,基于国际预后指数(international prognosis index,ipi)的危险分层在预测tcl患者的预后方面取得了重大进展,这种精准化的危险分层可以为临床决策提供重要的参考,从而改善患者的预后。然而,基于ipi的危险分层仍不能对所有tcl患者的预后进行精准预测。因此,需要进一步探索改善tcl危险分层的新型生物标志物。
3.细胞内泛素编辑蛋白肿瘤坏死因子α诱导蛋白3(tumor necrosis factor alpha inducing protein 3,tnfaip3),也称为a20,通过肿瘤坏死因子和toll样受体在多种途径中负调控nf
‑
κb的活性。tnfaip3基因位点位于染色体6q23,其缺失常发生于b细胞淋巴瘤,尤其是结外边缘区b细胞淋巴瘤和弥漫性大b细胞淋巴瘤。此外,之前的一些研究表明,tnfaip3缺失常见于皮肤t细胞淋巴瘤和nk
‑
t细胞淋巴瘤。但是,多个研究中心探讨了nk
‑
t细胞淋巴瘤患者中tnfaip3缺失的预后价值,发现其结果相互矛盾。在我们之前的研究中,在t细胞肿瘤中发现了tnfaip3的非编码序列(non
‑
coding sequence,non
‑
cds)区域发生了突变。然而,tnfaip3的non
‑
cds突变对tcl患者的预后方面的评估仍然缺乏。
技术实现要素:
4.本发明的首要目的在于克服现有技术的缺点与不足,提供tnfaip3非编码序列突变检测试剂在制备预测t细胞淋巴瘤预后试剂盒中的应用。当检测到tnfaip3非编码序列突变时,表明tcl患者的预后良好可能性大,可以作为预测tcl患者预后评估的指标。
5.本发明的另一目的在于提供一种预测t细胞淋巴瘤预后的试剂盒。
6.本发明的目的通过下述技术方案实现:
7.tnfaip3非编码序列突变检测试剂在制备预测t细胞淋巴瘤预后试剂盒中的应用,是基于本发明的发明人首次发现tcl患者外周血单个核细胞中tnfaip3非编码序列突变情况与t细胞淋巴瘤患者的预后相关。
8.在所述的应用中,通过检测临床患者的外周血单个核细胞中tnfaip3非编码序列突变情况,从而预测t细胞淋巴瘤预后。
9.进一步地,所述的突变的区域为如下区域的至少一个区域或多个区域的组合:
10.1)tnfaip3基因5
′‑
utr的部分或全部区域;
11.2)tnfaip3基因3
′‑
utr的部分或全部区域;
12.3)tnfaip3基因内含子的部分或全部区域。
13.更进一步地,所述的突变的区域为tnfaip3基因如下六个位点的至少一个位点或多个位点的组合:g.3918、g.3637、g.3869、g.13751、g.14244、g.11822。
14.更进一步地,所述的突变为如下突变情况的至少一种情况或多种情况的组合:g.3918c>t突变、g.3637t>a突变、g.3869c>g、g.13751a>c突变、g.14244c>t突变、g.11822t>c突变。
15.所述的预测具体指:
16.①
当tnfaip3非编码序列有突变时,tcl患者临床预后良好的可能性较大;
17.②
当tnfaip3非编码序列无突变时,tcl患者临床预后差的可能性较大。
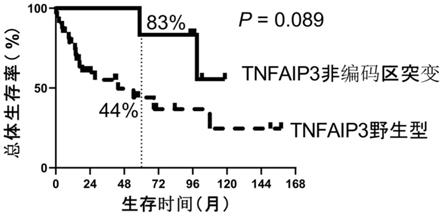
18.所述的预后良好是指当tnfaip3非编码序列有突变时,tcl患者的总体生存率大于83%;
19.所述的预后差是指当tnfaip3非编码序列无突变时,tcl患者的总体生存率小于44%。
20.一种预测t细胞淋巴瘤预后的试剂盒,包括用于扩增包含tnfaip3基因非编码序列的序列的引物中的一组或多组引物的组合。
21.进一步地,所述的试剂盒包括如下用于扩增tnfaip3基因5
′‑
utr启动子序列片段的引物、用于扩增tnfaip3基因3
′‑
utr序列片段的引物和用于扩增tnfaip3基因外显子和内含子序列片段的引物中的一组或多组引物的组合:
22.(1)用于扩增tnfaip3基因5
′‑
utr启动子序列片段的引物:
23.promoter(g.2933
‑
3687)(f):5'
‑
tttacaaaggagcaccagcaggaga
‑
3';
24.promoter(g.2933
‑
3687)(r):5'
‑
attacatttaagaatacttgtcagg
‑
3';
25.promoter(g.3568
‑
4249)(f):5'
‑
aagtgccaccctccatcc
‑
3';
26.promoter(g.3568
‑
4249)(r):5'
‑
agcggtgacagcctttgg
‑
3';
27.promoter(g.4110
‑
4744)(f):5'
‑
ggtgagtgttgttctgattc
‑
3';
28.promoter(g.4110
‑
4744)(r):5'
‑
tcacgtgactctctgggtcg
‑
3';
29.(2)用于扩增tnfaip3基因3
′‑
utr序列片段的引物:
[0030]3’‑
utr(g.18828
‑
19347)(f):5'
‑
caacggctactgcaacgaat
‑
3';
[0031]3’‑
utr(g.18828
‑
19347)(r):5'
‑
ctcgctgccatgaggatct
‑
3';
[0032]3’‑
utr(g.19272
‑
19787)(f):5'
‑
gagaagccagagccattccacct
‑
3';
[0033]3’‑
utr(g.19272
‑
19787)(r):5'
‑
gctcatgccccaacaacaacca
‑
3';
[0034]3’‑
utr(g.19717
‑
20407)(f):5'
‑
gctgccctagaagtacaata
‑
3';
[0035]3’‑
utr(g.19717
‑
20407)(r):5'
‑
gacagcaaccacaaagcacac
‑
3';
[0036]3’‑
utr(g.20455
‑
20938)(f):5'
‑
cccagagataaaggctgccat
‑
3';
[0037]3’‑
utr(g.20455
‑
20938)(r):5'
‑
ggaagcacagtcttaatatc
‑
3';
[0038]
(3)用于扩增tnfaip3基因外显子和内含子序列片段的引物:
[0039]
exon2(f):5'
‑
ggagtcgtattaaagtcaggctaa
‑
3';
[0040]
exon2(r):5'
‑
ggcaaaagaaacacaacagaac
‑
3';
[0041]
exon3(f):5'
‑
ttgctgggtcttacatgcag
‑
3';
[0042]
exon3(r):5'
‑
cccaccatggagctctgtta
‑
3';
[0043]
exon4(f):5'
‑
gggagtacaggatacattcaagc
‑
3';
[0044]
exon4(r):5'
‑
gctgaaagcatttaagtacagatcc
‑
3';
[0045]
exon5(f):5'
‑
acctaagggcctcattttcc
‑
3';
[0046]
exon5(r):5'
‑
agcaaaaaggaaaaccctga
‑
3';
[0047]
exon6(f):5'
‑
tgagatctacttacctatggccttg
‑
3';
[0048]
exon6(r):5'
‑
cagatgacacaggagagagctg
‑
3';
[0049]
part1 of exon 7(f):5'
‑
ggttctacaattcttgccataatcc
‑
3';
[0050]
part1 of exon 7(r):5'
‑
caagtgccttgtgtggtctg
‑
3';
[0051]
part2 of exon 7(f):5'
‑
cacaacggattttgtgaacg
‑
3';
[0052]
part2 of exon 7(r):5'
‑
aggaacaaaaccccttctgg
‑
3';
[0053]
exon8(f):5'
‑
ctctgtatcggtggggtgac
‑
3';
[0054]
exon8(r):5'
‑
caaaaagcatcgaacacacg
‑
3';
[0055]
exon9(f):5'
‑
tgatctgcctgttctttcca
‑
3';
[0056]
exon9(r):5'
‑
gggttcagaggatagcacca
‑
3'。
[0057]
所述的试剂盒还包括用于dna提取的试剂、用于聚合酶链式反应(polymerase chain reaction,pcr)的试剂、核苷酸序列测序的试剂、核苷酸序列分析的试剂中的任意一种或至少两种。
[0058]
所述的用于dna提取的试剂优选为tiangen的血液基因组dna提取试剂盒。
[0059]
上述预测tcl预后的试剂盒在非诊断检测tnfaip3非编码序列突变中应用。
[0060]
所述的应用包括如下步骤:
[0061]
(1)在待测外周血样本中加入细胞裂解液,混匀,离心,向所得沉淀中加入缓冲液,混匀;
[0062]
(2)加入蛋白酶溶液,混匀;加入缓冲液,混匀;静置;
[0063]
(3)加入无水乙醇,混匀;
[0064]
(4)将步骤(3)所得的溶液和絮状沉淀加入吸附柱中,离心,倒掉废液;
[0065]
(5)向吸附柱中加入缓冲液,离心,倒掉废液;
[0066]
(6)将吸附柱置于室温晾干;
[0067]
(7)将吸附柱转入离心管中,向吸附膜中间位置悬空滴加洗脱缓冲液,静置,离心,将含有dna的溶液收集到离心管中;
[0068]
(8)将步骤(7)得到的dna,利用所述的试剂盒进行pcr检测;
[0069]
(9)将步骤(8)得到的pcr产物进行sanger测序和分析,得到tnfaip3非编码序列突变情况。
[0070]
步骤(1)中所述的离心的条件优选为:10000rpm(~11500xg)离心1分钟。
[0071]
步骤(2)中所述的静置的条件优选为:56℃静置10分钟。
[0072]
步骤(4)中所述的离心的条件优选为:12000rpm(~13400xg)离心30秒。
[0073]
步骤(5)中所述的离心的条件优选为:12000rpm(~13400xg)离心30秒。
[0074]
步骤(6)中所述的室温晾干的条件优选为:室温(20~30℃)静置5分钟。
[0075]
步骤(8)中所述的pcr检测通过用于pcr的试剂实现。
[0076]
步骤(9)中所述的sanger测序通过invitrogen公司广州分公司实现。
[0077]
步骤(9)中所述的分析方法为:将sanger测序结果通过ncbi(http://www.ncbi.nlm.nih.gov/和http://blast.ncbi.nlm.nih.gov/blast.cgi)基因库进行比对,以确定tnfaip3非编码序列突变情况。
[0078]
本发明相对于现有技术具有如下的优点及效果:
[0079]
1.本发明采用pcr和sanger测序方法检测tcl患者外周血中tnfaip3非编码序列突变情况,首次发现tnfaip3非编码序列突变与tcl患者良好的临床预后有关。tnfaip3非编码序列突变对于tcl患者的预后判断和临床治疗方案的制定具有重要的指导意义。
[0080]
2.本发明可为tcl患者的应用靶向治疗提供更多的临床预后研究资料,在预测tcl患者预后评价及靶向药物应用方面具有广阔的应用前景。
[0081]
3.本发明使用pcr和sanger测序方法检测tcl患者外周血中tnfaip3非编码序列突变情况,该方法简单易行,方法稳定。当检测到tnfaip3非编码序列突变时,表明tcl患者良好的预后可能性大,可以作为预测tcl患者预后评估的指标。
附图说明
[0082]
图1是tnfaip3非编码序列突变对初发tcl患者预后的影响分析图。
[0083]
图2是tnfaip3非编码序列突变患者的具体突变情况图。
具体实施方式
[0084]
下面结合实施例及附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。
[0085]
实施例中所用试剂信息具体如下:
[0086]
血液基因组dna提取试剂盒(购自tiangen);
[0087]
pcr试剂盒(购自takara);
[0088]
sanger测序(invitrogen公司广州分公司)。
[0089]
实施例1
[0090]
(1)在与患者签署知情同意书的前提下采外周血。收集暨南大学附属第一医院血液内科41例初发tcl患者成人外周血样本,所有标本取自于入院时的外周血肝素抗凝,该部分研究方案已经获得本单位伦理委员会通过。同时收集tcl患者生存时间和生存状态等临床资料(如表1所示)。
[0091]
(2)dna提取
[0092]
2.1参照血液基因组dna提取试剂盒说明书,在血液样品中加入1
‑
2.5倍体积的细胞裂解液cl,颠倒混匀,10000rpm(~11500xg)离心1分钟,吸取上清,留下细胞核沉淀,向离心收集到的细胞核沉淀中加200μl缓冲液gs,振荡至彻底混匀;
[0093]
2.2加入20μl蛋白酶k溶液,混匀;加200μl缓冲液gb,充分颠倒混匀,56℃放置10分钟,期间颠倒混匀数次,溶液应变清亮;
[0094]
2.3加200μl无水乙醇,充分颠倒混匀,此时可能会出现絮状沉淀;
[0095]
2.4将上一步所得的溶液和絮状沉淀加入一个吸附柱cb3中(吸附柱cb3放入收集管中),12000rpm(~13400xg)离心30秒,倒掉收集管中的废液,将吸附柱cb3放入收集管中;
[0096]
2.5向吸附柱cb3中加入500μl缓冲液gd,12000rpm(~13400xg)离心30秒,倒掉收
集管中的废液,将吸附柱cb3放入收集管中;
[0097]
2.6向吸附柱cb3中加入600μl缓冲液gd,12000rpm(~13400xg)离心30秒,倒掉收集管中的废液,将吸附柱cb3放入收集管中;
[0098]
2.7重复操作步骤2.6;
[0099]
2.8 12000rpm(~13400xg)离心2分钟,倒掉废液,将吸附柱cb3置于室温放置5分钟,以彻底晾干吸附材料中残余的漂洗液;
[0100]
2.9将吸附柱cb3转入1.5ml离心管中,向吸附膜中间位置悬空滴加50
‑
200μl洗脱缓冲液tb,室温放置2
‑
5分钟,12000rpm(~13400xg)离心2分钟,将含有dna的溶液收集到离心管中。
[0101]
(3)pcr扩增tnfaip3基因启动子序列
[0102]
3.1扩增tnfaip3启动子的pcr反应体系为20μl:dna 1μl、taq聚合酶0.2μl、5
×
pcr buffer 4μl、dntp 2μl、mg
2
2μl、上下游引物各1μl以及ddh2o 8.8μl。反应在pcr仪中进行;
[0103]
3.2扩增tnfaip3的pcr反应条件为:94℃,5min;94℃,1min,60℃,1min,72℃,1min,40个循环,72℃,10min,4℃保存;
[0104]
3.3取pcr产物在100v,1.5%(w/v)琼脂糖凝胶中电泳检测。
[0105]
(4)pcr扩增tnfaip3基因非编码序列
[0106]
4.1pcr反应体系为30μl:其中dna 1μl、taq聚合酶0.3μl、5
×
pcr buffer 6μl、dntp3μl、mg
2
3μl、上下游引物各1.5μl以及超纯水13.7μl。反应在pcr仪中进行;
[0107]
4.2pcr反应条件为:94℃,5min,94℃,1min,57℃,1min,72℃,1min,40个循环,72℃;10min,4℃保存;
[0108]
4.3取pcr产物在100v,1.5%(w/v)琼脂糖凝胶中电泳检测。
[0109]
其中,所用于扩增tnfaip3基因启动子序列片段的引物如下:
[0110]
promoter(g.2933
‑
3687)(f):5'
‑
tttacaaaggagcaccagcaggaga
‑
3';
[0111]
promoter(g.2933
‑
3687)(r):5'
‑
attacatttaagaatacttgtcagg
‑
3';
[0112]
promoter(g.3568
‑
4249)(f):5'
‑
aagtgccaccctccatcc
‑
3';
[0113]
promoter(g.3568
‑
4249)(r):5'
‑
agcggtgacagcctttgg
‑
3';
[0114]
promoter(g.4110
‑
4744)(f):5'
‑
ggtgagtgttgttctgattc
‑
3';
[0115]
promoter(g.4110
‑
4744)(r):5'
‑
tcacgtgactctctgggtcg
‑
3';
[0116]
所用于扩增tnfaip3基因3
′‑
utr序列片段的引物如下:
[0117]3’‑
utr(g.18828
‑
19347)(f):5'
‑
caacggctactgcaacgaat
‑
3';
[0118]3’‑
utr(g.18828
‑
19347)(r):5'
‑
ctcgctgccatgaggatct
‑
3';
[0119]3’‑
utr(g.19272
‑
19787)(f):5'
‑
gagaagccagagccattccacct
‑
3';
[0120]3’‑
utr(g.19272
‑
19787)(r):5'
‑
gctcatgccccaacaacaacca
‑
3';
[0121]3’‑
utr(g.19717
‑
20407)(f):5'
‑
gctgccctagaagtacaata
‑
3';
[0122]3’‑
utr(g.19717
‑
20407)(r):5'
‑
gacagcaaccacaaagcacac
‑
3';
[0123]3’‑
utr(g.20455
‑
20938)(f):5'
‑
cccagagataaaggctgccat
‑
3';
[0124]3’‑
utr(g.20455
‑
20938)(r):5'
‑
ggaagcacagtcttaatatc
‑
3';
[0125]
所用于扩增tnfaip3基因外显子和内含子序列片段的引物如下:
[0126]
exon2(f):5'
‑
ggagtcgtattaaagtcaggctaa
‑
3';
[0127]
exon2(r):5'
‑
ggcaaaagaaacacaacagaac
‑
3';
[0128]
exon3(f):5'
‑
ttgctgggtcttacatgcag
‑
3';
[0129]
exon3(r):5'
‑
cccaccatggagctctgtta
‑
3';
[0130]
exon4(f):5'
‑
gggagtacaggatacattcaagc
‑
3';
[0131]
exon4(r):5'
‑
gctgaaagcatttaagtacagatcc
‑
3';
[0132]
exon5(f):5'
‑
acctaagggcctcattttcc
‑
3';
[0133]
exon5(r):5'
‑
agcaaaaaggaaaaccctga
‑
3';
[0134]
exon6(f):5'
‑
tgagatctacttacctatggccttg
‑
3';
[0135]
exon6(r):5'
‑
cagatgacacaggagagagctg
‑
3';
[0136]
part1 of exon 7(f):5'
‑
ggttctacaattcttgccataatcc
‑
3';
[0137]
part1 of exon 7(r):5'
‑
caagtgccttgtgtggtctg
‑
3';
[0138]
part2 of exon 7(f):5'
‑
cacaacggattttgtgaacg
‑
3';
[0139]
part2 of exon 7(r):5'
‑
aggaacaaaaccccttctgg
‑
3';
[0140]
exon8(f):5'
‑
ctctgtatcggtggggtgac
‑
3';
[0141]
exon8(r):5'
‑
caaaaagcatcgaacacacg
‑
3';
[0142]
exon9(f):5'
‑
tgatctgcctgttctttcca
‑
3';
[0143]
exon9(r):5'
‑
gggttcagaggatagcacca
‑
3'。
[0144]
(5)sanger测序及tnfaip3基因突变的鉴定
[0145]
凝胶电泳检测质量较好的pcr产物送invitrogen公司广州分公司进行sanger测序。所获得的核苷酸序列通过ncbi(http://www.ncbi.nlm.nih.gov/和http://blast.ncbi.nlm.nih.gov/blast.cgi)基因库进行比对,确定tnfaip3基因突变。
[0146]
tnfaip3基因突变情况以及tcl患者临床预后资料如表1所示。
[0147]
将tnfaip3基因非编码突变情况结合tcl患者临床预后资料进行分析,在r语言软件(4.0.2版,https://www.r
‑
project.org/)中通过输入tnfaip3基因非编码突变状态、生存状态和生存时间,用“survival”r软件包绘制生存曲线。发现tnfaip3基因非编码突变时的tcl患者的预后较好(图1)。
[0148]
tnfaip3非编码序列突变患者的突变情况图如图2所示。
[0149]
上述实验结果表明tnfaip3基因非编码突变在预测tcl临床预后的评估中具有重要意义,其为临床应用靶向药物提供预后研究资料。
[0150]
表1 tcl患者tnfaip3突变情况和临床资料
[0151][0152][0153]
从上述测得的基因突变虽然不能直接得出将来诊断结果和健康状况,但其作为中间结果,可以作为患者临床治疗方案制定的参考信息之一。
[0154]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的
限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
