1.本发明涉及以利用酯交换催化剂的酯交换反应作为固化反应的热固化性树脂组合物以及利用该组合物的涂膜形成方法和固化涂膜。
背景技术:
2.本发明人对于以酯交换反应作为固化反应的热固化性树脂组合物进行了研究(专利文献1)。根据最近的研究可知,通过以酯交换反应作为固化反应,能够确保与通常已知的使用三聚氰胺树脂或多异氰酸酯化合物的固化同等的固化性能。
3.三聚氰胺树脂、多异氰酸酯化合物的热反应性良好,所得到的固化树脂的性质优异,因此已广泛得到常规使用。但是,三聚氰胺树脂由于会产生甲醛而被认为是病态建筑综合征的原因,因此近年来也存在用途受到限制的情况。另外,多异氰酸酯化合物虽然固化反应性能高,但由于价格高等理由,认为若能发现更为廉价的能够低温固化的固化剂则是优选的。因此,通过以酯交换反应作为固化反应,具有能够改善这些问题的可能性。
4.上述专利文献1中,必须使用叔烷基酯作为烷基酯。但是,在使用叔烷基酯作为烷基酯的情况下,在固化时会产生推测以异丁烯为主要成分的气体成分,要求对其进行抑制。若使用伯烷基酯,则能够改善这样的问题,但在专利文献1中并未记载能够确保达到可实用的水准的固化性的方法。
5.专利文献2中记载了使用伯烷基酯的酯交换反应而得到的粉体涂料。但是,参与酯交换反应的酯基是与丙烯酸类树脂的主链直接键合的。这样的伯酯基与羟基的酯交换反应的反应性低。
6.现有技术文献
7.专利文献
8.专利文献1:日本专利第6398026号公报
9.专利文献2:日本特开平8
‑
67833号公报
技术实现要素:
10.发明所要解决的课题
11.鉴于上述情况,本发明的目的在于得到一种热固化性树脂组合物,其能够通过伯烷基酯或仲烷基酯与羟基之间的酯交换反应而得到良好的固化性能。
12.用于解决课题的手段
13.本发明涉及一种热固化性树脂组合物,其特征在于,其含有化合物(a)、具有2个以上羟基的多元醇(b)以及酯交换催化剂(c),上述化合物(a)为具有2个以上的
‑
coor(r为伯烷基或仲烷基)的化合物(a
‑
a)和/或具有1个
‑
coor(r为伯烷基或仲烷基)和羟基的化合物(a
‑
b)。
14.酯交换催化剂(c)优选为含有碱金属以外的金属的金属化合物。化合物(a)的分子量优选为3000以下。优选化合物(a)的分子量/
‑
coor基数=300以下。
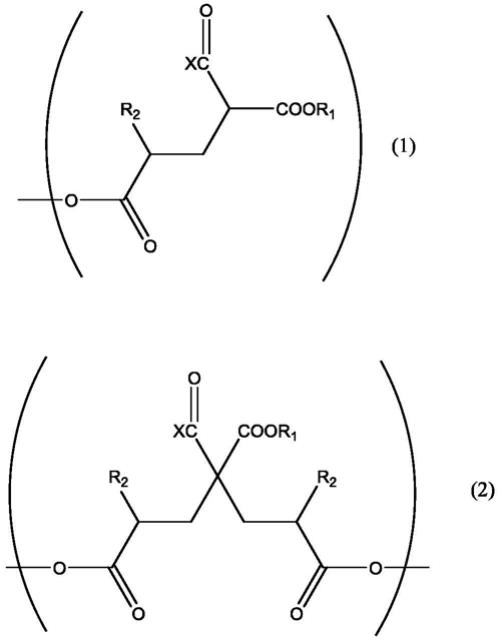
15.化合物(a)优选为具有至少1种下述通式(1)和/或通式(2)所表示的结构的化合物。
16.[化1]
[0017][0018]
(r1表示伯烷基或仲烷基。x表示碳原子数5以下的烃基或
‑
or1基。在分子中存在2个以上的r1的情况下,它们可以相同也可以不同)。r2表示氢或甲基。在分子中存在2个以上的r2的情况下,它们可以相同也可以不同。
[0019]
化合物(a)优选为具有下述通式(3)所表示的结构的化合物。
[0020]
[化2]
[0021][0022]
(式中,r1表示伯烷基或仲烷基。r3表示羟基、可以具有酯基的碳原子数1~50的烷基或亚烷基。n为2~20的整数)
[0023]
多元醇树脂(b)的重均分子量优选为1000~1000000。
[0024]
上述热固化性树脂组合物优选为无溶剂、粉体、溶剂系或水系。上述热固化性树脂组合物在仅含有成分(a)~(c)和溶剂的状态下,在固体成分为55重量%以上时,在25℃的粘度优选为200mpa
·
s以下、进一步优选为100mpa
·
s以下。本发明还涉及一种固化膜,其特征在于,其是通过将上述热固化性树脂组合物进行三维交联而形成的。
[0025]
发明的效果
[0026]
本发明的热固化性树脂组合物能够通过伯烷基酯或仲烷基酯与羟基之间的酯交换反应而得到良好的固化性能。
附图说明
[0027]
图1是实施例1的刚体摆锤试验机数据。
[0028]
图2是实施例2的刚体摆锤试验机数据。
[0029]
图3是实施例6的刚体摆锤试验机数据。
[0030]
图4是实施例7的刚体摆锤试验机数据。
[0031]
图5是实施例8的刚体摆锤试验机数据。
[0032]
图6是实施例10的刚体摆锤试验机数据。
[0033]
图7是实施例13的刚体摆锤试验机数据。
[0034]
图8是比较例7的刚体摆锤试验机数据。
[0035]
图9是比较例11的刚体摆锤试验机数据。
[0036]
图10是比较例12的刚体摆锤试验机数据。
[0037]
图11是实施例15的刚体摆锤试验机数据。
具体实施方式
[0038]
以下详细说明本发明。本发明发现,在通过具有伯烷基酯基或仲烷基酯基的化合物与具有羟基的化合物之间的酯交换反应进行固化的热固化性树脂组合物中,可得到良好的固化反应,从而完成了本发明。
[0039]
以(甲基)丙烯酸的伯烷基酯或仲烷基酯作为结构单元的聚合物是作为热固化性树脂组合物用材料而公知的材料。已知这样的聚合物通常作为还具有羟基的聚合物,通过与固化剂合用而进行固化。
[0040]
但是,在如这种公知的聚丙烯酸类树脂等这样、伯烷基酯基或仲烷基酯基直接键合在树脂的主链上的情况下,该酯基的反应性低,难以通过酯交换反应进行良好的固化。据推测,这是由于主链附近的伯烷基酯基或仲烷基酯基被主链约束,自由度小,因此往往难以接近羟基。
[0041]
因此,使用具有伯烷基酯基或仲烷基酯基的化合物,通过酯交换反应使热固化性树脂组合物固化的技术迄今尚未得到充分的研究。本发明人通过进行各种研究,发现了通过伯烷基酯基或仲烷基酯基与羟基的反应能够得到良好的固化的组成,从而完成了本发明。
[0042]
若能够通过伯烷基酯基或仲烷基酯基与羟基的反应得到良好的固化,则能够改善在使用叔烷基酯基(特别是叔丁基酯)的情况下成为问题的、因气体成分的产生使固化物表面发泡所带来的外观劣化的问题,从这方面出发是优选的。
[0043]
另外,专利文献1中所公开的具有叔烷基酯基的化合物的酯交换反应最适合利用酸催化剂进行催化。这意味着难以在碱性条件下进行反应。另一方面,在伯烷基酯基或仲烷基酯基的情况下,利用非酸的催化剂(例如金属催化剂、碱催化剂等)也可促进反应。因此,可良好地进行碱性条件下的固化反应,从这方面出发也是优选的。
[0044]
作为这样的通过伯烷基酯基或仲烷基酯基与羟基的反应而实现固化的方法,具体而言,为含有化合物(a)的方法,该化合物(a)为具有2个以上的
‑
coor基的化合物(a
‑
a)和/或具有1个以上的
‑
coor(r为伯烷基或仲烷基)和/或羟基的化合物(a
‑
b)。即,在1分子中具有2个以上的参与酯交换反应的官能团的化合物(a)是必须的。
[0045]
本发明中,从得到良好的固化性的方面出发,特别优选使用下述化合物(a),该化合物(a)为具有2个以上的
‑
coor基的化合物(a
‑
a)和/或具有1个以上的
‑
coor(r为伯烷基或仲烷基)和/或羟基的化合物(a
‑
b),且分子量为3000以下。据推测,由此,烷基酯基不被约束而能够容易地接近羟基,因此反应可良好地进行。
[0046]
需要说明的是,在使用这样的低分子量的化合物的情况下,除了固化反应性优异以外,还能够实现涂料的高固体成分化(高固体化),从这方面出发也是优选的。在涂料等热固化性树脂组合物的领域中,从涂装效率、降低排出溶剂量的方面考虑,优选提高组合物中的固体成分的含量。这种情况下,即使增加固体成分,粘性也不容易上升,从这方面出发是优选的。优选为能够适用于喷雾等常规涂装方法的粘性。即,优选即使高固体成分化,粘性也不会变得过高。
[0047]
本发明的热固化性树脂组合物中,在多元醇(b)为上述低分子量的成分时,能够在维持低粘性的情况下实现高固体成分化,从这方面出发也是优选的。具体而言,通过使用这样的低分子量的酯化合物作为反应性稀释剂,能够使固体成分为55重量%以上。
[0048]
本发明中,含有2个以上的
‑
coor(r为伯烷基或仲烷基)的分子量为3000以下的化合物(a)是指含有至少1种以分子量计为3000以下的化合物。即,并非意味着从平均分子量的观点来看为3000以下,而是意味着含有分子量为3000以下的化合物。并且,并不妨碍合用分子量大于3000的含有2个以上的
‑
coor(r为伯烷基或仲烷基)的化合物。
[0049]
此外,上述化合物(a)的分子量更优选为2500以下、进一步优选为2000以下、最优选为1000以下。
[0050]
本发明中,上述化合物(a)的分子量是指通过利用nmr、质谱等公知的化学分析对化合物(a)进行分析而测定的值。
[0051]
另外,为了得到高固体化成分的涂料并且使涂膜物性良好,优选使用作为反应点的官能团的数目多的化合物作为化合物(a)。从这样的方面考虑,化合物(a)中,优选分子量/
‑
coor基数=300以下。上述分子量/
‑
coor基数更优选为200以下、进一步优选为150以下。
[0052]
r只要为伯基或仲基就没有特别限定,可以使用碳原子数50以下的烷基。r的碳原子数更优选为20以下、进一步优选为10以下、最优选为4以下。具体而言,可以举出甲基、乙基、丙基、丁基等。这些基团无需为直链状,只要是伯烷基或仲烷基,也可以是支链状。
[0053]
本发明的热固化性树脂组合物中,相对于组合物总量(固体物质换算),优选以1~99重量%的比例含有化合物(a)。上述含量的下限更优选为5重量%、进一步优选为10重量%。上述含量的上限更优选为90重量%、进一步优选为80重量%。
[0054]
化合物(a)也可以进一步具有烷基酯基以外的官能团。作为可以存在于分子中的官能团,可以举出羟基、酰胺基、酯基、醚基、烷基、烯基、炔基、氨基等。另外还可以具有芳香环、脂环结构。
[0055]
关于能够作为上述化合物(a)使用的化合物没有特别限定,只要是分子量为3000以下且具有2个以上的与羟基之间发生酯交换反应的烷基酯基即可,更具体地说,例如可以举出下述化合物。
[0056]
(a
‑
1)作为具有活性亚甲基的化合物的衍生物得到的化合物
[0057]
下述通式(6)所表示的具有活性亚甲基的化合物可以通过活性亚甲基的反应通过
与各种化合物(例如具有乙烯基的化合物、具有卤基的化合物等)的反应而得到具有烷基酯基的化合物。通过这样的反应得到的化合物也可以作为本发明的化合物(a)使用。
[0058]
[化3]
[0059][0060]
(式中,r1表示伯烷基或仲烷基。x表示or1基或碳原子数为5以下的烃基。需要说明的是,在1分子中存在2个r1的情况下,这些r1可以相同也可以不同。)
[0061]
上述r1的结构没有特别限定,可以使用具有甲基、乙基、苄基、正丙基、异丙基、正丁基、异丁基、仲丁基等公知的烷基的化合物。
[0062]
作为这种具有活性亚甲基的化合物,具体而言,可以举出丙二酸酯和乙酰乙酸酯等。可以使用使这些化合物与乙烯基化合物或含卤基化合物反应而得到的化合物。下面分别对它们进行说明。
[0063]
(a
‑1‑
1)通过具有活性亚甲基的化合物与含有乙烯基的化合物的反应得到的化合物
[0064]
具有活性亚甲基的化合物可以通过迈克尔加成反应加成到双键上。用下式表示基于这种具有活性亚甲基的化合物的一般的迈克尔加成反应。
[0065]
[化4]
[0066][0067]
在上述反应中,也可以通过活性亚甲基的两个氢两者发生迈克尔反应而得到下述通式(7
‑
1)所示的化合物。
[0068]
[化5]
[0069][0070]
通过这种反应得到的化合物具有通式(7)所示的结构和/或通式(7
‑
1)所示的结构,其为具有2个以上烷基酯基的化合物,因此可以特别优选地用于本发明的目的。
[0071]
特别是在使用(甲基)丙烯酸或其衍生物作为上述通式的乙烯基化合物的情况下,发生下述反应。
[0072]
[化6]
[0073][0074]
上述通式中,r1表示碳原子数50以下的伯烷基或仲烷基。r2表示氢或甲基。r
16
没有特别限定,可以根据目的为任意的官能团。
[0075]
上述反应中,也可以通过活性亚甲基的两个氢两者发生迈克尔反应而得到下述通式(9)所表示的化合物。
[0076]
[化7]
[0077][0078]
上述通式(9)所表示的化合物可以通过在原料的混配中调整(甲基)丙烯酸酯与活性亚甲基化合物的摩尔比而获得。此外,通过调整它们的摩尔比,也可以作为上述通式(8)所表示的化合物与上述通式(9)所表示的化合物的混合物而获得。通过这种反应得到的酯化合物在分子中具有下述结构所示的结构单元。
[0079]
[化8]
[0080][0081]
在上述反应中,通过使用具有2个以上不饱和键的丙烯酸衍生物作为原料,也可以制成在分子中具有2个以上的上述通式所示的结构(1)和/或(2)所示的结构的酯化合物。即,在本发明中可以优选使用具有该官能团的具有下述通式所表示的结构的化合物。
[0082]
[化9]
[0083][0084]
这样的化合物由于酯交换反应性高、在分子中具有较多的coor基,因此能够得到良好的固化性,从这方面出发是优选的。上述通式中的n3、n4最优选为2~12。另外,l、m、c只要是该化合物的分子量为3000以下的结构就没有特别限定,表示可以具有羟基、酯基、醚基等任意的官能团的烃基。
[0085]
另外,上述“(a
‑1‑
1)通过具有活性亚甲基的化合物与含有乙烯基的化合物的反应得到的化合物”使用以在一分子中具有2个以上不饱和键的化合物为原料的化合物,也可以是在一分子中具有2个以上的上述通式(10)所表示的结构和/或通式(11)所表示的结构的化合物。
[0086]
已知多种具有来自具有活性亚甲基的化合物酯的结构的化合物,具有上述结构的化合物容易进行丙二酸酯或乙酰乙酸酯与乙烯基的加成反应,容易合成,通过选择起始原料能够调整酯基的数目,因此从能够容易地调整固化性能、固化后的树脂的性能的方面出发是特别优选的。具体而言,可以优选使用丙二酸二甲酯、丙二酸二乙酯、丙二酸二正丁酯、乙酰乙酸甲酯、乙酰乙酸乙酯等。
[0087]
这样的化合物通过以各种具有1个以上的不饱和键的(甲基)丙烯酸衍生物作为原料,与具有活性亚甲基的化合物进行迈克尔加成反应而获得。作为上述“具有1个以上的不饱和键的(甲基)丙烯酸衍生物”没有特别限定,例如可以举出以下的物质。
[0088]
官能团数为1的(甲基)丙烯酸酯的示例可以举出(甲基)丙烯酸甲酯、(甲基)丙烯酸乙酯、(甲基)丙烯酸异丙酯、(甲基)丙烯酸正丁酯、(甲基)丙烯酸异丁酯、(甲基)丙烯酸仲丁酯、(甲基)丙烯酸叔丁酯等。
[0089]
官能团数为2的(甲基)丙烯酸酯的示例包括1,4
‑
丁二醇二(甲基)丙烯酸酯、1,3
‑
丁二醇二(甲基)丙烯酸酯、1,6
‑
己二醇二(甲基)丙烯酸酯、乙二醇二(甲基)丙烯酸酯、二乙二醇二(甲基)丙烯酸酯、三乙二醇二(甲基)丙烯酸酯、聚乙二醇二(甲基)丙烯酸酯、二丙二
醇二(甲基)丙烯酸酯、三丙二醇二(甲基)丙烯酸酯、聚丙二醇二(甲基)丙烯酸酯、新戊二醇二(甲基)丙烯酸酯、羟基特戊酸新戊二醇二(甲基)丙烯酸酯、1,6
‑
己二醇二(甲基)丙烯酸酯、1,9
‑
壬二醇二(甲基)丙烯酸酯、1,10
‑
癸二醇二(甲基)丙烯酸酯、甘油二(甲基)丙烯酸酯、二羟甲基三环癸烷二(甲基)丙烯酸酯(dcp
‑
a)、双酚a的eo加成物二丙烯酸酯(共荣社化学公司制造;light
‑
acrylate bp
‑
4ea、bp
‑
10ea)、双酚a的po加成物二丙烯酸酯(共荣社化学公司制造;bp
‑
4pa、bp
‑
10pa等)。其中,可以优选使用双酚a的po加成物二丙烯酸酯(共荣社化学公司制造;bp
‑
4pa)、二羟甲基三环癸烷二(甲基)丙烯酸酯(dcp
‑
a)等。
[0090]
官能团数为3的(甲基)丙烯酸酯的示例包括三羟甲基甲烷三(甲基)丙烯酸酯、三羟甲基丙烷三(甲基)丙烯酸酯、三羟甲基丙烷环氧乙烷改性三(甲基)丙烯酸酯、三羟甲基丙烷环氧丙烷改性三(甲基)丙烯酸酯、季戊四醇三(甲基)丙烯酸酯、甘油丙氧基三(甲基)丙烯酸酯、三(2
‑
(甲基)丙烯酰氧基乙基)异氰脲酸酯等。其中,可以优选使用三羟甲基丙烷三甲基丙烯酸酯、季戊四醇三甲基丙烯酸酯等。
[0091]
官能团数为4的(甲基)丙烯酸酯的示例包括二季戊四醇四(甲基)丙烯酸酯、季戊四醇四(甲基)丙烯酸酯、季戊四醇环氧乙烷改性四(甲基)丙烯酸酯、季戊四醇环氧丙烷改性四(甲基)丙烯酸酯、双三羟甲基丙烷四(甲基)丙烯酸酯等。其中,可以优选使用双三羟甲基丙烷四(甲基)丙烯酸酯、季戊四醇四(甲基)丙烯酸酯等。
[0092]
官能团数为5以上的(甲基)丙烯酸酯的示例可以举出二季戊四醇五(甲基)丙烯酸酯、双三羟甲基丙烷五(甲基)丙烯酸酯、丙酸改性二季戊四醇五(甲基)丙烯酸酯、二季戊四醇六(甲基)丙烯酸酯、双三羟甲基丙烷六(甲基)丙烯酸酯、二季戊四醇的己内酯改性物的六(甲基)丙烯酸酯等多官能性(甲基)丙烯酸酯。
[0093]
(a
‑1‑
2)通过具有活性亚甲基的化合物与含有卤素的化合物的反应得到的化合物
[0094]
由此得到的化合物也可以在本发明中适当地使用。特别是可以举出酯基的羰基碳直接被卤化而成的化合物。作为卤素没有特别限定,可以举出氯、溴、碘等。作为这样的化合物,可以举出通过下述通式(15)所表示的反应式得到的化合物。
[0095]
[化10]
[0096][0097]
r1、r2为碳原子数50以下的伯烷基或仲烷基(r1与r2可以相同),x为碳原子数5以下的烃基或
‑
or1基,y为卤素,n为1或2。
[0098]
对应于上述化合物(a
‑
1)的化合物的具体例如下所示。
[0099]
[化11]
[0100][0101]
[化12]
[0102]
[0103][0104]
式中r表示相同或不同的伯烷基或仲烷基。n5表示1至10。
[0105]
上述化合物(a
‑
1)优选在分子中存在3个以上作为交联点的伯烷基酯或仲烷基酯。即,分子中的烷基酯基的数目越多,固化后的树脂的交联密度越高,因此固化物的硬度良好,可得到物性优异的固化物,从这方面出发是优选的。伯烷基酯或仲烷基酯更优选在分子中存在5个以上。
[0106]
(a
‑
2)具有下述通式(31)所表示的官能团的化合物
[0107]
[化13]
[0108][0109]
n=0~20
[0110]
r1为碳原子数50以下的烷基。
[0111]
r3为氢或碳原子数10以下的烷基。
[0112]
上述化合物(a)中,烷基酯基可以具有上述通式(31)所表示的结构。
[0113]
虽然原因尚不明确,但上述通式(31)所表示的酯基的酯交换反应的反应性高。因此,通过使用具有该官能团的酯化合物作为化合物(a)的一部分或全部,能够制成具有优异的固化性能的热固化性树脂组合物。
[0114]
(关于通式(31)的结构)
[0115]
上述通式(31)的结构以α取代羧酸酯骨架作为基础。
[0116]
通式(31)中,n为0~20。
[0117]
n的下限更优选为1。n的上限更优选为5。
[0118]
此外,也可以为上述通式(31)中的n值不同的多种成分的混合物。这种情况下,n的平均值nav优选为0~5。nav的下限更优选为1。nav的上限更优选为3。nav的测定可以通过nmr分析来进行。此外,n的值也可以通过nmr分析来测定。
[0119]
n也可以为0,但从能够得到反应性更高的热固化性树脂组合物的方面考虑,优选n为大于0的值。
[0120]
即,n为1以上时,能够实现更低温度下的固化,由此能够更适当地发挥出本发明的效果。
[0121]
上述通式(31)中,作为r1可以使用碳原子数50以下的伯烷基或仲烷基,可以为伯基、仲基中的任一者。
[0122]
上述烷基酯基中的烷基(即上述通式中的r1)是碳原子数为50以下的烷基,更优选碳原子数为1~20的范围内,进一步优选为1~10的范围内,进而优选为1~6的范围内。最优选为1~4的范围内。通过为这样的范围内,能够适当地进行固化反应,从这方面出发是优选的。
[0123]
作为上述烷基,具体而言,例如可以使用具有甲基、乙基、苄基、正丙基、异丙基、正丁基、异丁基、仲丁基等公知的烷基的化合物。
[0124]
具有上述官能团(31)的化合物可以通过使具有下述通式(32)
[0125]
[化14]
[0126][0127]
(x表示卤素、羟基)
[0128]
的结构的在羰基的α位引入有活性基x的酯化合物与对应于目标化合物的结构的羧酸或羧酸盐化合物反应而得到。若将其用通式表示,则如下所示。
[0129]
[化15]
[0130][0131]
上述通式中,关于可以作为通式(33)所表示的原料使用的化合物,只要是能够发生上述反应的羧酸或羧酸衍生物,则可对任意的羧酸进行。作为羧酸衍生物,可以举出y为om(羧酸盐)、oc=or(酸酐)、cl(酰氯)等的羧酸衍生物。在上述y=om的羧酸盐的情况下,作为羧酸盐,可以举出钠盐、钾盐、胺盐、锌盐等。需要说明的是,在作为聚合物的单体使用的情况下,可以使用具有不饱和基团的化合物作为通式(33)所表示的化合物。
[0132]
作为上述通式(32)所表示的化合物,可以为具有与作为目标的通式(31)所表示的结构相对应的骨架的化合物。
[0133]
另外,对于上述通式(32)所表示的化合物,其制造方法没有特别限定。上述通式(32)所表示的化合物中,n=0的化合物是在α位具有x所表示的活性基团的化合物,可以举出各种α羟基酸、α卤代羧酸。具体而言,可以举出氯乙酸甲酯、氯乙酸乙酯、溴乙酸甲酯、溴乙酸乙酯、2
‑
氯丙酸甲酯、乙醇酸甲酯、乳酸甲酯、乳酸乙酯、乳酸丁酯等。
[0134]
上述通式(32)所表示的化合物中,关于n=1以上的化合物,以下示出其制造方法的一例。
[0135]
需要说明的是,以下所示的内容为制造方法的一例,本发明中并不限于通过下述制造方法得到的化合物。
[0136]
例如,可以通过在α位具有卤素的羧酸、其盐或其衍生物与在α位具有卤素或羟基
的羧酸烷基酯的反应而得到。若将其以通式表示,则如下所示。
[0137]
[化16]
[0138][0139]
作为在α位具有卤素的羧酸、其盐或其衍生物,可以举出羧酸的碱金属盐(钾盐、钠盐等)、酸酐、酰氯等。作为上述通式(34)所表示的化合物,具体而言,可以使用氯乙酸钠等。
[0140]
作为在α位具有卤素或羟基的羧酸烷基酯,可以举出氯乙酸、溴乙酸、乳酸等α取代羧酸化合物的烷基酯。上述烷基酯的烷基没有特别限定,为碳原子数1~50的烷基即可。
[0141]
这样的烷基可以为伯烷基、仲烷基中的任一者,具体而言,可以举出甲基、乙基、苄基、正丙基、异丙基、正丁基、异丁基、仲丁基等。
[0142]
上述反应中,优选使x1和x2为不同种类。优选使它们为不同种类的官能团而使反应性不同、并按照x1未反应而残留的方式选择官能团的组合。具体而言,特别优选x1为溴基、x2为氯基的组合。
[0143]
另外,上述反应中,可以通过调整2种原料的混合比而对n值进行调整。上述反应中,通常以具有不同的n的多种化合物的混合物的形式得到。具有通式(31)的结构的化合物进行精制可以通过精制而仅使用n具有特定值的化合物,也可以为n值不同的多种化合物的混合物。
[0144]
上述通式(31)所表示的化学结构可以通过使上述通式(32)所表示的化合物与各种羧酸化合物反应而形成。因此,使上述通式(32)所表示的化合物与具有2个以上的羧基的化合物、或者具有1个羧基的化合物以及具有羟基的化合物反应而得到的化合物可以适当地用于本发明中。
[0145]
上述化合物在本发明的热固化性树脂组合物中使用时,优选为具有2个以上的官能团的化合物,可以使用具有2个以上的羧基的多元羧酸、具有羧基和羟基的羟基羧酸等。
[0146]
各种多元羧酸是在聚酯原料、聚酰胺原料、中和剂、合成原料等多种用途中广泛且低成本地提供的通用原料。将这样的多元羧酸利用公知的方法转换成上述通式(31)所表示的官能团而成的化合物也可以在本发明中使用。
[0147]
在使用这样的化合物作为具有通式(31)所表示的官能团的化合物时,能够利用公知的方法低成本地进行酯化,能够以比较低的分子量引入多元酯基。另外,通过进行酯化,在有机溶剂中的相容性变得良好,能够适当地使用,从这方面出发是优选的。
[0148]
作为此处使用的多元羧酸没有特别限定,例如可以使用碳原子数为50以下的多元羧酸。
[0149]
更具体而言,可以举出:丙二酸、琥珀酸、戊二酸、己二酸、庚二酸、辛二酸、壬二酸、癸二酸、十一烷二酸、十二烷二酸、巴西基酸、十八烷二酸、丁烷四羧酸、甲烷三羧酸等脂肪族多元羧酸;
[0150]
1,2
‑
环己烷二羧酸、1,3
‑
环己烷二羧酸、1,4
‑
环己烷二羧酸、4
‑
环己烯
‑
1,2
‑
二羧酸、3
‑
甲基
‑
1,2
‑
环己烷二羧酸、4
‑
甲基
‑
1,2
‑
环己烷二羧酸、1,2,4
‑
环己烷三羧酸、1,3,5
‑
环己烷三羧酸等脂环族多元羧酸;
[0151]
邻苯二甲酸、间苯二甲酸、对苯二甲酸、萘二羧酸、4,4
’‑
联苯二羧酸、偏苯三酸、苯均四酸等芳香族多元羧酸;
[0152]
乙醇酸、柠檬酸、乳酸、3
‑
羟基丁酸、3
‑
羟基
‑4‑
乙氧基苯甲酸等羟基羧酸;等等。
[0153]
需要说明的是,作为这样的化合物的一例,以下示出使用柠檬酸作为多元羧酸进行上述反应时的化合物的一般结构。
[0154]
[化17]
[0155][0156]
具有下述通式(41)所表示的官能团和/或下述通式(42)所表示的官能团的化合物
[0157]
[化18]
[0158][0159]
[化19]
[0160][0161]
(上述通式(41)、通式(42)的任一者中,r1均为碳原子数50以下的烷基。
[0162]
r2是可以在一部分包含氧原子、氮原子的碳原子数50以下的亚烷基)
[0163]
即,coor基可以具有上述通式(41)所表示的结构和/或通式(42)所表示的结构。另外,上述通式(41)、通式(42)所表示的结构中,由于是除了
‑
coor基以外还具有羟基的化合物,因此只要是具有1个这样的官能团的化合物,就能够发生基于酯交换反应的交联。但是,从得到更合适的固化性能的方面出发,优选coor8基具有2个以上的上述通式(41)所表示的结构和/或通式(42)所表示的结构。
[0164]
具有上述结构的化合物在结构中具有羟基。据推测该羟基也有助于酯交换反应。因此,只要是在分子中具有1个上述通式(41)所表示的结构和/或通式(42)所表示的结构的化合物,就能够具有热固化性。但是,为了得到更合适的固化性能,优选具有2个以上的该结构。
[0165]
此外,在分子中具有上述通式(41)所表示的结构和/或通式(42)所表示的结构的化合物的酯交换反应性高,从这方面考虑是优选的。
[0166]
上述烷基酯基中的烷基(即上述通式中的r1)是碳原子数为50以下的伯烷基或仲烷基,更优选碳原子数为1~20的范围内,进一步优选为1~10的范围内,进一步优选为1~6的范围内。最优选为1~4的范围内。通过为这样的范围内,能够适当地进行固化反应,从这方面出发是优选的。
[0167]
作为上述烷基,具体而言,例如可以使用具有甲基、乙基、苄基、正丙基、异丙基、正丁基、异丁基、仲丁基等公知的烷基的化合物。
[0168]
上述通式(41)中的r2基是可以在一部分包含氧原子、氮原子的碳原子数50以下的亚烷基,具体而言,可以包含亚甲基、亚乙基、正亚丙基、异亚丙基、正亚丁基、或苯环、环己环之类的环状结构(碳链1~50)。其中,从原料成本低、反应性优异的方面出发,特别优选为亚乙基。
[0169]
作为具有上述通式(41)所表示的官能团的酯化合物的制造方法没有特别限定,可以举出使环氧化物与具有烷基酯基和羧基的化合物进行反应的方法。若将其用通式表示,则为下述的反应。
[0170]
[化20]
[0171][0172]
上述反应中,所使用的具有烷基酯基和羧基的化合物例如可以通过下述反应这样的酸酐与醇的反应来制造。
[0173]
[化21]
[0174][0175]
关于作为上述通式(52)所表示的反应中的原料的酸酐没有特别限定,例如可以使用具有环状结构的琥珀酸酐、马来酸酐、邻苯二甲酸酐、六氢邻苯二甲酸酐、甲基六氢邻苯二甲酸酐、苯甲酸酐、衣康酸酐等各种二元酸的酸酐。上述通式(52)所表示的反应为公知的常规反应,关于其反应条件等,可以按照常规条件来进行。
[0176]
需要说明的是,上述通式(51)所表示的合成方法中使用的具有烷基酯基和羧基的化合物并不限于通过上述通式(52)的方法得到的化合物,也可以为通过其他方法得到的化合物。
[0177]
上述通式(51)所表示的合成方法中,使用环氧化物作为必要成分。上述环氧化物没有特别限定,可以使用任意的环氧化物。
[0178]
例如,若使用环氧氯丙烷,则可以通过使其与酚化合物、羧酸化合物、含有羟基的化合物等进行反应而在具有各种骨架的化合物中引入环氧基。通过对这样的任意环氧化物进行上述反应,能够得到具有上述通式(41)所表示的官能团的化合物。这样的反应的通式如下所示。
[0179]
[化22]
[0180][0181]
此外,上述环氧化物可以为环状环氧化物。
[0182]
即,将环状环氧化物作为环氧化物使用的情况下,可以通过下述反应得到具有通式(42)所表示的结构的化合物。
[0183]
[化23]
[0184][0185]
作为可以在上述通式中使用的脂环式环氧化物,可以举出甲基丙烯酸
‑
3,4
‑
环氧环己基甲酯、3,4
‑
环氧环己基甲酸
‑3’
,4
’‑
环氧环己基甲酯等。
[0186]
具有通式(41)所表示的官能团和/或通式(42)所表示的官能团的化合物可以通过上述的制造方法来得到。
[0187]
具有2个以上的这样的官能团的化合物、具有这样的官能团和羟基的化合物可以适当地作为以酯交换反应作为固化反应的树脂组合物的成分使用。
[0188]
具有通式(41)所表示的官能团和/或通式(42)所表示的官能团的化合物作为固化性树脂组合物中的固化性官能团使用。因此,优选为具有2个以上的官能团的化合物。更具体而言,可以具有2个以上的上述通式(41)所表示的官能团和/或通式(42)所表示的官能团,也可以除了具有上述通式(41)所表示的官能团和/或通式(42)所表示的官能基所表示的官能团以外还进一步具有羟基等。
[0189]
如上所述,通过对各种环氧化物进行通式(51)所表示的反应或通式(54)所表示的反应,能够引入上述通式(41)所表示的官能团和/或通式(42)所表示的官能团。
[0190]
因此,通过对公知的环氧化物进行上述通式(54)所表示的反应而得到的化合物也可以在本发明中使用。
[0191]
作为能够在这样的反应中使用的环氧化物没有特别限定,例如可以举出脂肪族系多官能液态环氧树脂、双酚a型环氧树脂、双酚f型环氧树脂、联苯型环氧树脂、线型酚醛型环氧树脂、甲酚线型酚醛型环氧树脂、双酚衍生物环氧树脂、含有萘骨架或脂环式骨架的酚醛清漆系环氧树脂等,可以举出环氧乙烷环为缩水甘油醚的环氧树脂等。
[0192]
上述环氧化物优选为在1分子中具有2个以上环氧基的化合物。
[0193]
此外,可以如上所述通过对羧酸或其衍生物进行通式(53)所表示的反应而得到环氧化物。
[0194]
并且,可以通过对该环氧化物进行上述通式(51)所表示的反应而得到具有通式(41)所表示的官能团和/或通式(42)所表示的官能团的化合物。
[0195]
因此,通过对各种多元羧酸、羟基羧酸进行上述的反应,能够得到具有这样的官能团的化合物、具有这样的官能团和羟基的化合物。
[0196]
作为在通过上述反应制成具有通式(41)所表示的官能团和/或通式(42)所表示的官能团的化合物时可以作为原料的多元羧酸没有特别限定,例如可以使用碳原子数为50以下的多元羧酸。
[0197]
更具体而言,可以举出作为获得具有上述通式(31)的结构的化合物时的原料所记载的各种多元羧酸和羟基羧酸。
[0198]
此外,还可以举出椰油脂肪酸、棉籽油脂肪酸、麻籽油脂肪酸、米糠油脂肪酸、鱼油脂肪酸、妥尔油脂肪酸、大豆油脂肪酸、亚麻籽油脂肪酸、桐油脂肪酸、菜籽油脂肪酸、蓖麻油脂肪酸、脱水蓖麻油脂肪酸、红花籽油脂肪酸等脂肪酸;月桂酸、肉豆蔻酸、棕榈酸、硬脂酸、油酸、亚油酸、亚麻酸、苯甲酸、对叔丁基苯甲酸、环己烷酸、10
‑
苯基十八烷酸等单羧酸。
[0199]
作为这样的化合物的具体例,例如可以举出具有以下所示结构的化合物。
[0200]
[化24]
[0201][0202]
(a
‑
4)多官能羧酸的烷基酯化物
[0203]
通过多官能羧酸或其衍生物与醇的反应得到的化合物也可以作为本发明的酯化合物(a)使用。这样的反应可以由下述通式表示。
[0204]
[化25]
[0205]
r
1g
‑
(cooh)
n6
n6ho
‑
r1→
r
1g
‑
(coor1)
n6
n6h2o
[0206]
各种多官能羧酸是在聚酯原料、聚酰胺原料、中和剂、合成原料等多种用途中广泛且低成本地提供的通用原料。将这样的多官能羧酸利用公知的方法进行烷基酯化而成的化合物也可以在本发明中使用。酯化可以基于上述碳原子数为50以下的伯烷基或仲烷基来进行。
[0207]
在使用这样的化合物作为酯化合物(a)时,能够利用公知的方法低成本地进行酯化,能够以比较低的分子量引入多元酯基。另外,通过进行酯化,在有机溶剂中的相容性变得良好,能够适当地使用,从这方面出发是优选的。
[0208]
作为此处使用的多官能羧酸没有特别限定,例如可以使用碳原子数为50以下的多官能羧酸。更具体而言,可以举出作为获得具有上述通式(31)的结构的化合物时的原料所记载的各种多元羧酸和羟基羧酸等。
[0209]
本发明中,上述多官能羧酸的烷基酯化的方法没有特别限定,可以应用与醇的脱水缩合等公知的方法。另外,作为原料也可以使用这些化合物的酸酐。
[0210]
在对应于上述(a
‑
1)~(a
‑
4)的化合物中,具有羟基和烷基酯基这两者的化合物具有自交联性,从这方面出发是优选的。通过在同一化合物中同时存在这些官能团,在同一化合物间发生酯交换反应,由此固化性能更为良好。在对应于(a
‑
1)的化合物中,作为在分子中具有羟基的化合物,可以举出以具有羟基的化合物作为原料而得到的对应于(a
‑
1)、(a
‑
2)的各化合物。此外,对应于(a
‑
3)的化合物均相当于具有羟基的化合物。此外,在对应于(a
‑
4)的化合物中,具有羟基的多官能羧酸的烷基酯化物相当于具有羟基的化合物。
[0211]
本发明中,也可以将2种以上的上述化合物(a)合用。
[0212]
本发明中,优选将2官能的化合物(a)和3官能以上的化合物(a)合用。通过采用这样的组成,容易得到作为树脂组合物的低粘度化或相容性提高的效果,还容易提高热固化膜的交联密度,从这方面出发是优选的。这种情况下,关于混合比例,优选以2官能的化合物(a):3官能以上的化合物(a)=1:9~9:1(重量比)的比例进行混合。
[0213]
另外,本发明的热固化性树脂组合物中,相对于羟基数,酯化合物(a)中的酯基可以任意地混配,优选为1%~200%(个数比)。
[0214]
在本发明的热固化性树脂组合物中混配具有2个以上的羟基的化合物(a)的情况下,具有下述优点:作为多元醇,可以直接使用在使用了多异氰酸酯固化剂或三聚氰胺树脂等现有的热固化性树脂组合物中所使用的多元醇。
[0215]
在使用上述化合物(a)的情况下,以下详细说明的多元醇化合物的羟值优选为1~300mgkoh/g。
[0216]
另外,在使用上述(a)的情况下,与其组合使用的多元醇树脂(b)的重均分子量优选为1000~1000000。由此,能够容易地进行涂装等工序,从这方面出发是优选的。上述下限更优选为2000、进一步优选为3000。上述上限更优选为800000、进一步优选为700000。
[0217]
(b)多元醇
[0218]
本发明中,除了上述化合物(a)以外,还含有多元醇(b)。由此,使分子中具有至少2个羟基的化合物(b)与上述酯化合物(a)发生反应,使涂膜高效地固化。
[0219]
作为这样的化合物(b)没有特别限定,可以举出丙烯酸多元醇、聚酯多元醇、聚醚多元醇、聚碳酸酯多元醇、聚氨酯多元醇等。这些之中,也可以同时使用2种以上。其中特别优选使用丙烯酸多元醇和/或聚酯多元醇。此外也可以使用低分子量多元醇。此处使用的丙烯酸多元醇和/或聚酯多元醇可以使用在涂料领域中通用的树脂。另外,上述多元醇(b)也可以为上述具有烷基酯基的聚合物。以下对它们进行详细说明。
[0220]
(b
‑
1)丙烯酸多元醇
[0221]
丙烯酸多元醇例如可以通过将含羟基聚合性不饱和单体(b1)和能够与上述(b1)共聚的其他聚合性不饱和单体(b2)利用公知的方法进行共聚而制造。更具体而言,可以举出有机溶剂中的溶液聚合法、水中的乳液聚合法、水中的细乳液聚合法、水溶液聚合法等聚合方法。
[0222]
含羟基聚合性不饱和单体(b1)是在1分子中分别具有1个以上的羟基和聚合性不饱和键的化合物。作为含羟基聚合性不饱和单体(b1)没有特别限定。作为这样的含羟基乙烯基单体,以下例示出特别具有代表性的物质。2
‑
羟基乙基乙烯基醚、3
‑
羟基丙基乙烯基
醚、2
‑
羟基丙基乙烯基醚、4
‑
羟基丁基乙烯基醚、3
‑
羟基丁基乙烯基醚、2
‑
羟基
‑2‑
甲基丙基乙烯基醚、5
‑
羟基戊基乙烯基醚或6
‑
羟基己基乙烯基醚之类的各种含有羟基的乙烯基醚类;或者上述这些各种乙烯基醚与ε
‑
己内酯的加成反应产物;2
‑
羟基乙基(甲基)烯丙基醚、3
‑
羟基丙基(甲基)烯丙基醚、2
‑
羟基丙基(甲基)烯丙基醚、4
‑
羟基丁基(甲基)烯丙基醚、3
‑
羟基丁基(甲基)烯丙基醚、2
‑
羟基
‑2‑
甲基丙基(甲基)烯丙基醚、5
‑
羟基戊基(甲基)烯丙基醚或6
‑
羟基己基(甲基)烯丙基醚之类的各种含有羟基的烯丙基醚;或者上述这些各种烯丙基醚与ε
‑
己内酯的加成反应产物;或者(甲基)丙烯酸
‑2‑
羟基乙酯、(甲基)丙烯酸
‑2‑
羟基丙酯、(甲基)丙烯酸
‑3‑
羟基丙酯、(甲基)丙烯酸
‑2‑
羟基丁酯、(甲基)丙烯酸
‑3‑
羟基丁酯、(甲基)丙烯酸
‑4‑
羟基丁酯、聚乙二醇单(甲基)丙烯酸酯或聚丙二醇单(甲基)丙烯酸酯之类的各种含有羟基的(甲基)丙烯酸酯类;或者上述这些各种(甲基)丙烯酸酯与ε
‑
己内酯的加成反应主成分等。
[0223]
上述丙烯酸多元醇具有烷基酯基的情况下,优选为容易发生酯交换反应的烷基酯基。以下详细说明这样的烷基酯基。上述丙烯酸多元醇具有烷基酯基的情况下,优选为以下述通式(4)所表示的单体作为部分或全部结构单元的聚合物。
[0224]
[化26]
[0225][0226]
n1:1~10(式中,r4、r5、r6相同或不同,表示氢、烷基、羧基、烷基酯基或下述r7‑
[coor8]n1所表示的结构。r7为脂肪族、脂环族或芳香族亚烷基,该脂肪族、脂环族或芳香族亚烷基的主链的原子数为50以下,主链中可以具有选自由酯基、醚基、酰胺基、氨基甲酸酯基组成的组中的1种或2种以上的官能团,该脂肪族、脂环族或芳香族亚烷基可以具有侧链。r8是碳原子数50以下的烷基。上述通式(4)所表示的化合物中,r7‑
[coor8]n1基可以为下述通式(4
‑
1)的内酯结构。)
[0227]
[化27]
[0228][0229]
(rx是可以具有支链的碳原子数2~10的烃基)
[0230]
上述通式(4)所表示的单体为具有伯烷基酯或仲烷基酯的单体。来自这样的单体的伯烷基酯基或仲烷基酯基容易与羟基发生反应,因此能够充分实现本发明的目的。
[0231]
这样的化合物可以通过利用不饱和键进行聚合反应而得到聚合物。在将这样得到的聚合物用于以酯交换反应作为固化反应的热固化性树脂组合物的情况下,基于不饱和键的聚合而形成的主链与烷基酯基藉由连接基团而分开地存在。因此,烷基酯基能够比较自由地活动。因此,本发明人发现,烷基酯基与羟基容易接近,酯交换的反应性提高。这样,通
过提高酯交换反应的反应性,能够实现短时间固化和固化温度的降低,能够提高基于酯交换反应的热固化性树脂组合物的有用性。
[0232]
另外,在烷基酯基为叔丁基酯基的情况下,在加热固化时产生气体成分。推测叔丁基通过脱离反应而成为异丁烯,可知由此会在固化树脂中产生气泡,可能产生外观劣化、强度降低等各种问题。本发明中,由于具有伯烷基酯或仲烷基酯,因此可改善这样的问题。需要说明的是,从这样的方面考虑,本发明中的组合物优选不具有叔丁基,但也可以在不产生上述问题的范围内具有叔丁基。
[0233]
推测在使用上述本发明的含有不饱和基团的酯化合物时,通过降低固化中的涂膜粘度而抑制发泡,大幅改善上述问题。从这方面考虑,本发明也具有合适的效果。
[0234]
上述含有不饱和基团的酯化合物中,烷基酯基只要是伯烷基酯基或仲烷基酯基就没有限定。
[0235]
作为上述烷基酯基的烷基没有特别限定,可以使用具有甲基、乙基、苄基、正丙基、异丙基、正丁基、异丁基、仲丁基等公知的烷基的化合物。需要说明的是,烷基优选碳原子数为50以下。上述烷基优选在酯交换反应中生成为醇而挥散,因此,作为烷基,更优选碳原子数为20以下,进一步优选为10以下。另外,在固化反应中挥发的醇的沸点优选为300℃以下、进一步优选为200℃以下。
[0236]
上述烷基酯基中的烷基(即,上述通式中的r5)是碳原子数为50以下的烷基,更优选碳原子数为1~20的范围内,进一步优选为1~10的范围内,进一步优选为1~6的范围内。最优选为1~4的范围内。通过为这样的范围内,能够适当地进行固化反应,从这方面考虑是优选的。
[0237]
另外,上述烷基酯基为内酯基的情况也包含在本发明中。这种内酯基的酯基也能够发生本发明的酯交换反应,能够用于固化反应。这样的化合物具有上述(4
‑
1)的化学结构。作为上述通式(4)所表示的结构,更具体而言,可例示出例如下述通式所表示的结构。
[0238]
[化28]
[0239][0240]
n2:1~10(式中,r9为h或甲基。r
10
为亚烷基,该亚烷基的主链的原子数为48以下,主链中可以具有酯基、醚基和/或酰胺基,该亚烷基可以具有侧链。r1为伯烷基或仲烷基。)。这样的化合物为(甲基)丙烯酸的衍生物,可以使用(甲基)丙烯酸或其衍生物作为原料通过公知的合成方法而得到。
[0241]
上述r1的主链的原子数更优选为40以下,进一步优选为30以下,进一步优选为20以下。作为r
10
的主链中可以含有的原子没有特别限定,除了碳原子以外,也可以具有氧原子、氮原子、硫原子、硅原子等。更具体而言,在r
10
的主链中,除了烷基以外,也可以具有醚基、酯基、氨基、酰胺基、硫醚基、磺酸酯基、硫酯基、硅氧烷基等。
[0242]
以下作为(b
‑1‑
1)~(b
‑1‑
4)示出上述通式(5)所表示的化合物的具体例。
[0243]
(b
‑1‑
1)
[0244]
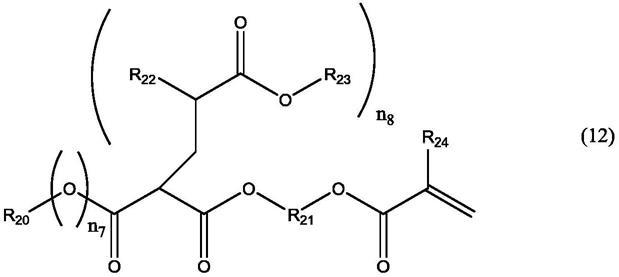
作为上述通式(5)所表示的结构,更具体而言,例如可以举出下述通式(12)所表示的化合物等。
[0245]
[化29]
[0246][0247]
(式中,r
20
是碳原子数1~50的烷基。r
21
为亚烷基,该亚烷基的主链的原子数为44以下,主链中可以具有酯基、醚基和/或酰胺基,该亚烷基可以具有侧链。r
22
为h或甲基。r
23
为伯烷基或仲烷基。r
24
为h或甲基。n7为0或1。n8为1或2。)
[0248]
上述通式(12)所表示的化合物是通过在分子中具有不饱和键的丙二酸酯、乙酰乙酸酯等产生活性阴离子的化合物与具有烷基酯基的不饱和化合物的反应而合成的化合物。
[0249]
即,丙二酸酯、乙酰乙酸酯具有被羧基碳夹着的亚甲基,该亚甲基容易被阴离子化,作为容易产生阴离子反应的物质而广为人知。通过使在这样的丙二酸酯、乙酰乙酸酯的烷基中具有不饱和键的化合物(例如,丙二酸或乙酰乙酸与下文中作为“含有羟基的单体”进行详细说明的具有羟基的不饱和单体的酯化合物)与具有不饱和基团的烷基酯化合物反应,能够合成具有不饱和基团和烷基酯基这两种基团的化合物。
[0250]
对于具有这种结构的化合物,使用广泛通用的原料能够容易地仅变更烷基酯基,结果,能够容易地调节固化反应性。另外,通过改变活性亚甲基的反应率也能够调节固化反应性,从这方面考虑是特别优选的。
[0251]
能够用作在上述反应中使用的“具有不饱和基团的烷基酯化合物”的化合物没有特别限定,可以使用(甲基)丙烯酸烷基酯、亚甲基丙二酸烷基酯、具有不饱和基团的内酯化合物(例如,γ
‑
巴豆酰内酯、5,6
‑
二氢
‑
2h
‑
吡喃
‑2‑
酮)等。
[0252]
该反应可以在碱性条件下进行,例如可以通过在碱金属盐的冠醚存在下的有机溶剂中的反应等来进行。以下示出这样的合成反应的一例。
[0253]
[化30]
[0254][0255]
(b
‑1‑
2)上述通式(5)所表示的烷基酯化合物也可以通过该化合物所对应的羧酸的酯化而得到。即,下述通式(5
‑
1)所表示的化合物为上述通式(5)所表示的烷基酯化合物所对应的羧酸。
[0256]
[化31]
[0257][0258]
n2:1~10(式中,r9为h或甲基。r
10
为亚烷基,该亚烷基的主链的原子数为48以下,主链中可以具有酯基、醚基和/或酰胺基,该亚烷基可以具有侧链。)
[0259]
作为上述通式(5
‑
1)所表示的化合物,存在公知的化合物。通过对这样的公知的化合物进行通常的酯化反应(例如,与目标烷基酯的烷基所对应的醇的反应),也能够制成本发明的含有不饱和基团的酯化合物。
[0260]
以下示出可通过以上例示的方法合成的化合物的具体的化学结构的示例。需要说明的是,本发明并不限定于以下例示的化合物。
[0261]
[化32]
[0262][0263]
(上述通式中,r表示伯烷基或仲烷基)
[0264]
上述通式所表示的化合物中,通式中的r也是碳原子数为50以下的烷基,更优选碳原子数为1~20的范围内,进一步优选为1~10的范围内,进一步优选为1~6的范围内。最优选为1~4的范围内。通过为这样的范围内,能够适当地进行固化反应,从这方面考虑是优选的。
[0265]
(b
‑1‑
3)
[0266]
上述通式(5)所表示的化合物可以为具有下述通式(31)所表示的官能团和不饱和基团的化合物。
[0267]
[化33]
[0268][0269]
n=0~20
[0270]
r1为碳原子数50以下的烷基。
[0271]
r3为氢或碳原子数10以下的烷基。
[0272]
即,可以使用(a
‑
2)中详细说明的具有通式(31)所表示的结构和不饱和基团的化合物。
[0273]
具体而言,例如使上述通式(32)所表示的化合物与(甲基)丙烯酸反应时,可得到下述通式(36)所表示的化合物。
[0274]
[化34]
[0275][0276]
(式中,r1为碳原子数50以下的烷基。
[0277]
r2为氢或甲基。
[0278]
n为1~20)
[0279]
此外,可以使用通过使具有各种不饱和基团的化合物与上述通式(32)所表示的化合物反应而得到的化合物。
[0280]
(b
‑1‑
4)
[0281]
上述通式(5)所表示的化合物可以为具有下述通式(41)所表示的官能团和/或下述通式(42)所表示的官能团以及不饱和基团的化合物。
[0282]
[化35]
[0283][0284]
[化36]
[0285][0286]
(上述通式(41)、通式(42)的任一者中,r1均为碳原子数50以下的烷基。
[0287]
r2是可以在一部分包含氧原子、氮原子的碳原子数50以下的亚烷基)
[0288]
即,通式(5)所表示的化合物中,coor8基可以具有上述通式(41)所表示的结构和/或通式(42)所表示的结构。
[0289]
上述烷基酯基中的烷基(即上述通式中的r1)是碳原子数为50以下的烷基,更优选碳原子数为1~20的范围内,进一步优选为1~10的范围内,进而优选为1~6的范围内。最优选为1~4的范围内。通过为这样的范围内,能够适当地进行固化反应,从这方面出发是优选的。
[0290]
作为上述烷基,具体而言,可以使用例如具有甲基、乙基、苄基、正丙基、异丙基、正丁基、异丁基、仲丁基等公知的烷基的化合物。
[0291]
上述通式(41)中的r2基是可以在一部分包含氧原子、氮原子的碳原子数50以下的亚烷基,具体而言,可以包含亚甲基、亚乙基、正亚丙基、异亚丙基、正亚丁基或苯环、环己基环之类的环状结构(碳链1~50)。其中,从原料成本低、反应性优异的方面出发,特别优选为亚乙基。
[0292]
作为具有上述通式(41)所表示的结构的化合物,例如可以举出下述通式(43)所表示的化合物。
[0293]
[化37]
[0294][0295]
(式中,r1为碳原子数50以下的烷基。
[0296]
r2是可以在一部分包含氧原子、氮原子的碳原子数50以下的亚烷基。
[0297]
r3为氢或甲基。)
[0298]
上述通式(43)所表示的酯化合物中,更优选下述通式(45)所表示的酯化合物。
[0299]
[化38]
[0300][0301]
作为能够与含有羟基的聚合性不饱和单体(b1)共聚的其他聚合性不饱和单体
(b2),例如可以举出下述单体(i)~(xix)等、以及它们的任意组合。
[0302]
(i)(甲基)丙烯酸烷基酯或(甲基)丙烯酸环烷基酯:例如(甲基)丙烯酸甲酯、(甲基)丙烯酸乙酯、(甲基)丙烯酸正丙酯、(甲基)丙烯酸异丙酯、(甲基)丙烯酸正丁酯、(甲基)丙烯酸异丁酯、(甲基)丙烯酸叔丁酯、(甲基)丙烯酸正己酯、(甲基)丙烯酸正辛酯、(甲基)丙烯酸
‑2‑
乙基已酯、(甲基)丙烯酸壬酯、(甲基)丙烯酸十三烷基酯、(甲基)丙烯酸月桂酯、(甲基)丙烯酸硬脂酯、(甲基)丙烯酸异硬脂酯、(甲基)丙烯酸环己酯、(甲基)丙烯酸甲基环己酯、(甲基)丙烯酸叔丁基环己酯、(甲基)丙烯酸环十二烷基酯、甲基丙烯酸三环癸基酯等
[0303]
(ii)具有异冰片基的聚合性不饱和单体:(甲基)丙烯酸异冰片酯等
[0304]
(iii)具有金刚烷基的聚合性不饱和单体:(甲基)丙烯酸金刚烷基酯等
[0305]
(iv)具有三环癸烯基的聚合性不饱和单体:(甲基)丙烯酸三环癸烯酯等
[0306]
(v)含有芳香环的聚合性不饱和单体:(甲基)丙烯酸苄酯、苯乙烯、α
‑
甲基苯乙烯、乙烯基甲苯等
[0307]
(vi)具有烷氧基甲硅烷基的聚合性不饱和单体:乙烯基三甲氧基硅烷、乙烯基三乙氧基硅烷、乙烯基三(2
‑
甲氧基乙氧基)硅烷、γ
‑
(甲基)丙烯酰氧基丙基三甲氧基硅烷、γ
‑
(甲基)丙烯酰氧基丙基三乙氧基硅烷等
[0308]
(vii)具有氟化烷基的聚合性不饱和单体:(甲基)丙烯酸全氟丁基乙酯、(甲基)丙烯酸全氟辛基乙酯等(甲基)丙烯酸全氟烷基酯;氟代烯烃等
[0309]
(viii)具有马来酰亚胺基等光聚合性官能团的聚合性不饱和单体
[0310]
(ix)乙烯基化合物:n
‑
乙烯基吡咯烷酮、乙烯、丁二烯、氯丁二烯、丙酸乙烯酯、乙酸乙烯酯等
[0311]
(x)含有羧基的聚合性不饱和单体:(甲基)丙烯酸、马来酸、巴豆酸、丙烯酸
‑
β
‑
羧基乙酯等
[0312]
(xi)含氮聚合性不饱和单体:(甲基)丙烯腈、(甲基)丙烯酰胺、(甲基)丙烯酸
‑
n,n
‑
二甲氨基乙酯、(甲基)丙烯酸
‑
n,n
‑
二乙氨基乙酯、n,n
‑
二甲氨基丙基(甲基)丙烯酰胺、亚甲基双(甲基)丙烯酰胺、亚乙基双(甲基)丙烯酰胺、(甲基)丙烯酸缩水甘油酯与胺化合物的加成物等
[0313]
(xii)在1分子中具有2个以上的聚合性不饱和基团的聚合性不饱和单体:(甲基)丙烯酸烯丙酯、1,6
‑
己二醇二(甲基)丙烯酸酯等
[0314]
(xiii)含有环氧基的聚合性不饱和单体:(甲基)丙烯酸缩水甘油酯、(甲基)丙烯酸
‑
β
‑
甲基缩水甘油酯、(甲基)丙烯酸
‑
3,4
‑
环氧环己基甲酯、(甲基)丙烯酸
‑
3,4
‑
环氧环己基乙酯、(甲基)丙烯酸
‑
3,4
‑
环氧环己基丙酯、烯丙基缩水甘油醚等
[0315]
(xiv)具有分子末端为烷氧基的聚氧乙烯链的(甲基)丙烯酸酯
[0316]
(xv)具有磺酸基的聚合性不饱和单体:2
‑
丙烯酰胺
‑2‑
甲基丙磺酸、(甲基)丙烯酸
‑2‑
磺基乙酯、烯丙基磺酸、4
‑
苯乙烯磺酸等;这些磺酸的钠盐和铵盐等
[0317]
(xvi)具有磷酸基的聚合性不饱和单体:酸性磷酰氧基乙基(甲基)丙烯酸酯、酸性磷酰氧基丙基(甲基)丙烯酸酯、酸性磷酰氧基聚(氧亚乙基)二醇(甲基)丙烯酸酯、酸性磷酰氧基聚(氧亚丙基)二醇(甲基)丙烯酸酯等
[0318]
(xvii)具有紫外线吸收性官能团的聚合性不饱和单体:2
‑
羟基
‑4‑
(3
‑
甲基丙烯酰氧基
‑2‑
羟基丙氧基)二苯甲酮、2
‑
羟基
‑4‑
(3
‑
丙烯酰氧基
‑2‑
羟基丙氧基)二苯甲酮、2,2
’‑
二羟基
‑4‑
(3
‑
甲基丙烯酰氧基
‑2‑
羟基丙氧基)二苯甲酮、2,2
’‑
二羟基
‑4‑
(3
‑
丙烯酰氧基
‑2‑
羟基丙氧基)二苯甲酮、2
‑
(2
’‑
羟基
‑5’‑
甲基丙烯酰氧基乙基苯基)
‑
2h
‑
苯并三唑等
[0319]
(xviii)紫外线稳定性聚合性不饱和单体:4
‑
(甲基)丙烯酰氧基
‑
1,2,2,6,6
‑
五甲基哌啶、4
‑
(甲基)丙烯酰氧基
‑
2,2,6,6
‑
四甲基哌啶、4
‑
氰基
‑4‑
(甲基)丙烯酰氨基
‑
2,2,6,6
‑
四甲基哌啶、1
‑
(甲基)丙烯酰基
‑4‑
(甲基)丙烯酰氨基
‑
2,2,6,6
‑
四甲基哌啶、1
‑
(甲基)丙烯酰基
‑4‑
氰基
‑4‑
(甲基)丙烯酰氨基
‑
2,2,6,6
‑
四甲基哌啶、4
‑
巴豆酰氧基
‑
2,2,6,6
‑
四甲基哌啶、4
‑
巴豆酰氨基
‑
2,2,6,6
‑
四甲基哌啶、1
‑
巴豆酰基
‑4‑
巴豆酰氧基
‑
2,2,6,6
‑
四甲基哌啶等
[0320]
(xix)具有羰基的聚合性不饱和单体:丙烯醛、双丙酮丙烯酰胺、双丙酮甲基丙烯酰胺、甲基丙烯酸乙酰乙酰氧基乙酯、甲酰基苯乙烯、碳原子数为约4~约7的乙烯基烷基酮(例如,乙烯基甲基酮、乙烯基乙基酮、乙烯基丁基酮)等
[0321]
本说明书中,“聚合性不饱和基团”是指可进行自由基聚合或离子聚合的不饱和基团。作为上述聚合性不饱和基团,可以举出例如乙烯基、(甲基)丙烯酰基等。
[0322]
关于制造丙烯酸多元醇(b
‑
1)时的含有羟基的聚合性不饱和单体(b1)的比例,以单体成分的总量为基准,优选为0.5~50重量%。通过为这样的范围内,能够产生适度的交联反应,能够得到优异的涂膜物性。上述下限更优选为1.0重量%,进一步优选为1.5重量%。上述上限更优选为40重量%。
[0323]
从所形成的涂膜的耐水性等方面考虑,丙烯酸多元醇(b
‑
1)的羟值优选为1~200mgkoh/g。上述下限更优选为2mgkoh/g、进一步优选为5mgkoh/g。上述上限更优选为180mgkoh/g、进一步优选为170mgkoh/g。
[0324]
作为这样的丙烯酸多元醇(b
‑
1),也可以使用市售品。作为市售品没有特别限定,例如可以举出dic株式会社制品acrydica
‑
801
‑
p、a
‑
817、a
‑
837、a
‑
848
‑
rn、a
‑
814、57
‑
773、a
‑
829、55
‑
129、49
‑
394
‑
im、a
‑
875
‑
55、a
‑
870、a
‑
871、a
‑
859
‑
b、52
‑
668
‑
ba、wzu―591、wxu
‑
880、bl
‑
616、cl
‑
1000、cl
‑
408等。
[0325]
(b
‑
2)聚酯多元醇
[0326]
聚酯多元醇(b
‑
2)通常可以通过酸成分与醇成分的酯化反应或酯交换反应来制造。作为上述酸成分,可以举出在制造聚酯树脂时作为酸成分通常使用的化合物。作为上述酸成分,可以举出例如脂肪族多元酸、脂环族多元酸、芳香族多元酸等以及它们的酸酐和酯化物。
[0327]
作为上述脂肪族多元酸以及它们的酸酐和酯化物,通常可以举出在1分子中具有2个以上的羧基的脂肪族化合物、上述脂肪族化合物的酸酐和上述脂肪族化合物的酯化物,例如琥珀酸、戊二酸、己二酸、庚二酸、辛二酸、壬二酸、癸二酸、十一烷二酸、十二烷二酸、巴西基酸、十八烷二酸、柠檬酸、丁烷四羧酸等脂肪族多元羧酸;上述脂肪族多元羧酸的酸酐;上述脂肪族多元羧酸的碳原子数为约1~约4的低级烷基的酯化物等;以及它们的任意组合。作为上述脂肪族多元酸,从所得到的涂膜的平滑性的方面出发,优选为己二酸和/或己二酸酐。
[0328]
上述脂环族多元酸、以及它们的酸酐和酯化物通常可以举出在1分子中具有1个以上的脂环式结构和2个以上的羧基的化合物、上述化合物的酸酐和上述化合物的酯化物。脂环式结构主要为4~6元环结构。作为上述脂环族多元酸、以及它们的酸酐和酯化物,可以举
出例如1,2
‑
环己烷二羧酸、1,3
‑
环己烷二羧酸、1,4
‑
环己烷二羧酸、4
‑
环己烯
‑
1,2
‑
二羧酸、3
‑
甲基
‑
1,2
‑
环己烷二羧酸、4
‑
甲基
‑
1,2
‑
环己烷二羧酸、1,2,4
‑
环己烷三羧酸、1,3,5
‑
环己烷三羧酸等脂环族多元羧酸;上述脂环族多元羧酸的酸酐;上述脂环族多元羧酸的碳原子数为约1~约4的低级烷基的酯化物等、以及它们的任意组合。
[0329]
作为上述脂环族多元酸、以及它们的酸酐和酯化物,从所得到的涂膜的平滑性的方面考虑,优选1,2
‑
环己烷二羧酸、1,2
‑
环己烷二羧酸酐、1,3
‑
环己烷二羧酸、1,4
‑
环己烷二羧酸、4
‑
环己烯
‑
1,2
‑
二羧酸、4
‑
环己烯
‑
1,2
‑
二羧酸酐,并且更优选1,2
‑
环己烷二羧酸和/或1,2
‑
环己烷二羧酸酐。
[0330]
上述芳香族多元酸、以及它们的酸酐和酯化物通常是在1分子中具有2个以上羧基的芳香族化合物、上述芳香族化合物的酸酐和上述芳香族化合物的酯化物,例如可以举出邻苯二甲酸、间苯二甲酸、对苯二甲酸、萘二甲酸、4,4
’‑
联苯二羧酸、偏苯三酸、均苯四酸等芳香族多元羧酸;上述芳香族多元羧酸的酸酐;上述芳香族多元羧酸的碳原子数为约1~约4的低级烷基的酯化物等、以及它们的任意组合。作为上述芳香族多元酸、以及它们的酸酐和酯化物,优选邻苯二甲酸、邻苯二甲酸酐、间苯二甲酸、偏苯三酸和偏苯三酸酐。
[0331]
另外,作为上述酸成分,可以举出上述脂肪族多元酸、脂环族多元酸和芳香族多元酸以外的酸成分,例如椰油脂肪酸、棉籽油脂肪酸、麻籽油脂肪酸、米糠油脂肪酸、鱼油脂肪酸、妥尔油脂肪酸、大豆油脂肪酸、亚麻籽油脂肪酸、桐油脂肪酸、菜籽油脂肪酸、蓖麻油脂肪酸、脱水蓖麻油脂肪酸、红花籽油脂肪酸等脂肪酸;月桂酸、肉豆蔻酸、棕榈酸、硬脂酸、油酸、亚油酸、亚麻酸、苯甲酸、对叔丁基苯甲酸、环己甲酸、10
‑
苯基十八烷酸等单羧酸;乳酸、3
‑
羟基丁酸、3
‑
羟基
‑4‑
乙氧基苯甲酸等羟基羧酸等、以及它们的任意组合。
[0332]
作为上述醇成分,可以举出在1分子中具有2个以上的羟基的多元醇,例如乙二醇、丙二醇、二乙二醇、1,3
‑
丙二醇、四乙二醇、三乙二醇、二丙二醇、1,4
‑
丁二醇、1,3
‑
丁二醇、2,3
‑
丁二醇、1,2
‑
丁二醇、2
‑
甲基
‑
1,3
‑
丙二醇、3
‑
甲基
‑
1,2
‑
丁二醇、1,1,1
‑
三羟甲基丙烷、2
‑
丁基
‑2‑
乙基
‑
1,3
‑
丙二醇、1,2
‑
戊二醇、1,5
‑
戊二醇、1,4
‑
戊二醇、2,4
‑
戊二醇、2,3
‑
二甲基1,3
‑
丙二醇、四亚甲基二醇、3
‑
甲基
‑
4,3
‑
戊二醇、3
‑
甲基
‑
1,5
‑
戊二醇、2,2,4
‑
三甲基
‑
1,3
‑
戊二醇、1,6
‑
己二醇、1,5
‑
己二醇、1,4
‑
己二醇、2,5
‑
己二醇、新戊二醇、1,4
‑
环己烷二甲醇、三环癸烷二甲醇、羟基特戊酸新戊二醇酯、氢化双酚a、氢化双酚f、二羟甲基丙酸等2元醇;在上述2元醇上加成ε
‑
己内酯等内酯化合物而成的聚内酯二醇;对苯二甲酸双(羟基乙酯)等酯二醇化合物;双酚a的环氧烷加成物、聚乙二醇、聚丙二醇、聚丁二醇等聚醚二醇化合物;甘油、三羟甲基乙烷、三羟甲基丙烷、二甘油、三甘油、1,2,6
‑
己三醇、季戊四醇、二季戊四醇、三(2
‑
羟基乙基)异氰脲酸酯、山梨醇、甘露醇等3元以上的醇;在上述3元以上的醇上加成ε
‑
己内酯等内酯化合物而成的聚内酯多元醇化合物;甘油的脂肪酸酯化物等。
[0333]
另外,作为上述醇成分,可以举出上述多元醇以外的醇成分,例如甲醇、乙醇、丙醇、丁醇、硬脂醇、2
‑
苯氧基乙醇等一元醇;使环氧丙烷、环氧丁烷、“cardura e10”(商品名、hexion specialty chemicals公司制、合成高支化饱和脂肪酸的缩水甘油酯)等单环氧化合物与酸反应而得到的醇化合物等。
[0334]
聚酯多元醇(b
‑
2)没有特别限定,可以按照通常的方法进行制造。例如,将上述酸成分和醇成分在氮气气流中在约150℃~约250℃下加热约5小时~约10小时,实施上述酸成分与醇成分的酯化反应或酯交换反应,由此能够制造聚酯多元醇(b
‑
2)。
[0335]
上述聚酯多元醇也可以使用市售的树脂。作为可以使用的市售的聚酯树脂,可以举出arakyd系列(商品名、荒川化学工业公司制造)、vylon系列(商品名、东洋纺公司制造)、beckolite系列(dic公司制造)、adekanewace系列(adeka公司制造)等。
[0336]
上述多元醇(b)为上述的丙烯酸多元醇、聚酯多元醇的情况下,其分子量没有特别限定,例如优选重均分子量为3,000~300,000。上述多元醇(b)的重均分子量的上限更优选为100,000、进一步优选为50,000、进而优选为30,000。上述多元醇(b)的重均分子量的下限进一步优选为5,000。
[0337]
(b
‑
3)低分子量多元醇
[0338]
作为可以在本发明中使用的多元醇(b),还可以举出具有2个以上的羟基的低分子量多元醇化合物。作为此处可以使用的低分子量多元醇化合物没有特别限定,例如可以举出乙二醇、丙二醇、二乙二醇、1,3
‑
丙二醇、四乙二醇、三乙二醇、二丙二醇、1,4
‑
丁二醇、1,3
‑
丁二醇、2,3
‑
丁二醇、1,2
‑
丁二醇、2
‑
甲基
‑
1,3
‑
丙二醇、3
‑
甲基
‑
1,2
‑
丁二醇、1,1,1
‑
三羟甲基丙烷、2
‑
丁基
‑2‑
乙基
‑
1,3
‑
丙二醇、1,2
‑
戊二醇、1,5
‑
戊二醇、1,4
‑
戊二醇、2,4
‑
戊二醇、2,3
‑
二甲基
‑
1,3
‑
丙二醇、四亚甲基二醇、3
‑
甲基
‑
4,3
‑
戊二醇、3
‑
甲基
‑
1,5
‑
戊二醇、2,2,4
‑
三甲基
‑
1,3
‑
戊二醇、1,6
‑
己二醇、1,5
‑
己二醇、1,4
‑
己二醇、2,5
‑
己二醇、新戊二醇、1,4
‑
环己烷二甲醇、三环癸烷二甲醇、羟基特戊酸新戊二醇酯、氢化双酚a、氢化双酚f、二羟甲基丙酸等2元醇;在上述2元醇上加成ε
‑
己内酯等内酯化合物而成的聚内酯二醇;对苯二甲酸双(羟基乙酯)等酯二醇化合物;双酚a的环氧烷加成物、聚乙二醇、聚丙二醇、聚丁二醇等聚醚二醇化合物;甘油、三羟甲基乙烷、三羟甲基丙烷、双甘油、三甘油、1,2,6
‑
己烷三醇、季戊四醇、二季戊四醇、三(2
‑
羟基乙基)异氰脲酸酯、山梨糖醇、甘露醇、环糊精、纤维素等3元以上的醇等。需要说明的是,此处所说的“低分子量多元醇”是指分子量为3000以下的多元醇。此处的分子量为通过nmr、质谱等通用的化学分析明确化学结构并根据该化学结构而计算出的值。上述分子量更优选为2500以下、最优选为2000以下。另外,羟基最优选立体位阻的影响小的伯羟基。
[0339]
使用了这样的低分子量多元醇的热固化性树脂组合物中,所使用的成分的低分子多元醇作为通用品而已知,能够以低成本获得。此外,低分子多元醇的水溶性强,在以水系中的固化为目的的情况下,可作为交联剂而适当使用。近年来呼吁重视环境问题,为了推进voc的降低、实现高固体化,可以作为非常重要的交联剂而适当使用。
[0340]
本发明的热固化性树脂组合物中,相对于组合物总量(固体物质换算),优选以1~99重量%的比例含有多元醇(b)。上述含量的下限更优选为5重量%、进一步优选为10重量%。上述含量的上限更优选为90重量%、进一步优选为80重量%。
[0341]
作为上述多元醇(b),可以将丙烯酸多元醇、聚酯多元醇之类的树脂与低分子量多元醇合用。特别是使用分子量低的物质作为上述(a)成分的情况下,优选合用丙烯酸多元醇(b
‑
1)和/或聚酯多元醇(b
‑
2)以及低分子量多元醇(b
‑
3)。通过使用低分子量多元醇,能够在低分子量的(a)成分间生成交联链,由此能够得到高交联密度的固化物,由此能够提高固化物的物性,从这方面出发是优选的。此外,能够提高组合物整体中的低分子量成分的含量。因此,能够使组合物的粘度为低粘度。例如,在将本发明的热固化性树脂组合物制成涂料组合物的情况下,需要调整为能够进行喷雾涂装的粘度。这种情况下,为了达到最佳粘度,通常添加有机溶剂。若能够如上所述使热固化性树脂组合物的粘度为低粘度化,则具有
能够实现组合物的高固体化、由此能够降低溶剂的用量的优点。
[0342]
另外,将聚酯多元醇与上述(a)成分组合而成的热固化性树脂组合物能够形成挠性、光泽性、密合性优异的被膜,从这方面出发是优选的。
[0343]
将上述丙烯酸多元醇(b
‑
1)和/或上述聚酯多元醇(b
‑
2)与低分子量多元醇(b
‑
3)合用的情况下,关于混合比例,(b
‑
3)相对于[(b
‑
1)与(b
‑
2)的总量]的重量%优选为0.5~50的范围内。通过为这样的范围内,可得到良好的固化性能,从这方面出发是特别优选的。
[0344]
本发明中,在将上述化合物(a)与多元醇(b)混合的状态下,羟基与烷基酯基之比优选为1:100~100:1。通过为这样的比例,可得到良好的固化性,从这方面出发是优选的。
[0345]
(c)酯交换催化剂
[0346]
本发明的热固化型树脂组合物含有酯交换催化剂(c)。即,为了高效地发生酯基与羟基之间的酯交换反应、得到充分的热固化性,混配有酯交换催化剂(c)。
[0347]
作为上述酯交换催化剂(c),可以使用作为能够活化酯交换反应的酯交换催化剂所公知的任意化合物。
[0348]
具体而言,例如可以举出盐酸、硫酸、硝酸、乙酸、磷酸或磺酸、杂多酸等各种酸性化合物;lioh、koh或naoh、胺类、膦类等各种碱性化合物;pbo、氧化镁、乙酸锌、丙烯酸锌、乙酰丙酮锌、氧化锌、乙酸铅、乙酸锰、乙酸铜、乙酸镍、乙酸钯、异丙醇铝、氧化铝、乙酰丙酮锆、氧化锆、氯化铁、氯化钴、氯化钯、二硫代氨基甲酸锌、三氧化锑、钛酸四异丙酯、氧化钛、二月桂酸二丁基锡、二辛酸二丁基锡、二乙酸二辛基锡、单丁基氧化锡或单丁基锡酸等各种金属化合物;四甲基氯化铵、十二烷基三甲基溴化铵、三乙基苄基氯化铵、四甲基氢氧化铵、三甲基苄基甲基碳酸铵等季铵盐等;四丁基溴化鏻、四丁基氢氧化鏻等鏻盐等;1,8
‑
二氮杂双环[5.4.0]十一碳
‑7‑
烯等强碱等。另外,还可以使用通过光或热而产生酸的光响应性催化剂、热潜催化剂。此外,还可以使用锌簇催化剂(例如东京化成工业株式会社制造的zntac24(商品名))等。
[0349]
此外,上述化合物中,也可以将2种以上合用。
[0350]
本发明中,作为酯交换催化剂,最优选使用金属化合物催化剂。该金属化合物催化剂可以通过选择金属种类、与其他化合物合用等而得到酯交换反应性。此外,通过与树脂组成的组合能够适当地得到所需要的性能,从这方面出发是优选的。
[0351]
上述金属化合物催化剂优选为包含选自由锌、锡、钛、铝、锆和铁组成的组中的至少1种金属元素的化合物(c
‑
1)。这样的化合物具有适当的酯交换反应性,从这方面出发是优选的。
[0352]
作为上述金属化合物,在使用金属乙酰丙酮化物作为阴离子成分时,具有可得到比同种金属化合物更优异的酯交换能力的倾向,从这方面出发是优选的。例如可以特别优选使用乙酰丙酮锌、乙酰丙酮锆。
[0353]
使用上述金属化合物作为催化剂的情况下,在进一步合用选自由有机磷化合物、脲、烷基化脲、亚砜化合物、吡啶和吡啶衍生物组成的组中的至少1种化合物(c
‑
2)时,催化性能提高,从这方面出发更为优选。
[0354]
在使用通过合用这些化合物而被活化的金属化合物时,能够得到上述固化开始温度和凝胶分数,从这方面出发是特别优选的。
[0355]
得到这样的效果的作用尚不明确,据推测,通过该化合物(c
‑
2)配位在金属化合物
上,提高了催化活性。因此,作为化合物(c
‑
2),优选选择能够配位在金属化合物上的化合物。
[0356]
作为上述有机磷化合物没有特别限定,例如可以举出磷酸、亚磷酸、膦酸、次膦酸、亚膦酸、有机氧化膦、有机膦化合物以及它们的各种酯、酰胺和盐。酯可以为烷基、支链烷基、取代烷基、二官能性烷基、烷基醚、芳基以及取代芳基的酯。酰胺可以为烷基、支链烷基、取代烷基、二官能性烷基、烷基醚、芳基以及取代芳基的酰胺。
[0357]
这些之中,特别优选为选自由膦酸酯、磷酸酰胺和有机氧化膦化合物组成的组中的至少1种化合物。在使用这些有机磷化合物时,酯交换催化功能最好。更具体而言,可以优选使用三苯基氧化膦、三辛基氧化膦、三环己基氧化膦等有机氧化膦化合物;六甲基磷酸三酰胺、三(n,n
‑
四亚甲基)磷酸三酰胺等磷酸酰胺化合物、三苯基硫化膦、三丁基硫化膦、三辛基硫化膦等有机硫化膦化合物等。
[0358]
作为上述烷基化脲没有特别限定,可以举出脲、二甲基脲、二甲基亚丙基脲等。需要说明的是,可以如二甲基亚丙基脲等那样具有环状结构。
[0359]
作为上述烷基化硫脲没有特别限定,可以举出二甲基硫脲等。
[0360]
作为上述亚砜化合物,可以举出二甲基亚砜、二苯基亚砜等。
[0361]
作为上述吡啶衍生物,可以举出喹啉、异喹啉、烟酸酯等。
[0362]
本发明的酯交换催化剂中,化合物(c
‑
1)与化合物(c
‑
2)优选以(c
‑
1):(c
‑
2)=100:1~1:100(重量比)的比例含有。通过以这样的比例进行混配,能够得到特别合适的结果。上述下限更优选为50:1、进一步优选为10:1。上述上限更优选为1:50、进一步优选为1:10。
[0363]
上述化合物(c
‑
1)相对于发生反应时的反应体系中的参与反应的化合物的量,优选以0.01~50重量%的比例含有。
[0364]
上述化合物(c
‑
2)相对于发生反应时的反应体系中的参与反应的化合物的量,优选以0.01~50重量%的比例含有。
[0365]
此外,本发明的热固化性树脂组合物中,即使不使用酸催化剂也能够发生良好的固化反应,因此可以制成添加有碱性化合物的热固化性树脂组合物,从这方面出发也是优选的。
[0366]
即,作为颜料分散剂等添加剂,有时会使用胺化合物。此外,在将涂料水性化的情况下,广泛进行的是向树脂中引入羧酸基、磺酸基等酸基,利用胺化合物等将其中和而进行水溶化。这种情况下,难以与酸性催化剂合用。这是妨碍以酯交换催化作为固化反应的热固化性树脂组合物的水性化的问题。本发明中,即使在碱性条件下也能够使其固化,因此能够实现水性化。
[0367]
另外,即使将本发明的热固化性树脂组合物作为溶剂系涂料组合物使用的情况下,有时也会组合使用水性涂料作为多层涂膜中的一部分层。这种情况下,在将多层涂膜同时进行加热固化的情况下,有时会从形成多层涂膜的其他层中产生胺、氨等。即使在这样的情况下也能够进行良好的固化,从这方面出发是优选的。
[0368]
上述酯交换催化剂(c)的用量相对于化合物(a)与多元醇(b)的合计重量优选为0.01~50重量%。通过为这样的范围内,能够在低温下进行良好的固化反应,从这方面出发是优选的。
[0369]
本发明的热固化性树脂组合物的形态没有特别限定,特别优选具有有机溶剂系或水系的形态。由此,能够进行薄膜涂装,能够进行低温固化,从这方面出发是优选的。作为水系,可以为水溶性、水分散性中的任一者,除了水以外,还可以含有乙醇、甲醇、醇系、二醇系、醚系、酮系等能够与水以任意的比例混合的水性溶剂。
[0370]
有机溶剂系的热固化性树脂组合物是上述成分溶解或分散于各种有机溶剂中而成的状态的组合物。可使用的有机溶剂没有特别限定,可以使用己烷、辛烷、癸烷、十四烷、环己烷、苯、二甲苯等烃、二甲醚、二乙醚等醚、丙酮、甲基乙基酮等酮、三氯甲烷、四氯化碳、二氯乙烷、三氯乙烷、四氯乙烷等氯系烃、乙醇、甲醇、丙醇、丁醇、丙酮、环己酮等公知的任意有机溶剂。
[0371]
本发明的热固化性树脂组合物为溶剂系组合物的情况下,可以制成高固体化成分的组合物。具体而言,可以制成满足下述条件的组合物:在不包含颜料等添加剂而仅含有成分(a)~(c)和溶剂的状态下,在固体成分为55重量%以上时,在25℃的粘度为200mpa
·
s以下,从这方面出发是优选的。
[0372]
需要说明的是,上述“在仅含有成分(a)~(c)和溶剂的状态下,在固体成分为55重量%以上时,在25℃的粘度为200mpa
·
s以下”是指,仅以构成热固化性树脂组合物的树脂成分进行测定而得到的粘度满足上述范围,可以是仅含有这样的树脂组合物的热塑性树脂组合物,也可以是在满足这样的参数的树脂组合物中混配包括颜料的各种添加剂而成的组合物。
[0373]
另外,作为2液型的树脂组合物,可以将包含化合物(a)的溶液与包含多元醇(b)的主剂溶液组合,在即将使用前混合后进行使用。由此,保存稳定性变得良好,从这方面出发是优选的。另外,也可以制成在包含化合物(a)和多元醇(b)的溶液中混合包含酯交换催化剂(c)的催化剂溶液的类型的2液型。
[0374]
此外,在制成粉末涂料等粉体形状的热固化性树脂组合物的情况下,可以通过将化合物(a)、多元醇(b)和酯交换催化剂(c)利用通常的方法进行干燥、混合、粉碎来制造。
[0375]
本发明的热固化性组合物中,除了上述(a)~(c)的成分以外,可以进一步组合使用在涂料、粘接剂的领域中通常使用的其他交联剂。作为可使用的交联剂没有特别限定,可以举出异氰酸酯化合物、封端异氰酸酯化合物、三聚氰胺树脂、环氧树脂、硅烷化合物等。另外,也可以合用乙烯基醚、阴离子聚合性单体、阳离子聚合性单体、自由基聚合性单体等。也可以合用用于促进这些合用的交联剂的反应的固化剂。
[0376]
需要说明的是,上述其他交联剂不是必须的,本发明的热固化性树脂组合物即使不含有上述其他交联剂也能够得到良好的固化性,从这方面出发是优选的。
[0377]
本发明的热固化性树脂组合物中,根据目的,在必要的情况下可以含有非水分散树脂(nad)。但是,非水分散树脂(nad)不是必须的,也可以不含有该非水分散树脂(nad)。
[0378]
本发明的热固化性树脂组合物可以在热固化性涂料、热固化性粘接剂等领域中适当地使用。
[0379]
在作为热固化性涂料使用的情况下,除了上述各成分以外,还可以合用在涂料领域中通常使用的添加剂。例如可以合用着色颜料、体质颜料、光辉性颜料等、以及它们的任意组合。
[0380]
在使用颜料的情况下,以树脂成分的总固体成分100重量%为基准,优选在合计为
1~500重量%的范围内含有颜料。上述下限更优选为3重量%,进一步优选为5重量份。上述上限更优选为400重量%,进一步优选为300重量%。
[0381]
作为上述着色颜料,可以举出例如氧化钛、锌白、炭黑、钼红、普鲁士蓝、钴蓝、偶氮系颜料、酞菁系颜料、喹吖啶酮系颜料、异吲哚啉系颜料、士林(threne)系颜料、苝系颜料、二噁嗪系颜料、吡咯并吡咯二酮系颜料等、以及它们的任意组合。
[0382]
作为上述体质颜料,可以举出例如粘土、高岭土、硫酸钡、碳酸钡、碳酸钙、滑石、二氧化硅、矾土白等,优选硫酸钡和/或滑石,并且更优选硫酸钡。
[0383]
作为上述光辉性颜料,可以举出例如铝(包括蒸镀铝)、铜、锌、黄铜、镍、氧化铝、云母、被氧化钛或氧化铁被覆的氧化铝、被氧化钛或氧化铁被覆的云母、玻璃鳞片、全息颜料等、以及它们的任意组合。上述铝颜料包括非浮型铝和浮型铝。
[0384]
上述热固化性涂料可以根据期望进一步含有增稠剂、紫外线吸收剂、光稳定剂、消泡剂、增塑剂、上述疏水性溶剂以外的有机溶剂、表面调整剂、防沉降剂等涂料用添加剂。
[0385]
作为上述增稠剂,可以举出例如硅酸盐、金属硅酸盐、蒙脱土、胶体状氧化铝等无机系增稠剂;(甲基)丙烯酸与(甲基)丙烯酸酯的共聚物、聚丙烯酸钠等聚丙烯酸系增稠剂;在1分子中具有亲水性部分和疏水性部分,在水性介质中,上述疏水性部分吸附到涂料中的颜料或乳液颗粒的表面,上述疏水性部分彼此通过进行缔合等而显示出增稠作用的缔合型增稠剂;羧甲基纤维素、甲基纤维素、羟乙基纤维素等纤维素衍生物系增稠剂;酪蛋白、酪蛋白酸钠、酪蛋白酸铵等蛋白质系增稠剂;藻酸钠等藻酸系增稠剂;聚乙烯醇、聚乙烯基吡咯烷酮、聚乙烯基苄基醚共聚物等聚乙烯基系增稠剂;普朗尼克聚醚、聚醚二烷基酯、聚醚二烷基醚、聚醚环氧改性物等聚醚系增稠剂;乙烯基甲基醚
‑
马来酸酐共聚物的偏酯等马来酸酐共聚物系增稠剂;聚酰胺胺盐等聚酰胺系增稠剂等、以及它们的任意组合。
[0386]
上述聚丙烯酸系增稠剂有市售,可以举出例如罗门哈斯公司制造的“acrysolase
‑
60”、“acrysoltt
‑
615”、“acrysolrm
‑
5”(以上为商品名)、san nopco limited公司制造的“sn thickener 613”、“sn thickener 618”、“sn thickener 630”、“sn thickener 634”、“sn thickener 636”(以上为商品名)等。
[0387]
另外,上述缔合型增稠剂有市售,可以举出例如adeka公司制造的“uh
‑
420”、“uh
‑
450”、“uh
‑
462”、“uh
‑
472”、“uh
‑
540”、“uh
‑
752”、“uh
‑
756vf”、“uh
‑
814n”(以上为商品名)、罗门哈斯公司制造的“acrysolrm
‑
8w”、“acrysolrm
‑
825”、“acrysolrm
‑
2020npr”、“acrysolrm
‑
12w”、“acrysolsct
‑
275”(以上为商品名)、san nopco limited公司制造的“sn thickener 612”、“sn thickener 621n”、“sn thickener 625n”、“sn thickener 627n”、“sn thickener 660t”(以上为商品名)等。
[0388]
作为可应用上述热固化性涂料的被涂物,没有特别限制,可以举出例如轿车、卡车、摩托车、公共汽车等汽车车身的外板部;汽车部件;移动电话、音响设备等家电产品、建筑材料、家具、粘接剂、膜或玻璃的涂布剂等各种示例。在作为汽车用涂料使用的情况下,可以用于中间涂料、基底涂料、透明涂料等的任意层的效果。
[0389]
上述被涂物可以是在上述金属材料和由其成型的车身等的金属表面实施了磷酸盐处理、铬酸盐处理、复合氧化物处理等表面处理的被涂物,另外也可以是具有涂膜的被涂物。作为上述具有涂膜的被涂物,可以举出根据期望对基材实施表面处理、并在其上形成有底涂涂膜的被涂物等。特别优选利用电沉积涂料形成有底涂涂膜的车身,更优选利用阳离
子电沉积涂料形成有底涂涂膜的车身。
[0390]
上述被涂物可以是根据期望在上述塑料材料、由该塑料材料成型的汽车部件等的塑料表面进行了表面处理、底漆涂装等的被涂物。另外,也可以是上述塑料材料与上述金属材料组合而成的被涂物。
[0391]
作为上述热固化性涂料的涂装方法,没有特别限制,可以举出例如气喷涂装、无气喷涂涂装、旋转雾化涂装、帘式涂布涂装等,优选气喷涂装、旋转雾化涂装等。涂装时,可以根据期望施加静电。利用上述涂装方法,能够由上述水性涂料组合物形成湿涂膜。
[0392]
上述湿涂膜可以通过加热进行固化。该固化可以利用公知的加热手段、例如热风炉、电炉、红外线感应加热炉等干燥炉来实施。上述湿涂膜可以通过在优选为约80℃~约180℃、更优选为约100℃~约170℃、并且进一步优选为约120℃~约160℃的范围的温度下进行优选为约10分钟~约60分钟、并且更优选为约15分钟~约40分钟的加热而固化。另外,还能够应对80℃~140℃下的低温固化,从这方面考虑是优选的。
[0393]
需要说明的是,本发明的热固化性树脂组合物在涂料领域中使用的情况下,认为需要具有平滑性、耐水性/耐酸性等性能的充分的固化性能。另一方面,在粘接剂、粘合剂等领域中使用的情况下,不需要像在涂料中所要求的那样高的固化性能。本发明的热固化性树脂组合物能够制成可作为涂料使用的水平的组合物,但即使是未达到这种水平的组合物,有时也可以在粘接剂、粘合剂等领域中使用。
[0394]
本发明涉及一种固化膜,其特征在于,其是通过将上述热固化性树脂组合物进行三维交联而形成的。这样的固化膜具有能够作为涂料、粘接剂使用的充分的性能。
[0395]
[实施例]
[0396]
以下,基于实施例进一步详细地说明本发明。需要说明的是,本发明并不限定于以下的实施例。需要说明的是,文中的份表示重量。
[0397]
(合成例1)
[0398]
将乙二醇单乙酰乙酸酯单甲基丙烯酸酯54份、丙烯酸正丁酯58份、碳酸钾38份、18
‑
冠
‑6‑
醚2份、四氢呋喃112份混合,在50℃搅拌3小时。反应结束后,投入环己烷和水,进行水洗。有机层用饱和氯化铵水溶液中和后,进行2次水洗,将所得到的有机层在减压下浓缩,得到单体a。
[0399]
(合成例2)
[0400]
将乙二醇单乙酰乙酸酯单甲基丙烯酸酯54份、丙烯酸甲酯43份、碳酸钾33份、18
‑
冠
‑6‑
醚2份、四氢呋喃97份混合,在50℃搅拌3小时。反应结束后,投入环己烷和水,进行水洗。有机层用饱和氯化铵水溶液中和后,进行2次水洗,将所得到的有机层在减压下浓缩,得到单体b。
[0401]
(合成例3)
[0402]
将甲基丙烯酸正丁酯(共荣社化学株式会社制品:light ester nb)240份、甲基丙烯酸羟乙酯(共荣社化学株式会社制品:light ester ho
‑
250)110份、苯乙烯30份制成单体混合液,将作为引发剂的2,2
’‑
偶氮双(2,4
‑
二甲基戊腈)(和光纯药v
‑
65)25份溶解在芳香族烃(t
‑
sol100)中,制成引发剂溶液。在可进行搅拌的烧瓶中加入芳香族烃(t
‑
sol100)250份和环己酮250份,一边封入氮气一边滴加单体溶液和引发剂溶液。将此时的聚合温度设定为100℃。用2小时进行滴加,进而在100℃进行4小时熟化,得到重均分子量7300、分散度
2.05的聚合物溶液a。
[0403]
(合成例4)
[0404]
将甲基丙烯酸正丁酯(共荣社化学株式会社制品:light ester nb)200份、单体b175份、甲基丙烯酸羟乙酯(共荣社化学株式会社制品:light ester ho
‑
250)90份、苯乙烯25份制成单体混合液,将作为引发剂的2,2
’‑
偶氮双(2,4
‑
二甲基戊腈)(和光纯药v
‑
65)25份溶解在芳香族烃(t
‑
sol100)中,制成引发剂溶液。在可进行搅拌的烧瓶中加入芳香族烃(t
‑
sol100)490份,一边封入氮气一边滴加单体溶液和引发剂溶液。将此时的聚合温度设定为100℃。用2小时进行滴加,进而在100℃进行4小时熟化,得到重均分子量9500、分散度1.99的聚合物溶液b。
[0405]
(合成例5)
[0406]
将三羟甲基丙烷三丙烯酸酯40份、丙二酸二甲酯55份、碳酸钾56份、18
‑
冠
‑6‑
醚1.5份、四氢呋喃95份混合,在50℃搅拌3小时。反应结束后,投入环己烷和水,进行水洗。有机层用饱和氯化铵水溶液中和后,进行2次水洗,将所得到的有机层在减压下浓缩,由此得到酯化合物a。酯化合物a的分子量为692.7。
[0407]
(合成例6)
[0408]
将二羟甲基三环癸烷二丙烯酸酯40份、丙二酸二甲酯35份、碳酸钾56份、18
‑
冠
‑6‑
醚1.5份、四氢呋喃75份混合,在50℃搅拌3小时。反应结束后,投入环己烷和水,进行水洗。有机层用饱和氯化铵水溶液中和后,进行2次水洗,将所得到的有机层在减压下浓缩,由此得到酯化合物b。酯化合物b的分子量为568.6。
[0409]
(合成例7)
[0410]
将三羟甲基丙烷三丙烯酸酯40份、丙二酸二异丙酯76份、碳酸钾56份、18
‑
冠
‑6‑
醚1.5份、四氢呋喃116份混合,在50℃搅拌3小时。反应结束后,投入环己烷和水,进行水洗。有机层用饱和氯化铵水溶液中和后,进行2次水洗,将所得到的有机层在减压下浓缩,由此得到酯化合物c。酯化合物c的分子量为861.0。
[0411]
(合成例8)
[0412]
将三羟甲基丙烷三丙烯酸酯40份、丙二酸二正丁酯88份、碳酸钾56份、18
‑
冠
‑6‑
醚1.5份、四氢呋喃128份混合,在50℃搅拌3小时。反应结束后,投入环己烷和水,进行水洗。有机层用饱和氯化铵水溶液中和后,进行2次水洗,将所得到的有机层在减压下浓缩,由此得到酯化合物d。酯化合物d的分子量为945.1。
[0413]
(合成例9)
[0414]
将二羟甲基三环癸烷二丙烯酸酯52份、丙二酸二甲酯30份、碳酸钾56份、18
‑
冠
‑6‑
醚1.5份、四氢呋喃82份混合,在50℃搅拌3小时。反应结束后,过滤出沉淀物,将滤液在减压下浓缩,由此得到酯化合物e。酯化合物e的重均分子量为1810。
[0415]
(合成例10)
[0416]
将三羟甲基丙烷三丙烯酸酯40份、丙二酸二叔丁酯88份、碳酸钾56份、18
‑
冠
‑6‑
醚1.5份、四氢呋喃128份混合,在50℃搅拌3小时。反应结束后,投入环己烷和水,进行水洗。有机层用饱和氯化铵水溶液中和后,进行2次水洗,将所得到的有机层在减压下浓缩,由此得到酯化合物f。酯化合物f的分子量为945.1。
[0417]
(合成例11)
[0418]
将乙酰乙酸甲酯40份、丙烯酸甲酯60份、碳酸钾48份、18
‑
冠
‑6‑
醚1.5份、四氢呋喃100份混合,在50℃搅拌3小时。反应结束后,投入环己烷和水,进行水洗。有机层用饱和氯化铵水溶液中和后,进行2次水洗,将所得到的有机层在减压下浓缩,由此得到酯化合物g。酯化合物g的分子量为288.3。
[0419]
(合成例12)
[0420]
在琥珀酸单甲酯190份、三羟甲基丙烷三缩水甘油醚(共荣社化学株式会社epolight 100mf)201.5份中加入三乙基苄基氯化铵、阻聚剂,在90℃反应10小时以上,得到酯化合物h。酯化合物h的分子量为698.6。
[0421]
(合成例13)
[0422]
将丙二酸二乙酯16份、碳酸钾14份、四氢呋喃60份混合,升温至50℃。用1小时滴加氯甲酸乙酯12份,在70℃搅拌10小时。反应结束后,投入甲苯140份、10%盐水100份。将有机层用水100份进行2次水洗后,在减压下浓缩,得到酯化合物i。酯化合物i的分子量为232.2。
[0423]
(合成例14)
[0424]
向具备精馏塔的反应装置中投入间苯二甲酸118份、己二酸50份、新戊二醇47份和三羟甲基丙烷80份,升温至160℃,进一步用时3小时缓慢地升温至160~230℃。
[0425]
接着,在230℃持续反应30分钟后,将精馏塔置换为分水器,向内容部中加入二甲苯13份,向分水器中也加入二甲苯,使水与二甲苯共沸而除去水,反应至酸值达到10mgkoh/g以下后进行冷却,用环己酮调整固体成分,得到作为树脂固体成分50%的聚酯树脂溶液的聚酯多元醇a。所得到的聚酯多元醇a中,以树脂固体成分计具有122mgkoh/g的羟值、3,500的数均分子量。
[0426]
需要说明的是,本实施例中,mn(数均分子量)、mw(重均分子量)为通过凝胶渗透色谱(gpc)测定的聚苯乙烯换算分子量的值。柱使用gpc kf
‑
804l(昭和电工株式会社制造、聚合物溶液a~d)、或kf
‑
802(昭和电工株式会社制造、酯化合物e),溶剂使用四氢呋喃。另外,对于酯化合物a~i,在通过化学分析确认得到了具有目标结构的化合物后,根据这样的化合物的化学结构计算出分子量。
[0427]
(涂料组合物的制备和固化条件)
[0428]
实施例1~80、比较例1~15
[0429]
将表1~11所示的各成分混合,使用涂布器利用湿式法(wet)制作400μm的涂膜,在150℃进行30分钟固化。
[0430]
(评价方法)
[0431]
关于凝胶分数,将实施例中得到的被膜使用索氏提取器在丙酮回流中进行30分钟溶解,测定被膜的残留重量%,将其作为凝胶分数。将凝胶分数为0~40%、不耐实用的情况记为
×
。将凝胶分数为40~60%、确认到一定的固化的情况记为
△
。将凝胶分数为60~80%、可耐实用的情况记为
○
。将凝胶分数为80~100%、性能优异的情况记为
◎
。
[0432]
关于二甲苯摩擦,将实施例的热固化性树脂在pet膜上形成涂膜,用浸有二甲苯的医用纱布擦拭10次,对表面进行观察。关于评价,将不耐实用的情况记为
×
,将可耐实用的情况记为
○
,将性能更优异的情况记为
◎
。
[0433]
关于涂膜外观,将实施例的热固化性树脂在pet膜上形成涂膜,使固化后的膜厚为50~60μm,对表面进行观察。关于评价,将可耐实用的情况记为无异常,将观察到外观不良
的情况记载为异常内容。
[0434]
刚体摆锤试验器
[0435]
使用a&d公司制造的刚体摆锤试验器(型号rpt
‑
3000w),以3℃/分钟的升温速度升温至180℃,求出此时的周期和对数衰减率的变化。特别是用于确认涂膜的固化状态。摆锤:frb
‑
100膜厚(wet):100μm
[0436]
拉伸试验
[0437]
将热固化性组合物制成涂膜,使干燥膜厚为100μm,在150℃烘烤30分钟,得到涂膜。将各涂膜剥离,切出长度30mm
×
宽度4mm的长条状。
[0438]
将sun scientific公司制造的流变仪(型号cr
‑
500dx)设定为速度10mm/min的拉伸模式,对长条状的涂膜实施拉伸试验。由所得到的s
‑
s曲线计算出屈服点处的拉伸强度和拉伸断裂伸长率,按下述基准进行评价。
[0439]
屈服点
[0440]
◎
:20mpa以上
[0441]
○
:10~20mpa
[0442]
×
:10mpa以下
[0443]
拉伸断裂伸长率
[0444]
◎
:100%以上
[0445]
○
:50~100%
[0446]
△
:10~50%
[0447]
×
:10%以下
[0448]
实施例1~13、比较例1~12
[0449]
将表1~3所示的各成分混合,使用涂布器利用湿式法(wet)制作400μm的涂膜,在150℃进行30分钟固化。之后,进行凝胶分数、二甲苯摩擦试验并利用制备液进行刚体摆锤试验。将结果示于表1~3。
[0450][0451]
[表2]
[0452] 比较例1比较例2比较例3比较例4比较例5比较例6
聚合物溶液a100100100100100100二月桂酸二辛基锡1.5
ꢀꢀꢀꢀꢀ
乙酰丙酮锌 1.5
ꢀꢀꢀꢀ
乙酰丙酮铁(iii)
ꢀꢀ
1.5
ꢀꢀꢀ
乙酰丙酮钛(iv)ipa溶液
ꢀꢀꢀ
2.4
ꢀꢀ
alumichelate d
ꢀꢀꢀꢀ
1.5 2
‑
乙基己酸铋
ꢀꢀꢀꢀꢀ
1.5固化温度150℃150℃150℃150℃150℃150℃固化时间30分钟30分钟30分钟30分钟30分钟30分钟凝胶分数
××××××
二甲苯摩擦
××××××
刚体摆锤
ꢀꢀꢀꢀꢀꢀ
涂膜外观无异常
‑‑‑‑‑
[0453][0454]
由表1~3的结果可知,本发明的热固化性树脂组合物具有良好的热固化性能。另外可知,在不含有酯化合物的比较例1~6、使用了叔烷基酯化合物的比较例7~12中,未能
获得具有良好的固化性能和/或涂膜外观的组合物,此外由于胺的存在,固化性能大幅降低。
[0455]
实施例14~16
[0456]
将表4所示的各成分混合,使用涂布器通过湿式法(wet)制作400μm的涂膜,在150℃进行30分钟固化。之后,进行凝胶分数、二甲苯摩擦试验并利用制备液进行刚体摆锤试验。将结果示于表4。
[0457]
[表4]
[0458] 实施例14实施例15实施例16聚合物溶液a140140140酯化合物a303030二月桂酸二辛基锡1.5
ꢀꢀ
乙酰丙酮锌 1.5 乙酰丙酮铁(iii)
ꢀꢀ
1.52
‑
氨基
‑2‑
甲基
‑1‑
丙醇0.20.50.4固化温度150℃150℃150℃固化时间30分钟30分钟30分钟凝胶分数
◎◎◎
二甲苯摩擦
◎◎◎
刚体摆锤 图11 涂膜外观无异常无异常无异常
[0459]
由上述各实施例的结果可知,本发明的热固化性树脂组合物具有良好的固化性能。此外,由表4的结果可知,本发明的热固化性树脂组合物即使在胺存在下也可没有问题地发生固化。
[0460]
实施例17~80、比较例13~15
[0461]
利用与上述实施例1相同的方法进行组合物的制备、涂膜的形成,并进行评价。将结果示于表5~11。
[0462]
[0463][0464]
由表5~6的结果可知,本发明的热固化性树脂组合物即使在含有聚酯多元醇树脂的情况下也具有良好的热固化性能。
[0465]
[表7]
[0466] 实施例42实施例43实施例44实施例45聚酯多元醇a140140140140酯化合物a30303030甲醇
ꢀꢀꢀ
10乙二醇 3
ꢀꢀ
新戊二醇
ꢀꢀ
5 β
‑
环糊精
ꢀꢀꢀ
2.5二丁基二甲氧基锡3333固化温度150℃150℃150℃150℃固化时间30分钟30分钟30分钟30分钟凝胶分数
◎◎◎◎
二甲苯摩擦
◎◎◎◎
涂膜外观无异常无异常无异常无异常屈服点强度
○◎◎◎
拉伸断裂伸长率
◎○○
δ
[0467][0468]
[表9]
[0469] 实施例56实施例57实施例58实施例59实施例60
聚酯多元醇a140140140140140酯化合物a22.522.57.522.522.5癸二酸二乙酯7.57.522.57.57.5甲醇 5555二乙酸二辛基锡3
ꢀꢀꢀꢀ
乙酰丙酮锌 333 三辛基氧化膦
ꢀꢀꢀ
3 乙酰丙酮锆
ꢀꢀꢀꢀ
3固化温度150℃150℃150℃150℃150℃固化时间30分钟30分钟30分钟30分钟30分钟凝胶分数
◎◎◎◎◎
二甲苯摩擦
◎○◎◎◎
涂膜外观无异常无异常无异常无异常无异常
[0470]
[0471][0472]
由表7~11的结果可知,本发明的热固化性树脂组合物能够与低分子量多元醇(b
‑
3)合用、与具有2官能和3官能以上的烷基酯基的化合物(a)合用、与其他交联剂合用,可根
据期望得到更好的涂膜物性。
[0473]
(实施例81的涂料的制备和涂装方法)
[0474]
将甲基丙烯酸
‑2‑
乙基己酯(共荣社化学株式会社light ester eh)136份、单体b68份、甲基丙烯酸
‑2‑
羟基乙酯68份、甲基丙烯酸
‑2‑
羟基丁酯68份、苯乙烯114份、2
‑
甲基丙烯酰氧基乙基琥珀酸(共荣社化学株式会社light ester ho
‑
ms(n))45份制成单体混合液,将作为引发剂的2,2
’‑
偶氮双(2,4
‑
二甲基戊腈)(富士胶片和光纯药株式会社v
‑
65)25份溶解在芳香族烃(t
‑
sol 100)中,制成引发剂溶液。在可进行搅拌的烧瓶中加入芳香族烃(t
‑
sol 100)500份,一边封入氮气一边滴加单体溶液和引发剂溶液。将此时的聚合温度设定为100℃。用2小时进行滴加,进而在100℃进行4小时熟化,得到重均分子量8,500、分散度1.93的聚合物溶液f。
[0475]
接着,制作表12所示的热固化性组合物,对105℃的固体成分和25℃的粘度(e型粘度计:株式会社atago制)进行测定。对于热固化性组合物,将其喷雾涂装在厚度0.8mm的毛面钢板上,使干燥后膜厚10μm,在150℃进行30分钟烘烤。对所得到的涂膜实施涂膜状态的目视评价、凝胶分数、耐二甲苯摩擦性试验。将结果示于表12。
[0476]
[表12]
[0477] 实施例81聚合物溶液f140酯化合物g20单丁基氧化锡2.7固体成分浓度(%)56粘度(25℃、mpa
·
s)80涂装方法气喷涂装干燥膜厚10μm固化温度150℃固化时间30分钟凝胶分数
◎
二甲苯摩擦
◎
涂膜外观无异常
[0478]
由上述实施例81的结果可知,将本发明的热固化性组合物作为高固体化组合物使用的情况下也可得到良好的涂布性、固化性能、涂膜性能。
[0479]
工业实用性
[0480]
本发明的热固化性树脂组合物能够作为固化膜用作各种涂料组合物、粘接剂组合物、粘合剂组合物。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。