1.本发明涉及用于治疗或预防癌症的新型的癌症肽疫苗。更详细而言,涉及:能够对想要使其接触癌症肽疫苗的免疫细胞进行特异性递送的癌症肽疫苗。
背景技术:
2.作为癌症的新的治疗方法之一,研究了癌症肽疫苗。癌症肽疫苗疗法是目的在于使针对癌细胞表达的肿瘤抗原的特异性免疫应答在患者体内活化/增殖、从而预防或治疗癌症的治疗方法,是给予由作为肿瘤抗原蛋白的一部分的肽构成的抗原作为疫苗的方法。
3.在这样的研究中,自1990年代开始,许多有关肿瘤抗原的研究及以靶向这些肿瘤抗原的疫苗的开发逐渐推进,但作为癌症肽疫苗,在研究室水平还有报道诱发癌症特异性免疫的效果(非专利文献1:fifis t.et al.,vaccine.2004nov 25;23(2):258-66)。另外,报道了一部分癌症疫苗在早期临床试验中具有免疫诱导、存活期延长之类的探索性的有效性(非专利文献2:cancer sci.2018sep;109(9):2660-2669、非专利文献3:cancer sci.2017dec;108(12):2430-2437)
4.然而,这些癌症疫苗中,尚未发现在验证性的临床试验中证实了具有充分有效性(治疗效果)的疫苗,尚不存在已被批准的疫苗。作为未获得有效性的原因,认为一个原因是疫苗向免疫细胞的递送、免疫细胞的激活并不充分。
5.现有技术文献
6.专利文献
7.专利文献1:wo2016/186206
8.专利文献2:wo2018/230257
9.非专利文献
10.非专利文献1:fifis t.et al.,vaccine.2004nov 25;23(2):258-66
11.非专利文献2:cancer sci.2018sep;109(9):2660-2669
12.非专利文献3:cancer sci.2017dec;108(12):2430-2437
技术实现要素:
13.发明要解决的问题
14.本发明的课题在于提供一种肽疫苗,其经过了复合体化,从而能够将肽疫苗特异性递送至特定的免疫细胞表面。本发明的目的另外还在于提供将肽疫苗特异性递送至特定的免疫细胞表面的方法。
15.用于解决问题的方案
16.本发明的发明人等进行了深入研究,结果示出通过提供肽疫苗而能够解决上述课题,所述肽疫苗是与igg结合肽组合而成的,所述igg结合肽特征在于为针对特定免疫细胞(例如树突细胞)的表面的分子的激动剂且能够与igg结合。
17.更具体而言,本件申请为了解决前述课题而提供以下方式:
18.[1]:一种肽疫苗,其是与igg结合肽组合而成的;
[0019]
[2]:根据[1]所述的肽疫苗,其中,肽疫苗选自由癌症疫苗、感染症疫苗组成的组;
[0020]
[3]:根据[2]所述的肽疫苗,其中,肽疫苗为选自由肿瘤相关抗原、肿瘤新抗原、肿瘤个体化新抗原组成的组中的癌症疫苗;
[0021]
[4]:根据权利要求[1]~[3]中任一项所述的肽疫苗,其中,igg结合肽选自由如下序列组成的组:
[0022]
xaa1 xaa2 xaa3 cys xaa4 xaa5 his xaa6 gly xaa7 leu val trp cys xaa8 xaa9 xaa10(序列号1)
[0023]
[序列号1中,
[0024]
xaa1、xaa2、xaa9、xaa10各自为除cys以外的任意的氨基酸,或者不存在xaa1、xaa2、xaa9、xaa10,或者xaa1与xaa2一起为arg arg gly pro,
[0025]
xaa3、xaa4、xaa5、xaa8各自为除cys以外的任意的氨基酸,
[0026]
xaa6为lys、cys、asp、glu、arg、leu、2-氨基辛二酸、或二氨基丙酸,
[0027]
xaa7为glu、asn或gln];或者
[0028]
xaa11 xaa12 asn met gln cys gln arg arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala xaa13 ile xaa14 ser ile arg asp asp cys(序列号2)
[0029]
[序列号2中,
[0030]
xaa11选自由gly、ala、val、leu、ile、met、pro、phe、trp、lys、鸟氨酸、cys、asp、glu、β-ala、2-氨基辛二酸、二氨基丙酸、和nh2-(peg)n-co(n=1~50)组成的组,或者不存在xaa11,
[0031]
xaa12选自由lys、鸟氨酸、cys、asp、glu、phe、2-氨基辛二酸、和二氨基丙酸组成的组,
[0032]
xaa13和xaa14各自独立地选自由arg、his、asp、glu、ser、thr、asn、gln、tyr、和cys组成的组];
[0033]
[5]:根据[1]~[4]中任一项所述的肽疫苗,其中,xaa4选自由ala、ser、以及thr组成的组,
[0034]
xaa5为tyr或trp;
[0035]
[6]:根据权利要求[4]所述的肽疫苗,其中,igg结合肽选自由如下序列组成的组:
[0036]
asp cys ala tyr his xaa6 gly glu leu val trp cys thr(序列号3)
[0037]
gly pro asp cys ala tyr his xaa6 gly glu leu val trp cys thr phe his(序列号4)
[0038]
arg cys ala tyr his xaa6 gly glu leu val trp cys ser(序列号5)
[0039]
gly pro arg cys ala tyr his xaa6 gly glu leu val trp cys ser phe his(序列号6)
[0040]
ser pro asp cys ala tyr his xaa6 gly glu leu val trp cys thr phe his(序列号7)
[0041]
gly asp asp cys ala tyr his xaa6 gly glu leu val trp cys thr phe his(序列号8)
[0042]
gly pro ser cys ala tyr his xaa6 gly glu leu val trp cys thr phe his(序列号9)
[0043]
gly pro asp cys ala tyr his xaa6 gly glu leu val trp cys ser phe his(序列号10)
[0044]
gly pro asp cys ala tyr his xaa6 gly glu leu val trp cys thr his his(序列号11)
[0045]
gly pro asp cys ala tyr his xaa6 gly glu leu val trp cys thr phe tyr(序列号12)
[0046]
ser pro asp cys ala tyr his xaa6 gly glu leu val trp cys thr phe tyr(序列号13)
[0047]
ser asp asp cys ala tyr his xaa6 gly glu leu val trp cys thr phe tyr(序列号14)
[0048]
arg gly asn cys ala tyr his xaa6 gly gln leu val trp cys thr tyr his(序列号15)
[0049]
gly xaa2 asp cys ala tyr his xaa6 gly glu leu val trp cys thr xaa9his(序列号16)
[0050]
arg arg gly pro asp cys ala tyr his xaa6 gly glu leu val trp cys thr phe his(序列号17)
[0051]
phe asn met gln cys gln arg arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号18)、
[0052]
gly phe asn met gln cys gln arg arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号19)、
[0053]
lys asn met gln cys gln arg arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号20)、
[0054]
gly phe asn met gln cys gln lys arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号21)、
[0055]
lys asn met gln cys gln lys arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号22)、
[0056]
phe asn met gln gln gln arg arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp(序列号23)、或
[0057]
gly lys asn met gln cys gln arg arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号24);
[0058]
[7]:根据权利要求[6]所述的肽疫苗,其中,igg结合肽为:
[0059]
gly pro asp cys ala tyr his arg gly glu leu val trp cys thr phe his(序列号25)、
[0060]
gly pro asp cys ala tyr his lys gly glu leu val trp cys thr phe his(序列号26)、
[0061]
gly pro asp cys ala trp his arg gly glu leu val trp cys thr phe his(序列号39)、
[0062]
gly pro asp cys ala trp his leu gly glu leu val trp cys thr phe his(序列号40);
[0063]
[8]:根据[1]~[7]中任一项所述的肽疫苗,其中,igg结合肽上结合了igg;
[0064]
[9]:根据权利要求[8]所述的肽疫苗,其中,igg为针对要被递送肽疫苗的免疫细胞特征性的靶标物质的抗体;
[0065]
[10]:根据权利要求[9]所述的肽疫苗,其中,免疫细胞选自由抗原提呈细胞、树突细胞、b细胞组成的组;
[0066]
[11]:根据[8]~[10]中任一项所述的肽疫苗,其中,igg选自由抗cd40抗体、抗pd-l1抗体、抗dec205抗体、抗dcir抗体、抗甘露糖受体抗体、抗dc-sign抗体、抗cd11c抗体、抗dectin-1抗体组成的组;
[0067]
[12]:一种递送肽疫苗的方法,其使用igg、igg结合肽、与igg结合肽组合而成的肽疫苗将肽疫苗递送至在细胞表面具有igg所靶向的分子的细胞;
[0068]
[13]:根据[12]所述的方法,其中,肽疫苗选自由癌症疫苗、感染症疫苗组成的组;
[0069]
[14]:根据[13]所述的方法,其中,肽疫苗为选自由肿瘤相关抗原、肿瘤新抗原、肿瘤个体化新抗原组成的组中的癌症疫苗;
[0070]
[15]:根据[12]~[14]中任一项所述的方法,其中,igg结合肽选自由如下序列组成的组:
[0071]
xaa1 xaa2 xaa3 cys xaa4 xaa5 his xaa6 gly xaa7 leu val trp cys xaa8 xaa9 xaa10(序列号1)
[0072]
[序列号1中,
[0073]
xaa1、xaa2、xaa9、xaa10各自为除cys以外的任意的氨基酸,或者不存在xaa1、xaa2、xaa9、xaa10,或者xaa1与xaa2一起为arg arg gly pro,
[0074]
xaa3、xaa4、xaa5、xaa8各自为除cys以外的任意的氨基酸,
[0075]
xaa6为lys、cys、asp、glu、arg、leu、2-氨基辛二酸、或二氨基丙酸,xaa7为glu、asn或gln];或者
[0076]
xaa11 xaa12 asn met gln cys gln arg arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala xaa13 ile xaa14 ser ile arg asp asp cys(序列号2)
[0077]
[序列号2中,
[0078]
xaa11选自由gly、ala、val、leu、ile、met、pro、phe、trp、lys、鸟氨酸、cys、asp、glu、β-ala、2-氨基辛二酸、二氨基丙酸、和nh2-(peg)n-co(n=1~50)组成的组,或者不存在xaa11,
[0079]
xaa12选自由lys、鸟氨酸、cys、asp、glu、phe、2-氨基辛二酸、和二氨基丙酸组成的
asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号19)、
[0101]
lys asn met gln cys gln arg arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号20)、
[0102]
gly phe asn met gln cys gln lys arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号21)、
[0103]
lys asn met gln cys gln lys arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号22)、
[0104]
phe asn met gln gln gln arg arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp(序列号23)、或
[0105]
gly lys asn met gln cys gln arg arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号24);
[0106]
[18]:根据[17]所述的方法,其中,igg结合肽为:
[0107]
gly pro asp cys ala tyr his arg gly glu leu val trp cys thr phe his(序列号25)、或
[0108]
gly pro asp cys ala tyr his lys gly glu leu val trp cys thr phe his(序列号26)、
[0109]
gly pro asp cys ala trp his arg gly glu leu val trp cys thr phe his(序列号39)
[0110]
gly pro asp cys ala trp his leu gly glu leu val trp cys thr phe his(序列号40);
[0111]
[19]:根据[12]~[18]中任一项所述的方法,其中,igg为针对要被递送肽疫苗的免疫细胞特征性的靶标物质的抗体;
[0112]
[20]:根据[19]所述的方法,其中,免疫细胞选自由抗原提呈细胞、树突细胞、b细胞组成的组;
[0113]
[21]:根据[19]或[20]所述的方法,其中,igg选自由抗cd40抗体、抗pd-l1抗体、抗dec205抗体、抗dcir抗体、抗甘露糖受体抗体、抗dc-sign抗体、抗cd11c抗体、抗dectin-1抗体组成的组。
[0114]
发明的效果
[0115]
本发明中公开的、与igg结合肽组合而成的肽疫苗能够有效地进行肽疫苗向特定免疫细胞(例如树突细胞)表面的递送,能够增强其的活化、增强肽疫苗的效果。
附图说明
[0116]
图1是示出与igg结合肽组合而成的肽疫苗的示意图。
[0117]
图2是示出使与igg结合肽组合而成的肽疫苗通过igg结合肽部分与igg结合而成
的复合体(肽疫苗-igg复合体)的示意图。
[0118]
图3是示出在体内调查实施例3中制作的具有各种igg结合性肽的h-2kb限制性ova来源肽对igg的亲和性的、肽对igg的亲和性解析的结果的图。
[0119]
图4是示出在体外调查使用了实施例3中制作的肽疫苗的抗体-肽疫苗复合体(共价键型、非共价键型)是否具有免疫诱导能力的、体外免疫诱导试验(whole pbmc法)的结果的图。
[0120]
图5是示出在体外调查使用了实施例3中制作的肽疫苗的抗体-肽疫苗复合体(共价键型、非共价键型)是否具有免疫诱导能力的、体外免疫诱导试验(monocyte derived dendritic cell(mddc,单核细胞来源的树突细胞)法)的结果的图。
[0121]
图6是示出在体内调查在皮下给药使用了实施例3中制作的肽疫苗的抗体-肽复合体的情况下抗体-肽复合体是否被摄入树突细胞中的、野生型小鼠中的肽向树突细胞的摄入评价的结果的图。
[0122]
图7是示出野生型小鼠中的免疫诱导试验的日程的图。
[0123]
图8是示出在体内调查使用了实施例3中制作的肽疫苗的抗体-肽疫苗复合体(非共价键型)是否具有免疫诱导能力的、野生型小鼠中的免疫诱导试验的结果的图。
[0124]
图9是示出在体内调查使用了实施例3中制作的肽疫苗的抗体-肽疫苗复合体(非共价键型)是否具有免疫诱导能力的、野生型小鼠中的免疫诱导试验(抗体-疫苗混合比率的比较试验)的结果的图。
[0125]
图10是示出在体内调查使用了实施例3中制作的肽疫苗的抗体-肽疫苗复合体(非共价键型)是否具有免疫诱导能力的、野生型小鼠中的免疫诱导试验(用量依赖性试验)的结果的图。
[0126]
图11示出在体内调查使用了实施例3中制作的肽疫苗的抗体-肽疫苗复合体(非共价键型)是否具有抗肿瘤效果的、荷瘤小鼠试验的结果的图。该图中,抗体:抗原肽-igg结合肽组在生物体内也显示出高的肿瘤增殖抑制效果。
[0127]
图12是示出在体内调查使用了实施例3中制作的肽疫苗的抗体-肽疫苗复合体(非共价键型)是否具有抗肿瘤效果的、荷瘤小鼠试验的结果的图。该图中,抗体:抗原肽-igg结合肽组显示出显著的存活期的延长效果。
[0128]
图13是示出野生型小鼠中的免疫诱导试验的日程的图。
[0129]
图14是示出在临床外推性更高的试验体系中调查使用了实施例3中制作的肽疫苗的抗体-肽疫苗复合体(非共价键型)是否具有免疫诱导能力的、野生型小鼠中的免疫诱导试验(新抗原模型)的结果的图。该图中,抗体:抗原-igg结合肽组显示出最高的免疫诱导效果。
[0130]
图15是示出野生型小鼠中的免疫诱导试验的日程的图。
[0131]
图16是示出在体内调查使用实施例3中制作的肽疫苗,与cd40抗体或pd-l1抗体组合而成的抗体-肽疫苗复合体(非共价键型)是否具有免疫诱导能力的、野生型小鼠中的免疫诱导试验的结果的图。
[0132]
图17是示出在体内调查使用实施例3中制作的肽疫苗,cd40抗体或pd-l1抗体组合而成的抗体-肽疫苗复合体(非共价键型)是否具有免疫诱导能力的、野生型小鼠中的免疫诱导试验的结果的图。
[0133]
图18是示出在体内调查使用实施例3中制作的肽疫苗,与抗pd-l1抗体组合而制作的抗体-肽疫苗复合体(非共价键型)是否具有抗肿瘤效果的、荷瘤小鼠试验的结果的图。该图中,抗体:抗原肽-igg结合肽组在生物体内也显示出高的肿瘤增殖抑制效果。
[0134]
图19是示出在体内调查使用了实施例3中制作的肽疫苗的抗体-肽疫苗复合体(非共价键型)是否具有抗肿瘤效果的、荷瘤小鼠试验的结果的图。该图中,抗体:抗原肽-igg结合肽组显示出显著的存活期的延长效果。
[0135]
图20是示出野生型小鼠中的免疫诱导试验的日程的图。
[0136]
图21是示出在体内调查包含小鼠肿瘤细胞株的非同义体细胞突变序列的抗体-肽疫苗复合体(非共价键型)是否具有抗肿瘤效果的、野生型小鼠中的免疫诱导试验的结果的图。
具体实施方式
[0137]
如下所述对本发明中使用的术语进行定义:
[0138]
(a)癌症疫苗:作为药品给予在癌细胞中表达增强或仅在癌细胞中表达的蛋白质的全部或一部分(肿瘤抗原),唤起针对该肿瘤抗原的免疫来消除癌症的治疗药;
[0139]
(b)树突细胞:在针对肿瘤抗原等外来异物的免疫系统的唤起中,在初期识别该异物的免疫细胞;
[0140]
(c)t细胞:被赋予了基于通过树突细胞所识别的肿瘤抗原的信息来特异性杀伤癌细胞的功能的免疫细胞;
[0141]
(d)cd40:在以树突细胞为代表的抗原提呈细胞表面表达的蛋白质之一。通过配体等激动剂分子的结合,能够增强抗原提呈细胞的功能;
[0142]
(e)抗体疫苗:疫苗与抗体的复合体。
[0143]
《肽疫苗》
[0144]
本发明中,作为一方式,公开了关于与igg结合肽组合而成的肽疫苗的发明(图1)。该方式中,肽疫苗只要是使用了具有抗原性的肽的疫苗,该抗原的来源就可以是任意的,可以用作针对病原体的疫苗、针对癌症的疫苗(癌症疫苗)等。利用针对病原体的疫苗作为肽疫苗的情况,可以使用hiv疫苗、hbv疫苗、rsv疫苗等病原体的抗原性肽。另外,利用癌症疫苗作为肽疫苗的情况,可以使用脑瘤、骨髄瘤、胃癌、大肠直肠癌、子宫癌、头颈部癌、胃癌、大肠直肠癌、乳腺癌、肺癌、胰腺癌、间皮瘤、卵巢癌、前列腺癌、黑色素瘤等癌症特异性抗原性肽。通常可以使用认为适于免疫疗法的肿瘤抗原来源的抗原性肽作为癌症疫苗的抗原。例如可以选择:
[0145]
·
在特定的肿瘤细胞中表达,但在正常组织中仅在睾丸中表达者(ny-eso-1、magea1-4、prame、ssx2、ct83等)、
[0146]
·
与正常细胞相比在肿瘤细胞中以非常高水平表达者(wt1、her2、cea、muc1、细胞周期蛋白b1、egfr、间皮素、端粒酶等)、
[0147]
·
在肿瘤细胞中表达,在正常的组织中仅在有限的系列的细胞中表达者(mart1、psa、psma、cd19、gp100等)、
[0148]
·
虽在正常组织中也表达,但在肿瘤细胞中进行了特殊修饰者(muc1t、lsp1等)、
[0149]
·
由于在疾病普遍观察到的基因易位、点突变等异常而疾病特异性产生的新型蛋
白质(bcr-abl1、hras、kras等)、
[0150]
·
源自仅在肿瘤细胞中产生的突变蛋白质(新抗原)的肽组,所述突变蛋白质(新抗原)是在肿瘤细胞中经常观察到的源自基因组不稳定性等的基因突变的结果,等。
[0151]
对于肽疫苗,在以单体给药的情况下,已知通常无法产生充分的免疫诱导。作为其理由,认为无法实现将肽疫苗递送至目标免疫细胞中。本发明中的肽疫苗出于弥补这样的通常观察到的肽疫苗的缺点,为了对目标免疫细胞递送肽疫苗而利用igg,将肽疫苗与igg结合肽组合而提供。
[0152]
本发明中使用的igg结合肽可以使用公知的能够将igg和肽疫苗的肽结合的igg结合肽,例如可以使用wo2016/186206(专利文献1)中记载的igg结合肽(类型1)、wo2018/230257(专利文献2)中记载的igg结合肽(类型2),但不限定于这些。本发明中,可以在这些igg结合肽中组合肽疫苗而提供。本发明的一方式中可以使用的igg结合肽可以使用选自由下述类型组成的组中的igg结合肽:
[0153]
《类型1》
[0154]
xaa1 xaa2 xaa3 cys xaa4 xaa5 his xaa6 gly xaa7 leu val trp cys xaa8 xaa9 xaa10(序列号1)
[0155]
[序列号1中,
[0156]
xaa1、xaa2、xaa9、xaa10各自为除cys以外的任意的氨基酸,或者不存在xaa1、xaa2、xaa9、xaa10,或者xaa1与xaa2一起为arg arg gly pro,
[0157]
xaa3、xaa4、xaa5、xaa8各自为除cys以外的任意的氨基酸,更优选地,xaa4可以选自由ala、ser、以及thr组成的组,xaa5可以为tyr或trp,
[0158]
xaa6为lys、cys、asp、glu、arg、leu、2-氨基辛二酸、或二氨基丙酸,xaa7为glu、asn或gln]
[0159]
《类型2》
[0160]
xaa11 xaa12 asn met gln cys gln arg arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala xaa13 ile xaa14 ser ile arg asp asp cys(序列号2)
[0161]
[序列号2中,
[0162]
xaa11选自由gly、ala、val、leu、ile、met、pro、phe、trp、lys、鸟氨酸、cys、asp、glu、β-ala、2-氨基辛二酸、二氨基丙酸、和nh2-(peg)n-co(n=1~50)组成的组,或者不存在xaa11,
[0163]
xaa12选自由lys、鸟氨酸、cys、asp、glu、phe、2-氨基辛二酸、和二氨基丙酸组成的组,
[0164]
xaa13和xaa14各自独立地选自由arg、his、asp、glu、ser、thr、asn、gln、tyr、和cys组成的组],可以将这些igg结合肽与肽疫苗组合而使用。
[0165]
更具体而言,本发明的一方式中可以使用的igg结合肽可以选自由下述类型组成的组:
[0166]
《类型1》:
[0167]
asp cys ala tyr his xaa6 gly glu leu val trp cys thr(序列号3);
[0168]
gly pro asp cys ala tyr his xaa6 gly glu leu val trp cys thr phe his
(序列号4);
[0169]
arg cys ala tyr his xaa6 gly glu leu val trp cys ser(序列号5);
[0170]
gly pro arg cys ala tyr his xaa6 gly glu leu val trp cys ser phe his(序列号6);
[0171]
ser pro asp cys ala tyr his xaa6 gly glu leu val trp cys thr phe his(序列号7);
[0172]
gly asp asp cys ala tyr his xaa6 gly glu leu val trp cys thr phe his(序列号8);
[0173]
gly pro ser cys ala tyr his xaa6 gly glu leu val trp cys thr phe his(序列号9);
[0174]
gly pro asp cys ala tyr his xaa6 gly glu leu val trp cys ser phe his(序列号10);
[0175]
gly pro asp cys ala tyr his xaa6 gly glu leu val trp cys thr his his(序列号11);
[0176]
gly pro asp cys ala tyr his xaa6 gly glu leu val trp cys thr phe tyr(序列号12);
[0177]
ser pro asp cys ala tyr his xaa6 gly glu leu val trp cys thr phe tyr(序列号13);
[0178]
ser asp asp cys ala tyr his xaa6 gly glu leu val trp cys thr phe tyr(序列号14);
[0179]
arg gly asn cys ala tyr his xaa6 gly gln leu val trp cys thr tyr his(序列号15);
[0180]
gly xaa2 asp cys ala tyr his xaa6 gly glu leu val trp cys thr xaa9his(序列号16);
[0181]
arg arg gly pro asp cys ala tyr his xaa6 gly glu leu val trp cys thr phe his(序列号17);
[0182]
《类型2》:
[0183]
phe asn met gln cys gln arg arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号18);
[0184]
gly phe asn met gln cys gln arg arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号19);
[0185]
lys asn met gln cys gln arg arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号20);
[0186]
gly phe asn met gln cys gln lys arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号21);
[0187]
lys asn met gln cys gln lys arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号22);
[0188]
phe asn met gln gln gln arg arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp(序列号23);
[0189]
gly lys asn met gln cys gln arg arg phe tyr glu ala leu his asp pro asn leu asn glu glu gln arg asn ala arg ile arg ser ile arg asp asp cys(序列号24)。
[0190]
这样的igg结合肽中,本发明中特别有用的是xaa6为arg、lys、或leu的igg结合肽,例如,作为这样的有用的igg结合肽的具体的氨基酸序列,可以列举出:
[0191]
gly pro asp cys ala tyr his arg gly glu leu val trp cys thr phe his(序列号25)、或
[0192]
gly pro asp cys ala tyr his lys gly glu leu val trp cys thr phe his(序列号26)、
[0193]
gly pro asp cys ala trp his arg gly glu leu val trp cys thr phe his(序列号39)、
[0194]
gly pro asp cys ala trp his leu gly glu leu val trp cys thr phe his(序列号40)。
[0195]
本发明的igg结合肽优选为用于与人的igg(可以为例如人igg1、igg2、igg3、igg4中任意的igg亚类)或人源化型igg结合的igg结合肽,也可以对除人以外的动物、例如大鼠、小鼠和兔子的igg使用。
[0196]
将igg结合肽与肽疫苗组合的方法可以是任意的方法,可以通过下述方法来制造:利用惯用的液相合成法、固相合成法等肽合成法、基于自动肽合成机的肽合成等,将igg结合肽和肽疫苗的肽生成为一个连续的肽而进行组合的方法;或者,通过将独立合成的igg结合肽与肽疫苗的肽借助接头进行组合的方法。或者也可以通过使用了编码本发明的肽的核酸的基因重组法来制造肽。例如将编码使本发明的igg结合肽和肽疫苗的肽连接成一个的肽的氨基酸序列的dna整合于表达载体中,导入宿主细胞中进行培养,由此也能够制造目标肽。
[0197]
在考虑到合成的容易性等的情况下,作为进行组合的方法,优选合成为igg结合肽与肽疫苗的肽连接成一个的肽。采用这样的方法的情况下,可以设计与igg结合肽组合的肽疫苗的目标序列,使用肽合成机(例如,gyros protein technologies公司制的symphony(注册商标)x等)来合成。可以通过例如凝胶过滤色谱法、离子交换柱色谱法、亲和色谱法、反相柱色谱法等色谱法、硫酸铵分级、超滤、和免疫吸附法等,去除合成肽时所包含的夹杂物,能够纯化肽。在进行基于色谱法的纯化时,可以使用高效液相色谱仪(hplc)等设备。
[0198]
《与igg的复合体》
[0199]
本发明中,特征在于,提供使与igg结合肽组合而成的肽疫苗通过igg结合肽部分与igg结合而成的复合体(图2)。本发明中使用的igg可以根据想要递送肽疫苗的免疫细胞进行选择,本发明中,可以使用如下igg:目的在于与成为对象的免疫细胞结合的igg、用于与成为对象的免疫细胞结合的同时激活该免疫细胞的igg等。例如使用树突细胞作为免疫
细胞的情况下,可以使用抗cd40抗体(igg)、抗pd-l1抗体(igg)、抗dec205抗体(igg)、抗dcir抗体(igg)、抗甘露糖受体抗体(igg)、抗dc-sign抗体(igg)、抗cd11c抗体(igg)、抗dectin-1抗体(igg)等,但即使是除此以外的抗体,也可以根据目的使用其他igg。
[0200]
利用针对病原体的疫苗作为肽疫苗的情况、以及利用癌症疫苗作为肽疫苗的情况,递送至树突细胞或b细胞等免疫细胞均是有效的。因此,本发明中,用于对各细胞进行递送的igg可以使用公知的针对要被递送肽疫苗的免疫细胞特征性的靶标物质的igg,为了递送至树突细胞,可以使用:将cd40作为靶标物质的抗体(j&j,roche,seattle genetics公司等临床开发)、将dec205作为靶标物质的抗体(celldex临床开发)、将dcir作为靶标物质的抗体(ascend biopharmaceuticals临床开发)等。
[0201]
用于形成本发明中复合体而可以使用的igg结合肽部分与igg的结合可以如下方式进行:用交联剂修饰本发明的igg结合肽部分的特定的氨基酸残基,通过该交联剂,与igg fc的特定的氨基酸残基之间形成交联结构,从而进行。作为通过交联剂修饰本发明的与igg结合肽组合而成的肽疫苗的igg结合肽部分的方法,可以通过如下方式进行:使用通过交联剂修饰的氨基酸残基进行与igg结合肽组合而成的肽疫苗的肽合成,从而进行;在合成与igg结合肽组合而成的肽疫苗后,特异性修饰igg结合肽部分中的特定的氨基酸残基的侧链,从而进行。
[0202]
对于本发明中可以用于形成复合体的交联剂,本领域技术人员可以进行适宜选择,可以使用具有能与igg结合肽部分的特定的氨基酸残基结合的至少2个位点的化合物,作为其例子,可以使用:双琥珀酰亚胺戊二酸酯(disuccinimidyl glutarate、dsg)、二琥珀酰亚胺辛二酸酯(disuccinimidyl suberate、dss)等包含至少1个、优选2个以上的琥珀酰亚胺基的交联剂;己二亚氨酸二甲酯二盐酸盐(dimethyl adipimidate
·
2hcl、dma)、庚二亚氨酸二甲酯二盐酸盐(dimethyl pimelimidate
·
2hcl、dmp)、或辛二亚氨酸二甲酯二盐酸盐(dimethyl suberimidate
·
2hcl、dms)等包含至少1个、优选2个以上酰亚胺酸部分的交联剂;以及3,3
’‑
二硫基二亚胺代丙酸二甲酯二盐酸盐(dimethyl 3,3
’‑
dithiobispropionimidate
·
2hcl、dtbp)或3,3
’‑
二硫代二丙酸二(n-羟基丁二酰亚胺酯)(dithiobis(succinimidyl propionate)、dsp)等除了前述官能团之外还具有二硫键的交联剂(wo2016/186206(专利文献1)、wo2018/230257(专利文献2)),但不限定于这些。
[0203]
基于交联剂的特定的氨基酸残基的修饰可以通过选择交联剂与特定的氨基酸残基的种类的组合而进行(wo2016/186206(专利文献1)、wo2018/230257(专利文献2))。例如,使用dss或dsg等包含琥珀酰亚胺基的交联剂的情况,与赖氨酸残基的侧链的胺(ε氨基)和存在于多肽的n末端的伯胺(α氨基)反应,因此在封闭igg结合肽部分的n末端后与dss或dsg反应,由此能够通过dss或dsg仅特异性修饰作为igg结合肽部分的特定的氨基酸残基配置的赖氨酸残基的侧链。本领域技术人员可以适宜选择这样的氨基酸残基与交联剂的组合。另外,使用dss或dsg的情况,在不包含赖氨酸残基的肽中,通过使存在于多肽的n末端的伯胺(α氨基)非修饰,从而能够特异性修饰α氨基。
[0204]
本发明中,用交联剂修饰了igg结合肽部分的本发明的肽疫苗通过与igg混合,从而能够与igg结合形成复合体。对于进行该混合的工序的条件,只要在用交联剂修饰的本发明的igg结合肽部分与igg之间发生交联反应的条件下进行就没有特别限定。例如,将包含用交联剂修饰的igg结合肽部分的本发明的肽疫苗与igg在适当的缓冲液中在室温(例如约
15℃~30℃)下混合,由此能够进行交联反应。该进行混合的工序中,也可以根据需要加入适量的促进交联反应的催化剂来进行。
[0205]
此时,为了提高igg结合肽部分与igg之间的结合性,考虑到包含用交联剂修饰的igg结合肽部分的本发明的肽疫苗和igg的种类等,可以适宜调整该进行混合的工序的其他反应条件,例如,对于反应时的ph,可以选择ph4.5~6.5(例如ph5.0~6.0、ph5.2~5.8、ph5.4~5.6、或ph约5.5)、或ph6.5~8.5(例如ph6.9~7.9、ph7.2~7.7、ph7.3~7.5、或ph约7.4)等条件,对于包含用交联剂修饰的igg结合肽部分的本发明的肽疫苗与igg的混合比率,以摩尔比计可以设为例如1:1~20:1、2:1~20:1或5:1~10:1,对于混合时间(反应时间),例如可以设为1分钟~5小时,10分钟~2小时或15分钟~1小时。
[0206]
《复合体的用途》
[0207]
本发明中,作为另一方式,可以提供递送肽疫苗的方法,其中,使用组合了上述的igg结合肽部分的本发明的肽疫苗与igg的复合体,对细胞表面具有igg所靶向的靶分子的细胞特异性递送肽疫苗。通过选择免疫细胞作为这种期望的细胞,将肽疫苗特异性递送至该免疫细胞中,由此能够有效地进行针对肽疫苗的抗体生成,能够诱导针对肽疫苗的t细胞的激活等,诱导针对肽疫苗的细胞免疫。
[0208]
本发明中,作为又一方式,可以提供目标疾病的治疗用或预防用的疫苗组合物,其包含组合了上述的igg结合肽部分的本发明的肽疫苗与igg的复合体。成为本发明的疫苗组合物的治疗/预防对象的目标疾病是指成为本发明的肽疫苗的抗原的来源的对象,例如可以列举出针对病原体的感染症、癌症等。另外,根据想要递送肽疫苗的免疫细胞来选择igg,由此能够诱导对应于免疫细胞的免疫应答,因此,可以将本发明的疫苗组合物作为用于有效地诱导针对肽疫苗的抗体生成的疫苗组合物、用于诱导针对肽疫苗的t细胞的激活等、或用于诱导针对肽疫苗的细胞免疫的疫苗组合物等。
[0209]
出于治疗目标疾病而使用的情况,本发明的疫苗组合物可以包含:针对目标疾病的肽疫苗、及针对已患有目标疾病的患者诱导想要诱导的免疫反应的免疫细胞所对应的igg。通过将该本发明的疫苗组合物向已患有目标疾病的患者给予,从而能够在该患者的体内治疗目标疾病。
[0210]
出于预防目标疾病的目的而使用的情况,本发明的疫苗组合物可以包含:针对目标疾病的肽疫苗、及针对目标疾病诱导想要诱导的优选的免疫反应的免疫细胞所对应的igg。通过向未患目标疾病的被检体给予该本发明的疫苗组合物,从而能够在该被检体的体内诱导目标疾病的原因侵入体内、在体内发生时的免疫应答。
[0211]
对于本发明的疫苗组合物,从使用igg将本发明的肽疫苗递送至免疫细胞的目的方面考虑,可以通过非经口给药(例如,静脉注射、肌肉注射、皮下给药、或腹腔内给药等)的路径给药,以对应于该给药路径的适合的剂型的形式制成各种制剂形态。本领域技术人员可以根据患者的性别、年龄、体重、症状等适宜选择给药方法和剂型。
[0212]
本发明的疫苗组合物可以包括医药上可接受的载体、添加物并且依据该技术领域中的通常的见解进行制剂化。例如,作为注射用制剂使用时,可以使用:将本发明的复合体溶解于包含例如生理盐水、缓冲液、葡萄糖溶液等的溶液中,在其中加入防容器吸附剂、例如tween80、tween20、明胶、人血清白蛋白等所得者。或者为了制成在使用前溶解而再构成的剂型,也可以为冷冻干燥品,作为用于冷冻干燥的稳定剂,例如可以使用甘露糖醇、葡萄
糖等糖醇和/或糖类。
[0213]
以下列举实施例具体地示出本发明。下述所示的实施例并非通过任意方法来限定本发明。
[0214]
实施例
[0215]
实施例1:抗cd40抗体的制造
[0216]
本实施例出于以下目的而进行:为了选择诱导疫苗特异性t细胞的树突细胞作为递送本发明的肽疫苗的免疫细胞并激活该细胞,制作针对作为其表面抗原的、特异性的cd40的激动剂抗体。
[0217]
(1)抗小鼠cd40抗体的制造
[0218]
抗小鼠cd40抗体制作成融合了作为抗小鼠cd40激动剂抗体的公知的fgk45克隆的可变区和人抗体的恒定区的嵌合抗体。fgk45克隆的可变区序列使用在ncbi(https://www.ncbi.nlm.nih.gov/)中公开的序列(重链:aei27236.1、轻链:aei27235.1)。作为表达用的载体,构建了将轻链表达元件(ef-1α启动子、分泌信号、轻链可变区、轻链恒定区串联连接)、重链表达元件(ef-1α启动子、分泌信号、重链可变区、重链恒定区串联连接)与pci-neo连接而成的质粒。
[0219]
重链可变区和轻链可变区的dna序列基于由前述的数据库获得的序列,基于按照仓鼠表达体系最适化的密码子而设计。重链恒定区和轻链恒定区的氨基酸序列可以利用规定公知的人抗体的重链恒定区部分和轻链恒定区部分的氨基酸序列或其变体的dna序列,本实施例中,作为重链恒定区部分和轻链恒定区部分的氨基酸序列,分别使用在人igg1的ch2区域具有l4a和l5a置换的突变体(igg1-lala)和人igg kappa的序列。
[0220]
作为抗体表达用的细胞,使用expicho细胞(invitrogen a2910002)。该细胞使用expicho expression medium(gibco,a2910002)进行培养,使用expicho
tm expression system(gibco a29129)将抗体表达质粒转染后,培养14天,回收培养上清液。使用蛋白a柱(monospin proa,gl sciences inc.7510-11314)将培养上清液纯化而获得抗体。
[0221]
对于纯化的抗体,基于sds-page和与小鼠脾脏细胞的结合性,确认纯度和结合性,确认得到了目标抗小鼠cd40激动剂抗体。
[0222]
(2)抗人cd40抗体的制造
[0223]
抗人cd40抗体制作成融合了作为抗人cd40激动剂抗体的公知的21.4.1克隆的可变区和人抗体的恒定区的嵌合抗体。21.4.1克隆的序列使用专利文献(日本专利第4616555号)中公开的序列。
[0224]
抗人cd40抗体表达用的载体的制造和抗体的表达/纯化利用与(1)中所述的抗小鼠cd40抗体时使用的方法相同的方法实施。
[0225]
对于纯化的抗体,基于sds-page和cd40强制表达细胞中的目标活化能力,确认纯度和结合性,确认得到了目标抗人cd40激动剂抗体。
[0226]
实施例2:肽制造
[0227]
本实施例是为了制作作为本发明的肽疫苗的例子的、针对各种靶标物质的抗原性肽而进行的。
[0228]
作为疫苗肽序列,使用:
[0229]
·
包含报道了具有在小鼠体内诱导抗原特异性t细胞的功能的h-2kb限制性ova来
源的抗原肽序列(siinfekl[肽(1)、序列号28])(vaccine.2004nov25;23(2):258-66)的16mer肽(eqlesiinfekltewt[肽(2)]、序列号29)、
[0230]
·
具有人a24:02限制性cmv来源的抗原肽序列(pvaalfff[肽(5)、序列号32])(j transl med.2005may 26;3:23)的16mer肽(rqydpvaalfffdidl[肽(6)]、序列号33)、或
[0231]
·
具有h-2db限制性新抗原adpgk来源肽序列(asmtnmelm[肽(8)、序列号35])(nature.2014nov 27;515(7528):572-6)的17mer肽(hlelasmtnmelmssiv[肽(9)]、序列号36)。
[0232]
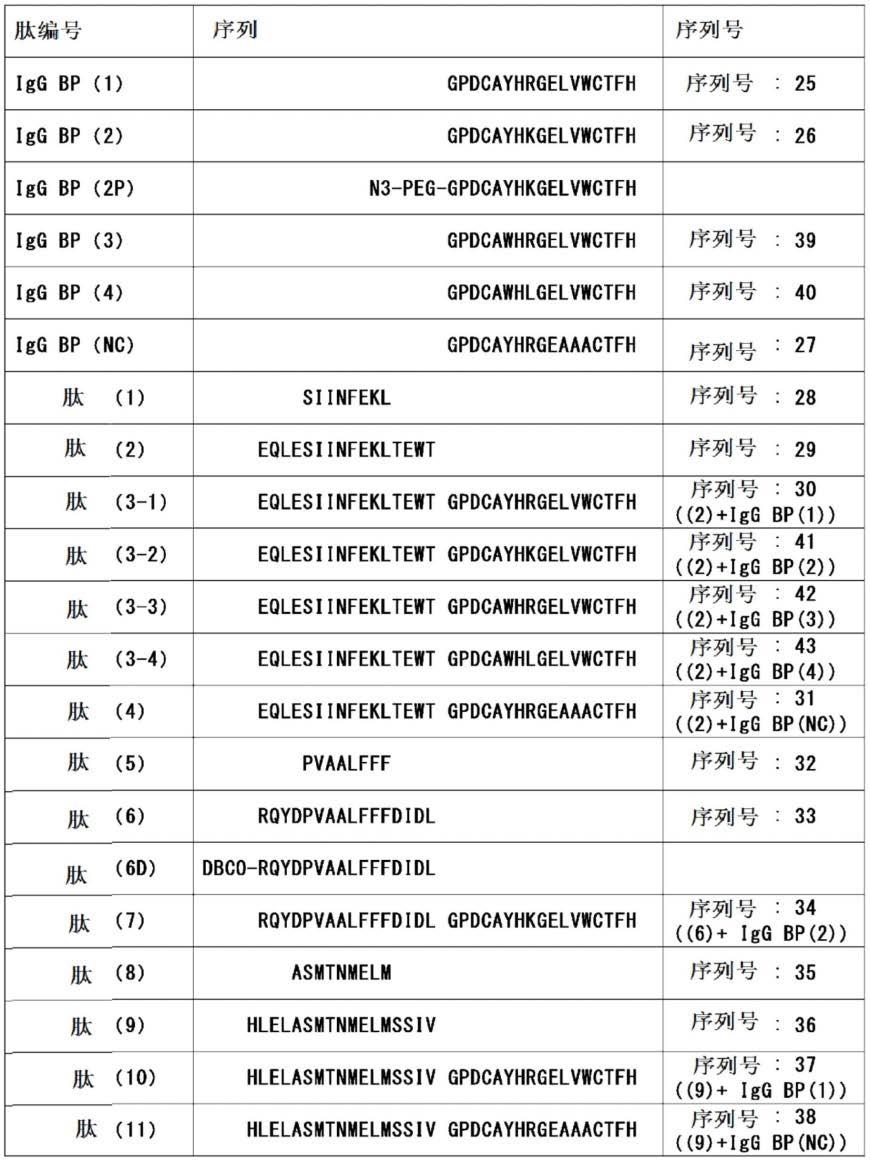
作为igg结合肽序列,使用:专利文献pct/jp2016/065061中报道的序列(gpdcayhrgelvwctfh[igg bp(1)、(序列号25)]或gpdcayhkgelvwctfh[igg bp(2)、(序列号26)])、以及新制作的序列(gpdcawhrgelvwctfh[igg bp(3)、(序列号39)]、或gpdcawhlgelvwctfh[igg bp(4)、(序列号40)])。这些序列是序列号4所述的肽的xaa6为arg、lys或leu的序列。另外,作为阴性对照的igg非结合肽序列,使用在igg结合肽中加入了部分突变的序列(gpdcayhrgeaaactfh[igg bp(nc)、序列号27])。这些igg结合肽的特征在于通过非共价键与igg抗体结合而形成复合体。
[0233]
作为基于非共价键的肽疫苗与抗体的复合体(抗体-肽疫苗复合体(非共价键型))的形成用的肽,将疫苗肽串联连接至igg结合肽的n末端侧,合成了通过二硫键交联了存在于igg结合肽的两个半胱氨酸的肽[肽(3-1)(序列号30)和肽(7)(序列号34)和(10)(序列号37)]。另外,作为对照肽,将疫苗肽串联连接至igg非结合肽(上述[igg bp(nc)(序列号27)])的n末端侧,合成了通过二硫键交联了存在于igg非结合肽序列中的两个半胱氨酸的肽[肽(4)(序列号31)和(11)(序列号38)]。
[0234]
这些肽可以利用化学合成制造。进而,作为抗体-肽疫苗复合体(共价键型)的形成用的肽,分别制作了:在抗原肽的n末端侧赋予了dbco(dibenzylcyclooctyne,二苯基环亲炔)基的dbco衍生物肽[肽(6d)]、在igg结合肽的n末端侧赋予了peg接头和叠氮基、通过二硫键交联了两个半胱氨酸的igg结合肽衍生物(igg结合肽-peg-n3[肽(2p)])。
[0235]
[表1]
[0236][0237]
实施例3:肽疫苗-抗体复合体的制作
[0238]
本实施例出于制作肽疫苗与抗体的复合体的目的而进行。在制作复合体时,使用以非共价键方式对抗体和肽疫苗进行复合体化的方法和以共价键方式进行复合体化的方法。
[0239]
基于非共价键的肽疫苗与抗体的复合体(抗体-肽疫苗复合体(非共价键型))通过如下方式制作:在室温条件下混合实施例2中制作的与igg结合肽组合而成的肽疫苗(肽(3-1)(序列号30)、肽(3-2)(序列号41)、肽(3-3)(序列号42)、肽(3-4)(序列号43)、或肽(7)(序
列号34)或肽(10)(序列号37))和实施例1中制作的抗小鼠cd40抗体或抗人cd40抗体或市售的人pd-l1抗体(medchemexpress cas no:1380723-44-3),由此进行制作。
[0240]
基于共价键的肽疫苗与抗体的复合体(抗体-肽疫苗复合体(共价键型))的情况下,首先,使用dmso,分别将dbco衍生物肽[肽(6d)]和igg结合肽-peg-n3[igg bp(2p)]制成10mm和10.8mm,进行混合并在室温下孵育2小时,由此制作两肽的融合肽(cmv-igg结合肽),接下来,将cmv-igg结合肽加入以成为摩尔比1.4倍的方式溶解于乙腈中的dsg(二琥珀酰亚胺基戊二酸酯)中,在吡啶的存在下、在50℃下孵育4小时,制作了具有与肽(7)相同的序列、经琥珀酰亚胺基戊二酸酯化的cmv-igg结合肽。
[0241]
使用hplc将该肽纯化后,以10:1的摩尔比将实施例1中制作的抗人cd40抗体或同种型对照抗体(人igg1-lala抗体、自家制备品)混合,在室温下孵育3小时。通过电泳确认抗体-肽疫苗复合体(共价键型)的生成后,通过超滤去除了低分子。
[0242]
实施例4:肽针对igg的亲和性解析
[0243]
本实施例出于调查实施例3中制作的、具有各种igg结合性肽的h-2kb限制性ova来源肽与igg的亲和性的目的而进行。
[0244]
作为评价对象的肽,使用肽(3-1)(序列号30)、肽(3-2)(序列号41)、肽(3-3)(序列号42)、肽(3-4)(序列号43)、以及肽(4)(阴性对照、序列号31)。
[0245]
对于上述4种具有不同的igg结合性肽序列的h-2kb限制性ova来源的肽,评价了与抗体的结合活性。用于评价亲和性的igg使用实施例1中制作的抗cd40抗体,进行在cm5传感器芯片(ge health care)上的固相化。
[0246]
具体而言,使用biacore 8k(ge health care),针对固相化于cm5传感器芯片上的抗cd40抗体,对于各肽的试样溶液,从3nm至243nm制备公比3倍的稀释系列,以单动力学(single kinetics)模式进行测定、解析。观测结果的解析使用biacore insight evaluation软件计算出解离常数。
[0247]
其结果,肽(3-3)的解离速率常数(kd)是与肽(3-1)同等程度的值,确认具有比肽(3-2)更高的亲和性。相对于此,确认了肽(3-4)具有比肽(3-2)肽(3-3)进一步高的亲和性。另外,作为阴性对照的肽(4)与抗cd40抗体的亲和性低而未能计算出解离速率常数、亲和性(图3、表2)。
[0248]
[表2]
[0249][0250]
备注:n.d.表示无法计算。
[0251]
实施例5:体外免疫诱导试验1(whole pbmc法)
[0252]
本实施例出于在体外调查使用了实施例3中制作的肽疫苗的抗体-肽疫苗复合体(共价键型、非共价键型)是否具有免疫诱导能力的目的而进行。
[0253]
使用包含10%血清(biowest,s4190)的rpmi1640培养基(thermo61870-0362),将由健康的志愿者获得的外周血单核细胞(pbmc)制成2
×
106个细胞/ml,以各500μl接种至24孔板(falcon,353047)中,在37℃、5%co2条件下进行培养。
[0254]
抗cd40抗体和肽(7)(序列号34)使用包含10%血清和200u/ml il-2(nipro,87890)的rpmi1640培养基,分别调整为20μg/ml和1μg/ml后,以各500μl的方式添加至接种了pbmc的孔中(终浓度分别为10μg/ml和0.5μg/ml)(组2)。
[0255]
对于基于抗cd40抗体-cmv肽的抗体-肽疫苗复合体(共价键型),使用包含与上述的组2同样的添加物的rpmi1640培养基,调整为21μg/ml,以各500μl的方式添加至接种了pbmc的孔中(终浓度10.5μg/ml)(组3)。
[0256]
作为对照,准备:
[0257]
·
使用包含10%血清和200u/ml il-2(nipro,87890)的rpmi1640培养基将抗cd40抗体调整为20μg/ml后,以各500μl的方式添加至接种了pbmc的孔中(终浓度10μg/ml)(组1),
[0258]
·
使用包含10%血清和200u/ml il-2(nipro,87890)的rpmi1640培养基,将同种型对照抗体(人igg1-lala抗体、自家制备品)和肽(7)分别调整为20μg/ml和1μg/ml后,以各500μl的方式添加至接种了pbmc的孔中(终浓度分别为10μg/ml和0.5μg/ml)(组4),以及
[0259]
·
使用包含与上述的组2同样的添加物的rpmi1640培养基,将同种型对照抗体和基于实施例3中制作的dsg化肽的抗体-肽疫苗复合体(共价键型)调整为21μg/ml,以各500μl的方式添加至接种了pbmc的孔中(终浓度10.5μg/ml)(组5)。
[0260]
使用包含10%血清和200u/ml il-2的rpmi1640培养基,将lps(sigma,l2762)、r848(invivogen,vac-r848)、poly i:c(invivogen,tlrl-pic)分别调整为800ng/ml、2mm、4μg/ml后,以各330μl的方式添加至接种了pbmc的孔中。
[0261]
在37℃、5%co2条件下培养7天后回收细胞,使用apc-cmv-tetramer(mbl,ts-0020-2c)、bv421-抗人cd3抗体(biolegend,300434)和fitc-抗人cd8抗体(biolegend,300906)进行染色,供于facs解析。
[0262]
将结果示于图4。基于cd3和cd8阳性细胞中的四聚体阳性细胞比例,评价了肽特异性的t细胞诱导。其结果,与同种型对照抗体疫苗复合体(组4和组5)相比,抗cd40抗体-肽疫苗复合体不论是非共价键型(组2)还是共价键型(组3),均有效地诱导了疫苗特异性t细胞(图4)。
[0263]
实施例6:体外免疫诱导试验2(monocyte derived dendritic cell(mddc,单核细胞来源的树突细胞)法)
[0264]
本实施例出于如下目的而进行:利用与实施例5不同的方法,在体外调查使用了实施例3中制作的肽疫苗的抗体-肽疫苗复合体(共价键型、非共价键型)是否具有免疫诱导能力。
[0265]
使用由健康的志愿者获得的pbmc,使用cd14 macs微珠(miltenyl biotec,130-050-20110)对cd14阳性单核细胞进行纯化。cd14阴性细胞使用细胞冷冻保存液(takara,
cb011)另行进行冷冻保存。
[0266]
使用包含10%fbs(sigma,172072-500ml)、10mm hepes(nacalai,17557-94)、50μm 2-巯基乙醇(2-me;nacalai,21438-82)、6.5ng/ml il-4(peprotech,200-04)、100ng/ml gm-csf(r&d,215-gm-500)的rpmi1640培养基(thermo,61870-036),将纯化的cd14阳性单核细胞制成1
×
106个细胞/ml,以各1ml接种至24孔板(falcon,353047)中,在37℃、5%co2条件下进行培养。
[0267]
自培养开始6天后回收细胞,使用包含10% fbs(sigma,172072-500ml)、非必需氨基酸(nacalai,06344-56)、1mm丙酮酸钠(nacalai,06977-34)、10mm hepes(nacalai,17557-94)、50μm 2me(nacalai,21438-82)的rpmi1640调整为6
×
104个细胞/ml,以各50μl接种至96孔u底孔板(falcon,353077)中。
[0268]
使用与上述培养单核细胞时同样的培养基,将抗人cd40抗体和肽(7)(序列号34)分别调整为40μg/ml和2μg/ml后,以各50μl添加至接种了cd14阳性单核细胞的96孔板中(终浓度分别为10μg/ml和0.5μg/ml)(组2)。
[0269]
对于基于抗cd40抗体-cmv肽的抗体-肽疫苗复合体(共价键型),使用包含与上述的组2同样的添加物的rpmi1640培养基调整为42μg/ml,以各50μl添加至接种了cd14阳性单核细胞的96孔板中(终浓度10.5μg/ml)(组3)。
[0270]
作为对照,准备:
[0271]
·
使用包含10%血清和200u/ml il-2(nipro,87890)的rpmi1640培养基,将抗人cd40抗体调整为40μg/ml后,以各50μl添加至接种了cd14阳性单核细胞的96孔板中(终浓度10μg/ml)(组1),
[0272]
·
使用包含10%血清和200u/ml il-2(nipro,87890)的rpmi1640培养基,将同种型对照抗体(人igg1-lala抗体、自家制备品)和肽(7)分别调整为40μg/ml和2μg/ml后,以各50μl添加至接种了cd14阳性单核细胞的96孔板中(终浓度分别为10μg/ml和0.5μg/ml)(组4),以及
[0273]
·
使用包含与上述的组2同样的添加物的rpmi1640培养基,将同种型对照抗体和基于实施例3中制作的dsg化肽的抗体-肽疫苗复合体(共价键型)调整为42μg/ml,以各50μl添加至接种了cd14阳性单核细胞的96孔板中(终浓度10.5μg/ml)(组5)。
[0274]
进而,与实施例5同样地,使用同样的培养基,将lps、r848、poly i:c、il-2分别调整为800ng/ml、2mm、4μg/ml、80u/ml后,以各50μl进行添加。
[0275]
在37℃、5%co2条件下在培养开始后第7天,唤醒冷冻的cd14阴性细胞,使用cd8 macs微珠(miltenyl biotec,130-045-201)对cd8阳性细胞进行纯化。使用包含10% fbs、非必需氨基酸、1mm丙酮酸钠、10mm hepes、50μm2me的rpmi1640,将细胞调整为1.8
×
106个细胞/ml,以各50μl进行添加并在37℃下培养。自试验开始后第14天回收细胞,使用apc-cmv-tetramer(mbl,ts-0020-2c)、bv421-抗cd3抗体(biolegend,300434)和fitc-抗cd8抗体(biolegend,300906)进行染色,供于facs解析。
[0276]
将结果示于图5。基于cd3和cd8阳性细胞中的四聚体阳性细胞比例,评价了肽特异性的t细胞诱导。其结果,与同种型对照抗体疫苗复合体(组4和组5)相比,抗cd40抗体疫苗复合体不论是非共价键型(组2)还是共价键型(组3),均有效地诱导了疫苗特异性t细胞(图5)。
[0277]
实施例7:野生型小鼠中的肽向树突细胞的摄入评价
[0278]
本实施例出于如下目的而进行:在体内调查皮下给药使用了实施例3中制作的肽疫苗的抗体-肽复合体时抗体-肽复合体是否被摄入存在于给药部位附近的淋巴结内的树突细胞(classical dendritic cell 1/2、(cdc1/cdc2))中。
[0279]
本实施例中,使用添加标记了荧光色素fam(6-carboxyfluorescein,6-羧基荧光素)的肽(k*rrk*rrk*rr)(“k*”表示fam-结合赖氨酸)的igg bp(1)肽(序列号25)(整体的序列为k*rrk*rrk*rrgpdcayhrgelvwctfh)作为被检肽。
[0280]
将野生型小鼠c57bl/6(clea japan,inc.)7周龄、雌性分成3组,每组3只,以表3的组构成进行实验。具体而言,分别将下述给药至腹股沟部皮下:
[0281]
·
组1:仅佐剂polyic:lc(oncovir公司制);
[0282]
·
组2:添加了荧光标记的igg bp(1)肽(被检肽)与佐剂polyic:lc(oncovir公司制)的混合物;
[0283]
·
组3:基于被检肽和抗小鼠cd40抗体的抗体-肽疫苗复合体(非共价键型)中进一步添加了佐剂polyic:lc(oncovir公司制)的混合物。
[0284]
各成分的给药量如表3所述。
[0285]
[表3]
[0286]
表3:小鼠的组构成
[0287][0288]
给药通过对每个组的小鼠单次给药药剂而进行。在5小时后回收给药部位附近的腹股沟淋巴结,将组织破碎制备淋巴结细胞后,通过抗cd11c抗体、抗i-a/i-e抗体、抗xcr1抗体、以及抗cd172a抗体进行染色,供于流式细胞术解析。
[0289]
基于cdc1细胞(cd11c /i-a/i-e /xcr1 /cd172-)和cdc2细胞(cd11c /i-a/i-e /xcr1-/cd172 )中的fam阳性细胞的比例,评价了荧光标记化igg bp(1)肽的摄入。
[0290]
将结果示于图6。根据组1与组2的对比和组1与组3的对比的结果,与没有抗体而仅单独给予肽疫苗的组(组2)相比,给予了抗体-肽疫苗复合体(非共价键型)的组(组3)中,就肽向cdc1细胞和cdc2细胞中的摄入而言显示出肽摄入的促进(图6)。
[0291]
实施例8:野生型小鼠中的免疫诱导试验1(与现有疫苗方案的比较试验)
[0292]
本实施例出于在体内调查使用了实施例3中制作的肽疫苗的抗体-肽疫苗复合体(非共价键型)是否具有免疫诱导能力的目的而进行。
[0293]
将野生型小鼠c57bl/6(clea japan,inc.)7周龄、雌性分成5组,每组6只,以表4的
组构成进行实验。具体而言,分别给予:
[0294]
·
组1:仅肽疫苗(实施例2的h-2kb限制性ova来源的肽(3-1)、序列号30);
[0295]
·
组2:肽(3-1)与佐剂polyic:lc(oncovir公司制)的混合物;
[0296]
·
组3:基于肽(3-1)和抗小鼠cd40抗体的抗体-肽疫苗复合体(非共价键型);
[0297]
·
组4:在基于肽(3-1)和抗小鼠cd40抗体的抗体-肽疫苗复合体(非共价键型)中进一步添加了佐剂polyic:lc(oncovir公司制)的混合物;
[0298]
·
组5:肽(3-1)、抗小鼠cd40抗体及佐剂均不包含的阴性对照。
[0299]
各成分的给药量如表4所述。
[0300]
给药以图7所示的日程进行。具体而言,针对每个组的小鼠,每7天进行2次皮下给药药剂(将初次给药日作为第0天,第0天和第7天)。在第14天回收脾脏,将组织破碎制备脾细胞后,通过抗cd8抗体和pe-ova tetramer(mbl,ts-5001-1c)进行染色,供于流式细胞术解析。基于cd8阳性t细胞中的四聚体阳性细胞比例,评价了ova特异性t细胞诱导。
[0301]
[表4]
[0302]
表4:小鼠的组构成
[0303][0304]
将结果示于图8。根据组1与组2的对比和组3与组4的对比的结果,在佐剂polyic:lc的存在下,显示出t细胞诱导促进能力(组1与组2、以及组3与组4)(图8)。另外,在佐剂polyic:lc的存在下,根据组2与组4的对比的结果,没有抗体而仅单独给予肽疫苗的组(组2)虽然也显示出t细胞诱导促进能力,但给予了抗体-肽疫苗复合体(非共价键型)的组(组4)与组2相比,显示出显著的t细胞诱导促进能力(组2和组4)(图8)。
[0305]
实施例9:野生型小鼠中的免疫诱导试验2(抗体-疫苗混合比率的比较试验)
[0306]
本实施例出于如下目的而进行:在体内调查使用了实施例3中制作的肽疫苗的抗体-肽疫苗复合体(非共价键型)的抗体和肽疫苗的混合比率对免疫诱导能力的影响。
[0307]
将野生型小鼠c57bl/6(clea japan,inc.)7周龄、雌性分为每组4只,以表5的组构成进行实验。具体而言,分别给予:
[0308]
·
组1:在基于2当量的肽疫苗(实施例2的h-2kb限制性ova来源的肽(3-1)、序列号30)和1当量的抗小鼠cd40抗体的抗体-肽疫苗复合体(非共价键型)中进一步添加了佐剂polyic:lc(oncovir公司制)的混合物;
[0309]
·
组2:2当量的作为对照肽的igg非结合肽(肽(4)、序列号31)、1当量的抗小鼠cd40抗体、以及佐剂polyic:lc(oncovir公司制)的混合物;
[0310]
·
组3:在基于4当量的肽(3-1)和1当量的抗小鼠cd40抗体的抗体-肽疫苗复合体(非共价键型)中进一步添加了佐剂polyic:lc(oncovir公司制)的混合物;
[0311]
·
组4:4当量的作为对照肽的igg非结合肽(肽(4))、1当量的抗小鼠cd40抗体、以及佐剂polyic:lc(oncovir公司制)的混合物。
[0312]
各给药量如表5所述。
[0313]
给药以图7所示的日程进行。具体而言,针对每个组的小鼠,每7天进行2次皮下给药药剂(将初次给药日作为第0天,第0天和第7天)。在第14天回收脾脏,利用与实施例8同样的方法,评价了ova特异性t细胞诱导。
[0314]
[表5]
[0315]
表5:小鼠的组构成
[0316][0317]
将结果示于图9。若将抗体-肽疫苗复合体(非共价键型)(抗cd40抗体:ova-igg结合肽)的组与抗体和ova-igg非结合肽的混合物的组进行比较,则2当量组(组1和组2)和4当量组(组3和组4)的任一者中,观察到复合体中的免疫诱导的效率化(图9)。基于该结果,以2当量组和4当量组进行比较的情况下,抗体与ova-igg结合肽组(组1和组3)和抗体与ova-igg非结合肽组(组2和组4)的任一者中,也观察到4当量组具有较强的免疫诱导。证实了4当量组中通过加入了过量的肽而诱导效果得到提高。
[0318]
实施例10:野生型小鼠中的免疫诱导试验3(用量依赖性试验)
[0319]
本实施例出于在体内调查使用了实施例3中制作的肽疫苗的抗体-肽疫苗复合体(非共价键型)的用量依赖性的目的而进行。
[0320]
将野生型小鼠c57bl/6(clea japan,inc.)7周龄、雌性分成每组4只,以表6的组构成进行实验。具体而言,组1~组4是给予肽疫苗的大用量组(10.5μg的肽疫苗)的情况,组5~组8是给予肽疫苗的中用量组(2.1μg的肽疫苗)的情况。具体而言,分别给予:
[0321]
·
组1:大用量(10.5μg)的肽疫苗(实施例2的h-2kb限制性ova来源的肽(3-1)、序列号30)与佐剂polyic:lc(oncovir公司制)的混合物;
[0322]
·
组2:大用量(10.5μg、相当于2当量)的基于肽疫苗(实施例2的肽(3-1))和抗小鼠cd40抗体(200μg、相当于1当量)的抗体-肽疫苗复合体(非共价键型)与佐剂polyic:lc(oncovir公司制)的混合物;
[0323]
·
组3:大用量(10.0μg)的作为对照肽的igg非结合肽(肽(4)、序列号31)与佐剂
polyic:lc(oncovir公司制)的混合物;
[0324]
·
组4:大用量(10.0μg、相当于2当量)的作为对照肽的igg非结合肽(肽(4))、抗小鼠cd40抗体(200μg、相当于1当量)的抗小鼠cd40抗体、以及佐剂polyic:lc(oncovir公司制)的混合物;
[0325]
·
组5:中用量(2.1μg)的肽疫苗(实施例2的肽(3-1))与佐剂polyic:lc(oncovir公司制)的混合物;
[0326]
·
组6:中用量(2.1μg、相当于2当量)的基于肽疫苗(实施例2的肽(3-1))和抗小鼠cd40抗体(40μg、相当于1当量)的抗体-肽疫苗复合体(非共价键型)与佐剂polyic:lc(oncovir公司制)的混合物;
[0327]
·
组7:中用量(2.0μg)的作为对照肽的igg非结合肽(肽(4))与佐剂polyic:lc(oncovir公司制)的混合物;
[0328]
·
组8:中用量(2.0μg、相当于2当量)的作为对照肽的igg非结合肽(肽(4))、抗小鼠cd40抗体(40μg、相当于1当量)的抗小鼠cd40抗体、以及佐剂polyic:lc(oncovir公司制)的混合物。
[0329]
各给药量如表6所述。
[0330]
给药以图7所示的日程进行。具体而言,针对每个组的小鼠,每7天进行2次皮下给药药剂(将初次给药日作为第0天,在第0天和第7天给药)。在第14天回收脾脏,利用与实施例8同样的方法,评价了ova特异性t细胞诱导。
[0331]
[表6]
[0332]
表6:小鼠的组构成
[0333][0334]
将结果示于图10。抗体:ova-igg结合肽组(组2和组6)与ova-igg结合肽组(组1和
组5)、ova-igg非结合肽组(组3和组7)、以及抗体:ova-igg非结合肽组(组4和组8)相比显示出高的免疫诱导效果。另外,用量依赖性地确认到该效果(图10)。
[0335]
实施例11:荷瘤小鼠试验1(抗体-肽疫苗复合体的评价:与抗cd40抗体的复合体)
[0336]
本实施例出于在体内调查使用实施例3中制作的肽疫苗与抗cd40抗体组合而制作的抗体-肽疫苗复合体(非共价键型)是否具有抗肿瘤效果。
[0337]
对于野生型小鼠c57bl/6(clea japan,inc.)7周龄、雌性,每只皮下移植1
×
106个作为强制表达了ova抗原的小鼠t细胞淋巴瘤细胞株的e.g7(atcc(注册商标)crl-2113)细胞。将移植日设为第0天,在第3天基于肿瘤体积进行分组(每组6只)。针对每个组,以表7的组构成进行实验。具体而言,针对各组,分别皮下给予:
[0338]
·
组1:仅生理盐水(阴性对照);
[0339]
·
组2:佐剂polyic:lc(oncovir公司制)(阴性对照);
[0340]
·
组3:肽(3-1)(序列号30)与佐剂polyic:lc(oncovir公司制)的混合物;
[0341]
·
组4:基于肽(3-1)和抗小鼠cd40抗体的抗体-肽疫苗复合体(非共价键型)与佐剂polyic:lc(oncovir公司制)的混合物;
[0342]
·
组5:作为对照肽的igg非结合肽(肽(4)、序列号31)与佐剂polyic:lc(oncovir公司制)的混合物;
[0343]
·
组6:作为对照肽的igg非结合肽(肽(4))、抗小鼠cd40抗体、以及佐剂polyic:lc(oncovir公司制)的混合物。
[0344]
各接种量如表7所述。
[0345]
对于每个组的药剂的给药,针对每个组的小鼠,在第3天和第10天总计皮下进行2次,自药剂给药开始日起以每周2次的频率进行肿瘤体积和体重的观察。
[0346]
[表7]
[0347]
表7:小鼠的组构成
[0348][0349]
将结果示于图11和图12。证实了抗体:ova-igg结合肽组(组4)与ova-igg结合肽组(组3)、ova-igg非结合肽组(组5)、以及抗体:ova-igg非结合肽组(组6)相比,在生物体内也
14572)、20mm hepes(wako,345-06681)、1%青霉素-链霉素(nakarai、26253-84)的rpmi-1640(thermo 61870-0362))中,添加溶解有肽(8)(序列号35)的溶液100μl而使其终浓度为10μg/ml,在37℃、5%co2条件下培养15小时。
[0365]
添加10
×
brefeldin a(biolegend 420601)22μl并孵育3~4小时后,以2000rpm进行离心并回收细胞,用zombie紫(biolegend 423114)、apc抗小鼠cd4(biolegend 100412)、fitc抗小鼠cd8a(biolegend 100706)、pe抗小鼠ifn-g(biolegend 505807)进行染色并供于流式细胞术解析。基于cd8阳性细胞中的ifnγ阳性细胞比例,评价了针对adpgk肽的免疫激活。
[0366]
将结果示于图14。抗体:adpgk-igg结合肽组(组2)与adpgk-igg结合肽组(组1)、adpgk-igg非结合肽组(组3)、以及抗体:adpgk-igg非结合肽组(组4)相比,显示出高的免疫诱导效果。如此,在抗体结合新抗原(组2)中得到了最高的免疫诱导,因此在本模型中启示出抗体疫苗的有用性。
[0367]
实施例13:野生型小鼠中的免疫诱导试验5(多种抗体-疫苗肽的评价)
[0368]
本实施例出于如下目的而进行:在体内调查使用实施例3中制作的肽疫苗、并且组合cd40抗体或pd-l1抗体而成的抗体-肽疫苗复合体(非共价键型)是否具有免疫诱导能力。
[0369]
本实施例的情况,首先,将野生型小鼠c57bl/6(clea japan,inc.)7周龄、雌性分成4组,每组5只,以表9的组构成进行实验。具体而言,分别给予:
[0370]
·
组1:仅佐剂polyic:lc(oncovir公司制);
[0371]
·
组2:肽疫苗(实施例2的h-2kb限制性ova来源的肽(3-1)、序列号30)与佐剂polyic:lc(oncovir公司制)的混合物;
[0372]
·
组3:在基于肽(3-1)和抗小鼠cd40抗体的抗体-肽疫苗复合体(非共价键型)中进一步添加了佐剂polyic:lc(oncovir公司制)的混合物;
[0373]
·
组4:在基于肽(3-1)和抗pd-l1抗体的抗体-肽疫苗复合体(非共价键)中进一步添加了佐剂polyic:lc(oncovir公司制)的混合物。
[0374]
本实施例中,作为pd-l1抗体,使用人pd-l1抗体(medchemexpress casno:1380723-44-3)。各成分的给药量如表9所述。
[0375]
[表9]
[0376]
表9:小鼠的组构成
[0377][0378]
给药以图15所示的日程进行。具体而言,针对每个组的小鼠,将药剂每隔7天进行2次皮下给药(将初次给药日作为第0天,在第0天和第7天给药)。在第14天回收脾脏,利用与实施例8同样的方法,评价了ova特异性t细胞诱导。
[0379]
将结果示于图16。根据组2与组3的对比和组2与组4的对比的结果,没有抗体而给予了肽疫苗及佐剂的组(组2)中也显示出t细胞诱导促进能力,但与给予了cd40抗体-肽疫苗非共价键复合体的组(组3)同样地,给予了pd-l1抗体-肽疫苗非共价键复合体的组(组4)与组2相比,显示出显著的t细胞诱导促进能力(组3和组4)(图16)。
[0380]
实施例14:野生型小鼠中的免疫诱导试验6(多种抗体-疫苗肽的评价)
[0381]
本实施例出于如下目的而进行:与实施例13同样地,在体内调查使用实施例3中制作的肽疫苗、并且组合cd40抗体或pd-l1抗体而成的抗体-肽疫苗复合体(非共价键型)相对于未形成复合体的肽疫苗和抗体的混合给药而言是否具有增强免疫诱导的能力。
[0382]
将野生型小鼠c57bl/6(clea japan,inc.)7周龄、雌性分成5组,每组6只,以表10的组构成进行实验。具体而言,分别给药:
[0383]
·
组1:仅佐剂polyic:lc(oncovir公司制);
[0384]
·
组2:在作为对照肽的igg非结合肽(肽(4)、序列号31)和抗小鼠cd40抗体中进一步添加了佐剂polyic:lc(oncovir公司制)的混合物;
[0385]
·
组3:在基于肽(3-1)和抗小鼠cd40抗体的抗体-肽疫苗复合体(非共价键型)中进一步添加了佐剂polyic:lc(oncovir公司制)的混合物;
[0386]
·
组4:在肽(4)和抗pd-l1抗体中进一步添加了佐剂polyic:lc(oncovir公司制)的混合物;
[0387]
·
组5:在基于肽(3-1)和抗pd-l1抗体的抗体-肽疫苗复合体(非共价键型)中进一步添加了佐剂polyic:lc(oncovir公司制)的混合物。
[0388]
本实施例中,作为pd-l1抗体,使用人pd-l1抗体(medchemexpress casno:1380723-44-3)。各成分的给药量如表10所述。
[0389]
[表10]
[0390]
表10:小鼠的组构成
[0391][0392]
给药与实施例13同样地以图15所示的日程进行。具体而言,针对每个组的小鼠,将药剂每隔7天进行2次皮下给药(将初次给药日作为第0天,在第0天和第7天给药)。在第14天回收脾脏,利用与实施例8同样的方法,评价了ova特异性t细胞诱导。
[0393]
将结果示于图17。根据组2与组3的对比和组4与组5的对比的结果,给予了未与抗体结合的肽疫苗及抗体的组(组2和组4)中也显示出t细胞诱导,但给予了cd40抗体-肽疫苗复合体(非共价键型)(组3)、或者pd-l1抗体-肽疫苗复合体(非共价键型)的组(组5)中,t细胞诱导显示出显著的亢进(图17)。
[0394]
实施例15:荷瘤小鼠试验2(抗体-肽疫苗复合体的评价:与抗pd-l1抗体的复合体)
[0395]
本实施例出于如下目的而进行:在体内调查使用实施例3中制作的肽疫苗、与抗pd-l1抗体组合而制作的抗体-肽疫苗复合体(非共价键型)是否具有抗肿瘤效果。
[0396]
针对野生型小鼠c57bl/6(clea japan,inc.)7周龄、雌性,每只皮下移植1
×
106个作为强制表达了ova抗原的小鼠t细胞淋巴瘤细胞株的e.g7(atcc(注册商标)crl-2113)细胞。将移植日设为第0天,在第4天基于肿瘤体积进行分组(每组6只)。对每个组以表11的组构成进行实验。具体而言,针对每个组,分别皮下给予:
[0397]
·
组1:佐剂polyic:lc(oncovir公司制)(阴性对照);
[0398]
·
组2:肽(3-1)(序列号30)与佐剂polyiclc(oncovir公司制)的混合物;
[0399]
·
组3:抗pd-l1抗体单体和佐剂polyiclc(oncovir公司制)的混合物(对照);
[0400]
·
组4:基于肽(3-1)和抗pd-l1抗体的抗体-肽疫苗复合体(非共价键型)与佐剂polyic:lc(oncovir公司制)的混合物。
[0401]
本实施例中,作为pd-l1抗体,使用人pd-l1抗体(medchemexpress casno:1380723-44-3)。各接种量如表11所述。
[0402]
对于每个组的药剂的给药,针对每个组的小鼠,在第4天和第11天总计在皮下进行2次,自药剂给药开始日起以每周2次的频率进行肿瘤体积和体重的观察。
[0403]
[表11]
[0404]
表11:小鼠的组构成
[0405][0406]
将结果示于图18和图19。证实了抗体:ova-igg结合肽组(组4)与ova-igg结合肽组(组2)、抗pd-l1抗体单体组(组3)相比,在体内也显示出高的肿瘤增殖抑制效果(图18)。
[0407]
进而,对每个个体的存活期进行了确认,结果确认,ova-igg结合肽组(组4)与抗体:ova-igg结合肽组(组2)、抗pd-l1抗体单体组(组3)相比,有显著的存活期延长效果(图19)。
[0408]
实施例16:野生型小鼠中的免疫诱导试验7(新抗原模型)
[0409]
本实施例出于在体内调查包含小鼠肿瘤细胞株的非同义体细胞突变序列的抗体-肽疫苗复合体(非共价键型)是否具有抗肿瘤效果而进行。
[0410]
首先,作为小鼠肿瘤细胞株的非同义体细胞突变序列,基于由小鼠肿瘤细胞株mc-38得到的基因组序列的解析结果,如下述的表12所示制作了包含非同义体细胞突变序列的肽(各27mer、肽(101)~肽(130)的30种肽)。
[0411]
[表12]
[0412]
表12:小鼠肿瘤细胞株的非同义体细胞突变序列
[0413][0414]
接下来,如下述的表13所示制作了对上述表所述的肽疫苗(27mer、肽(101)~肽(130))添加了igg bp(1)(序列号25)的肽(各44mer、肽(101bp)~肽(130bp)的30种肽)。
[0415]
[表13]
[0416]
表13:基于小鼠肿瘤细胞株的非间义体细饱突变序列的igg结合性肽
[0417][0418]
注:igg bp(1):gpdcayhrgelvwctfh(序列号:25)
[0419]
将野生型小鼠c57bl/6(clea japan,inc.)7周龄、雌性分为2组,以表14的组构成进行实验。具体而言,针对每个组,对2只小鼠,将下述各池的每一池进行皮下给予:
[0420]
·
组1:对于上述表12所述的肽疫苗(各27mer、肽(101)~肽(130)),制成各6种肽的池的疫苗肽(例:池01(肽(101)~肽(106))、池06(肽(125)~肽(130)))与佐剂polyic:lc
(oncovir公司制)的混合物;
[0421]
·
组2:将使抗小鼠cd40抗体与上述表13记载的igg结合性肽(各44mer、肽(101bp)~肽(130bp))复合体化而成的抗体-肽疫苗复合体(非共价键型)制成各3种肽的池的抗体-肽疫苗复合体(非共价键型)(例:池11(肽(101bp)~肽(103bp))、池20(肽(128bp)~肽(130bp))),组2为该各3种肽的池的抗体-肽疫苗复合体与佐剂polyic:lc(oncovir公司制)的混合物。
[0422]
各接种量如表14所述。
[0423]
[表14]
[0424]
表14:小鼠的组构成
[0425][0426]
给药以图20所示的日程进行。具体而言,针对每个组的小鼠,将药剂每隔7天皮下给药(将初次给药日作为第0天,在第0天、第7天和第14天给药),给药3次。在第21天回收脾脏后,将2
×
106个细胞悬浮于100μl的脾细胞生长培养基(包含10%fbs(biowest,s4190)、1mm丙酮酸钠(wako,190-14881)、0.05mm 2-me(wako,131-14572)、20mm hepes(wako,345-06681)、1%青霉素-链霉素(nakarai、26253-84)的rpmi-1640(thermo 61870-0362))中,接种至涂敷有小鼠ifn-γ抗体(mabtech)的过滤板(millipore)中,以终浓度为10μg/ml的方式添加分别溶解有表15中记载的作为各肽的表位肽的肽(101e)~肽(130e))(序列号74~序列号103)的溶液100μl,在37℃、5%co2条件下培养15小时。
[0427]
[表15]
[0428]
表15:各肽的表位肽序列
[0429]
表位肽序列序列号肽(101e)msyflqgtl序列号:74肽(102e)fslsfqhpv序列号:75肽(103e)sawvpfggl序列号:76肽(104e)saiqanipl序列号:77肽(105e)svtvfvnnl序列号:78肽(106e)asyngflpv序列号:79肽(107e)vlygliaam序列号:80肽(108e)vspqhrpvl序列号:81肽(109e)savdfklhi序列号:82肽(110e)amqsrlptl序列号:83肽(111e)sappllegpl序列号:84
肽(112e)vvldvtasl序列号:85肽(113e)asmtnmelm序列号:86肽(114e)svltrlrtpm序列号:87肽(115e)vsfrsifkdl序列号:88肽(116e)ssltssvpv序列号:89肽(117e)vatinfrrl序列号:90肽(118e)isfknltrv序列号:91肽(119e)aampinkati序列号:92肽(120e)ctlqfeaal序列号:93肽(121 e)vtffcfqvl序列号:94肽(122e)malstyyal序列号:95肽(123e)ysfcdvkqyi序列号:96肽(124e)kgyphwpal序列号:97肽(125e)aqlqnltst序列号:98肽(126e)aspvspgepl序列号:99肽(127e)rsftgavtl序列号:100肽(128e)rsptsvnav序列号:101肽(129e)vswnqdpfl序列号:102肽(130e)walriritl序列号:103
[0430]
通过送气(aspirate)去除脾细胞和添加的各肽,进而清洗过滤板后,添加生物素标记小鼠ifn-γ抗体(mabtech)100μl并在37℃下孵育2小时。清洗过滤板,添加链霉亲和素-alp(mabtech)100μl进而孵育1小时。再次清洗过滤板,添加底物溶液(mabtech;bcip/nbt-plus)100μl,检测细胞分泌的ifnγ。
[0431]
将结果示于图21。确认了:与27mer肽疫苗组(组1)相比,给予了基于抗小鼠cd40抗体的抗体-肽疫苗复合体(非共价键型)的组(组2)对于同一表位序列引起了更强的免疫应答。
[0432]
产业上的可利用性
[0433]
本发明中公开的、与igg结合肽组合而成的肽疫苗能够有效地进行肽疫苗向特定的免疫细胞(例如树突细胞)表面的递送,增强其激活,能够增强肽疫苗的效果。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。