longum)在治疗和预防肠炎方面的用途,所述长栖粪杆菌于2016年6月13日保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏地址为中国北京市朝阳区北辰西路1号院3号,保藏编号为cgmcc 1.5208,分类命名为:长栖粪杆菌faecalibacterium longum。根据本发明实施例的长栖粪杆菌cm04-06对dss诱导的uc小鼠在抑制uc小鼠体重下降、dai升高及结肠缩短病症的治疗和预防作用显著优于现有商业溃疡性肠炎药物。
10.在本发明的第二方面,本发明提出了长栖粪杆菌(faecalibacterium longum)在制备药物、保健品、食品或组合物中的用途,所述长栖粪杆菌于2016年6月13日保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏地址为中国北京市朝阳区北辰西路1号院 3号,保藏编号为cgmcc 1.5208,分类命名为:长栖粪杆菌faecalibacterium longum,所述药物、保健品、食品或组合物用于下列的至少之一:治疗和预防肠炎、抑制肠炎诱导的体重下降、dai升高、改善肠道变化。
11.根据本发明的实施例,上述用途还可以进一步包括如下附加技术特征至少之一:
12.根据本发明的实施例,所述肠炎为溃疡性肠炎。
13.根据本发明的实施例,所述溃疡性肠炎为溃疡性结肠炎。
14.根据本发明的实施例,所述肠道的变化为结肠组织缩短。
15.根据本发明实施例的长栖粪杆菌cm04-06具有很好的抑制肠炎诱导的体重下降、疾病活动指数(dai)的升高及改善肠炎诱导的肠道变化的作用,利用根据本发明实施例的长栖粪杆菌cm04-06所制备的药物、保健品、食品及组合物在治疗、预防溃疡性结肠炎上效果显著。
16.根据本发明的实施例,所述长栖粪杆菌的浓度为1.0
×
106cfu/ml~1.0
×
109cfu/ml。进而利用长栖粪杆菌cm04-06所制备的药物、保健品或食品在治疗、预防或缓解溃疡性肠炎、抑制肠炎诱导的体重下降、dai的升高及改善肠道变化方面效果更优。
17.在本发明的第三方面,本发明提出了一种组合物。根据本发明的实施例,所述组合物包含:前面所述的长栖粪杆菌(faecalibacterium longum),所述长栖粪杆菌于2016年6月13日保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏地址为中国北京市朝阳区北辰西路1号院3号,保藏编号为cgmcc 1.5208,分类命名为:长栖粪杆菌 faecalibacterium longum。包含根据本发明实施例的长栖粪杆菌cm04-06的组合物在抑制肠炎诱导的体重下降、dai的升高及改善肠道变化方面优于现有溃疡性肠炎药物。
18.在本发明的第四方面,本发明提出了一种药物。根据本发明的实施例,所述药物包含:长栖粪杆菌(faecalibacterium longum),所述长栖粪杆菌于2016年6月13日保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏地址为中国北京市朝阳区北辰西路1号院3号,保藏编号为cgmcc 1.5208,分类命名为:长栖粪杆菌faecalibacterium longum。包含根据本发明实施例的长栖粪杆菌cm04-06的药物在抑制肠炎诱导的体重下降、dai的升高及改善肠道变化方面优于现有溃疡性肠炎药物。
19.根据本发明的实施例,所述药物还可以进一步包括如下附加技术特征至少之一:
20.根据本发明的实施例,所述药物组合物进一步包括:药学上可接受的辅剂。
21.根据本发明的实施例,所述药学上可接受的辅剂包括稳定剂、湿润剂、乳化剂、粘合剂、等渗剂的至少之一。
22.根据本发明的实施例,所述药物呈片剂、颗粒剂、散剂、胶囊剂、溶液剂、悬浮剂、冻
干制剂的至少一种。进而,根据本发明实施例的药物方便给药,适于保持长栖粪杆菌的最佳活性。
23.根据本发明的实施例,所述药物的给药剂量不受特别限制,实际应用中,可以根据给药对象的健康状况灵活选择。
24.根据本发明的一些实施例,该实施例所述的药物为复合益生菌。
25.在本发明的第五方面,本发明提出了一种长栖粪杆菌胶囊。根据本发明的实施例,所述长栖粪杆菌胶囊包含:长栖粪杆菌冻干粉、麦芽糊精,所述长栖粪杆菌冻干粉与所述麦芽糊精的质量比为1:1,其中,所述长栖粪杆菌于2016年6月13日保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏地址为中国北京市朝阳区北辰西路1号院3号,保藏编号为cgmcc 1.5208,分类命名为:长栖粪杆菌faecalibacterium longum。包含根据本发明实施例的长栖粪杆菌cm04-06的胶囊在抑制肠炎诱导的体重下降、dai的升高及改善肠道变化方面优于现有溃疡性肠炎药物。
26.根据本发明的实施例,上述长栖粪杆菌胶囊还可以进一步包括如下附加技术特征至少之一:
27.根据本发明的实施例,所述长栖粪杆菌胶囊进一步包括:0.5g的长栖粪杆菌冻干粉以及0.5g的麦芽糊精。
28.根据本发明的实施例,所述长栖粪杆菌冻干粉是将活菌含量为1~500
×
106cfu/ml的长栖粪杆菌活菌进行冻干获得的。
29.根据本发明的实施例,所述长栖粪杆菌冻干粉包括:0.8~1.2质量份所述长栖粪杆菌活菌、1.8~2.2质量份的乳糖、1.8~2.2质量份的酵母粉、0.8~1.2质量份的蛋白胨、90~95质量份的纯净水及0.3~1质量份的维生素c可保持较高活性。
30.在本发明的第六方面,本发明提出了一种长栖粪杆菌制剂。根据本发明的实施例,所述制剂包含:4~6体积生长因子、0.5~1.5体积的维生素c、95~105体积的长栖粪杆菌发酵菌液,其中,所述长栖粪杆菌于2016年6月13日保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏地址为中国北京市朝阳区北辰西路1号院3号,保藏编号为cgmcc 1.5208,分类命名为:长栖粪杆菌faecalibacterium longum。包含根据本发明实施例的长栖粪杆菌cm04-06的制剂在抑制肠炎诱导的体重下降、dai的升高及改善肠道变化方面优于现有溃疡性肠炎药物。
31.根据本发明的实施例,上述长栖粪杆菌制剂还可以进一步包括如下附加技术特征至少之一:
32.根据本发明的实施例,所述生长因子为牛奶生长因子粗提物。
33.根据本发明的实施例,所述生长因子进一步为维生素类物质、嘌呤类物质、嘧啶类物质的至少之一。
34.根据本发明的实施例,所述生长因子是通过将脱脂牛奶、酪蛋白依次进行混合处理、离心处理和超滤处理后获得的牛奶生长因子粗提物。
35.根据本发明的实施例,所述长栖粪杆菌发酵菌液是通过将所述长栖粪杆菌在37℃的条件下进行厌氧发酵处理2~3天后获得的。
36.根据本发明的实施例,所述长栖粪杆菌制剂进一步包括:麦芽糊精。
37.在本发明的第七方面,本发明提出了一种食品。根据本发明的实施例,所述食品包
含:长栖粪杆菌(faecalibacterium longum),所述长栖粪杆菌于2016年6月13日保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏地址为中国北京市朝阳区北辰西路1号院3号,保藏编号为cgmcc 1.5208,分类命名为:长栖粪杆菌faecalibacterium longum。
38.需要说明的是,本技术所述的食品应做广义的理解,任何可咀嚼、吞咽或能为机体提供能量的物质均可视为食品,如膨化食品、乳制品、饼干、口香糖、冰激凌等。
39.根据本发明的实施例,上述食品还可以进一步包括如下附加技术特征至少之一:
40.根据本发明的实施例,所述食品进一步包括:食品学上可接受的添加剂。进而所述食品的口感更佳。
41.根据本发明的实施例,所述食品为牛乳、口香糖、饼干、压片糖果、固体饮料等。进而长栖粪杆菌cm04-06可在食品中保持较佳的活性,适于在机体中发挥功效。
42.另外,需要说明的是,本发明的长栖粪杆菌cm04-06可以与通常的食品中所使用的食品材料配合食用。例如,谷类及薯类:谷类包括米、面、杂粮,薯类包括马铃薯、红薯等;动物性食物,包括肉、禽、鱼、奶、蛋等;豆类及其制品,包括大豆及其他干豆类;蔬菜水果类,包括鲜豆、根茎、叶菜、茄果等;纯热能食物,包括动植物油、淀粉、食用糖和酒类等。
43.在本发明的第八方面,本发明提出了一种食品组合物。根据本发明的实施例,所述食品包含:0.3~0.8质量份长栖粪杆菌活菌、85~95质量份牛奶、8.5~9.5质量份白糖以及0.3~0.8 质量份的维生素c,所述长栖粪杆菌于2016年6月13日保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏地址为中国北京市朝阳区北辰西路1号院3号,保藏编号为 cgmcc 1.5208,分类命名为:长栖粪杆菌faecalibacterium longum。
44.根据本发明的实施例,上述食品组合物还可以进一步包括如下附加技术特征至少之一:
45.根据本发明的实施例,所述食品组合物中所述长栖粪杆菌的含量为1~100
×
106cfu/g可保持较高活性。
46.根据本发明的实施例,所述食品组合物是通过将所述牛奶、白糖依次进行混合、均质、灭菌以及冷却处理,其中,所述均质是在20mpa的条件下进行,所述灭菌是在90℃的条件下进行5~10分钟,所述冷却处理后的温度为40~43℃,将冷却处理产物中加入所述维生素 c,再向所述冷却处理产物与所述维生素c的混合物中接入所述长栖粪杆菌。进而长栖粪杆菌cm04-06可在食品组合物中保持较佳的活性,适于在机体中发挥功效。
47.本发明的附加方面和优点将在下面的描述中部分给出,部分将从下面的描述中变得明显,或通过本发明的实践了解到。
48.保藏信息:
49.菌株名称:faecalibacterium longum
50.保藏日期:2016年6月13日
51.保藏单位:中国微生物菌种保藏管理委员会普通微生物中心
52.保藏编号:cgmcc 1.5208
53.地址:中国北京市朝阳区北辰西路1号院3号
附图说明
54.本发明的上述和/或附加的方面和优点从结合下面附图对实施例的描述中将变得
明显和容易理解,其中:
55.图1是根据本发明实施例的长栖粪杆菌cm04-06使用megax软件绘制的邻接法进化树;
56.图2是根据本发明实施例的长栖粪杆菌cm04-06干预小鼠后小鼠体重变化的结果图;以及
57.图3是根据本发明实施例的长栖粪杆菌cm04-06干预小鼠后小鼠dai评分变化的结果图。
具体实施方式
58.下面详细描述本发明的实施例,所述实施例的示例在附图中示出。下面通过参考附图描述的实施例是示例性的,旨在用于解释本发明,而不能理解为对本发明的限制。
59.以下实施例通过体外益生特性评估筛选出了一株有预防治疗溃疡性肠炎的长栖粪杆菌 cm04-06菌株,为了验证该菌株在体内治疗和缓解溃疡性肠炎的功效,发明人采用了一种肠炎小鼠模型来开展功能验证实验。利用葡聚糖硫酸钠(dextran sulfate sodium,dss)作为诱导剂,引起小鼠腹泻、诱导肠道炎症发生,以建立肠炎小鼠模型,dss诱发的小鼠模型是应用最为广泛的急性溃疡性肠炎动物模型。
60.根据下面的实施例可以看出,本发明选用的长栖粪杆菌cm04-06(cm04-06于2016 年6月13日保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏地址为中国北京市朝阳区北辰西路1号院3号,保藏编号为cgmcc 1.5208具有较好的缓解溃疡性肠炎功效。具体表现在显著缓解dss所致的溃疡性肠炎小鼠的表观状态,降低小鼠疾病活动指数及炎症性反应。
61.下面将对实施例作具体介绍。
62.实施例1长栖粪杆菌cm04-06的筛选鉴定
63.1、cm04-06的分离培养
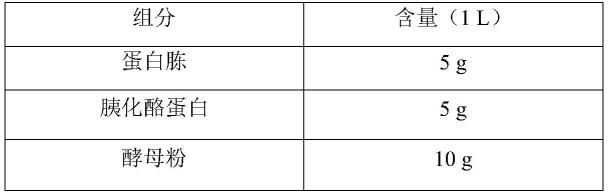
64.本发明所述长栖粪杆菌cm04-06分离于深圳市一位健康的儿童(男性)的粪便样品。分离培养的环境是严格厌氧条件,具体的分离过程是:在厌氧操作箱中取0.2g左右的粪便样品,使用1ml无菌的pbs进行悬浮分散,充分震荡混匀后进行梯度稀释涂布,培养基采用厌氧的pyg培养基,具体组分见表1,其中,无机盐溶液组成如表2 所示:
65.表1:pyg培养基配方
66.[0067][0068]
表2:无机盐溶液配方
[0069]
无机盐组分含量(1g/l)cacl2·
2h2o0.25mgso4·
7h2o0.5k2hpo41kh2po41nahco310nacl2
[0070]
涂布平板置于37℃厌氧条件下培养3~4天,待平板表面生长出菌落后,挑取单菌落进行划线分纯,直至获得纯培养菌株,分离到的菌株采用甘油进行-80℃冷冻保藏。
[0071]
2、长栖粪杆菌cm04-06的16s rdna鉴定
[0072]
(1)基因组提取:对分离到的菌株进行培养,待菌浓达到108cfu/ml数量级时取 2ml菌液进行基因组dna提取。
[0073]
(2)16s rdna的pcr扩增:以dna作为模板进行16s rdna扩增,扩增引物选用16s rdna的通用扩增引物:8f-1492r(5
’‑
agagtttgatcatggctcag-3’和 5
’‑
tagggttaccttgttacgactt-3’),pcr扩增程序是:
[0074]
ezbiocloud数据库的比对,获得同cm04-06亲缘关系较近的物种,将这些物种和 cm04-06的16s rdna序列进行对序列比对,然后使用megax软件绘制邻接法 (neighbour-joining)进化树(图1)。根据进化树可以进一步确定cm04-06的分类位置为faecalibacterium属,进化关系最近的物种是atcc 27768。
[0083]
4、cm04-06的微生物学特征
[0084]
(1)形态学特征:cm04-06在厌氧环境中37℃培养2~3天,菌落为黄白色,含水量较高,有点黏稠,近圆形,不透明,扁平中间凸起,菌落直径约2-3mm。
[0085]
(2)显微学特征:在1000倍显微镜放大下,cm04-06的菌体为长杆状,革兰氏染色反应为阴性,未发现芽孢和鞭毛,菌体的直径大约为1um,长度为4~10um。
[0086]
(3)生理生化特征:氧化酶和过氧化氢酶反应均为阴性,生长温度的范围是 30~45℃,ph值范围是4.0~9.0,最适温度和ph值是37℃和ph 7.0。能耐受3%的nacl。 cm04-06同亲缘关系最近的参考菌atcc 27768的生理生化反应(包括底物利用情况 api 20a和酶反应api zym)的比较如表3所示:( ,表示阳性反应;-,表示阴性反应;w表示弱阳性反应)。
[0087]
表3:cm04-06和atcc 27768生物生化特征
[0088][0089]
通过上述对cm04-06同参考菌的生理生化反应比较显示,cm04-06在棉籽糖和海藻糖的利用,七叶灵和明胶水解以及酯酶(c4)、缬氨酸芳胺酶、胱氨酸芳胺酶、胰凝乳蛋白酶、
萘酚-as-bi-磷酸水解酶、β-糖醛酸甙酶、α-葡萄糖甙酶和n-乙酰-葡萄糖胺酶的活性等方面有显著区别,可以证明cm04-06是一株不同于已知菌的新种。
[0090]
5、细胞脂肪酸的分析
[0091]
将培养至稳定期的cm04-06和atcc 27768进行菌体收集,然后进行细胞脂肪酸的提取,检测。通过气相色谱分析两株菌细胞脂肪酸的含量及差异,具体结果如表4所示。
[0092]
表4:cm04-06和atcc 27768细胞脂肪酸含量
[0093][0094]
脂肪酸的分析结果显示,cm04-06同参考菌株atcc 27768相比,主要脂肪酸(》10%) 组成较为相似,包含十四碳饱和脂肪酸,十六碳饱和脂肪酸,ω9c-十八碳双不饱和脂肪酸,但具体含量具有一定差异。
[0095]
综合以上cm04-06表型、16s rdna进化分析、生理生化反应以及细胞化学组分的分析数据显示,cm04-06是faecalibacterium属的一株新种,将其命名为长栖粪杆菌 faecalibacterium longum。
[0096]
实施例2长栖粪杆菌faecalibacterium longum cm04-06分泌的生物活性物质
[0097]
1、短链脂肪酸(scfa)的检测
[0098]
(1)样品制备:取培养48h的cm04-06菌液1ml,12000r/min离心5min,吸取上清液,备用。
[0099]
(2)scfa的测定:短链脂肪酸的测定采用外标法,选用乙酸、丙酸、丁酸、戊酸进行标准曲线的制作。采用安捷伦气象色谱仪(gc-7890b,agilent),选用 hp-innowax(cross-linked peg),30m
×
0.25mm
×
0.25um的毛细柱进行分析,检测器为氢火焰离子检测器,gc参数设置为柱温:180~200℃;气化室温度:240℃;检测温度:210℃;进样量:2μl;载气流量:n2,50ml/min;氢气流量:50ml/min;空气流量:600~700ml/ min。
[0100]
(3)结果:测定得出scfa产量为:甲酸(7.62mmol/l),乙酸(44.8mmol/l),丁酸 (40.03mmol/l)。
[0101]
2、有机酸的检测
[0102]
(1)样品制备:同上述scfa的检测
[0103]
(2)有机酸的测定:有机酸的检测标准品选用:3-甲基丁酸,戊酸,奎宁酸,乳酸,草酸,丙二酸,苯甲酸,马来酸,丁二酸,反富马酸,苹果酸,己二酸,酒石酸,莽草酸,柠檬酸,异柠檬酸和l-抗坏血酸。仍然采用安捷伦气象色谱仪(gc-7890b,agilent),色谱柱选用122-5532g db-5ms(40m
×
0.25mm
×
0.25um),柱温:270~290℃;进样口温度: 250℃;气体流量:0.86ml/min。
[0104]
(3)结果:测定得出有机酸产量详见表5。
[0105]
表5:长栖粪杆菌cm04-06有机酸产量
[0106]
有机酸3-甲基丁酸戊酸奎宁酸乳酸草酸丙二酸含量(mmol/l)0.260.49030.5300有机酸苯甲酸马来酸丁二酸反富马酸苹果酸己二酸含量(mmol/l)1.7900.88000.60有机酸酒石酸莽草酸柠檬酸异柠檬酸l-抗坏血酸 含量(mmol/l)000.00.11 [0107]
实施例3长栖粪杆菌faecalibacterium longum cm04-06对uc小鼠的治疗
[0108]
本实施例所选取的小鼠模型为:dss诱导的溃疡性肠炎小鼠模型,采用c57bl/6小鼠 (购自广东省医学实验动物中心),8周龄,体重20g
±
2g,小鼠饲养环境为spf级,适应性喂养1周进行dss诱导,连续给小鼠饮用2.5%的dss(分子量36000-50000)7天。采用vsl#3(购自美国sigma tau)作为阳性对照,比较长栖粪杆菌cm04-06和vsl#3的治疗效果。
[0109]
试验小鼠总计48只,随机分为4组,每组15只,其中包括对照组(control组),dss 诱导的模型组(每只每天灌胃0.2ml pbs),长栖粪杆菌cm04-06治疗组和vsl#3治疗组。
[0110]
长栖粪杆菌cm04-06处理过程为:厌氧培养24h的长栖粪杆菌cm04-06菌液,离心收集菌体,用pbs进行悬浮,调整菌浓度至1
×
109cfu/ml,每只小鼠每天灌胃200μl的长栖粪杆菌cm04-06。
[0111]
vsl#3处理过程为:采用pbs进行悬浮,同样调节浓度至1
×
109cfu/ml,每只小鼠每天灌胃200μl。
[0112]
治疗采用预防给药的方式,dss处理前三天灌胃益生菌,每天记录小鼠体重、饮食和饮水情况,同时观察小鼠的粪便性状及粪便隐血情况,分别在dss处理第1天、第3天、第5天和第7天计算小鼠的dai评分,dai评分详见表6。dss处理持续7天,益生菌和 pbs的日灌胃量为200μl。实验结束后处死小鼠,所有小鼠取血、脱颈、取结肠、拍照、称重、量取结肠长度。结肠组织保存于-80℃冰箱和多聚甲醛中。
[0113]
表6:dai指数评分表
[0114]
体重下降(%)大便性状大便隐血/弱眼血便积分0正常正常01-5
ꢀꢀ
15-10松散隐血阳性210-15
ꢀꢀ
3》15稀便肉眼血便4
[0115]
表中的大便性状:正常大便—成形大便;松散大便—不粘附于肛门的糊状、半成型大便;稀便—可粘附于肛门的稀样水便。其中便血情况:正常小鼠便血为阳性;肉眼血便为红色或褐色;隐血阳性为不明显的肉眼血便,使用四甲基联苯胺进行检测。dai指数等于体重、大便性状以及大便隐血/弱眼血便三个积分之和。
[0116]
试验结果:
[0117]
(1)治疗前后小鼠的体重变化如下表7和图2所示:
[0118]
表7:cm04-06对小鼠体重的影响
[0119][0120][0121]
由表7和图2可知,对照组小鼠体重基本维持缓慢升高的趋势,dss诱导的模型组小鼠的体重逐渐下降,第3天开始体重下降的比较显著(*p《0.05),第5天开始,二者之间的差异显著程度更加明显(**p《0.01)。而cm04-06和vsl#3的治疗可以减缓uc小鼠体重的下降,分别在第5天和第7天,cm04-06和vsl#3小鼠体重下降的抑制相对于模型组具有显著差异(
▲
p《0.05)。上述结果说明cm04-06和vsl#3这两组益生菌可以抑制uc 引起的小鼠体重下降情况。通过比较第7天各组的体重数值可以发现cm04-06组小鼠的体重略高于vsl#3,对小鼠体重下降的抑制更加显著(
▲▲
p《0.01),说明cm04-06抑制uc 小鼠体重降低的能力好于vsl#3。
[0122]
(2)治疗前后小鼠dai评分的变化
[0123]
dss诱导的溃疡性肠炎的小鼠由于体重下降、大便性状和便血情况的变化引起dai指数的变化,具体结果见表8和图3:
[0124]
表8:cm04-06对小鼠dai评分的影响
[0125]
分组第1天第3天第5天第7天对照组1.0
±
0.51.2
±
0.61.1
±
0.61.3
±
0.5模型组1.2
±
0.43.5
±
1.1**6.8
±
1.6**8.9
±
1.9**cm04-061.1
±
0.53.1
±
1.25.2
±
1.5
▲▲
7.0
±
1.8
▲▲
vsl
#
31.2
±
0.63.3
±
1.15.8
±
1.8
▲▲
7.4
±
1.6
▲
[0126]
表8和图3数据表明,对照组小鼠dai评分维持在稳定的低水平,而dss诱导的小鼠由于出现一系列病理,导致dai评分逐渐升高,第3天开始模型组小鼠dai评分与对照组相比差异极显著(**p《0.01),第7天模型组小鼠dai评分达到最高水平。益生菌的干预可以抑制
dai评分的升高,cm04-06和vsl#3组小鼠在第5天和第7天的dai评分相比于模型组得到了一定程度的控制(
▲
p《0.05,
▲▲
p《0.01)。由第7天结果可发现cm04-06 组小鼠dai评分略低于vsl#3组,cm04-06组与模型组dai评分差异极显著(
▲▲
p《0.01),由此说明cm04-06在抑制uc小鼠dai评分升高的效果优于vsl#3。
[0127]
(3)结肠长度的变化
[0128]
uc模型小鼠的结肠组织会发生改变,主要是因为溃疡和炎症的发生导致结肠组织缩短,治疗结束后解剖并测量小鼠结肠长度,实验结果见表9。
[0129]
表9:cm04-06对小鼠结肠长度的影响
[0130]
分组结肠长度(cm)对照组7.16
±
0.82模型组4.58
±
0.98**vsl
#
3组5.43
±
0.90
▲
cm04-06组5.70
±
0.85
▲
[0131]
表9结果显示,经dss诱导7天后的小鼠(模型组)结肠组织缩短情况比较严重,与对照组相比差异极显著(**p《0.01)。而益生菌cm04-06和vsl#3的干预可以显著抑制小鼠结肠的缩短,cm04-06和vsl#3这两组分别与模型组相比均差异显著(
▲
p《0.05)。由表9数据可发现cm04-06组小鼠结肠长度比vsl#3组小鼠结肠长度要长,说明cm04-06 控制uc小鼠结肠缩短的能力略强于vsl#3。
[0132]
实施例4含长栖粪杆菌cm04-06的食品组合物
[0133]
表10:食品组合物原料配方
[0134]
原料质量百分比(%)长栖粪杆菌cm04-060.5牛奶90.0白糖9.0维生素c0.5
[0135]
按照表10所述配方比例混合牛奶、白糖,搅拌至完全混合,预热,20mpa压力均质, 90℃左右杀菌5~10分钟,冷却至40~43℃,混入保护剂维生素c,接种1~100
×
106cfu/g 的长栖粪杆菌cm04-06菌,即制成含长栖粪杆菌cm04-06菌的食品组合物
[0136]
实施例5含长栖粪杆菌cm04-06的胶囊的制备
[0137]
表11:胶囊原料配方
[0138]
原料质量百分比(%)长栖粪杆菌cm04-061.0乳糖2.0酵母粉2.0蛋白胨1.0纯净水93.5维生素c0.5
[0139]
按照表11所述配方比例将乳糖、酵母粉、蛋白胨以纯净水混合均匀,预热到60~65
℃,20mpa压力均质,90℃左右杀菌20~30分钟,冷却至36~38℃,混入保护剂维生素c,接入长栖粪杆菌cm04-06活菌(1~500
×
106cfu/ml),36~38℃发酵至ph值为6.0,离心,冷冻干燥至水份含量小于3%,即制备长栖粪杆菌cm04-06菌冷冻干燥物。称取0.5g长栖粪杆菌cm04-06冷冻干燥物与麦芽糊精等量混合后装入胶囊中,即制成含长栖粪杆菌 cm04-06的药物组合物。
[0140]
实施例6用于治疗溃疡性肠炎的制剂的制备
[0141]
1、菌液准备:将长栖粪杆菌cm04-06(1
×
109cfu/ml)进行厌氧培养,厌氧培养基采用pyg培养基,经过37℃厌氧发酵2~3天。
[0142]
2、生长因子制备:将脱脂牛奶、酪蛋白进行混合、离心、超滤获得牛奶生长因子粗提物(含有维生素类物质、嘌呤类物质、嘧啶类物质等成分)。
[0143]
3、药物剂型制作:将5体积生长因子和1体积的保护剂维生素c加入到100体积的 cm04-06发酵的菌液中,充分搅拌混匀,然后加入淀粉辅料(如麦芽糊精)制备药物剂型。
[0144]
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任一个或多个实施例或示例中以合适的方式结合。此外,在不相互矛盾的情况下,本领域的技术人员可以将本说明书中描述的不同实施例或示例以及不同实施例或示例的特征进行结合和组合。
[0145]
尽管上面已经示出和描述了本发明的实施例,可以理解的是,上述实施例是示例性的,不能理解为对本发明的限制,本领域的普通技术人员在本发明的范围内可以对上述实施例进行变化、修改、替换和变型。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。
