1.本发明涉及一种基于8-苯基喹啉及其衍生物配位的二价铂或钯金属配合物磷光材料,尤其涉及一种二价铂或钯金属配合物、有机发光器件和显示或照明装置,属于金属有机光电材料领域。
背景技术:
2.与液晶显示(lcd)相比,有机发光器件(例如有机发光二极管器件(oled)具有很多优势,例如无需背光源,节能、轻薄、颜色绚丽、色彩饱和度高、视角广、响应速度快,此外还具有很宽的使用温度范围等。因此,有机发光器件在显示和照明领域具有巨大的应用潜力,从而受到学术界和工业界的广泛关注。发光材料的设计和开发是oled领域的核心。早期oled器件中其发光材料主要为有机小分子荧光材料。然而自旋统计量子学表明,在电致发光的情况下,单线态激子和三线态激子(exciton)比例为1:3,且传统荧光材料只能利用处于单线态激发态的激子,因此,其理论内部量子效率仅为25%。美国普林斯顿大学的forrest教授和南加州大学的thompson教授于1998年发现了室温下重金属有机配合物分子的磷光电致发光现象。由于重金属原子的强自旋轨道耦合,此类配合物可以有效促进激子由单线态到三线态的系间蹿越(isc),从而oled器件可以充分利用电激发所产生所有单线态和三线态激子,使发光材料的理论内部量子效率可达到100%(参见nature,1998,395,151)。
3.目前能够满足实际应用的重金属磷光有机配合物分子基本均为环金属三价铱(铱(iii))配合物分子,且数量有限。地壳中金属铂元素的含量和世界范围内的年产均为金属铱元素的约十倍,用于制备三价铱配合物磷光材料的ircl
3.
h2o价格也要远高于制备二价铂(铂(ii))配合物磷光材料的k2ptcl4或ptcl2。此外,制备三价铱配合物磷光材料时涉及含三价铱二聚体、三价铱中间体配体交换生成mer-铱(iii)配合物和mer-到fac-铱(iii)配合物异构体转换三步反应,使总收率大为降低,大大降低了原料ircl
3.
h2o的利用率,因此,提高了三价铱配合物磷光材料的制备成本。相比之下,二价铂配合物磷光材料的制备只有最后一步配体的金属化设计铂盐的反应,铂元素利用率高,可进一步降低二价铂配合物磷光材料的制备成本。综上所述,二价铂配合物磷光材料的制备成本要远低于三价铱配合物磷光材料。
4.基于双齿配体的二价铂金属配合物分子刚性较低,两个双齿配体易扭曲、振动而导致非辐射衰减,使其磷光量子效率低下(一般小于30%,参见inorganic chemistry 2002,41,3055-3066.);而基于三齿配体的环二价铂金属配合物分子需要第二个配阴离子(如炔负离子、cl-、卡宾等),也会导致配合物的化学稳定性和热稳定性降低。上述原因均不利于其作为磷光材料在oled器件中的应用。采用新型的四齿配体则有利于提高材料分子的量子效率和稳定性。虽然二价铂或钯配合物磷光材料已有报道,但能够满足实际使用要求的二价铂或钯配合物磷光材料尚未见报道,开发稳定而高效的新型磷光发光材料,对oled
产业的发展依然具有举足轻重的意义。为了满足全彩显示的三基色需要,发射波长处于600-650nm之间的红光材料是必不可少的,因此,有必要开发一种结构新颖的基于8-苯基喹啉及其衍生物配位的二价铂或钯金属配合物发光材料。
技术实现要素:
5.本发明针对现有技术中的不足,提供了一种基于8-苯基喹啉及其衍生物配位的二价铂或钯金属配合物磷光材料(如红光磷光材料)及包括其的有机发光器件。
6.为了实现上述目的,本发明的技术方案如下:
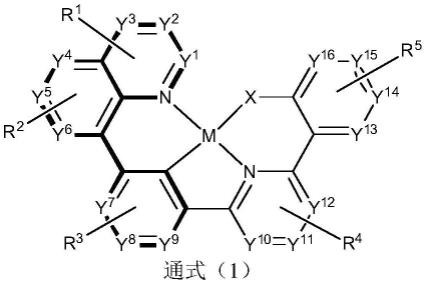
7.本发明提供了一种二价铂或钯金属配合物,其具有通式(i)所示的结构:
[0008][0009]
其中:
[0010]
m为pt或pd;
[0011]
x为o、s或nr;
[0012]
y1、y2、y3、y4、y5、y6、y7、y8、y9、y
10
、y
11
、y
12
、y
13
、y
14
、y
15
和y
16
各自独立地选自n或c原子;
[0013]
r、r1、r2、r3、r4和r5各自独立地可以为单取代、双取代、三取代、四取代或者无取代;r1、r2、r3、r4和r5各自独立地表示为氢、氘、c1-c24的烷基、c1-c24的卤代烷基、c1-c24的环烷基、c1-c24的烷氧基、c1-c24的芳基、c1-c24的杂芳基、c1-c24的芳氧基、卤素、环烯基、杂环基、烯基、炔基、羟基、巯基、硝基、氰基、氨基、单或二c1-c24的烷基氨基、单或二c1-c24的芳基氨基、酯基、腈基、异腈基、烷氧基羰基、酰氨基、烷氧基羰基氨基、芳氧基羰基氨基、磺酰基氨基、氨磺酰基、氨基甲酰基、烷硫基、亚磺酰基、脲基、磷酰胺基、亚胺基、磺基、羧基、肼基、甲硅烷基或取代的甲硅烷基或聚合的基团,且两个或两个以上邻近的r、r1、r2、r3、r4和r5可以选择性链接形成环。
[0014]
进一步地,该二价铂金属配合物为pt-1~pt-649中之一的结构,但不限于此。
[0015]
本发明还提供了一种有机发光器件,其包括阴极、阳极和有机层,该有机层至少包括发光层,有机层包含该基于8-苯基喹啉及其衍生物配位的二价铂或钯金属配合物磷光材料。
[0016]
进一步地,所述有机层还包括空穴注入层、空穴传输层、电子传输层和电子注入层中的一种或多种。
[0017]
进一步地,所述发光层还包含主体材料,其中该主体材料与该基于8-苯基喹啉及其衍生物配位的二价铂或钯金属配合物磷光材料的体积比为1:99至99:1,主体材料没有任何限制。
[0018]
进一步地,该有机发光器件为全彩显示器、光伏器件、发光显示器件或有机发光二极管。
[0019]
本发明又提供了一种显示或照明装置,其包括该有机发光器件。
[0020]
本发明的有益效果是:本发明材料的分子结构设计采取了新的8-苯基喹啉及其衍生物和中心金属离子配位形成六元金属环,同时结合邻吡啶基酚氧负离子及其衍生物构成新型的四齿配体,四齿配体与中心金属离子配位形成6/5/6型四齿环金属配合物磷光材料;此类型配体结构中喹啉和酚氧负离子之间的位阻小,易于和中心金属配位,所形成的金属配合物母核具有很好的平面性;材料分子具有较高的量子效率和高的热稳定性,适合作为发光材料用于oled器件的制备。因此,本发明的二价铂金属配合物在oled显示和照明等诸多领域具有一定的应用价值。且将本发明的二价铂金属配合物应用于有机发光器件时,该器件相比常规的有机发光器件,电流效率有了显著提高,同时其寿命也有所提高。
附图说明
[0021]
图1为本发明的化合物pt-14、pt-124、pt-134、pt-137和pt-139在二氯甲烷溶液中室温下的光致发光光谱图;
[0022]
图2为本发明的化合物pt-1、pt-126、pt-183和pt-167在二氯甲烷溶液中室温下的光致发光光谱图;
[0023]
图3为本发明的化合物pt-169、pt-593、pt-592和pt-591在二氯甲烷溶液中室温下的光致发光光谱图;
[0024]
图4为本发明的化合物pt-129、pt-210、pt-144和pt-142在二氯甲烷溶液中室温下的光致发光光谱图;
[0025]
图5为本发明的化合物pd-124、pd-210和pd-183在二氯甲烷溶液中室温下的光致发光光谱图比较。
具体实施方式
[0026]
以下对本发明的内容进行详细说明。以下所记载的构成要件的说明有时是基于本发明的代表性实施方式或具体例而成,但本发明并不限定于此种实施方式或具体例。
[0027]
下面举例说明下述通式(1)代表的本发明的二价铂金属配合物(磷光材料)的具体实例,然而,不解释为限制本发明。
[0028]
本发明提供了一种有机发光器件,其包括第一电极、第二电极及设置于该第一电极和该第二电极之间的有机层;该有机层包括基于三甲基苯基吡啶结构单元的二价铂金属配合物。
[0029]
本发明又提供了基于三甲基苯基吡啶结构单元的二价铂金属配合物(磷光材料)在有机发光器件中的应用,其中该有机发光器件为有机发光二极管或发光电化学电池。
[0030]
具体地,本发明的含有喹啉结构单元的的二价铂金属配合物发光材料在作为有机发光器件的发光层中的应用。在有机发光器件中,从正负两电极向发光材料中注入载子,产生激发态的发光材料并使其发光。通过通式(1)代表的本发明的化合物可作为发光材料应用于有机光致发光器件或有机电致发光器件等有机发光器件。有机光致发光器件具有在衬底上至少形成了发光层的结构。另外,有机发光器件具有至少形成了阳极、阴极、及阳极和
阴极之间的有机层的结构。有机层至少包含发光层,可以仅由发光层构成,也可以除发光层以外具有1层以上的有机层。作为这种其它有机层,可以列举空穴传输层、空穴注入层、电子阻挡层、空穴阻挡层、电子注入层、电子传输层、激子阻挡层等。空穴传输层也可以是具有空穴注入功能的空穴注入传输层,电子传输层也可以是具有电子注入功能的电子注入传输层。
[0031]
实施例
[0032]
除非另有说明,以下实例中所涉及的所有市售试剂购买后直接使用,没有进一步纯化。核磁共振氢谱均在氘代氯仿(cdcl3)或氘代二甲基亚砜(dmso-d6)溶液中测得,氢谱使用400或500兆赫兹的核磁共振谱仪。如果用cdcl3作溶剂,则氢谱以cdcl3(δ=7.26ppm)作为内标。如果用dmso-d6作溶剂,则氢谱以dmso-d6(δ=2.50ppm)作为内标。以下缩写(或组合)用于解释氢谱峰:s=单峰,d=双重峰,t=三重峰,q=四重峰,p=五重峰,m=多重峰,br=宽峰。理论计算中利用密度泛函理论(dft)优化了金属配合物基态(s0)分子的几何结构;使用b3lyp泛函进行dft计算,其中c、h、o和n原子使用6-31g(d)基组,pt和pd原子使用lanl2dz基组。
[0033]
实施例1:四齿环金属铂(ii)配合物磷光发光材料pt-1合成路线如下:
[0034][0035]
中间体(l-1-ome)的合成:向带有磁力搅拌子的schlenk管中加入1a(500mg,1.51mmol,1.0当量)、1b(397mg,1.51mmol,1.0当量)、四三苯基膦钯(52mg,0.045mmol,3mol%)和碳酸钾(417mg,3.02mmol,2.0当量)。然后抽换氮气三次,在氮气保护下加入1,4-二氧六环(5ml)和水(1ml)。85℃油浴锅中反应48小时后冷却至室温,减压蒸馏除去溶剂后粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=50:1-10:1,得到灰黄色固体470mg,收率80%。1h nmr(500mhz,cdcl3)δ3.88(s,3h),7.01(d,j=8.0hz,1h),7.09(td,j=7.5,1.0hz,1h),7.37(ddd,j=8.0,7.5,2.0hz,1h),7.43(dd,j=8.0,4.0hz,1h),7.59
–
7.64(m,2h),7.72(dd,j=8.0,1.0hz,1h),7.74
–
7.78(m,2h),7.81
–
7.86(m,3h),8.01(dd,j=7.5,2.0hz,1h),8.16(dt,j=8.0,1.5hz,1h),8.23(dd,j=8.0,2.0hz,1h),8.37(t,j=2.0hz,1h),8.96(dd,j=4.0,2.0hz,1h)。
[0036]
配体l-1的合成:向带有磁力搅拌子的schlenk管中加入l-1-ome(450mg,1.16mmol,1.0当量)、吡啶盐酸盐(1.34g,11.59mmol,10.0当量)。然后抽换氮气三次,在氮气保护下加入1,3-二甲基-2-咪唑啉酮(4ml)。180℃油浴锅中反应15小时后冷却至室温,加入乙酸乙酯稀释,用水洗涤有机相,分液后用无水硫酸钠干燥,过滤,滤液减压蒸馏除去溶剂。所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=20:1-5:1,得到白色固体
327mg,收率75%。1h nmr(500mhz,dmso-d6)δ6.92
–
6.97(m,2h),7.33(ddd,j=8.5,7.0,1.5hz,1h),7.60(dd,j=8.0,4.0hz,1h),7.70(t,j=8.0hz,1h),7.75(dd,j=8.0,7.0hz,1h),7.81(dt,j=8.0,1.0hz,1h),7.90(dd,j=7.0,1.5hz,1h),8.01
–
8.04(m,2h),8.08(ddd,j=10.0,8.0,1.5hz,2h),8.13(t,j=8.0hz,1h),8.22(d,j=8.0hz,1h),8.28(t,j=2.0hz,1h),8.48(dd,j=8.0,2.0hz,1h),8.94(dd,j=4.0,2.0hz,1h),14.41(s,1h)。
[0037]
pt-1的合成:向带有磁力搅拌子的三口瓶中加入l-1(100mg,0.27mmol,1.0当量)、四氯铂酸钾(116mg,0.28mmol,1.05当量)和四丁基溴化铵(9mg,0.027mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(10ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,室温搅拌12小时,升温120℃反应73小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=10:1-1:1,得到红色固体56mg,收率37%。1h nmr(500mhz,dmso-d6)δ6.68(ddd,j=8.0,6.5,1.5hz,1h),7.17(dd,j=8.5,1.5hz,1h),7.33(ddd,j=8.5,6.5,2.0hz,1h),7.40(t,j=7.5hz,1h),7.92(t,j=8.0hz,1h),7.94
–
8.01(m,3h),8.14(dd,j=7.5,1.5hz,1h),8.19
–
8.29(m,4h),8.82(dd,j=8.0,1.0hz,1h),8.94(dd,j=8.0,1.5hz,1h),10.79(dd,j=5.5,1.5hz,1h)。
[0038]
实施例2:四齿环金属铂(ii)配合物磷光发光材料pt-126合成路线如下:
[0039][0040]
中间体(l-126-ome)的合成:向带有磁力搅拌子的schlenk管中加入2a(500mg,1.23mmol,1.0当量)、2b(448mg,1.35mmol,1.1当量)、四三苯基膦钯(43mg,0.037mmol,3mol%)和碳酸钾(340mg,2.46mmol,2.0当量)。然后抽换氮气三次,在氮气保护下加入1,4-二氧六环(5ml)和水(1ml)。100℃油浴锅中反应41小时后冷却至室温,减压蒸馏除去溶剂后粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=30:1-10:1,得到白色固体610mg,收率86%。1h nmr(500mhz,cdcl3)δ1.33(s,9h),1.45(s,9h),3.42(s,3h),7.34
–
7.39(m,1h),7.39(d,j=2.5hz,1h),7.42
–
7.49(m,3h),7.64(dd,j=8.0,7.0hz,1h),7.71(d,j=2.5hz,1h),7.76
–
7.83(m,5h),7.85
–
7.89(m,2h),7.99(t,j=1.5hz,1h),8.24(dd,j=8.0,2.0hz,1h),8.45(d,j=1.5hz,2h),8.98(dd,j=4.0,2.0hz,1h)。
[0041]
配体l-126的合成:向带有磁力搅拌子的schlenk管中加入l-126-ome(580mg,1.0mmol,1.0当量)、吡啶盐酸盐(1.16g,10.0mmol,10.0当量)。然后抽换氮气三次,在氮气保护下加入1,3-二甲基-2-咪唑啉酮(3ml)。180℃油浴锅中反应14小时后冷却至室温,加入乙酸乙酯稀释,用水洗涤有机相,分液后用无水硫酸钠干燥,过滤,滤液减压蒸馏除去溶剂。所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=20:1-5:1,得到白色固体
520mg,收率92%。1h nmr(500mhz,cdcl3)δ1.38(s,9h),1.51(s,9h),7.39(tt,j=7.0,1.0hz,1h),7.42(d,j=2.0hz,1h),7.44
–
7.51(m,3h),7.67(dd,j=8.0,7.0hz,1h),7.72(d,j=2.5hz,1h),7.73(dd,j=6.5,2.0hz,1h),7.77
–
7.82(m,2h),7.87
–
7.94(m,4h),8.05(t,j=1.5hz,1h),8.23
–
8.29(m,2h),8.31(t,j=1.5hz,1h),9.05(dd,j=4.0,2.0hz,1h),14.94(s,1h)。
[0042]
pt-126的合成:向带有磁力搅拌子的三口瓶中加入l-126(300mg,0.53mmol,1.0当量)、四氯铂酸钾(232mg,0.56mmol,1.05当量)和四丁基溴化铵(17mg,0.05mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(30ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,室温搅拌9小时,升温120℃反应79小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=10:1-1:1,得到红色固体314mg,收率78%。1h nmr(500mhz,cdcl3)δ1.37(s,9h),1.62(s,9h),7.40(tt,j=7.5,1.5hz,1h),7.47
–
7.53(m,3h),7.58
–
7.63(m,2h),7.72
–
7.79(m,4h),7.85
–
7.90(m,2h),7.93
–
8.01(m,2h),8.16(d,j=1.0hz,1h),8.52(dd,j=8.0,1.5hz,1h),8.62(dd,j=8.0,1.5hz,1h),10.91(dd,j=5.0,1.5hz,1h)。
[0043]
实施例3:四齿环金属铂(ii)配合物磷光发光材料pt-183合成路线如下:
[0044][0045]
中间体(l-183-ome)的合成:向带有磁力搅拌子的schlenk管中加入3a(500mg,1.01mmol,1.0当量)、2b(436mg,1.31mmol,1.3当量)、四三苯基膦钯(58mg,0.05mmol,5mol%)和碳酸钾(279mg,2.02mmol,2.0当量)。然后抽换氮气三次,在氮气保护下加入1,4-二氧六环(8ml)和水(2ml)。100℃油浴锅中反应36小时后冷却至室温,减压蒸馏除去溶剂后粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=20:1-10:1,得到灰黄色固体542mg,收率81%。1h nmr(500mhz,cdcl3)δ1.30(s,9h),1.44(s,9h),3.41(s,3h),7.30(t,j=7.5hz,2h),7.38(d,j=2.5hz,1h),7.43
–
7.49(m,3h),7.63
–
7.69(m,2h),7.78
–
7.85(m,5h),7.89(dd,j=8.0,1.0hz,1h),7.96(dd,j=7.0,1.0hz,1h),8.09(t,j=1.5hz,1h),8.16(d,j=8.0hz,2h),8.25(dd,j=8.0,1.5hz,1h),8.45(t,j=1.5hz,1h),8.59(t,j=1.5hz,1h),9.04(dd,j=4.0,1.5hz,1h)。
[0046]
配体l-183的合成:向带有磁力搅拌子的schlenk管中加入l-183-ome(512mg,0.78mmol,1.0当量)、吡啶盐酸盐(901mg,7.80mmol,10.0当量)。然后抽换氮气三次,在氮气保护下加入1,3-二甲基-2-咪唑啉酮(3ml)。180℃油浴锅中反应19小时后冷却至室温,加入
乙酸乙酯稀释,用水洗涤有机相,分液后用无水硫酸钠干燥,过滤,滤液减压蒸馏除去溶剂。所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=20:1-5:1,得到白色固体430mg,收率85%。1h nmr(500mhz,cdcl3)δ1.38(s,9h),1.54(s,9h),7.33(ddd,j=8.0,7.0,1.0hz,2h),7.44(d,j=2.0hz,1h),7.49(dd,j=8.0,4.0hz,1h),7.53(ddd,j=8.5,7.5,1.0hz,2h),7.68(dd,j=8.0,7.0hz,1h),7.70
–
7.73(m,2h),7.89
–
7.94(m,5h),7.96(dd,j=7.0,1.5hz,1h),8.16
–
8.20(m,3h),8.24
–
8.27(m,2h),8.37(t,j=1.5hz,1h),9.11(dd,j=4.0,2.0hz,1h),14.85(s,1h)。
[0047]
pt-183的合成:向带有磁力搅拌子的三口瓶中加入l-183(200mg,0.31mmol,1.0当量)、四氯铂酸钾(137mg,0.33mmol,1.05当量)和四丁基溴化铵(10mg,0.031mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(18ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,室温搅拌8小时,升温120℃反应72小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=10:1-1:1,得到红色固体190mg,收率73%。1h nmr(500mhz,dmso-d6)δ1.34(s,9h),1.58(s,9h),7.31(ddd,j=8.0,5.0,3.0hz,2h),7.42
–
7.49(m,5h),7.64(d,j=2.5hz,1h),7.85(t,j=8.0hz,1h),7.97(dd,j=8.0,5.5hz,1h),8.17
–
8.25(m,5h),8.28
–
8.31(m,3h),8.77(dd,j=8.0,1.5hz,1h),9.00(dd,j=8.0,1.5hz,1h),10.77(dd,j=5.5,1.5hz,1h)。
[0048]
实施例4:四齿环金属铂(ii)配合物磷光发光材料pt-167合成路线如下:
[0049][0050]
中间体(l-167-ome)的合成:向带有磁力搅拌子的schlenk管中加入4a(89mg,0.52mmol,1.1当量)、3b(300mg,0.47mmol,1.0当量)、四三苯基膦钯(17mg,0.014mmol,3mol%)和碳酸钾(163mg,1.18mmol,2.5当量)。然后抽换氮气三次,在氮气保护下加入1,4-二氧六环(6ml)和水(1ml)。85℃油浴锅中反应36小时后冷却至室温,减压蒸馏除去溶剂后粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=40:1-10:1,得到白色固体245mg,收率76%。1h nmr(500mhz,cdcl3)δ1.35(s,9h),1.39(s,18h),1.44(s,9h),3.43(s,3h),7.39
–
7.46(m,2h),7.50
–
7.55(m,3h),7.64(q,j=8.0hz,2h),7.68(d,j=2.5hz,1h),7.80(dt,j=9.0,1.0hz,1h),7.83
–
7.86(m,2h),7.92(q,j=1.5hz,2h),8.22
–
8.24(m,2h),8.49(t,j=3.5hz,1h),8.97(dd,j=4.0,2.0hz,1h)。
[0051]
配体l-167的合成:向带有磁力搅拌子的schlenk管中加入l-167-ome(230mg,0.33mmol,1.0当量)、吡啶盐酸盐(385mg,3.3mmol,10.0当量)。然后抽换氮气三次,在氮气保护下加入1,3-二甲基-2-咪唑啉酮(3ml)。180℃油浴锅中反应12小时后冷却至室温,加入乙酸乙酯稀释,用水洗涤有机相,分液后用无水硫酸钠干燥,过滤,滤液减压蒸馏除去溶剂。所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=100:1,得到白色固体210mg,收率94%。1h nmr(500mhz,cdcl3)δ1.36(s,9h),1.41(s,18h),1.51(s,9h),7.43
–
7.47(m,2h),7.52(d,j=2.0hz,2h),7.58(t,j=3.5hz,1h),7.65(dd,j=8.0,7.0hz,1h),7.70(t,j=7.7hz,1h),7.76(d,j=2.5hz,1h),7.83
–
7.88(m,4h),8.00(d,j=1.5hz,1h),8.08(dt,j=8.0,1.5hz,1h),8.23(dd,j=8.0,1.5hz,1h),8.36(t,j=3.5hz,1h),9.02(dd,j=4.0,1.5hz,1h),14.72(s,1h)。
[0052]
pt-167的合成:向带有磁力搅拌子的三口瓶中加入l-167(150mg,0.22mmol,1.0当量)、四氯铂酸钾(101mg,0.24mmol,1.1当量)和四丁基溴化铵(8mg,0.022mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(14ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,室温搅拌12小时,升温120℃反应48小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=100:1-4:1,得到红色固体130mg,收率68%。1h nmr(500mhz,cdcl3)δ1.36(s,9h),1.45(s,18h),1.63(s,9h),7.38(t,j=7.5hz,1h),7.52(d,j=2.5hz,1h),7.60
–
7.63(m,2h),7.66(d,j=1.5hz,2h),7.68(d,j=2.5hz,1h),7.75
–
7.79(m,2h),7.87
–
7.89(m,2h),8.00(d,j=8.0hz,1h),8.13(d,j=1.5hz,1h),8.53(dd,j=8.0,1.5hz,1h),8.56(d,j=6.0hz,1h),10.93(dd,j=5.5,2.0hz,1h)。
[0053]
实施例5:四齿环金属铂(ii)配合物磷光发光材料pt-169合成路线如下:
[0054][0055]
中间体(l-169-ome)的合成:向带有磁力搅拌子的schlenk管中加入5a(54mg,0.2mmol,1.0当量)、4b(140mg,0.2mmol,1.0当量)、四三苯基膦钯(21mg,0.018mmol,9mol%)和碳酸钾(69mg,0.5mmol,2.5当量)。然后抽换氮气三次,在氮气保护下加入1,4-二氧六环(5ml)和水(1ml)。85℃油浴锅中反应24小时后冷却至室温,减压蒸馏除去溶剂后粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=30:1,得到白色固体30mg,收率20%。1h nmr(500mhz,cdcl3)δ1.34(s,9h),1.39(s,18h),1.44(s,9h),1.47(s,9h),3.43(s,3h),
二氧六环(4ml)和水(1ml)。95℃油浴锅中反应40小时后冷却至室温,减压蒸馏除去溶剂后粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=20:1-5:1,得到白色固体74mg,收率29%。1h nmr(500mhz,cdcl3)δ1.33(s,9h),1.39(s,18h),1.44(s,9h),3.44(s,3h),7.39
–
7.43(m,2h),7.45(dd,j=8.0,4.0hz,1h),7.48
–
7.54(m,5h),7.64
–
7.69(m,2h),7.76
–
7.79(m,2h),7.86(dt,j=8.0,1.0hz,1h),7.94(s,2h),8.03(d,j=2.0hz,1h),8.12(d,j=2.0hz,1h),8.24(dt,j=8.0,1.5hz,1h),8.28(dd,j=8.0,1.5hz,1h),8.54(t,j=1.5hz,1h),8.96(dd,j=4.0,2.0hz,1h)。
[0061]
配体l-593的合成:向带有磁力搅拌子的schlenk管中加入l-593-ome(74mg,0.096mmol,1.0当量)、吡啶盐酸盐(111mg,0.96mmol,10.0当量)。然后抽换氮气三次,在氮气保护下加入1,3-二甲基-2-咪唑啉酮(1ml)。180℃油浴锅中反应9小时后冷却至室温,加入乙酸乙酯稀释,用水洗涤有机相,分液后用无水硫酸钠干燥,过滤,滤液减压蒸馏除去溶剂。所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=30:1-5:1,得到白色固体66mg,收率91%。1h nmr(500mhz,cdcl3)δ1.36(s,9h),1.41(s,18h),1.50(s,9h),7.40
–
7.43(m,2h),7.47(dd,j=8.0,4.0hz,1h),7.49
–
7.54(m,4h),7.58(t,j=2.0hz,1h),7.73(d,j=8.0hz,1h),7.76(d,j=2.5hz,1h),7.78
–
7.81(m,2h),7.85(d,j=1.5hz,1h),7.91(dt,j=7.5,1.0hz,1h),8.01(d,j=1.5hz,1h),8.05(d,j=2.5hz,1h),8.09(dt,j=8.0,1.5hz,1h),8.13(d,j=2.0hz,1h),8.29(dd,j=8.0,1.5hz,1h),8.41(t,j=1.5hz,1h),9.01(dd,j=4.0,2.0hz,1h),14.72(s,1h)。
[0062]
pt-593的合成:向带有磁力搅拌子的三口瓶中加入l-593(63mg,0.084mmol,1.0当量)、四氯铂酸钾(37mg,0.088mmol,1.05当量)和四丁基溴化铵(3mg,0.008mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(5ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,室温搅拌12小时,升温120℃反应48小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=10:1-1:1,得到黄色固体54mg,收率68%。1h nmr(500mhz,cdcl3)δ1.37(s,9h),1.45(s,18h),1.64(s,9h),7.39(t,j=7.5hz,1h),7.46
–
7.50(m,1h),7.53(d,j=2.5hz,1h),7.55
–
7.58(m,2h),7.62
–
7.67(m,4h),7.69(d,j=2.5hz,1h),7.79
–
7.84(m,3h),7.88(d,j=1.5hz,1h),8.05(d,j=2.0hz,1h),8.07(d,j=8.0hz,1h),8.14(d,j=1.5hz,1h),8.57(dd,j=8.0,1.5hz,1h),8.79(d,j=2.0hz,1h),10.91(dd,j=5.5,1.5hz,1h)。
[0063]
实施例7:四齿环金属铂(ii)配合物磷光发光材料pt-14合成路线如下:
[0064][0065]
中间体(l-14-ome)的合成:向带有磁力搅拌子的schlenk管中加入7a(800mg,
2.07mmol,1.0当量)、1b(543mg,2.07mmol,1.0当量)、四三苯基膦钯(48mg,0.041mmol,2mol%)和碳酸钾(572mg,4.14mmol,2.0当量)。然后抽换氮气三次,在氮气保护下加入1,4-二氧六环(6ml)和水(1ml)。85℃油浴锅中反应34小时后冷却至室温,减压蒸馏除去溶剂后粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=50:1-10:1,得到棕色固体803mg,收率87%。1h nmr(500mhz,cdcl3)δ1.47(s,9h),3.89(s,3h),7.01(dd,j=8.5,1.0hz,1h),7.08(td,j=7.5,1.0hz,1h),7.34
–
7.41(m,2h),7.61(t,j=7.5hz,1h),7.72(dd,j=8.0,1.0hz,1h),7.74
–
7.78(m,3h),7.85(dd,j=7.5,1.0hz,1h),7.89(d,j=2.0hz,1h),8.03(dd,j=7.5,1.5hz,1h),8.15(ddd,j=7.5,2.0,1.0hz,1h),8.18(dd,j=8.0,2.0hz,1h),8.37(t,j=1.5hz,1h),8.90(dd,j=4.0,2.0hz,1h)。
[0066]
配体l-14的合成:向带有磁力搅拌子的schlenk管中加入l-14-ome(750mg,1.69mmol,1.0当量)、吡啶盐酸盐(1.95g,16.87mmol,10.0当量)。然后抽换氮气三次,在氮气保护下加入1,3-二甲基-2-咪唑啉酮(4ml)。180℃油浴锅中反应28小时后冷却至室温,加入乙酸乙酯稀释,用水洗涤有机相,分液后用无水硫酸钠干燥,过滤,滤液减压蒸馏除去溶剂。所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=50:1-10:1,得到白色固体623mg,收率86%。1h nmr(500mhz,dmso-d6)δ1.47(s,10h),6.90
–
6.98(m,2h),7.30
–
7.35(m,1h),7.56(ddd,j=8.0,4.0,1.0hz,1h),7.70(t,j=7.5hz,1h),7.82
–
7.85(m,1h),7.97(s,2h),8.02(d,j=7.5hz,2h),8.09(dt,j=8.0,1.5hz,1h),8.14(td,j=8.0,1.0hz,1h),8.22(d,j=8.0hz,1h),8.28(q,j=1.5hz,1h),8.44(dt,j=8.0,1.5hz,1h),8.86(dd,j=4.0,2.0hz,1h),14.47(s,1h)。
[0067]
pt-14的合成:向带有磁力搅拌子的三口瓶中加入l-14(300mg,0.70mmol,1.0当量)、四氯铂酸钾(304mg,0.73mmol,1.05当量)和四丁基溴化铵(23mg,0.07mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(42ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,室温搅拌13小时,升温120℃反应62小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=10:1-1:1,得到棕红色固体363mg,收率83%。1h nmr(500mhz,dmso-d6)δ1.52(s,9h),6.68(ddd,j=8.0,6.5,1.5hz,1h),7.16(dd,j=8.5,1.5hz,1h),7.32(ddd,j=8.5,6.5,1.5hz,1h),7.41(t,j=7.5hz,1h),7.92(dd,j=8.0,5.5hz,1h),7.96(d,j=7.5hz,1h),7.98(dd,j=8.5,1.5hz,1h),8.13
–
8.15(m,2h),8.20
–
8.27(m,3h),8.78(d,j=2.0hz,1h),8.91(dd,j=8.0,1.5hz,1h),10.71(dd,j=5.5,1.5hz,1h)。
[0068]
实施例8:四齿环金属铂(ii)配合物磷光发光材料pt-124合成路线如下:
[0069][0070]
中间体(l-124-ome)的合成:向带有磁力搅拌子的schlenk管中加入7a(600mg,
1.55mmol,1.0当量)、5b(613mg,1.63mmol,1.05当量)、四三苯基膦钯(36mg,0.031mmol,2mol%)和碳酸钾(428mg,3.10mmol,2.0当量)。然后抽换氮气三次,在氮气保护下加入1,4-二氧六环(5ml)和水(1ml)。100℃油浴锅中反应20小时后冷却至室温,减压蒸馏除去溶剂后粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=30:1-5:1,得到白色固体735mg,收率85%。1h nmr(500mhz,cdcl3)δ1.32(s,9h),1.44(s,9h),1.47(s,9h),3.39(s,3h),7.37
–
7.40(m,2h),7.61
–
7.64(m,2h),7.72
–
7.79(m,5h),7.89(d,j=2.0hz,1h),8.16
–
8.19(m,2h),8.44(t,j=2.0hz,1h),8.90(dd,j=4.0,2.0hz,1h)。
[0071]
配体l-124的合成:向带有磁力搅拌子的schlenk管中加入l-124-ome(700mg,1.26mmol,1.0当量)、吡啶盐酸盐(1.45g,12.57mmol,10.0当量)。然后抽换氮气三次,在氮气保护下加入1,3-二甲基-2-咪唑啉酮(3ml)。180℃油浴锅中反应19小时后冷却至室温,加入乙酸乙酯稀释,用水洗涤有机相,分液后用无水硫酸钠干燥,过滤,滤液减压蒸馏除去溶剂。所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=50:1-10:1,得到白色固体621mg,收率91%。1h nmr(500mhz,dmso-d6)δ1.33(s,9h),1.41(s,9h),1.46(s,9h),7.33(d,j=2.5hz,1h),7.55(dd,j=8.0,4.0hz,1h),7.71(t,j=7.5hz,1h),7.84(d,j=2.5hz,1h),7.85(dt,j=7.5,1.0hz,1h),7.95
–
7.97(m,2h),8.01
–
8.06(m,2h),8.12(t,j=8.0hz,1h),8.23
–
8.25(m,1h),8.27(t,j=2.0hz,1h),8.43(dd,j=8.0,1.5hz,1h),8.88(dd,j=4.0,2.0hz,1h),15.08(s,1h)。
[0072]
pt-124的合成:向带有磁力搅拌子的三口瓶中加入l-124(300mg,0.55mmol,1.0当量)、四氯铂酸钾(241mg,0.58mmol,1.05当量)和四丁基溴化铵(19mg,0.06mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(35ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,室温搅拌12小时,升温120℃反应72小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=10:1-1:1,得到棕黄色固体347mg,收率86%。1h nmr(500mhz,cdcl3)δ1.36(s,9h),1.52(s,9h),1.60(s,9h),7.36(t,j=7.5hz,1h),7.50(d,j=2.5hz,1h),7.56
–
7.58(m,2h),7.68(d,j=7.5hz,2h),7.78(d,j=2.0hz,1h),7.91
–
7.98(m,3h),8.48(dd,j=8.0,1.5hz,1h),8.62(d,j=2.0hz,1h),10.80(dd,j=5.5,1.5hz,1h)。
[0073]
实施例9:四齿环金属铂(ii)配合物磷光发光材料pt-139合成路线如下:
[0074][0075]
中间体(l-139-ome)的合成:向带有磁力搅拌子的schlenk管中加入7a(900mg,2.32mmol,1.0当量)、6b(767mg,2.44mmol,1.05当量)、四三苯基膦钯(54mg,0.046mmol,2mol%)和碳酸钾(641mg,4.64mmol,2.0当量)。然后抽换氮气三次,在氮气保护下加入1,4-二氧六环(8ml)和水(2ml)。90℃油浴锅中反应60小时后冷却至室温,减压蒸馏除去溶剂后
粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=30:1-10:1,得到白色固体1.09g,收率95%。1h nmr(500mhz,cdcl3)δ1.44(s,9h),3.87(s,3h),7.29
–
7.35(m,2h),7.38(dd,j=8.5,4.0hz,2h),7.41(dd,j=7.5,1.0hz,1h),7.57(t,j=7.5hz,1h),7.63
–
7.67(m,1h),7.72
–
7.75(m,2h),7.79
–
7.92(m,5h),8.11(ddd,j=7.5,2.0,1.0hz,1h),8.16(dd,j=8.0,1.5hz,1h),8.33(t,j=1.5hz,1h),8.88(dd,j=4.0,2.0hz,1h)。
[0076]
配体l-139的合成:向带有磁力搅拌子的schlenk管中加入l-139-ome(1.0g,2.01mmol,1.0当量)、吡啶盐酸盐(2.33g,20.14mmol,10.0当量)。然后抽换氮气三次,在氮气保护下加入1,3-二甲基-2-咪唑啉酮(3ml)。180℃油浴锅中反应24小时后冷却至室温,加入乙酸乙酯稀释,用水洗涤有机相,分液后用无水硫酸钠干燥,过滤,滤液减压蒸馏除去溶剂。所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=50:1-10:1,得到白色固体847mg,收率88%。1h nmr(500mhz,dmso-d6)δ1.42(s,9h),7.24
–
7.33(m,3h),7.50
–
7.54(m,2h),7.57
–
7.61(m,2h),7.70(dt,j=7.5,1.5hz,1h),7.82
–
7.86(m,2h),7.89(d,j=2.0hz,1h),7.92(d,j=2.5hz,1h),8.02(d,j=1.5hz,1h),8.03(s,1h),8.10(dt,j=8.0,1.5hz,1h),8.30(t,j=1.5hz,1h),8.40(dd,j=8.5,1.5hz,1h),8.83(dd,j=4.0,2.0hz,1h),10.11(s,1h)。
[0077]
pt-139的合成:向带有磁力搅拌子的三口瓶中加入l-139(300mg,0.62mmol,1.0当量)、四氯铂酸钾(272mg,0.66mmol,1.05当量)和四丁基溴化铵(20mg,0.06mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(40ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,室温搅拌13小时,升温120℃反应56小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=10:1-1:1,得到橙黄色固体371mg,收率89%。1h nmr(500mhz,dmso-d6)δ1.52(s,9h),7.18(ddd,j=8.0,7.0,1.0hz,1h),7.36(ddd,j=8.5,7.0,1.5hz,1h),7.39(d,j=9.0hz,1h),7.44(t,j=7.5hz,1h),7.78(dd,j=8.0,1.0hz,1h),7.81(d,j=9.0hz,1h),7.89
–
7.98(m,4h),8.09(dd,j=8.0,1.0hz,1h),8.13
–
8.19(m,2h),8.21(d,j=8.0hz,1h),8.77(d,j=2.0hz,1h),8.92(dd,j=8.5,1.5hz,1h),10.66(dd,j=5.5,1.5hz,1h)。
[0078]
实施例10:四齿环金属铂(ii)配合物磷光发光材料pt-137合成路线如下:
[0079][0080]
中间体(l-137-ome)的合成:向带有磁力搅拌子的schlenk管中加入7a(600mg,1.55mmol,1.0当量)、7b(511mg,1.63mmol,1.05当量)、四三苯基膦钯(36mg,0.031mmol,2mol%)和碳酸钾(428mg,3.10mmol,2.0当量)。然后抽换氮气三次,在氮气保护下加入1,4-二氧六环(5ml)和水(1ml)。100℃油浴锅中反应47小时后冷却至室温,减压蒸馏除去溶剂后
粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=30:1-10:1,得到白色固体693mg,收率90%。1h nmr(500mhz,cdcl3)δ1.48(s,9h),3.78(s,3h),7.41(dd,j=8.0,4.0hz,1h),7.50
–
7.57(m,2h),7.64(t,j=7.5hz,1h),7.71(d,j=8.5hz,1h),7.76
–
7.80(m,3h),7.83
–
7.88(m,2h),7.91(d,j=2.0hz,1h),8.08(d,j=7.5hz,1h),8.17(d,j=8.5hz,1h),8.18
–
8.22(m,2h),8.26(dd,j=8.0,1.5hz,1h),8.44(t,j=1.5hz,1h),8.91(dd,j=4.0,2.0hz,1h)。
[0081]
配体l-137的合成:向带有磁力搅拌子的schlenk管中加入l-137-ome(670mg,1.35mmol,1.0当量)、吡啶盐酸盐(1.57g,13.55mmol,10.0当量)。然后抽换氮气三次,在氮气保护下加入1,3-二甲基-2-咪唑啉酮(3ml)。180℃油浴锅中反应16小时后冷却至室温,加入乙酸乙酯稀释,用水洗涤有机相,分液后用无水硫酸钠干燥,过滤,滤液减压蒸馏除去溶剂。所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=50:1-10:1,得到浅黄色固体588mg,收率91%。1h nmr(500mhz,dmso-d6)δ1.50(s,9h),7.47(d,j=8.5hz,1h),7.52(ddd,j=8.0,6.5,1.5hz,1h),7.56
–
7.59(m,2h),7.74(t,j=7.5hz,1h),7.88(d,j=8.0hz,1h),7.91(dt,j=7.5,1.5hz,1h),7.99(d,j=2.5hz,1h),8.03
–
8.05(m,2h),8.08(ddd,j=7.5,2.0,1.0hz,1h),8.15
–
8.21(m,2h),8.30
–
8.34(m,2h),8.35(t,j=1.5hz,1h),8.45(dd,j=8.0,1.5hz,1h),8.91(dd,j=4.0,2.0hz,1h),16.39(s,1h)。
[0082]
pt-137的合成:向带有磁力搅拌子的三口瓶中加入l-137(300mg,0.62mmol,1.0当量)、四氯铂酸钾(272mg,0.66mmol,1.05当量)和四丁基溴化铵(20mg,0.06mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(40ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,室温搅拌12小时,升温120℃反应58小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=10:1-1:1,得到棕黄色固体152mg,收率36%。1h nmr(500mhz,cdcl3)δ1.54(s,9h),7.12(d,j=9.0hz,1h),7.38(t,j=7.5hz,1h),7.49
–
7.57(m,2h),7.68(dd,j=7.5,1.5hz,1h),7.69
–
7.75(m,3h),7.79(d,j=2.0hz,1h),7.88(d,j=9.0hz,1h),7.95
–
8.0(m,1h),8.03(d,j=8.0hz,2h),8.50(dd,j=8.0,1.5hz,1h),8.68(d,j=2.0hz,1h),8.79
–
8.82(m,1h),10.98(dd,j=5.5,1.5hz,1h)。
[0083]
实施例11:四齿环金属铂(ii)配合物磷光发光材料pt-134合成路线如下:
[0084][0085]
中间体(l-134-ome)的合成:向带有磁力搅拌子的schlenk管中加入7a(600mg,1.55mmol,1.0当量)、8b(553mg,1.63mmol,1.05当量)、四三苯基膦钯(61mg,0.046mmol,3mol%)和碳酸钾(610mg,3.87mmol,2.5当量)。然后抽换氮气三次,在氮气保护下加入1,4-二氧六环(8ml)和水(2ml)。85℃油浴锅中反应48小时后冷却至室温,减压蒸馏除去溶剂后粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=10:1,得到白色固体730mg,收率
80%。1h nmr(500mhz,cdcl3)δ1.44(s,9h),3.93(s,3h),7.09(d,j=8.5hz,1h),7.28
–
7.31(m,1h),7.35
–
7.40(m,3h),7.59
–
7.63(m,4h),7.74
–
7.76(m,3h),7.79(dd,j=10.5hz,1h),7.85(dd,j=8.0,1.5hz,1h),7.87(d,j=2.5hz,1h),8.14
–
8.18(m,2h),8.24(d,j=2.5hz,1h),8.41(t,j=3.0hz,1h),8.86(dd,j=4.0,1.5hz,1h)。
[0086]
配体l-134的合成:向带有磁力搅拌子的schlenk管中加入l-134-ome(710mg,1.36mmol,1.0当量)、吡啶盐酸盐(1.58g,13.6mmol,10.0当量)。然后抽换氮气三次,在氮气保护下加入1,3-二甲基-2-咪唑啉酮(4ml)。180℃油浴锅中反应12小时后冷却至室温,加入乙酸乙酯稀释,用水洗涤有机相,分液后用无水硫酸钠干燥,过滤,滤液减压蒸馏除去溶剂。所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=5:1,得到白色固体550mg,收率94%。1h nmr(500mhz,cdcl3)δ1.50(s,9h),7.11(d,j=8.5hz,1h),7.32
–
7.35(m,1h),7.41(dd,j=8.0,4.0hz,1h),7.44
–
7.47(m,2h),7.56(dd,j=8.5,2.0hz,1h),7.60
–
7.63(m,2h),7.68(t,j=7.5hz,1h),7.74(dd,j=6.0,1.0hz,1h),7.79(d,j=2.0hz,1h),7.84(dt,j=8.0,1.5hz,1h),7.91
–
7.98(m,3h),8.02(ddd,j=7.5,2.0,1.5hz,1h),8.07(d,j=2.0hz,1h),8.20(dd,j=8.5,2.0hz,1h),8.28(t,j=3.5hz,1h),8.92(dd,j=4.0,1.5hz,1h),14.82(s,1h)。
[0087]
pt-134的合成:向带有磁力搅拌子的三口瓶中加入l-134(300mg,0.59mmol,1.0当量)、四氯铂酸钾(257mg,0.62mmol,1.05当量)和四丁基溴化铵(19mg,0.06mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(35ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,室温搅拌12小时,升温120℃反应62小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=10:1-1:1,得到橙黄色固体318mg,收率77%。1h nmr(500mhz,dmso-d6)δ1.52(s,9h),7.25
–
7.29(m,2h),7.41
–
7.45(m,3h),7.68(dd,j=8.5,2.5hz,1h),7.72
–
7.74(m,2h),7.93(dd,j=8.5,5.5hz,1h),7.97(d,j=8.0hz,1h),8.15
–
8.17(m,2h),8.20(d,j=2.5hz,1h),8.25(t,j=7.0hz,2h),8.43(d,j=8.5hz,1h),8.78(d,j=2.5hz,1h),8.92(dd,j=8.5,2.0hz,1h),10.70(d,j=5.5,2.0hz,1h)。
[0088]
实施例12:四齿环金属铂(ii)配合物磷光发光材料pt-129合成路线如下:
[0089][0090]
中间体(l-129-ome)的合成:向带有磁力搅拌子的schlenk管中加入8a(443mg,1.0mmol,1.0当量)、2b(332mg,1.0mmol,1.0当量)、四三苯基膦钯(35mg,0.03mmol,3mol%)和碳酸钾(276mg,2.0mmol,2.0当量)。然后抽换氮气三次,在氮气保护下加入1,4-二氧六环
(4ml)和水(1ml)。100℃油浴锅中反应34小时后冷却至室温,减压蒸馏除去溶剂后粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=30:1-10:1,得到白色固体457mg,收率75%。1h nmr(500mhz,cdcl3)δ1.33(s,9h),1.45(s,9h),1.47(s,9h),1.47(s,9h),3.42(s,3h),7.37
–
7.40(m,2h),7.72
–
7.79(m,6h),7.88(d,j=2.5hz,1h),8.18(dd,j=8.0,2.0hz,1h),8.22(t,j=1.5hz,1h),8.27(t,j=1.5hz,1h),8.89(dd,j=4.0,2.0hz,1h)。
[0091]
配体l-129的合成:向带有磁力搅拌子的schlenk管中加入l-129-ome(424mg,0.69mmol,1.0当量)、吡啶盐酸盐(799mg,6.92mmol,10.0当量)。然后抽换氮气三次,在氮气保护下加入1,3-二甲基-2-咪唑啉酮(3ml)。180℃油浴锅中反应17小时后冷却至室温,加入乙酸乙酯稀释,用水洗涤有机相,分液后用无水硫酸钠干燥,过滤,滤液减压蒸馏除去溶剂。所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=50:1-10:1,得到黄色固体392mg,收率95%。1h nmr(500mhz,cdcl3)δ1.37(s,9h),1.49(s,9h),1.50(s,18h),7.39
–
7.42(m,2h),7.65
–
7.69(m,1h),7.72(d,j=2.5hz,1h),7.78(d,j=2.5hz,1h),7.85(t,j=1.5hz,1h),7.87
–
7.89(m,2h),7.93(d,j=2.0hz,1h),8.08
–
8.11(m,2h),8.19(dd,j=8.0,2.0hz,1h),8.94(dd,j=4.0,2.0hz,1h),15.09(s,1h)。
[0092]
pt-129的合成:向带有磁力搅拌子的三口瓶中加入l-129(250mg,0.42mmol,1.0当量)、四氯铂酸钾(182mg,0.44mmol,1.05当量)和四丁基溴化铵(14mg,0.042mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(25ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,室温搅拌12小时,升温120℃反应72小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=10:1-1:1,得到棕黄色固体170mg,收率51%。1h nmr(500mhz,cdcl3)δ1.36(s,9h),1.49(s,9h),1.53(s,9h),1.61(s,9h),7.50(d,j=2.5hz,1h),7.56(dd,j=8.0,5.5hz,1h),7.59(d,j=2.5hz,1h),7.71
–
7.73(m,2h),7.77(d,j=2.0hz,1h),7.90
–
7.98(m,2h),8.01(d,j=1.0hz,1h),8.47(dd,j=8.0,1.5hz,1h),8.62(d,j=2.0hz,1h),10.79(dd,j=5.5,2.0hz,1h)。
[0093]
实施例13:四齿环金属铂(ii)配合物磷光发光材料pt-210合成路线如下:
[0094][0095]
中间体(l-210-ome)的合成:向带有磁力搅拌子的schlenk管中加入8a(410mg,0.92mmol,1.05当量)、8b(300mg,0.88mmol,1.00当量)、四三苯基膦钯(30mg,0.026mmol,3mol%)和碳酸钾(304mg,2.2mmol,2.5当量)。然后抽换氮气三次,在氮气保护下加入1,4-二氧六环(6ml)和水(2ml)。85℃油浴锅中反应48小时后冷却至室温,减压蒸馏除去溶剂后粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=50:1-10:1,得到白色固体450mg,收率88%。1h nmr(500mhz,cdcl3)δ1.45(s,9h),1.48(s,9h),3.94(s,3h),7.09(d,j=4.0hz,
1h),7.28
–
7.31(m,1h),7.34
–
7.41(m,3h),7.61
–
7.65(m,3h),7.72
–
7.74(m,2h),7.77
–
7.80(m,2h),7.87(d,j=6.0hz,1h),7.90(dd,j=7.5,1.0hz,1h),8.17(dd,j=8.0,1.5hz,1h),8.20(t,j=3.5hz,2h),8.39(d,j=2.5hz,1h),8.85(dd,j=4.0,2.0hz,1h)。
[0096]
配体l-210的合成:向带有磁力搅拌子的schlenk管中加入l-210-ome(430mg,0.75mmol,1.0当量)、吡啶盐酸盐(861mg,7.5mmol,10.0当量)。然后抽换氮气三次,在氮气保护下加入1,3-二甲基-2-咪唑啉酮(3ml)。180℃油浴锅中反应12小时后冷却至室温,加入乙酸乙酯稀释,用水洗涤有机相,分液后用无水硫酸钠干燥,过滤,滤液减压蒸馏除去溶剂。所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=10:1,得到白色固体300mg,收率72%。1h nmr(500mhz,cdcl3)δ1.50(s,9h),1.50(s,9h),7.12(d,j=8.0hz,1h),7.32
–
7.35(m,1h),7.41(d,j=8.5,4.5hz,1h),7.44
–
7.47(m,2h),7.56(dd,j=8.5,2.0hz,1h),7.61
–
7.63(m,2h),7.74(dd,j=7.5,1.5hz,1h),7.78(d,j=2.5hz,1h),7.85(t,j=3.5hz,1h),7.91
–
7.97(m,3h),8.07(t,j=3.5hz,2h),8.09(t,j=3.5hz,1h),8.20(dd,j=8.5,2.0hz,1h),8.92(dd,j=4.0,1.5hz,1h),14.78(s,1h)。
[0097]
pt-210的合成:向带有磁力搅拌子的三口瓶中加入l-210(200mg,0.36mmol,1.0当量)、四氯铂酸钾(162mg,0.400mmol,1.1当量)和四丁基溴化铵(11mg,0.036mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(15ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,室温搅拌12小时,升温120℃反应48小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=10:1,得到黄色固体205mg,收率76%。1h nmr(500mhz,dmso-d6)δ1.49(s,9h),1.54(s,9h),7.24
–
7.29(m,2h),7.44(t,j=7.5hz,2h),7.68(dd,j=8.5,2.0hz,1h),7.74(dd,j=8.5,1.5hz,2h),7.94(dd,j=8.0,5.5hz,1h),8.02(d,j=1.5hz,1h),8.08(d,j=1.0hz,1h),8.17(d,j=2.0hz,1h),8.20(d,j=2.5hz,1h),8.24(t,j=7.0hz,1h),8.30
–
8.31(m,1h),8.42
–
8.44(m,1h),8.73(d,j=2.5hz,1h),8.94(dd,j=8.5,1.5hz,1h),10.69(dd,j=5.5,2.0hz,1h)。
[0098]
实施例14:四齿环金属铂(ii)配合物磷光发光材料pt-144合成路线如下:
[0099][0100]
中间体(l-144-ome)的合成:向带有磁力搅拌子的schlenk管中加入8a(590mg,1.33mmol,1.05当量)、6b(400mg,1.27mmol,1.0当量)、四三苯基膦钯(44mg,0.038mmol,3mol%)和碳酸钾(351mg,2.54mmol,2.0当量)。然后抽换氮气三次,在氮气保护下加入1,4-二氧六环(4ml)和水(1ml)。90℃油浴锅中反应24小时后冷却至室温,减压蒸馏除去溶剂后粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=30:1-10:1,得到白色固体633mg,收
率86%。1h nmr(500mhz,cdcl3)δ1.43(s,9h),1.44(s,9h),3.88(s,3h),7.30
–
7.35(m,2h),7.36
–
7.39(m,2h),7.42(dd,j=7.5,1.0hz,1h),7.72(d,j=2.5hz,1h),7.73
–
7.76(m,2h),7.79
–
7.82(m,2h),7.83(d,j=2.0hz,1h),7.87(t,j=7.5hz,1h),7.90(d,j=9.0hz,1h),8.12(t,j=2.0hz,1h),8.14
–
8.17(m,2h),8.87(dd,j=4.0,2.0hz,1h)。
[0101]
配体l-144的合成:向带有磁力搅拌子的schlenk管中加入l-144-ome(603mg,1.09mmol,1.0当量)、吡啶盐酸盐(1.26g,10.9mmol,10.0当量)。然后抽换氮气三次,在氮气保护下加入1,3-二甲基-2-咪唑啉酮(4ml)。180℃油浴锅中反应22小时后冷却至室温,加入乙酸乙酯稀释,用水洗涤有机相,分液后用无水硫酸钠干燥,过滤,滤液减压蒸馏除去溶剂。所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=50:1-10:1,得到白色固体478mg,收率82%。1h nmr(500mhz,cdcl3)δ1.48(s,9h),1.49(s,9h),7.26
–
7.28(m,1h),7.34(ddd,j=8.0,6.5,1.0hz,1h),7.40(dd,j=8.0,4.0hz,1h),7.44
–
7.48(m,1h),7.77
–
7.82(m,4h),7.84(t,j=1.5hz,1h),7.87(dd,j=8.0,1.0hz,1h),7.90(d,j=2.0hz,1h),7.95(t,j=8.0hz,1h),8.15(dt,j=5.5,1.5hz,2h),8.19(dd,j=8.0,1.5hz,1h),8.28(d,j=8.5hz,1h),8.91(dd,j=4.0,2.0hz,1h),13.04(s,1h)。
[0102]
pt-144的合成:向带有磁力搅拌子的三口瓶中加入l-144(200mg,0.37mmol,1.0当量)、四氯铂酸钾(162mg,0.39mmol,1.05当量)和四丁基溴化铵(12mg,0.037mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(25ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,室温搅拌12小时,升温120℃反应72小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=10:1-1:1,得到棕红色固体231mg,收率86%。1h nmr(500mhz,cdcl3)δ1.51(s,9h),1.54(s,9h),7.16(ddd,j=8.0,6.5,1.0hz,1h),7.30(ddd,j=8.5,7.0,1.5hz,1h),7.47(d,j=9.0hz,1h),7.62(dd,j=8.0,5.5hz,1h),7.71(dd,j=8.0,1.0hz,1h),7.72
–
7.74(m,2h),7.77
–
7.78(m,2h),7.91(t,j=7.5hz,1h),7.94
–
7.96(m,2h),8.07(d,j=1.5hz,1h),8.48(dd,j=8.0,1.5hz,1h),8.69(d,j=2.0hz,1h),10.75(dd,j=5.5,1.5hz,1h)。
[0103]
实施例15:四齿环金属铂(ii)配合物磷光发光材料pt-142合成路线如下:
[0104][0105]
中间体(l-142-ome)的合成:向带有磁力搅拌子的schlenk管中加入8a(593mg,1.34mmol,1.05当量)、7b(400mg,1.27mmol,1.0当量)、四三苯基膦钯(45mg,0.04mmol,3mol%)和碳酸钾(351mg,2.54mmol,2.0当量)。然后抽换氮气三次,在氮气保护下加入1,4-二氧六环(6ml)和水(1ml)。85℃油浴锅中反应70小时后冷却至室温,减压蒸馏除去溶剂后
二氧六环(5ml)和水(1ml)。100℃油浴锅中反应20小时后冷却至室温,减压蒸馏除去溶剂后粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=30:1-10:1,得到白色固体505mg,收率74%。1h nmr(500mhz,cdcl3)δ1.33(s,9h),1.45(s,9h),1.48(s,9h),3.43(s,3h),7.38
–
7.46(m,3h),7.49
–
7.53(m,2h),7.74
–
7.80(m,6h),7.83(t,j=1.5hz,1h),8.02(d,j=2.0hz,1h),8.09(d,j=2.0hz,1h),8.27(dd,j=8.0,2.0hz,1h),8.29(t,j=1.5hz,1h),8.30(t,j=1.5hz,1h),8.96(dd,j=4.0,2.0hz,1h)。
[0111]
配体l-591的合成:向带有磁力搅拌子的schlenk管中加入l-591-ome(468mg,0.74mmol,1.0当量)、吡啶盐酸盐(855mg,7.4mmol,10.0当量)。然后抽换氮气三次,在氮气保护下加入1,3-二甲基-2-咪唑啉酮(3ml)。180℃油浴锅中反应12小时后冷却至室温,加入乙酸乙酯稀释,用水洗涤有机相,分液后用无水硫酸钠干燥,过滤,滤液减压蒸馏除去溶剂。所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=50:1-10:1,得到白色固体392mg,收率86%。1h nmr(500mhz,cdcl3)δ1.37(s,9h),1.49(s,18h),7.41
–
7.45(m,2h),7.46(dd,j=8.0,4.0hz,1h),7.51
–
7.54(m,2h),7.69(dd,j=6.0,2.5hz,1h),7.72(d,j=2.5hz,1h),7.78
–
7.81(m,2h),7.86
–
7.90(m,3h),8.05(d,j=2.0hz,1h),8.10(d,j=2.0hz,1h),8.15(dt,j=6.5,1.5hz,2h),8.28(dd,j=8.5,1.5hz,1h),9.01(dd,j=4.0,2.0hz,1h),15.08(s,1h)。
[0112]
pt-591的合成:向带有磁力搅拌子的三口瓶中加入l-591(250mg,0.40mmol,1.0当量)、四氯铂酸钾(176mg,0.42mmol,1.05当量)和四丁基溴化铵(14mg,0.04mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(24ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,室温搅拌12小时,升温120℃反应74小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=10:1-1:1,得到棕黄色固体250mg,收率77%。1h nmr(500mhz,cdcl3)δ1.37(s,9h),1.48(s,9h),1.63(s,9h),7.47
–
7.51(m,1h),7.51(d,j=2.5hz,1h),7.56
–
7.62(m,4h),7.74(d,j=7.5hz,1h),7.75(d,j=1.5hz,1h),7.80
–
7.83(m,2h),7.92(d,j=7.5hz,1h),7.98(t,j=8.0hz,1h),8.02(d,j=2.0hz,1h),8.07(d,j=1.0hz,1h),8.55(dd,j=8.0,1.5hz,1h),8.74(d,j=2.0hz,1h),10.86(dd,j=5.5,1.5hz,1h)。
[0113]
实施例17:四齿环金属铂(ii)配合物磷光发光材料pt-592合成路线如下:
[0114][0115]
中间体(l-592-ome)的合成:向带有磁力搅拌子的schlenk管中加入10a(407mg,1.0mmol,1.0当量)、2b(332mg,1.0mmol,1.0当量)、四三苯基膦钯(35mg,0.03mmol,3mol%)和碳酸钾(276mg,2.0mmol,2.0当量)。然后抽换氮气三次,在氮气保护下加入1,4-二氧六环
(4ml)和水(1ml)。100℃油浴锅中反应20小时后冷却至室温,减压蒸馏除去溶剂后粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=30:1-10:1,得到白色固体443mg,收率77%。1h nmr(500mhz,cdcl3)δ1.30(s,9h),1.44(s,9h),3.40(s,3h),7.37(d,j=2.5hz,1h),7.39
–
7.43(m,1h),7.45(dd,j=8.0,4.0hz,1h),7.48
–
7.52(m,2h),7.63
–
7.66(m,2h),7.74
–
7.78(m,5h),7.84(ddd,j=7.5,2.0,1.5hz,1h),8.03(d,j=2.5hz,1h),8.10(d,j=2.0hz,1h),8.21(ddd,j=8.0,2.0,1.0hz,1h),8.28(dd,j=8.5,2.0hz,1h),8.50(t,j=3.5hz,1h),8.96(dd,j=4.0,2.0hz,1h)。
[0116]
配体l-592的合成:向带有磁力搅拌子的schlenk管中加入l-592-ome(415mg,0.72mmol,1.0当量)、吡啶盐酸盐(831mg,7.2mmol,10.0当量)。然后抽换氮气三次,在氮气保护下加入1,3-二甲基-2-咪唑啉酮(3ml)。180℃油浴锅中反应15小时后冷却至室温,加入乙酸乙酯稀释,用水洗涤有机相,分液后用无水硫酸钠干燥,过滤,滤液减压蒸馏除去溶剂。所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/乙酸乙酯=50:1-10:1,得到白色固体360mg,收率89%。1h nmr(500mhz,cdcl3)δ1.37(s,9h),1.48(s,9h),7.40(d,j=2.5hz,1h),7.43(dt,j=7.0,1.5hz,1h),7.47(dd,j=8.0,4.0hz,1h),7.50
–
7.54(m,2h),7.68
–
7.71(m,3h),7.78
–
7.81(m,2h),7.88
–
7.90(m,3h),8.02
–
8.04(m,1h),8.05(d,j=2.0hz,1h),8.12(d,j=2.5hz,1h),8.29(dd,j=8.5,2.0hz,1h),8.35(t,j=7.5hz,1h),9.01(dd,j=4.0,1.5hz,1h),14.82(s,1h)。
[0117]
pt-592的合成:向带有磁力搅拌子的三口瓶中加入l-592(200mg,0.36mmol,1.0当量)、四氯铂酸钾(154mg,0.37mmol,1.05当量)和四丁基溴化铵(12mg,0.036mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(23ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,室温搅拌12小时,升温120℃反应73小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=10:1-1:1,得到棕黄色固体250mg,收率92%。1h nmr(500mhz,cdcl3)δ1.37(s,9h),1.62(s,9h),7.36(t,j=7.5hz,1h),7.46
–
7.52(m,2h),7.55
–
7.59(m,3h),7.62(dd,j=8.0,5.5hz,1h),7.69(dt,j=7.5,1.0hz,2h),7.80
–
7.82(m,2h),7.92
–
7.99(m,2h),8.03
–
8.05(m,2h),8.56(dd,j=8.0,1.5hz,1h),8.77(d,j=2.0hz,1h),10.88(dd,j=5.5,1.5hz,1h)。
[0118]
实施例18:四齿环金属钯(ii)配合物磷光发光材料pd-183合成路线如下:
[0119][0120]
pd-183的合成:向带有磁力搅拌子的三口瓶中加入l-183(200mg,0.31mmol,1.0当量)、醋酸钯(72mg,0.22mmol,1.05当量)和四丁基溴化铵(10mg,0.03mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(20ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,升温100℃反应75小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=5:1-1:1,得到黄色固体150mg,收率64%。1h nmr(500mhz,cdcl3)δ1.37(s,9h),1.60(s,9h),7.32(ddd,j=8.0,7.0,1.0hz,2h),7.42
–
7.50(m,6h),7.60(dd,j=6.5,2.5hz,1h),7.68
–
7.72(m,2h),7.81(d,j=2.0hz,1h),7.86
–
7.91(m,2h),7.93(dd,j=8.0,1.0hz,1h),8.05(d,j=1.5hz,1h),8.20(t,j=1.0hz,1h),8.21(t,j=1.0hz,1h),8.43(dd,j=8.0,1.5hz,1h),8.52(dd,j=8.0,1.5hz,1h),10.65(dd,j=5.0,1.5hz,1h)。
[0121]
实施例19:四齿环金属钯(ii)配合物磷光发光材料pd-124合成路线如下:
[0122][0123]
pd-124的合成:向带有磁力搅拌子的三口瓶中加入l-124(270mg,0.50mmol,1.0当量)、醋酸钯(117mg,0.52mmol,1.05当量)和四丁基溴化铵(16mg,0.05mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(30ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,升温120℃反应90小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=5:1-1:1,得到黄色固体121mg,收率37%。1h nmr(500mhz,cdcl3)δ1.35(s,9h),1.52(s,9h),1.56(s,9h),7.35(t,j=7.5hz,1h),7.42
–
7.45(m,2h),7.60(dd,j=8.0,5.0hz,1h),7.63
–
7.66(m,2h),7.80
–
7.82(m,2h),7.88(q,j=7.5hz,2h),8.43(dd,j=8.0,1.5hz,1h),8.57(d,j=2.0hz,1h),10.48(dd,j=5.0,1.5hz,1h)。
[0124]
实施例20:四齿环金属钯(ii)配合物磷光发光材料pd-210合成路线如下:
[0125][0126]
pd-210的合成:向带有磁力搅拌子的三口瓶中加入l-210(150mg,0.27mmol,1.0当量)、醋酸钯(63mg,0.28mmol,1.05当量)和四丁基溴化铵(9mg,0.027mmol,0.1当量),抽换氮气三次,在氮气保护下加入醋酸(15ml),氮气鼓泡除氧30min。将三口瓶放入带有磁力搅拌的油浴锅中,升温120℃反应48小时,反应冷却至室温后减压蒸馏除去溶剂,所得粗产品用硅胶层析柱分离,洗脱剂:石油醚/二氯甲烷=1:1,得到黄色固体80mg,收率44%。1h nmr(500mhz,cdcl3)δ1.38(s,9h),1.40(s,9h),6.67(dd,j=8.0,5.0hz,1h),7.15(d,j=2.0hz,1h),7.23
–
7.25(m,2h),7.43(t,j=7.5hz,2h),7.51
–
7.57(m,3h),7.69(d,j=7.5hz,1h),7.78
–
7.80(m,2h),7.91(d,j=2.5hz,1h),8.00(t,j=7.0hz,1h),8.06(d,j=2.0hz,1h),8.11(d,j=8.0hz,1h),8.16(d,j=2.5hz,1h),9.95
–
9.96(m,1h)。
[0127]
实验数据及分析:
[0128]
基于双齿配体的二价铂金属配合物磷光量子效率一般较低,一般小于30%,(inorganic chemistry 2002,41,3055-3066.);经典的红光四齿环金属铂配合物pton11me(organic electronics 2014,15,1862-1867.)在室温下二氯甲烷溶液中发射光谱的半峰
宽约为100nm,在聚甲基丙烯酸甲酯(pmma)中的量子效率为40%。
[0129][0130]
表1及图1-图5为本发明的二价铂和钯金属配合物(磷光材料)在室温下二氯甲烷溶液中的光物理性能测试结果,从表中数据可知二价铂金属配合物磷光材料的发射波长处于611-626nm之间,为红光发光区域;半峰宽较小,均在60nm及以下,具有较高的色纯度;其在聚甲基丙烯酸甲酯(pmma)中的量子效率较高,多在50%以上,甚至可达80%及以上;热分解温度高于300℃,甚至在350℃以上,可满足热蒸镀oled器件的制备。同时,通过中心金属离子的调控可对光物理性质进行高效调控,如pd-124可实现单分子的白光发光。
[0131]
表1.本发明的二价铂和钯金属配合物在室温下二氯甲烷溶液中的光物理性能测试结果
[0132][0133]
注:分子结构如下:
[0134][0135]
因此,本发明的二价铂金属配合物分子在oled显示和照明等诸多领域具一定的应用价值。
[0136]
同时,我们对部分铂配合物进行了dft理论计算,如下表2中所示,通过配体结构和类型的调控可对材料分子的最低非占有轨道(lumo)和最高占有轨道(homo)的能级进行调控,以满足和不同器件结构的匹配;同时,从表2中亦可看出homo和lumo之间的带隙为2.30-2.70ev。
[0137]
表2.理论计算得到的配合物的前线轨道能级及带隙
[0138]
[0139][0140]
注:分子结构如下:
[0141]
[0142][0143]
器件实施例
[0144]
本发明的有机发光器件的各层可采用真空蒸镀、溅射、离子电镀等方法,或湿法成膜如旋涂、打印、印刷等方法形成,所用的溶剂没有特别限制。
[0145]
在本发明的一种优选实施方式中,本发明的oled器件中含有空穴传输层,空穴传输材料可以优选自已知或未知的材料,特别优选地选自以下结构,但并不代表本发明限于以下结构:
[0146][0147]
在本发明的一种优选实施方式中,本发明的oled器件中含有的空穴传输层,其包含一种或多种p型掺杂剂。本发明优选的p型掺杂剂为以下结构,但并不代表本发明限于以下结构:
[0148][0149]
本发明的一种优选实施方式中,所述的电子传输层可以选自化合物et-1至et-13的至少一种,但并不代表本发明限于以下结构:
[0150][0151]
电子传输层可以有机材料与一种或多种n型掺杂剂(如liq)共同形成。
[0152]
oled器件实施例:
[0153]
具体实施底发射oled器件的结构为在含有ito的玻璃上,空穴注入层(hil)为ht-1:p-3(95:5v/v%),厚度为10纳米;空穴传输层(htl)为ht-1,厚度为90纳米;电子阻挡层(ebl)为ht-10,厚度为10纳米,发光层(eml)为主体材料(rh):本发明铂金属配合物(95:5v/v%),厚度为35纳米,电子传输层(etl)为et-13:liq(50:50v/v%),厚度为35纳米,然后蒸镀阴极al为70纳米。主体材料(rh)可选自如下结构:
[0154][0155]
制作的有机发光器件采用本领域公知的标准方法在10ma/cm2电流条件下测试电压、效率和寿命。
[0156]
表3.本发明实施例和对比例制备得到的有机发光器件的性能检测结果。
[0157][0158]
如表3所示,上述实施例和对比例中的器件结构除了发光层不同外,其它均一致,基于pton11me的器件性能为参考,包含本发明的二价铂金属配合物的器件,相比常规的有机发光器件,电流效率有了显著提高,同时其寿命也有所提高。综上所述,本发明中新型的二价铂金属配合物在有机光电器件上具有较大的应用价值。
[0159]
本领域的普通技术人员可以理解,上述各实施方式是实现本发明的具体实施例,而在实际应用中,可以在形式上和细节上对其作各种改变,而不偏离本发明的精神和范围。例如,在不背离本发明的精神的情况下,这里描述的许多取代基结构可以用其它结构代替。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。