1.本发明涉及荧光探针技术领域,特别是涉及一种用于快速检测半胱氨酸的荧光探针及其合成方法与应用。
背景技术:
2.半胱氨酸(cys)、同型半胱氨酸(hcy)和谷胱甘肽(gsh)等生物硫醇在生物系统中发挥着关键作用,这些生物硫醇的异常水平与许多疾病有关,因而日益受到关注。例如,cys缺乏与许多综合症有关,如儿童生长发育迟缓、毛发异常、水肿、嗜睡、肌肉和脂肪损失以及皮肤损伤等。谷胱甘肽缺乏症也与许多疾病有关,如肝损伤、白细胞丢失、癌症、艾滋病和神经退行性疾病等。因此,开发快速、方便、灵敏地检测这些微量生物硫醇的技术仍然具有非常重要的意义。
3.过去的几十年中,基于高效液相色谱法(hplc)、分光光度法和电化学检测分析技术的多种复杂分析方法已经开发出来。其中,基于荧光的分子成像是最有吸引力的方法,因为其具有操作简单、灵敏度高、选择性好、响应时间短、检测限低以及对生物样品的良好生物相容性等优点。
4.目前已经开发了许多基于不同反应机制的cys荧光探针,在这些方法中,已报道的能够检测亚半胱氨酸的荧光探针通常分子结构复杂,在复杂环境中性质不稳定,无法实现快速、可视化的检测,荧光探针的选择性和灵敏性较差。
技术实现要素:
5.本发明的目的在于提供一种用于快速检测半胱氨酸的荧光探针及其合成方法与应用,以解决上述背景技术中提出的问题。
6.本发明是通过以下技术方案实现的:
7.一种用于快速检测半胱氨酸的荧光探针,包括cac-1和cac-2,cac-1为2-甲氧基-4-((e)-(3-((e)-2-甲氧基亚苄基)-2氧代亚环戊基)甲基)丙烯酸苯酯,cac-2为4-((e)-(3-((e)-4-(丙烯酰氧基)-2-甲氧基亚苄基)-2-氧代环戊基亚甲基)甲基)-2-甲氧基苯基丙烯酸酯,其化学结构式如下:
[0008][0009]
本发明还提供了一种上述用于快速检测半胱氨酸的荧光探针的合成方法,具体包括如下步骤:
[0010]
(1)化合物1的合成:取香草醇溶解于混合溶液1中并搅拌均匀,将混合均匀的溶液
缓慢滴加至混合溶液2中,在室温下搅拌10~20h,过滤得到固体,将所得固体溶于水中,并用稀盐酸酸化直至产生浅黄色固体,抽滤后用乙醇重结晶得到黄色固体产物,即化合物1;
[0011]
(2)化合物ca-1的合成:分别称取步骤(1)得到的化合物1与邻甲氧基苯甲醛,并将其溶解于无水乙醇中,再加入催化剂反应0.5~2h,反应完全后室温下密封放置2天,减压抽滤,并依次用无水乙醇和二次蒸馏水水洗至中性,得到粗产品,利用柱层析法对粗产品进行提纯处理,除去溶剂干燥后得到产物ca-1;
[0012]
(3)化合物cac-1的合成:分别称取步骤(2)得到的化合物ca-1与三乙胺,并将其溶解于无水二氯甲烷中,再逐滴加入丙烯酰氯,室温下搅拌过夜,得到粗产物,通过柱层析法对粗产品进行提纯处理,除去溶剂干燥后得到产物cac-1;
[0013]
(4)化合物ca-2的合成:分别称取步骤(1)得到的化合物1与4-羟基-2-甲氧基苯甲醛,并将其溶解于无水乙醇中,再加入催化剂反应0.5~2h,反应完全后室温下密封放置2天,减压抽滤,并依次用无水乙醇和二次蒸馏水水洗至中性,得到粗产品,利用柱层析法对粗产品进行提纯处理,除去溶剂干燥后得到产物ca-2;
[0014]
(5)化合物cac-2的合成:分别称取步骤(4)得到的化合物ca-2与三乙胺,并将其溶解于无水二氯甲烷中,在0℃冰水浴中充分搅拌,再逐滴加入丙烯酰氯,室温下搅拌过夜,得到粗产物,通过柱层析法对粗产品进行提纯处理,除去溶剂干燥后得到产物cac-2。
[0015]
优选的,步骤(2)和(4)中,使用的催化剂均为浓hcl。
[0016]
优选的,步骤(2)和(4)中,水洗使用的无水乙醇和二次蒸馏水均为低于室温的溶剂。
[0017]
优选的,步骤(2)、(3)、(5)中,层析使用的洗脱剂为pe-ea,其中pe和ea的体积比为2:1;步骤(4)中,层析使用的洗脱剂为dcm-ea,其中dcm和ea的体积比为5:1。
[0018]
作为本发明的进一步方案,步骤(1)中,混合溶液1为乙醇和5~15%naoh水溶液的混合溶液,乙醇与5~15%naoh水溶液的体积比为10~20:5~15;混合溶液2为环戊酮和5~15%naoh水溶液的混合溶液,环戊酮和5~15%naoh水溶液的体积比为1~4:3~10。
[0019]
本发明还提供了一种上述荧光探针在检测环境或食品中半胱氨酸的应用。
[0020]
与现有技术相比,本发明的有益效果是:
[0021]
1.本发明是以姜黄素衍生物为荧光母体、丙烯酰酯为检测基团的荧光探针,分子结构简单,本发明提供的探针能够用于快速地裸眼识别半胱氨酸。
[0022]
2.本发明提供的荧光探针对半胱氨酸的检测限低,在识别半胱氨酸时,对其他离子没有响应,具备高选择性和良好的抗干扰能力和ph适应性。
附图说明
[0023]
为了更清楚地说明本发明实施例的技术方案,下面将对实施例描述所需要使用的附图作简单地介绍,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
[0024]
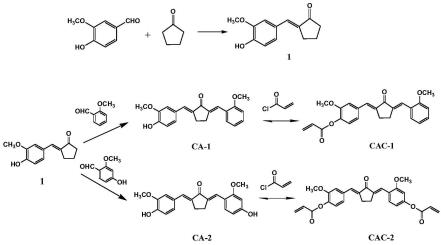
图1为本发明的合成路线示意图;
[0025]
图2为cac-1与cys/hcy/gsh(200μm)响应的紫外光谱(a)和荧光光谱(b),λ
ex
=400nm,λ
em
=525nm;
[0026]
图3为cac-2与cys/hcy/gsh(200μm)响应的紫外光谱(a)和荧光光谱(b),λ
ex
=
400nm;
[0027]
图4为cac-1与cys(200μm)的时间响应荧光光谱图(λ
ex
=400nm);
[0028]
图5为cac-2与cys(200μm)的时间响应荧光光谱图(λ
ex
=400nm);
[0029]
图6为cac-1与不同浓度cys响应的浓度滴定线性关系图(λ
ex
=400nm);
[0030]
图7为cac-2与不同浓度cys响应的浓度滴定线性关系图(λ
ex
=400nm);
[0031]
图8为cac-1与不同氨基酸(20eq)响应的荧光光谱(a)和荧光强度比较(b),λ
ex
=400nm;
[0032]
图9为探针cac-1检测cys(20eq)的抗干扰性测试结果示意图;
[0033]
图10为探针cac-2与不同氨基酸(20eq)响应的荧光光谱(a)和荧光强度比较(b),λ
ex
=400nm;
[0034]
图11为探针cac-2检测cys(20eq)的抗干扰性测试结果示意图;
[0035]
图12为本发明探针cac-1的质谱图;
[0036]
图13为本发明探针cac-2的质谱图;
[0037]
图14为化合物cac-1的1h nmr谱图;
[0038]
图15为化合物cac-2的1h nmr谱图。
具体实施方式
[0039]
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0040]
若如无特别说明,实施例中所使用的材料均可容易地从商业公司获取。
[0041]
实施例1:
[0042]
本实施例提供了一种用于快速检测半胱氨酸的荧光探针的合成方法,合成路线如图1所示,具体包括如下步骤:
[0043]
(1)化合物1的合成:取1~2g香草醇溶解于混合溶液1中并搅拌均匀,将混合均匀的溶液缓慢滴加至混合溶液2中,在室温下搅拌10~20h,过滤得到固体,将所得固体溶于水中,并用稀盐酸酸化直至产生浅黄色固体,抽滤后用乙醇重结晶得到黄色固体产物,即化合物1;
[0044]
其中,混合溶液1为10~20ml的5~15%naoh水溶液和5~15ml乙醇的混合溶液,混合溶液2为3~10ml的5~15%naoh水溶液和1~4ml环戊酮的混合溶液。
[0045]
(2)化合物ca-1的合成:分别称取1~2g步骤(1)得到的化合物1与0.5~1g邻甲氧基苯甲醛,并将其溶解于10~30ml无水乙醇中,再加入0.05~0.2ml浓hcl作为催化剂反应0.5~2h,反应完全后室温下密封放置2天,减压抽滤,并依次用冷的无水乙醇和二次蒸馏水水洗至中性,得到粗产品,利用柱层析法对粗产品进行提纯处理,洗脱剂pe:ea=2:1,除去溶剂干燥后得到产物ca-1。
[0046]
(3)化合物cac-1的合成:分别称取0.5~2g步骤(2)得到的化合物ca-1与0.3~2ml三乙胺,并将其溶解于5~20ml无水二氯甲烷中,再逐滴加入0.1~1ml丙烯酰氯,室温下搅拌过夜,得到粗产物,通过柱层析法对粗产品进行提纯处理,洗脱剂pe:ea=2:1,除去溶剂干燥后得到产物cac-1。
[0047]
本实施例还提供了一种根据上述合成方法制备得到的用于快速检测半胱氨酸的荧光探针cac-1,根据附图12质谱图和图14核磁谱图可知,荧光探针cac-1为2-甲氧基-4-((e)-(3-((e)-2-甲氧基亚苄基)-2氧代亚环戊基)甲基)丙烯酸苯酯,且cac-1的纯度高于80%。
[0048]
本实施例还提供了一种上述荧光探针在检测环境或食品中半胱氨酸的应用。
[0049]
实施例2:
[0050]
本实施例提供了一种用于快速检测半胱氨酸的荧光探针的合成方法,合成路线如图1所示,具体包括如下步骤:
[0051]
(1)化合物1的合成:取1~2g香草醇溶解于混合溶液1中并搅拌均匀,将混合均匀的溶液缓慢滴加至混合溶液2中,在室温下搅拌10~20h,过滤得到固体,将所得固体溶于水中,并用稀盐酸酸化直至产生浅黄色固体,抽滤后用乙醇重结晶得到黄色固体产物,即化合物1;
[0052]
其中,混合溶液1为10~20ml的5~15%naoh水溶液和5~15ml乙醇的混合溶液,混合溶液2为3~10ml的5~15%naoh水溶液和1~4ml环戊酮的混合溶液。
[0053]
(2)化合物ca-2的合成:分别称取1~2g步骤(1)得到的化合物1与0.5~1g的4-羟基-2-甲氧基苯甲醛,并将其溶解于10~30ml无水乙醇中,再加入0.05~0.2ml浓hcl作为催化剂反应0.5~2h,反应完全后室温下密封放置2天,减压抽滤,并依次用冷的无水乙醇和二次蒸馏水水洗至中性,得到粗产品,利用柱层析法对粗产品进行提纯处理,洗脱剂dcm:ea=5:1,除去溶剂干燥后得到产物ca-2;
[0054]
(3)化合物cac-2的合成:分别称取1~2g步骤(4)得到的化合物ca-2与0.5~1ml三乙胺,并将其溶解于5~20ml无水二氯甲烷中,在0℃冰水浴中充分搅拌,再逐滴加入0.1~1ml丙烯酰氯,室温下搅拌过夜,得到粗产物,通过柱层析法对粗产品进行提纯处理,洗脱剂pe:ea=2:1,除去溶剂干燥后得到产物cac-2。
[0055]
本实施例还提供了一种根据上述合成方法制备得到的用于快速检测半胱氨酸的荧光探针cac-2,根据附图13质谱图和图15核磁谱图可知,荧光探针cac-2为4-((e)-(3-((e)-4-(丙烯酰氧基)-2-甲氧基亚苄基)-2-氧代环戊基亚甲基)甲基)-2-甲氧基苯基丙烯酸酯,且cac-2的纯度高于80%。
[0056]
本实施例还提供了一种上述荧光探针在检测环境或食品中半胱氨酸的应用。
[0057]
实施例3:
[0058]
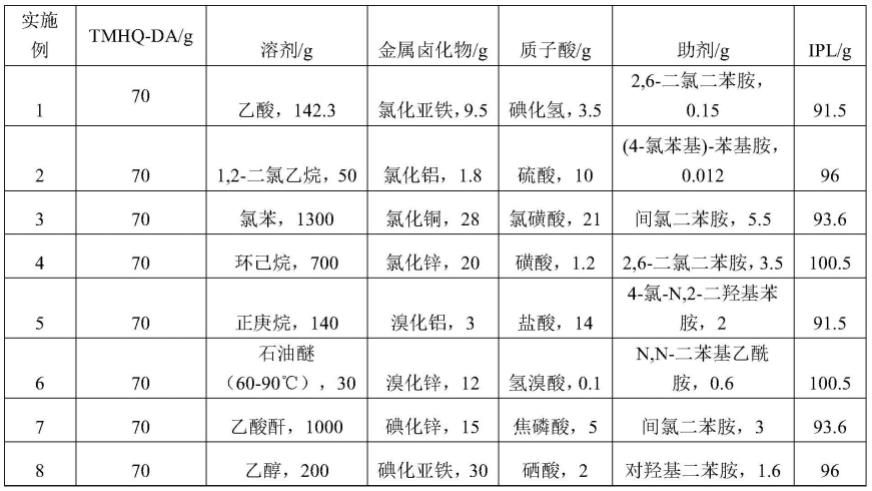
本实施例提供了一种利用荧光探针检测半胱氨酸的方法,具体步骤为:通过na2hpo4、kh2po4、kcl和nacl配制pbs磷酸盐缓冲溶液,并由稀naoh和/或稀hci调节酸碱度得到不同ph的pbs溶液,将半胱氨酸溶解在pbs溶液中并配制成0.010m的待测液。分别称取实施例1中制备得到的探针cac-1和实施例2制备得到的cac-2,用二甲基亚砜dmso溶液配制成0.010m的探针溶液,cac-1在ph=5~10的溶液中表现出良好的ph适应性,cac-2在ph=6~11的溶液中表现出良好的ph适应性。探针cac-1和cac-2能单独使用,也能混合使用。测样时,在比色皿中加入2.0ml pbs溶液与dmso的混合溶液(dmso:pbs=4:6,ph=7.4),再向其中加入2.0μl探针溶液,配成10μm的探针体系,利用紫外可见吸收光谱仪和荧光光谱仪检测探针体系的荧光性质。
[0059]
按照上述检测方法,向探针体系中分别加入200μm(20eq)的cys、hcy和gsh,待响应
完全后分别进行光谱扫描,检测结果如图2-5所示。
[0060]
由图2(a)可知,只有加入cys的紫外吸收光谱发生明显变化,其375nm处的吸收峰消失并在407nm处产生新的紫外吸收峰,且溶液颜色由无色变为淡粉色,可实现裸眼识别;然而加入hcy和gsh并不能使吸收峰发生明显变化。由图2(b)的荧光光谱可知,空白探针cac-1的最大发射峰位于525nm处,加入cys后探针的荧光强度明显降低且伴随15nm的红移;而hcy和gsh加入后探针的荧光强度无明显变化,且cys加入后体系的荧光由黄绿色变为浅粉色。上述结果表明探针cac-1可以实现裸眼特异性识别cys。
[0061]
由图3(a)可知,空白探针cac-2溶液(dmso:pbs=4:6,10μm,ph=7.4)在350-470nm区域内有紫外吸收,且最大吸收峰在377nm处,只有在加入cys时探针cac-2的吸收光谱有明显变化,在377nm处的吸收峰消失并在407nm处产生了新的吸收峰,且溶液裸眼颜色由无色变为粉色;而加入hcy和gsh后吸收峰强度小幅度降低但并没有新的吸收峰生成。由图3(b)可知,探针cac-2的最大发射峰位于512nm,加入cys后,原发射峰消失并在540nm处出现了新的发射峰,且荧光颜色由绿色变为黄色;但加入hcy和gsh后发射峰并没有明显变化。上述结果表明探针cac-2可以实现裸眼特异性识别cys。
[0062]
由图4(a)荧光光谱可知,cac-1加入cys后,探针体系的荧光强度逐渐减弱且红移了15nm,最终趋于平稳。根据图4(b)时间与荧光强度的变化关系曲线可知,待测物cys加入后荧光强度立刻发生了明显且强烈的变化,1min内荧光强度衰减到50%,2min时已衰减到90%,3min时已基本响应完全,上述结果表明,探针cac-1与cys的反应迅速且响应时间短。
[0063]
由图5(a)荧光光谱可知,cac-2加入cys后,探针体系在512nm处的发射峰强度逐渐减弱,在540nm处生成新的发射峰并逐渐增强,最终趋于稳定。根据图5(b)为i
540
/i
512
与时间的变化曲线可知,随着时间增加,纵坐标i
540
/i
512
比值逐渐增大,表明在512nm处的发射峰值逐渐减小,540nm处的发射峰值逐渐增大。4min开始曲线趋于稳定,表明探针响应完全。上述结果表明,探针cac-2对cys的响应迅速且响应方式呈比率型。
[0064]
按照上述检测方法,对不同浓度的进行检测,检测结果如图6-7所示。
[0065]
由图6(a)探针cac-1对不同浓度cys的滴定荧光光谱图可知,随着加入cys浓度的增加(0~50eq),探针在525nm处的荧光强度逐渐降低。将525nm处的荧光强度与cys浓度绘制成相关曲线,如图6(b)所示,在0~100μm范围内荧光强度与cys含量有良好的线性关系,线性方程为:f=-6.29
×
[cys] 1062.01,相关系数r2=0.9933。对空白探针溶液进行检测得到标准差,再根据检测限公式lod=3σ/k得到检测限为14.19μm。
[0066]
由图7(a)探针cac-2对不同浓度cys的滴定荧光光谱图可知,随着加入cys浓度的增加,探针在512nm处的发射峰强度逐渐降低,在540nm处生成新的发射峰且强度逐渐增大。由图7(b)探针cac-2在540nm与512nm处的发射峰强度比值i
540
/i
512
与cys浓度的线性关系图可知,在0-100μm范围内探针荧光强度与cys含量有良好的线性关系,线性方程为:f=0.00597
×
[cys] 0.654相关系数r2=0.9942。对空白探针溶液进行检测得到标准差,再根据检测限公式lod=3σ/k得到检测限为27.02mm。
[0067]
按照上述检测方法,对不同氨基酸进行检测,检测结果如图8-11所示。
[0068]
由图8(a)探针cac-1的选择性实验荧光光谱图可知,加入其他氨基酸并不会引起探针cac-1荧光强度的显著降低,只有加入cys时探针体系溶液谱图会发生明显变化,在525nm处的发射峰强度明显降低且向长波长方向移动15nm。由图8(b)可知,探针cac-1只对
cys进行选择性识别,说明本发明提供的探针cac-1对cys具有良好的选择性。
[0069]
分别在含有其他干扰氨基酸的cac-1探针体系中加入cys(20eq)并进行检测,检测结果如图9所示。如图9所示,加入cys后,所有体系的荧光强度都有明显降低,说明其他氨基酸并不会影响探针cac-1对cys的识别,探针cac-1对cys的识别具有良好的抗干扰性。
[0070]
由图10(a)可知,只有干扰氨基酸存在时,探针在512nm处的最大发射波长没有变化,只是不同氨基酸的发射峰强度随浓度变化有所改变,并不能证明发生了相应的响应。相反,在探针溶液中加入cys时最大发射峰波长会有明显28nm的红移,这与其他氨基酸有明显的区分之处。如图10(b)所示,探针溶液中只加入其他氨基酸时,i
540
/i
512
值没有明显变化,在加入cys后i
540
/i
512
比值显著增大,这说明在其他氨基酸并不会与探针cac-2响应并产生红移,因此可知探针cac-2对cys具有高度选择性。
[0071]
分别在含有其他干扰氨基酸的cac-2探针体系中加入cys(20eq)并进行检测,检测结果如图11所示。如图11所示,加入cys后,所有体系i
540
/i
512
比值明显增大,说明其他氨基酸存在时并不会影响探针cac-2对cys的识别,即探针cac-2对cys的识别具有良好的抗干扰性。
[0072]
综上所述,本发明提供的探针cac-1和cac-2是以姜黄素衍生物为荧光母体、丙烯酰酯为检测基团的荧光探针,能够裸眼识别半胱氨酸,对半胱氨酸响应迅速,检测时间短,检测限低,具备高灵敏性。且本发明提供的探针cac-1和cac-2在快速识别半胱氨酸时,对其他离子没有响应,具备高选择性和良好的抗干扰能力和ph适应性。
[0073]
以上公开的本发明优选实施例只是用于帮助阐述本发明。优选实施例并没有详尽叙述所有的细节,也不限制该发明仅为所述的具体实施方式。显然,根据本说明书的内容,可作很多的修改和变化。本说明书选取并具体描述这些实施例,是为了更好地解释本发明的原理和实际应用,从而使所属技术领域技术人员能很好地理解和利用本发明。本发明仅受权利要求书及其全部范围和等效物的限制。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。