1.本发明属于无机化学和材料化学科学领域,特别是一种金属有机框架化合物、制备方法及其在吸附分离中的应用。
背景技术:
2.乙炔在石油、化工、能源等领域具有举足轻重的作用,既是一种重要的燃料,也是制备橡胶、纤维等化工品的重要原料。乙炔主要来源于石油的热解过程,以及甲烷的不完全燃烧,因此乙炔中往往含有不同量的甲烷和二氧化碳等杂质气体。乙炔的纯化对于乙炔在工业中的高效使用具有重要的经济意义和价值。
3.金属有机框架化合物,简称为mof,是一种由金属中心和有机配体通过相互连接而形成的具有周期性网络结构的多孔材料。相比于传统的多孔碳、沸石等材料,mof的特点在于结构的可设计性、孔尺寸的可调控性,以及孔表面的可修饰性,因此mof在催化、储存、分离、药物传输等众多领域,具有非常重要的应用前景。
4.在mof的合成过程中,采用由多个金属离子与氧(o)中心连接形成多核单元的方法,已被广泛地证实是构筑mof最有效的策略之一。同时,由此制备的mof在乙炔的吸附分离方面表现出特殊的功能。然而由多个金属离子与氟(f)中心形成的多核单元在mof中却极为少见。通过比较o原子和f原子可以发现,与o原子相比,具有更大电负性的f原子能够与乙炔形成更强的氢键作用,将更加有利于乙炔的吸附。因此,合成基于金属离子与f中心形成的多核单元的mof并应用于乙炔的吸附分离,对于新型mof材料的开发和应用具有重要的意义。
技术实现要素:
5.针对现有技术存在的上述不足,本发明的目的在于提供一种金属有机框架化合物、制备方法及其在吸附分离中的应用。
6.为实现以上目的,本发明一方面涉及一种金属有机框架化合物,所述金属有机框架化合物化学式为[(ch3)2nh2]
0.5
·
[zn(bdc)
0.5
f
1.5
]
·
dmf
·
h2o,式中bdc为脱质子的对苯二甲酸,dmf为n,n
‑
二甲基甲酰胺,(ch3)2nh2为二甲胺阳离子,所述金属有机框架化合物具有三维框架结构,含有一维四方形孔道,孔隙率为43.1%,兰格缪尔比表面积为632.1m2g
‑1,孔体积为0.40cm3g
‑1。
[0007]
进一步地,所述一维四方形孔道,孔尺寸为
[0008]
进一步地,所述金属有机框架化合物属于四方晶系i4/mmm空间群,晶胞参数为:α=90
°
,β=90
°
,γ=90
°
,
[0009]
本发明另一方面涉及所述金属有机框架化合物的合成方法,包括以下步骤:
[0010]
1)将七水合硫酸锌和对苯二甲酸加入到n,n
‑
二甲基甲酰胺
‑
甲醇
‑
氢氟酸混合溶
剂中;
[0011]
2)将步骤1)得到的混合液置于反应釜中,密闭加热到115~120℃并保持70~80小时,得到中间产物;
[0012]
3)以4~6℃/小时的速度将反应釜中的温度冷却到室温,得到无色块状晶体,为锌金属有机框架化合物;
[0013]
4)将步骤3)获得的锌金属有机框架化合物在二氯甲烷中交换65~75小时,然后在真空、150℃下活化3~5小时,得到金属有机框架化合物。
[0014]
优选的,所述七水合硫酸锌与对苯二甲酸的摩尔比为1:1。
[0015]
优选的,所述n,n
‑
二甲基甲酰胺:甲醇:氢氟酸体积比为7:3:0.05。
[0016]
优选的,所述混合溶剂用量为七水合硫酸锌质量的300~320倍。
[0017]
本发明还涉及所述金属有机框架化合物在乙炔吸附分离中的应用。
[0018]
进一步地,所述金属有机框架化合物在乙炔
‑
甲烷混合物以及乙炔
‑
二氧化碳混合物吸附分离中的应用。
[0019]
进一步地,在298k温度下,所述金属有机框架化合物对乙炔、甲烷和二氧化碳的吸附量分别为79.5、8.5和23.6cm3g
‑1。
[0020]
与现有技术相比,本发明具有以下有益效果:
[0021]
(1)本发明所述金属有机框架化合物是含有一维孔道的三维框架,孔径分布均匀、孔尺寸适中,且孔表面含有f原子;
[0022]
(2)本发明所述金属有机框架化合物的合成方法为溶剂热法,步骤简单、易操作、设备要求低;所述的原料易得,金属盐为七水合硫酸锌,配体为对苯二甲酸;所述的溶剂为n,n
‑
二甲基甲酰胺和甲醇混合溶剂,尤其是在溶剂中加入了少量的氢氟酸,作为必不可少的f
‑
离子来源;
[0023]
(3)本发明所述金属有机框架化合物能够应用于乙炔吸附分离,特别是对乙炔
‑
甲烷混合物以及乙炔
‑
二氧化碳混合物表现出优异的分离效果,在石油、化工等领域乙炔的分离纯化方面具有重要的应用价值。
附图说明
[0024]
通过阅读参照以下附图对非限制性实施例所作的详细描述,本发明的其它特征、目的和优点将会变得更明显:
[0025]
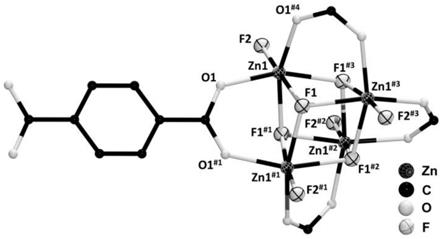
图1为本发明金属有机框架化合物中的zn
2
离子的配位环境以及[zn4(μ3‑
f)4]四核中心单元。
[0026]
图2为本发明金属有机框架材料中的一维链结构。
[0027]
图3为本发明金属有机框架材料中的三维框架结构。
[0028]
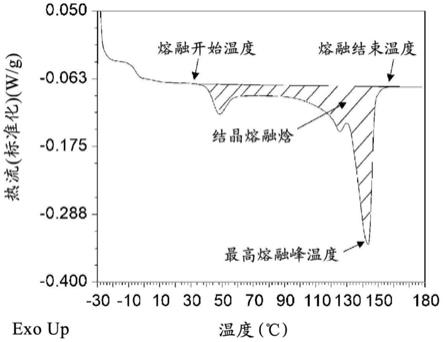
图4为本发明金属有机框架材料在195k下的二氧化碳吸附等温线。
[0029]
图5为本发明金属有机框架材料在298k下的乙炔、甲烷和二氧化碳吸附等温线。
[0030]
图6为通过理想吸附溶液理论计算的所述金属有机框架材料在298k下的乙炔/甲烷吸附选择性曲线。
[0031]
图7为通过理想吸附溶液理论计算的所述金属有机框架材料在298k下的乙炔/二氧化碳吸附选择性曲线。
具体实施方式
[0032]
下面结合具体实施例对本发明进行详细说明。以下实施例将有助于本领域的技术人员进一步理解本发明,但不以任何形式限制本发明。应当指出的是,对本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进。这些都属于本发明的保护范围。
[0033]
一种金属有机框架化合物,所述金属有机框架化合物化学式为[(ch3)2nh2]
0.5
·
[zn(bdc)
0.5
f
1.5
]
·
dmf
·
h2o,式中bdc为脱质子的对苯二甲酸,dmf为n,n
‑
二甲基甲酰胺,(ch3)2nh2为二甲胺阳离子,其中bdc的结构式如下:
[0034][0035]
所述金属有机框架化合物具有三维框架结构,含有一维四方形孔道,孔隙率为43.1%,兰格缪尔比表面积为632.1m2g
‑1,孔体积为0.40cm3g
‑1;孔尺寸约为孔道的表面主要含有苯环以及f原子等。
[0036]
所述金属有机框架化合物属于四方晶系i4/mmm空间群,晶胞参数为:α=90
°
,β=90
°
,γ=90
°
,
[0037]
所述金属有机框架化合物的一个不对称单元含有0.5个zn
2
离子、0.25个bdc有机配体、0.5个配位的f
‑
阴离子,以及0.25个me2nh
2
阳离子。每个zn
2
离子采用六配位的八面体配位构型,其中的六个配位原子中,两个来自于两个bdc配体的羧酸o原子,另外四个则来自于f
‑
离子,形成了o2f4配位环境;所述金属有机框架化合物中含有分别具有二桥联和三桥联模式的f
‑
离子,并且四个zn
2
离子与四个三桥联f
‑
离子相互连接形成具有立方烷结构的[zn4(μ3‑
f)4]四核中心单元,如图1所示。该四核单元进一步通过二桥联f
‑
离子的连接,形成一维链结构,如图2所示。一维链通过bdc配体的连接形成含有一维孔道的三维框架结构化合物,如图3所示。
[0038]
所述金属有机框架化合物采用溶剂热合成方法,以七水合硫酸锌和对苯二甲酸为原料,包括以下步骤:
[0039]
1)将七水合硫酸锌(0.029g,0.10mmol),对苯二甲酸(0.017g,0.10mmol)以摩尔比1:1加入到n,n
‑
二甲基甲酰胺(7ml)
‑
甲醇(3ml)
‑
氢氟酸(1滴,约为0.05ml)混合溶剂中。
[0040]
2)将步骤(1)得到的混合液置于25ml的反应釜中,密闭加热到115~120℃并保持70~80小时,得到中间产物。
[0041]
3)以4~6℃/小时的速度将反应釜中的温度冷却到室温,得到无色块状晶体,即为所述锌金属有机框架化合物。
[0042]
4)将步骤(3)获得的锌金属有机框架化合物在二氯甲烷中交换65~75小时,然后在真空以及150℃下活化4小时,得到用于乙炔
‑
甲烷、乙炔
‑
二氧化碳吸附分离的金属有机框架化合物。
[0043]
所述金属有机框架化合物能够应用于乙炔吸附分离,特别是在等组分的乙炔
‑
甲烷混合物以及乙炔
‑
二氧化碳混合物吸附分离中的应用。
[0044]
利用asap2020m物理比表面积测定仪测定所述金属有机框架化合物在195k温度下对二氧化碳的吸附等温线,如图4所示,从中可计算出化合物的兰格缪尔比表面积为632.1m2g
‑1,孔体积为0.40cm3g
‑1。同时使用该仪器测定所述金属有机框架化合物在298k温度下分别对乙炔、甲烷和二氧化碳的吸附等温线,如图5所示。从图5中的结果可以发现,在298k和100kpa压力下,所述金属有机框架化合物对乙炔、甲烷和二氧化碳的吸附量分别为79.5、8.5和23.6cmg
‑1,即对乙炔的吸附远高于对甲烷和二氧化碳的吸附,吸附量比值达到乙炔/甲烷=9.4,乙炔/二氧化碳=3.4,表现出明显的乙炔吸附分离功能。化合物对乙炔的吸附选择性主要来源于化合物孔道表面含有裸露的f原子,它们能够与乙炔形成强的氢键作用。
[0045]
根据298k温度下测试的气体吸附等温线,利用理想吸附溶液理论分别计算所述金属有机框架化合物在不同压力下对混合气体的分离选择性。如图6所示,对于等组分的乙炔
‑
甲烷混合物,在1~100kpa压力下范围内,乙炔/甲烷选择性数值约为10~13。如图7所示,对于等组分的乙炔
‑
二氧化碳混合物,在1~100kpa压力下范围内,乙炔/二氧化碳选择性数值约为4。
[0046]
以上对本发明的具体实施例进行了描述。需要理解的是,本发明并不局限于上述特定实施方式,本领域技术人员可以在权利要求的范围内做出各种变形或修改,这并不影响本发明的实质内容。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。