1.本发明属于荧光分析和生物小分子的检测领域,特别涉及一种基于亚硫酸氢根离子的比率型荧光探针及其合成和应用。
背景技术:
2.亚硫酸氢盐在病理和生理上发挥着重要作用,当生物体中亚硫酸氢根离子浓度过高时则会引起哮喘、荨麻疹、癌症等疾病。因此,检测生物体中的亚硫酸氢根离子的浓度具有重要的意义。
3.传统的“off-on”荧光探针在应用上容易受探针浓度、仪器效率、外界环境等因素影响,相比之下,比率型荧光探针在应用时能够有效的消除上诉因素的影响,因而具备准确度高的优点,进而实现更精准的分析。因此,设计和合成一种快速、灵敏、高选择性的比率型荧光探针,对于改进现有的荧光检测方法是很有意义的。
技术实现要素:
4.为了克服上述现有技术的缺点与不足,本发明的首要目的在于提供一种基于亚硫酸氢根离子的比率型荧光探针。
5.本发明另一目的在于提供上述基于亚硫酸氢根离子的比率型荧光探针的合成方法。
6.本发明再一目的在于提供上述基于亚硫酸氢根离子的比率型荧光探针的应用。
7.本发明的目的通过下述方案实现:
8.一种基于亚硫酸氢根离子的比率型荧光探针,其结构如下所示:
[0009][0010]
一种上述的基于亚硫酸氢根离子的比率型荧光探针的合成方法,包括以下步骤:
[0011]
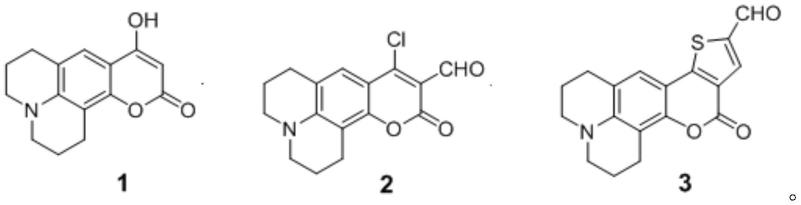
(1)在氮气或惰性气氛保护下,将化合物1和三氯氧磷在溶剂中反应,得到化合物2;
[0012]
(2)将化合物2和1,4-二硫-2,5-二醇在碱和溶剂存在条件下反应,得到化合物3;
[0013]
(3)将化合物3和2-氰基乙酸乙酯在溶剂以及有机碱四氢吡咯存在条件下反应,即得到基于亚硫酸氢根离子的比率型荧光探针。
[0014]
步骤(1)-(3)中所述的化合物1、化合物2以及化合物3的结构如下所示:
[0015][0016]
步骤(1)中所述的溶剂为n,n-二甲基甲酰胺(dmf)。
[0017]
步骤(1)中所述的化合物1和三氯氧磷的摩尔比为1:1~1:10,优选为1:1.8;
[0018]
步骤(1)中所述的反应是指先在室温下搅拌0.1-2h后再升温至30-80℃反应1~24h;优选为在室温下搅拌0.5h后再升温至60℃反应10h;
[0019]
步骤(1)中为了充分反应,优选为先将三氯氧磷加入到溶剂中搅拌均匀形成悬浮液,同时将化合物1也溶于溶剂中形成化合物1的溶液,再将化合物1的溶液加入到三氯氧磷的悬浮液中进行反应;化合物1的溶液加入方式更优选为滴加加入。
[0020]
步骤(1)中反应结束后还包括一个纯化步骤,具体如下:将所得反应液倒入冰水中,加碱调节其ph值至中性,待有黄色沉淀析出后,过滤,用水清洗干燥后,再用乙醇重结晶所得白色固体即为纯化后的化合物2;
[0021]
步骤(2)中所述的碱为碳酸钾、碳酸钠中的至少一种,优选为碳酸钾;
[0022]
步骤(2)中所述的溶剂为丙酮、四氢呋喃、乙醇中的至少一种,优选为丙酮;
[0023]
步骤(2)中所述的化合物2和1,4-二硫-2,5-二醇的摩尔比为1:0.1~1:1,优选为1:0.6;步骤(2)中所述的化合物2和碱的摩尔比为1:1~1:10,优选为1:3。
[0024]
步骤(2)中所述的反应是指在20-45℃搅拌0.1-10h后再回流反应1-10h,优选为在45℃搅拌反应1h后再65℃回流3h;
[0025]
步骤(2)中反应结束后还包括一个纯化步骤,具体步骤如下:将所得反应液在冰箱(0℃)中冷却,待黄色固体析出后,过滤收集黄色沉淀物并用冰乙醇洗涤,再用硅胶柱提纯即得纯化后的化合物3。
[0026]
化合物3的合成步骤如下所示:
[0027][0028]
步骤(3)中所述的溶剂为二氯甲烷、三氯甲烷、四氯化碳、四氢呋喃中的至少一种,优选为二氯甲烷。
[0029]
步骤(3)中所述的化合物3和2-氰基乙酸乙酯的摩尔比为1:1~1:10,优选为1:2;步骤(3)中所述的四氢吡咯与化合物3的摩尔比为0.1:1~10:1;
[0030]
步骤(3)中所述的反应是指在室温下搅拌过夜;步骤(3)中反应完毕后还包括一个纯化步骤,具体步骤如下:将所得反应液浓缩得到粗产物,由二氯甲烷/乙醇(1/6)重结晶,过滤,再用冷乙醇洗涤,得到探针ncs。
[0031]
步骤(3)中的反应路线如下所示:
[0032][0033]
本发明所述的荧光探针分子ncs在亚硫酸氢根离子的检测中的应用,尤其是在细胞环境中亚硫酸氢根离子的检测中的应用。当激发波长分别为410nm和540nm时,荧光发射波长在494nm和715nm的荧光光强比(i
494
/i
715
)与亚硫酸氢根离子的浓度呈线性正相关(激发波长为410nm时,发射波长为494nm时的荧光发射波长i
494
;激发波长为540nm时,发射波长为715nm时的荧光发射波长i
715
)。
[0034]
本发明相对于现有技术,具有如下的优点及有益效果:
[0035]
本发明所述的荧光探针分子ncs对亚硫酸氢根离子具有很好的响应能力,且在荧光波长为494nm和715nm处的荧光强度呈现比率型变化,并且本发明所述的荧光探针分子ncs还可应用于细胞环境中的亚硫酸氢根离子的快速检测和细胞成像。
附图说明
[0036]
图1为比率型荧光探针分子ncs溶液在加入亚硫酸氢根离子前后的颜色外观变化;其中(a)为在日照光下;(b)为在紫外灯下。
[0037]
图2为荧光探针分子ncs中逐渐滴加亚硫酸氢根离子(0~90μmol)后的荧光发射光谱图。
[0038]
图3为荧光探针分子ncs的荧光发射波长在494nm和715nm的荧光强度比值(i
494nm
/i
715nm
)与亚硫酸氢根离子(0~60μmol)的线性关系图。
[0039]
图4为荧光探针分子ncs对于常见检测对象的荧光强度比值(i494nm/i715nm)变化图,其中,1-15分别指空白、氟离子(f-)、碘离子(i-)、碳酸根(co
32-)、磷酸根离子(po
4-)、醋酸根离子(no
2-)亚硝酸根离子(no
2-)、硝酸根离子(no
3-)、硫酸根离子(so
42-)、过氧化氢(h2o2)、水合肼(n2h4)、半胱氨酸(cys)、同型半胱氨酸(hcy)、谷胱甘肽(gsh)、亚硫酸氢根离子(hso
4-)。
[0040]
图5为荧光探针分子ncs在活细胞中亚硫酸氢根离子检测时的生物成像图。
具体实施方式
[0041]
下面结合实施例和附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
[0042]
实施例中的比率型探针ncs的合成路线如下所示:
[0043][0044]
实施例1:化合物2的合成
[0045]
在氮气的保护下,将三氯氧磷(1.1ml)缓慢地滴加到干燥的dmf(2.5ml)中,室温下搅拌30分钟,得到粉红色悬浮液。然后将化合物1(1.03g,4mmol)的n,n-二甲基甲酰胺(dmf)溶液(5ml)缓慢地滴加到上述悬浮液中,在室温下搅拌0.5h,接着在60℃下搅拌10h,并冷却至室温。再将混合液倒入冰水中,用氢氧化钠将溶液的ph调节至中性。此时有黄色沉淀析出,过滤,用水清洗和干燥,继而用无水乙醇重结晶得到白色固体。
[0046]1h nmr(400mhz,cdcl3)δ10.31(s,1h),7.48(s,1h),3.43~3.38(m,4h),2.93~2.88(m,2h),2.83(t,j=6.0hz,2h),2.09~1.96(m,4h).
[0047]
实施例2:化合物3合成
[0048]
将碳酸钾(1.21g,9.0mmol)和1,4-二硫-2,5-二醇(276mg,1.80mmol)添加到化合物2(912mg,3.0mmol)的丙酮(120ml)溶液中。然后将混合物在45℃搅拌1h,65℃下回流3h,随后在冰箱(0℃)中冷却。待大量黄色固体析出,过滤收集黄色沉淀物,并用冰乙醇(10ml
×
4次)洗涤。接着用短硅胶柱(二氯甲烷)提纯化合物3,得到黄色固体(542mg,产率56%)。
[0049]1h nmr(400mhz,cdcl3)δ9.92(s,1h),8.18(s,1h),7.14(s,1h),3.36~3.30(m,4h),2.94(t,j=6.4hz,2h),2.83(t,j=6.0hz,2h),2.06~1.98(m,4h).
[0050]
13
c nmr(125mhz,cdcl3)δ182.37,157.75,156.49,149.79,146.76,139.14,136.82,121,58,120.70,119.24,106.96,104.50,50.05,49.62,27.54,21.27,20.61,20.43.
[0051]
ms-apci(c
18h16
o3ns):calcd.for[m h]
326.1;found:325.9.
[0052]
实施例3:荧光探针分子ncs的制备
[0053]
向化合物3(100mg,0.31mmol)的无水二氯甲烷溶液中(20ml)添加2-氰基乙酸乙酯(70mg,0.62mmol)。在加入一滴四氢吡咯后,将反应混合物在室温下搅拌过夜。然后将混合物浓缩得到粗产物,再由二氯甲烷/乙醇(1/6)重结晶。过滤,用冷乙醇洗涤,得到探针ncs,并在真空下干燥以得到红色固体(120mg,92%产率)。
[0054]1h nmr(400mhz,cdcl3)δ8.32(s,1h),8.03(s,1h),7.19(s,1h),4.40(q,j=7.2hz,2h),3.38~3.30(m,4h),2.94(t,j=6.4hz,2h),2.82(t,j=6.0hz,2h),2.08~1.97(m,4h),1.42(t,j=7.2hz,3h).
[0055]
13
c nmr(125mhz,cdcl3)δ162.73,157.40,156.24,149.91,146.97,146.29,139.13,131.62,121.87,120.32,119.49,116.00,106.96,104.43,98.35,62.60,50.14,
49.69,27.45,21.25,20.59,20.41,14.24.
[0056]
ms-esi(c
23h20
o4n2s):calcd.for[m]-420.1;found:420.0.
[0057]
实施例4:荧光探针对亚硫酸氢根离子的检测
[0058]
pbs缓冲溶液的配制:称取716.3mg十二水合磷酸氢二钠、78.0mg二水合磷酸二氢钠于250ml容量瓶中,用蒸馏水定容,摇匀,静置片刻,取1.0ml用ph计测量其ph=7.40;密封冷冻保存待用。
[0059]
荧光探针测试溶液的配制:用n,n-二甲基甲酰胺(dmf)溶解探针固体,得到浓度为1mmol/l的探针母液。测试时取3ml的pbs缓冲溶液与乙腈体积比为3:2的混合溶液,加入30μl的探针母液,得到比率型荧光探针分子ncs溶液,再向其中加入不同体积的亚硫酸氢钠溶液,从而获得了含有不同浓度的亚硫酸氢钠(nahso3)的探针分子ncs测试溶液。比率型荧光探针分子ncs溶液在加入亚硫酸氢根离子前后的颜色外观变化如图1所示,其中(a)为在日照光下;(b)为在紫外灯下。比率型荧光探针分子ncs溶液中随着加入的亚硫酸氢根离子浓度的变化其荧光发射光谱图如图2所示,从图1和图2中可以看出,本发明所述的荧光探针分子ncs对亚硫酸氢根离子具有很好的响应能力。
[0060]
荧光探针分子ncs的荧光发射波长在494nm和715nm的荧光强度比值(i
494nm
/i
715nm
)与亚硫酸氢根离子(0~60μmol)的线性关系图如图3所示,从图3可以看出,本发明所述的荧光探针分子ncs的荧光波长为494nm和715nm处的荧光强度比值与亚硫酸氢根离子具有较好的线性关系,因此可以用于亚硫酸氢根离子的检测。
[0061]
实施例5:荧光探针对亚硫酸氢根离子的选择性实验
[0062]
选择性测试是决定荧光探针性能的一项重要测试。因此在本发明中研究了探针ncs对其他常见的阴离子(如氟离子(f-)、碘离子(i-)、碳酸根(co
32-)、磷酸根离子(po
4-)、醋酸根离子(no
2-)亚硝酸根离子(no
2-)、硝酸根离子(no
3-)、硫酸根离子(so
42-)等)、分子(如过氧化氢(h2o2)、水合肼(n2h4)、半胱氨酸(cys)、同型半胱氨酸(hcy)、谷胱甘肽(gsh)等)的响应情况;即向比率型荧光探针分子ncs溶液中分别加入等浓度(终浓度为70μm)的氟离子(f-)、碘离子(i-)、碳酸根(co
32-)、磷酸根离子(po
4-)、醋酸根离子(no
2-)亚硝酸根离子(no
2-)、硝酸根离子(no
3-)、硫酸根离子(so
42-)、过氧化氢(h2o2)、水合肼(n2h4)、半胱氨酸(cys)、同型半胱氨酸(hcy)、谷胱甘肽(gsh)中的一种,然后与加入等浓度的亚硫酸氢根离子的进行对比,荧光探针分子ncs对于常见检测对象的荧光强度比值(i494nm/i715nm)变化如图4所示,在图4中可知,探针ncs对亚硫酸氢根离子有很强的响应,而其他分子或者离子基本无法引起任何荧光变化。这一结果表面,荧光探针分子ncs对亚硫酸氢钠具有很好的选择性。
[0063]
实施例6:荧光探针ncs在活细胞中检测亚硫酸氢根离子的应用
[0064]
在荧光成像实验前,将hela细胞种植在14mm玻璃盖玻片上,贴壁24h。然后用探针ncs(细胞液中的探针浓度为10μmol/l)在37℃下孵育30分钟,并用pbs缓冲液洗涤(3次);再以405或者565nm半导体激光器为激发光源,在640-740nm处(红色信号通道)与460-525nm处(蓝色信号通道)收集两块的荧光信号。荧光探针分子ncs在活细胞中亚硫酸氢根离子检测时的生物成像图如图5所示。
[0065]
由图5可以得知,用探针ncs在37℃下孵育hela细胞30min,可以观察到很强的红色荧光,说明探针ncs对细胞有很好的渗透性。随后,往细胞培养液中加入亚硫酸氢钠并孵育
0.5h后,我们可以观察到,随着亚硫酸氢钠浓度的增加,细胞内的红色荧光强度开始减弱,而蓝色荧光的强度逐渐地增强。上述的实验结果表明,本发明所述的荧光探针分子ncs对细胞内的亚硫酸氢根离子具有很好的检测能力,在生物测试方面上具有很好的应用价值。
[0066]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
