1.本发明涉及生物技术领域。具体地,本发明涉及一种人乳头瘤病毒嵌合蛋白,及由其形成的五聚体或病毒样颗粒,以及所述人乳头瘤病毒嵌合蛋白、其五聚体或病毒病毒样颗粒在制备预防受试者中乳头瘤病毒感染及感染诱发的疾病的疫苗中的用途。
背景技术:
2.人乳头瘤病毒(human papillomavirus,hpv)是一类感染上皮组织的无包膜小dna病毒,目前已鉴定200余型,其中40余型主要感染肛周、泌尿生殖器及口咽部的粘膜及附近皮肤;根据感染诱发病变性质不同,分为诱发恶性肿瘤的致癌型(hpv16/-18/-31/-33/-45/-52/-58等)和诱发疣状增生的低危型(hpv 6/-11等)。分子流行病学研究发现,致癌型hpv持续感染可诱发约100%的宫颈癌、88%的肛门癌、70%的阴道癌、50%的阴茎癌、43%的阴户癌及72%的头颈癌。目前已鉴定20余型,在宫颈癌组织中常见的12种型别,如hpv16/-18/-31/-33/-35/-39/-45/-51/-52/-56/-58/-59,又称为高危型(high-risk hpv,hr-hpv)。hr-hpv累计诱发95.2%~96.5%的宫颈癌;其余致癌性hpv相对少见,除hpv68以外,单型检出率小于0.5%。hpv16和hpv18在世界范围内宫颈癌中的检出率最高,分别为55.4%及14.6%。hpv31是世界范围内相对常见的hr-hpv,在宫颈癌组织中的检出率为3.5%,位列第六位;在宫颈高度癌前病变组织中的检出率为10.4%,位列第三位,仅次于hpv16(45.1%)及hpv52(11%);在细胞学正常的宫颈组织中的检出率为1.3%,位列第三位,仅次于hpv16(2.9%)及hpv58(1.5%)。值得注意的是,在某些发达地区宫颈高度癌前病变中,hpv31的检出率高达12.4%,仅次于hpv16(46.8%);另外在拉丁美洲细胞学正常宫颈组织中hpv31的检出率仅次于hpv16(3.3%),为1.2%。
3.hpv l1蛋白的c端含有核定位信号,l1蛋白在真核细胞表达后,经核定位信号的介导入核,在细胞核内组装成病毒样颗粒。研究发现,通过删除法去除核定位信号,可使l1蛋白翻译后分布在胞浆。因此,在不影响参与vlp组装的l1蛋白c端helix 5结构域的基础上,去除核定位信号,获得的l1 c端截短基因,在真核表达体系(如昆虫细胞)表达后,l1 vlp主要分布在胞浆,利于细胞的破碎及下游纯化。利用昆虫细胞表达体系研究发现,牛乳头瘤病毒1型(bpv1)l1截短c端24个氨基酸的突变体、hpv16 l1的c端截短23个氨基酸的突变体、hpv58 l1的c端截短25个氨基酸的突变体,均不影响l1蛋白组装成vlp的活性,且bpv1 l1截短蛋白突变体的组装效率提高了3倍,hpv58 l1截短蛋白的表达量提高了2倍。其他型别的截短突变体对表达水平、组装活性及产量的影响尚未见有报道。现有报道的采用大肠杆菌表达体系进行l1 vlp表达的l1基因的c端均为天然完整序列。
4.根据l1氨基酸序列的差异,每种hpv型别的l1存在许多不同的型内变异株。现有报道的数据显示,hpv16l1的变异株在昆虫细胞及酵母细胞中的表达水平存在差异。有报道分析了5株16l1变异株在昆虫细胞内l1 vlp的表达水平,发现其中2株变异株(phil1和fra63)的l1表达水平及vlp的产量显著高于原型l1对照组(phil1和fra63的表达水平较原型分别提高了32倍和16倍,产量分别提高了39倍和42倍),另一变异株(alg1)的表达水平较原型提
高了8倍,产量提高了24倍,其余2株的表达水平和产量与原型的相当。采用酵母表达体系对2株16l1变异株(b27和t3)的vlp表达水平进行分析,发现2株变异株的vlp产量均显著高于原型对照组。氨基酸分析发现,上述7株16l1变异株的氨基酸一级序列均不相同,酵母种表达水平较高的2个变异株及昆虫细胞中表达水平较高的3个变异株,虽然其共同特征是202位和266位的氨基酸相同(分别是asp和ala),但与其有相同特征的fra25的表达水平及vlp产量很低(与对照组相当),表明不同变异株中的特征性构成氨基酸可能影响l1的表达水平,这是无法预测的。上述数据表明,通过对不同变异株的表达水平分析,可以发现vlp表达量提高的变异株序列,用于l1 vlp疫苗的生产,可望降低疫苗的生产成本。目前尚未见有其他型别变异株序列对表达水平的影响的报道。
5.采用大肠杆菌表达体系对c端完整的hpv 16l1的表达研究显示,n端分别截短4、6、8、9、10个氨基酸,不影响l1 vlp的组装(x.chen et al,journal of molecular biology,2001)。采用大肠杆菌表达体系对合计9种型别l1的n端截短突变体的表达水平与其相应型别n端全长l1表达水平进行比较分析,包括2种16l1的n端截短突变体(
△
n5、
△
n10),其表达水平均较对照组的显著提高;2种18l1n端截短突变体(
△
n5、
△
n10),其中
△
n5的表达水平显著提高,
△
n10的显著降低;2种31l1n端截短突变体(
△
n5、
△
n10),其表达水平均与对照组相当;3种33l1n端截短突变体(
△
n5、
△
n10、
△
n15),其中
△
n10的表达水平显著提高,其余2种的表达水平降低;2种45l1n端截短突变体(
△
n4、
△
n9),其表达水平均降低;4种58l1n端截短突变体(
△
n5、
△
n10、
△
n15、
△
n19),其中
△
n15的表达水平显著提高,其余3种与对照组相当;3种52l1n端截短突变体(
△
n5、
△
n10、
△
n15),其表达水平均显著提高;3种6l1n端截短突变体(
△
n3、
△
n6、
△
n9),其中
△
n6的表达水平显著提高,
△
n9表达水平不变,
△
n3表达水平降低;2种11 1n端截短突变体(
△
n5、
△
n9),其中
△
n5的表达水平显著提高,
△
n9的表达水平不变(m.wei et al,emerging microbes&infections,2018)。上述数据显示,l1的n端截短突变体可影响蛋白在大肠杆菌中的表达水平,n端截短的长度对表达水平的影响是没有规律的、不可预测的。目前尚未见有n端截短突变体在昆虫细胞中表达水平的研究。另外,目前也未见有利用c端截短l1突变体进行n端截短,研究n端截短策略对截短蛋白在真核表达体系中表达水平的影响。
6.l1 vlp是由72个l1五聚体(360个l1单体)组装成的直径为55nm的正二十面体。l1依赖的中和抗体表位按一定间隔在其表面规律性密集排列,每种表位重复360次,因此l1vlp利于bcr的交联及高滴度中和抗体的产生。动物实验及临床研究数据显示,hpv l1vlp可诱发产生高滴度的持久性的l1特异的中和抗体,三种上市的vlp疫苗在全球100多个国家和地区应用后,未见型内变异株逃逸的现象,表明vlp诱发的是针对多个l1表位的。
7.另外,vlp还可以作为表位肽疫苗的载体,以hpv16 l1为载体,构建的表面展示16rg-1、58rg-1、33rg-1及31rg-1的hpv16 cvlp疫苗相对成功,可同时诱发不同型别rg-1依赖的交叉中和抗体及hpv16l1依赖的型别特异性中和抗体,其中hpv16的中和抗体滴度与16l1vlp的相当,各型rg-1依赖的交叉中和抗体滴度相对较高,中和范围涵盖的型别较多(大于10种),其他文献也报道了一些hpv16 cvlp疫苗的研究数据,嵌合的表位包括16rg-1及16l2其他的表位区,但由于插入位点、插入策略及选择表位的长度不同,其获得的16cvlp诱发的交叉中和活性相对较差。用16cvlp替换cervarix(hpv16/18l1vlp)中的16vlp,配制16cvlp/18vlp混合疫苗,初步研究显示,疫苗不仅可同时诱发高滴度的hpv16/18的中和抗
体,同时还可诱发针对hpv58的交叉保护活性。提示,采用hpv cvlp疫苗进行新一代的预防性疫苗的研发,可望扩大疫苗保护范围的同时降低疫苗的成本。gsk公司在其二价苗cervarix成功的基础上,又进行了hpv16 cvlp及hpv18 cvlp疫苗的研究,但数据显示其嵌合33rg-1的16cvlp的表达量较低,交叉中和范围也不理想;其嵌合33rg-1的18cvlp疫苗交叉中和范围虽然仅涵盖7种型别(4种高危型、2种低危型、1种皮肤型),交叉中和抗体滴度除hpv58的中和滴度较高之外,其余6种型别的中和滴度均相对较低,但其免疫活性显著优于目前huber等报道的嵌合45rg-1的18cvlp(b.huber et al,plos one,2017;m.boxus et al,journal of virology,2016)。上述数据提示,16cvlp已相对成功,18cvlp的实验研究处于初级阶段,尚需进一步优化插入表位、插入位点,以期进一步提高其免疫保护活性涵盖的范围;其他型别的cvlp疫苗尚未见有报道。
8.依据目前报道的hpv16/18cvlp疫苗的研究数据可以看出,cvlp疫苗的研究面临许多挑战。首先是需要选择免疫原性强的嵌合l2保守表位,包括rg-1表位及l2蛋白中其他保守表位。目前rg-1表位的选择是经验性的,常选择优势流行株型别的rg-1表位,而不是免疫原性强的rg-1表位,主要原因是目前缺乏不同型别rg-1表位免疫原性比较的数据。其次,rg-1表位肽的长度,即表位核心序列的旁侧序列对表位在嵌合蛋白表面的正确展示具有影响。第三,表位肽的插入位点和插入方式的不同对嵌合蛋白的组装及活性影响很大,插入位点的不同包括在l1的不同表面区的插入位点、同一表面区不同位置的插入位点;插入方式的不同包括直接插入、置换插入、插入位点区骨架氨基酸是否存在修饰(包括是否增加连接子)。第四,hpv31 l1 vlp载体对嵌合表位的耐受性及其免疫活性的影响除了存在上述所列的3种情况之外,还存在许多其他挑战,主要是由于hpv31 l1 vlp的结构特点及主要中和抗体表位区均不清楚,目前成功的hpv16和18cvlp的插入位点均是de loop,鉴于hpv31 l1 vlp合适的展示外源表位的位点不清楚,如果插入位点选择不当,将会影响hpv31 l1vlp骨架的免疫原性,其31cvlp诱发产生的hpv31中和抗体滴度较hpv31 l1 vlp的显著降低,即使获得了嵌合表位依赖的广谱中和抗体,其在不同型别cvlp混合疫苗的配制中也失去了对hpv31的免疫保护优势。
9.因而,目前需要开发新型别的hpv cvlp,首先要求其表达量高、具有研发优势,另外还需要同时诱发高滴度的针对载体型别的中和抗体,同时诱发的交叉中和抗体的活性较强,其中型别特异性的l1依赖的中和抗体滴度最好与其相应型别l1 vlp诱发的相当,这样在不同型别cvlp混合疫苗的研究中,才可保持针对骨架型别的保护优势;交叉中和活性涵盖的型别多、滴度较高,而且其优势交叉中和型别与目前报道的其他型别的cvlp相比具有特点。
技术实现要素:
10.有鉴于此,本发明的目的在于提供一种乳头瘤病毒嵌合蛋白,用于制备预防受试者中乳头瘤病毒感染及感染诱发的疾病的疫苗。
11.本发明人出人意料地发现,对hpv31 l1蛋白骨架进行适当的截短、点突变和/或c端氨基酸改造,可不同程度的提高其表达水平,且不影响其组装成vlp的活性;在全长或截短型hpv31型l1蛋白或其突变体的表面区插入hpv73型l2蛋白多肽,可提高hpv73型l2蛋白多肽的免疫原性,获得的嵌合蛋白在大肠杆菌或昆虫细胞表达系统中可高水平表达,该嵌
合蛋白可组装成vlp,并可诱发针对来自不同属/亚属的多种型别hpv的广谱保护性免疫反应。
12.因而,在第一方面,本发明提供了一种人乳头瘤病毒嵌合蛋白,其包含hpv31型l1蛋白或hpv31型l1蛋白的突变体、以及插入所述hpv31型l1蛋白或hpv31型l1蛋白的突变体中的来自hpv73型l2蛋白的多肽,或由其组成,其中所述hpv31型l1蛋白如seq id no.1所示,所述hpv73型l2蛋白如seq id no.2所示。
13.在本发明的人乳头瘤病毒嵌合蛋白的优选的实施方案中,所述的hpv31型l1蛋白来自但不限于ncbi数据库中的p17388.1、aei61021.1、aei60949.1、aaa92894.1、aig59245.1、aig59235.1等来自hpv31原型或变异株的l1蛋白。优选地,所述的hpv31型l1蛋白的氨基酸序列如seq id no.1所示。
14.在本发明的人乳头瘤病毒嵌合蛋白的进一步优选的实施方案中,本发明所述的hpv31型l1蛋白的突变体与seq id no.1所示的hpv31型l1蛋白相比,包含:
15.选自以下的任何一种或多种置换突变:
16.t274n、r475g、r483g、r496 g、k477s、k497s、k501s、k479a、k482a、k498a、k495g、k500 g和r473g;和/或
17.n端截短2、4、5、8或10个氨基酸的截短突变;和/或
18.c端截短29个氨基酸的截短突变。
19.在本文所使用的置换突变的表示中,中间的数字代表与对照序列相比(例如,seq id no.1所示的氨基酸序列)的氨基酸位置,数字前面的字母代表突变前的氨基酸残基,数字后的字母代表突变后的氨基酸残基。
20.在进一步优选的实施方案中,所述的hpv31型l1蛋白的突变体选自:
21.将seq id no.1所示的氨基酸序列第274位苏氨酸(t)替换为天冬酰胺(n),其序列如seq id no.3所示;
22.将seq id no.1所示的氨基酸序列第274位苏氨酸(t)替换为天冬酰胺(n),并将氨基酸序列的n端截短4个氨基酸,其序列如seq id no.4所示;
23.将seq id no.1所示的氨基酸序列的c端截短29个氨基酸的突变体,其序列如seq id no.5所示;
24.将seq id no.1所示的氨基酸序列第274位苏氨酸(t)替换为天冬酰胺(n),并将氨基酸序列的c端截短29个氨基酸的突变体,其序列如seq id no.6所示;
25.将seq id no.1所示的氨基酸序列第274位苏氨酸(t)替换为天冬酰胺(n),将氨基酸序列的c端截短29个氨基酸的突变体,并将氨基酸序列的n端截短2个氨基酸的突变体,其序列如seq id no.7所示;
26.将seq id no.1所示的氨基酸序列第274位苏氨酸(t)替换为天冬酰胺(n),将氨基酸序列的c端截短29个氨基酸的突变体,并将氨基酸序列的n端截短4个氨基酸的突变体,其序列如seq id no.8所示;
27.将seq id no.1所示的氨基酸序列第274位苏氨酸(t)替换为天冬酰胺(n),将氨基酸序列的c端截短29个氨基酸的突变体,并将氨基酸序列的n端截短5个氨基酸的突变体,其序列如seq id no.9所示;
28.将seq id no.1所示的氨基酸序列第274位苏氨酸(t)替换为天冬酰胺(n),并将氨
基酸序列的c端截短29个氨基酸的突变体,并将氨基酸序列的n端截短8个氨基酸的突变体,其序列如seq id no.10所示;
29.将seq id no.1所示的氨基酸序列第274位苏氨酸(t)替换为天冬酰胺(n),将氨基酸序列的c端截短29个氨基酸的突变体,并将氨基酸序列的n端截短10个氨基酸的突变体,其序列如seq id no.11所示;
30.将seq id no.1所示的氨基酸序列第274位苏氨酸(t)替换为天冬酰胺(n),将氨基酸序列的n端截短4个氨基酸,并将氨基酸序列的第475位、第483位及496位的精氨酸(r)替换为甘氨酸(g),第477位、第497位及第501位的赖氨酸(k)替换为丝氨酸(s),第479位、第482位及第498位赖氨酸(k)替换为丙氨酸(a),第495位及第500位赖氨酸(k)替换为甘氨酸(g)的突变体,其序列如seq id no.12所示;
31.将seq id no.1所示的氨基酸序列第274位苏氨酸(t)替换为天冬酰胺(n),将氨基酸序列的n端截短4个氨基酸,并将氨基酸序列的第473位、第475位、第483位及496位的精氨酸(r)替换为甘氨酸(g),第477位、第497位及第501位的赖氨酸(k)替换为丝氨酸(s),第479位、第482位及第498位赖氨酸(k)替换为丙氨酸(a),第495位及第500位赖氨酸(k)替换为甘氨酸(g)的突变体,其序列如seq id no.13所示;
32.将seq id no.1所示的氨基酸序列第274位苏氨酸(t)替换为天冬酰胺(n),将氨基酸序列的n端截短4个氨基酸,并将氨基酸序列的第475位、第483位及496位的精氨酸(r)替换为甘氨酸(g),第477位、第497位及第501位的赖氨酸(k)替换为丝氨酸(s),第482位及第498位赖氨酸(k)替换为丙氨酸(a),第495位及第500位赖氨酸(k)替换为甘氨酸(g)的突变体,其序列如seq id no.14所示。
33.在本发明的人乳头瘤病毒嵌合蛋白的进一步优选的实施方案中,所述的来自hpv73型l2蛋白的多肽为seq id no.2所示氨基酸aa.1-50区域内的任意连续的8-33个氨基酸的片段;优选地,所述的多肽为seq id no.2所示的hpv73型l2蛋白rg-1表位肽或其突变体表位肽;更优选地,所述的多肽为seq id no.2所示的氨基酸17至39的多肽,或seq id no.2所示的氨基酸17至39的多肽的n端延长或截短1至6个氨基酸和/或c端延长或截短1至6个氨基酸的突变体。
34.优选地,所述的来自hpv73型l2蛋白的多肽如seq id no.15、seq id no.16或seq id no.17所示。
35.可选地,所述的来自hpv73型l2蛋白的多肽还可以是与seq id no.15、seq id no.16或seq id no.17所示的氨基酸序列具有大于60%、优选大于70%、大于80%、大于90%,甚至更优选大于95%的序列同一性的多肽。
36.可选地,所述的来自hpv73型l2蛋白的多肽插入所述的hpv31型l1蛋白或所述hpv31型l1蛋白的突变体的表面区,优选插入所述的hpv31型l1蛋白或所述hpv31型l1蛋白的突变体的de环或h4区域,更优选为通过直接插入的方式插入所述的hpv31型l1蛋白或所述hpv31型l1蛋白的突变体的氨基酸132和氨基酸133之间、或氨基酸134和135之间、或氨基酸136和137之间、或氨基酸137和138之间、或氨基酸432和433之间、或氨基酸434和435之间、或氨基酸435和436之间;或者通过非等长置换的方式插入所述的hpv31型l1蛋白或所述hpv31型l1蛋白的突变体的氨基酸132至136区域、或氨基酸135至139区域、或氨基酸428-431区域、或氨基酸431-434区域。
37.如本文所用,术语“直接插入”是指在相邻两个氨基酸之间插入所选择的肽片段。例如,在seq id no.1的氨基酸132和氨基酸133之间的直接插入指的是将所选择的肽片段直接插入到seq id no.1的氨基酸132和氨基酸133之间。
38.如本文所用,术语“非等长置换”指的是在删除指定氨基酸区间的序列后,将所选的肽片段插入到指定的氨基酸区间。例如,在seq id no.1的氨基酸132至136区域的非等长置换指的是,删除seq id no.1的氨基酸133-135之后,将所选择的肽片段插入到seq id no.1的氨基酸氨基酸132至136之间。
39.可选地,在所述直接插入或非等长置换的方式中,所述来自hpv73型l2蛋白的多肽在其n端和/或c端包含1至3个氨基酸残基长的连接子。
40.可选地,所述的连接子由选自甘氨酸(g)、丝氨酸(s)、丙氨酸(a)及脯氨酸(p)的氨基酸任意组合构成。优选地,n端的连接子由g(甘氨酸)p(脯氨酸)组成,c端的连接子由p(脯氨酸)组成。
41.可选地,在所述直接插入的方式中,所述来自hpv73型l2蛋白的多肽的氨基酸序列是seq id no.15、seq id no.16或seq id no.17,插入位点为所述n端完整的hpv31型l1蛋白及所述突变体的氨基酸137和氨基酸138之间或氨基酸432和433之间。
42.可选地,在所述直接插入的方式中,所述来自hpv73型l2蛋白的多肽的氨基酸序列是seq id no.15、seq id no.16或seq id no.17,插入位点为所述n端截短4个氨基酸的hpv31型l1蛋白及所述突变体的氨基酸134和氨基酸135之间或氨基酸429和430之间。
43.可选地,在所述直接插入的方式中,所述来自hpv73型l2蛋白的多肽的氨基酸序列是n端含有gp连接子和/或c端含有p连接子的seq id no.15、seq id no.16或seq id no.17所示序列,插入位点为所述n端完整的hpv31型l1蛋白及所述突变体的氨基酸137和氨基酸138之间或氨基酸432和433之间。
44.可选地,在所述直接插入的方式中,所述来自hpv73型l2蛋白的多肽的氨基酸序列是n端含有gp连接子和/或c端含有p连接子的seq id no.15、seq id no.16或seq id no.17所示序列,插入位点为n端截短4个氨基酸的hpv31型l1蛋白及所述突变体的氨基酸134和氨基酸135之间或氨基酸429和430之间。
45.可选地,在所述非等长置换的方式中,删除n端完整的hpv31型l1蛋白及所述突变体的氨基酸136-138区域后,在所述n端完整的hpv31型l1蛋白及所述突变体的氨基酸135及139之间插入来自hpv73型l2蛋白的多肽,所述来自hpv73型l2蛋白的多肽其n端增加了甘氨酸-脯氨酸连接子,所述来自hpv73型l2蛋白的多肽的氨基酸序列如seq id no.15、seq id no.16或seq id no.17所示。
46.可选地,在所述非等长置换的方式中,删除n端截短4个氨基酸的hpv31型l1蛋白及所述突变体的氨基酸133-135区域后,在所述n端截短4个氨基酸的hpv31型l1蛋白及所述突变体的氨基酸132及136之间插入来自hpv73型l2蛋白的多肽,所述来自hpv73型l2蛋白的多肽其n端增加了甘氨酸-脯氨酸连接子,所述来自hpv73型l2蛋白的多肽的氨基酸序列如seq id no.15、seq id no.16或seq id no.17所示。
47.可选地,在所述非等长置换的方式中,删除n端完整的hpv31型l1蛋白及所述突变体的氨基酸432-433区域后,在所述n端完整的hpv31型l1蛋白及所述突变体的氨基酸431及434之间插入来自hpv73型l2蛋白的多肽,所述来自hpv73型l2蛋白的多肽的氨基酸序列如
seq id no.15、seq id no.16或seq id no.17所示。
48.可选地,在所述非等长置换的方式中,删除n端截短4个氨基酸的hpv31型l1蛋白及所述突变体的氨基酸429-430区域后,在所述n端截短4个氨基酸的hpv31型l1蛋白及所述突变体的氨基酸428及431之间插入来自hpv73型l2蛋白的多肽,所述来自hpv73型l2蛋白的多肽的氨基酸序列如seq id no.15、seq id no.16或seq id no.17所示。
49.优选地,在所述非等长置换的方式中,删除所述hpv31型l1蛋白突变体的氨基酸133-135区域后,在所述hpv31型l1蛋白突变体的氨基酸132及136之间插入来自hpv73型l2蛋白的多肽,所述来自hpv73型l2蛋白的多肽其n端增加了甘氨酸-脯氨酸连接子,所述来自hpv73型l2蛋白的多肽的氨基酸序列如seq id no.15或seq id no.17所示,获得的嵌合蛋白氨基酸序列如seq id no.18、seq id no.19、seq id no.20、seq id no.21、seq id no.22、seq id no.23、seq id no.24或seq id no.25所示。
50.优选地,在所述非等长置换的方式中,删除所述hpv31型l1蛋白突变体的氨基酸429-430区域后,在所述hpv31型l1蛋白突变体的氨基酸428及431之间插入来自hpv73型l2蛋白的多肽,所述来自hpv73型l2蛋白的多肽的氨基酸序列如seq id no.16或seq id no.17所示,获得的嵌合蛋白氨基酸序列如seq id no.26、seq id no.27、seq id no.28、seq id no.29、seq id no.30、seq id no.31、seq id no.32或seq id no.33所示。
51.本发明的另一方面涉及编码上述的人乳头瘤病毒嵌合蛋白的多核苷酸。
52.本发明还提供了包含上述的多核苷酸的载体,以及包含所述的载体的细胞。
53.本发明涉及的编码上述的人乳头瘤病毒嵌合蛋白的多核苷酸序列适用于不同的表达系统。可选地,这些核苷酸序列采用大肠杆菌密码子进行全基因优化,可在大肠杆菌表达系统中高水平表达;或采用昆虫细胞密码子进行全基因优化,可在昆虫细胞表达系统中高水平表达。
54.本发明还提供了一种多聚物,优选地,所述多聚物为人乳头瘤病毒嵌合五聚体或嵌合病毒样颗粒,其中所述多聚物包含本发明所述的人乳头瘤病毒嵌合蛋白,或者由本发明所述的人乳头瘤病毒嵌合蛋白所形成。
55.本发明还提供了上述的乳头瘤病毒嵌合蛋白、乳头瘤病毒嵌合五聚体或上述的乳头瘤病毒嵌合病毒样颗粒在制备预防乳头瘤病毒感染和/或所述乳头瘤病毒感染诱发的疾病的疫苗中的用途,优选地,所述乳头瘤病毒感染诱发的疾病包括但不限于宫颈癌、阴道癌、阴唇癌、阴茎癌、肛门肛周癌、口咽癌、扁桃体癌及口腔癌;
56.优选地,所述乳头瘤病毒感染为一种或多种选自以下人乳头瘤病毒型别的感染:hpv16、hpv18、hpv26、hpv31、hpv33、hpv35、hpv39、hpv45、hpv51、hpv52、hpv53、hpv56、hpv58、hpv59、hpv66、hpv68、hpv70、hpv73;hpv6、hpv11、hpv2、hpv5、hpv27和hpv57。
57.本发明还提供了一种用于预防乳头瘤病毒感染及感染诱发的疾病的疫苗,其包含上述的乳头瘤病毒嵌合五聚体或嵌合病毒样颗粒、佐剂、以及疫苗用赋形剂或载体,优选地,还包含至少一种嗜黏膜组和/或嗜皮肤组的hpv的病毒样颗粒或嵌合病毒样颗粒。其中,这些病毒样颗粒的含量分别为能诱发保护性免疫反应的有效量。
58.可选地,所述佐剂为人用佐剂。
59.发明中相关术语的说明及解释
60.根据本发明,术语“昆虫细胞表达系统”包括昆虫细胞、重组杆状病毒、重组bacmid
及表达载体。其中昆虫细胞来源于市场上可得到的细胞,在此举例但不限于:sf9,sf21,high five。
61.根据本发明,术语“原核表达系统”包括但不限于大肠杆菌表达系统。其中表达宿主菌来源于市场上可得到的菌株,在此举例但不限于:bl21(de3),bl21(de3)plyss,c43(de3),rosetta-gami b(de3)。
62.根据本发明,术语“全长hpv31型l1蛋白”的例子包括但不限于ncbi数据库中编号为p17388.1、aei61021.1、aei60949.1、aaa92894.1、aig59245.1、aig59235.1的蛋白等长的全长l1蛋白。
[0063]“截短型hpv31型l1蛋白”的基因片段指的是其与野生型hpv31型l1蛋白基因相比,在其5’端和/或3’端缺失编码1个或多个氨基酸的核苷酸,其中“野生型hpv31型l1蛋白”的全长序列例如但不限于ncbi数据库中的如下序列:p17388.1、aei61021.1、aei60949.1、aaa92894.1、aig59245.1、aig59235.1等。
[0064]
根据本发明,术语“疫苗用赋形剂或载体”是指选自一种或多种,包括但不限于:ph调节剂,表面活性剂,离子强度增强剂。例如,ph调节剂举例但不限于磷酸盐缓冲液,表面活性剂包括阳离子、阴离子或非离子型表面活性剂,举例但不限于聚山梨酯80(tween-80),离子强度增强剂举例但不限于氯化钠。
[0065]
根据本发明,术语“人用佐剂”是指在临床上可应用于人体的佐剂,包括当前已获得批准的和将来可能获得批准的各种佐剂,例如但不限于铝佐剂、mf59及各种形式的佐剂组合物。
[0066]
根据本发明,本发明的疫苗可采用患者可接受的形式,包括但不限于口服或者注射,优选注射。
[0067]
根据本发明,本发明疫苗优选单位剂型使用,其中单位剂型中蛋白病毒样颗粒的剂量为5μg-100μg,例如5、10、15、20、25、30、35、40、45、50、55、60、65、70、75、80、85、90、95、100μg、以及上述任意两个数值之间的范围;优选30μg-60μg。
附图说明
[0068]
图1a-图1b:本发明实施例7中31型l1蛋白突变体及包含其的嵌合蛋白在昆虫细胞中的表达鉴定。结果显示,11种31型l1蛋白及突变体、16种嵌合蛋白均可在昆虫细胞中表达。
[0069]
图1a:31型l1蛋白及其突变体蛋白在昆虫细胞中的表达鉴定:1为31l1;2为t
274
n;3为31l1mδc;4为t
274
nδc;5为t
267
aδc;6为t
267
at
274
nδc;7为t
274
nδn2c;8为t
274
nδn4c;9为t
274
nδn5c;10为t
274
nδn8c;11为t
274
nδn10c;
[0070]
图1b:包含31型l1蛋白突变体的嵌合蛋白在昆虫细胞中的表达鉴定:1为31l1de
132-136
/de;2为31l1de
132-136
/des;3为31l1h4
428-431
/de;4为31l1h4
428-431
/des;5为31l1de
132-136
/de-cs1;6为31l1de
132-136
/des-cs1;7为31l1h4
428-431
/de-cs1;8为31l1h4
428-431
/des-cs1,9为31l1de
132-136
/de-cs2;10为31l1de
132-136
/des-cs2;11为31l1h4
428-431
/de-cs2;12为31l1h4
428-431
/des-cs2;13为31l1de
132-136
/de-cs3;14为31l1de
132-136
/des-cs3;15为31l1h4
428-431
/de-cs3;16为31l1h4
428-431
/des-cs3。
[0071]
图2a-图2f:本发明实施例8中纯化后获得的vlp及cvlp的动态光散射分析结果。结
果显示31l1mδc、t
274
nδc、t
274
nδn4c、31l1de
132-136
/de、31l1h4
428-431
/de及31l1h4
428-431
/de-cs1重组蛋白形成的病毒样颗粒水化动力学直径分别为103.3nm、99.78nm、106.8nm、104.59nm、47.8nm及42.4nm,颗粒组装的百分比均为100%。
[0072]
图2a:31l1mδc;图2b:t
274
nδc;图2c:t
274
nδn4c;图2d:31l1de
132-136
/de;图2e:31l1h4
428-431
/de;图2f:31l1h4
428-431
/de-cs1。
[0073]
图3a-图3e:本发明实施例8中纯化后获得的vlp及cvlp的透射电镜观察结果。视野中可见大量的病毒样颗粒。bar=50nm。
[0074]
图3a:31l1mδc;图3b:t
274
nδn4c;图3c:31l1de
132-136
/de;图3d:31l1h4
428-431
/de;图3e:31l1h4
428-431
/de-cs1。
[0075]
图4:本发明实施例11所述的小鼠免疫血清采用hpv31假病毒进行中和抗体滴度检测结果。ns:无统计学差异(p》0.05)。
具体实施方式
[0076]
下面将通过下述非限制性实施例进一步说明本发明,本领域技术人员公知,在不背离本发明精神的情况下,可以对本发明做出许多修改,这样的修改也落入本发明的范围。下面的实施例仅用于说明本发明,而不应视为限定本发明的范围,因为实施方案必然是多样的。本说明书中使用的用语仅是为了阐述特定的实施方案,而非作为限制,本发明的范围已界定在所附的权利要求中。
[0077]
除非特别说明,本说明书中所使用的所有技术和科学用语均和本案所属技术领域的技术人员所普遍明了的意义相同。下面就本发明的优选方法和材料加以叙述,但是与本说明书中所述方法和材料类似或等效的任何方法和材料均可用以实施或测试本发明。下述实验方法如无特别说明,均为常规方法或产品说明书所描述的方法,所使用的实验材料如无特别说明,均可容易地从商业公司获取。本说明书中所提到的所有公开文献均被并入于此作为参考,以揭示并说明所述公开文献中的方法和/或材料。
[0078]
实施例1:hpv31变异株的l1序列分析
[0079]
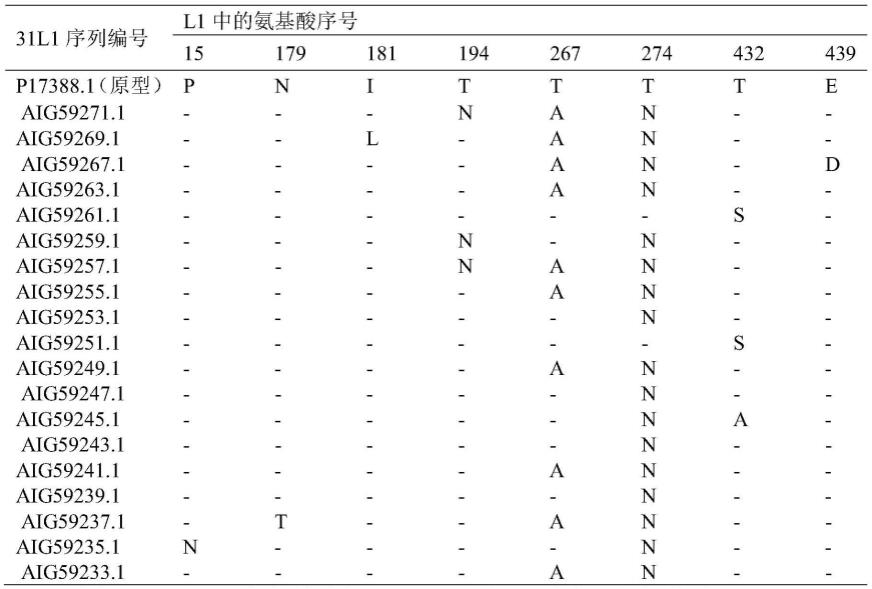
在ncbi genbank中输入“major capsid protein l1[human papillomavirus type31]”或“late protein l1[human papillomavirus type 31]”关键词,获得19例自然界中存在的hpv31 l1变异株,利用dnaman软件进行氨基酸序列比对(表1),发现l1的第15、179、181、194、267、274、432、439位氨基酸发生了变异,其中第267位(突变频率53%)和第274位(突变频率89%)为高频变异位点,其他位点氨基酸突变频率在5%~15%之间。对于第267位和第274位氨基酸而言,第267位由苏氨酸(t)突变为丙氨酸(a)的占53%,第274位由苏氨酸(t)突变为天冬酰胺(n)的占89%,因此a和t分别是第267位和第274位的优势氨基酸。
[0080]
表1.不同hpv31 l1变异株的氨基酸序列比对
[0081][0082]
*以连字号(-)表示的氨基酸与hpv31l1原型对应位置的氨基酸相同。
[0083]
实施例2:不同型别rg-1表位肽的免疫活性检测
[0084]
采用化学合成法合成hpv35、-39、-51、-53、-56、-68、-73、-82的rg-1表位肽,表位肽序列如表1所示,多肽由上海吉尔生化有限公司合成,为了提高合成肽的免疫原性,各合成肽通过1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc,cas no.25952-53-8)活化羧基后与钥孔血蓝蛋白(klh)偶联。
[0085]
取2.0-2.5kg体重的新西兰大白兔,随机分组,每组2-4只,于免疫前4天背部多点皮下注射15mg灭活的与等体积弗氏完全佐剂充分混匀的dh5a(含0.5%v/v甲醛的pbs,37℃处理24-48h)进行免疫刺激,首次免疫采用背部、大腿内侧多点皮下注射1mg与等体积弗氏完全佐剂充分混匀的klh-多肽。加强免疫4次,每次间隔2周,加强免疫的抗原为0.5mg与等体积弗氏不完全佐剂充分混匀的klh-多肽。最后一次免疫后2周采血,分离血清。
[0086]
使用17种hpv假病毒对免疫血清的中和抗体滴度进行检测,结果如表3所示。73rg-1表位肽的免疫活性最好,其抗血清可中和所有17种检测型别,其中hpv45,-18,-16的中和抗体的滴度均在103以上,hpv68,-57,-59,-39,-5的中和抗体滴度在500-1000之间。
[0087]
多肽合成、假病毒制备及假病毒中和实验的方法均是公开的,例如专利cn104418942a及108676057a。
[0088]
表2.合成的不同型别rg-1表位肽的序列
[0089]
型别合成肽序列seq id no.hpv35tqlyrtckaagtcppdvipkveg53hpv39stlyrtckqsgtcppdvvdkveg54hpv51tqlystckaagtcppdvvnkveg55hpv53tqlyqtckqsgtcpedvinkieh56hpv56tqlyktcklsgtcpedvvnkieq57
hpv68stlyktckqsgtcppdvinkveg58hpv73tqlyktckqagtcppdvipkveg59hpv82tqlystckaagtcppdvipkvkg60
[0090]
表3.不同的rg1-klh偶联肽在兔子中诱发的血清中和抗体滴度
[0091][0092]
实施例3:hpv31l1蛋白及其突变体的基因的合成及表达载体构建
[0093]
合计11种hpv31l1蛋白及突变体,分别为:
[0094]
1)31l1原型:其氨基酸序列如seq id no.1所示,编码31l1原型蛋白的核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建;
[0095]
2)t
274
n突变体:将seq id no.1序列的第274位苏氨酸突变为天冬酰胺,其氨基酸序列如seq id no.3所示,编码t
274
n突变体的核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建;
[0096]
3)31l1mδc突变体:将hpv31l1的c端截短29个氨基酸,其氨基酸序列如seq id no.5所示,编码31l1mδc的核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其核苷酸序列如seq id no.34所示;
[0097]
4)t
274
nδc突变体:将seq id no.5序列的第274位苏氨酸突变为天冬酰胺,其氨基
酸序列如seq id no.6所示,编码t274nδc的核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其核苷酸序列如seq id no.35所示;
[0098]
5)t
267
aδc突变体:将seq id no.5序列的第267位苏氨酸突变为丙氨酸,编码t267aδc的核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建;
[0099]
6)t
267
at
274
nδc突变体:将seq id no.6序列的第267位苏氨酸突变为丙氨酸,编码t267at
274
nδc的核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建;
[0100]
7)t
274
nδn2c突变体:将seq id no.6所示序列的n端截短2个氨基酸,其序列如seq id no.7所示,编码t
274
nδn2c的核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建;
[0101]
8)t
274
nδn4c突变体:将seq id no.6所示序列的n端截短4个氨基酸,其序列如seq id no.8所示,编码t
274
nδn4c的核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其核苷酸序列如seq id no.36所示;
[0102]
9)t
274
nδn5c突变体:将seq id no.6所示序列的n端截短5个氨基酸,其序列如seq id no.9所示,编码t
274
nδn5c的核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建;
[0103]
10)t
274
nδn8c突变体:将seq id no.6所示序列的n端截短8个氨基酸,其序列如seq id no.10所示,编码t
274
nδn8c的核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建;
[0104]
11)t
274
nδn10c突变体:将seq id no.6所示序列的n端截短10个氨基酸,其序列如seq id no.11所示,编码t
274
nδn10c的核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建。
[0105]
昆虫细胞密码子优化的hpv31l1蛋白及突变体基因经bamhi/xbai酶切后,分别插入商业化表达载体pfastbac1(invitrogen公司生产)中。得到包含嵌合蛋白基因的表达载体,分别为:pfastbac1-31l1,pfastbac1-t
274
n,pfastbac1-31l1mδc,pfastbac1-t
274
nδc,pfastbac1-t
267
aδc,pfastbac1-t
267
at
274
nδc,pfastbac1-t
274
nδn2c,pfastbac1-t
274
nδn4c,pfastbac1-t
274
nδn5c,pfastbac1-t
274
nδn8c,pfastbac1-t
274
nδn10c。上述酶切、连接及克隆构建的方法都是公知的,例如专利cn101293918b。
[0106]
实施例4:hpv31l1嵌合蛋白及其突变体的基因的合成及表达载体构建
[0107]
合计16种嵌合蛋白及突变体,分别为:
[0108]
1)嵌合l1蛋白31l1de
132-136
/de:骨架为t
274
nδn4c(即在第274位苏氨酸突变为天冬酰胺的基础上n端截短4个氨基酸,c端截短29个氨基酸,其序列如seq id no.8所示),删除其aa.133-135区域,并在aa.132/136之间融合n端包含gp连接子的hpv73型l2蛋白的aa.18-38多肽(在seq id no.8的aa.132-136区域非等长置换插入),插入片段的氨基酸序列为seq id no.15所示序列的n端添加甘氨酸-脯氨酸,31l1de
132-136
/de嵌合蛋白的氨基酸序列如seq id no.18所示。编码31l1de
132-136
/de的多核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其序列如seq id no.37所示;
[0109]
2)嵌合l1蛋白31l1de
132-136
/des:骨架为t
274
nδn4c(其序列如seq id no.8所示),删除其aa.133-135区域,并在aa.132/136之间融合n端包含gp连接子的hpv73型l2蛋白的aa.19-35多肽(在seq id no.8的aa.132-136区域非等长置换插入),插入片段的氨基酸序
列为seq id no.17所示序列的n端添加甘氨酸-脯氨酸,31l1de
132-136
/des嵌合蛋白的氨基酸序列如seq id no.19所示。编码31l1de
132-136
/des的多核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其序列如seq id no.38所示;
[0110]
3)嵌合l1蛋白31l1de
132-136
/de-cs1:骨架为t
274
nδn4c-cs1(即在第274位苏氨酸突变为天冬酰胺的基础上n端截短4个氨基酸,并对c端29个氨基酸之内的碱性氨基酸进行置换,其序列如seq id no.12所示),删除其aa.133-135区域,并在aa.132/136之间融合n端包含gp连接子的hpv73型l2蛋白的aa.18-38多肽(在seq id no.12的aa.132-136区域非等长置换插入),插入片段的氨基酸序列为seq id no.15所示序列的n端添加甘氨酸-脯氨酸,31l1de
132-136
/de-cs1嵌合蛋白的氨基酸序列如seq id no.20所示。编码31l1de
132-136
/de-cs1的多核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其序列如seq id no.39所示;
[0111]
4)嵌合l1蛋白31l1de
132-136
/des-cs1:骨架为t
274
nδn4c-cs1(其序列如seq id no.12所示),删除其aa.133-135区域,并在aa.132/136之间融合n端包含gp连接子的hpv73型l2蛋白的aa.19-35多肽(在seq id no.12的aa.132-136区域非等长置换插入),插入片段的氨基酸序列为seq id no.17所示序列的n端添加甘氨酸-脯氨酸,31l1de
132-136
/des-cs1嵌合蛋白的氨基酸序列如seq id no.21所示。编码31l1de
132-136
/des-cs1的多核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其序列如seq id no.40所示;
[0112]
5)嵌合l1蛋白31l1de
132-136
/de-cs2:骨架为t
274
nδn4c-cs2(即在第274位苏氨酸突变为天冬酰胺的基础上n端截短4个氨基酸,并对c端29个氨基酸之内的碱性氨基酸进行置换,其序列如seq id no.13所示),删除其aa.133-135区域,并在aa.132/136之间融合n端包含gp连接子的hpv73型l2蛋白的aa.18-38多肽(在seq id no.13的aa.132-136区域非等长置换插入),插入片段的氨基酸序列为seq id no.15所示序列的n端添加甘氨酸-脯氨酸,31l1de
132-136
/de-cs2嵌合蛋白的氨基酸序列如seq id no.22所示。编码31l1de
132-136
/de-cs2的多核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其序列如seq id no.41所示;
[0113]
6)嵌合l1蛋白31l1de
132-136
/des-cs2:骨架为t
274
nδn4c-cs2(其序列如seq id no.13所示),删除其aa.133-135区域,并在aa.132/136之间融合n端包含gp连接子的hpv73型l2蛋白的aa.19-35多肽(在seq id no.13的aa.132-136区域非等长置换插入),插入片段的氨基酸序列为seq id no.17所示序列的n端添加甘氨酸-脯氨酸,31l1de
132-136
/des-cs2嵌合蛋白的氨基酸序列如seq id no.23所示。编码31l1de
132-136
/des-cs2的多核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其序列如seq id no.42所示;
[0114]
7)嵌合l1蛋白31l1de
132-136
/de-cs3:骨架为t
274
nδn4c-cs3(即在第274位苏氨酸突变为天冬酰胺的基础上n端截短4个氨基酸,并对c端29个氨基酸之内的碱性氨基酸进行置换,其序列如seq id no.14所示),删除其aa.133-135区域,并在aa.132/136之间融合n端包含gp连接子的hpv73型l2蛋白的aa.18-38多肽(在seq id no.14的aa.132-136区域非等长置换插入),插入片段的氨基酸序列为seq id no.15所示序列的n端添加甘氨酸-脯氨酸,31l1de
132-136
/de-cs3嵌合蛋白的氨基酸序列如seq id no.24所示。编码31l1de
132-136
/de-cs3的多核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其序列如seq id no.43所示;
[0115]
8)嵌合l1蛋白31l1de
132-136
/des-cs3:骨架为t
274
nδn4c-cs3(其序列如seq id no.14所示),删除其aa.133-135区域,并在aa.132/136之间融合n端包含gp连接子的hpv73型l2蛋白的aa.19-35多肽(在seq id no.14的aa.132-136区域非等长置换插入),插入片段的氨基酸序列为seq id no.17所示序列的n端添加甘氨酸-脯氨酸,31l1de
132-136
/des-cs3嵌合蛋白的氨基酸序列如seq id no.25所示。编码31l1de
132-136
/des-cs3的多核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其序列如seq id no.44所示;
[0116]
9)嵌合l1蛋白31l1h4
428-431
/de:骨架为t
274
nδn4c(即在第274位苏氨酸突变为天冬酰胺的基础上n端截短4个氨基酸,c端截短29个氨基酸,其序列如seq id no.8所示),删除其aa.429-430区域,并在aa.428/431之间融合hpv73型l2蛋白的aa.19-39多肽(在seq id no.8的aa.428-431区域非等长置换插入),插入片段的氨基酸序列为seq id no.16所示,31l1h4
428-431
/de嵌合蛋白的氨基酸序列如seq id no.26所示。编码31l1h4
428-431
/de的多核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其序列如seq id no.45所示;
[0117]
10)嵌合l1蛋白31l1h4
428-431
/des:骨架为t
274
nδn4c(其序列如seq id no.8所示),删除其aa.429-430区域,并在aa.428/431之间融合hpv73型l2蛋白的aa.19-35多肽(在seq id no.8的aa.428-431区域非等长置换插入),插入片段的氨基酸序列为seq id no.17所示序列,31l1h4
428-431
/des嵌合蛋白的氨基酸序列如seq id no.27所示。编码31l1h4
428-431
/des的多核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其序列如seq id no.46所示;
[0118]
11)嵌合l1蛋白31l1h4
428-431
/de-cs1:骨架为t
274
nδn4c-cs1(即在第274位苏氨酸突变为天冬酰胺的基础上n端截短4个氨基酸,并对c端29个氨基酸之内的碱性氨基酸进行置换,其序列如seq id no.12所示),删除其aa.429-430区域,并在aa.428/431之间融合hpv73型l2蛋白的aa.19-39多肽(在seq id no.12的aa.428-431区域非等长置换插入),插入片段的氨基酸序列为seq id no.16所示,31l1h4
428-431
/de-cs1嵌合蛋白的氨基酸序列如seq id no.28所示。编码31l1h4
428-431
/de-cs1的多核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其序列如seq id no.47所示;
[0119]
12)嵌合l1蛋白31l1h4
428-431
/des-cs1:骨架为t
274
nδn4c-cs1(其序列如seq id no.12所示),删除其aa.429-430区域,并在aa.428/431之间融合hpv73型l2蛋白的aa.19-35多肽(在seq id no.12的aa.428-431区域非等长置换插入),插入片段的氨基酸序列为seq id no.17所示序列,31l1h4
428-431
/des-cs1嵌合蛋白的氨基酸序列如seq id no.29所示。编码31l1h4
428-431
/des-cs1的多核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其序列如seq id no.48所示;
[0120]
13)嵌合l1蛋白31l1h4
428-431
/de-cs2:骨架为t
274
nδn4c-cs2(即在第274位苏氨酸突变为天冬酰胺的基础上n端截短4个氨基酸,并对c端29个氨基酸之内的碱性氨基酸进行置换,其序列如seq id no.13所示),删除其aa.429-430区域,并在aa.428/431之间融合hpv73型l2蛋白的aa.19-39多肽(在seq id no.13的aa.428-431区域非等长置换插入),插入片段的氨基酸序列为seq id no.16所示,31l1h4
428-431
/de-cs2嵌合蛋白的氨基酸序列如seq id no.30所示。编码31l1h4
428-431
/de-cs2的多核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其序列如seq id no.49所示;
[0121]
14)嵌合l1蛋白31l1h4
428-431
/des-cs2:骨架为t
274
nδn4c-cs2(其序列如seq id no.13所示),删除其aa.429-430区域,并在aa.428/431之间融合hpv73型l2蛋白的aa.19-35多肽(在seq id no.13的aa.428-431区域非等长置换插入),插入片段的氨基酸序列为seq id no.17所示序列,31l1h4
428-431
/des-cs2嵌合蛋白的氨基酸序列如seq id no.31所示。编码31l1h4
428-431
/des-cs2的多核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其序列如seq id no.50所示;
[0122]
15)嵌合l1蛋白31l1h4
428-431
/de-cs3:骨架为t
274
nδn4c-cs3(即在第274位苏氨酸突变为天冬酰胺的基础上n端截短4个氨基酸,并对c端29个氨基酸之内的碱性氨基酸进行置换,其序列如seq id no.14所示),删除其aa.429-430区域,并在aa.428/431之间融合hpv73型l2蛋白的aa.19-39多肽(在seq id no.13的aa.428-431区域非等长置换插入),插入片段的氨基酸序列为seq id no.16所示,31l1h4
428-431
/de-cs3嵌合蛋白的氨基酸序列如seq id no.32所示。编码31l1h4
428-431
/de-cs3的多核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其序列如seq id no.51所示;
[0123]
16)嵌合l1蛋白31l1h4
428-431
/des-cs3:骨架为t
274
nδn4c-cs3(其序列如seq id no.14所示),删除其aa.429-430区域,并在aa.428/431之间融合hpv73型l2蛋白的aa.19-35多肽(在seq id no.14的aa.428-431区域非等长置换插入),插入片段的氨基酸序列为seq id no.17所示序列,31l1h4
428-431
/des-cs3嵌合蛋白的氨基酸序列如seq id no.33所示。编码31l1h4
428-431
/des-cs3的多核苷酸序列经昆虫细胞密码子优化设计,采用全基因合成的方式构建,其序列如seq id no.52所示。
[0124]
昆虫细胞密码子优化的hpv31l1蛋白及突变体基因经bamhi/xbai酶切后,分别插入商业化表达载体pfastbac1(invitrogen公司生产)中。得到包含嵌合蛋白基因的表达载体,分别为:pfastbac1-31l1de
132-136
/de,pfastbac1-31l1de
132-136
/des,pfastbac1-31l1de
132-136
/de-cs1,pfastbac1-31l1de
132-136
/des-cs1,pfastbac1-31l1de
132-136
/de-cs2,pfastbac1-31l1de
132-136
/des-cs2,pfastbac1-31l1de
132-136
/de-cs3,pfastbac1-31l1de
132-136
/des-cs3,pfastbac1-31l1h4
428-431
/de,pfastbac1-31l1h4
428-431
/des,pfastbac1-31l1h4
428-431
/de-cs1,pfastbac1-31l1h4
428-431
/des-cs1,pfastbac1-31l1h4
428-431
/de-cs2,pfastbac1-31l1h4
428-431
/des-cs2,pfastbac1-31l1h4
428-431
/de-cs3,pfastbac1-31l1h4
428-431
/des-cs3。上述酶切、连接及克隆构建的方法都是公知的,例如专利cn101293918b。
[0125]
本发明涉及的氨基酸序列如下所述:
[0126]
[0127]
[0128]
[0129]
[0130]
[0131]
[0132]
[0133]
[0134]
[0135]
[0136]
[0137]
[0138]
[0139]
[0140]
[0141]
[0142]
[0143]
[0144]
[0145][0146]
实施例5:l1蛋白、嵌合l1蛋白基因的重组bacmid及重组杆状病毒的构建
[0147]
分别使用包含l1基因的重组表达载体pfastbac1-31l1,pfastbac1-t
274
n,pfastbac1-31l1mδc,pfastbac1-t
274
nδc,pfastbac1-t
267
aδc,pfastbac1-t
267
at
274
nδc,pfastbac1-t
274
nδn2c,pfastbac1-t
274
nδn4c,pfastbac1-t
274
nδn5c,pfastbac1-t
274
nδn8c,pfastbac1-t
274
nδn10c;或嵌合l1基因的重组表达载体pfastbac1-31l1de
132-136
/de,pfastbac1-31l1de
132-136
/des,pfastbac1-31l1de
132-136
/de-cs1,pfastbac1-31l1de
132-136
/des-cs1,pfastbac1-31l1de
132-136
/de-cs2,pfastbac1-31l1de
132-136
/des-cs2,pfastbac1-31l1de
132-136
/de-cs3,pfastbac1-31l1de
132-136
/des-cs3,pfastbac1-31l1h4
428-431
/de,pfastbac1-31l1h4
428-431
/des,pfastbac1-31l1h4
428-431
/de-cs1,pfastbac1-31l1h4
428-431
/des-cs1,pfastbac1-31l1h4
428-431
/de-cs2,pfastbac1-31l1h4
428-431
/des-cs2,pfastbac1-31l1h4
428-431
/de-cs3,pfastbac1-31l1h4
428-431
/des-cs3转化大肠杆菌dh10bac感受态,筛选获得重组bacmid,然后用重组bacmid转染昆虫细胞sf9,在sf9内扩增重组杆状病毒。重组bacmid的筛选及重组杆状病毒的扩增方法都是公知的,例如专利cn101148661b。
[0148]
实施例6:l1蛋白、嵌合l1蛋白的基因在sf9细胞中的表达
[0149]
sf9细胞分别接种11种含31l1蛋白或突变体基因的重组杆状病毒,或16种含嵌合l1基因的重组杆状病毒,进行蛋白的表达,27℃培养约88h后收发酵液,3000rpm离心15min,弃上清,用pbs洗涤细胞后,用于表达鉴定及纯化。感染表达的方法是公开的,例如专利cn 101148661 b。
[0150]
实施例7:l1蛋白、嵌合l1蛋白的表达鉴定
[0151]
取实施例6中所述表达不同l1蛋白或嵌合l1蛋白的细胞各1
×
106个,重悬于200μl pbs溶液中,加入6
×
loading buffer 50μl,75℃变性8分钟,分别取10μl进行sds-page电泳
及western blot鉴定。结果如图1a至图1b所示,11种31l1蛋白或突变体、16种嵌合l1蛋白均可在昆虫细胞中高水平表达,其中31l1、t
274
n、31l1de
132-136
/de、31l1de
132-136
/des、31l1h4
428-431
/de、31l1h4
428-431
/des蛋白大小约55kda,31l1mδc、t
274
nδc、t
267
aδc、t
267
at
274
nδc、t
274
nδn2c、t
274
nδn4c、t
274
nδn5c、t
274
nδn8c、t
274
nδn10c蛋白大小约50kd,31l1de
132-136
/de-cs1、31l1de
132-136
/des-cs1、31l1de
132-136
/de-cs2、31l1de
132-136
/des-cs2、31l1de
132-136
/des-cs3、31l1de
132-136
/des-cs3、31l1h4
428-431
/de-cs1、31l1h4
428-431
/des-cs1、31l1h4
428-431
/de-cs2、31l1h4
428-431
/des-cs2、31l1h4
428-431
/de-cs3、31l1h4
428-431
/des-cs3a大小约59kda。sds-page电泳及western blot鉴定的方法是公开的,例如专利cn101148661b。
[0152]
实施例8:l1蛋白、嵌合l1蛋白在昆虫细胞中的表达量比较
[0153]
取实施例6所述的表达不同重组蛋白的细胞各1
×
106个,重悬于200μl pbs溶液中,采用超声破碎法(宁波新芝超声破碎仪,2#探头,100w,超声5s,间隔7s,总时间3min)破碎细胞,12000rpm高速离心10分钟。收取裂解上清,采用夹心elisa法检测上清中的l1含量,该方法是公知的,例如专利cn104513826a。
[0154]
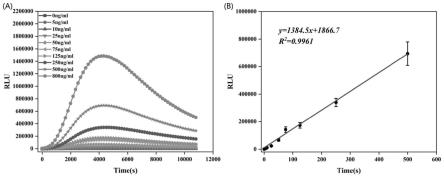
使用本发明人制备的hpv31l1单克隆抗体包被酶标板,80ng/孔,4℃孵育过夜;使用5%bsa-pbst室温封闭2h,再用pbst洗板3次。用pbs将裂解上清进行连续2倍稀释,并且将hpv31l1 vlp标准品也进行梯度稀释,浓度从2μg/ml-0.0625μg/ml,分别加入酶标板,每孔100μl,37℃孵育1h。用pbst洗板3次,加入1:3000稀释的hpv31l1兔多抗,每孔100μl,37℃孵育1h。用pbst洗板3次,加入1:3000稀释的hrp标记的山羊抗小鼠igg(1:3000稀释,中杉金桥公司),37℃孵育45分钟。用pbst洗板5次,每孔加入100μl opd底物(sigma公司),37℃显色5分钟,用50μl 2m硫酸终止反应,在490nm处测定吸光值。依据标准曲线计算裂解上清中31l1蛋白、31l1蛋白突变体或嵌合l1蛋白的浓度。
[0155]
结果如表4所示,本发明的c端截短29个氨基酸的31l1突变体蛋白(31l1mδc)的表达量显著高于hpv31l1全长蛋白;对31l1蛋白进行点突变获得的突变体蛋白的表达量也各不相同,其中t
274
n突变体的表达量显著高于hpv31l1原型蛋白,t
274
nδc突变体蛋白的表达量也较31l1mδc蛋白的进一步提高,表明第274位苏氨酸突变为天冬酰胺可提高31l1蛋白的表达量;在t
274
nδc的基础上进行不同的n端截短,发现不同的截短对表达量的影响各不相同,其中n端截短4个氨基酸(t
274
nδn4c)或n端截短8个氨基酸(t
274
nδn8c)获得的截短突变的表达量分别是t
274
nδc的2倍和1.28倍。在t
274
nδn4c的基础上构建的嵌合蛋白(31l1de
132-136
/de、31l1de
132-136
/des、31l1h4
428-431
/de、31l1h4
428-431
/des)表达量均与其骨架t
274
nδn4c的相当;此外,12种以c端置换的31l1突变体为骨架的嵌合蛋白表达量均高于相应的c端截短的嵌合蛋白。
[0156]
表4. 31l1蛋白、31l1蛋白突变体及嵌合l1蛋白表达量分析
[0157][0158][0159]
实施例9:l1蛋白、嵌合l1蛋白的纯化及动态光散射粒径分析
[0160]
取表达上述重组蛋白的细胞发酵液适量,使用10ml pbs重悬细胞,加pmsf至终浓度1mg/ml,超声破碎(宁波新芝超声破碎仪,6#探头,200w,超声5s,间隔7s,总时间10min),取破碎上清进行纯化,纯化步骤在室温进行。在裂解液中加入4%β-巯基乙醇(w/w)对vlp进行解聚,然后使用0.22μm滤器过滤样品,依次使用dmae阴离子交换层析或cm阳离子交换层析(20mm tris,180mm nacl,4%β-me,ph7.9洗脱)、tmae阴离子交换层析或q阳离子交换层析(20mm tris,180mm nacl,4%β-me,ph7.9洗脱)及羟基磷灰石层析(100mm nah2po4,30mm nacl,4%β-me,ph 6.0洗脱)纯化。纯化产物采用planova超滤系统进行浓缩,并更换缓冲液(20mm nah2po4,500mm nacl,ph6.0)促使vlp组装。以上纯化方法均是公开的,例如专利cn101293918b、cn1976718a等。
[0161]
纯化后的hpv31l1蛋白、31l1突变体蛋白及嵌合l1蛋白均可有效组装。取组装后的蛋白溶液进行dls粒径分析(zetasizer nano zs 90动态光散射仪,malvern公司),结果如表5所示,其中31l1mδc、t
274
nδc、t
274
nδn4c、31l1de
132-136
/de、31l1h4
428-431
/de、的dls分析图如图2a至图2f所示。
[0162]
表5.l1蛋白及嵌合l1蛋白的dls分析
[0163][0164][0165]
实施例10:vlp、嵌合vlp的透射电镜观察
[0166]
按实施例9所述的层析纯化方法,分别纯化重组蛋白,使用组装后嵌合制备铜网,并用1%醋酸铀进行染色,充分干燥后使用jem-1400电镜(奥林巴斯)进行观察。结果显示,昆虫细胞表达的hpv31l1、t
274
n、31l1mδc、t
274
nδc、t
267
aδc及t
267
at
274
nδc蛋白均可组装成直径约为50-60nm的vlp;n端截短联合c端截短的31l1蛋白突变体可组装成直径17-35nm的vlp;在de环表面区插入73l2多肽的嵌合蛋白可组装成30-50nm的cvlp;在h4区域插入73l2多肽的嵌合蛋白可组装成直径约为17-30nm的cvlp。其中31l1mδc、t
274
nδn4c、31l1de
132-136
/de、31l1h4
428-431
/de、31l1h4
428-431
/de-cs1的vlp或cvlp的电镜图片如图3a至图3e所示。铜网制备及电镜观察的方法均是公开的,例如专利cn101148661b。
[0167]
实施例11:hpv31l1或突变体vlp的小鼠免疫及中和抗体滴度测定
[0168]
取4-6周龄的balb/c小鼠,随机分组,每组5只,用0.1μg vlp免疫小鼠。皮下注射,于第0,2周免疫,共2次。第2次免疫后2周尾静脉采血,分离血清。
[0169]
使用hpv31假病毒对免疫血清的中和抗体滴度进行检测,结果各种31l1突变体的vlp免疫小鼠后,诱发hpv31特异性中和抗体水平均与原型相当。其中31l1mδc、t
274
nδc、
t
274
nδn4c的免疫结果如图4所示。
[0170]
实施例12:嵌合vlp的小鼠免疫及中和抗体滴度测定
[0171]
取4-6周龄的balb/c小鼠,随机分组,每组5只,用10μg cvlp联合al(oh)
3 50μg及mpl佐剂5μg免疫小鼠。皮下注射,于第0,4,7,10周免疫,共4次。第4次免疫后2周尾静脉采血,分离血清。
[0172]
使用17种hpv假病毒对抗血清的中和抗体滴度进行检测,结果显示各种cvlp免疫小鼠后,诱发的交叉中和抗体水平及中和范围各有不同。其中,在h4表面区嵌合表位的cvlp诱发的骨架型别hpv31型中和抗体滴度与hpv31l1vlp的相当,且其抗血清的交叉中和抗体滴度高、可中和17种检测型别的假病毒;在de loop表面区嵌合表位的cvlp诱发的hpv31型中和抗体滴度较31l1vlp的降低了1个数量级,其免疫血清的交叉中和谱也相对较窄。部分cvlp免疫血清的交叉中和活性如表5所示,其中31l1h4
428-431
/de、31l1h4
428-431
/des及31l1h4
428-431
/de-cs1抗血清可中和至少17个型别的假病毒,31l1de
132-136
/de及31l1de
132-136
/des抗血清分别仅中和10个及8个型别的假病毒。值得一提的是,31l1h4
428-431
/de、31l1h4
428-431
/des及31l1h4
428-431
/de-cs1抗血清对hpv16,-18及-45型的中和滴度均大于103,31l1h4
428-431
/de-cs1抗血清对hpv73型的中和抗体滴度也大于103。
[0173]
此外,本发明中采用c端置换的31l1突变体构建的cvlp,采用上述策略免疫小鼠后,诱发的交叉中和抗体水平及中和范围均与相应的c端截短的cvlp的一致。
[0174]
假病毒制备及假病毒中和实验的方法均是公开的,例如专利cn104418942a。
[0175]
表6.不同cvlp在小鼠中诱发的中和抗体滴度
[0176]
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。