一种ctni蛋白抗原决定簇多肽及其应用
技术领域
1.本发明涉及多肽化学领域,具体为一种ctni蛋白抗原决定簇多肽及其应用。
背景技术:
2.急性心肌梗死(ami)是临床常见的心血管疾病之一,被认为是心血管疾病患者死亡的主要原因。ami发病后1-3小时是溶栓和介入治疗的“黄金”窗口,这意味着早期ami的快速诊断是治疗的关键。传统的ami诊断主要依靠心绞痛症状、心电图和生物标志物检测,其中生物标志物检测非典型心肌梗死表现(即没有胸痛或没有心电图st段抬高)的患者的鉴别尤为重要。心肌肌钙蛋白i(ctni)被认为是ami早期诊断的金标准,它具有很高的心肌组织特异性和临床敏感性,甚至可以反映微小区域的心肌缺血或坏死。健康人的ctni浓度通常低于0.4 ng/ ml,而高于2.0 ng/ml的水平意味着未来发生严重心脏事件的风险增加。
3.因此,ctni的浓度测定对于心血管疾病患者的临床诊断、危险分层和预后管理有重要的临床意义与价值。常规的ctni的检测方法通常是免疫检测,即使用ctni抗体检测其水平,所以,合适的ctni蛋白抗原决定簇多肽的发现和制备也成为了ctni检测的重点。
4.随着医学检验领域的发展,临床上需要一种兼具高度特异性和抗原性的ctni蛋白抗原决定簇多肽,以适用于高度特异性抗体的制备与生产。因此,提出一种ctni蛋白抗原决定簇多肽及其应用,具有良好的应用前景和现实意义。
技术实现要素:
5.针对上述背景技术中的不足,本发明提供一种ctni蛋白抗原决定簇多肽及其应用,本发明的抗原决定簇多肽抗原性高,特异性强,可用于制备对应的ctni特异性抗原和抗体,及ctni检测试剂盒和应用。
6.为实现上述目的,本发明提供如下技术方案:第一方面,本发明提供一种ctni蛋白抗原决定簇多肽,所述抗原决定簇多肽ⅰ和ⅱ的氨基酸序列为如seq id no.1所示的序列和seq id no.2所示的序列,具体为:(1)leu-cys-arg-gln-leu-his-ala-tyr;和(2)asp-lys-val-asp-glu-glu-arg-tyr-asp-ile-tyr。
7.第二方面,本发明提供一种ctni蛋白抗原,所述的ctni蛋白抗原是通过使用如第一方面所述的抗原决定簇多肽与载体蛋白偶联制备的。
8.第三方面,本发明提供一种ctni蛋白抗体,所述的ctni蛋白抗体是有如第二方面所述抗原制备成的单克隆抗体或多克隆抗体。
9.第四方面,本发明提供一种如第三方面所述ctni蛋白抗体在制备ctni检测试剂盒中的应用。
10.第五方面,本发明提供一种ctni蛋白检测试剂盒,所述ctni检测试剂盒包含如第三方面所述抗体作为包被抗体,优选为单克隆抗体。
11.优选地,所述ctni蛋白检测试剂盒用于定量检测人血清中的ctni蛋白水平。
12.与现有技术相比,本发明具有如下有益效果:1. 本发明提供的一种ctni蛋白抗原决定簇多肽具有良好的抗原性,使用其制备的抗原免疫动物能够产生特异性抗体;2. 本发明提供的一种ctni蛋白抗原具有良好的免疫原性,可刺激抗体免疫动物发生免疫应答;3. 本发明提供的一种ctni蛋白抗体可以特异性地结合人血清中的ctni;4. 本发明提供的一种ctni检测试剂盒可有效检测人血清中的ctni蛋白水平。
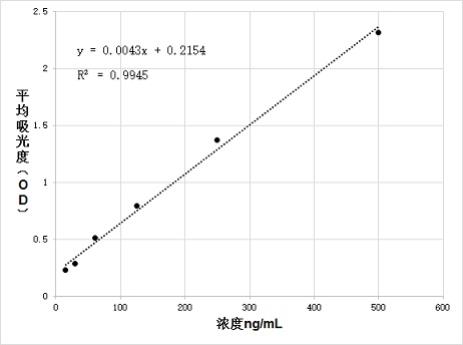
13.说明书附图图1为ctni蛋白检测试剂盒中ctni蛋白校准品浓度与吸光度标准曲线。
具体实施方式
14.为了能够更清楚地理解本发明专利的技术内容,特通过以下具体实施方式的描述进一步说明。
15.本发明所用术语具有相关领域普通技术人员通常理解的含义。然而,为了更好地理解本发明,对一些定义和相关术语的解释如下:如本发明所使用的术语“抗原决定簇”,指决定抗原性的化学基团,多位于抗原物质表面,可以由连续的氨基酸序列或不连续的蛋白质三维结构组成。本文所使用的“抗原决定簇”特指人ctni蛋白的抗原决定簇ⅰ和ⅱ多肽。
16.一、ctni蛋白抗原决定簇。
17.本发明中所述的ctni蛋白是本领域已知的,其氨基酸序列是已知的,可以在专业数据库中查询到。
18.本发明提供一种ctni蛋白抗原决定簇多肽,所述抗原决定簇多肽ⅰ和
ⅱꢀ
的氨基酸序列为如seq id no.1所示的序列和seq id no.2所示的序列,具体为:(1)leu-cys-arg-gln-leu-his-ala-tyr;和(2)asp-lys-val-asp-glu-glu-arg-tyr-asp-ile-tyr。
19.经过理论研究和实验探索,筛选出的ctni蛋白抗原决定簇多肽具有良好的抗原性,可以特异性结合对应抗体。
20.所述抗原决定簇ⅰ是人ctni蛋白(swiss-prot登录号:p19429.3)n端第96位至第102位的多肽段,并且在c末端加上氨基酸y得到,总计含有8个氨基酸。
21.所述抗原决定簇ⅱ是人ctni蛋白(swiss-prot登录号:p19429.3)n端第105位至第114位的多肽段,并且在c末端加上氨基酸y得到,总计含有11个氨基酸。
22.c末端添加氨基酸y是为了使抗原决定簇通过双偶氮联苯胺(bis-diazotized benzidine,bdb)交联到载体蛋白上,从而可以作为抗原制备对应抗体。所述抗原决定簇具有亲水性高、抗原性强、易于合成的特点。
23.上述ctni抗原决定簇多肽片段可使用固相法合成,合成方法参见实施例1。
24.本发明提供的抗原决定簇具有如下特点:1. 抗原性强,可特异性结合对应抗体;2. 使用该抗原决定簇与载体蛋白结合后,可刺激抗原免疫动物制备单克隆抗体;3. 使用该抗原决定簇制备的抗体可以特异性结合人血ctni。
25.本发明提供的抗原决定簇的分子量为1003.18可用质谱确定分子量。
26.二. ctni蛋白抗原。
27.本发明提供的ctni蛋白抗原是通过使用本发明提供的ctni蛋白抗原决定簇多肽与载体蛋白偶联制备出的。
28.可用的载体蛋白包括血蓝蛋白(keyhole limpet hemacyanin,klh)、牛血清白蛋白(bovine serum albumin,bsa)和卵清蛋白(ovalbumin,ova)等,其中优选的载体蛋白是klh,klh免疫原性强,免疫效果好,且不易引起交叉反应。制备方法采用现有成熟技术,参见实施例2。
29.三. ctni蛋白抗体。
30.本发明提供的ctni蛋白抗体是利用本发明提供的ctni蛋白抗原结合载体蛋白抗原制备的单克隆抗体和多克隆抗体,制备方法为本领域的常规技术,可用于制备ctni蛋白检测试剂盒,试剂盒可以基于免疫方法对人血液样本中的ctni蛋白进行检测。制备方法采用现有成熟技术,参见实施例2。
31.四. ctni蛋白检测试剂盒。
32.本发明提供的ctni蛋白检测试剂盒优选采用elisa双抗夹心法测定人ctni蛋白,所述试剂盒包含包被抗体、结合抗体、酶标记的第二抗体等必要试剂。
33.其中,当所述包被抗体为所述ctni蛋白单克隆抗体ⅰ时,结合抗体应为ctni蛋白多克隆抗体ⅱ;当所述包被抗体为所述ctni蛋白单克隆抗体ⅱ时,结合抗体应为ctni蛋白多克隆抗体ⅰ。
34.此外,所述ctni蛋白检测试剂盒还可以包含测定所需的任何试剂或工具,如预包被板、洗涤液、终止液等。试剂盒的制备参见实施例3。
35.本发明还提供了所述ctni蛋白检测试剂盒在定量测定人血清ctni蛋白中的应用。试剂盒的应用参见实施例3。
36.为进一步阐述本发明所采取的技术手段及其效果,以下结合实施例对本发明做进一步的说明,但本发明的保护范围不受具体的实施方式所限制,以权利要求书为准,显然,所描述的实施例仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例都属于本发明保护的范围。实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。所用的试剂或仪器未注明生产厂商者,均为可通过正规渠道商购获得的常规产品。
37.实施例1. ctni蛋白抗原决定簇ⅰ和ⅱ的制备。
38.本发明所述的ctni蛋白抗原决定簇ⅰ和ⅱ的制备方法采用化学固相法合成抗原决定簇,原理是将氨基酸的c末端固定在不溶性树脂上,然后依次进行缩合反应并延长肽链,直至多肽制备完成。
39.本发明的ctni蛋白抗原决定簇ⅰ和ⅱ的制备步骤如下。
40.1. 试剂与原料:hmp resin(p-羟甲基苯氧甲基多聚乙烯树脂,wang树脂);fmoc-aa(9-芴基甲氧羰酰基保护的氨基酸);nmp(氮甲基吡咯烷酮);
dcm(二氯甲烷);meoh(甲醇);piperidine(哌啶);dmap(二甲基氨基吡啶);hobt(羟基苯并三唑);dcc(二环已基碳二亚胺);tfa(三氟乙酸);edt(1,2-乙二硫醇);硫代苯甲醚;结晶苯酚;乙腈。
41.2. 使用仪器:多肽自动合成仪;高效液相色谱仪。
42.3. 合成方法与过程:步骤1. fmoc-aa的活化。
43.所述fmoc-aa的结构式如下所示:可简写为:所述fmoc-aa通过与dcc和hobt反应活化,反应式如下所示:步骤2. 将活化的氨基酸连接到树脂上。
44.将所述活化氨基酸与hmp resin在dmap条件下反应,得到连接上氨基酸的树脂,反应式如下所示:
步骤3. 脱除连接上氨基酸的树脂的fmoc基团。
45.在piperidine的催化作用下,脱除连接上氨基酸的树脂的fmoc基团,反应式如下所示:步骤4. 重复步骤1、步骤2,得到另一个活化氨基酸后,将得到的活化氨基酸与步骤3所得的树脂偶联,并脱去偶联后氨基组分中的氨基,反应式如下所示:步骤5. 重复步骤3、步骤4,至合成结束,得到连接了所有氨基酸的多肽树脂。
46.步骤6. 使用步骤5中得到的连接了所有氨基酸的多肽树脂,对其进行分离纯化,即可得到具有免疫活性的ctni蛋白抗原决定簇ⅰ和ⅱ。关于两种抗原决定簇分析和纯化的步骤如下:步骤6-1. 使用tfa结合edt、硫代苯甲醚和水混合的清除剂与步骤5得到的连接了所有氨基酸的多肽树脂反应,将所述具有免疫活性的ctni蛋白抗原决定簇ⅰ和ⅱ从多肽树脂上分离,反应时间为3小时;步骤6-2. 除去清除剂,使用乙醚进行萃取,得到具有免疫活性的ctni蛋白抗原决定簇ⅰ和ⅱ粗品;步骤6-3. 将具有免疫活性的ctni蛋白抗原决定簇ⅰ和ⅱ粗品进行纯化,得到具有
免疫活性的ctni蛋白抗原决定簇ⅰ和ⅱ。
47.其中,所述纯化采用高效液相色谱分离纯化,条件如下表所示:表1. 高效液相色谱分离纯化条件实施例2 . 使用实施例1所得抗原决定簇ⅰ和ⅱ分别制备单克隆抗体和多克隆抗体。
48.将实施例1所得的ctni蛋白抗原决定簇ⅰ和ⅱ分别与载体蛋白连接,并制备ctni蛋白抗原ⅰ和ⅱ,使用所述抗原ⅰ和ⅱ分别免疫动物,制备特异性的单克隆抗体与多克隆抗体。
49.本发明的ctni蛋白抗体的制备步骤如下:1. ctni蛋白抗原的制备。
50.步骤1. 取实施例1中得到的ctni蛋白抗原决定簇ⅰ或ⅱ10 mg,用1 ml 0.1 m的pbs缓冲液(ph值为7.4)溶解。
51.步骤2. 取载体蛋白(klh)10 mg,用20 ml 0.2 m的硼酸盐缓冲液(ph为8.6)溶解。
52.步骤3. 混合步骤1和步骤2中所得溶液,冷却至0 ℃,取bdb偶联剂氯化铬110 μl,室温下反应1.5小时,透析过夜后分装,即得到ctni蛋白抗原ⅰ或ⅱ,并置于-20 ℃保存。
53.2. 使用免疫动物制备单克隆抗体。
54.步骤1. 动物免疫。取1中制备的ctni蛋白抗原ⅰ或ⅱ作为免疫原,balb/c小鼠作为免疫动物,使用弗氏完全佐剂和弗氏不完全佐剂来增加ctni蛋白抗原的免疫原性。将等量的所述抗原与弗氏完全佐剂充分混匀后,以50 μg/只的剂量皮下多点注射免疫小鼠,完成初次免疫;间隔四周后,将等量的所述抗原与弗氏不完全佐剂充分混匀后,以50 μg/只的剂量皮下多点注射免疫小鼠,完成二次免疫;间隔四周后,使用所述抗原以50 μg/只的剂量皮下多点注射免疫小鼠,完成三次免疫,七天后采血检测效价,获得免疫小鼠。
55.步骤2. 细胞融合。对步骤1中所得免疫小鼠,开腹取脾,洗涤后剥去周围结缔组织,制成细胞悬液后使用不完全培养基培养,制得单细胞悬液;使用所述单细胞悬液与准备好的骨髓瘤细胞sp2/0在50%peg的介导下进行融合,获得融合细胞。
56.步骤3. 杂交瘤细胞的筛选与克隆培养。将步骤2中所得融合细胞置于培养箱中37 ℃培养7-9天后,出现较大的细胞克隆,筛选出阳性孔进行克隆化培养,获得杂交瘤细胞,并冻存。
57.步骤4. 单克隆抗体的生产。使用成年balb/c小鼠空腹接种降植烷或液体石蜡,每只小鼠0.3-0.5 ml,7-10天后接种杂交瘤细胞0.5 ml,间隔五天后采集腹部明显膨大小鼠收集腹水,离心收集上清并分装冻存,即获得所述ctni蛋白抗原决定簇多肽ⅰ或ⅱ制备的单克隆抗体ⅰ或ⅱ。
58.步骤5. 测定抗体效价。所述利用ctni蛋白抗原决定簇ⅰ或ⅱ多肽制备的单克隆抗体ⅰ或ⅱ的效价,经elisa方法测定,均达到1:32000以上。
59.3. 使用免疫动物制备多克隆抗体。
60.步骤1. 动物免疫。取1中制备的ctni蛋白抗原ⅰ或ⅱ作为免疫原,新西兰大白兔作为免疫动物,使用弗氏完全佐剂和弗氏不完全佐剂来增加ctni蛋白抗原的免疫原性。将等量的所述抗原与弗氏完全佐剂充分混匀后,以100 μg/只的剂量皮下多点注射免疫兔子,完成初次免疫;间隔四周后,将等量的所述抗原与弗氏不完全佐剂充分混匀后,以100 μg/只的剂量皮下多点注射免疫兔子,完成二次免疫;间隔四周后,使用所述抗原以100 μg/只的剂量皮下多点注射免疫兔子,完成三次免疫;四次免疫后,间隔十天采血检测效价,获得免疫兔子,颈动脉放血分离血清后,即获得所述ctni蛋白抗原决定簇多肽ⅰ或ⅱ制备的多克隆抗体ⅰ或ⅱ。
61.步骤2. 测定抗体效价。所述利用ctni蛋白抗原决定簇ⅰ或ⅱ多肽制备的多克隆抗体ⅰ或ⅱ的效价,经elisa方法测定,均达到1:16000以上。
62.实施例3. 使用实施例2所得单克隆抗体和多克隆抗体制备ctni蛋白检测试剂盒。
63.在本实施例中,使用实施例2中使用ctni蛋白抗原决定簇ⅰ多肽制备的单克隆抗体ⅰ作为ctni蛋白检测试剂盒中的包被抗体,使用ctni蛋白抗原决定簇ⅱ多肽制备的多克隆抗体ⅱ作为ctni蛋白检测试剂盒中的结合抗体。
64.1. 试剂和缓冲液。
65.包被缓冲液:0.05 m、ph9.6的碳酸盐缓冲液;样品/洗涤缓冲液:ph7.2的10
×
pbs-tween20;酶标志物稀释液:10
×
pbs-tween20(10 ml)、fcs(小牛血清)(20 ml)、蒸馏水稀释至1000 ml,酶稳定剂(1 g)、生物防腐剂(1 ml);显色剂a:柠檬酸(35.5 g)、过氧化脲(10 g),蒸馏水稀释至1000 ml,tween20(10 ml);显色剂b:柠檬酸(120 g)、edta-2na(1 g)、tmb-2hcl(2 g),蒸馏水稀释至1000 ml;终止液:2 m h2so4。
66.2. 预包被板制备。
67.将ctni蛋白单克隆抗体ⅰ溶于ph为9.6的0.05 m的碳酸盐缓冲液中,制成预包被液,在酶标板上每孔按0.1 μg/孔加入100 μl,置4 ℃温度放置18-24小时,甩掉包被液后洗涤,经bsa封闭16小时、过夜干燥后装入铝铂袋中抽真空密封,并置于4 ℃保存。
68.3. 试剂盒的组成。
69.预包被板:48/96孔;ctni校准品:6个,6
×
1.0 ml,浓度分别为0 ng/ml、2 ng/ml、5 ng/ml、10 ng/ml、25 ng/ml、50 ng/ml;ctni结合抗体:1
×
10 ml;酶联物:1
×
10 ml;浓缩洗涤液(25
×
pbs-tween20):1
×
20 ml;显色剂a:1
×
6.0 ml;显色剂b:1
×
6.0 ml;终止液:1
×
6.0 ml。
70.4. 试剂盒使用步骤。
71.在预包被板的各孔中分别加入待检血样以及标准品100 μl/孔,均为双孔,37 ℃孵育60分钟,用1
×
洗涤缓冲液洗涤5次,拍干;在各孔内加入ctni结合抗体100 μl/孔,37 ℃孵育30分钟,用1
×
洗涤缓冲液洗涤5次,拍干;再在各孔内加入酶联物100 μl/孔,37 ℃孵育30分钟,用1
×
洗涤缓冲液洗涤5次,拍干。加入显色剂a、b液,每孔各50 μl,混匀,37 ℃孵育15分钟;加终止液50 μl/孔终止反应,用酶联检测仪,双波长(450 nm、620 nm)检测吸光度。
72.5. 试剂盒检测结果判定。
73.根据试剂盒中ctni校准品的浓度和吸光度绘制标准曲线,样品检测后通过标准曲线计算待测样本的ctni浓度。下表为ctni校准品浓度和对应的平均吸光度值(od),该平均吸光度值为若干批次的平均吸光度值,仅作为参考使用,实际使用时应当以ctni校准品的实际吸光度值为准。
74.表2. 可溶性ctni校准品浓度和对应的平均吸光度(od)如图1所示,为根据上表中ctni校准品浓度和对应的平均吸光度绘制的标准曲线,标准曲线的拟合优度r2=0.9938。
75.根据试剂盒使用步骤和试剂盒检验结果判定对110名急性心衰患者和138名健康个体进行血清ctni蛋白检测,检测结果显示如表2所示,心衰患者的血清ctni蛋白含量显著高于健康组(2.49 v.s. 0.23),且差异具有统计学意义(p=0.0166)。
76.表3 . 急性心衰患者组与健康组中血清ctni含量比较由上述结果可知,本发明的ctni蛋白检测试剂盒能够特异性地检测出血清中ctni含量。
77.需要说明的是,在本文中,诸如第一和第二等之类的关系术语仅仅用来将一个实体或者操作与另一个实体或操作区分开来,而不一定要求或者暗示这些实体或操作之间存在任何这种实际的关系或者顺序。而且,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。
78.以上所述仅为本发明的优选实例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。