治疗在gla基因中具有g9331a突变的患者的法布里病的方法
本技术是申请日为2017年3月15日、申请号为201780028175.5、发明名称为“治疗在gla基因中具有g9331a突变的患者的法布里病的方法”的发明专利申请的分案申请。
技术领域
1.本发明的原理和实施例总体上涉及药理学伴侣用于治疗法布里病的用途,特别是在gla基因的内含子4中具有剪接位点突变的患者中。
背景技术:
2.许多人类疾病由导致蛋白质氨基酸序列变化的突变引起,这些变化降低蛋白质稳定性并可阻止其正确折叠。蛋白质通常在称为内质网或er的细胞的特定区域折叠。细胞具有质量控制机制,其确保蛋白质在它们可以从er移动到细胞中的合适目的地之前被折叠成它们正确的三维形状,这一过程通常被称为蛋白质运输。错误折叠的蛋白质通常在最初保留在er中后通过质量控制机制消除。在某些情况下,错误折叠的蛋白质可以在被消除之前累积在er中。错误折叠的蛋白质在er中的保留打断了它们的正确运输,并且所得的降低的生物活性可导致细胞功能受损并最终导致疾病。另外,错误折叠的蛋白质在er中的积累可能导致对细胞的各种类型的压力,这也可能有助于细胞的功能障碍和疾病。
3.导致产生不太稳定或错误折叠的蛋白质的大多数遗传突变被称为错义突变。这些突变导致蛋白质中单个氨基酸被另一个氨基酸取代。然而,除了错义突变之外,还存在可导致具有降低的生物活性的蛋白质的其他类型的突变。可引起疾病的另一种类型的突变是剪接位点突变。剪接位点突变是如下突变,其中在内含子剪接发生位点处有核苷酸的插入、缺失或数量改变。这种突变可导致mrna前体的不正确加工,包括在隐蔽剪接点处的外显子跳跃或剪接,导致总的结构和功能改变。
4.此类突变可导致溶酶体贮积病(lsd),其特征在于由于编码溶酶体酶的基因突变导致的溶酶体酶的缺陷。这导致那些酶的底物的病理积累,这些底物包括脂质、碳水化合物和多糖。尽管有与每个lsd相关的许多不同的突变基因型,但是许多突变是错义突变,其可导致产生较不稳定的酶。这些较不稳定的酶有时通过er相关的降解途径过早降解。这导致溶酶体中的酶缺陷以及底物的病理积累。此类突变酶有时在相关领域中被称为“折叠突变体”或“构象突变体”。
5.法布里病是由编码α-半乳糖苷酶a(α-gal a)的gla基因的突变引起的lsd。突变导致底物球形三酰神经酰胺(gb3,gl-3或神经酰胺三己糖苷)积累在各种组织和器官中。患有法布里病的男性是半合子,因为这些疾病基因在x染色体上编码。法布里病估计会影响40,000和60,000名男性中的1名,并且女性发生率较低。已经有几种治疗法布里病的途径。
6.用于治疗法布里病的一种批准的疗法是酶替代疗法(ert),其典型地涉及静脉内输注纯化形式的相应野生型蛋白质(基因酶公司(genzyme corp.))。酶替代疗法的主要难题之一是达到并维持治疗有效量的体内蛋白,这归因于输注的蛋白的快速降解。目前克服这个问题的方法是执行许多昂贵的高剂量输注。ert还有一些额外的警告,例
如大量生成、纯化和存储正确折叠蛋白质的困难;获得糖基化天然蛋白;产生抗蛋白免疫应答;并且蛋白质不能穿过血脑屏障缓解中枢神经系统病理(即,低生物利用度)。此外,替代酶不能以足够的量渗透心脏或肾脏,以减少肾足细胞或心肌细胞中的底物积累,这在法布里病理学中表现突出。
7.使用含有编码功能性蛋白质的核酸序列的重组载体或使用表达功能性蛋白质的遗传修饰的人细胞进行的基因疗法也正在开发中,以治疗从蛋白质替代中受益的蛋白质缺陷症和其他病症。
8.治疗一些酶缺陷的第三种途径涉及使用小分子抑制剂来减少缺陷酶蛋白质的天然底物的产生,从而改善病理学。这种“底物还原”途径已被具体描述,其针对一类约40种相关的酶障碍,称为溶酶体贮积病,包括鞘糖脂贮积病。提出用作治疗的小分子抑制剂特异性地抑制参与糖脂合成的酶,减少需要由缺陷酶分解的细胞糖脂的量。
9.治疗法布里病的另一个途径是用所谓的特异性药理学伴侣(spc)治疗。这样的spc包括α-gal a的小分子抑制剂,其可以结合α-gal a以增加突变酶和相应野生型的稳定性。然而,spc疗法的成功候选者应该具有导致产生如下酶的突变,该酶有潜力被稳定并且折叠成允许运输出er的构象。严格地截断酶的突变,如无义突变,或阻止伴侣分子结合的催化结构域中的突变,将不太可能是使用spc疗法“可挽救的”或“可增强的”,即响应spc疗法。尽管催化位点之外的错义突变更可能使用spc来挽救,但是不能保证,从而有必要筛选响应性突变。
10.因此,即使通过检测血浆或外周白细胞(wbc)中缺陷型α-gal a活性来诊断法布里病,如果有可能的话,预测具体的法布里患者是否会对spc的治疗有响应是非常困难的。此外,由于wbc只能在短时间内在培养(体外)中存活,所以筛选α-gal a的spc增强是困难的,并且对于患者来说并不是最佳的。
11.虽然开发了一些评估筛选患者对spc疗法的响应性的方法,但这些方法可能不适用于引起法布里病的所有gla突变。这意味着存在没有接受spc治疗的法布里患者,因为他们没有被确定为可治疗,尽管他们实际上可能是好的候选者。因此,仍然需要确定响应spc的新的gla突变,并使具有这些突变的法布里患者可用新的治疗方法。
技术实现要素:
12.本发明的一个方面涉及治疗被诊断患有法布里病的患者的方法。该方法包括向患者给予治疗有效剂量的α-半乳糖苷酶a的药理学伴侣,其中患者在编码α-半乳糖苷酶a的核酸序列的内含子4中具有剪接位点突变。在一个或多个实施例中,该突变是相对于seq id no:1的g9331a。在一些实施例中,该药理学伴侣包括1-脱氧半乳糖野尻霉素或其盐。在一个或多个实施例中,1-脱氧半乳糖野尻霉素或其盐的剂量为从约25mg至约250mg。在一些实施例中,1-脱氧半乳糖野尻霉素的盐是1-脱氧半乳糖野尻霉素盐酸盐。在一个或多个实施例中,该剂量为每隔一天约150mg的1-脱氧半乳糖野尻霉素盐酸盐或等效剂量的1-脱氧半乳糖野尻霉素或其除了盐酸盐以外的盐。在一些实施例中,该1-脱氧半乳糖野尻霉素或其盐是口服或通过注射给予。这些实施例可以彼此组合或与本发明的其他实施例组合,例如涉及在诊断患有或疑似患有法布里病的患者中增强α-半乳糖苷酶a的方法、α-半乳糖苷酶a的药理学伴侣用来制造用于治疗被诊断患有法布里病的患者的药剂的用途或用于治疗被诊
断患有法布里病的患者的α-半乳糖苷酶a的药理学伴侣的实施例,连同涉及顺从性突变、合适的spc及其剂量、配制品和给药途径的实施例。
13.本发明的另一方面涉及在诊断患有或疑似患有法布里病的患者中增强α-半乳糖苷酶a的方法。该方法包括向患者给予治疗有效剂量的α-半乳糖苷酶a的药理学伴侣,其中患者在编码α-半乳糖苷酶a的核酸序列的内含子4中具有剪接位点突变。在一个或多个实施例中,该突变是相对于seq id no:1的g9331a。在一些实施例中,该药理学伴侣包括1-脱氧半乳糖野尻霉素或其盐。在一个或多个实施例中,1-脱氧半乳糖野尻霉素或其盐的剂量为从约25mg至约250mg。在一些实施例中,1-脱氧半乳糖野尻霉素的盐是1-脱氧半乳糖野尻霉素盐酸盐。在一个或多个实施例中,该剂量为每隔一天约150mg的1-脱氧半乳糖野尻霉素盐酸盐或等效剂量的1-脱氧半乳糖野尻霉素或其除了盐酸盐以外的盐。在一些实施例中,该1-脱氧半乳糖野尻霉素或其盐是口服或通过注射给予。这些实施例可以彼此组合或与本发明的其他实施例组合,例如涉及治疗患有法布里病的患者的方法、α-半乳糖苷酶a的药理学伴侣用来制造用于治疗被诊断患有法布里病的患者的药剂的用途或用于治疗被诊断患有法布里病的患者的α-半乳糖苷酶a的药理学伴侣的实施例,连同涉及顺从性突变、合适的spc及其剂量、配制品和给药途径的实施例。
14.本发明的另一方面涉及α-半乳糖苷酶a的药理学伴侣用来制造用于治疗被诊断患有法布里病的患者的药剂的用途,其中患者在编码α-半乳糖苷酶a的核酸序列的内含子4中具有剪接位点突变。在一个或多个实施例中,该突变是相对于seq id no:1的g9331a。在一些实施例中,该药理学伴侣包括1-脱氧半乳糖野尻霉素或其盐。在一个或多个实施例中,1-脱氧半乳糖野尻霉素或其盐的剂量为从约25mg至约250mg。在一些实施例中,1-脱氧半乳糖野尻霉素的盐是1-脱氧半乳糖野尻霉素盐酸盐。在一个或多个实施例中,该剂量为每隔一天约150mg的1-脱氧半乳糖野尻霉素盐酸盐或等效剂量的1-脱氧半乳糖野尻霉素或其除了盐酸盐以外的盐。在一些实施例中,该1-脱氧半乳糖野尻霉素或其盐是口服或通过注射给予。这些实施例可以彼此组合或与本发明的其他实施例组合,例如涉及治疗患有法布里病的患者的方法、在诊断患有或疑似患有法布里病的患者中增强α-半乳糖苷酶a的方法、或用于治疗被诊断患有法布里病的患者的α-半乳糖苷酶a的药理学伴侣的实施例,连同涉及顺从性突变、合适的spc及其剂量、配制品和给药途径的实施例。
15.本发明的另一方面涉及用于治疗被诊断患有法布里病的患者的α-半乳糖苷酶a的药理学伴侣,其中患者在编码α-半乳糖苷酶a的核酸序列的内含子4中具有剪接位点突变。在一个或多个实施例中,该突变是相对于seq id no:1的g9331a。在一些实施例中,该药理学伴侣包括1-脱氧半乳糖野尻霉素或其盐。在一个或多个实施例中,1-脱氧半乳糖野尻霉素或其盐的剂量为从约25mg至约250mg。在一些实施例中,1-脱氧半乳糖野尻霉素的盐是1-脱氧半乳糖野尻霉素盐酸盐。在一个或多个实施例中,该剂量为每隔一天约150mg的1-脱氧半乳糖野尻霉素盐酸盐或等效剂量的1-脱氧半乳糖野尻霉素或其除了盐酸盐以外的盐。在一些实施例中,该1-脱氧半乳糖野尻霉素或其盐是口服或通过注射给予。这些实施例可以彼此组合或与本发明的其他实施例组合,例如涉及治疗患有法布里病的患者的方法、在诊断患有或疑似患有法布里病的患者中增强α-半乳糖苷酶a的方法或α-半乳糖苷酶a的药理学伴侣用来制造用于治疗被诊断患有法布里病的患者的药剂的用途的实施例,连同涉及顺从性突变、合适的spc及其剂量、配制品和给药途径的实施例。
16.本发明的另一方面涉及用于治疗法布里病的包含α-半乳糖苷酶a的药理学伴侣的药物组合物,其中患者在编码α-半乳糖苷酶a的核酸序列的内含子4中具有剪接位点突变。
17.下面列出了不同实施例。应当理解,下面列出的实施例可以不仅如下所列组合,而且可以根据本发明的范围进行其他合适的组合。
附图说明
18.图1a-e显示人野生型gla基因的完整dna序列(seq id no:1);
19.图2显示野生型gla蛋白(seq id no:2);
20.图3显示示出了剪接位点突变g9331a的gla基因的部分序列(seq id no:3);
21.图4显示暴露于dgj的突变淋巴母细胞中的α-gal a活性;
22.图5显示暴露于dgj的对照淋巴母细胞中的α-gal a活性;
23.图6是显示在用和未用dgj孵育的突变淋巴母细胞中α-gal a活性的蛋白质印迹;
24.图7是显示sry基因的存在的电泳凝胶;
25.图8是显示bfa i限制位点的存在或不存在的电泳凝胶;并且
26.图9显示来自淋巴母细胞基因组dna的三个扩增的pcr片段的测序。
具体实施方式
27.在描述本发明若干示例性实施例之前,应当理解的是,本发明不限于以下描述中列出的构建或工艺步骤的细节。本发明能够有其他的实施例,并且能够以不同的方式被实施或进行。
28.本发明的不同方面涉及鉴定将对药理学伴侣的治疗有响应的法布里患者中的新的gla突变。本发明的其他方面也涉及对这些法布里患者的治疗。例如,已经出人意料地发现,当暴露于药理学伴侣时,由gla基因中剪接位点突变g9331a造成的低α-gal a活性可以增加。通过延伸,具有这些类型突变的患者将响应药理学伴侣的治疗,其中先前认为,在gla基因中具有剪接位点突变的患者不会响应治疗,因为剪接位点突变通常引起该酶中此种主要变化。
29.定义
30.在本说明书中使用的术语在本发明的上下文中以及在使用每个术语的特定上下文中通常具有其在本领域中的普通含义。某些术语在下文或说明书中的其他地方讨论,以向从业者提供描述本发明的组合物和方法以及如何制作和使用它们的另外指导。
31.术语“法布里病”是指由于缺乏溶酶体α-半乳糖苷酶a活性而导致的鞘糖脂分解代谢的x连锁先天错误。这种缺陷导致心脏、肾脏、皮肤和其他组织的血管内皮溶酶体中球形三酰神经酰胺(神经酰胺三己糖苷)和相关的鞘糖脂的积累。
32.术语“非典型法布里病”是指具有主要为α-gal a缺陷的心脏表现的患者,即心肌细胞中的渐进式球形三酰神经酰胺(gl-3)积累,导致心脏特别是左心室的显着增大。
[0033]“携带者”是一个女性,其具有一个有缺陷型α-gal a基因的x染色体和一个有正常基因的x染色体,并且其中一种或多种细胞类型中存在正常等位基因的x染色体失活。携带者通常被诊断具有法布里病。
[0034]“患者”是指被诊断患有或疑似患有特定疾病的受试者。患者可以是人类或动物。
[0035]“法布里病”是指被诊断患有或疑似患有法布里病并且具有以下进一步定义的突变型α-gal a的个体。法布里病的特征标记物可以发生在具有相同患病率的男性半合子和女性携带者中,但女性受到的影响通常不太严重。
[0036]
人α-半乳糖苷酶a(α-gal a)是指由人gla基因编码的酶。包括内含子和外显子的α-gal a的完整dna序列可以在genbank登录号x14448.1中得到,并显示在图1a-e(seq id no:1)中。人α-gal a酶由429个氨基酸组成,并可以在genbank登录号x14448.1和u78027中获得,并示于图2(seq id no:2)。
[0037]
术语“突变蛋白质”包括在编码该蛋白质的基因中具有突变的一种蛋白质,该突变导致该蛋白质在通常存在于er中的条件下不能达到稳定构象。不能达到稳定构象导致大量的酶被降解,而不是被转运到溶酶体。这样一种突变有时称为“构象突变体”。这样的突变包括但不限于错义突变以及框内小缺失和插入。
[0038]
如本文在一个实施例中所使用的,术语“突变型α-gal a”包括在编码α-gal a的基因中具有突变的一种α-gal a,该突变导致该酶在通常存在于er中的条件下不能达到稳定构象。不能达到稳定构象导致大量的酶被降解,而不是被转运到溶酶体。
[0039]
如本文所用,术语“特异性药理学伴侣”(“spc”)或“药理学伴侣”是指特异性地结合蛋白质并具有一种或多种以下作用的任何分子,包括小分子、蛋白质、肽、核酸、碳水化合物等:(i)增强蛋白质的稳定分子构象的形成;(ii)诱导蛋白从er到另一个细胞位置(优选地原细胞定位)的运输,即,防止蛋白的er相关的降解;(iii)防止错误折叠的蛋白质的聚集;和/或(iv)恢复或增强蛋白的至少部分野生型功能和/或活性。一种化合物特异性地结合到例如α-gal a,意味着它结合到该酶并对该酶而不是相关或不相关的酶的群组施加伴侣效应。更具体地,此术语不是指内源伴侣例如bip,或指对各种蛋白质表现非特异性伴侣活性的非特异性试剂例如甘油、dmso或氘化水,即化学伴侣。在本发明中,该spc可以是可逆的竞争性抑制剂。
[0040]
酶的“竞争性抑制剂”可以指在结构上类似于酶底物的化学结构和分子几何形状以在与底物大致相同的位置结合酶的化合物。因此,抑制剂与底物分子竞争相同的活性位点,从而增加km。如果足够的底物分子可用于取代抑制剂,竞争性抑制通常是可逆的,即竞争性抑制剂可以可逆地结合。因此,酶抑制的量取决于抑制剂浓度、底物浓度、以及抑制剂和底物对活性位点的相对亲和力。
[0041]
如本文所用,术语“特异性地结合”是指药理学伴侣与蛋白质如α-gal a的相互作用,特别是与该蛋白质的氨基酸残基的相互作用,这些氨基酸残基直接参与接触药理学伴侣。药理学伴侣特异性地结合靶蛋白例如α-gal a,以对该蛋白而不是相关或不相关蛋白的群组施加伴侣作用。与任何给定的药理学伴侣相互作用的蛋白的氨基酸残基可以在或可以不在蛋白质的“活性位点”内。可以通过常规结合测定或通过结构研究(例如共结晶、nmr等)评价特异性结合。α-gal a的活性位点是底物结合位点。
[0042]“缺陷型α-gal a活性”是指来自患者的细胞中的α-gal a活性,其低于正常范围,如相比于(使用相同的方法)不患有或没有疑似患有法布里或任何其他疾病(尤其是血液病)的正常个体中的活性。
[0043]
如本文所用,术语“增强α-gal a活性”或“增加α-gal a活性”是指相对于在不与对α-gal a具有特异性的药理学伴侣接触的细胞(优选是相同细胞类型或相同细胞,例如,在
较早的时间)中采用稳定构象的α-gal a的量,在与对α-gal a具有特异性的药理学伴侣接触的细胞中增加采用稳定构象的α-gal a的量。此术语还指相对于不与对蛋白α-gal a具有特异性的药理学伴侣接触的α-gal a的运输,在与对α-gal a具有特异性的药理学伴侣接触的细胞中增加α-gal a向溶酶体的运输。这些术语是指野生型和突变型α-gal a两者。在一个实施例中,细胞中α-gal a的量的增加是通过测量来自已经用spc处理的细胞的裂解物中人工底物的水解来测量。水解的增加表明α-gal a活性增加。
[0044]
术语“α-gal a活性”是指细胞中野生型α-gal a的正常生理功能。例如,α-gal a活性包括gl-3的水解。
[0045]“响应者”是诊断患有或疑似患有溶酶体贮积病例如法布里病的个体,响应于接触spc,其细胞分别展现出足够增加的α-gal a活性、和/或症状的减轻或替代标记物的改善。法布里替代标记物的改善的非限制性实例是溶血gb3和美国专利申请公开号us 2010-0113517中披露的那些。
[0046]
us 2010/0113517中披露的法布里病替代标记物的改善的非限制性实例包括细胞(例如成纤维细胞)和组织中的α-gal a水平或活性增加;gl-3积累减少;高半胱氨酸和血管细胞粘附分子-1(vcam-1)的血浆浓度降低;心肌细胞和瓣膜纤维细胞内gl-3的积累减少;心脏肥大(尤其是左心室)减少,瓣膜功能不全和心律失常减轻;蛋白尿减轻;脂质如cth、乳糖神经酰胺、神经酰胺的尿浓度降低,以及葡萄糖神经酰胺和鞘磷脂的尿浓度增加;在肾小球上皮细胞中不存在层叠包涵体(斑马体);肾功能改善;少汗症缓和;血管角质瘤不存在;以及听力异常如高频感觉神经性听力损失进行性听力损失、突发性耳聋或耳鸣改善。神经症状的改善包括短暂性缺血发作(tia)或中风的预防;以及自身表现为肢端感觉异常(四肢灼烧或刺痛)的神经性疼痛的减轻。可以针对法布里病进行评估的另一个类型的临床标记物是有害的心血管表现形式的流行。法布里病常见的心脏相关征象和症状包括左心室肥大、瓣膜疾病(尤其是二尖瓣脱垂和/或反流)、早发性冠状动脉疾病、心绞痛、心肌梗塞、传导异常、心律失常、充血性心力衰竭。
[0047]
实现一个或多个上述响应的剂量是“治疗有效剂量”。
[0048]
短语“药学上可接受的”是指生理学可耐受的并且当给予人时不会典型地产生不良反应的分子实体和组合物。在一些实施例中,如本文所用,术语“药学上可接受的”是指由联邦或州政府的管理机构批准的或者在美国药典或其他普遍认可的药典中列出的,用于在动物体内并且更具体地在人体内的使用。就药物载体而论的术语“载体”是指稀释剂、辅助剂、赋形剂、或与化合物一起给予的运载体。这些药学载体可以是无菌液体,如水和油类。优选地应用水或水溶液盐溶液和葡萄糖和甘油水溶液溶液作为载体,特别是用于可注射溶液。适合的药物载体描述于由e.w.马丁(martin)编辑的“雷明顿药学大全(remington’s pharmaceutical sciences)”第18版,或其他版本。
[0049]
如本文所用,术语“分离的”意指将参比材料从其通常发现的环境中去除。因此,分离的生物材料可以不含细胞组分,即发现或产生该材料的细胞的组分。在核酸分子的情况下,分离的核酸包括pcr产物、凝胶上的mrna条带、cdna或限制性片段。在另一个实施例中,分离的核酸优选地从可以在其被发现的染色体上切除,并且更优选地不再与非调节性非编码区连接,或与位于当在染色体中发现时由分离的核酸分子包含的基因上游或下游的其他基因连接。在又另一个实施例中,分离的核酸缺少一个或多个内含子。分离的核酸包括插入
质粒、粘粒、人工染色体等中的序列。因此,在一个具体实施例中,重组核酸是分离的核酸。分离的蛋白质可以与其在细胞中结合的其他蛋白质或核酸或两者结合,或者如果其是膜结合蛋白质则与细胞膜结合。将分离的细胞器、细胞或组织从其在生物体中发现的解剖部位去除。分离的材料可以是但不必是纯化的。
[0050]
术语“约”和“大约”通常意指在给定测量的性质或精度的情况下测量的量的可接受的误差程度。典型地,示例性的误差程度在给定的数值或数值范围的20%以内,优选在10%以内,并且更加优选在5%以内。可替代地,特别是在生物系统中,术语“约”和“近似地”可以表示在给定值的一个数量级内,优选地在10倍或5倍内,更优选地在2倍内的值。除非另有说明,本文给出的数字量是近似地,意味着当没有明确说明时,可以推断出术语“约”或“近似地”。
[0051]
术语“酶替代疗法”或“ert”是指将非天然的、经纯化的酶引入具有这种酶缺陷的个体中。给予的蛋白质可以从自然来源或通过重组表达而获得(如下文更详细描述的)。该术语也指将经纯化的酶引入个体,该个体在其他情况下需要或受益于给予经纯化的酶,例如该个体遭受酶不足。该引入的酶可以是在体外产生的经纯化的重组酶,或从离体组织或体液(例如像胎盘或动物奶)或从植物纯化的蛋白质。
[0052]
药理学伴侣
[0053]
与lsd相关的酶的小分子抑制剂的结合可以增加突变酶和相应的野生型酶的稳定性(参见美国专利号6,274,597;6,583,158;6,589,964;6,599,919;6,916,829;和7,141,582,全部通过引用结合在此)。特别地,葡萄糖和半乳糖的小分子衍生物(其是用于几种靶标溶酶体酶的特异性、选择性竞争性抑制剂)的给予有效地增加了体外细胞中酶的稳定性,并因此增加了酶到溶酶体的运输。因此,通过增加溶酶体中酶的量,酶底物的水解预期增加。此策略背后的原有理论如下:由于突变酶蛋白在er中不稳定(石井(ishii)等人,生物化学和生物物理研究通讯(biochem.biophys.res.comm.)1996;220:812-815),因此酶蛋白在正常转运途径(er
→
高尔基体
→
核内体
→
溶酶体)中延迟并过早降解。因此,结合并增加突变酶稳定性的化合物可以充当酶的“伴侣”,并增加可以离开er并移动到溶酶体的量。另外,由于一些野生型蛋白质的折叠和运输是不完全的,在一些情况下一些野生型蛋白质的多达70%在达到其最终细胞位置之前被降解,所以这些伴侣可用于稳定野生型酶,并增加可以离开er并被运输到溶酶体的酶的量。这种策略已经显示在体外和体内增加几种溶酶体酶,包括β-葡糖脑苷脂酶和α-葡糖苷酶,其缺陷分别与戈谢病和庞贝病有关。
[0054]
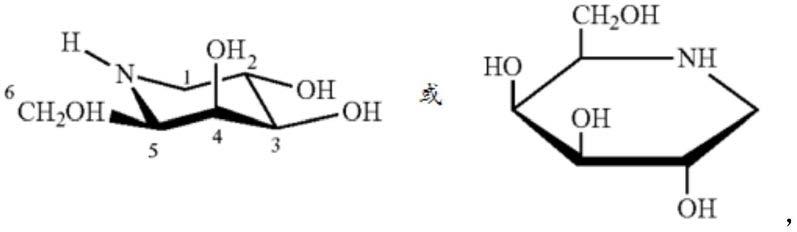
在一个或多个实施例中,该spc是1-脱氧半乳糖野尻霉素(dgj),其是指具有以下结构的化合物:或1-脱氧半乳糖野尻霉素的药学上可接受的盐、酯或前药。dgj的盐酸盐已知是米
加司他盐酸盐(米加司他)。
[0055]
还有其他α-gal a的spc描述于美国专利号6,274,597、6,774,135和6,599,919,并且包括α-3,4-二-差向-高野尻霉素、4-差向-荞麦碱、α-别高野尻霉素、n-甲基-脱氧半乳糖野尻霉素、β-1-c-丁基-脱氧半乳糖野尻霉素、α-半乳糖-高野尻霉素、打碗花素a3、打碗花素b2、打碗花素b3、n-甲基-打碗花素a3、n-甲基-打碗花素b2和n-甲基-打碗花素b3。
[0056]
在具体实施例中,该spc包括1-脱氧半乳糖野尻霉素或其盐。在另外的实施例中,该spc包括1-脱氧半乳糖野尻霉素盐酸盐。
[0057]
α-gal a的这些spc中任一个都可以与本发明的任何其他实施例组合使用,例如涉及治疗患有法布里病的患者的方法、在诊断患有或疑似患有法布里病的患者中增强α-半乳糖苷酶a的方法、α-半乳糖苷酶a的药理学伴侣用来制造用于治疗被诊断患有法布里病的患者的药剂的用途或用于治疗被诊断患有法布里病的患者的α-半乳糖苷酶a的药理学伴侣的实施例,连同涉及spc的合适剂量、顺从性突变以及对在编码α-半乳糖苷酶a的核酸序列的内含子4中具有剪接位点突变的法布里患者的治疗的实施例。
[0058]
鉴定响应于药理学伴侣的gla突变
[0059]
由于法布里病罕见,涉及多器官,发病年龄范围广,并且是异质性的,正确诊断是一个挑战。卫生保健专业人员中的意识较低,并且误诊也频繁。一旦患者有症状,加上突变分析,法布里病的诊断最常基于血浆或外周白细胞(wbc)中降低的α-gal a活性来证实。在女性中,诊断甚至更具挑战性,因为携带者女性的酶鉴定由于携带者的一些细胞中的随机x染色体失活而不太可靠。例如,一些专性携带者(受正统影响的男性的女儿)具有从正常到非常低活性范围的α-gal a酶活性。由于携带者在白细胞中具有正常的α-gal a酶活性,所以仅通过遗传学检验鉴定α-gal a突变提供了精确的携带者鉴定和/或诊断。
[0060]
如本文所用的“顺从性突变”意指当用α-gal a的药理学伴侣孵育时具有该突变的细胞的α-gal a活性将增加。在一些实施例中,将满足以下标准:在10μm药理学伴侣孵育后≥约1.2倍的α-gal a活性相对增加,和/或≥约3.0%的野生型(wt)绝对增加。在一些实施例中,该药理学伴侣是米加司他。涉及顺从性突变的任何实施例可以与本发明的任何其他实施例组合,例如涉及治疗患有法布里病的患者的方法、在诊断患有或疑似患有法布里病的患者中增强α-半乳糖苷酶a的方法、α-半乳糖苷酶a的药理学伴侣用来制造用于治疗被诊断患有法布里病的患者的药剂的用途或用于治疗被诊断患有法布里病的患者的α-半乳糖苷酶a的药理学伴侣的实施例,连同涉及spc、其合适的剂量以及涉及对在编码α-半乳糖苷酶a的核酸序列的内含子4中具有剪接位点突变的法布里患者的治疗的实施例。
[0061]
已提供以前的筛选方法,其在开始治疗之前评估酶增强。例如,使用hek-293细胞的测定已经在临床试验中用于预测给定的突变是否响应于药理学伴侣(例如米加司他)治疗。在此测定中,建立了cdna构建体。相应的α-gal a突变形式在hek-293细胞中瞬时表达。然后将细胞
±
米加司他(17nm至1mm)孵育4至5天。之后,在细胞裂解物中使用合成的荧光底物(4-mu-α-gal)或通过蛋白质印迹测量α-gal a水平。这已经针对已知的导致疾病的错义或小的框内插入/缺失突变进行。以前使用这些方法鉴定为响应spc(例如dgj)的突变在us 8592362中列出。然而,此hek-293测定使用重组gla cdna;因此,突变体α-gal a独立于前mrna剪接而表达,并且hek-293测定不能用于预测剪接位点突变的响应。
[0062]
然而,如本文所述,淋巴母细胞测定可以替代地用于鉴定符合上述顺从性标准的
突变。对于本文所述的剪接位点突变,淋巴母细胞培养物可源自具有该突变的男性患者,随后进行该测定。可以通过在培养基(例如,补充以胎牛血清和青霉素-链霉素,在37℃,5%co2下)的悬浮液中培养来得到淋巴母细胞。然后可以使用血液样品通过对外周血单核细胞进行的植物血凝素刺激的爱泼斯坦-巴尔病毒(epstein
–
barr virus)转化来永生化和建立法布里患者淋巴母细胞系。然后可以将淋巴母细胞进行接种并用不同浓度的伴侣孵育,并使用本领域已知的方法进行评估(参见例如本杰明(benjamin)e.r.等人,遗传代谢疾病(inherited metab.dis.)2009;32:424-440)。
[0063]
因此,本发明的另一方面涉及用于确定法布里病患者是否将响应于用α-半乳糖苷酶a的药理学伴侣进行的治疗的方法,其中该患者在编码α-半乳糖苷酶a的核酸序列(seq id no:1)的外显子中不具有错义突变,该方法包括从患者的淋巴母细胞样品中分离编码α-半乳糖苷酶a的基因组dna,任选地扩增包含内含子4的dna或其片段,并确定内含子4中存在或不存在剪接位点突变,其中在内含子4中具有剪接位点突变的患者响应于用α-半乳糖苷酶a的药理学伴侣进行的治疗。
[0064]
内含子4中的剪接位点突变和法布里病的治疗
[0065]
因此,一个或多个实施例涉及在编码α-半乳糖苷酶a的核酸序列的内含子4中具有剪接位点突变的法布里患者的治疗。因为剪接位点突变发生在内含子中,相对于示于图1a-e(seq id no:1)的完全gla dna序列描述突变。相对于seq id no:1,内含子4跨越核酸位置8413至10130。一个这样的突变是g9331a突变(也称为ivs4 919g
→
a)。显示这种突变的gla dna序列的摘录如图3和seq id no:3所示。这种突变与法布里病的心脏变体形式相关。具体来说,患有这种形式的疾病的患者可经历左心室肥大并且患有心肌病。在中国台湾人群中,这种突变在新生儿(1600名男性中约1人)和特发性肥大型心肌病患者中也已显示出高流行率(林(lin),h.等人,心血管遗传学(cardiovascular genetics.)2009;2:450-456))。事实上,在中国台湾人群中,在针对法布里病筛选出阳性的82%的新生儿中发现该突变(参考同上)。在gla基因中,g9331a发生在内含子4的中部(石井(ishii)等人美国人类遗传学杂志(am.j.hum.genet.)70:994-1002,2002)。此突变导致正常较弱剪接位点的增加的识别,导致另外的57个核苷酸的序列插入到α-gal a转录物中。插入的序列在外显子4的下游引入了提前终止密码子,其具有222个氨基酸残基的预测截短的蛋白质产物。异常的α-gal a mrna构成源自具有此突变的男性法布里患者的淋巴母细胞中总α-gal a mrna的多于70%。然而,一些野生型α-gal a mrna被表达,并且所得的残留α-gal a活性低于正常的10%(石井,中尾(nakao)等人,2002)。
[0066]
如以下实例所示,在雄性法布里患者衍生的淋巴母细胞测定中针对响应dgj来评估g9331a突变。男性法布里患者淋巴母细胞测定与hek检测相关(吴(wu)等人,人类突变(human mutation)2011,图5),并且此突变符合基于淋巴母细胞测定的顺从性标准。因为该突变在淋巴母细胞测定中符合上述顺从性标准,所以认为该突变将在体内显示响应dgj。此外,法布里病的发病年龄、进展和严重度至少部分依赖于与溶酶体中酶活性相关的底物积累速率。因此,完全缺乏残留活性可对应于快速的底物积累,并因此是该疾病的更严重形式(具有早期发作和快速进展)。然而,甚至少量的残留活性可足以降解大量的底物。这进而会导致疾病更轻,发病更迟且因为缓慢下来而进展更慢。考虑到这些因素,认为酶活性甚至适度的增加也可以降低严重临床表型的影响。数据表明,对于大多数lsd,正常活性的仅1%至
6%被估计为足以延缓或预防疾病发病或产生更温和的疾病形式。也就是说,活性上仅小的增加可对底物水平具有显着影响,并因此对疾病严重度和疾病进展速率具有显着影响。相反,预期体外未显示响应的突变体溶酶体酶也不会在体内响应。
[0067]
因此,本发明的一个方面涉及spc在编码α-半乳糖苷酶a的基因中具有突变的患者中治疗法布里病的用途,其中该患者被鉴定为相对于seq id no:1所列的核酸序列编码的人α-半乳糖苷酶a在内含子4中具有剪接位点突变。本发明的另一方面涉及治疗被诊断患有法布里病的患者的方法。在一个或多个实施例中,该方法包括向患者给予治疗有效剂量的α-gal a的药理学伴侣(spc)。在另外的实施例中,患者在编码α-半乳糖苷酶a的核酸序列的内含子4中具有剪接位点突变。本发明的另一方面涉及在诊断患有或疑似患有法布里病的患者中增强α-半乳糖苷酶a的方法。在一个或多个实施例中,该方法包括向患者给予治疗有效剂量的α-gal a的药理学伴侣(spc),其中患者具有由相对于seq id no:1具有剪接位点突变的核酸序列编码的突变型α-半乳糖苷酶a。这些用途和方法的细节和另外的实施例如下。涉及治疗患有法布里病的患者的方法、在诊断患有或疑似患有法布里病的患者中增强α-半乳糖苷酶a的方法、α-半乳糖苷酶a的药理学伴侣用来制造用于治疗被诊断患有法布里病的患者的药剂的用途或用于治疗被诊断患有法布里病的患者的α-半乳糖苷酶a的药理学伴侣的实施例中任一项(其中该患者被鉴定为相对于seq id no:1所列的核酸序列编码的人α-半乳糖苷酶a在内含子4中具有剪接位点突变)可以与本发明的任何其他实施例组合,例如涉及spc及其合适的剂量的实施例。
[0068]
在一个或多个实施例中,患者可能在其gla基因中具有其他突变。例如,内含子区域可能存在可能影响或不影响所得α-gal a酶的其他突变。因此,在一个或多个实施例中,患者具有由与seq id no:1具有95%、96%、97%、98%、99%或99.5%一致性的核酸序列编码的突变型α-半乳糖苷酶a。在一些实施例中,患者具有相对于seq id no:1基本上由g9331a组成的突变。再次,这些实施例中的任何一个可以与本发明的任何其他实施例组合,例如涉及顺从性突变、spc及其合适的剂量的实施例。
[0069]
令人意想不到的是,药理学伴侣将有效地治疗归因于此类剪接位点突变的法布里病。如上所讨论的,甚至不可能通过标准hek-293测定来测试这样的突变,以确定对用药理学伴侣进行的孵育的响应性。此外,关于g9331a,先前认为g9331a突变对用dgj治疗无响应(参见本杰明(benjamin)e.r.等人,遗传代谢疾病(inherited metab.dis.)2009;32:424-440)。此外,由于剪接位点突变可导致mrna前体的不正确加工,包括外显子跳跃或隐形剪接位点的剪接,导致总结构和功能改变,g9331a的顺从性不能从已知为响应的突变中预测。虽然不希望受到任何特定的理论的约束,但是认为药理学伴侣通过增强产生的小量野生型酶的活性而是有效的。野生型酶的合成、折叠和运输可能不是完全有效的。该药理学伴侣可以稳定该野生型。
[0070]
对在内含子4中具有g9331突变或另一个剪接位点突变的患者的治疗预期会导致上述一种或多种症状的减轻。治疗进展可以通过跟踪某些参数进行评估和监测。例如,如上所讨论的,可以针对法布里病进行评估的一种临床标记物是有害的心血管表现形式的流行。心脏并发症在法布里病中很常见,并且是造成死亡的主要原因。最频繁的心脏表现形式是lvh,这是心脏事件的重要风险因素。已经显示lv-质量的减少会改善这些患者中的结果。长达24个月的米加司他治疗显着减少lvmi,在具有基线lvh的患者中看到更大的减少。ert
对lv-质量的影响显现不一致。在最近的研究中,lvmi在用ert治疗了的》30岁的男性中持续增加。另一项ert研究发现,lvmi的初始改善随着时间的推移减少。如由稳定的左心室后壁厚度和心室内间隔壁厚度的减少所示,在我们的研究中米加司他治疗的患者中lvmi的减少不是由于纤维化引起的。预期lvmi的这种减少将促成法布里病中常见的心脏并发症的减少。
[0071]
肾功能渐进式衰退也是法布里病的主要并发症。例如,与经典法布里表型相关的患者,其与进行性肾损伤相关,可导致透析或肾移植。慢性肾脏疾病预后联盟(chronic-kidney-disease-prognosis-consortium),egfrckd-epi衰退已显示是随后的终末期肾脏疾病和死亡风险的可靠替代。
[0072]
监测治疗的另一种方法是追踪作为生物标记物的溶血gb3(球丙糖酰基鞘氨醇)。溶血gb3通常在患有该疾病的患者中增加,并且可以在尿液中检测到。因此,患者的成功治疗将以溶血gb3的量减少来标示。
[0073]
配制与给药
[0074]
因为突变之间存在如此多的异质性,药理学伴侣(例如,dgj)给药的剂量和给药方案可以根据患者而变化,并且取决于患者的残留α-gal活性。作为非限制性实例,预期以下剂量和方案足以在大多数“可挽救的”个体中增加α-gal:25mg一天两次(b.i.d);50mg一天一次;50mg b.i.d.;50mg每隔一天一次,75mg一天一次;75mg b.i.d.;100mg一天一次;100mg b.i.d.;150mg一天一次;150mg b.i.d.,150mg每隔一天一次;250mg一天一次;250mg b.i.d.和250mg每隔一天一次。在特定实施例中,这些剂量为50mg一天一次;50mg每隔一天一次;150mg一天一次;150mg每隔一天一次。在一个或多个实施例中,这些剂量涉及1-脱氧半乳糖野尻霉素盐酸盐或等效剂量的1-脱氧半乳糖野尻霉素或其除了盐酸盐以外的盐。在一些实施例中,这些剂量涉及游离碱。在替代实施例中,这些剂量涉及1-脱氧半乳糖野尻霉素的盐。在另外的实施例中,1-脱氧半乳糖野尻霉素的盐是1-脱氧半乳糖野尻霉素盐酸盐。应注意,150mg 1-脱氧半乳糖野尻霉素盐酸盐相当于123mg游离碱形式的1-脱氧半乳糖野尻霉素。因此,在一个或多个实施例中,该剂量为150mg每隔一天一次的1-脱氧半乳糖野尻霉素盐酸盐或等效剂量的1-脱氧半乳糖野尻霉素或其除了盐酸盐以外的盐。在另外的实施例中,该剂量为150mg每隔一天一次的1-脱氧半乳糖野尻霉素盐酸盐。在其他实施例中,该剂量为123mg每隔一天一次的1-脱氧半乳糖野尻霉素游离碱。
[0075]
根据本发明的dgj的给予可以是适于任何给药途径的配制品,但优选以口服剂型例如片剂、胶囊或溶液给药。作为一个实例,患者是口服给予胶囊,每个胶囊含有25mg、50mg、75mg、100mg或150mg 1-脱氧半乳糖野尻霉素盐酸盐或等效剂量的1-脱氧半乳糖野尻霉素或其除了盐酸盐以外的盐。
[0076]
在具体实施例中,spc(例如,1-脱氧半乳糖野尻霉素或其盐)的剂量为从约25mg至约250mg 1-脱氧半乳糖野尻霉素盐酸盐或等效剂量的1-脱氧半乳糖野尻霉素或其除了盐酸盐以外的盐。在另外的实施例中,spc(例如,1-脱氧半乳糖野尻霉素盐酸盐)的剂量为每隔一天约150mg。在一些实施例中,该spc(例如1-脱氧半乳糖野尻霉素或其盐)是口服给予的。在一个或多个实施例中,该spc(例如1-脱氧半乳糖野尻霉素或其盐)是通过注射给予的。该spc可以伴随药学上可接受的载体,其可取决于给药方法。
[0077]
在本发明的一个实施例中,该伴侣化合物作为单一疗法给予,并且可以处于适合
于任何给药途径的形式,包括例如以片剂或胶囊或液体的形式口服,以处于注射用无菌水溶液,或以在重建期间或之后立即加入到替代酶的配制品中以防止在给予前在体外的酶聚集的干燥冻干粉末。
[0078]
当该伴侣化合物被配制来供口服给予时,可以通过常规手段与以下项一起来制备片剂或胶囊:药学上可接受的赋形剂,诸如粘合剂(例如预胶凝化淀粉、聚乙烯吡咯烷酮或羟丙基甲基纤维素);填充剂(例如乳糖、微晶纤维素或磷酸氢钙);润滑剂(例如硬脂酸镁、滑石或二氧化硅);崩解剂(例如马铃薯淀粉或羟基乙酸淀粉钠);或湿润剂(例如十二烷基硫酸钠)。可以用本领域熟知的方法将这些片剂进行包衣。用于口服给药的液体制剂可以采取例如溶液、糖浆或悬浮液的形式,或它们可以作为一种干产品(在使用前用水或其他合适的载体进行组合)而存在。此类液体制剂可以通过常规方法用药学上可接受的添加剂来制备,这些添加剂为诸如助悬剂(例如山梨糖醇糖浆、纤维素衍生物或氢化的可食用脂肪);乳化剂(例如卵磷脂或阿拉伯胶);非水性载体(例如杏仁油、油状酯、乙醇或分馏的植物油);以及防腐剂(例如,对羟基苯甲酸甲酯或丙酯或山梨酸)。适当时制剂还可以包含缓冲盐、调味剂、着色剂和甜味剂。可以适当地配制口服制剂以使活性伴侣化合物能够可控制地释放。
[0079]
适合于肠胃外/可注射使用的伴侣化合物的药物配制品一般包括无菌水溶液(在水溶性的情况下)或分散体以及用于临时制备无菌可注射溶液或分散液的无菌粉末。在所有情况下,所述形式必须是无菌的且必须具有达到容易注射的程度的流动性。它在制造和保存的条件下必须是稳定的,并且必须防止微生物如细菌和真菌的污染作用来保存。该载体可以是包含以下各项的一种溶剂或分散介质:例如,水、乙醇、多元醇(例如,甘油、丙二醇和聚乙二醇等)、其适合的混合物、以及植物油。可以例如通过使用一种包衣(如卵磷脂)、通过在分散情况下维持所需颗粒大小以及通过使用表面活性剂来维持适当的流动性。防止微生物的作用可以通过不同的抗细菌以及抗真菌剂,例如对羟苯甲酸酯、氯丁醇、苯酚、苄醇、山梨酸等来实现。在许多情况下,合乎情理地包括等渗剂,例如,糖或氯化钠。可通过使用延迟吸收的试剂(例如单硬脂酸铝和明胶)的组合物来实现可注射组合物的延长的吸收。
[0080]
按照需要,可以通过将纯化的酶和该伴侣化合物以需要的量掺入具有以上列举的各种其他成分中的适当溶剂中,随后进行过滤或最终灭菌来制备无菌可注射溶液。总体上,通过将各种灭菌的活性成分掺入无菌载体中来制备分散体,该无菌载体含有基础分散介质以及来自以上枚举的那些的所需其他成分。在用于制备无菌的可注射溶液的无菌粉末的情况下,优选的制备方法是从它的以前无菌过滤的溶液进行真空干燥以及冷冻干燥的技术,它们给出了活性成分加上任何另外的所希望的成分的一种粉末。
[0081]
该配制品可以含有赋形剂。在配制品中包括的药学上可接受的赋形剂是缓冲液,如柠檬酸盐缓冲液、磷酸盐缓冲液、乙酸盐缓冲液、和碳酸氢盐缓冲液、氨基酸、尿素、醇、抗坏血酸、磷脂;蛋白质,诸如血清白蛋白、胶原、以及明胶;盐,诸如edta或egta、以及氯化钠;脂质体;聚乙烯吡咯烷酮;糖,诸如右旋糖酐、甘露醇、山梨糖醇、以及甘油;丙二醇以及聚乙二醇(例如,peg-4000、peg-6000);甘油;甘氨酸或其他氨基酸;以及脂类。与配制品一起使用的缓冲剂体系包括柠檬酸盐;乙酸盐;碳酸氢盐;以及磷酸盐缓冲剂。磷酸盐缓冲剂是一个优选的实施例。
[0082]
该伴侣化合物的给予途径可以是口服的(优选地)或肠胃外的,包括静脉内、皮下、动脉内、腹膜内、眼内、肌内、口颊、直肠、阴道、眼眶内、脑内、真皮内、颅内、脊柱内、心室内、
鞘内、脑池内、囊内、肺内、鼻内、经粘膜、经皮肤、或通过吸入。
[0083]
该伴侣化合物的上述肠胃外配制品的的给予可以是通过周期性注射制剂的推注,或可以从一个储库通过静脉内或腹膜内给药来给予,该储库可以是外部的(例如静脉注射袋)或内部的(例如生物可蚀性植入物)。
[0084]
涉及药剂配制品和给药的实施例可以与本发明的任何其他实施例组合,例如涉及治疗患有法布里病的患者的方法、在诊断患有或疑似患有法布里病的患者中增强α-半乳糖苷酶a的方法、α-半乳糖苷酶a的药理学伴侣用来制造用于治疗被诊断患有法布里病的患者的药剂的用途或用于治疗被诊断患有法布里病的患者的α-半乳糖苷酶a的药理学伴侣的实施例,连同涉及顺从性突变、spc及其合适的剂量的实施例。
[0085]
在一个或多个实施例中,伴侣与酶替代疗法组合给予。酶替代疗法通过外源性引入野生型或生物功能性酶通过输注来增加蛋白质的量。已经针对许多遗传疾病(包括溶酶体贮积病法布里病,如上所提及的)开发了这种疗法。输注后,预期外源酶通过非特异性或受体特异性机制被组织吸收。一般来说,吸收效率不高,并且外源蛋白的循环时间短。此外,外源蛋白是不稳定的,并且经受快速的细胞内降解,而且在随后治疗的情况下具有不利免疫反应的潜力。在一个或多个实施例中,该伴侣与替代酶在相同时间给予。在一些实施例中,该伴侣与替代酶共配制。
[0086]
在整篇说明书中对“一个实施例”、“某些实施例”、“不同实施例”、“一个或多个实施例”或“实施例”的引用意味着与实施例相联系地描述的具体的特征、结构、材料、或特性是包括在本发明的至少一个实施例中的。因此,在整篇说明书中多个位置中出现的短语如“在一个或多个实施例中”、“在某些实施例中”、“不同实施例”、“在一个实施例中”或“在实施例中”不一定是指本发明中的相同实施例。此外,在一个或多个实施例中,具体的特征、结构、材料、或特性可以是以任何适合的方式进行组合。
[0087]
尽管此处的发明已参照具体实施例进行了说明,应理解这些实施例对于本发明的原理和应用仅仅是说明性的。对本领域的普通技术人员而言将明显地是,在不偏离本发明的范围和精神的情况下,可以对本发明的方法和设备进行多种修改和变化。因此,意图是本发明包括在所附的权利要求书及其等效物的范围内的修改和变化。实例
[0088]
实例1:dgj对g9331a突变的影响
[0089]
研究了dgj在证实存在g9331a gla突变的雄性法布里淋巴母细胞系中的作用,以确定大小和ec
50
值。g9331a或正常人(阳性对照)淋巴母细胞以每孔25,000个细胞接种(于96孔板中)。然后将淋巴母细胞
±
dgj孵育5天(10点浓度响应曲线)。两种细胞系的浓度范围为5nm至100μm。使用4-mug合成荧光底物测量细胞裂解物中的α-gal a活性。在存在dgj的情况下最大水平被定义为s形浓度响应曲线的顶部。然后确定α-gal a水平是否响应于dgj而增加。酶测定结果通过蛋白质印迹证实。
[0090]
图4和5分别显示突变体和正常淋巴母细胞中代表性的α-gal a活性数据。如图中看到的,g9331a和正常阳性对照淋巴母细胞均显示响应dgj的浓度依赖性增加的水平。数据点是一式四份测定的平均值
±
sem。数据表示四个独立实验的结果。
[0091]
α-gal a活性的总结示于下表1中。表1:淋巴母细胞α-gal a活性数据总结
α-gal a活性,nmol/mg蛋白/小时;wt的%,无at1001的野生型α-gal a活性的百分比;带有符号“#”的栏表示使用假设希尔(hill)斜率为1(在at1001存在时的最大水平被定义为s形浓度响应曲线的顶部)的s形浓度响应方程式,基于测量的基线、最大值和ec
50
值来计算10μm at1001处的值;*p《0.05,**p《0.01,***p《0.001,通过双尾配对t检验比较基线和最大α-gal a活性。
[0092]
如表1所示,对于这种
‘
遗漏性剪接位点’突变,g9331a淋巴母细胞具有低于正常基线的α-gal a活性。然而,最大相对增加和ec
50
值几乎等于正常淋巴母细胞的那些。此外,响应于此法布里细胞系的dgj孵育,观察到α-gal a蛋白水平的显着增加,与正常淋巴母细胞的那些相似(g9331a,2.1
±
0.5倍,n=3;野生型,1.8
±
0.1倍,n=3)。来自ivs4 919g
→
a型淋巴母细胞的结果满足
‘
合格突变’的hek-293细胞标准:α-gal a突变形式,相对增加为高于基线≥1.2倍,并且绝对增加为≥3%的野生型(用10μm dgj孵育后)。
[0093]
蛋白质印迹数据用于证实以前的结果。每个泳道加载40μg裂解物。g9331a淋巴母细胞的代表性蛋白质印迹数据显示在图6中。如图所示,用1mm dgj孵育后,蛋白质印迹表明α-gal a蛋白增加约1.68倍。此数据表示四个独立实验的结果。
[0094]
实例2:验证g9331突变
[0095]
通过测序在细胞系中证实g9331a的存在。从突变体(测试的两种不同培养物)或正常人类淋巴母细胞(野生型)中分离的基因组dna中pcr扩增ivs4 919g
→
a突变位点周围的1000bp片段。对每个片段进行测序(金唯智(genewiz)),并在两批g9331a细胞中证实ivs4 919g
→
a突变的存在,而在正常细胞中证实野生型序列。
[0096]
实例3:g9331淋巴母细胞中不存在野生型gla的验证
[0097]
接下来,验证野生型gla基因不存在于测试的突变型淋巴母细胞中。使用三种单独的策略来证明野生型gla基因不存在于g9331a淋巴母细胞中。在所有三种策略中,将g9331a淋巴母细胞样品与野生型淋巴母细胞以及1:1g9331a:野生型混合物进行比较。将来自野生型淋巴母细胞的样品用作对照,以显示该方法对于纯野生型基因的检测是灵敏的。将来自突变体和野生型淋巴母细胞混合物的样品用作对照,以显示该方法对在从杂合雌性预期(因为没有雌性g9331a淋巴母细胞可用)的水平检测野生型基因是灵敏的。
[0098]
策略1:y染色体特异性基因的pcr扩增
[0099]
在这种策略下,如果细胞系来自雄性,则证实不存在野生型gla。如果细胞系来自雄性,则只存在突变等位基因。选择sry(性别决定区y,614-bp;acc#l08063)作为y染色体特异性基因进行pcr扩增。sry容易从ivs4 919g
→
a淋巴母细胞(fb-11细胞系)扩增,表明来自这些细胞的基因组dna含有y染色体。sry也容易从野生型淋巴母细胞(野生型细胞系)和从两个细胞系的基因组dna的1:1混合物中扩增,表明野生型基因组dna也含有y染色体。此实验的结果示于图7,这里清楚地显示了所有三个样品中sry的存在。总之,这些结果表明,ivs4 919g
→
a淋巴母细胞系是雄性的
[0100]
策略2:证明在g9331a处不存在bfa i限制位点
[0101]
在此策略中,在基因组dna的pcr扩增片段中g9331a处不存在bfa i限制位点,表明不存在野生型gla基因。g9331a突变破坏了存在于野生型gla基因中的bfa i切割位点(参见石井(ishii)等人美国人类遗传学杂志(am.j.hum.genet.)70:994-1002,2002)。
[0102]
从淋巴母细胞基因组dna扩增了包围ivs4 919的334-bp pcr片段,用bfa i消化,并通过琼脂糖凝胶电泳分析。在ivs4 919处的g
→
a转换型突变去除了bfa i识别位点。如果存在野生型gla,则预期有三个条带(334、122和212bp)。如果存在ivs4 919g
→
a,则预期只有一个条带(334bp)。
[0103]
结果示于图8中。如图所示,在来自对照野生型淋巴母细胞和来自两个细胞系的基因组dna的1:1混合物的样品中检测到bfa i消化。在ivs4 919g
→
a淋巴母细胞中未检测到bfa i消化,表明在这些细胞的基因组dna中没有野生型gla基因存在。
[0104]
策略3:显示表明g9331a的纯粹存在的最佳测序结果
[0105]
使用这种策略,产生最佳的测序结果,其清楚地显示了突变“a”核苷酸的纯粹存在,而没有野生型“g”的任何暗示。首先,使用基因特异性引物和高保真度聚合酶从淋巴母细胞基因组dna扩增1962bp的pcr片段。接下来,使用该1962bp片段内的内部引物扩增721bp的pcr片段。将三个pcr样品送到金唯智(genewiz)进行dna测序。结果如图9所示,表明该样品中只存在“a”,野生型样品中只存在“g”,而混合样品中“a”和“g”都存在。这表明ivs4 919g
→
a淋巴母细胞的基因组dna中不存在野生型gla基因
[0106]
总结和结论
[0107]
如以上述实例所示,在该测定中评估的和通过蛋白质印迹得到的α-gal a活性显示在g9331a淋巴母细胞中响应于dgj,α-gal a水平增加。此外,对dgj的响应大小符合“合格突变”的法布里药物遗传学参考表标准。此外,证实该响应仅仅来自从ivs4 919g
→
gla产生的α-gal a,因为这些细胞显示为雄性,并且没有从这些细胞中的基因组dna检测到野生型gla等位基因的证据。这表明具有g9331a剪接位点突变的细胞将响应于用伴侣进行的治疗,并且因此可以选择具有此基因型的法布里患者用dgj治疗。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。