1.本发明属于生物细胞培养技术领域,具体涉及一种促进胚胎样干细胞向起搏样细胞分化方法。
背景技术:
2.干细胞分化的影响因素包括外源性影响因素和内源性影响因素。其中的干细胞分化的外源性因素包括细胞间的分化诱导、细胞间的分化抑制和细胞外物质的介导作用,而另外一方面的内源性影响因素包括基因的差异表达、基因表达水平的影响和奢侈基因影响,基因的差异性表达为干细胞的不对称分裂提供了基础,干细胞可以表达特定基因来分化成其他细胞。
3.基因差异表达是指基因指导下的蛋白质合成过程,生物体生命活动中并不是所有的基因都同时表达,代谢过程中所需要的各种酶和蛋白质的基因以及构成细胞化学成分的各种编码基因,正常情况下是经常表达的,而与生物发育过程有关的基因则要在特定的反应式表达。
4.基因的不同表达水平与基因的差异化表达相合配合,利于干细胞的分化作用发挥。奢侈基因即组织特异性基因,是指不同类型细胞中特异性表达的基因,奢侈基因的产物赋予各种类型细胞特异的形态结构特征与功能。多能干细胞具有高的自我更新能力、非免疫原性和可塑性,这使它们成为再生目的的理想来源。mirnas是外泌体的主要功能成分之一,可能在细胞通讯和生物功能调节中发挥关键作用。
技术实现要素:
5.本发明的目的在于提供一种促进胚胎样干细胞向起搏样干细胞分化方法,可显著提高诱导干细胞向起搏样细胞分化的效率。
6.为达到上述目的,本发明提供一种促进胚胎样干细胞向起搏样干细胞分化方法,所述方法包括:将胚胎样干细胞做分组处理并进行培养,在培养基中加入外泌体抑制剂;提取并鉴定外泌体;所述起搏样干细胞产生外泌体 mir
‑
127
‑
5p和mirna,所述胚胎样干细胞产生外泌体nkx2.5,所述外泌体 mir
‑
127
‑
5p通过靶向调节外泌体nkx2.5促进胚胎样干细胞分化成起搏样干细胞。
7.进一步地,所述胚胎样干细胞分组包括:培养所述胚胎样干细胞;所述起搏样干细胞和胚胎样干细胞共同培养;在培养基中加入外泌体抑制剂gw4869。
8.进一步地,所述外泌体mir
‑
127
‑
5p促进所述胚胎样干细胞分化包括如下步骤:
9.利用生物信息学网站预测靶向nkx2.5的共同mirna,qpcr检测mirna的表达情况;
10.通过生物学预测mir
‑
127
‑
5p与nkx2.5的结合位点,设计荧光素酶报告基因实验证明mir
‑
127
‑
5p与nkx2.5的启动子区结合。
11.进一步地,所述nkx2.5调节胚胎样干细胞化为起搏样干细胞包括如下步骤:通过rt
‑
qpcr分析胚胎样干细胞分化成起搏样干细胞过程中不同时间节点细胞样本中nkx2.5的
表达水平;
12.构建nkx2.5敲除稳转株,qpcr、western blot、流式细胞术并检测基因表达。
13.进一步地,所述qpcr、wb检测相关mrna的表达,免疫荧光检测各组中起搏相关蛋白表达水平,检测搏动频率并验证mir
‑
127
‑
5p的过表达可抑制 nkx2.5的水平表达,进而促进胚胎样干细胞的分化。
14.进一步地,所述提取外泌体包括如下步骤:
15.培养皿的细胞汇合率达到80%时,把原有培养基吸掉,加0.25%胰蛋白酶进行消化;
16.细胞变圆后加入等体积的含正常血清培养基终止消化;
17.用移液器吹打细胞,把细胞都悬浮起来并收集,1100转/分钟,离心5分钟;
18.吸掉上清液,用无exosome血清的培养基清洗细胞一次,1100转/分钟,离心5分钟;
19.吸掉上清液,加入无exosome血清的培养基,悬浮细胞,传到培养皿中;
20.继续培养48h后,收集细胞上清,2000rpm,离心10min,然后10000转/分钟,离心30min,去除细胞或者细胞碎片,取上清。
21.进一步地,所述鉴定外泌体包括如下步骤:
22.取20
‑
40μl外泌体沉淀悬液于载样铜网上,室温下静置5min,用滤纸从侧面吸干液体滴加ph=7.0,4%磷钨酸溶液10μl于铜网上,室温负染5min;滤纸吸干负染液,白炽灯下烤干15min,负染15min后置于透射电子显微镜下观察外泌体形态并拍照;
23.将离心得到的外泌体进行径粒分布检测;
24.用pkh67对分离提取的外泌体进行标记染色。
25.本发明所达到的有益效果:
26.本发明提供的一种促进胚胎样干细胞向起搏样干细胞分化方法有助于揭示起搏细胞分化的重要理论机制,使人们更好地了解心脏起搏细胞发生过程;在实践上将有助于建立一套长期稳定高效生物起搏技术体系,为优化生物起搏器进入临床阶段提供新的策略。
附图说明:
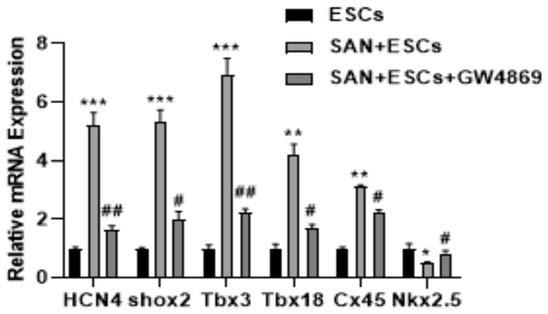
27.图1为本发明实施例提供的细胞共培养,起搏相关基因的表达示意图;
28.图2为本发明实施例提供的外泌体共培养,荧光定位示意图;
29.图3为本发明实施例提供的外泌体共培养,qpcr检测起搏相关基因的表达示意图;
30.图4为本发明实施例提供的qpcr检测外泌体相关基因的表达示意图;
31.图5为本发明实施例提供的luciferase检测不同组别的nkx2.5wt和 nkx2.5mut示意图;
32.图6为本发明实施例提供的wb检测不同组别起搏相关基因的表达示意图;
33.图7为本发明实施例提供的qpcr检测escs分化过程中nkx2.5表达示意图;
34.图8为本发明实施例提供的构建nkx2.5敲除稳转株,qpcr检测表达示意图;
35.图9为本发明实施例提供的敲降nkx2.5,qpcr检测起搏相关基因表达示意图;
36.图10为本发明实施例提供的流式检测%nkx2.5
‑
ctnt
示意图;
37.图11为本发明实施例提供的qpcr检测相关mrna的表达示意图;
38.图12为本发明实施例提供的免疫荧光检测了各组中起搏相关蛋白表达水平示意图;
39.图13为本发明实施例提供的流式检测%nkx2.5
‑
ctnt
示意图;
40.图14为本发明实施例提供的检测不同组别的搏动频率示意图。
具体实施方式
41.下面对本发明作进一步描述。以下实施例仅用于更加清楚地说明本发明的技术方案,而不能以此来限制本发明的保护范围。
42.本发明实施例提供了一种促进胚胎样干细胞向起搏样干细胞分化方法,所述方法包括:将胚胎样干细胞做分组处理并进行培养,所述胚胎样干细胞分组包括:培养所述胚胎样干细胞;所述起搏样干细胞和胚胎样干细胞共同培养;在培养基中加入外泌体抑制剂gw4869。在培养基中加入外泌体抑制剂;提取并鉴定外泌体;所述起搏样干细胞产生外泌体mir
‑
127
‑
5p和mirna,所述胚胎样干细胞产生外泌体nkx2.5,所述外泌体mir
‑
127
‑
5p通过靶向调节外泌体nkx2.5促进胚胎样干细胞分化成起搏样干细胞。
43.所述外泌体mir
‑
127
‑
5p促进所述胚胎样干细胞分化包括如下步骤:利用生物信息学网站预测靶向nkx2.5的共同mirna,qpcr检测这些mirna的表达情况;通过生物学预测mir
‑
127
‑
5p与nkx2.5的结合位点,设计荧光素酶报告基因实验证明mir
‑
127
‑
5p与nkx2.5的启动子区结合,所述qpcr、wb检测相关mrna的表达,免疫荧光检测各组中起搏相关蛋白表达水平,检测搏动频率并验证mir
‑
127
‑
5p的过表达可抑制nkx2.5的水平表达,进而促进胚胎干细胞的分化。
44.具体地,所述荧光素酶报告基因检测包括一下步骤:
45.将细胞种于24孔板中,细胞密度为105个/孔,细胞在10%fbs、1%ps 的dmem
‑
high glucose培养基中培养,细胞汇合度达到60%
‑
70%进行转染,转染前用pbs将每孔的中的双抗洗去,将正常细胞培养液换为每孔400μl的 opti
‑
mem培养基;
46.共将0.8μg质粒(0.5μg相应的报告质粒,0.3μg的β
‑
gal内参质粒),15pmol negative control/inhibitor nc/mir
‑
127
‑
5p mimic/mir
‑
127
‑
5p inhibitor 加入50μl opti
‑
mem中,2μl lipo
‑
2000加入50μl opti
‑
mem中,混匀,静置 5min后两者轻轻混匀,再静置20min之后加入24孔板中,每孔100μl,摇匀;
47.设置温度37℃、5%co2培养4
‑
6h,将opti
‑
mem i换成含有2%fbs、1% ps的培养基400μl,以每孔计,37℃、5%co2培养24h或48h,每组做三个复孔。
48.进行luciferase质粒与β
‑
gal质粒测定48h后,将每个孔中的培养基吸尽,并用pbs洗一遍,每孔加入50μl 1
×
cell culture lysis reagent,剧烈震荡,之后将每孔裂解的细胞分别加到200μl离心管中,用液氮冻融3次,离心速度 10,000g,5min离心,细胞碎片沉在底部;从每个离心管中取20μl的上清液加入不同的1.5ml离心管中,加入80μl荧光蛋白底物,短暂振荡后进行检测,测三次,记录荧光值最高的读数。另外从200μl离心管分别取10μl上清液分别置于不同的1.5ml离心管中,每管加入1μl 100
×
mg2 溶液、22μl 1
×ꢀ
onpg溶液、67μl 0.1m磷酸钠溶液,振荡混匀后,置于37℃水浴,30min 后每孔加入167μl 1m碳酸钠溶液终止反应,混匀后取150μl加入96孔板中,使用酶标仪测定420nm下的吸光度。
49.具体地,所述wb检测相关蛋白的表达的验证处理,包括如下步骤:
50.提取蛋白,收集胚胎干细胞,加入ripa裂解液(加入蛋白酶抑制剂和磷酸酶抑制剂,按照100:1的比例)反复吹打,冰浴裂解30min。裂解完成后 12000g,4℃离心10min。将上清转移至新的1.5ml离心管中;
51.采用bca蛋白浓度测定试剂盒进行蛋白定量,严格按照其说明书要求测量总蛋白的浓度:制备标准蛋白,浓度分别为0μg/ml、25μg/ml、125μg/ml、 250μg/ml/、500μg/ml、750μg/ml、1000μg/ml、1500μg/ml、2000μg/ml,通过制备标准曲线来检测样品蛋白的浓度;
52.将标准蛋白及样品蛋白加入酶标板,每孔25μl;配制bca液,先配制a 液,所述a液等于1
×
n,所述b液等于50
×
n,其中,n为待测样品蛋白的数量,将配好的混合液加入蛋白所在孔中,每孔200μl,震荡30秒以充分混合,将微孔板密封,37℃下孵育30分钟;
53.微孔板冷却到室温后,用酶标仪测定波长562nm下的od值,得到标准曲线,根据标准曲线计算待测蛋白样品的浓度;
54.根据各样本蛋白浓度,计算各样品相同蛋白量所需体积。蛋白样品中加入10
×
loading buffer,于变性仪95℃下变性10min,室温下冷却后上样进行 sds
‑
page电泳,电压为80v,30min,120v,1h;
55.电泳后进行湿转转膜,恒定电流300ma转膜1~2h;
56.转膜后将其置于5%脱脂奶的tbst封闭液室温摇床上封闭1h,1
×
tbst洗涤3
×
5min;
57.加入特异性一抗4℃冰箱中过夜孵育,摇床上摇30min,1
×
tbst洗涤 3
×
5min,再加入相应的二抗室温孵育1h,1
×
tbst洗涤3
×
5min;
58.化学发光,显影处理。
59.具体地,所述提取外泌体包括如下步骤:
60.培养皿的细胞汇合率达到80%时;把原有培养基吸掉,加适当的0.25%胰蛋白酶进行消化;
61.细胞变圆后加入等体积的含正常血清培养基终止消化;
62.用移液器吹打细胞,把细胞都悬浮起来,收集,1100rpm,离心5分钟;
63.吸掉上清液,用无exosome血清的培养基清洗细胞一次,1100rpm,离心5分钟;
64.吸掉上清液,加入无exosome血清的培养基,悬浮细胞,传到培养皿中;
65.继续培养48h后,收集细胞上清,2000rpm,离心10min,然后10000rpm,离心30min,去除细胞或者细胞碎片,取上清即可。
66.具体地,所述鉴定外泌体包括如下步骤:
67.取20
‑
40μl外泌体沉淀悬液于载样铜网上,室温下静置5min,用滤纸从侧面吸干液体滴加ph=7.0,4%磷钨酸溶液约10μl于铜网上,室温负染5min。滤纸吸干负染液,白炽灯下烤干约15min,负染15min后置于透射电子显微镜下观察外泌体形态并拍照;
68.将离心分离得到的外泌体用1ml过滤后的pbs稀释,并用注射器将上述稀释得到的样品注射至仪器的检测槽中,并注意不要留有气泡,待仪器自动读数,然后记录并生成报告。过滤的pbs用作对照。仪器的设置条件为:温度23.75
±
0.5℃,采集频率25帧/秒,测量时间60秒。
69.用pkh67 fluorescent cell linker kits(sigma)对分离提取的外泌体进行标记染色,即50μl外泌体悬液中加250μl diluent c液再加1.5μl dye染液,室温染色10分钟;
70.随后加入3%的过氧化氢室温避光25分钟,以阻断内源性的过氧化物酶;
71.用invitrogen公司的exosome spin columns(mw3000)纯化外泌体,去除未结合的染料;
72.用完全培养基重悬稀释标记后的外泌体,加入到细胞培养上清中;
73.培养24h后固定、破膜、染核,激光共聚焦显微镜观察。
74.如图1所示:qpcr分析san细胞与escs细胞共培养时起搏相关基因的表达结果发现,与escs组相比,san escs组hcn4,shox2,tbx3,tbx18及cx45的mrna表达量显著增高,nkx2.5的mrna表达水平降低;在san escs 中加入外泌体抑制剂sw4896后hcn4,shox2,tbx3,tbx18及cx45的mrna 表达量降低,nkx2.5的mrna表达水平升高,暗示san细胞促进胚胎干细胞分化为起搏样细胞的,在这一过程中可能是san细胞外泌体在起作用。
75.pkh67标记的san的外泌体悬液与escs共培养,进行荧光定位,实验结果如图2所示:pkh67标记外泌体呈绿色,dapi标记细胞核呈蓝色,在激光共聚焦显微镜下观察到外泌体被escs细胞摄取。
76.如图3所示,为了探索san外泌体在胚胎干细胞分化成起搏样细胞中的作用,qpcr检测san外泌体及293t细胞外泌体分别与escs共培养时,起搏相关基因hcn4,shox2,tbx3,tbx18,cx45及nkx2.5的mrna水平表达,结果如图5所示:与293t exosome escs组相比,san exosome escs组hcn4, shox2,tbx3,tbx18及cx45的mrna表达量增高显著,nkx2.5的mrna表达水平降低。以上数据暗示san外泌体可以促进胚胎干细胞分化成起搏样细胞。
77.我们利用生物信息学网站mirwalk及targetscan预测靶向nkx2.5的共同 mirna共有13个,如图4所示,我们从来自293t及san的exos中分离出rna, qpcr检测这些mirna的表达情况。结果如图4所示,与293t exosome组相比,san exosome组中有三个mirna表达发生显著上调,分别是mir
‑
127
‑
5p,mir
‑
216a
‑
3p及mir
‑
139
‑
3p,其中mir
‑
127
‑
5p上调最为显著。与293t exosome 组相比,san exosome组mir
‑
1965
‑
5p、mir
‑
377
‑
5p、mir
‑
125b
‑2‑
3p、mir
‑
1188
‑
5p、 mir
‑
344a
‑
5p、mir
‑
3594
‑
5p、mir
‑
6328、mir
‑
328a
‑
3p、mir
‑
328b
‑
3p、mir
‑
874
‑
3p 的mrna表达量均无显著性差异。因为猜测可能是sam外泌体中的mir
‑
127
‑
5p 通过靶向调节nkx2.5影响胚胎干细胞分化成起搏样细胞。
78.通过生物学预测预测mir
‑
127
‑
5p与nkx2.5的结合位点,进一步设计荧光素酶报告基因实验证明mir
‑
127
‑
5p是否可以与nkx2.5的启动子区结合。如图 5所示,荧光素报告基因检测结果显示,nkx2.5
‑
wt组在mir
‑
127
‑
5p过表达的影响下荧光素酶活性下降,mir
‑
127
‑
5p抑制的情况下荧光素酶活性升高;而突变型mkx2
‑5‑
mut组(突变了mir
‑
127
‑
5p可以与nkx2.5的结合位点),过表达或抑制mir
‑
127
‑
5p荧光素酶信号没有显著性变化,说明mir
‑
127
‑
5p可以靶向调节nkx2.5并发挥作用。
79.如图6所示,为了探索mir
‑
127
‑
5p在胚胎干细胞分化成起搏样细胞中的作用,western blot检测不同组别起搏相关蛋白表达量,结果如图6所示,与 nc mimic组相比,mir
‑
127
‑
5p mimic组hcn4的蛋白表达量无显著性差异。与 nc mimic组相比,mir
‑
127
‑
5p mimic组hcn4,shox2,tbx3,tbx18及cx45 的蛋白表达量显著增高,nkx2.5的蛋白表达量显著降低。
80.为了探索nkx2.5在胚胎干细胞分化成起搏样细胞中的作用,通过rt
‑
qpcr 分析胚胎干细胞分化成起搏样细胞过程中不同时间节点细胞样本中nkx2.5的表达水平,如图7所
示,发现随着胚胎干细胞分化的进行nkx2.5的表达降低。以上结果暗示nkx2.5可能在胚胎干细胞分化为起搏样细胞的过程中发挥作用。
81.如图8所示中,为了探索nkx2.5在胚胎干细胞分化成起搏样细胞中的作用,首先通过细胞转染实验敲降nkx2.5。构建nkx2.5敲除稳转株,qpcr检测表达,结果如图8所示。与nc shrna组相比,nkx2.5 shrna
‑
1组nkx2.5的 mrna表达量显著降低(***p<0.001);与nc shrna组相比,nkx2.5 shrna
‑
2 组nkx2.5的mrna表达量显著降低(**p<0.01);与nc shrna组相比,nkx2.5 shrna
‑
3组nkx2.5的mrna表达量显著降低(**p<0.01)。说明nkx2.5 shrna
‑
1 转染效率最佳,后续选择该质粒进行后续实验。
82.如图9所示,为了探索nkx2.5在胚胎干细胞分化成起搏样细胞中的作用, rt
‑
qpcr通过检测起搏相关基因hcn4,shox2,tbx3,tbx18,cx45及nkx2.5 的mrna水平表达,验证敲降nkx2.5对胚胎干细胞分化成起搏样细胞的影响。发现敲降nkx2.5会促进胚胎干细胞分化成起搏样细胞。
83.为确定nkx2.5对在胚胎干细胞分化为起博样细胞的影响,在胚胎干细胞中敲降nkx2.5流式细胞术检测不同时间点心肌形成转录因子nkx2.5阴性和心肌肌钙蛋白t(ctnt)阳性细胞占比,结果如10图所示,发现随着时间延长,其比例增加。
84.如图11所示,为了进一步说明mir
‑
127
‑
5p和nkx2.5在胚胎干细胞的分化过程中的作用,我们设置了nc mimics pc ctrl组,mir
‑
127
‑
5p mimics pc ctrl 组,mir
‑
127
‑
5p mimics pc nkx2.5。首先我们用rt
‑
qpcr检测了各组mir
‑
127
‑
5p 及nkx2.5的表达水平,发现过表达mir
‑
127
‑
5p,mir
‑
127
‑
5p的表达水平显著升高,nkx2.5的水平显著下调;在过表达mir
‑
127
‑
5p的基础上进一步过表达 nkx2.5的表达,mir
‑
127
‑
5p的表达与mir
‑
127
‑
5p mimic pc ctrl组相比无显著变化,nkx2.5 mrna表达量恢复到nc mimics pc ctrl组。以上结果说明nkx2.5 的表达水平受mir
‑
127
‑
5p的调控。进一步地,我们也检测了各组hcn4,shox2, tbx3,tbx18及cx45的转录水平,发现过表达mir
‑
127
‑
5p时,hcn4,shox2, tbx3,tbx18及cx45mrna表达量显著提高,而在过表达mir
‑
127
‑
5p的基础上进一步过表达nkx2.5,hcn4,shox2,tbx3,tbx18及cx45mrna表达量恢复到nc组的水平。以上结果说明mir
‑
127
‑
5p的过表达可抑制nkx2.5的转录水平表达,进而促进胚胎干细胞的分化。
85.免疫荧光检测了各组中起搏相关蛋白表达水平,结果如图12所示。发现过表达mir
‑
127
‑
5p,nkx2.5的蛋白水平显著下调;在过表达mir
‑
127
‑
5p的基础上进一步过表达nkx2.5的表达,nkx2.5蛋白表达量恢复到nc mimics pc ctrl 组;过表达mir
‑
127
‑
5p后hcn4,shox2,tbx3,tbx18及cx45的蛋白水平升高,在过表达mir
‑
127
‑
5p的基础上进一步过表达nkx2.5的表达,hcn4,shox2, tbx3,tbx18及cx45的蛋白水平回落。说明mir
‑
127
‑
5p的过表达可抑制nkx2.5 的蛋白水平表达,进而促进胚胎干细胞的分化。
86.在图13所示中,流式检测%nkx2.5
‑
ctnt
。与nc minics pc ctrl组相比, mir
‑
127
‑
5p minics pc ctrl组%nkx2.5
‑
ctnt
显著增高;与mir
‑
127
‑
5p minics pcctrl组相比,mir
‑
127
‑
5p minics pc nkx2.5组%nkx2.5
‑
ctnt
显著降低。
87.检测搏动频率的结果如图14所示,与nc minics pc ctrl组相比,mir
‑
127
‑
5pminics pc ctrl组搏动频率显著增高;与mir
‑
127
‑
5p minics pc ctrl组相比, mir
‑
127
‑
5p minics pc nkx2.5组搏动频率显著降低。以上结果说明mir
‑
127
‑
5p 的过表达可抑制nkx2.5的水平表达,进而促进胚胎干细胞的分化。
88.本发明实施例所提供的一种促进胚胎样干细胞向起搏样干细胞分化方法有助于揭示起搏细胞分化的重要理论机制,使人们更好地了解心脏起搏细胞发生过程;在实践上将有助于建立一套长期稳定高效生物起搏技术体系,为优化生物起搏器进入临床阶段提供新的策略。
89.以上所述仅为本发明的优选实例而已,并不用于限制本发明,尽管参照前述实施例对本发明进行了详细的说明,对于本领域的技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。