1.本发明涉及多肽制备技术领域,尤其涉及普卡那肽的制备方法。
背景技术:
2.蛋白质和多肽类药物具有作用位点专一,疗效明确等优点,近年来,蛋白质和多肽类药物的研究和发展已经成为生物医药领域研究的一个热点。二硫键是蛋白质或多肽分子中位于不同肽链或同一肽链的两个不同位点cys的巯基(-sh)被氧化形成的s-s共价键。它可以将肽链折叠成特定的空间结构,在维持多肽和蛋白质的空间立体结构及由此决定的生物活性中发挥着重要的作用。二硫键数目越多,蛋白质分子对抗外界因素影响的稳定性就愈大。
3.普卡那肽(plecanatide)就是含有两对二硫键的多肽药物,它是由16个l-型氨基酸残基组成,其中cys4、cys
12
及cys7、cys
15
分别由二硫键相连。其肽序如下:
4.h-asn-asp-glu-cys
4-glu-leu-cys
7-val-asn-val-ala-cys
12-thr-gly-cys
15-leu-oh(其中cys4、cys
12
,cys7、cys
15
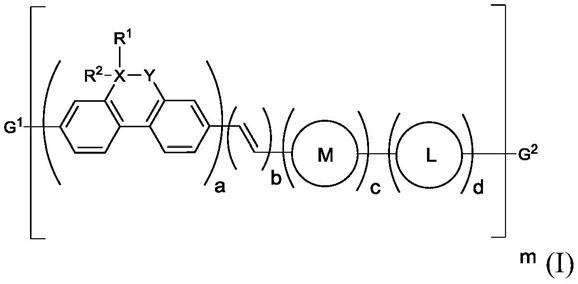
分别由二硫键相连),其结构式如式i:
[0005][0006]
普卡那肽是一种鸟苷酸环化酶c(gc-c)受体激动剂,其商品名为trulance。其为尿鸟苷蛋白(uroguanylin)的类似物,在肠道中,鸟苷肽和尿鸟苷素充当体液和电解质平衡的调节剂。这些肽释放进入肠腔,在肠腔中它们结合至定位于肠细胞(小肠和结肠的单层柱状上皮细胞)的管腔膜上的鸟苷酸环化酶c。鸟苷肽与鸟苷酸环化酶c的结合经由环单磷酸鸟苷(cgmp)的增加引发的复杂细胞内信号传递级联而诱导电解质和水排泄进入肠腔,从而增加胃肠动力,从而治疗成人慢性特发性便秘。于2017年01月19日获得美国食品和药物监督管理局(fda)的批准上市。
[0007]
cn 103764672 a、cn 105764916 a及cn 107090016 a均为原研公司申请专利。主要介绍的是固液相结合的片段缩合方法来合成普卡那肽的方法。将普卡那肽的16个残基分成a、b、c三个片段,先利用fmoc/tbu固相多肽合成方法合成得到:a(boc-aa
1-aa
6-oh)、b(fmoc-aa
7-aa
14-oh)的全保护肽片段,在液相中合成片段c(h-aa
15-aa1
6-otbu),然后液相中连接片段b及c后脱去n末端的fmoc保护基,再与片段a连接。合成完成后得到的全保护肽经裂解后再进行二硫键的环化即得到普卡那肽的粗肽。
[0008]
cn103694320 a及cn104211777 a均为已授权申请专利,主要关于普卡那肽固液相结合定位成两对二硫键的不同方法的介绍。cn103694320a介绍的是采用tbu及acm分别作为两对二硫键上巯基的保护基团,通过h2o2及i2分别氧化形成两对二硫键的方法。cn104211777 a则是采用stbu、acm、mmt、trt四种中的任意两种作为普卡那肽两对二硫键上巯基的保护基团,通过不同的氧化方法成第一对及第二对二硫键。
[0009]
cn104628827 a介绍了一种全固相合成定位成两对二硫键的方法,此专利与前两篇专利最大的不同点在于第一对二硫键的cys(cys4、cys
12
)巯基保护基团选择的是stbu及mmt,而第二对二硫键的cys(cys7、cys
15
)巯基保护基团则是acm。前期肽树脂合成完成后首先在固相上用巯基乙醇脱除stbu,然后加入dtnp与裸露出的巯基反应,然后用一定浓度的tfa脱除mmt,同时进行第一对二硫键(cys4、cys
12
)的环化,而第二对二硫键(cys7、cys
15
)的环化则采用i2氧化。这样即在固相上完成的两对二硫键的氧化。
技术实现要素:
[0010]
有鉴于此,本发明要解决的技术问题在于提供普卡那肽的制备方法,以其降低拓扑杂质的含量。
[0011]
本发明提供了一种可溶性片段肽树脂,其结构为:mmsb-[lys(boc)]
n-树脂;
[0012]
其中,n=2~10;所述树脂为wang树脂、rink树脂或2ctc树脂。
[0013]
本发明提供的可溶性片段在肽序的c端引入可溶性片段,通过连接臂与肽序相连。能大幅降低二硫键环化后的拓扑杂质的占比,同时由于c端可溶性片段的引入,肽树脂在偶联过程中树脂的溶胀性增大,一定程度上降低了肽序在偶联过程中的难度,提高线性粗肽的纯度,从而提高收率。其中,mmsb(cas:1234793-64-6,其结构如式i)作为linker将肽序列与可溶性的片段连接。
[0014][0015]
本发明提供的可溶性片段肽树脂中,lys可以被peg、arg、asn、gly、pro、gln、glu、asp替换。例如,所述可溶性片段肽树脂为:
[0016]
mmsb-[lys(boc)]
n-wang树脂、mmsb-[lys(boc)]
n-rink树脂、mmsb-[lys(boc)]
n-2ctc树脂、mmsb-[peg]
n-wang树脂、mmsb-[peg]
n-rink树脂、mmsb-[peg]
n-2ctc树脂、mmsb-[arg(pbf)]
n-wang树脂、mmsb-[arg(pbf)]
n-rink树脂、mmsb-[arg(pbf)]
n-2ctc树脂、mmsb-[asn(trt)]
n-wang树脂、mmsb-[asn(trt)]
n-rink树脂、mmsb-[asn(trt)]
n-2ctc树脂、mmsb-[gly]
n-wang树脂、mmsb-[gly]
n-rink树脂、mmsb-[gly]
n-2ctc树脂、mmsb-[pro]
n-wang树脂、mmsb-[pro]
n-rink树脂、mmsb-[pro]
n-2ctc树脂、mmsb-[gln(trt)]
n-wang树脂、mmsb-[gln(trt)]
n-rink树脂、mmsb-[gln(trt)]
n-2ctc树脂、mmsb-[glu(otbu)]
n-wang树脂、mmsb-[glu(otbu)]
n-rink树脂、mmsb-[glu(otbu)]
n-2ctc树脂、mmsb-[asp(otbu)]
n-wang树脂或mmsb-[asp(otbu)]
n-rink树脂、mmsb-[asp(otbu)]
n-2ctc树脂;
[0017]
其中,n=2~10。例如,n可为2、3、4、5、6、7、8、9、10。作为优选,n=2~4。前期验证结果表明,采用lys对于降低普卡那肽拓扑杂质含量更有效。因此,本发明实施例中,所述可溶性片段肽树脂为mmsb-lys(boc)-lys(boc)-rinkresin。
[0018]
本发明中,可溶性片段肽树脂按fmoc/tbu固相合成策略合成。具体的,所述可溶性片段肽树脂的制备方法包括:
[0019]
树脂与fmoc-lys(boc)-oh偶联,制备h-[lys(boc)]
n-树脂;然后与mmsb偶联,制备
mmsb-[lys(boc)]
n-树脂;
[0020]
其中,n=2~10;所述树脂为wang树脂、rink树脂或2ctc树脂。
[0021]
本发明中,所述树脂的替代度为0.2~1.0mmol/g。优选的,树脂的替代度为0.3~0.5mmol/g。
[0022]
所述可溶性片段肽树脂的制备方法中,所述偶联的溶剂选自四氢呋喃、二甲基亚砜、二甲基甲酰胺、二恶烷、丙酮、乙醚、乙腈、四氯化碳、二硫化碳、苯、甲苯、己烷、氯仿、二氯甲烷中至少一种。一些实施例中,所述溶剂为二甲基甲酰胺与二氯甲烷的混合溶液;作为优选,溶剂中二甲基甲酰胺与二氯甲烷的体积比为1:1。
[0023]
所述可溶性片段肽树脂的制备方法中,所述偶联的偶联剂为dipcdi和化合物a的组合物或dipea和化合物a和化合物b的组合物,其中化合物a为hoat或hobt,化合物b为pyaop、pybop、hatu、hbtu或tbtu,优选为dipcdi和化合物a的组合物。一些实施例中,所述偶联的偶联剂为hobt和dipcdi。其中,保护氨基酸(lys)的比例以摩尔比计为dipcdi:a:lys=1.3:1.2:1.0,dipea:a:b:lys=2.0:1.2:1.0:1.0。
[0024]
所述可溶性片段肽树脂的制备方法中,偶联反应的温度为室温,例如20℃
±
5℃。反应时间为1.5~4小时,优选2~3小时。
[0025]
一些具体实施例中,所述可溶性片段的连接采用固相多肽合成策略包括(以优选树脂为例):1)将树脂用溶剂在固相反应柱中进行溶胀,所选溶剂包括dmf、nmp、二氯甲烷等,优选dmf;2)用20%的哌啶/dmf溶液的脱除fmoc保护基,用溶剂反复洗涤树脂;3)将合适量的待偶联氨基酸和偶联剂在溶剂中溶解并活化后,一起加入到固相反应柱中,直至用茚三酮检测方法检测到反应终止为止;4)重复2)和3)。
[0026]
普卡那肽的制备方法,其包括:
[0027]
步骤1:根据普卡那肽的肽序,在mmsb-[lys(boc)]
n-树脂的c端依次偶联各保护氨基酸残基,制备普卡那肽树脂;
[0028]
步骤2:使cys4与cys
12
形成二硫键、cys7与cys
15
形成二硫键;
[0029]
步骤3:脱除树脂和mmsb-[lys(boc)]
n
,获得普卡那肽粗肽;
[0030]
其中,n=2~10;所述树脂为wang树脂、rink树脂或2ctc树脂。
[0031]
所述普卡那肽的制备方法中,所述依次偶联的氨基酸原料为:fmoc-leu-oh、fmoc-cys(mmt)-oh、fmoc-gly-oh、fmoc-thr(tbu)-oh、fmoc-cys(acm)-oh、fmoc-ala-oh、fmoc-val-oh、fmoc-asn(trt)-oh、fmoc-val-oh、fmoc-cys(mmt)-oh、fmoc-leu-oh、fmoc-glu(otbu)-oh、fmoc-cys(acm)-oh、fmoc-glu(otbu)-oh、fmoc-asp(otbu)-oh、fmoc-asn(trt)-oh。
[0032]
本发明所述的普卡那肽制备方法中,引入本发明所述的可溶性片段肽树脂。在可溶性片段后偶联mmsb-h作为linker,随后依次偶联各残基。其中cys7、cys
15
及cys4、cys
12
两组cys残基采用mmt或trt与acm正交保护。肽树脂偶联完成后,采用一定浓度的tfa脱除mmt或trt保护基团,然后采用h2o2先进行固相氧化成第一对二硫键;然后继续采用一定当量的i2进行第二对二硫键的氧化。肽树脂经收缩干燥后裂解,粗肽经乙醚沉淀及洗涤后真空干燥得到目的肽粗品,经hplc纯化后得到精肽。采用本方法后使普卡那肽两对二硫键环化完成后拓扑杂质的占比由20%以上降低至3%左右,得到的环化后的普卡那肽粗品的纯度一般在75%以上,纯化后精肽的收率>40%。同时整个操作过程全部在固相完成,操作简单可
行。
[0033]
一些具体实施例中,所述普卡那肽树脂的制备过程中,氨基酸的偶联步骤主要包括:将树脂用溶剂在固相反应柱中进行溶胀,所选溶剂包括dmf、nmp、二氯甲烷等,优选dmf;2)用20%的哌啶/dmf溶液的脱除fmoc保护基,用溶剂反复洗涤树脂;3)将合适量的待偶联氨基酸和偶联剂在溶剂中溶解并活化后,一起加入到固相反应柱中,直至用茚三酮检测方法检测到反应终止为止;4)重复2)和3)。
[0034]
因fmoc-leu-oh与mmsb-[lys(boc)]
n-树脂的偶联发生的是酯化反应,因此,选择添加dmap促进反应的进程。dmap的摩尔比是树脂合成规模的0.1~0.2。
[0035]
所述普卡那肽的制备方法中,所述fmoc-leu-oh与mmsb-[lys(boc)]
n-树脂偶联的步骤中,偶联剂为dipcdi、hobt和dmap;
[0036]
其他氨基酸的偶联步骤中,偶联剂为dipcdi和化合物a的组合物或dipea、化合物a和化合物b的组合物;其中,化合物a为hoat或hobt,化合物b为pyaop、pybop、hatu、hbtu或tbtu。一些实施例中,偶联氨基酸的偶联剂为dipcdi和化合物a的组合物。一些具体实施例中,偶联剂中各成分与保护氨基酸(aa)的比例以摩尔比计为dipcdi:a:aa=1.3:1.2:1.0,dipea:a:b:aa=2.0:1.2:1.0:1.0。所述普卡那肽的制备方法中,偶联反应的温度为室温,例如20℃
±
5℃。反应时间为1.5~4小时,优选2~3小时。
[0037]
所述普卡那肽的制备方法中,在步骤2与步骤1之间,还包括脱除cys残基的mmt保护基的步骤;所述脱除mmt保护基的试剂为tfa、tis和dcm的组合物。一些实施例中,tfa:tis:dcm的体积比为(1~5):(2~10):(97~85)。一些具体实施例中,tfa:tis:dcm的体积比为2:5:93。脱除mmt保护的条件为室温反应15~30次,每次1~5min。一些具体实施例中,脱除mmt保护的条件为室温反应20次,每次2min。
[0038]
所述普卡那肽的制备方法中,使所述cys4与cys
12
形成二硫键的氧化剂为h2o2;使所述cys7与cys
15
形成二硫键的氧化剂为i2。
[0039]
所述cys4与cys
12
形成二硫键的步骤中,溶剂选自四氢呋喃、二甲基亚砜、二甲基甲酰胺、二恶烷、丙酮、乙醚、乙腈、四氯化碳、二硫化碳、苯、甲苯、己烷、氯仿、二氯甲烷。优选的,溶剂为二甲基甲酰胺。h2o2与树脂的当量比为(1~30):1,优选为10:1。具体的,该步骤包括:1~30当量的h2o2与树脂反应0.5~3小时,优选10当量反应1小时。反应结束后,以0.1~0.2mmol/l的dtnb溶液在碱性环境下检测,若树脂无色则表示二硫键环合完成,然后以反应溶剂对树脂进行洗涤再进行cys7与cys
15
之间二硫键的键合。
[0040]
所述cys7与cys
15
形成二硫键的步骤中,溶剂选自四氢呋喃、二甲基亚砜、二甲基甲酰胺、二恶烷、丙酮、乙醚、乙腈、四氯化碳、二硫化碳、苯、甲苯、己烷、氯仿、二氯甲烷。优选的,溶剂为二甲基甲酰胺。i2与树脂的当量比为(0.8~10):1,优选为3:1。具体的,该步骤包括:0.8~10当量的i2与树脂反应0.5~3小时,优选3当量反应1小时。反应完成后经洗涤、收缩得到肽树脂。
[0041]
所述普卡那肽的制备方法中,所述脱除树脂的裂解液选自tfa、h2o、tis、苯甲醚、苯甲硫醚、苯酚中至少一种。本发明实施例中,所述脱除树脂的试剂为tfa、tis和水的组合物。一些实施例中,所述裂解液中tfa:tis:h2o的体积比为(80~90):(0~10):(0~10),一些具体实施例中,所述裂解液中tfa:tis:h2o的体积比为92:4:4。裂解步骤中,所述树脂与裂解液的质量体积比为1g:10ml。脱除树脂的反应温度为室温,优选为20℃
±
5℃,反应时间
为2~5h,优选的,反应时间为3h。
[0042]
所述脱除mmsb-[lys(boc)]
n
的试剂为nh4i和dms,其中nh4i和dms的摩尔比为1:1。nh4i及dms的用量均为合成规模的20倍。
[0043]
本发明中,脱除mmsb-[lys(boc)]
n
后,产物用乙醚或甲基叔丁基醚沉淀,获得普卡那肽粗肽。实施例中,采用乙醚沉淀粗肽,沉淀后还包括用无水乙醚洗涤沉淀的步骤。
[0044]
所述普卡那肽的制备方法中,所述还包括对普卡那肽粗肽纯化的步骤;所述纯化采用反相高压液相色谱法。
[0045]
所述普卡那肽的制备方法中,所述反相高压液相色谱法的固定相为反相十八烷基硅烷,流动相中,a相为0.1%三氟乙酸水溶液b相为乙腈。
[0046]
本发明利用可溶性片段肽树脂:mmsb-[lys(boc)]
n-树脂在肽序的c端引入可溶性片段,通过连接臂依次偶联各保护的氨基酸残基,然后固相中进行两对二硫键的环化,得到的肽树脂裂解后的滤液与nh4i及dms反应断开可溶性片段后经乙醚沉淀获得粗肽,后经反相色谱制备得到精肽。由于可溶性片段的存在改变了环化时的肽序列结构,使环化后产生的拓扑杂质的占比大大降低,大幅提高了环化后粗肽的纯度,同时由于c端可溶性片段的引入,一定程度上增强了偶联过程中肽树脂的溶胀性,使后续氨基酸残基偶联难度降低,提高终产物的收率。
附图说明
[0047]
图1示本发明中plecanatide合成方法;
[0048]
图2示实施例4制得可溶性片段得的粗肽色谱图;
[0049]
图3示实施例5制得可溶性片段得的精肽色谱图;
[0050]
图4示实施例5制得精肽质谱图(mw:1681.95)。
具体实施方式
[0051]
本发明提供了普卡那肽的制备方法,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
[0052]
本发明采用的试材皆为普通市售品,皆可于市场购得。
[0053]
文中涉及物质名称及缩写如表1:
[0054]
表1物质名称及缩写
[0055][0056]
下面结合实施例,进一步阐述本发明:
[0057]
实施例1:可溶性片段肽树脂(mmsb-(lys)2-rink树脂)的制备
[0058]
称取替代度为0.32mmol/g的rinkamide树脂31.3g(10mmol)于固相反应柱中,用dmf洗涤2次后用dmf溶胀树脂30分钟,然后用150ml的dblk脱保护5min 7min,后用150ml的dmf洗涤6次。称取14.1g(30mmol)fmoc-lys(boc)-oh和4.1g(36mmol)hobt用100ml的dmf溶解后加入5.1ml(39mmol)dipcdi活化2-3min后,将混合液加入到反应柱中,室温反应2小时,以茚三酮检测反应终点(如树脂无色透明则终止反应;如树脂显色则延长反应0.5-1小时)。反应结束,用150ml的dmf洗涤树脂3次,加入150ml的dblk脱保护5min 7min,150ml的dmf洗
涤树脂6次,茚三酮检测树脂有颜色。重复上述偶联操作,继续偶联1组fmoc-lys(boc)-oh。其投料为30mmol,其它物料投料比与保护氨基酸对应。偶联、洗涤、脱保护、洗涤完成后继续偶联mmsb,偶联操作步骤同上,物料如下:mmsb,7.3g(30mmol);4.1g(36mmol)hobt;5.1ml(39mmol)dipcdi。室温反应2小时后洗涤5次完成可溶性片段肽树脂(mmsb-lys(boc)-lys(boc)-rinkresin)的合成。
[0059]
实施例2:全保护肽树脂的制备
[0060]
称取7.1gfmoc-leu-oh(20mmol)、3.2g(24mmol)hobt、0.3g(2mmol)dmap溶于120ml体积比为1:1的dcm和dmf混合溶液,于冰盐水浴中搅拌,控制温度0-10℃时滴加加入3.4ml(26mmol)dipcdi后活化2-3min,将上述溶液加入固相反应柱中室温反应2-3h。反应结束后用dmf洗涤4次后加入70ml醋酸酐和60ml吡啶及适量dmf,混合封闭反应8小时以上。反应结束后用dmf洗涤5次后用150ml的dblk脱保护5min 7min,150mldmf洗涤6次。称取30.8g(50mmol)fmoc-cys(mmt)-oh和8.1g(60mmol)hobt用100ml的dmf/dcm(1:1)溶解,冰水浴下加入10ml(65mmol)dipcdi活化2-3min后,将混合液加入到反应柱中,室温反应2小时,以茚三酮检测反应终点(如树脂无色透明则终止反应;如树脂显色则延长反应1小时)。反应结束,用150mldmf洗涤树脂3次,加入150mldblk脱保护5min 7min,150mldmf洗涤树脂6次,茚三酮检测树脂有颜色。重复上述偶联操作,按照上步骤2中所述按肽序列顺序继续依次偶联fmoc-gly-oh、fmoc-thr(tbu)-oh、fmoc-cys(acm)-oh、fmoc-ala-oh、fmoc-val-oh、fmoc-asn(trt)-oh、fmoc-val-oh、fmoc-cys(mmt)-oh、fmoc-leu-oh、fmoc-glu(otbu)-oh、fmoc-cys(acm)-oh、fmoc-glu(otbu)-oh、fmoc-asp(otbu)-oh、fmoc-asn(trt)-oh。各保护氨基酸均投料50mmol,其它物料投料比与保护氨基酸对应。
[0061]
实施例3:全保护肽树脂的固相氧化
[0062]
脱fmoc保护结束dmf洗涤树脂6次后,肽树脂继续用dcm洗涤3次并抽干,然后采用tfa:tis:dcm=2:5:93、反应次数为10次及每次5分钟来对肽树脂进行脱mmt处理,结束后树脂用dmf洗涤6次。量取30%的双氧水5.1ml(50mmol)及0.5-1ml的dipea加入到150ml的dmf中,加入到固相反应柱中与树脂进行第一对二硫键的键合反应,鼓气反应1h,反应完毕后继续dmf洗涤6次后进行第二对二硫键的键合。称取7.6g(30mmol)的i2溶解于150ml的dmf后加入反应柱中。反应时间为1h。反应完成后用150ml的dblk脱保护5min 7min,150mldmf洗涤5次后dcm洗涤2次,然后用150ml甲醇收缩树脂2次,每次5min,减压抽干肽树脂,最终得到肽树脂72.5克。
[0063]
实施例4:肽树脂的裂解
[0064]
将实施例3中得到的72.5g肽树脂置于1000ml圆底烧瓶中,以10ml/g肽树脂的比例加入730ml的裂解试剂(tfa:tis:h2o=92:4:4(v/v)),室温搅拌2h。反应物用砂芯漏斗过滤,过滤结束后加入少量tfa洗涤树脂。反应结束后过滤,将得到的滤液加入加入nh4i(200mmol)及dms(200mmol)继续搅拌反应30min。反应完成后将反应液加入冰冻的无水乙醚(100ml/g肽树脂)沉淀1-4h,然后离心、去除上清液后将沉淀用无水乙醚洗涤3次,真空干燥得到类白色固体粉末的粗肽17.5g。粗肽纯度为81.3%,拓扑杂质:3.5%(如图2,hplc检测条件:waters、c18 150
×
4.6mm、缓冲液:50mm磷酸铵缓冲液(磷酸调ph=6.2);a相:乙腈:缓冲液=10:90(v:v);b相:缓冲液=50:50(v:v)、梯度:5-45%(20min)/45.1-95%(10min);流速:0.4ml/min检测波长:220nm。下同)。
[0065]
实施例5:普卡那肽的制备
[0066]
将实施例3中获得的17.5g粗肽经以十八烷基硅烷为固定相,以0.1%三氟乙酸水溶液/乙腈为流动相进行反相液相制备纯化,收集目的峰馏分,浓缩冻干。得到精肽7.6g,纯度98.9%,收率45.2%(图3~4)。
[0067]
对比例1:肽树脂的制备
[0068]
称取替代度为0.35mmol/g的fmoc-leu-wang树脂28.6g(10mmol)于固相反应柱中,用dmf洗涤2次后用dmf溶胀树脂30分钟,然后用150ml的dblk脱保护5min 7min,150mldmf洗涤6次。称取30.8g(50mmol)fmoc-cys(mmt)-oh和8.1g(60mmol)hobt用100ml的dmf/dcm(1:1)溶解,冰水浴下加入10ml(65mmol)dipcdi活化2-3min后,将混合液加入到反应柱中,室温反应2小时,以茚三酮检测反应终点(如树脂无色透明则终止反应;如树脂显色则延长反应1小时)。反应结束,用150mldmf洗涤树脂3次,加入100mldblk脱保护6min 8min,100mldmf洗涤树脂6次,茚三酮检测树脂有颜色。重复上述偶联操作,按照上文步骤2中所述按肽序列顺序继续依次偶联fmoc-gly-oh、fmoc-thr(tbu)-oh、fmoc-cys(acm)-oh、fmoc-ala-oh、fmoc-val-oh、fmoc-asn(trt)-oh、fmoc-val-oh、fmoc-cys(mmt)-oh、fmoc-leu-oh、fmoc-glu(otbu)-oh、fmoc-cys(acm)-oh、fmoc-glu(otbu)-oh、fmoc-asp(otbu)-oh、fmoc-asn(trt)-oh。各保护氨基酸均投料50mmol,其它物料投料比与保护氨基酸对应。
[0069]
对比例2:肽树脂的氧化
[0070]
脱fmoc保护结束dmf洗涤树脂6次后,肽树脂继续用dcm洗涤3次并抽干,然后采用tfa:tis:dcm=2:5:93、反应次数为10次及每次5分钟来对肽树脂进行脱mmt处理,结束后树脂用dmf洗涤6次。量取30%的双氧水5.1ml(50mmol)及0.5-1ml的dipea加入到150ml的dmf中,加入到固相反应柱中与树脂进行第一对二硫键的键合反应,鼓气反应1h,反应完毕后继续dmf洗涤6次后进行第二对二硫键的键合。称取7.6g(30mmol)的i2溶解于150ml的dmf后加入反应柱中。反应时间为1h。反应完成后用150ml的dblk脱保护5min 7min,150mldmf洗涤5次后dcm洗涤2次,然后用150ml甲醇收缩树脂2次,每次5min,减压抽干肽树脂,最终得到肽树脂66.8克。
[0071]
对比例3:肽树脂的裂解
[0072]
将实施例7中得到的66.8g(10mmol)肽树脂全部置于1000ml圆底烧瓶中,以10ml/g肽树脂的比例加入670ml的裂解试剂(tfa:tis:h2o=92:4:4(v/v)),室温搅拌2h。反应物用砂芯漏斗过滤,过滤结束后加入少量tfa洗涤树脂,收集并合并滤液后减压浓缩至一定体积。加入冰冻的无水乙醚(100ml/g肽树脂)使溶液沉淀,离心、去除上清液后将沉淀用无水乙醚洗涤3次,真空干燥得到类白色固体粉末的粗肽16.8g。粗肽纯度为60.8%,拓扑杂质为19.8%。
[0073]
对比例4普卡那肽的制备
[0074]
将实施例8中获得的16.8g粗肽经以十八烷基硅烷为固定相,以0.1%三氟乙酸水溶液/乙腈为流动相进行反相液相制备纯化,收集目的峰馏分,浓缩冻干。得到精肽4.9g,纯度99.0%,收率28.8%。
[0075]
以上仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。