1.本发明涉及多肽制备技术领域,尤其涉及寡肽-1盐酸盐的制备方法。
背景技术:
2.寡肽-1是一个三肽分子,序列是ghk。寡肽-1自然存在于人的血液、唾液和尿液当中。1973年dr.loren pickart首先分离到了ghk-cu,它是在研究对老化组织和年轻组织同样起作用的活性物质中发现的三肽物质,接下来的研究证明这种三肽的序列是甘氨酸-组氨酸-赖氨酸,并且与铜离子有很强的亲和力,形成ghk-cu复合物。研究证明ghk是以与铜离子形成复合物的形式发挥功能。最初实验发现,ghk能增加大鼠正常肝细胞的存活率,能促进肝癌细胞的生长,刺激这些细胞dna和rna的合成。接下来的研究中发现,ghk和ghk-cu复合物能促进多种细胞和组织的生长、分裂和分化。ghk-cu复合物还可以在纤维原细胞培养液中促进或抑制金属蛋白酶的合成。另据报道,ghk存在于人的i型胶原a2(i)链中,说明可能参与伤口愈合和组织修复的过程。有实验表明,ghk-cu复合物可加速大鼠、小鼠、猪和马伤口的愈合。
3.生物材料中提取寡肽-1往往会造成生物活性的损失,且常伴随铜离子或铁离子的螯合。这些金属离子对从血浆中分离寡肽-1的多个步骤都会产生干扰,因此目前采用化学合成法制备寡肽-1。
4.已报道的寡肽-1固相方法中以2-ctc树脂为载体,逐步偶联fmoc-gly-oh,fmoc-his(trt)-oh,fmoc-lys(boc)-oh,然后采用tfa将ghk从树脂上切除下来,得到ghk粗品。也有关于液相合成法合成三肽ghk的报道,该方法对甘氨酸的氨基、组氨酸的咪唑基、赖氨酸的侧链氨基进行保护,得到中间体boc-gly、his(trt)和lys(boc);接肽反应以dmf为反应溶剂,n-羟基苯并三唑(hobt),n,n-二环己基碳二酰亚胺(dcc)为复合缩合剂,三氟乙酸(tfa)切除保护基团。寡肽-1的另一种液相合成方法中,先将trt gly oh与n羟基琥珀酰亚胺反应生成trt gly osu,再与hhis(trt)oh反应生成trt glyhis(trt)oh,然后与n羟基琥珀酰亚胺反应生成trtgly his(trt)osu,最后与lys(trt)oh反应生成trt gly his(trt)lys(trt)oh,将trt gly his(trt)lys(trt)oh在醋酸中脱掉保护基团即可生成ghk醋酸盐。
5.可见,目前合成ghk方法主要有固相合成与液相合成两种,固相方法反应,后处理简便,溶剂用量小,绿色环保。但由于非均相反应反应效率低下,需要大量的反应原料,而且单批次产量一般均在几十公斤以下,造成制备成本很高。液相反应属于均相反应,反应易于规模化,可单批在百公斤甚至吨以上,从而实现较低的生产成本。但液相反应使用大量的有机溶剂,特别是商业化生产时,单位溶剂的损耗量十分巨大,部分还需要危险操作,不符合绿色环保的要求。
技术实现要素:
6.有鉴于此,本发明要解决的技术问题在于提供一种寡肽-1盐酸盐的制备方法,该方法能够降低有机溶剂的用量,收率高。
7.本发明提供的寡肽-1盐酸盐的制备方法,包括:
8.步骤1:以二氯甲烷为溶剂,将fmoc-lys(boc)-oh与peg偶联,制备fmoc-lys(boc)-peg;
9.步骤2:依次偶联fmoc-his(trt)-oh和boc-gly-oh,制得boc-gly-his(trt)-lys(boc)-peg;
10.步骤3:boc-gly-his(trt)-lys(boc)-peg经裂解,制得寡肽-1盐酸盐。
11.从原料及试剂使用量来说,本发明提供的方法替换了固相昂贵的反应树脂,采用了价格低廉的peg,与液相反应相比,氨基酸采用固相常用氨基酸,价格也比液相的特定氨基酸价格低廉。并且,固相反应氨基酸一般使用量都要在3倍以上,而本发明只需要1.2倍。与液相相比,溶液使用种类相对单一,使用量一般为液相反应的1/3,具有明显环保优势。从反应步骤考虑,反应步骤相比液相合成处理方式单一简便,有发展为自动化的潜力。从规模上考虑,由于反应时是均相反应,理论上也液相一致,本发明提供的方案可以实现单批吨级产量,比固相反应具有明显优势。
12.实验表明,合成中载体分子量是影响合成效果的关键的因素,分子量过低,在各种溶剂中都可能部分或全部溶解,无法作为合成的载体。并且,随着偶联氨基酸数量的增加,氨基酸的性质也会逐步影响peg的性质,因此,peg的分子量不能过小。但peg的分子量过大会降低溶解性,使其很难实现反应均质。因此,必须选择适当的分子量的peg。
13.本发明中,所述peg的分子量为2000~8000。一些实施例中,所述peg的分子量为3000~6000,另一些实施例中,peg的分子量为2000~4000。一些具体实施例中,peg的分子量为2000或4000。
14.本发明步骤1中所述偶联的偶联剂为edc、hcl和化合物a的组合物;所述化合物a为hobt或hoat;步骤1中,peg、fmoc-lys(boc)-oh、化合物a、edc的摩尔比为1:1.2:1.2:1.2。所述偶联反应的条件为室温搅拌3h。
15.实验表明,反应中要选择合适的反应溶剂,该溶剂需在反应时能够溶解peg及氨基酸偶联peg后的物质。且反应结束后,反应液减压蒸馏,除去部分反应溶剂,需要选择合适的沉淀剂,使已偶联氨基酸的peg载体能够完全从溶剂中析出。本发明中,偶联反应的溶液选自二氯甲烷,四氢呋喃,氯仿等,其中,采用二氯甲烷作为溶剂进行反应的收率最优。一些实施例中,所述沉淀剂为正己烷,乙醚或甲基叔丁基醚。
16.第一个氨基酸偶联完后需要用乙酰化试剂处理,确保所有peg上可能的残余基团被封闭;本发明步骤1中,所述偶联后还包括乙酰化的步骤,所述乙酰化的试剂为乙酸酐和吡啶;所述乙酸酐、吡啶与peg的摩尔比为10:10:1。
17.本发明实施例中,步骤1包括:
18.将peg以二氯甲烷溶解,依次加入hobt、fmoc-lys(boc)-oh、edc
·
hcl,搅拌反应3小时后,加入乙酸酐和吡啶继续搅拌反应3小时;然后,反应液经浓缩后以正己烷或乙醚沉淀,获得fmoc-lys(boc)-peg。
19.所述沉淀的条件为搅拌2h,过滤后将滤饼用正己烷冲洗3次。滤饼与35℃鼓风干燥8h。
20.本发明步骤2中偶联fmoc-his(trt)-oh或boc-gly-oh前,经脱除fmoc保护的步骤;脱除fmoc的制剂为dbu和二乙胺;其中dbu和二乙胺的摩尔比为0.25:3.75。脱保护反应中的
条件为0~5℃添加脱保护剂,室温搅拌反应2h。步骤2中,带有fmoc保护剂的产物、dbu和二乙胺的摩尔比为0.25、0.25:3.75。
21.本发明步骤2中所述偶联的溶剂为二氯甲烷;所述偶联的偶联剂为edc、hcl和化合物a的组合物;所述化合物a为hobt或hoat;步骤2中,peg、氨基酸、化合物a、edc的摩尔比为1:1.2:1.2:1.2。
22.本发明实施例中,步骤2包括:
23.将fmoc-lys(boc)-peg溶于二氯甲烷,加入dbu后冷却至5℃以下,滴加二乙胺然后,升温至室温搅拌反应2小时,反应液浓缩后以正己烷沉淀制得nh
2-lys(boc)-peg;
24.将nh
2-lys(boc)-peg溶于二氯甲烷,依次加入hobt、fmoc-his(trt)-oh、edc
·
hcl,室温搅拌反应2小时,反应液经浓缩后以正己烷沉淀得到化合物fmoc-his(trt)-lys(boc)-peg;
25.将fmoc-his(trt)-lys(boc)-peg溶于二氯甲烷,加入dbu后冷却至5℃以下,滴加二乙胺然后,升温至室温搅拌反应2小时,反应液浓缩后以正己烷沉淀制得nh
2-his(trt)-lys(boc)-peg;
26.将nh
2-his(trt)-lys(boc)-peg溶于二氯甲烷,依次加入hobt、boc-gly-oh、edc
·
hcl,室温搅拌反应2小时,反应液经浓缩后以正己烷沉淀得到化合物boc-gly-his(trt)-lys(boc)-peg。
27.所述沉淀的条件为搅拌2h,过滤后将滤饼用正己烷冲洗3次。滤饼与35℃鼓风干燥8h。
28.本发明步骤3中所述裂解的裂解液为氯化氢/乙酸乙酯溶液与tis的混合物;其中,氯化氢乙酸乙酯的浓度为4n~6n,tis的体积比为5%~10%。
29.本发明实施例中步骤3包括:将boc-gly-his(trt)-lys(boc)-peg与裂解液混合,室温反应2小时后,反应液经浓缩以甲醇沉淀,制得寡肽-1盐酸盐。
30.本发明提供的方法,以peg为载体,以二氯甲烷为反应溶剂,该方法节约了原料的用量,降低了制备成本,同时也降低了有机溶剂的用量,提高了环保优势。实验表明,以该方法制备寡肽-1盐酸盐,总收率可达83.4%,产物纯度为98.3%。
附图说明
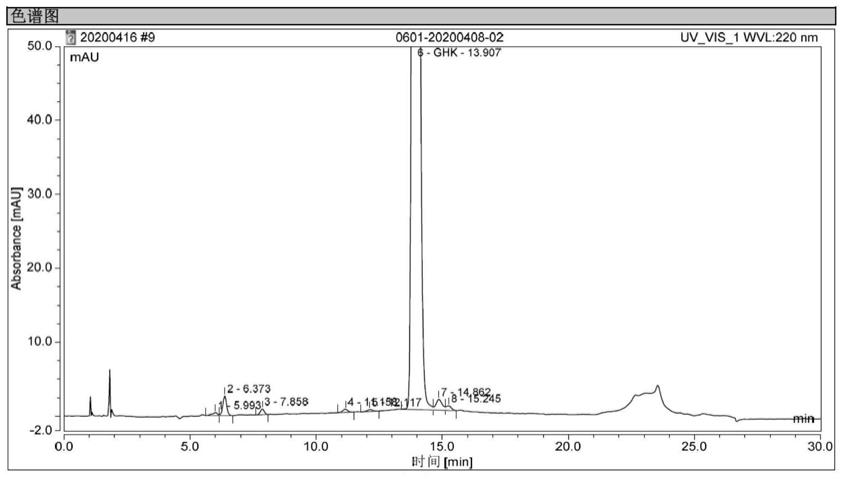
31.图1ghk盐酸盐的色谱图;
32.图2ghk盐酸盐的质谱图。
具体实施方式
33.本发明提供了寡肽-1盐酸盐的制备方法,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
34.本发明采用的试材皆为普通市售品,皆可于市场购得。
35.表1原料缩写及英文
36.缩写及英文含义hoat1-羟基-7-偶氮苯并三氮唑fmoc9-芴甲氧羰基hobt1-羟基苯并三唑edc
·
hcl1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐dmfn,n-二甲基甲酰胺dcm二氯甲烷boc叔丁氧羰基his组氨酸gly甘氨酸lys赖氨酸trt三苯甲基
37.下面结合实施例,进一步阐述本发明:
38.实施例1fmoc-lys(boc)-peg(4000)的合成
39.称取化合物peg4000(0.5mol)加入5l三口烧瓶内,向反应瓶中加入2l二氯甲烷,依次加入hobt(0.6mol)、fmoc-lys(boc)-oh(0.6mol)。搅拌溶解。加入edc
·
hcl(0.6mol),在室温条件下继续搅拌3小时。然后加入乙酸酐及吡啶(5mol/5mol),室温条件下继续搅拌3小时。反应结束后,反应液在30℃,减压浓缩至成粘稠物,向粘稠物中加入正己烷(1000ml),搅拌2小时。过滤,滤饼用正己烷(500ml
×
3)冲洗三次。将滤饼在35℃条件下鼓风干燥8小时,得到化合物fmoc-lys(boc)-peg(收率99.9%)。
40.实施例2fmoc-lys(boc)-peg(2000)的合成
41.称取化合物peg2000(0.5mol)加入5l三口烧瓶内,向反应瓶中加入1l二氯甲烷,依次加入hobt(0.6mol)、fmoc-lys(boc)-oh(0.6mol)。搅拌溶解。加入edc
·
hcl(0.6mol),在室温条件下继续搅拌3小时。然后加入乙酸酐及吡啶(5mol/5mol),室温条件下继续搅拌3小时。反应结束后,反应液在30℃,减压浓缩至成粘稠物,向粘稠物中加入冰乙醚(500ml),搅拌2小时。过滤,滤饼用冰乙醚(300ml
×
3)冲洗三次。将滤饼在35℃条件下鼓风干燥8小时,得到化合物fmoc-lys(boc)-peg(收率99.6%)。
42.实施例3fmoc-his(trt)-lys(boc)-peg(4000)的合成
43.称取fmoc-lys(boc)-peg(4000)(0.25mol)加入5l三口烧瓶内,向反应瓶中加入二氯甲烷(1l),搅拌溶解,再加入dbu(0.25mol)。将反应液冰浴冷却至5℃以下,缓慢滴加二乙胺(3.75mol),控温不超过5℃。滴加完后,将反应液升至室温继续搅拌2小时。tlc(dcm:meoh:hac=100:1:0.5)监控反应。反应完全后,将反应液在30℃条件下减压浓缩至成粘稠物,向粘稠物中加入正己烷(500ml),搅拌30分钟。过滤,滤饼用正己烷300ml冲洗两次。将滤饼在35℃鼓风干燥8小时,得到类白色固体。
44.称取上述固体加入5l三口烧瓶内,向反应瓶中加入1l二氯甲烷,依次加入hobt(0.3mol)、fmoc-his(trt)-oh(0.3mol)。搅拌溶解。加入edc
·
hcl(0.3mol),在室温条件下继续搅拌2小时。反应结束后,反应液在30℃,减压浓缩至成粘稠物,向粘稠物中加入正己烷(500ml),搅拌2小时。过滤,滤饼用正己烷(300ml
×
3)冲洗三次。将滤饼在35℃条件下鼓风干燥8小时,得到化合物fmoc-his(trt)-lys(boc)-peg(4000)(收率100.8%)。
45.实施例4fmoc-his(trt)-lys(boc)-peg(2000)的合成
46.称取fmoc-lys(boc)-peg(2000)(0.25mol)加入5l三口烧瓶内,向反应瓶中加入二氯甲烷(1l),搅拌溶解,再加入dbu(0.25mol)。将反应液冰浴冷却至5℃以下,缓慢滴加二乙胺(3.75mol),控温不超过5℃。滴加完后,将反应液升至室温继续搅拌2小时。tlc(dcm:meoh:hac=100:1:0.5)监控反应。反应完全后,将反应液在30℃条件下减压浓缩至成粘稠物,向粘稠物中加入正己烷(500ml),搅拌30分钟。过滤,滤饼用正己烷300ml冲洗两次。将滤饼在35℃鼓风干燥8小时,得到类白色固体。
47.称取上述固体加入5l三口烧瓶内,向反应瓶中加入1l二氯甲烷,依次加入hobt(0.3mol)、fmoc-his(trt)-oh(0.3mol)。搅拌溶解。加入edc
·
hcl(0.3mol),在室温条件下继续搅拌2小时。反应结束后,反应液在30℃,减压浓缩至成粘稠物,向粘稠物中加入正己烷(500ml),搅拌2小时。过滤,滤饼用正己烷(300ml
×
3)冲洗三次。将滤饼在35℃条件下鼓风干燥8小时,得到化合物fmoc-his(trt)-lys(boc)-peg(2000)(收率95.4%)。
48.实施例5boc-gly-his(trt)-lys(boc)-peg(4000)的合成
49.称取fmoc-his(trt)-lys(boc)-peg(4000)(0.25mol)加入5l三口烧瓶内,向反应瓶中加入二氯甲烷(1l),搅拌溶解,再加入dbu(0.25mol)。将反应液冰浴冷却至5℃以下,缓慢滴加二乙胺(3.75mol),控温不超过5℃。滴加完后,将反应液升至室温继续搅拌2小时。tlc(dcm:meoh:hac=100:1:0.5)监控反应。反应完全后,将反应液在30℃条件下减压浓缩至成粘稠物,向粘稠物中加入正己烷(500ml),搅拌30分钟。过滤,滤饼用正己烷300ml冲洗两次。将滤饼在35℃鼓风干燥8小时,得到类白色固体。
50.称取上述化合物加入5l三口烧瓶内,向反应瓶中加入1l二氯甲烷,依次加入hobt(0.3mol)、boc-gly-oh(0.3mol)。搅拌溶解。加入edc
·
hcl(0.3mol),在室温条件下继续搅拌2小时。反应结束后,反应液在30℃,减压浓缩至成粘稠物,向粘稠物中加入正己烷(500ml),搅拌2小时。过滤,滤饼用正己烷(300ml
×
3)冲洗三次。将滤饼在35℃条件下鼓风干燥8小时,得化合物boc-gly-his(trt)-lys(boc)-peg(4000)(收率98.6%)。
51.实施例6boc-gly-his(trt)-lys(boc)-peg(2000)的合成
52.称取fmoc-his(trt)-lys(boc)-peg(4000)(0.25mol)加入5l三口烧瓶内,向反应瓶中加入二氯甲烷(1l),搅拌溶解,再加入dbu(0.25mol)。将反应液冰浴冷却至5℃以下,缓慢滴加二乙胺(3.75mol),控温不超过5℃。滴加完后,将反应液升至室温继续搅拌2小时。tlc(dcm:meoh:hac=100:1:0.5)监控反应。反应完全后,将反应液在30℃条件下减压浓缩至成粘稠物,向粘稠物中加入正己烷(500ml),搅拌30分钟。过滤,滤饼用正己烷300ml冲洗两次。将滤饼在35℃鼓风干燥8小时,得到类白色固体。
53.称取上述化合物加入5l三口烧瓶内,向反应瓶中加入1l二氯甲烷,依次加入hobt(0.3mol)、boc-gly-oh(0.3mol)。搅拌溶解。加入edc
·
hcl(0.3mol),在室温条件下继续搅拌2小时。反应结束后,反应液在30℃,减压浓缩至成粘稠物,向粘稠物中加入正己烷(500ml),搅拌2小时。过滤,滤饼用正己烷(300ml
×
3)冲洗三次。将滤饼在35℃条件下鼓风干燥8小时,得化合物boc-gly-his(trt)-lys(boc)-peg(4000)(收率90.9%)。
54.实施例7nh
2-gly-his-lys-cooh的制备
55.称取上述boc-gly-his(trt)-lys(boc)-peg(4000)(约0.25mol)加入5l反应圆底烧瓶内,再向反应瓶中加入1l裂解液(4n氯化氢乙酸乙酯:tis=95:5),室温反应2小时,反
应结束后,减压浓缩至成粘稠物,加入甲醇(2l),充分搅拌2小时,过滤,滤饼用甲醇(500ml
×
3)冲洗三次。将滤饼在35℃条件下鼓风干燥8小时,得91.7g ghk盐酸盐(色谱图如图1,质谱图如图2),检测纯度为98.3%,总收率83.4%
56.实施例8nh
2-gly-his-lys-cooh的制备
57.称取上述boc-gly-his(trt)-lys(boc)-peg(2000)(约0.25mol)加入5l反应圆底烧瓶内,再向反应瓶中加入1l裂解液(4n氯化氢乙酸乙酯:tis=95:5),室温反应2小时,反应结束后,减压浓缩至成粘稠物,加入甲醇(2l),充分搅拌2小时,过滤,滤饼用甲醇(500ml
×
3)冲洗三次。将滤饼在35℃条件下鼓风干燥8小时,得85.6g ghk盐酸盐,检测纯度为98.1%,总收率77.9%
58.以上仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。