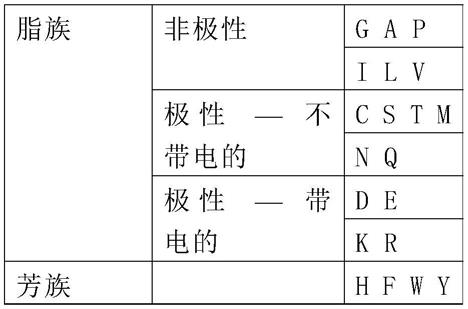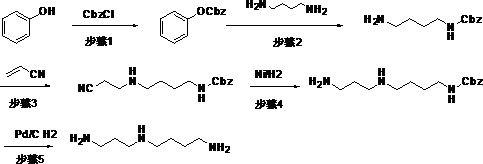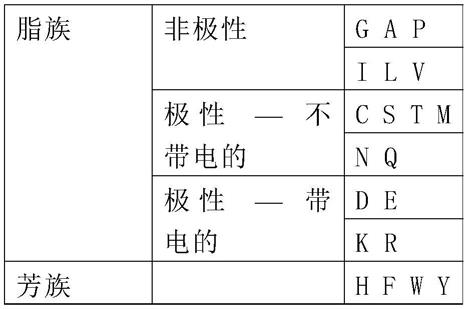
肾损伤的治疗
1.本技术要求于2019年2月22日提交的gb 1902419.9的优先权,该专利的内容和元素出于所有目的以引用方式并入本文。
技术领域
2.本发明涉及与肾损伤(具体地但并非排他性地为急性肾损伤)相关的疾病和病症的诊断、治疗和预防。
背景技术:
3.急性肾损伤(aki)是指对肾,尤其是对肾小管上皮细胞的快速损害。它通常是化学驱动的,例如由药品、化学品、造影染料或草药或膳食补充剂引起的肾损害或损伤。它也可能由局部缺血、机械或免疫因素引起。
4.aki是一种常见病症,并且影响多达10%的住院患者(silver,s.a.和chertow,g.m.,“急性肾损伤的经济后果”,nephron 137,297
–
301(2017))。与aki相关的死亡率很高,aki后需要重症监护的患者死亡率可高达50%。对于那些幸存的aki患者,存在进展为慢性肾病(ckd)、终末期肾衰竭、肾替代疗法或移植的长期风险(silver,s.a.和chertow,g.m.,“急性肾损伤的经济后果”,nephron 137;mehta,r.l.等人,“急性肾损伤网络:改善急性肾损伤结果的倡议报告”,crit.care 11;zuk,a.等人,“克服急性肾损伤的转化障碍:来自niddk研讨会的报告”,clin.j.am.soc.nephrol.13,1113
–
1123(2018))。
5.化疗剂顺铂(二氯二氨基铂;(sp
‑4‑
2)
‑
二胺二氯铂(ii))广泛用于治疗多种癌症,包括头颈癌、乳腺癌、肺癌、睾丸癌、卵巢癌、脑癌和膀胱癌。在给予单剂量顺铂(50
‑
100mg/m2)后,大多数患者出现一定程度的aki,并且高达30%的患者会出现肾毒性(ozkok,a.和edelstein,c.l.,“顺铂诱导的急性肾损伤的病理生理学”,biomed res.int.2014,967826(2014)),其定义为肾功能突然降低,表现为血清肌酸酐升高(mehta等人,同上)。在患有头颈癌的老年患者中,高达20%的患者会从aki进展为严重的肾功能障碍(yao,x.、panichpisal,k.、kurtzman,n.和nugent,k.,“顺铂肾毒性:综述”,am.j.med.sci.334,115
–
124(2007))。顺铂诱导的aki是剂量限制性的,并且治疗通常在几周内分成多个剂量,但是这仍然与肾毒性相关。在存在包括糖尿病、高血压、肾毒性药物和老年在内的预先存在的条件下,顺铂诱导的aki的严重程度更高。
6.aki的病理生理学主要由毒素、化学品、药物、免疫和机械因子或局部缺血对肾小管上皮细胞(tec)的损害来定义。还存在针对aki的血管成分和免疫成分。在接受顺铂治疗的患者中,肾中的药物含量高达血浆中药物含量的五倍。在肾中,顺铂在tec中积累,在tec中它诱导活性氧、消耗谷胱甘肽、引起线粒体功能障碍并通过细胞凋亡或坏死导致细胞死亡(ozkok等人,同上;wang,s.、wei,q.、dong,g.和dong,z.,“erk介导的纤毛抑制在顺铂诱导的肾小管细胞凋亡和急性肾损伤中的作用”,biochim.biophys.acta 1832,1582
–
1590(2013);jo,s.
‑
k.、cho,w.y.、sung,s.a.、kim,h.k.和won,n.h.,“mek抑制剂u0126通过减少炎症和细胞凋亡来减轻顺铂诱导的肾损伤”,kidney int.67;nowak,g.,“蛋白激酶c
‑
α和
erk1/2介导线粒体功能障碍、活性na 转运减少和顺铂诱导的肾细胞凋亡”,j.biol.chem.277,43377
–
43388(2002))。在缺血期间,氧需求很高的tec由于细胞凋亡或坏死而缺氧并经历细胞死亡。
7.aki后,肾功能可恢复。这被广泛地认为是由剩余tec的增殖所驱动的,这些剩余tec具有非常大的再生能力(yang,h.
‑
c.、liu,s.
‑
j.和fogo,a.b.,“哺乳动物的肾脏再生,nephron exp.”,nephrol.126,50(2014);coelho,s.、cabral,g.、lopes,j.a.和jacinto,a.,“急性肾损伤后的肾再生”,nephrology23,805
–
814(2018);chang
‑
panesso,m.和humphreys,b.d.,“肾损伤和修复中的细胞可塑性”,nat.rev.nephrol.13,39
–
46(2017))。当tec增殖不足时,会出现肾毒性,并且随着时间的推移,慢性肾病可能随之发生,并且纤维化可能作为继发现象发生。在最近的研究中,已经表明aki后tec功能障碍的一个关键决定因素是snail基因(也称为sna;snah;snail;slugh2;snail1)的重新表达(grande,m.t.等人,“snail1诱导的部分上皮
‑
间充质转化驱动小鼠肾纤维化,并可靶向逆转已建立的疾病”,nat.med.21,989
–
997(2015);simon
‑
tillaux,n.和hertig,a.,“snail和肾纤维化”,nephrol.dial.transplant 32,224
–
233(2017);lovisa,s.等人,“上皮
‑
间质转化诱导肾纤维化中的细胞周期停滞和实质损伤”,nat.med.21,998
–
1009(2015))。snail对于胚胎发生很重要,但很少在成人中表达,除了在癌症中它会导致上皮向间充质转化(emt)。在肾中,tgfβ1基因可诱导tec中的snail,这与tec功能和增殖受损相关(lovisa,s.等人,“上皮
‑
间质转化诱导肾纤维化中的细胞周期停滞和实质损伤”,nat.med.21,998
–
1009(2015))。
8.据报道,细胞因子白介素11(il
‑
11)对缺血再灌注损伤后的aki具有强大的保护作用,并抑制aki的细胞凋亡、坏死和炎症(lee,h.t.等人,“白介素
‑
11可防止肾缺血和再灌注损伤”,am.j.physiol.renal physiol.303,f1216
–
24(2012))。il
‑
11也已被证明在人tec和小鼠肾中被异氟烷上调,这与il
‑
11对急性缺血性肾损伤的关键保护作用相关(ham,a.等人,“il
‑
11在异氟醚介导的小鼠缺血性急性肾损伤保护中的关键作用”,anesthesiology 119,1389
–
1401(2013))。
9.据报道,il
‑
11治疗还通过减轻肾炎和预防肾损害来预防大鼠和小鼠的急性肾毒性肾炎(stangou,m.等人,“il
‑
11对wistar kyoto大鼠肾毒性肾炎tgf
‑
β和细胞外基质肾小球表达的影响”,j.nephrol.24,106
–
111(2011);lai,p.c.等人,“白介素
‑
11减轻wistar kyoto大鼠的肾毒性肾炎”,j.am.soc.nephrol.12,2310
–
2320(2001);lai,p.c.等人,“白介素
‑
11减少小鼠实验性肾小球肾炎的肾损伤和肾小球nf
‑
kappa b活性”,nephron exp.nephrol.101,e146
–
54(2005))。
技术实现要素:
10.与已报道的il
‑
11在肾损伤和损害中的保护作用相反,本发明涉及通过抑制il
‑
11信号传导来治疗和/或预防肾损伤和与肾损伤相关的障碍、疾病或病症。
11.在本发明的一个方面,提供了能够抑制白介素11(il
‑
11)介导的信号传导的药剂,该药剂用于治疗或预防肾损伤和/或与肾损伤相关的障碍、疾病或病症的方法中。
12.在本发明的另一个方面,提供了能够抑制白介素11(il
‑
11)介导的信号传导的药剂用于制备药物的用途,该药物用于治疗或预防肾损伤和/或与肾损伤相关的障碍、疾病或病症的方法中。
13.在本发明的另一个方面,提供了治疗或预防肾损伤和/或与肾损伤相关的障碍、疾病或病症的方法,该方法包括向需要治疗的受试者施用治疗有效量的能够抑制白介素11(il
‑
11)介导的信号传导的药剂。
14.本发明还提供了能够抑制白介素11(il
‑
11)介导的信号传导的药剂,该药剂用于逆转肾损伤的方法中。
15.还提供了能够抑制白介素11(il
‑
11)介导的信号传导的药剂用于制备药物的用途,该药物用于逆转肾损伤的方法中。
16.还提供了逆转肾损伤的方法,该方法包括向需要治疗的受试者施用治疗有效量的能够抑制白介素11(il
‑
11)介导的信号传导的药剂。
17.在一些实施方案中,肾损伤是急性肾损伤。在一些实施方案中,肾损伤是肾毒性。在一些实施方案中,肾损伤是药物诱导的肾损伤或缺血诱导的肾损伤。在一些实施方案中,肾损伤是顺铂诱导的肾损伤或顺铂诱导的肾毒性。在一些实施方案中,肾损伤的特征在于对肾小管上皮细胞(tec)的损害。
18.本发明还提供了能够抑制白介素11(il
‑
11)介导的信号传导的药剂,该药剂用于改善患有肾功能损害的受试者的肾功能的方法中。
19.还提供了能够抑制白介素11(il
‑
11)介导的信号传导的药剂用于制备药物的用途,该药物用于改善患有肾功能损害的受试者的肾功能的方法中。
20.还提供了改善患有肾功能损害的受试者的肾功能的方法,该方法包括向需要治疗的受试者施用治疗有效量的能够抑制白介素11(il
‑
11)介导的信号传导的药剂。
21.本发明还提供了能够抑制白介素11(il
‑
11)介导的信号传导的药剂,该药剂用于促进肾小管上皮细胞(tec)的增殖、存活和/或功能,和/或肾组织的生长、维持和/或功能(例如,在肾损伤后)的方法中。
22.还提供了能够抑制白介素11(il
‑
11)介导的信号传导的药剂用于制备药物的用途,该药物用于促进肾小管上皮细胞(tec)的增殖、存活和/或功能,和/或肾组织的生长、维持和/或功能(例如,在肾损伤后)的方法中。
23.还提供了促进肾小管上皮细胞(tec)的增殖、存活和/或功能,和/或肾组织的生长、维持和/或功能(例如,在肾损伤后)的方法,该方法包括向需要治疗的受试者施用治疗有效量的能够抑制白介素11(il
‑
11)介导的信号传导的药剂。
24.本发明还提供了能够抑制白介素11(il
‑
11)介导的信号传导的药剂,该药剂用于抑制snail表达(例如,在肾损伤后)的方法中。
25.还提供了能够抑制白介素11(il
‑
11)介导的信号传导的药剂用于制备药物的用途,该药物用于抑制snail表达(例如,在肾损伤后)的方法中。
26.还提供了抑制snail表达(例如,在肾损伤后)的方法,该方法包括向需要治疗的受试者施用治疗有效量的能够抑制白介素11(il
‑
11)介导的信号传导的药剂。
27.本发明还提供了能够抑制白介素11(il
‑
11)介导的信号传导的药剂,该药剂用于抑制或逆转肾小管上皮细胞(tec)向间充质细胞样表型的转化(例如,在肾损伤后)的方法中。
28.还提供了能够抑制白介素11(il
‑
11)介导的信号传导的药剂用于制备药物的用途,该药物用于抑制或逆转肾小管上皮细胞(tec)向间充质细胞样表型的转化(例如,在肾
损伤后)的方法中。
29.还提供了抑制或逆转肾小管上皮细胞(tec)向间充质细胞样表型的转化(例如,在肾损伤后)的方法,该方法包括向需要治疗的受试者施用治疗有效量的能够抑制白介素11(il
‑
11)介导的信号传导的药剂。
30.在根据本发明的各个方面的一些实施方案中,该药剂是能够阻止或减少白介素11(il
‑
11)与白介素11受体(il
‑
11r)结合的药剂。
31.在一些实施方案中,该药剂能够与白介素11(il
‑
11)或白介素11受体(il
‑
11r)结合。在一些实施方案中,该药剂选自:抗体或其抗原结合片段、多肽、肽、核酸、寡核苷酸、适体或小分子。该药剂可以是抗体或其抗原结合片段。该药剂可以是诱饵受体。
32.在一些实施方案中,该药剂是il
‑
11介导的信号传导的抗il
‑
11抗体拮抗剂,或其抗原结合片段。
33.在一些实施方案中,抗体或抗原结合片段包含:
34.(i)包含以下cdr的重链可变(vh)区:
35.具有seq id no:34的氨基酸序列的hc
‑
cdr1
36.具有seq id no:35的氨基酸序列的hc
‑
cdr2
37.具有seq id no:36的氨基酸序列的hc
‑
cdr3;和
38.(ii)包含以下cdr的轻链可变(vl)区:
39.具有seq id no:37的氨基酸序列的lc
‑
cdr1
40.具有seq id no:38的氨基酸序列的lc
‑
cdr2
41.具有seq id no:39的氨基酸序列的lc
‑
cdr3。
42.在一些实施方案中,抗体或抗原结合片段包含:
43.(i)包含以下cdr的重链可变(vh)区:
44.具有seq id no:40的氨基酸序列的hc
‑
cdr1
45.具有seq id no:41的氨基酸序列的hc
‑
cdr2
46.具有seq id no:42的氨基酸序列的hc
‑
cdr3;和
47.(ii)包含以下cdr的轻链可变(vl)区:
48.具有seq id no:43的氨基酸序列的lc
‑
cdr1
49.具有seq id no:44的氨基酸序列的lc
‑
cdr2
50.具有seq id no:45的氨基酸序列的lc
‑
cdr3。
51.在一些实施方案中,该药剂是il
‑
11介导的信号传导的抗il
‑
11rα抗体拮抗剂,或其抗原结合片段。
52.在一些实施方案中,抗体或抗原结合片段包含:
53.(i)包含以下cdr的重链可变(vh)区:
54.具有seq id no:46的氨基酸序列的hc
‑
cdr1
55.具有seq id no:47的氨基酸序列的hc
‑
cdr2
56.具有seq id no:48的氨基酸序列的hc
‑
cdr3;和
57.(ii)包含以下cdr的轻链可变(vl)区:
58.具有seq id no:49的氨基酸序列的lc
‑
cdr1
59.具有seq id no:50的氨基酸序列的lc
‑
cdr2
60.具有seq id no:51的氨基酸序列的lc
‑
cdr3。
61.在一些实施方案中,该药剂是il
‑
11的诱饵受体。在一些实施方案中,il
‑
11的诱饵受体包含:(i)对应于gp130的细胞因子结合模块的氨基酸序列和(ii)对应于il
‑
11rα的细胞因子结合模块的氨基酸序列。
62.在一些实施方案中,该药剂是il
‑
11突变蛋白。在一些实施方案中,il
‑
11突变蛋白是w147a。
63.在一些实施方案中,该药剂能够阻止或减少白介素11(il
‑
11)或白介素11受体(il
‑
11r)的表达。该药剂可以是寡核苷酸或小分子。
64.在一些实施方案中,该药剂是能够阻止或减少il
‑
11的表达的反义寡核苷酸。在一些实施方案中,能够阻止或减少il
‑
11的表达的反义寡核苷酸是靶向il11的sirna,该sirna包含seq id no:12、13、14或15的序列。在一些实施方案中,该药剂是能够阻止或减少il
‑
11rα的表达的反义寡核苷酸。在一些实施方案中,能够阻止或减少il
‑
11rα的表达的反义寡核苷酸是靶向il11ra的sirna,该sirna包含seq id no:16、17、18或19的序列。
65.在本文提供的任何实施方案中,白介素11受体可以是或包含il
‑
11rα。
66.在本文提供的任何实施方案中,肾损伤可以是急性肾损伤(aki)、肾毒性、药物诱导的肾损伤(diki)、急性肾衰竭、急性肾病、慢性肾病、肾损害、肾小管坏死、急性肾小管坏死和自身免疫性肾损伤之一。
67.在本文提供的任何实施方案中,该药剂可在肾损伤的诱因(例如,施用或服用肾毒性药品或暴露于肾损伤的物理、机械、化学或环境来源)之前、同时或之后施用。
68.在一些实施方案中,提供了本文的药剂、用途和方法用于治疗和/或预防药物诱导的肾损伤(diki)。diki可以是内源性的和/或特异的肾损伤。在任何实施方案中,可提供本文的药剂、用途和方法用于治疗和/或预防顺铂诱导的肾损伤和/或顺铂诱导的肾毒性。
69.在一些实施方案中,可提供本文的药剂、用途和方法用于治疗和/或预防缺血诱导的肾损伤(iiki)或缺血诱导的急性肾损伤。
70.在本文提供的任何实施方案中,与肾损伤相关的障碍、疾病或病症可以是其中病理学上涉及肾损伤的疾病、障碍或病症。病理可包括对肾小管上皮细胞的损害和/或tec向间充质细胞样表型的转化,其可能是近端和/或远端的。
71.在任何实施方案中,该方法包括向其中白介素11(il
‑
11)或il
‑
11受体(il
‑
11r)的表达可被上调的受试者施用药剂。
72.在任何实施方案中,该方法可包括向其中已确定白介素11(il
‑
11)或白介素11受体(il
‑
11r)的表达上调的受试者施用药剂。
73.在一些实施方案中,该方法包括确定受试者中白介素11(il
‑
11)或il
‑
11受体(il
‑
11r)的表达是否上调,并向其中白介素11(il
‑
11)或il
‑
11受体(il
‑
11r)的表达上调的受试者施用药剂。
74.还提供了用能够抑制白介素11(il
‑
11)介导的信号传导的药剂来确定受试者是否适合治疗或预防肾损伤和/或与肾损伤相关的障碍、疾病或病症的方法,该方法包括任选地在体外确定受试者中白介素11(il
‑
11)或il
‑
11受体(il
‑
11r)的表达是否上调。
75.还提供了用能够抑制白介素11(il
‑
11)介导的信号传导的药剂来选择用于治疗或预防肾损伤和/或与肾损伤相关的障碍、疾病或病症的受试者的方法,该方法包括任选地在
体外确定该受试者中白介素11(il
‑
11)或il
‑
11受体(il
‑
11r)的表达是否上调。
76.在一个方面,提供了诊断受试者中的肾损伤和/或与肾损伤相关的障碍、疾病或病症,或发展肾损伤和/或与肾损伤相关的障碍、疾病或病症的风险的方法,该方法包括任选地在体外确定从该受试者获得的样品中白细胞介素11(il
‑
11)或il
‑
11受体(il
‑
11r)的上调。在一些实施方案中,诊断的方法是确认疑似患有肾损伤和/或与肾损伤相关的障碍、疾病或病症的受试者的肾损伤和/或与肾损伤相关的障碍、疾病或病症的诊断的方法。在一些实施方案中,诊断的方法和/或确认诊断的方法包括选择受试者以用能够抑制白介素11(il
‑
11)介导的信号传导的药剂进行治疗。
77.还提供了一种为患有或疑似患有肾损伤和/或与肾损伤相关的障碍、疾病或病症的受试者提供预后的方法,该方法包括任选地在体外确定从该受试者获得的样品中白介素11(il
‑
11)或il
‑
11受体(il
‑
11r)的表达是否上调,并且基于该确定,提供用能够抑制白介素11(il
‑
11)介导的信号传导的药剂治疗该受试者的预后。在一些实施方案中,提供预后的方法包括选择被确定为白介素11(il
‑
11)或il
‑
11受体(il
‑
11r)表达上调的受试者,以用能够抑制白介素11(il
‑
11)介导的信号传导的药剂进行治疗。
78.在另一个方面,提供了诊断肾损伤和/或与肾损伤相关的障碍、疾病或病症,或发展肾损伤和/或与肾损伤相关的障碍、疾病或病症的风险的方法,该方法包括任选地在体外确定受试者中预测il
‑
11或il
‑
11受体的表达上调,或il
‑
11介导的信号传导的上调的一个或多个遗传因子。在一些实施方案中,该方法包括选择受试者以用能够抑制白介素11(il
‑
11)介导的信号传导的药剂进行治疗。
79.还提供了一种为患有或疑似患有肾损伤和/或与肾损伤相关的障碍、疾病或病症的受试者提供预后的方法,该方法包括任选地在体外确定受试者中预测il
‑
11或il
‑
11受体的表达上调,或il
‑
11介导的信号传导的上调的一个或多个遗传因子。
具体实施方式
80.对有效预防和治疗肾损伤,特别是急性肾损伤的需求持续存在。
81.据报道,细胞因子il
‑
11对缺血再灌注损伤后的急性肾损伤具有保护作用(lee等人,同上),并且据报道,il
‑
11在遭受异氟烷化学损害的人肾小管上皮细胞和小鼠肾中上调并具有保护作用(ham等人,同上)。
82.然而,相比之下,本发明人发现抑制il
‑
11介导的信号传导能有效保护肾小管上皮细胞,使它们增殖并从损害中恢复,该损害是急性肾损伤的常见致病因素。虽然不希望受理论束缚,但本发明人相信对il
‑
11的抑制使肾小管上皮细胞能够通过阻止或减少snail的表达而增殖,从而导致肾组织再生和恢复。
83.白介素11和il
‑
11受体
84.白介素11(il
‑
11),也称为脂肪形成抑制因子,是一种多效性细胞因子,是il
‑
6细胞因子家族的成员,该il
‑
6细胞因子家族包括il
‑
6、il
‑
11、il
‑
27、il
‑
31、制瘤素、白血病抑制因子(lif)、心肌营养素
‑
1(ct
‑
1)、心肌营养素样细胞因子(clc)、睫状神经营养因子(cntf)和神经营养素(np
‑
1)。
85.白介素11(il
‑
11)在多种间充质细胞类型中表达。il
‑
11基因组序列已被定位到7号染色体的着丝粒区域和19号染色体上,并用确保从细胞有效分泌的规范信号肽转录。位
于其启动子序列内的il
‑
11的激活蛋白复合物cjun/ap
‑
1对于il
‑
11的基础转录调节至关重要(du和williams,blood,1997年,第89卷:第3897
‑
3908页)。人il
‑
11的未成熟形式是199个氨基酸的多肽,而il
‑
11的成熟形式编码178个氨基酸残基的蛋白质(garbers和scheller.,biol.chem.2013;394(9):1145
‑
1161)。人il
‑
11氨基酸序列可以由uniprot登录号p20809(p20809.1 gi:124294;seq id no:1)获得。重组人il
‑
11(奥普瑞白介素)也可商购获得。来自其他物种(包括小鼠、大鼠、猪、牛、几种硬骨鱼和灵长类)的il
‑
11也已被克隆和测序。
86.在本说明书中,“il
‑
11”指来自任何物种的il
‑
11,并且包括来自任何物种的il
‑
11的同工型、片段、变体或同源物。在优选的实施方案中,该物种是人(智人(homo sapiens))。il
‑
11的同工型、片段、变体或同源物可任选地表征为与来自给定物种(例如,人)的未成熟或成熟il
‑
11的氨基酸序列具有至少70%,优选地80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%之一的氨基酸序列同一性。il
‑
11的同工型、片段、变体或同源物可任选地以结合il
‑
11rα(优选地来自相同物种)并刺激表达il
‑
11rα和gp130的细胞中的信号转导的能力为特征(例如,如curtis等人,blood,1997,90(11);或karpovich等人,mol.hum.reprod.2003 9(2):75
‑
80中所述)。il
‑
11的片段可具有任何长度(按氨基酸数目计),但可以任选地是成熟il
‑
11长度的至少25%,并且可具有成熟il
‑
11长度的50%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%之一的最大长度。il
‑
11的片段可具有10个氨基酸的最小长度,并且可具有15、20、25、30、40、50、60、70、80、90、100、110、120、130、140、150、160、170、180、190或195个氨基酸之一的最大长度。
87.il
‑
11通过遍在表达的糖蛋白130(gp130;也称为糖蛋白130、il
‑
6st、il
‑6‑
β或cd130)的同源二聚体传导信号。gp130是与il
‑
6受体家族形成i型细胞因子受体的一个亚基的跨膜蛋白。特异性是通过单个白介素11受体亚基α(il
‑
11rα)获得的,该亚基不直接参与信号转导,但最初α
‑
受体的细胞因子结合事件导致与gp130形成最终复合物。
88.人gp130(包括22个氨基酸的信号肽)是918个氨基酸的蛋白质,并且成熟形式是866个氨基酸,包括597个氨基酸的胞外结构域、22个氨基酸的跨膜结构域和277个氨基酸的胞内结构域。该蛋白的胞外结构域包含gp130的细胞因子结合模块(cbm)。gp130的cbm包括gp130的ig样结构域d1和纤连蛋白iii型结构域d2和d3。人gp130的氨基酸序列可以由uniprot登录号p40189
‑
1(seq id no:2)获得。
89.人il
‑
11rα是422个氨基酸的多肽(uniprot q14626;seq id no:3),与小鼠il
‑
11rα共有约85%的核苷酸和氨基酸序列同一性。据报道,il
‑
11rα有两种同工型,它们在胞质结构域中有所不同(du和williams,同上)。il
‑
11受体α
‑
链(il
‑
11rα)与il
‑
6受体α
‑
链(il
‑
6rα)在结构和功能上有许多相似之处。胞外结构域显示24%的氨基酸同一性,包括特征性保守的trp
‑
ser
‑
x
‑
trp
‑
ser(wsxws)基序。短的胞质结构域(34个氨基酸)缺乏jak/stat信号传导途径激活所需的box 1和box 2区域。
90.小鼠il
‑
11上的受体结合位点已被定位,并确定了三个位点—位点i、ii和iii。与gp130的结合因位点ii区中的置换和位点iii区中的置换而减少。位点iii突变体没有显示可检测的激动剂活性,并具有il
‑
11rα拮抗剂活性(cytokine inhibitors第8章;gennaro ciliberto和rocco savino编辑,marcel dekker,inc.2001)。
91.在本说明书中,il
‑
11受体(il
‑
11r)指能够结合il
‑
11的多肽或多肽复合物。在一些实施方案中,il
‑
11受体能够结合il
‑
11并在表达该受体的细胞中诱导信号转导。
92.il
‑
11受体可来自任何物种,并且包括来自任何物种的il
‑
11受体的同工型、片段、变体或同源物。在优选的实施方案中,该物种是人(智人(homo sapiens))。
93.在一些实施方案中,il
‑
11受体可为il
‑
11rα。在一些实施方案中,il
‑
11受体可为包含il
‑
11rα的多肽复合物。在一些实施方案中,il
‑
11受体可为包含il
‑
11rα和gp130的多肽复合物。在一些实施方案中,il
‑
11受体可为gp130或包含与il
‑
11结合的gp130的复合物。
94.il
‑
11rα的同工型、片段、变体或同源物可任选地表征为与来自给定物种(例如,人)的il
‑
11rα的氨基酸序列具有至少70%,优选地80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%之一的氨基酸序列同一性。il
‑
11rα的同工型、片段、变体或同源物可任选地以结合il
‑
11(优选地来自相同物种)并刺激表达il
‑
11rα和gp130的细胞中的信号转导的能力为特征(例如,如curtis等人,blood,1997,90(11);或karpovich等人,mol.hum.reprod.2003 9(2):75
‑
80中所述)。il
‑
11受体的片段可具有任何长度(按氨基酸数目计),但可以任选地是成熟il
‑
11rα长度的至少25%,并且可具有成熟il
‑
11rα长度的50%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%之一的最大长度。il
‑
11受体片段的片段可具有10个氨基酸的最小长度,并且可具有15、20、25、30、40、50、100、110、120、130、140、150、160、170、180、190、200、250、300、400或415个氨基酸之一的最大长度。
95.il
‑
11信号传导
96.il
‑
11以低亲和力(kd~10nmol/l)与il
‑
11rα结合,仅这些结合配偶体之间的相互作用不足以转导生物信号。能够进行信号转导的高亲和力受体(kd~400至800pmol/l)的产生需要il
‑
11rα和gp130的共表达(curtis等人,blood 1997;90(11):4403
‑
12;hilton等人,embo j 13:4765,1994;nandurkar等人,oncogene 12:585,1996)。il
‑
11与细胞表面il
‑
11rα的结合主要通过丝裂原激活的蛋白激酶(mapk)
‑
级联和janus激酶/信号转导和转录激活因子(jak/stat)途径诱导异二聚化、酪氨酸磷酸化、gp130的激活和下游信号传导(garbers和scheller,同上)。
97.原则上,可溶性il
‑
11rα也可与il
‑
11形成生物活性可溶性复合物(pflanz等人,1999 febs lett,450,117
‑
122),这提出了如下可能性:与il
‑
6相似,在某些情况下,il
‑
11可在结合细胞表面gp130之前结合可溶性il
‑
11rα(garbers和scheller,同上)。curtis等人(blood,1997年12月1日;90(11):4403
‑
12)描述了可溶性小鼠il
‑
11受体α链(sil
‑
11r)的表达,并检查了在表达gp130的细胞中的信号传导。在存在gp130但不存在跨膜il
‑
11r的情况下,sil
‑
11r介导的il
‑
11依赖性m1白血病细胞分化和ba/f3细胞增殖,以及早期细胞内事件,包括gp130、stat3和shp2的磷酸化,类似于通过跨膜il
‑
11r的信号传导。最近已经证实,由与可溶性il
‑
11rα结合的il
‑
11通过细胞膜结合的gp130来激活信号传导(lokau等人,2016 cell reports 14,1761
–
1773)。这种所谓的il
‑
11反式信号传导可能对疾病发病机制很重要,但尚未研究其在人类疾病中的作用。在优选的实施方案中,通过破坏il
‑
11介导的顺式信号传导来实现对il
‑
11介导的信号传导的抑制。
98.如本文所用,“il
‑
11反式信号传导”用于指由与il
‑
11rα结合的il
‑
11与gp130的结合所触发的信号传导。il
‑
11可以非共价复合物形式与il
‑
11rα结合。gp130与膜结合并由细胞表达,其中il
‑
11:il
‑
11rα复合物与gp130结合后发生信号传导。在一些实施方案中,il
‑
11rα可以是可溶性il
‑
11rα。在一些实施方案中,可溶性il
‑
11rα是il
‑
11rα的可溶性(分泌
型)同工型(例如,缺乏跨膜结构域)。在一些实施方案中,可溶性il
‑
11rα是细胞膜结合的il
‑
11rα的胞外结构域的蛋白水解切割的释放产物。在一些实施方案中,il
‑
11rα可以是细胞膜结合的,并且通过gp130的信号传导可由结合到细胞膜结合的il
‑
11rα的il
‑
11的结合触发,称为“il
‑
11顺式信号传导”。
99.il
‑
11介导的信号传导已被证明刺激造血和血小板生成、刺激破骨细胞活性、刺激神经形成、抑制脂肪形成、减少促炎性细胞因子表达、调节细胞外基质(ecm)代谢,并且介导胃肠上皮细胞的正常生长控制(du和williams,同上)。
100.白介素11(il
‑
11)的生理作用仍不清楚。il
‑
11与造血细胞的激活和血小板的产生密切相关。il
‑
11也已被证明能够预防移植物抗宿主病、炎性关节炎和炎性肠病,导致il
‑
11被认为是一种抗炎细胞因子(putoczki和ernst,j leukoc biol 2010,88(6):1109
‑
1117)。然而,这表明il
‑
11具有促炎性和抗炎性、促血管生成作用,并且对瘤形成很重要。最近的研究表明,在小鼠关节炎模型和癌症中,在病毒诱导的炎症期间,很容易检测到il
‑
11,这表明il
‑
11的表达可由病理刺激诱导。il
‑
11还与肿瘤性胃肠上皮中肿瘤促进靶基因的stat3依赖性激活有关(putoczki和ernst,同上)。
101.如本文所用,“il
‑
11信号传导”和“il
‑
11介导的信号传导”指通过il
‑
11或其具有成熟il
‑
11分子功能的片段与il
‑
11受体结合而介导的信号传导。应当理解,“il
‑
11信号传导”和“il
‑
11介导的信号传导”指由il
‑
11/其功能片段(例如,通过与il
‑
11受体结合)引发的信号传导。“信号传导”又指信号转导和其他控制细胞活动的细胞过程。
102.肾损伤
103.本发明的方面涉及肾损伤,特别是急性肾损伤(aki;也称为急性肾衰竭)和/或肾损伤(例如,aki)的诊断、治疗和预防。
104.在本文中,“肾损伤”是指对肾、肾组织和/或一个或多个肾细胞的损害。对细胞/组织/器官的损害可能由对细胞/组织/器官的侵害引起,例如化学或物理治疗/经历。在一些实施方案中,肾损伤可能是化学侵害的结果,例如在药物诱导的肾损伤的情况下,例如顺铂诱导的肾损伤。在一些实施方案中,肾损伤可能由物理侵害引起,例如在由于挤压引起的肾损伤的情况下,或由于对肾组织的手术损害引起的肾损伤的情况下,其可例如在治疗疾病和/或用于肾移植的手术期间发生(例如,肾损伤可具有医源性诱因)。在一些实施方案中,肾损伤可能是缺氧的结果,例如作为缺血的结果,或可能由再灌注引起。在一些实施方案中,肾损伤可能由感染、对感染的免疫应答、癌症和/或自身免疫引起。损害可以是可逆的或不可逆的。
105.在一些实施方案中,肾损伤包括对一个或两个肾的损害。在一些实施方案中,肾损伤包括对肾包膜、肾皮质、肾髓质、肾乳头、肾锥体、肾柱、肾盏、肾小盏、肾大盏、肾门、肾盂、输尿管、肾动脉和肾静脉中的一者或多者的损害。在一些实施方案中,肾损伤包括对肾上皮细胞、肾小管上皮细胞、肾近端小管上皮细胞、肾远端小管上皮细胞、肾壁细胞、足细胞、亨利氏环薄节片细胞(loop of henle thin segment cell)、厚升肢细胞、集合管主细胞、集合管闰细胞和间质肾细胞中的一者或多者的损害。在一些实施方案中,肾损伤包括对肾上皮细胞,例如肾小管上皮细胞,例如肾近端小管上皮细胞的损害。
106.对细胞/组织/器官的损害的特征可在于对细胞/组织/器官的结构和/或功能的改变。例如,对细胞/组织/器官的损害的特征可在于细胞/组织/器官的正常功能的相关性水
平的降低,和/或细胞/组织/器官的受损功能的相关性的增加。举例来说,对肾/肾组织/肾细胞的损害的特征可在于经历肾损害的受试者的尿排出量减少,和/或经历肾损害的受试者的血清肌酸水平增加。对细胞/组织/器官的损害的特征可在于细胞死亡,例如受损器官/组织的细胞死亡。细胞死亡可能由细胞凋亡(即,程序性细胞死亡)或坏死(由于损害导致的细胞过早死亡)引起。
107.如本文所用,“急性肾损伤”通常指肾功能突然恶化。急性肾损伤的特征可在于血清肌酸酐快速增加和/或尿排出量快速减少。
108.急性肾损伤可根据“肾脏疾病改善全球结果(kdigo)小组的推荐声明摘要”,kidney international supplements(2012)2,8
‑
12(全文据此以引用方式并入)来定义和分期。
109.在一些实施方案中,急性肾损伤定义为:(i)在48小时期间内血清肌酸的增加≥0.3mg/dl(≥26.5μmol/l);(ii)血清肌酸增加至≥基线的1.5倍,其已知或推测已在之前的7天内发生;或(iii)6小时内尿量<0.5ml/kg/h。
110.在一些实施方案中,急性肾损伤可以是1、2或3期急性肾损伤。1期急性肾损伤可定义为:(i)血清肌酸增加至基线的1.5
‑
1.9倍,(ii)血清肌酸增加至≥0.3mg/dl(≥26.5μmol/l),或(iii)6
‑
12小时内尿量<0.5ml/kg/h。2期急性肾损伤可定义为:(i)血清肌酸增加至基线的2.0
‑
2.9倍,或(ii)≥12小时尿量<0.5ml/kg/h。3期急性肾损伤可定义为:(i)血清肌酸增加至≥基线的3.0倍,(ii)血清肌酸增加至≥4.0mg/dl(≥353.6μmol/l),(iii)开始肾替代疗法,(iv)在<18岁的患者中,egfr降低至<35ml/min/1.73m2;(v)≥24小时尿量<0.3ml/kg/h,或(vi)≥12小时无尿。
111.肾损伤的特征可在于对肾小管上皮细胞(tec)的损害和/或tec向上皮
‑
间充质细胞样表型(即,emt)的转化。tec向间充质细胞样表型的转化的特征可以是,例如,e
‑
钙粘蛋白的表达降低、snail的表达增加和/或acta2的表达增加。
112.肾损伤可具有任何诱因,示例包括由机械(即,物理)损害或损伤、化学损害或损伤、缺血或遗传倾向引起的肾损伤。该诱因或损害通常将导致肾功能受损,这可能导致肾衰竭。
113.机械损害或损伤可包括对受试者、肾、tec或足细胞的物理损伤。它也可包括例如尿道的肾小管阻塞/堵塞。
114.化学损害或损伤可能由药物、药品、毒素、草药或膳食补充剂或其他向受试者施用、被受试者吸收或摄入的化学药剂引起。在一些实施方案中,化学损害是施用此类药剂以治疗不在肾中发生或在肾和一种或多种其他组织中均发生的疾病或病症的副作用。在一些实施方案中,化学损伤是为了预防或治疗癌症而向受试者施用的化疗剂的施用的副作用。在一些实施方案中,肾损伤是药物诱导的肾损伤或药物诱导的急性肾损伤。在一些实施方案中,由于施用某些化学剂例如磺胺类、甲氨蝶呤、阿昔洛韦、二甘醇、氨苯蝶啶,可能出现例如尿道的肾小管阻塞/堵塞。
115.缺血性损害可能是由于流向肾的血流量减少而引起的,这可能是由许多因素引起的,诸如由于败血症、失血或手术导致的低血压,或者是向受试者施用以治疗另一种疾病、障碍或病症的化学药剂(例如,药物或药品)的作用所引起的。缺血引起的肾损伤可以是缺血诱导的肾损伤,或缺血诱导的急性肾损伤。由挤压伤引起的肾损伤可以是缺血诱导的肾
损伤伴血管收缩,也可以由管型机械因子(tubular cast mechanical factor)或循环因子(例如,肌红蛋白)的毒性作用引起。
116.在一些实施方案中,肾损伤(其可为aki)的特征在于对肾的管状上皮细胞(tec)(即,肾小管上皮细胞)的损害,在一些情况下该损害可包括或导致其死亡。tec可能位于近端或远端,两者都可能在aki中受损,肾小球中的足细胞也可能受损。对tec的损害也可能是任何类型的损害、损伤或侵害,例如,如上所述,这可能是机械、化学或缺血性损害。对tec的损害是肾损伤(尤其是aki)的常见致病因素。tec的增殖提供了恢复和修复肾功能的机制,而tec增殖失败可导致疾病发展和进展,例如导致慢性肾病和肾衰竭。也可能发生足细胞前体增殖以修复肾小球功能,但不像tec增殖那样得到很好的描述。
117.在一些实施方案中,肾损伤是肾毒性,或特征在于肾毒性。如本文所用,肾毒性是指对肾的毒性。毒性又指损害,例如,如本文所述。肾毒性可以是某些物质对肾功能的毒性作用的结果,因此可被看作是化学损害或损伤的结果。与化学损害或损伤一样,肾毒性可能是施用药剂以治疗不在肾中发生或在肾和一种或多种其他组织中均发生的疾病或病症的副作用。在一些实施方案中,肾毒性可以是为了预防或治疗癌症而向受试者施用的化疗剂的施用的副作用。因此,肾毒性可以是药物诱导的肾损伤或药物诱导的急性肾损伤的形式。
118.如上所述,药物诱导的肾损伤、药物诱导的急性肾损伤或药物诱导的肾毒性可能是作为旨在治疗在肾外、肾内或两者的组织中发生的疾病、障碍或病症的药物或药品的施用副作用而出现。已知许多药物表现出这样的副作用,其可能取决于所治疗的病症、所治疗的受试者、剂量、给药方案或施用方式,以及受试者在治疗前表现出部分肾衰竭的程度。例如,据报道下列药剂都具有诱导肾损伤的潜力:利尿剂、β
‑
受体阻滞剂、血管扩张剂、ace抑制剂、氨基糖苷类抗生素(例如,庆大霉素)、两性霉素b、顺铂、nsaid(例如,阿司匹林、布洛芬、双氯芬酸)、环孢素、锂盐、环磷酰胺、磺胺类、甲氨蝶呤、阿昔洛韦、二甘醇、氨苯蝶啶、β
‑
内酰胺抗生素、万古霉素、利福平、环丙沙星、雷尼替丁、西咪替丁、呋塞米、噻嗪类、苯妥英。任选地,药物诱导的肾损伤不是叶酸诱导的肾损伤。
119.在一些实施方案中,药物诱导的肾损伤、药物诱导的急性肾损伤或药物诱导的肾毒性可能是作为旨在治疗或预防受试者的癌症的化疗剂的施用副作用而出现。化疗剂的示例包括烷化剂,诸如顺铂、卡铂、氮芥、环磷酰胺、苯丁酸氮芥、异环磷酰胺;嘌呤或嘧啶抗代谢物,诸如硫唑嘌呤或巯基嘌呤;生物碱和萜类化合物,诸如长春花生物碱(例如,长春新碱、长春碱、长春瑞滨、长春地辛)、鬼臼毒素、依托泊苷、替尼泊苷、紫杉烷类例如紫杉醇(taxol
tm
)、多西他赛;拓扑异构酶抑制剂,诸如i型拓扑异构酶抑制剂喜树碱、伊立替康和拓扑替康,或ii型拓扑异构酶抑制剂安吖啶、磷酸依托泊苷、替尼泊苷;抗肿瘤抗生素(例如,蒽环类抗生素),例如更生霉素、多柔比星(adriamycin
tm
)、表柔比星、博来霉素、雷帕霉素;基于抗体的药剂,诸如抗vegf、抗tnfα、抗il
‑
2、抗gpiib/iiia、抗cd
‑
52、抗cd20、抗rsv、抗her2/neu(erbb2)、抗tnf受体、抗egfr抗体、单克隆抗体或抗体片段,示例包括:西妥昔单抗、帕尼单抗、英夫利昔单抗、巴利昔单抗、贝伐单抗阿昔单抗、达克珠单抗、吉妥单抗、阿仑单抗、利妥昔单抗帕利珠单抗、曲妥珠单抗、依那西普、阿达木单抗、尼妥珠单抗;以及egfr抑制剂,诸如厄洛替尼、西妥昔单抗、吉非替尼。
120.在一些优选的实施方案中,本发明涉及顺铂诱导的肾损伤的诊断、治疗和/或预防。这可包括顺铂诱导的急性肾损伤或顺铂诱导的肾毒性。顺铂(二氯二氨基铂;(sp
‑4‑
2)
‑
二胺二氯铂(ii))是一种化疗剂,该化疗剂广泛用于治疗一系列癌症,包括头颈癌、乳腺癌、肺癌、睾丸癌、卵巢癌、脑癌和膀胱癌,并且被广泛认为会导致肾损伤和涉及肾小管损害和坏死的功能障碍(例如,oh等人,electrolyte blood press,2014年12月;12(2):55
‑
65;pa arunkumar等人,asian pac j trop biomed,2012年8月,2(8):640
‑
644)。其他基于铂的化疗剂也引起肾损害。
121.虽然认识到患有肾损伤的受试者也可能出现肾纤维化,作为具有可分离病因的疾病症状或作为肾损伤的继发效应,但在一些实施方案中,被诊断、治疗或预防的肾损伤不是肾纤维化,例如肾纤维化。在一些实施方案中,受试者没有纤维化。在一些实施方案中,tec损害在没有纤维化的情况下发生。在一些实施方案中,纤维化单独地(例如,继发于)aki出现,例如由于tec的不完全再生。在一些实施方案中,受试者中的受损tec不是促纤维化tec。在一些实施方案中,不出现纤维化。
122.能够抑制il
‑
11的作用的药剂
123.本发明的方面涉及对il
‑
11介导的信号传导的抑制。
124.在本文中,“抑制”是指相对于对照条件的减少、降低或减轻。例如,能够抑制il
‑
11介导的信号传导的药剂对il
‑
11作用的抑制是指相比于不存在该药剂和/或存在适当的对照药剂的情况,il
‑
11介导的信号传导的范围/程度的减少、降低或减轻。
125.抑制在本文中也可称为中和或拮抗。也就是说,能够抑制il
‑
11介导的信号传导(例如,il
‑
11或含il
‑
11的复合物介导的相互作用、信号传导或其他活性)的药剂可被称为关于相关功能或过程的“中和”或“拮抗剂”药剂。例如,能够抑制il
‑
11介导的信号传导的药剂可称为能够中和il
‑
11介导的信号传导的药剂,或者可被称为il
‑
11介导的信号传导的拮抗剂。
126.il
‑
11信号传导途径提供了对il
‑
11信号传导的抑制的多种途径。能够抑制il
‑
11介导的信号传导的药剂可例如通过抑制参与通过il
‑
11受体的信号传导或这种信号传导所必需的一种或多种因子的作用来抑制il
‑
11介导的信号传导。
127.例如,对il
‑
11信号传导的抑制可通过破坏il
‑
11(或含il
‑
11的复合物,例如il
‑
11和il
‑
11rα的复合物)和il
‑
11受体(例如il
‑
11rα,包含il
‑
11rα的受体复合物、gp130,或包含il
‑
11rα和gp130的受体复合物)之间的相互作用来实现。在一些实施方案中,通过抑制例如il
‑
11、il
‑
11rα和gp130中的一者或多者的基因或蛋白表达,实现对il
‑
11介导的信号传导的抑制。
128.在实施方案中,通过破坏il
‑
11介导的顺式信号传导但不破坏il
‑
11介导的反式信号传导来实现对il
‑
11介导的信号传导的抑制,例如,通过抑制gp130介导的涉及膜结合il
‑
11rα的顺式复合物来实现对il
‑
11介导的信号传导的抑制。在实施方案中,通过破坏il
‑
11介导的反式信号传导但不破坏il
‑
11介导的顺式信号传导来实现对il
‑
11介导的信号传导的抑制,即,通过抑制gp130介导的反式信号传导复合物(诸如与可溶性il
‑
11rα结合的il
‑
11或与可溶性il
‑
6r结合的il
‑
6)来实现对il
‑
11介导的信号传导的抑制。在实施方案中,通过破坏il
‑
11介导的顺式信号传导和il
‑
11介导的反式信号传导来实现对il
‑
11介导的信号传导的抑制。如本文所述的任何药剂都可用于抑制il
‑
11介导的顺式和/或反式信号传导。
129.在其他示例中,通过破坏il
‑
11/il
‑
11rα/gp130下游的信号传导途径,可实现对il
‑
11信号传导的抑制。也就是说,在一些实施方案中,对il
‑
11介导的信号传导的抑制/拮
抗包括对通过il
‑
11/il
‑
11受体复合物的信号传导下游的信号传导途径/过程/因子的抑制。
130.在一些实施方案中,对il
‑
11介导的信号传导的抑制/拮抗包括对通过il
‑
11/il
‑
11受体复合物所激活的细胞内信号传导途径的信号传导的抑制。在一些实施方案中,对il
‑
11介导的信号传导的抑制/拮抗包括对一种或多种因子的抑制,这些因子的表达/活性由于通过il
‑
11/il
‑
11受体复合物的信号传导而上调。
131.在一些实施方案中,本发明的方法采用能够抑制jak/stat信号传导的药剂。在一些实施方案中,能够抑制jak/stat信号传导的药剂能够抑制jak1、jak2、jak3、tyk2、stat1、stat2、stat3、stat4、stat5a、stat5b和/或stat6的作用。例如,药剂可能能够抑制jak/stat蛋白的激活,抑制jak蛋白或stat蛋白与细胞表面受体例如il
‑
11rα或gp130的相互作用,抑制jak蛋白的磷酸化,抑制jak蛋白和stat蛋白之间的相互作用,抑制stat蛋白的磷酸化,抑制stat蛋白的二聚化,抑制stat蛋白向细胞核的易位,抑制stat蛋白与dna的结合,和/或促进jak蛋白和/或stat蛋白的降解。在一些实施方案中,jak/stat抑制剂选自鲁索替尼(jakafi/jakavi;incyte)、托法替尼(xeljanz/jakvinus;nih/pfizer)、奥拉替尼(apoquel)、巴瑞替尼(olumiant;incyte/eli lilly)、非洛替尼(g
‑
146034/glpg
‑
0634;galapagos nv)、甘多替尼(ly
‑
2784544;eli lilly)、来他替尼(cep
‑
701;teva)、莫罗替尼(gs
‑
0387/cyt
‑
387;gilead sciences)、帕克替尼(sb1518;cti)、pf
‑
04965842(pfizer)、乌帕替尼(abt
‑
494;abbvie)、培非替尼(asp015k/jnj
‑
54781532;astellas)、菲卓替尼(sar302503;celgene)、葫芦素i(jsi
‑
124)和chz868。
132.在一些实施方案中,本发明的方法采用能够抑制mapk/erk信号传导的药剂。在一些实施方案中,能够抑制mapk/erk信号传导的药剂能够抑制grb2的作用、抑制raf激酶的作用、抑制mek蛋白的作用、抑制map3k/map2k/mapk和/或myc的激活和/或抑制stat蛋白的磷酸化。在一些实施方案中,能够抑制erk信号传导的药剂能够抑制erk p42/44。在一些实施方案中,erk抑制剂选自sch772984、sc1、vx
‑
11e、del
‑
22379、索拉非尼(nexavar;bayer/onyx)、sb590885、plx4720、xl281、raf265(novartis)、恩可非尼(lgx818/braftovi;array biopharma)、达拉菲尼(tafinlar;gsk)、维莫非尼(zelboraf;roche)、考比替尼(cotellic;roche)、ci
‑
1040、pd0325901、比美替尼(mek162/mektovi;array biopharma)、司美替尼(azd6244;array/astrazeneca)和曲美替尼(gsk1120212/mekinist;novartis)。在一些实施方案中,本发明的方法采用能够抑制c
‑
jun n
‑
末端激酶(jnk)信号传导/活性的药剂。在一些实施方案中,能够抑制jnk信号传导/活性的药剂能够抑制jnk(例如,jnk1、jnk2)的作用和/或磷酸化。在一些实施方案中,jnk抑制剂选自sp600125、cep 1347、tcs jnk 6o、c
‑
jun肽、su3327、aeg 3482、tcs jnk 5a、bi78d3、iq3、sr3576、iq1s、jip
‑
1(153
‑
163)和cc401二盐酸盐。
133.widjaja等人,biorxiv(2019)830018证实了,nox4表达和活性由通过il
‑
11/il
‑
11rα/gp130的信号传导而上调。nox4是一种nadph氧化酶,也是活性氧(ros)的来源。nox4的表达在具有肝细胞特异性的il11表达的转基因小鼠中被上调,而用il11刺激的原代人肝细胞上调nox4表达。
134.在一些实施方案中,本发明采用能够抑制nox4表达(基因或蛋白质表达)或功能的药剂。在一些实施方案中,本发明采用能够抑制il
‑
11介导的nox4表达/功能上调的药剂。能
够抑制nox4表达或功能的药剂在本文中可称为nox4抑制剂。例如,nox4抑制剂可能能够降低nox4的表达(例如,基因和/或蛋白质表达)、降低编码nox4的rna的水平、降低nox4蛋白质的水平和/或降低nox4活性的水平(例如,降低nox4介导的nadph氧化酶活性和/或nox4介导的ros产生)。
135.nox4抑制剂包括nox4结合分子和能够降低nox4表达的分子。nox4结合抑制剂包括表现为nox4功能拮抗剂的肽/核酸适体、抗体(和抗体片段)和nox4的相互作用配偶体的片段,以及nox4的小分子抑制剂。能够降低nox4表达的分子包括nox4的反义rna(例如,sirna、shrna)。在一些实施方案中,nox4抑制剂选自描述于altenhofer等人,antioxid redox signal.(2015)23(5):406
–
427或augsburder等人,redox biol.(2019)26:101272的nox4抑制剂,诸如gkt137831。
136.结合剂
137.在一些实施方案中,能够抑制il
‑
11介导的信号传导的药剂可与il
‑
11结合。在一些实施方案中,能够抑制il
‑
11介导的信号传导的药剂可与il
‑
11受体(例如,il
‑
11rα、gp130或含有il
‑
11rα和/或gp130的复合物)结合。这些药剂的结合可通过降低/阻止il
‑
11与il
‑
11受体结合的能力来抑制il
‑
11介导的信号传导,从而抑制下游信号传导。这些药剂的结合可通过降低/阻止il
‑
11与il
‑
11受体(例如,il
‑
11rα和/或gp130)结合的能力来抑制il
‑
11介导的顺式和/或反式信号传导,从而抑制下游信号传导。药剂可与反式信号传导复合物诸如il
‑
11和可溶性il
‑
11rα结合,并抑制gp130介导的信号传导。
138.能够与il
‑
11/含il
‑
11的复合物或il
‑
11受体结合的药剂可以是任何种类,但在一些实施方案中,该药剂可以是抗体、其抗原结合片段、多肽、肽、核酸、寡核苷酸、适体或小分子。该药剂可以分离或纯化的形式提供,或者可被配制为药物组合物或药物。
139.抗体和抗原结合片段
140.在一些实施方案中,能够与il
‑
11/含il
‑
11的复合物或il
‑
11受体结合的药剂是抗体或其抗原结合片段。在一些实施方案中,能够与il
‑
11/含il
‑
11的复合物或il
‑
11受体结合的药剂是多肽,例如诱饵受体分子。在一些实施方案中,能够与il
‑
11/含il
‑
11的复合物或il
‑
11受体结合的药剂可以是适体。
141.在一些实施方案中,能够与il
‑
11/含il
‑
11的复合物或il
‑
11受体结合的药剂是抗体或其抗原结合片段。“抗体”在本文中以最广泛的含义使用,并且涵盖单克隆抗体、多克隆抗体、单特异性和多特异性抗体(例如,双特异性抗体)和抗体片段,只要它们表现出与相关靶分子的结合。
142.鉴于当今与单克隆抗体技术相关的技术,可制备针对大多数抗原的抗体。抗原结合部分可以是抗体的一部分(例如,fab片段)或合成抗体片段(例如,单链fv片段[scfv])。针对选定抗原的单克隆抗体可通过已知技术制备,例如在“单克隆抗体:技术手册”,h zola(crc出版社,1988)和“单克隆杂交瘤抗体:技术和应用”,j g r hurrell(crc出版社,1982)中所公开的那些技术。neuberger等人(1988,第八届国际生物技术研讨会第二部分,792
‑
799)讨论了嵌合抗体。单克隆抗体(mab)在本发明的方法中特别有用,并且是特异性靶向抗原上的单个表位的抗体的同质群体。
[0143]
多克隆抗体也可用于本发明的方法中。单特异性多克隆抗体是优选的。合适的多克隆抗体可使用本领域熟知的方法制备。
[0144]
抗体的抗原结合片段诸如fab和fab2片段也可作为基因工程化的抗体和抗体片段使用/提供。抗体的可变重链(vh)和可变轻链(vl)结构域参与抗原识别,这一事实首先通过早期蛋白酶消化实验为人所知。啮齿动物抗体的“人源化”进一步证实了这一点。啮齿动物来源的可变结构域可与人来源的恒定结构域融合,使得所得抗体保留啮齿动物亲本抗体的抗原特异性(morrison等人,(1984)proc.natl.acad.sd.usa 81,6851
‑
6855)。
[0145]
根据本公开的抗体和抗原结合片段包含能够与相关靶分子(即,il
‑
11/含il
‑
11的复合物/il
‑
11受体)结合的抗体的互补决定区(cdr)。
[0146]
能够与il
‑
11结合的抗体包括,例如,单克隆小鼠抗人il
‑
11抗体克隆#22626,目录号mab218(r&d systems,mn,usa),用于例如bockhorn等人,nat.commun.(2013)4(0):1393;克隆6d9a(abbiotec);克隆kt8(abbiotec);克隆m3103f11(biolegend);克隆1f1(abnova corporation);克隆3c6(abnova corporation);克隆gf1(lifespan biosciences);克隆13455(source bioscience);11h3/19.6.1(hermann等人,arthritis rheum.(1998)41(8):1388
‑
97);ab
‑
218
‑
na(r&d systems);x203(ng等人,sci transl med.(2019)11(511)pii:eaaw1237,也发表为ng等人,“il
‑
11是特发性肺纤维化的治疗靶点”,biorxiv 336537;doi:https://doi.org/10.1101/336537);以及us 2009/0202533 a1、wo 99/59608a2、wo 2018/109174 a2和wo 2019/238882a1中公开的抗il
‑
11抗体。
[0147]
特别地,抗il
‑
11抗体克隆22626(也称为mab218)已表明是il
‑
11介导的信号传导的拮抗剂,例如在schaefer等人,nature(2017)552(7683):110
–
115中所述。单克隆抗体11h3/19.6.1在hermann等人,arthritis rheum.(1998)41(8):1388
‑
97中公开为中和抗il
‑
11igg1。来自r&d systems的ab
‑
218
‑
na(例如,用于mccoy等人,bmc cancer(2013)13:16中)是中和抗il
‑
11抗体的另一个示例。wo 2018/109174 a2和wo 2019/238882 a1公开了il
‑
11介导的信号传导的另一些示例性抗il
‑
11抗体拮抗剂。公开于ng等人,“il
‑
11是特发性肺纤维化的治疗靶点”,biorxiv 336537;doi:https://doi.org/10.1101/336537和wo 2019/238882 a1中的x203(也称为enx203)是il
‑
11介导的信号传导的抗il
‑
11抗体拮抗剂,并且包含根据wo 2019/238882 a1的seq id no:92的vh区(本公开的seq id no:22)和根据wo 2019/238882 a1的seq id no:94的vl区(本公开的seq id no:23)。x203的人源化形式描述于wo 2019/238882 a1中,包括henx203,其包含根据wo 2019/238882 a1的seq id no:117的vh区(本公开的seq id no:30)和根据wo 2019/238882 a1的seq id no:122的vl区(本公开的seq id no:31)。enx108a是il
‑
11介导的信号传导的抗il
‑
11抗体拮抗剂的另一个示例,并且包含根据wo 2019/238882 a1的seq id no:8的vh区(本公开的seq id no:26)和根据wo 2019/238882 a1的seq id no:20的vl区(本公开的seq id no:27)。
[0148]
能够与il
‑
11rα结合的抗体包括,例如,单克隆抗体克隆025(sino biological)、克隆epr5446(abcam)、克隆473143(r&d systems)、克隆8e2、8d10和8e4,以及us 2014/0219919 a1中所述的8e2的亲和力成熟变体、在blanc等人(j.immunol methods.2000jul 31;241(1
‑
2);43
‑
59)中所述的单克隆抗体、x209(widjaja等人,gastroenterology(2019)157(3):777
‑
792,也发表为widjaja等人,“il
‑
11中和疗法针对nash中肝星状细胞诱导的肝脏炎症和纤维化”,biorxiv 470062;doi:https://doi.org/10.1101/470062)、在wo 2014121325 a1和us 2013/0302277 a1中公开的抗体,以及在us 2009/0202533a1、wo 99/59608a2、wo 2018/109170 a2和wo 2019/238884 a1中公开的抗il
‑
11rα抗体。
31;241(1
‑
2);43
‑
59)中描述的测定来评价il
‑
11或il
‑
11rα结合抗体拮抗il
‑
11介导的信号传导的能力。简而言之,可在体外评价il
‑
11和il
‑
11rα结合抗体抑制来自适当物种的表达il
‑
11rα和gp130的ba/f3细胞以响应来自适当物种的il
‑
11刺激而增殖的能力。另选地,通过评价αsma表达(如在例如wo2018/109174a2(实施例6)和wo 2018/109170 a2(实施例6);ng等人,sci transl med.(2019)11(511)pii:eaaw1237;以及widjaja等人,gastroenterology(2019)157(3):777
‑
792中所述),可体外分析il
‑
11和il
‑
11rα结合抗体抑制用tgfβ1刺激成纤维细胞后成纤维细胞向肌成纤维细胞转化的能力。
[0155]
抗体通常包含六个cdr;轻链可变区(vl)中有三个:lc
‑
cdr1、lc
‑
cdr2、lc
‑
cdr3,并且重链可变区(vh)中有三个:hc
‑
cdr1、hc
‑
cdr2和hc
‑
cdr3。六个cdr一起限定了抗体的互补位,它是抗体的与靶分子结合的部分。vh区和vl区包含每个cdr任一侧的框架区(fr),其为cdr提供支架。从n末端到c末端,vh区包括以下结构:n末端
‑
[hc
‑
fr1]
‑
[hc
‑
cdr1]
‑
[hc
‑
fr2]
‑
[hc
‑
cdr2]
‑
[hc
‑
fr3]
‑
[hc
‑
cdr3]
‑
[hc
‑
fr4]
‑
c末端;并且vl区包括以下结构:n末端
‑
[lc
‑
fr1]
‑
[lc
‑
cdr1]
‑
[lc
‑
fr2]
‑
[lc
‑
cdr2]
‑
[lc
‑
fr3]
‑
[lc
‑
cdr3]
‑
[lc
‑
fr4]
‑
c末端。
[0156]
有几种不同的定义抗体cdr和fr的惯例,诸如在kabat等人,“具有免疫学意义的蛋白质序列”,第5版,国立卫生研究院公共卫生服务中心,贝塞斯达,马里兰州(1991),chothia等人,j.mol.biol.196:901
‑
917(1987)中描述的那些惯例;以及vbase2,如描述于retter等人,nucl.acids res.(2005)33(suppl 1):d671
‑
d674。本文所述抗体的vh区和vl区的cdr和fr根据kabat系统定义。
[0157]
在一些实施方案中,根据本公开的抗体或其抗原结合片段衍生自与il
‑
11特异性结合的抗体(例如,enx108a、enx203或henx203)。在一些实施方案中,根据本公开的抗体或其抗原结合片段衍生自与il
‑
11rα特异性结合的抗体(例如,enx209或henx209)。
[0158]
根据本公开的抗体和抗原结合片段优选地抑制il
‑
11介导的信号传导。这种抗体/抗原结合片段可被描述为il
‑
11介导的信号传导的拮抗剂,和/或可被描述为具有中和il
‑
11介导的信号传导的能力。
[0159]
在一些实施方案中,抗体/抗原结合片段包含与il
‑
11结合的抗体的cdr。在一些实施方案中,抗体/抗原结合片段包含本文所述的il
‑
11结合抗体(例如,enx108a、enx203或henx203)的cdr或衍生自这些cdr的cdr。
[0160]
在一些实施方案中,抗体/抗原结合片段包含掺入以下cdr的vh区:
[0161]
(1)
[0162]
具有seq id no:34的氨基酸序列的hc
‑
cdr1
[0163]
具有seq id no:35的氨基酸序列的hc
‑
cdr2
[0164]
具有seq id no:36的氨基酸序列的hc
‑
cdr3,
[0165]
或其变体,其中hc
‑
cdr1、hc
‑
cdr2或hc
‑
cdr3中的一者或多者中的一个或两个或三个氨基酸被另一氨基酸置换。
[0166]
在一些实施方案中,抗体/抗原结合片段包含掺入以下cdr的vl区:
[0167]
(2)
[0168]
具有seq id no:37的氨基酸序列的lc
‑
cdr1
[0169]
具有seq id no:38的氨基酸序列的lc
‑
cdr2
[0170]
具有seq id no:39的氨基酸序列的lc
‑
cdr3,
[0171]
或其变体,其中lc
‑
cdr1、lc
‑
cdr2或lc
‑
cdr3中的一者或多者中的一个或两个或三个氨基酸被另一氨基酸置换。
[0172]
在一些实施方案中,抗体/抗原结合片段包含掺入以下cdr的vh区:
[0173]
(3)
[0174]
具有seq id no:40的氨基酸序列的hc
‑
cdr1
[0175]
具有seq id no:41的氨基酸序列的hc
‑
cdr2
[0176]
具有seq id no:42的氨基酸序列的hc
‑
cdr3,
[0177]
或其变体,其中hc
‑
cdr1、hc
‑
cdr2或hc
‑
cdr3中的一者或多者中的一个或两个或三个氨基酸被另一氨基酸置换。
[0178]
在一些实施方案中,抗体/抗原结合片段包含掺入以下cdr的vl区:
[0179]
(4)
[0180]
具有seq id no:43的氨基酸序列的lc
‑
cdr1
[0181]
具有seq id no:44的氨基酸序列的lc
‑
cdr2
[0182]
具有seq id no:45的氨基酸序列的lc
‑
cdr3,
[0183]
或其变体,其中lc
‑
cdr1、lc
‑
cdr2或lc
‑
cdr3中的一者或多者中的一个或两个或三个氨基酸被另一氨基酸置换。
[0184]
在一些实施方案中,抗体/抗原结合片段包含掺入根据(1)的cdr的vh区和掺入根据(2)的cdr的vl区。在一些实施方案中,抗体/抗原结合片段包含掺入根据(3)的cdr的vh区和掺入根据(4)的cdr的vl区。
[0185]
在一些实施方案中,抗体/抗原结合片段包含与il
‑
11结合的抗体的vh区和vl区。在一些实施方案中,抗体/抗原结合片段包含本文所述的il
‑
11结合抗体(例如,enx108a、enx203或henx203)的vh区和vl区,或衍生自该vh区和vl区的vh区和vl区。
[0186]
在一些实施方案中,抗体/抗原结合片段包含vh区,该vh区包含与seq id no:26的氨基酸序列具有至少70%序列同一性,更优选地至少75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性之一的氨基酸序列。在一些实施方案中,抗体/抗原结合片段包含vl区,该vl区包含与seq id no:27的氨基酸序列具有至少70%序列同一性,更优选地至少75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性之一的氨基酸序列。在一些实施方案中,抗体/抗原结合片段包含vh区和vl区,该vh区包含与seq id no:26的氨基酸序列具有至少70%序列同一性,更优选地至少75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性之一的氨基酸序列,该vl区包含与seq id no:27的氨基酸序列具有至少70%序列同一性,更优选地至少75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性之一的氨基酸序列。
[0187]
在一些实施方案中,抗体/抗原结合片段包含vh区,该vh区包含与seq id no:22的氨基酸序列具有至少70%序列同一性,更优选地至少75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性之一的氨基酸序列。在一些实施方案中,抗体/抗原结合片段包含vl区,该vl区包含与seq id no:23的氨基酸序列具有至少70%序列同一性,更优选地至少75%、80%、85%、86%、87%、
88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性之一的氨基酸序列。在一些实施方案中,抗体/抗原结合片段包含vh区和vl区,该vh区包含与seq id no:22的氨基酸序列具有至少70%序列同一性,更优选地至少75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性之一的氨基酸序列,该vl区包含与seq id no:23的氨基酸序列具有至少70%序列同一性,更优选地至少75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性之一的氨基酸序列。
[0188]
在一些实施方案中,抗体/抗原结合片段包含vh区,该vh区包含与seq id no:30的氨基酸序列具有至少70%序列同一性,更优选地至少75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性之一的氨基酸序列。在一些实施方案中,抗体/抗原结合片段包含vl区,该vl区包含与seq id no:31的氨基酸序列具有至少70%序列同一性,更优选地至少75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性之一的氨基酸序列。在一些实施方案中,抗体/抗原结合片段包含vh区和vl区,该vh区包含与seq id no:30的氨基酸序列具有至少70%序列同一性,更优选地至少75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性之一的氨基酸序列,该vl区包含与seq id no:31的氨基酸序列具有至少70%序列同一性,更优选地至少75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性之一的氨基酸序列。
[0189]
在一些实施方案中,抗体/抗原结合片段包含与il
‑
11rα结合的抗体的cdr。在一些实施方案中,抗体/抗原结合片段包含本文所述的il
‑
11rα结合抗体(例如,enx209或henx209)的cdr或衍生自这些cdr的cdr。
[0190]
在一些实施方案中,抗体/抗原结合片段包含掺入以下cdr的vh区:
[0191]
(5)
[0192]
具有seq id no:46的氨基酸序列的hc
‑
cdr1
[0193]
具有seq id no:47的氨基酸序列的hc
‑
cdr2
[0194]
具有seq id no:48的氨基酸序列的hc
‑
cdr3,
[0195]
或其变体,其中hc
‑
cdr1、hc
‑
cdr2或hc
‑
cdr3中的一者或多者中的一个或两个或三个氨基酸被另一氨基酸置换。
[0196]
在一些实施方案中,抗体/抗原结合片段包含掺入以下cdr的vl区:
[0197]
(6)
[0198]
具有seq id no:49的氨基酸序列的lc
‑
cdr1
[0199]
具有seq id no:50的氨基酸序列的lc
‑
cdr2
[0200]
具有seq id no:51的氨基酸序列的lc
‑
cdr3,
[0201]
或其变体,其中lc
‑
cdr1、lc
‑
cdr2或lc
‑
cdr3中的一者或多者中的一个或两个或三个氨基酸被另一氨基酸置换。
[0202]
在一些实施方案中,抗体/抗原结合片段包含掺入根据(5)的cdr的vh区和掺入根据(6)的cdr的vl区。
[0203]
在一些实施方案中,抗体/抗原结合片段包含与il
‑
11rα结合的抗体的vh区和vl
区。在一些实施方案中,抗体/抗原结合片段包含本文所述的il
‑
11rα结合抗体(例如,enx209或henx209)的vh区和vl区,或衍生自该vh区和vl区的vh区和vl区。
[0204]
在根据本发明的实施方案中,其中参考氨基酸序列(例如,本文所述的cdr序列、vh区序列或vl区序列)的一个或多个氨基酸被另一氨基酸置换,这些置换可以是例如根据下表的保守置换。在一些实施方案中,中间列中相同区块中的氨基酸被置换。在一些实施方案中,最右列中同一行中的氨基酸被置换:
[0205][0206]
在一些实施方案中,置换可以是功能保守的。也就是说,在一些实施方案中,相对于等同的未置换的分子,置换可不影响(或可基本上不影响)包含该置换的抗体/片段的一种或多种功能特性(例如,靶结合)。
[0207]
在一些实施方案中,相对于参考vh区或vl区序列的置换可集中在vh区或vl区序列的特定区域或多个区域中。例如,来自参考vh区或vl区序列的变异可集中在框架区(fr1、fr2、fr3和/或fr4)中的一个或多个框架区中。
[0208]
根据本公开的抗体和抗原结合片段可使用能够与相关靶分子结合的单克隆抗体(mab)的序列来设计和制备。也可使用/提供抗体的抗原结合区,诸如单链可变片段(scfv)、fab和fab2片段。“抗原结合区”或“抗原结合片段”是能够与给定抗体所特异性针对的靶标结合的抗体的任何片段。
[0209]
在一些实施方案中,该抗体/片段包含能够与il
‑
11、含il
‑
11的复合物或il
‑
11受体结合的抗体的vl区和vh区。抗体的抗原结合区的vl区和vh区一起构成fv区。在一些实施方案中,该抗体/片段包含能够与il
‑
11、含il
‑
11的复合物或il
‑
11受体结合的抗体的fv区或由其组成。fv区可表达为单链,其中vh区和vl区例如通过柔性寡肽共价连接。因此,抗体/片段可包含scfv或由scfv组成,该scfv包含能够与il
‑
11、含il
‑
11的复合物或il
‑
11受体结合的抗体的vl区和vh区。
[0210]
抗体的抗原结合区的vl区和轻链恒定(cl)区以及vh区和重链恒定1(ch1)区一起构成fab区。在一些实施方案中,该抗体/片段包含能够与il
‑
11、含il
‑
11的复合物或il
‑
11受体结合的抗体的fab区或由其组成。
[0211]
在一些实施方案中,抗体/片段包含能够与il
‑
11、含il
‑
11的复合物或il
‑
11受体结合的全抗体或由其组成。“全抗体”指具有与免疫球蛋白(ig)结构基本上相似的结构的抗体。不同种类的免疫球蛋白和它们的结构描述于例如schroeder和cavacini,j allergy clin immunol.(2010)125(202):s41
‑
s52,该文献全文据此以引用方式并入。g型免疫球蛋白(即,igg)是包含两条重链和两条轻链的约150kda糖蛋白。从n末端到c末端,重链包含vh,
然后包含三个恒定结构域(ch1、ch2和ch3)的重链恒定区,并且类似地,轻链包含vl,然后包含cl。根据重链,免疫球蛋白可被分类为igg(例如,igg1、igg2、igg3、igg4)、iga(例如,iga1、iga2)、igd、ige或igm。轻链可以是κ或λ。
[0212]
在一些实施方案中,本公开的抗体/抗原结合片段包含免疫球蛋白重链恒定序列。在一些实施方案中,免疫球蛋白重链恒定序列可以是人免疫球蛋白重链恒定序列。在一些实施方案中,免疫球蛋白重链恒定序列是或衍生自igg(例如,igg1、igg2、igg3、igg4)、iga(例如,iga1、iga2)、igd、ige或igm,例如人igg(例如,higg1、higg2、higg3、higg4)、higa(例如,higa1、higa2)、higd、hige或higm的重链恒定序列。在一些实施方案中,免疫球蛋白重链恒定序列是或衍生自人igg1同种异型的重链恒定序列(例如,g1m1、g1m2、g1m3或g1m17)。
[0213]
在一些实施方案中,免疫球蛋白重链恒定序列是或衍生自人免疫球蛋白g1恒定的恒定区序列(ighg1;uniprot:p01857
‑
1,v1)。在一些实施方案中,免疫球蛋白重链恒定序列是或衍生自人免疫球蛋白g1恒定的恒定区序列(ighg1;uniprot:p01857
‑
1,v1),其包含置换k214r、d356e和l358m(即,g1m3同种异型)。在一些实施方案中,抗体/抗原结合片段包含与seq id no:52的氨基酸序列具有至少70%序列同一性,更优选地至少75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性之一的氨基酸序列。
[0214]
在一些实施方案中,免疫球蛋白重链恒定序列是或衍生自人免疫球蛋白g4恒定的恒定区序列(ighg4;uniprot:p01861,v1)。在一些实施方案中,免疫球蛋白重链恒定序列是或衍生自人免疫球蛋白g4恒定的恒定区序列(ighg4;uniprot:p01861,v1),其包含置换s241p和/或l248e。s241p突变是铰链稳定的,而l248e突变进一步降低igg4的已经很低的adcc效应子功能(davies和sutton,immunol rev.,2015年11月;268(1):139
–
159;angal等人,mol immunol.,1993年1月;30(1):105
‑
8)。在一些实施方案中,抗体/抗原结合片段包含与seq id no:53的氨基酸序列具有至少70%序列同一性,更优选地至少75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性之一的氨基酸序列。
[0215]
在一些实施方案中,本公开的抗体/抗原结合片段包含免疫球蛋白轻链恒定序列。在一些实施方案中,免疫球蛋白轻链恒定序列可以是人免疫球蛋白轻链恒定序列。在一些实施方案中,免疫球蛋白轻链恒定序列是或衍生自κ或λ轻链,例如人免疫球蛋白κ恒定序列(igkc;cκ;uniprot:p01834
‑
1,v2),或人免疫球蛋白λ恒定序列(iglc;cλ),例如iglc1(uniprot:p0cg04
‑
1,v1)、iglc2(uniprot:p0doy2
‑
1,v1)、iglc3(uniprot:p0doy3
‑
1,v1)、iglc6(uniprot:p0cf74
‑
1,v1)或iglc7(uniprot:a0m8q6
‑
1,v3)。
[0216]
在一些实施方案中,抗体/抗原结合片段包含免疫球蛋白轻链恒定序列。在一些实施方案中,免疫球蛋白轻链恒定序列是或衍生自人免疫球蛋白κ恒定序列(igkc;cκ;uniprot:p01834
‑
1,v2;seq id no:90)。在一些实施方案中,免疫球蛋白轻链恒定序列是人免疫球蛋白λ恒定序列(iglc;cλ),例如,iglc1、iglc2、iglc3、iglc6或iglc7。在一些实施方案中,抗体/抗原结合片段包含与seq id no:54的氨基酸序列具有至少70%序列同一性,更优选地至少75%、80%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%序列同一性之一的氨基酸序列。在一些实施方案中,抗体/抗原结合片段包含与seq id no:55的氨基酸序列具有至少70%序列同一性,更优选地至少
2012,4(2):182
‑
197中描述的那些形式,该文献全文据此以引用方式并入。例如,双特异性抗体或双特异性抗原结合片段可以是双特异性抗体偶联物(例如,igg2、f(ab’)2或covx
‑
body)、双特异性igg或igg样分子(例如,igg、scfv4
‑
ig、igg
‑
scfv、scfv
‑
igg、dvd
‑
ig、igg
‑
svd、svd
‑
igg、2in 1
‑
igg、mab2或tandemab通用lc)、非对称双特异性igg或igg样分子(例如,kih igg、kih igg通用lc、crossmab、kih igg
‑
scfab、mab
‑
fv、电荷对或seed
‑
body)、小的双特异性抗体分子(例如,双价抗体(db)、dsdb、dart、scdb、tandabs、串联scfv(tafv)、串联dab/vhh、三体、三头、fab
‑
scfv或f(ab’)2
‑
scfv2)、双特异性fc和ch3融合蛋白(例如,tafv
‑
fc、二双价抗体(di
‑
diabody)、scdb
‑
ch3、scfv
‑
fc
‑
scfv、hcab
‑
vhh、scfv
‑
kih
‑
fc或scfv
‑
kih
‑
ch3)或双特异性融合蛋白(例如,scfv2
‑
白蛋白、scdb
‑
白蛋白、tafv
‑
毒素、dnl
‑
fab3、dnl
‑
fab4
‑
igg、dnl
‑
fab4
‑
igg
‑
细胞因子2)。特别参见kontermann mabs 2012,4(2):182
‑
19的图2。
[0224]
产生双特异性抗体的方法包括化学交联抗体或抗体片段,例如,用可还原的二硫键或不可还原的硫醚键,例如如在segal和bast,2001,《双特异性抗体的产生,免疫学最新方案》,14:iv:2.13:2.13.1
–
2.13.16中所述的,该文献全文据此以引用方式并入。例如,n
‑
琥珀酰亚胺基
‑3‑
(2
‑
吡啶基二硫代)
‑
丙酸酯(spdp)可用于通过铰链区sh
‑
基团化学交联例如fab片段,以产生二硫键连接的双特异性f(ab)2异二聚体。
[0225]
用于产生双特异性抗体的其他方法包括将产生抗体的杂交瘤例如与聚乙二醇融合,以产生能够分泌双特异性抗体的四源杂交瘤(quadroma)细胞,例如如在d.m.和bast,b.j.2001.“production of bispecific antibodies.”,current protocols in immunology.14:iv:2.13:2.13.1
–
2.13.16中所述。
[0226]
双特异性抗体和双特异性抗原结合片段也可通过从例如编码抗原结合分子的多肽的核酸构建体表达而重组产生,例如如在《抗体工程:方法和方案》,第2版(humana出版社,2012),第40章:“双特异性抗体的产生:双体和串联scfv”(hornig和),或法文,“如何制造双特异性抗体”,methods mol.med.2000;40:333
‑
339中所述。
[0227]
例如,可通过分子克隆技术制备dna构建体,该dna构建体编码两个抗原结合结构域的轻链和重链可变结构域(即,能够与il
‑
11、含il
‑
11的复合物或il
‑
11受体结合的抗原结合结构域的轻链和重链可变结构域,以及能够与另一种靶蛋白结合的抗原结合结构域的轻链和重链可变结构域),并且包括编码抗原结合结构域之间的合适接头或二聚化结构域的序列。此后,重组双特异性抗体可通过在合适的宿主细胞(例如,哺乳动物宿主细胞)中(例如,在体外)表达构建体来产生,然后可任选地纯化所表达的重组双特异性抗体。
[0228]
诱饵受体
[0229]
能够与il
‑
11或含il
‑
11的复合物结合的基于肽或多肽的药剂可基于il
‑
11受体,例如il
‑
11受体的il
‑
11结合片段。
[0230]
在一些实施方案中,结合剂可包含il
‑
11rα链的il
‑
11结合片段,并且可优选地为可溶的和/或排除一个或多个或全部的跨膜结构域。在一些实施方案中,结合剂可包含gp130的il
‑
11结合片段,并且可优选地为可溶的和/或排除一个或多个或全部的跨膜结构域。此类分子可被描述为诱饵受体。这些药剂的结合可通过降低/阻止il
‑
11与il
‑
11受体(例如,il
‑
11rα或gp130)结合的能力来抑制il
‑
11介导的顺式和/或反式信号传导,从而抑制下游信号传导。
[0231]
curtis等人(blood 1997dec 1;90(11):4403
‑
12)报道了当在表达跨膜il
‑
11r和gp130的细胞上测试时,可溶性小鼠il
‑
11受体α链(sil
‑
11r)能够拮抗il
‑
11的活性。他们提出,观察到的sil
‑
11r对il
‑
11的拮抗取决于已表达跨膜il
‑
11r的细胞上gp130分子的有限数目。
[0232]
还报道了将可溶性诱饵受体用作抑制信号转导和治疗干预的基础,用于其他信号传导分子:受体对,例如vegf和vegf受体(de
‑
chao yu等人,molecular therapy(2012);20 5,938
‑
947;konner和dupont,clin colorectal cancer2004oct;4suppl 2:s81
‑
5)。
[0233]
因此,在一些实施方案中,结合剂可以是诱饵受体,例如il
‑
11和/或含il
‑
11的复合物的可溶性受体。据报道,由诱饵受体提供的对il
‑
11和/或含il
‑
11的复合物的竞争导致il
‑
11拮抗剂作用(curtis等人,同上)。诱饵il
‑
11受体也描述于wo 2017/103108 a1和wo 2018/109168 a1中,这些专利全文据此以引用方式并入。
[0234]
诱饵il
‑
11受体优选地结合il
‑
11和/或含il
‑
11的复合物,从而使这些物质不可用于与gp130、il
‑
11rα和/或gp130:il
‑
11rα受体结合。因此,它们作为il
‑
11和含il
‑
11的复合物的“诱饵”受体,与依那西普作为tnfα的诱饵受体的方式非常相似。与不存在诱饵受体时的信号传导水平相比,il
‑
11介导的信号传导降低。
[0235]
诱饵il
‑
11受体优选地通过一个或多个细胞因子结合模块(cbm)与il
‑
11结合。cbm是天然存在的il
‑
11受体分子的cbm,或衍生自或同源于天然存在的il
‑
11受体分子的cbm。例如,诱饵il
‑
11受体可包含一个或多个cbm或由一个或多个cbm组成,这些cbm来自、衍生自或同源于gp130和/或il
‑
11rα的cbm。
[0236]
在一些实施方案中,诱饵il
‑
11受体可包含与gp130的细胞因子结合模块对应的氨基酸序列或由其组成。在一些实施方案中,诱饵il
‑
11受体可包含与il
‑
11rα的细胞因子结合模块对应的氨基酸序列。在本文中,“对应于”给定肽/多肽的参考区或序列的氨基酸序列与参考区/序列的氨基酸序列具有至少60%,例如至少65%、70%、75%、80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性之一。
[0237]
在一些实施方案中,诱饵受体可能能够结合il
‑
11,例如以至少100μm或更低的结合亲和力,任选地以10μm或更低、1μm或更低、100nm或更低、或约1nm至100nm中的一者的结合亲和力结合。在一些实施方案中,诱饵受体可包含全部或部分的il
‑
11结合结构域,并可任选地缺少全部或部分的跨膜结构域。诱饵受体可任选地与免疫球蛋白恒定区(例如,igg fc区)融合。
[0238]
抑制剂
[0239]
本发明考虑使用能够与il
‑
11、含il
‑
11的复合物、il
‑
11rα、gp130或含il
‑
11rα和/或gp130的复合物中的一者或多者结合并抑制il
‑
11介导的信号传导的抑制剂分子。
[0240]
在一些实施方案中,药剂是基于il
‑
11的基于肽或多肽的结合剂,例如il
‑
11的突变体、变体或结合片段。合适的基于肽或多肽的药剂可以不导致信号转导起始或产生次优信号传导的方式与il
‑
11受体(例如,il
‑
11rα、gp130或含有il
‑
11rα和/或gp130的复合物)结合。这种il
‑
11突变体可作为内源性il
‑
11的竞争性抑制剂。
[0241]
例如,w147a是il
‑
11拮抗剂,其中氨基酸147从色氨酸突变为丙氨酸,这破坏了il
‑
11的所谓“位点iii”。该突变体可与il
‑
11rα结合,但无法与gp130同源二聚体结合,从而有效阻断il
‑
11信号传导(underhill
‑
day等人,2003;endocrinology,2003年8月;144(8):
3406
‑
14)。lee等人(am j respire cell mol biol.2008dec;39(6):739
‑
746)还报道了能够特异性抑制il
‑
11与il
‑
11rα结合的il
‑
11拮抗剂突变体(“突变蛋白”)的产生。il
‑
11突变蛋白也描述于wo 2009/052588 a1中。
[0242]
menkhorst等人(biology of reproduction,2009年5月1日,第80卷第5期,第920
‑
927页)描述了peg化的il
‑
11拮抗剂pegil11a(csl limited,parkvill,victoria,australia),它能有效抑制雌性小鼠中il
‑
11的作用。
[0243]
pasqualini等人,cancer(2015)121(14):2411
‑
2421描述了能够与il
‑
11rα结合的配体导向的模拟肽药物,即靶向骨转移的模拟肽
‑
11(bmtp
‑
11)。
[0244]
在一些实施方案中,能够与il
‑
11受体结合的结合剂可以il
‑
11rα、gp130或含il
‑
11rα和/或gp130的复合物之一的小分子抑制剂的形式提供。在一些实施方案中,结合剂可以il
‑
11或含il
‑
11的复合物的小分子抑制剂的形式提供,例如,在lay等人,int.j.oncol.(2012);41(2):759
‑
764中描述的il
‑
11抑制剂,该文献全文据此以引用方式并入。
[0245]
适体
[0246]
在一些实施方案中,能够与il
‑
11/含il
‑
11的复合物或il
‑
11受体(例如,il
‑
11rα、gp130或含il
‑
11rα和/或gp130的复合物)结合的药剂是适体。适体,也称为核酸/肽配体,是特征在于以高特异性和高亲和力与靶分子结合的能力的核酸或肽分子。迄今为止鉴定的几乎每种适体是非天然存在的分子。
[0247]
可通过指数富集配体的系统进化(selextm)方法,或通过开发somamer(慢解离速率修饰的适体)来鉴定和/或产生针对给定靶标(例如,il
‑
11、含il
‑
11的复合物或il
‑
11受体)的适体(gold l等人,(2010)plos one 5(12):e15004)。适体和selex描述于tuerk和gold,science(1990)249(4968):505
‑
10中,以及wo 91/19813中。应用selex和somamer技术包括,例如,添加模拟氨基酸侧链的官能团,以扩大适体的化学多样性。因此,可富集并鉴定靶标的高亲和力适体。
[0248]
适体可以是dna或rna分子,并且可以是单链或双链的。适体可包括化学修饰的核酸,例如其中糖和/或磷酸和/或碱基被化学修饰。这种修饰可改善适体的稳定性或使适体对降解更具抗性,并且可包括在核糖的2
′
位的修饰。
[0249]
适体可通过本领域技术人员熟知的方法合成。例如,适体可例如在固相支撑物上化学合成。固相合成可使用亚磷酰胺化学法。简而言之,将固相支撑的核苷酸脱三苯甲基化,然后与适当活化的核苷亚磷酰胺偶联以形成亚磷酸三酯键。然后可进行封端,接着用氧化剂(通常是碘)氧化亚磷酸三酯。然后可重复该循环来组装适体(例如,参见sinha,n.d.;biernat,j.;mcmanus,j.;h.nucleic acids res.1984,12,4539;以及beaucage,s.l.;lyer,r.p.(1992).tetrahedron 48(12):2223)。
[0250]
合适的核酸适体可任选地具有10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39或40个核苷酸之一的最小长度。合适的核酸适体可任选地具有20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79或80个核苷酸之一的最大长度。合适的核酸适体可任选地具有10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49、50、
51、52、53、54、55、56、57、58、59、60、61、62、63、64、65、66、67、68、69、70、71、72、73、74、75、76、77、78、79或80个核苷酸之一的长度。
[0251]
适体可以是经选择或工程化以结合特异性靶分子的肽。肽适体及其产生和鉴定方法综述于reverdatto等人,curr top med chem.(2015)15(12):1082
‑
101中,该文献全文据此以引用方式并入。肽适体可任选地具有2、3、4、5、6、7、8、9或10个氨基酸之一的最小长度。肽适体可任选地具有15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49或50个氨基酸之一的最大长度。合适的肽适体可任选地具有2
‑
30、2
‑
25、2
‑
20、5
‑
30、5
‑
25或5
‑
20个氨基酸之一的长度。
[0252]
适体可具有nm或pm范围内的k
d
,例如小于500nm、100nm、50nm、10nm、1nm、500pm、100pm中的一者。
[0253]
il
‑
11结合剂的特性
[0254]
能够与il
‑
11/含il
‑
11的复合物或根据本发明的il
‑
11受体结合的药剂可表现出下列特性中的一种或多种特性:
[0255]
·
与il
‑
11/含il
‑
11的复合物或il
‑
11受体特异性结合;
[0256]
·
与il
‑
11/含il
‑
11的复合物或il
‑
11受体结合,kd为10μm或更小,优选地为≤5μm、≤1μm、≤500nm、≤100nm、≤10nm、≤1nm或≤100pm中的一者;
[0257]
·
抑制il
‑
11和il
‑
11rα之间的相互作用;
[0258]
·
抑制il
‑
11和gp130之间的相互作用;
[0259]
·
抑制il
‑
11和il
‑
11rα:gp130受体复合物之间的相互作用;
[0260]
·
抑制il
‑
11:il
‑
11rα复合物和gp130之间的相互作用。
[0261]
这些特性可通过在合适的测定中分析相关药剂来确定,这可能涉及将药剂的性能与合适的对照药剂进行比较。技术人员能够确定用于给定测定的合适对照条件。
[0262]
例如,用于分析测试抗体/抗原结合片段与il
‑
11/含il
‑
11的复合物/il
‑
11受体结合的能力的合适阴性对照可以是针对非靶蛋白的抗体/抗原结合片段(即,对il
‑
11/含il
‑
11的复合物/il
‑
11受体为非特异性的抗体/抗原结合片段)。合适的阳性对照可以是已知的、经验证的(例如,市售的)il
‑
11或il
‑
11受体结合抗体。对照可以是与待分析的推定的il
‑
11/含il
‑
11的复合物/il
‑
11受体结合的抗体/抗原结合片段相同的同种型,并且可例如具有相同的恒定区。
[0263]
在一些实施方案中,药剂可能能够与il
‑
11或含il
‑
11的复合物或il
‑
11受体(例如,il
‑
11rα、gp130或含il
‑
11rα和/或gp130的复合物)特异性地结合。与给定靶分子特异性地结合的药剂优选地以比其与其他非靶分子结合更大的亲和力和/或更长的持续时间结合靶标。
[0264]
在一些实施方案中,药剂可以比与il
‑
6细胞因子家族的一个或多个其他成员(例如,il
‑
6、白血病抑制因子(lif)、制瘤素m(osm)、心肌营养素
‑
1(ct
‑
1)、睫状神经营养因子(cntf)和心肌营养素样细胞因子(clc))结合的亲和力更高的亲和力与il
‑
11或含il
‑
11的复合物结合。在一些实施方案中,药剂可以比与il
‑
6受体家族的一个或多个其他成员结合的亲和力更高的亲和力与il
‑
11受体(例如,il
‑
11rα、gp130或含il
‑
11rα和/或gp130的复合物)结合。在一些实施方案中,药剂可以比与il
‑
6rα、白血病抑制因子受体(lifr)、制瘤素m受体(osmr)、睫状神经营养因子受体α(cntfrα)和细胞因子受体样因子1(crlf1)中的一者
或多者结合的亲和力更高的亲和力与il
‑
11rα结合。
[0265]
在一些实施方案中,例如通过elisa、spr、生物层干涉测量法(bli)、微量热泳法(mst)或通过放射免疫测定法(ria)测量,结合剂与非靶标的结合程度小于该药剂与靶标结合的约10%。另选地,结合特异性可通过结合亲和力来反映,其中结合剂与il
‑
11、含il
‑
11的复合物或il
‑
11受体结合,其k
d
比与另一个非靶分子结合的k
d
大至少0.1个数量级(即,0.1
×
10n,其中n是代表该数量级的整数)。这可任选地为至少0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1.0、1.5或2.0中的一者。
[0266]
给定结合剂对其靶标的结合亲和力通常用其解离常数(k
d
)来描述。结合亲和力可通过本领域已知的方法来测量,例如通过elisa、表面等离子体共振(spr;参见,例如,hearty等人,methods mol biol(2012)907:411
‑
442;或rich等人,anal biochem.,2008年2月1日;373(1):112
‑
20)、生物层干涉测量法(参见,例如,lad等人,(2015)j biomol screen 20(4):498
‑
507;或concepcion等人,comb chem high throughput screen.,2009年9月;12(8):791
‑
800)、微量热泳法(mst)分析(参见,例如,jerabek
‑
willemse等人,assay drug dev technol.,2011年8月;9(4):342
‑
353),或通过放射性标记的抗原结合测定(ria)。
[0267]
在一些实施方案中,药剂能够与il
‑
11或含il
‑
11的复合物或il
‑
11受体结合,其中k
d
为50μm或更小,优选地为≤10μm、≤5μm、≤4μm、≤3μm、≤2μm、≤1μm、≤500nm、≤100nm、≤75nm、≤50nm、≤40nm、≤30nm、≤20nm、≤15nm、≤12.5nm、≤10nm、≤9nm、≤8nm、≤7nm、≤6nm、≤5nm、≤4nm、≤3nm、≤2nm、≤1nm、≤500pm、≤400pm、≤300pm、≤200pm或≤100pm中的一者。
[0268]
在一些实施方案中,药剂与il
‑
11、含il
‑
11的复合物或il
‑
11受体结合,其中ec50的结合亲和力(例如,如通过elisa确定)=10,000ng/ml或更小,优选地为≤5,000ng/ml、≤1000ng/ml、≤900ng/ml、≤800ng/ml、≤700ng/ml、≤600ng/ml、≤500ng/ml、≤400ng/ml、≤300ng/ml、≤200ng/ml、≤100ng/ml、≤90ng/ml、≤80ng/ml、≤70ng/ml、≤60ng/ml、≤50ng/ml、≤40ng/ml、≤30ng/ml、≤20ng/ml、≤15ng/ml、≤10ng/ml、≤7.5ng/ml、≤5ng/ml、≤2.5ng/ml或≤1ng/ml中的一者。这种elisa可按例如如在antibody engineering,第1卷(第2版),springer protocols,springer(2010),第v部分,第657
‑
665页中所述的方式进行。
[0269]
在一些实施方案中,药剂在对于与il
‑
11或含il
‑
11的复合物的受体(例如,gp130或il
‑
11rα)结合很重要的区域中与il
‑
11或含il
‑
11的复合物结合,从而抑制il
‑
11或含il
‑
11的复合物与il
‑
11受体之间的相互作用,和/或抑制通过该受体的信号传导。在一些实施方案中,药剂在对于与il
‑
11或含il
‑
11的复合物结合很重要的区域中与il
‑
11受体结合,从而抑制il
‑
11或含il
‑
11的复合物与il
‑
11受体之间的相互作用,和/或抑制通过该受体的信号传导。
[0270]
给定结合剂(例如,能够结合il
‑
11/含il
‑
11的复合物或il
‑
11受体的药剂)抑制两种蛋白之间相互作用的能力,可通过例如在结合剂存在的情况下或在一种或两种相互作用配偶体与结合剂温育后分析相互作用来确定。确定给定结合剂是否能够抑制两种相互作用配偶体之间的相互作用的合适测定的示例是竞争elisa。
[0271]
通过观察在结合剂存在的情况下或在一种或两种相互作用配偶体与结合剂温育后,相比于不存在结合剂时(或存在适当对照结合剂时)的相互作用水平,相互作用配偶体
之间的相互作用水平降低/减少,来识别能够抑制(例如,il
‑
11和il
‑
11rα之间,或il
‑
11和gp130之间,或il
‑
11和il
‑
11rα:gp130之间,或il
‑
11:il
‑
11rα和gp130之间)的给定相互作用的结合剂。合适的分析可例如使用重组相互作用配偶体或使用表达相互作用配偶体的细胞在体外进行。表达相互作用配偶体的细胞可内源性地表达相互作用配偶体,或者可由引入细胞的核酸表达相互作用配偶体。为了进行此类测定,相互作用配偶体和/或结合剂中的一者或两者可被标记或与可检测实体结合使用,以用于检测和/或测量相互作用的水平。例如,可用放射性原子或有色分子或荧光分子或可容易地以任何其他方式检测的分子来标记药剂。合适的可检测分子包括荧光蛋白、荧光素酶、酶底物和放射性标记。结合剂可用可检测标记直接标记,或者可被间接标记。例如,结合剂可以是未标记的,并且通过本身被标记的另一种结合剂来检测。另选地,第二结合剂可能已结合有生物素,并且标记的链霉亲和素与生物素的结合可用于间接地标记第一结合剂。
[0272]
结合剂抑制两个结合配偶体之间相互作用的能力也可通过分析这种相互作用的下游功能结果(例如,il
‑
11介导的信号传导)来确定。例如,il
‑
11和il
‑
11rα:gp130之间或il
‑
11:il
‑
11rα和gp130之间的相互作用的下游功能性结果可包括例如由il
‑
11介导的过程,或例如胶原或il
‑
11的基因/蛋白表达。
[0273]
对il
‑
11或含il
‑
11的复合物与il
‑
11受体之间相互作用的抑制可使用3h
‑
胸苷掺入和/或ba/f3细胞增殖测定,诸如在以下文献中描述的那些测定来进行分析:curtis等人,blood,1997,90(11)和karpovich等人,mol.hum.reprod.2003 9(2):75
‑
80。ba/f3细胞共表达il
‑
11rα和gp130。
[0274]
在一些实施方案中,相比于不存在结合剂时(或存在适当对照结合剂时)的il
‑
11和il
‑
11rα之间的相互作用水平,该结合剂可能能够将il
‑
11和il
‑
11rα之间的相互作用抑制为小于100%,例如,为99%或更小、95%或更小、90%或更小、85%或更小、75%或更小、70%或更小、65%或更小、60%或更小、55%或更小、50%或更小、45%或更小、40%或更小、35%或更小、30%或更小、25%或更小、20%或更小、15%或更小、10%或更小、5%或更小、或1%或更小之一。在一些实施方案中,相比于不存在结合剂时(或存在适当对照结合剂时)的il
‑
11和il
‑
11rα之间的相互作用水平,该结合剂可能能够将il
‑
11和il
‑
11rα之间的相互作用抑制为小于1倍,例如,为≤0.99倍、≤0.95倍、≤0.9倍、≤0.85倍、≤0.8倍、≤0.75倍、≤0.7倍、≤0.65倍、≤0.6倍、≤0.55倍、≤0.5倍、≤0.45倍、≤0.4倍、≤0.35倍、≤0.3倍、≤0.25倍、≤0.2倍、≤0.15倍、≤0.1倍之一。
[0275]
在一些实施方案中,相比于不存在结合剂时(或存在适当对照结合剂时)的il
‑
11和gp130之间的相互作用水平,该结合剂可能能够将il
‑
11和gp130之间的相互作用抑制为小于100%,例如,为99%或更小、95%或更小、90%或更小、85%或更小、75%或更小、70%或更小、65%或更小、60%或更小、55%或更小、50%或更小、45%或更小、40%或更小、35%或更小、30%或更小、25%或更小、20%或更小、15%或更小、10%或更小、5%或更小、或1%或更小之一。在一些实施方案中,相比于不存在结合剂时(或存在适当对照结合剂时)的il
‑
11和gp130之间的相互作用水平,该结合剂可能能够将il
‑
11和gp130之间的相互作用抑制为小于1倍,例如,为≤0.99倍、≤0.95倍、≤0.9倍、≤0.85倍、≤0.8倍、≤0.75倍、≤0.7倍、≤0.65倍、≤0.6倍、≤0.55倍、≤0.5倍、≤0.45倍、≤0.4倍、≤0.35倍、≤0.3倍、≤0.25倍、≤0.2倍、≤0.15倍、≤0.1倍之一。
[0276]
在一些实施方案中,相比于不存在结合剂时(或存在适当对照结合剂时)的il
‑
11和il
‑
11rα:gp130之间的相互作用水平,该结合剂可能能够将il
‑
11和il
‑
11rα:gp130之间的相互作用抑制为小于100%,例如,为99%或更小、95%或更小、90%或更小、85%或更小、75%或更小、70%或更小、65%或更小、60%或更小、55%或更小、50%或更小、45%或更小、40%或更小、35%或更小、30%或更小、25%或更小、20%或更小、15%或更小、10%或更小、5%或更小、或1%或更小之一。在一些实施方案中,相比于不存在结合剂时(或存在适当对照结合剂时)的il
‑
11和il
‑
11rα:gp130之间的相互作用水平,该结合剂可能能够将il
‑
11和il
‑
11rα:gp130之间的相互作用抑制为小于1倍,例如,为≤0.99倍、≤0.95倍、≤0.9倍、≤0.85倍、≤0.8倍、≤0.75倍、≤0.7倍、≤0.65倍、≤0.6倍、≤0.55倍、≤0.5倍、≤0.45倍、≤0.4倍、≤0.35倍、≤0.3倍、≤0.25倍、≤0.2倍、≤0.15倍、≤0.1倍之一。
[0277]
在一些实施方案中,相比于不存在结合剂时(或存在适当对照结合剂时)的il
‑
11:il
‑
11rα复合物和gp130之间的相互作用水平,该结合剂可能能够将il
‑
11:il
‑
11rα复合物和gp130之间的相互作用抑制为小于100%,例如,为99%或更小、95%或更小、90%或更小、85%或更小、75%或更小、70%或更小、65%或更小、60%或更小、55%或更小、50%或更小、45%或更小、40%或更小、35%或更小、30%或更小、25%或更小、20%或更小、15%或更小、10%或更小、5%或更小、或1%或更小之一。在一些实施方案中,相比于不存在结合剂时的il
‑
11:il
‑
11rα复合物和gp130之间的相互作用水平,该结合剂能够将il
‑
11:il
‑
11rα复合物和gp130之间的相互作用抑制为小于1倍,例如,为≤0.99倍、≤0.95倍、≤0.9倍、≤0.85倍、≤0.8倍、≤0.75倍、≤0.7倍、≤0.65倍、≤0.6倍、≤0.55倍、≤0.5倍、≤0.45倍、≤0.4倍、≤0.35倍、≤0.3倍、≤0.25倍、≤0.2倍、≤0.15倍、≤0.1倍之一。
[0278]
能够降低il
‑
11或il
‑
11受体表达的药剂
[0279]
在本发明的方面,能够抑制il
‑
11介导的信号传导的药剂可能能够阻止或减少il
‑
11、il
‑
11rα或gp130中的一者或多者的表达。
[0280]
表达可以是基因或蛋白质表达,并且可如本文所述或通过本领域技术人员熟知的本领域方法来确定。表达可通过受试者的细胞/组织/器官系统进行。
[0281]
合适的药剂可以是任何种类,但在一些实施方案中,能够阻止或减少il
‑
11、il
‑
11rα或gp130中的一者或多者的表达的药剂可以是小分子或寡核苷酸。
[0282]
能够阻止或减少il
‑
11、il
‑
11rα或gp130中的一者或多者的表达的药剂可例如通过如下方式来阻止或减少il
‑
11、il
‑
11rα或gp130中的一者或多者的表达:抑制编码il
‑
11、il
‑
11rα或gp130的基因的转录,抑制编码il
‑
11、il
‑
11rα或gp130的rna的转录后加工,降低编码il
‑
11、il
‑
11rα或gp130的rna的稳定性,促进编码il
‑
11、il
‑
11rα或gp130的rna的降解,抑制il
‑
11、il
‑
11rα或gp130多肽的翻译后加工,降低il
‑
11、il
‑
11rα或gp130多肽的稳定性,或促进il
‑
11、il
‑
11rα或gp130多肽的降解。
[0283]
taki等人,clin exp immunol,1998年4月;112(1):133
‑
138报道了在用吲哚美辛、地塞米松或干扰素
‑
γ(ifnγ)治疗后,类风湿性滑膜细胞中il
‑
11的表达降低。
[0284]
本发明考虑使用反义核酸来阻止/减少il
‑
11、il
‑
11rα或gp130的表达。在一些实施方案中,能够阻止或减少il
‑
11、il
‑
11rα或gp130的表达的药剂可通过rna干扰(rnai)引起表达减少。
[0285]
在一些实施方案中,药剂可以是抑制性核酸,诸如反义或小干扰rna,包括但不限
于shrna或sirna。
[0286]
在一些实施方案中,抑制性核酸在载体中提供。例如,在一些实施方案中,药剂可以是编码il
‑
11、il
‑
11rα或gp130中的一者或多者的shrna的慢病毒载体。
[0287]
寡核苷酸分子,特别是rna,可用于调节基因表达。这些包括反义寡核苷酸、小干扰rna(sirna)对mrna的靶向降解、转录后基因沉默(ptg)、微小rna(mirna)对mrna的发育调控的序列特异性翻译抑制以及靶向转录基因沉默。
[0288]
反义寡核苷酸是优选单链的寡核苷酸,其通过互补序列结合靶向并结合靶寡核苷酸,例如mrna。当靶寡核苷酸是mrna时,反义物与mrna的结合阻断mrna的翻译和基因产物的表达。反义寡核苷酸可被设计成结合有义基因组核酸并抑制靶核苷酸序列的转录。
[0289]
鉴于il
‑
11、il
‑
11rα和gp130的已知核酸序列(例如,可从genbank获得的已知mrna序列,登录号:bc012506.1gi:15341754(人il
‑
11)、bc134354.1gi:126632002(小鼠il
‑
11)、af347935.1gi:13549072(大鼠il
‑
11)、nm_001142784.2gi:391353394(人il
‑
11rα)、nm_001163401.1gi:254281268(小鼠il
‑
11rα)、nm_139116.1gi:20806172(大鼠il
‑
11rα)、nm_001190981.1gi:300244534(人gp130)、nm_010560.3gi:225007624(小鼠gp130)、nm_001008725.3gi:300244570(大鼠gp130)),寡核苷酸可被设计为抑制或沉默il
‑
11、il
‑
11rα或gp130的表达。
[0290]
这种寡核苷酸可具有任何长度,但可优选地较短,例如少于100个核苷酸,例如10
‑
40个核苷酸,或20
‑
50个核苷酸,并且可包含与靶寡核苷酸(例如,il
‑
11、il
‑
11rα或gp130 mrna)中对应长度的核苷酸序列具有完全或接近互补性(例如,80%、85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%或100%的互补性)的核苷酸序列。核苷酸序列的互补区可具有任何长度,但优选地至少5个,并且任选地不超过50个核苷酸长,例如6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、38、39、40、41、42、43、44、45、46、47、48、49或50个核苷酸之一。
[0291]
il
‑
11、il
‑
11rα或gp130表达的抑制将优选地导致细胞/组织/器官系统/受试者表达的il
‑
11、il
‑
11rα或gp130的量减少。例如,在给定的细胞中,通过施用合适的核酸抑制il
‑
11、il
‑
11rα或gp130,将导致该细胞表达的il
‑
11、il
‑
11rα或gp130的量相对于未处理的细胞减少。抑制可以是部分的。优选的抑制程度为至少50%,更优选地至少60%、70%、80%、85%或90%中的一者。90%和100%之间的抑制水平被认为是表达或功能的“沉默”。
[0292]
rnai机制和小rna在靶向异染色质复合物和特定染色体位点的表观遗传基因沉默中的作用已得到证实。双链rna(dsrna)依赖性转录后沉默,也称为rna干扰(rnai),是dsrna复合物可在短时间内靶向特定同源基因进行沉默的现象。它作为信号促进具有序列同一性的mrna的降解。20
‑
nt sirna通常足够长以诱导基因特异性沉默,但足够短以逃避宿主反应。靶基因产物表达的降低可能是广泛的,其中90%的沉默由sirna的一些分子诱导。基于rnai的疗法已进入针对多种适应症的i、ii和iii期临床试验(nature,2009年1月22日;457(7228):426
‑
433)。
[0293]
在本领域中,这些rna序列根据其来源被称为“短或小干扰rna”(sirna)或“微小rna”(mirna)。这两种类型的序列都可用于通过与互补rna结合、触发mrna消除(rnai)或阻止mrna翻译成蛋白质来下调基因表达。sirna通过加工长的双链rna而衍生,并且当存在于自然界中时,通常是外源来源的。微干扰rna(mirna)是内源编码的非编码小rna,其通过加
工短发夹而衍生。sirna和mirna均可抑制带有部分互补靶序列的mrna的翻译而不发生rna切割,并降解带有完全互补序列的mrna。
[0294]
sirna配体通常是双链的,并且为了优化rna介导的靶基因功能下调的有效性,优选的是选择sirna分子的长度以确保介导sirna对mrna靶标的识别的risc复合物正确识别sirna,并且使得sirna足够短以减少宿主反应。
[0295]
mirna配体通常是单链的,并且具有部分互补的区域,使得配体能够形成发夹。mirna是从dna转录但不翻译成蛋白质的rna基因。编码mirna基因的dna序列比mirna长。该dna序列包括mirna序列和近似的反向互补序列。当该dna序列转录成单链rna分子时,mirna序列及其反向互补碱基对形成部分双链rna区段。在john等人,plos biology,11(2),1862
‑
1879,2004中讨论了微小rna序列的设计。
[0296]
通常,旨在模拟sirna或mirna作用的rna配体具有10至40个核糖核苷酸(或其合成类似物),更优选地17至30个核糖核苷酸,更优选地19至25个核糖核苷酸,最优选地21至23个核糖核苷酸。在采用双链sirna的本发明的一些实施方案中,分子可具有对称的3'突出端,例如一个或两个(核糖)核苷酸的突出端,通常是dtdt 3'突出端的uu。基于本文提供的公开内容,技术人员可容易地设计合适的sirna和mirna序列,例如使用资源诸如ambion sirna finder。sirna和mirna序列可合成产生并外源添加以引起基因下调,或使用表达系统(例如,载体)产生。在优选的实施方案中,sirna是合成的。
[0297]
可在细胞中加工较长的双链rna以产生sirna(参见例如myers(2003)nature biotechnology 21:324
‑
328)。较长的dsrna分子可具有对称的3'或5'突出端,例如一个或两个(核糖)核苷酸的突出端,或可具有平端。较长的dsrna分子可为25个核苷酸或更长。优选地,较长的dsrna分子的长度为25至30个核苷酸。更优选地,较长的dsrna分子的长度为25至27个核苷酸。最优选地,较长的dsrna分子的长度为27个核苷酸。可使用载体pdecap表达长度为30个核苷酸或更长的dsrna(shinagawa等人,genes and dev.,17,1340
‑
5,2003)。
[0298]
另一种选择是在细胞中表达短发夹rna分子(shrna)。shrna比合成的sirna更稳定。shrna由被小的环序列分隔的短反向重复序列组成。一个反向重复序列与靶基因互补。在细胞中,shrna被dicer加工成sirna,从而降解靶基因mrna并抑制表达。在一个优选的实施方案中,shrna通过从载体转录而内源性地(在细胞内)产生。shrna可通过用在rna聚合酶iii启动子诸如人h1或7sk启动子或rna聚合酶ii启动子控制下编码shrna序列的载体转染细胞而在细胞内产生。另选地,可通过从载体转录来外源(体外)合成shrna。然后可将shrna直接引入细胞。优选地,shrna分子包含il
‑
11、il
‑
11rα或gp130的部分序列。优选地,shrna序列的长度为40至100个碱基,更优选地长度为40至70个碱基。发夹的主干的长度优选地为19至30个碱基对。主干可含有g
‑
u配对以稳定发夹结构。
[0299]
sirna分子、较长的dsrna分子或mirna分子可通过核酸序列(优选包含在载体内)的转录而重组制备。优选地,sirna分子、较长的dsrna分子或mirna分子包含il
‑
11、il
‑
11rα或gp130的部分序列。
[0300]
在一个实施方案中,sirna、较长的dsrna或mirna通过从载体转录而内源性地(在细胞内)产生。载体可以本领域已知的任何方式引入细胞。任选地,rna序列的表达可使用组织特异性(例如,心脏、肝脏或肾特异性)启动子来调节。在另一个实施方案中,sirna、较长的dsrna或mirna通过从载体转录而外源性地(体外)产生。
[0301]
合适的载体可以是被配置为表达能够抑制il
‑
11、il
‑
11rα或gp130的寡核苷酸药剂的寡核苷酸载体。此类载体可以是病毒载体或质粒载体。治疗性寡核苷酸可掺入病毒载体的基因组中,并与驱动其表达的调控序列(例如,启动子)可操作地连接。术语“可操作地连接”可包括这样的情况,其中选定的核苷酸序列和调控核苷酸序列以使得核苷酸序列的表达处于调控序列的影响或控制之下的方式共价连接。因此,如果调控序列能够影响形成选定的核苷酸序列的部分或全部的核苷酸序列的转录,则调控序列可操作地连接到选定的核苷酸序列。
[0302]
编码启动子表达的sirna序列的病毒载体是本领域已知的,并且具有长期表达治疗性寡核苷酸的益处。示例包括慢病毒(nature,2009年1月22日;457(7228):426
‑
433)、腺病毒(shen等人,febs lett,2003年3月27日;539(1
‑
3)111
‑
4)和逆转录病毒(barton和medzhitov,pnas,2002年11月12日,第99卷第23期,第14943
‑
14945页)。
[0303]
在其他实施方案中,载体可被配置为帮助将治疗性寡核苷酸递送至需要抑制il
‑
11、il
‑
11rα或gp130表达的位点。此类载体通常涉及将寡核苷酸与带正电荷的载体(例如,阳离子细胞穿透肽、阳离子聚合物和树枝状聚合物以及阳离子脂质)复合;将该寡核苷酸与小分子(例如,胆固醇、胆汁酸和脂质)、聚合物、抗体和rna缀合;或将寡核苷酸包封在纳米颗粒制剂中(wang等人,aaps j.,2010年12月;12(4):492
‑
503)。
[0304]
在一个实施方案中,载体可包含有义方向和反义方向的核酸序列,使得当表达为rna时,有义部分和反义部分将结合形成双链rna。
[0305]
另选地,可使用本领域已知的标准固相或溶液相合成技术合成sirna分子。核苷酸之间的连接可以是磷酸二酯键或替代物,例如,式p(o)s的连接基团,(硫代酸酯);p(s)s,(二硫代酸酯);p(o)nr'2;p(o)r';p(o)or6;co;或conr'2,其中r是h(或盐)或烷基(1
‑
12c),r6是烷基(1
‑
9c),通过
‑
o
‑
或
‑
s
‑
与相邻核苷酸连接。
[0306]
除了天然存在的碱基之外,还可使用修饰的核苷酸碱基,并且可赋予含有它们的sirna分子有利的特性。
[0307]
例如,修饰的碱基可增加sirna分子的稳定性,从而减少沉默所需的量。修饰的碱基的提供还可提供比未修饰的sirna更稳定或更不稳定的sirna分子。
[0308]
术语“修饰的核苷酸碱基”包括具有共价修饰的碱基和/或糖的核苷酸。例如,修饰的核苷酸包括具有糖的核苷酸,该糖共价连接到低分子量有机基团,而不是3'位置的羟基和5'位置的磷酸基团。因此,修饰的核苷酸还可包括2'取代的糖,诸如2'
‑
o
‑
甲基
‑
;2'
‑
o
‑
烷基;2'
‑
o
‑
烯丙基;2'
‑
s
‑
烷基;2'
‑
s
‑
烯丙基;2'
‑
氟
‑
;2'
‑
卤代或叠氮基
‑
核糖、碳环糖类似物、α
‑
异头糖;差向异构糖,诸如阿拉伯糖、木糖或来苏糖、吡喃糖、呋喃糖和景天庚酮糖。
[0309]
修饰的核苷酸是本领域已知的,并且包括烷基化嘌呤和嘧啶、酰化嘌呤和嘧啶以及其他杂环。这些类别的嘧啶和嘌呤是本领域已知的,并且包括假异胞嘧啶、n4,n4
‑
乙醇胞嘧啶、8
‑
羟基
‑
n6
‑
甲基腺嘌呤、4
‑
乙酰胞嘧啶、5
‑
(羧基羟甲基)尿嘧啶、5
‑
氟尿嘧啶、5
‑
溴尿嘧啶、5
‑
羧甲基氨基甲基
‑2‑
硫尿嘧啶、5
‑
羧甲基氨基甲基尿嘧啶、二氢尿嘧啶、肌苷、n6
‑
异戊基腺嘌呤、1
‑
甲基腺嘌呤、1
‑
甲基假尿嘧啶、1
‑
甲基鸟嘌呤、2,2
‑
二甲基鸟嘌呤、2
‑
甲基腺嘌呤、2
‑
甲基鸟嘌呤、3
‑
甲基胞嘧啶、5
‑
甲基胞嘧啶、n6
‑
甲基腺嘌呤、7
‑
甲基鸟嘌呤、5
‑
甲基氨基甲基尿嘧啶、5
‑
甲氧基氨基甲基
‑2‑
硫尿嘧啶、
‑
d
‑
甘露糖基辫苷(queosine)、5
‑
甲氧基羰基甲基尿嘧啶、5
‑
甲氧基尿嘧啶、2
‑
甲硫基
‑
n6
‑
异戊二烯基腺嘌呤、尿嘧啶
‑5‑
氧乙酸甲
酯、假尿嘧啶、2
‑
硫代胞嘧啶、5
‑
甲基
‑2‑
硫尿嘧啶、2
‑
硫尿嘧啶、4
‑
硫尿嘧啶、5
‑
甲基尿嘧啶、n
‑
尿嘧啶
‑5‑
氧乙酸甲酯、尿嘧啶
‑5‑
氧乙酸、辫苷、2
‑
硫代胞嘧啶、5
‑
丙基尿嘧啶、5
‑
丙基胞嘧啶、5
‑
乙基尿嘧啶、5
‑
乙基胞嘧啶、5
‑
丁基尿嘧啶、5
‑
戊基尿嘧啶、5
‑
戊基胞嘧啶,以及2,6
‑
二氨基嘌呤、甲基假尿嘧啶、1
‑
甲基鸟嘌呤、1
‑
甲基胞嘧啶。
[0310]
涉及使用rnai沉默秀丽隐杆线虫(c.elegans)、果蝇、植物和哺乳动物中的基因的方法是本领域已知的(fire a等人,1998 nature 391:806
‑
811;fire,a.trends genet.15,358
‑
363(1999);sharp,p.a.rna interference 2001.genes dev.15,485
‑
490(2001);hammond,s.m.等人,nature rev.genet.2,110
‑
1119(2001);tuschl,t.chem.biochem.2,239
‑
245(2001);hamilton,a.等人,science 286,950
‑
952(1999);hammond,s.m.等人,nature 404,293
‑
296(2000);zamore,p.d.等人,cell 101,25
‑
33(2000);bernstein,e.等人,nature 409,363
‑
366(2001);elbashir,s.m.等人,genes dev.15,188
‑
200(2001);wo0129058;wo9932619;以及elbashir s m,等人,2001 nature 411:494
‑
498)。
[0311]
因此,本发明提供了一种核酸,该核酸当被适当地引入或表达于原本表达il
‑
11、il
‑
11rα或gp130的哺乳动物(例如,人)细胞中时能够通过rnai抑制il
‑
11、il
‑
11rα或gp130表达。
[0312]
il
‑
11、il
‑
11rα和gp130的核酸序列(例如,可从genbank获得的已知mrna序列,登录号:bc012506.1gi:15341754(人il
‑
11)、bc134354.1gi:126632002(小鼠il
‑
11)、af347935.1gi:13549072(大鼠il
‑
11)、nm_001142784.2gi:391353394(人il
‑
11rα)、nm_001163401.1gi:254281268(小鼠il
‑
11rα)、nm_139116.1gi:20806172(大鼠il
‑
11rα)、nm_001190981.1gi:300244534(人gp130)、nm_010560.3gi:225007624(小鼠gp130)、nm_001008725.3gi:300244570(大鼠gp130))寡核苷酸可被设计为抑制或沉默il
‑
11、il
‑
11rα或gp130的表达。
[0313]
核酸可与il
‑
11、il
‑
11rα或gp130 mrna的一部分(例如,如在genbank登录号nm_000641.3gi:391353405(il
‑
11)、nm_001142784.2gi:391353394(il
‑
11rα)、nm_001190981.1gi:300244534(gp130)中所定义的)或所述mrna的互补序列具有实质上的序列同一性。
[0314]
核酸可以是双链sirna。(如本领域技术人员将理解的,并且如下文进一步解释的,sirna分子也可包括短的3’dna序列。)
[0315]
另选地,核酸可以是dna(通常是双链dna),当在哺乳动物细胞中转录时,产生具有两个通过间隔区连接的互补部分的rna,使得当互补部分彼此杂交时,rna采取发夹的形式。在哺乳动物细胞中,发夹结构可被dicer酶从分子上切割下来,以产生两个不同的但杂交的rna分子。
[0316]
在一些优选的实施方案中,核酸通常靶向seq id no:4至seq id no:7(il
‑
11)之一的序列或靶向seq id no:8至seq id no:11(il
‑
11rα)之一的序列。
[0317]
只有mrna转录物的单链(即,非自杂交)区域有望成为rnai的合适靶标。因此,提出il
‑
11或il
‑
11rαmrna转录物中与seq id no:4至seq id no:7或seq id no:8至seq id no:11之一所示序列非常接近的其他序列也可能是rnai的合适靶标。此类靶序列的长度优选为17
‑
23个核苷酸,并且优选地与seq id no:4至seq id no:7或seq id no:8至seq id no:11之一重叠至少1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18或所有19个核苷酸(在
seq id no:4至seq id no:7或seq id no:8至seq id no:11之一的任一端)。
[0318]
因此,本发明提供了一种核酸,该核酸当被适当地引入或表达于原本表达il
‑
11或il
‑
11rα的哺乳动物细胞中时能够通过rnai抑制il
‑
11或il
‑
11rα表达,其中该核酸通常靶向seq id no:4至seq id no:7或seq id no:8至seq id no:11之一的序列。
[0319]
所谓“通常靶向”是指该核酸可靶向与seq id no:4至seq id no:7或seq id no:8至seq id no:11重叠的序列。特别地,该核酸可靶向人il
‑
11或il
‑
11rα的mrna中的序列,该序列比seq id no:4至seq id no:7或seq id no:8至seq id no:11之一稍长或稍短(优选地长度为17
‑
23个核苷酸),但在其他方面与seq id no:4至seq id no:7或seq id no:8至seq id no:11之一相同。
[0320]
预期本发明的核酸和靶序列之间的完全同一性/互补性虽然是优选的,但不是必需的。因此,与il
‑
11或il
‑
11rα的mrna相比,本发明的核酸可包括单个错配。然而,预期即使存在单个错配也可能导致效率降低,因此优选不存在错配。当存在时,3’突出端可从错配数目的考虑中排除。
[0321]
术语“互补性”不限于由天然存在的核糖核苷酸和/或脱氧核糖核苷酸组成的核酸之间的常规碱基配对,还包括mrna和包括非天然核苷酸的本发明核酸之间的碱基配对。
[0322]
在一个实施方案中,核酸(本文称为双链sirna)包括seq id no:12至seq id no:15所示的双链rna序列。在另一个实施方案中,核酸(本文称为双链sirna)包括seq id no:16至seq id no:19所示的双链rna序列。
[0323]
然而,还预期针对il
‑
11或il
‑
11rαmrna的相同区域的稍短或稍长的序列也将是有效的。特别地,预期长度为17bp至23bp的双链序列也将是有效的。
[0324]
形成双链rna的链可具有短的3’二核苷酸突出端,其可以是dna或rna。与3’rna突出端相比,使用3’dna突出端对sirna活性没有影响,但降低了核酸链化学合成的成本(elbashir等人,2001c)。因此,dna二核苷酸可能是优选的。
[0325]
当存在时,二核苷酸突出端可以是彼此对称的,但这不是必需的。实际上,有义(上)链的3’突出端与rnai活性无关,因为它不参与mrna识别和降解(elbashir等人,2001a,2001b,2001c)。
[0326]
尽管果蝇中的rnai实验表明反义3’突出端可参与mrna识别和靶向(elbashir等人,2001c),但是3’突出端似乎不是哺乳动物细胞中sirna的rnai活性所必需的。因此认为3’突出端的不正确退火在哺乳动物细胞中几乎没有影响(elbashir等人,2001c;czauderna等人,2003)。
[0327]
因此,任何二核苷酸突出端可用于sirna的反义链中。然而,二核苷酸优选地为
‑
uu或
‑
ug(或
‑
tt或
‑
tg,如果突出端是dna),更优选地为
‑
uu(或
‑
tt)。
‑
uu(或
‑
tt)二核苷酸突出端是最有效的,并且与转录信号的rna聚合酶iii末端(终止子信号是ttttt)一致(即,能够形成其一部分)。因此,这种二核苷酸是最优选的。也可使用二核苷酸aa、cc和gg,但效果较差,因此不太优选。
[0328]
此外,sirna的3’突出端可完全被省略。
[0329]
本发明还提供了分别由上述双链核酸之一的组成链组成的单链核酸(本文中称为单链sirna),优选地具有3’突出端,但任选地不具有该突出端。本发明还提供了含有这种单链核酸对的试剂盒,该单链核酸对能够在体外彼此杂交以形成上述双链sirna,然后可将该
双链sirna引入细胞中。
[0330]
本发明还提供了当在哺乳动物细胞中转录时产生具有两个互补部分的rna(本文也称为shrna)的dna,这两个互补部分能够自杂交以产生双链基序,例如包括选自seq id no:12至seq id no:15或seq id no:16至seq id no:19的序列,或通过单碱基对置换而不同于前述序列中的任一序列的序列。
[0331]
互补部分通常通过间隔区连接,该间隔区具有合适的长度和序列以允许两个互补部分彼此杂交。两个互补(即,有义和反义)部分可以任一顺序在5
’‑3’
连接。间隔区通常是大约4
‑
12个核苷酸,优选地4
‑
9个核苷酸,更优选地6
‑
9个核苷酸的短序列。
[0332]
优选地,间隔区的5'端(紧接上游互补部分的3'端)由核苷酸
‑
uu
‑
或
‑
ug
‑
组成,同样优选地由
‑
uu
‑
组成(尽管同样地,使用这些特定的二核苷酸不是必需的)。推荐用于oligoengine(西雅图,美国华盛顿)的psuper系统的合适间隔区是uucaagaga。在这种情况和其他情况下,间隔区的末端可彼此杂交,例如将双链基序延伸超出seq id no:12至seq id no:15或seq id no:16至seq id no:19的确切序列少量(例如,1或2个)碱基对。
[0333]
类似地,转录的rna优选地包括来自下游互补部分的3’突出端。同样,这优选地为
‑
uu或
‑
ug,更优选地为
‑
uu。
[0334]
然后,可在哺乳动物细胞中通过dicer酶切割此类shrna分子,以产生如上所述的双链sirna,其中杂交的dsrna的一条链或每条链包括3’突出端。
[0335]
用于合成本发明核酸的技术当然是本领域熟知的。
[0336]
技术人员能够使用熟知的技术和市售的材料构建用于本发明dna的合适的转录载体。特别地,dna将与控制序列相关,包括启动子和转录终止序列。
[0337]
特别合适的是市售的oligoengine(西雅图,美国华盛顿)的psuper和psuperior系统。这些系统使用聚合酶
‑
iii启动子(h1)和t5转录终止子序列,该序列在转录物的3’末端提供两个u残基(这两个u残基在dicer加工后,提供sirna的一条链的3’uu突出端)。
[0338]
在shin等人(rna,2009年5月;15(5):898
‑
910)中描述了另一种合适的系统,该系统使用另一种聚合酶
‑
iii启动子(u6)。
[0339]
本发明的双链sirna可使用如下所述的已知技术在体外或体内引入哺乳动物细胞中,以抑制il
‑
11或il
‑
11受体的表达。
[0340]
类似地,含有本发明dna的转录载体可使用如下所述的用于rna的瞬时或稳定表达的已知技术在体外或体内引入肿瘤细胞中,以同样抑制il
‑
11或il
‑
11受体的表达。
[0341]
因此,本发明还提供了抑制哺乳动物(例如,人)细胞中il
‑
11或il
‑
11受体表达的方法,该方法包括向细胞施用本发明的双链sirna或本发明的转录载体。
[0342]
类似地,本发明还提供了治疗肾损伤和/或与肾损伤相关的障碍、疾病或病症的方法,该方法包括向受试者施用本发明的双链sirna或本发明的转录载体。
[0343]
本发明还提供了本发明的双链sirna和本发明的转录载体,用于治疗方法,优选地用于治疗肾损伤和/或与肾损伤相关的障碍、疾病或病症的方法。
[0344]
本发明还提供了本发明的双链sirna和本发明的转录载体在制备药物中的用途,该药物用于治疗肾损伤和/或与肾损伤相关的障碍、疾病或病症。
[0345]
本发明还提供了一种组合物,该组合物包含与一种或多种药学上可接受的载体混合的本发明的双链sirna或本发明的转录载体。合适的载体包括亲脂性载体或囊泡,其可有
助于穿透细胞膜。
[0346]
适于施用本发明的sirna双链体和dna载体的材料和方法是本领域熟知的,并且考虑到rnai技术的潜力,正在开发改进的方法。
[0347]
通常,许多技术可用于将核酸引入哺乳动物细胞中。技术的选择将取决于核酸是转移到体外培养的细胞中,还是转移到患者体内的细胞中。适于体外将核酸转移到哺乳动物细胞中的技术包括使用脂质体、电穿孔、显微注射、细胞融合、deae、葡聚糖和磷酸钙沉淀。体内基因转移技术包括用病毒(通常为逆转录病毒)载体转染和病毒外壳蛋白
‑
脂质体介导的转染(dzau等人,(2003)trends in biotechnology 11,205
‑
210)。
[0348]
特别地,在以下文章中公开了用于在体外和体内细胞施用本发明核酸的合适技术:
[0349]
一般性综述:borkhardt,a.2002.,“通过rna干扰阻断恶性细胞中的癌基因——高度特异性癌症治疗的新希望?”,cancer cell.2:167
‑
8。hannon,g.j.2002.,“rna干扰”,nature.418:244
‑
51。mcmanus,m.t.,和p.a.sharp.2002.,“哺乳动物中小干扰rna的基因沉默”,nat rev genet.3:737
‑
47。scherr,m.、m.a.morgan和m.eder.2003b.,“哺乳动物细胞中由小干扰rna介导的基因沉默”,curr med chem.10:245
‑
56。shuey,d.j.、d.e.mccallus和t.giordano.2002.,“rnai:治疗干预中的基因沉默”,drug discov today.7:1040
‑
6。
[0350]
使用脂质体的全身递送:lewis,d.l.、j.e.hagstrom、a.g.loomis、j.a.wolff和h.herweijer.2002.,“sirna的有效传递以抑制出生后小鼠的基因表达”,nat genet.32:107
‑
8。paul,c.p.、p.d.good、i.winer和d.r.engelke.2002.,“小干扰rna在人体细胞中的有效表达”,nat biotechnol.20:505
‑
8。song,e.、s.k.lee、j.wang、n.ince、n.ouyang、j.min、j.chen、p.shankar和j.lieberman.2003.,“靶向fas的rna干扰可保护小鼠免受暴发性肝炎的侵害”,nat med.9:347
‑
51。sorensen,d.r.、m.leirdal和m.sioud.2003.,“通过在成年小鼠中全身递送合成sirna进行基因沉默”,j mol biol.327:761
‑
6。
[0351]
病毒介导的转移:abbas
‑
terki,t.、w.blanco
‑
bose、n.deglon、w.pralong和p.aebischer.2002.,“慢病毒介导的rna干扰”,hum gene ther.13:2197
‑
201。barton,g.m.和r.medzhitov.2002.,“将小干扰rna逆转录病毒递送到原代细胞中”,proc natl acad sci u s a.99:14943
‑
5。devroe,e.和p.a.silver.2002.,“逆转录病毒递送的sirna”,bmc biotechnol.2:15。lori,f.、p.guallini、l.galluzzi和j.lisziewicz.2002.,“hiv感染的基因治疗方法”,am j pharmacogenomics.2:245
‑
52。matta,h.、b.hozayev、r.tomar、p.chugh和p.m.chaudhary.2003.,“使用慢病毒载体递送小干扰rna”,cancer biol ther.2:206
‑
10。qin,x.f.、d.s.an、i.s.chen和d.baltimore.2003.,“通过慢病毒介导的针对ccr5的小干扰rna递送抑制人类t细胞中的hiv
‑
1感染”,proc natl acad sci u s a.100:183
‑
8。scherr,m.、k.battmer、a.ganser和m.eder.2003a.,“通过慢病毒介导的小干扰rna递送调节基因表达”,cell cycle.2:251
‑
7。shen,c.、a.k.buck、x.liu、m.winkler和s.n.reske.2003.,“通过腺病毒传递的sirna进行基因沉默”,febs lett.539:111
‑
4。
[0352]
肽递送:morris,m.c.、l.chaloin、f.heitz和g.divita.2000.,“易位肽和蛋白质及其在基因传递中的用途”,curr opin biotechnol.11:461
‑
6。simeoni,f.、m.c.morris、f.heitz和g.divita.2003.,“深入了解基于肽的基因传递系统mpg的机制:将sirna传递到哺乳动物细胞中的意义”,nucleic acids res.31:2717
‑
24。其他可适于将sirna递送至靶
细胞的技术是基于纳米颗粒或纳米胶囊,诸如美国专利号6,649,192b和5,843,509b中描述的那些技术。
[0353]
抑制il
‑
11介导的信号传导
[0354]
在本发明的实施方案中,能够抑制il
‑
11作用的药剂可具有一种或多种下列功能特性:
[0355]
·
抑制il
‑
11介导的信号传导;
[0356]
·
抑制由il
‑
11与il
‑
11rα:gp130受体复合物结合介导的信号传导;
[0357]
·
抑制由il
‑
11:il
‑
11rα复合物与gp130结合介导的信号传导(即,il
‑
11反式信号传导);
[0358]
·
抑制il
‑
11介导的过程;
[0359]
·
抑制il
‑
11和/或il
‑
11rα的基因/蛋白表达。
[0360]
这些特性可通过在合适的测定中分析相关药剂来确定,这可能涉及将药剂的性能与合适的对照药剂进行比较。技术人员能够确定用于给定测定的合适对照条件。
[0361]
il
‑
11介导的信号传导和/或il
‑
11介导的过程包括il
‑
11片段和包含il
‑
11或其片段的多肽复合物介导的信号传导。il
‑
11介导的信号传导可以是由人il
‑
11和/或小鼠il
‑
11介导的信号传导。在il
‑
11或含il
‑
11的复合物与il
‑
11或所述复合物所结合的受体结合后,可发生il
‑
11介导的信号传导。
[0362]
在一些实施方案中,药剂可能能够抑制il
‑
11或含il
‑
11的复合物的生物活性。
[0363]
在一些实施方案中,药剂是一种或多种信号传导途径的拮抗剂,该一种或多种信号传导途径由通过包含il
‑
11rα和/或gp130的受体(例如,il
‑
11rα:gp130)的信号转导激活。在一些实施方案中,药剂能够抑制通过一种或多种包含il
‑
11rα和/或gp130的免疫受体复合物(例如,il
‑
11rα:gp130)的信号传导。在本发明的各个方面,本文提供的药剂能够抑制il
‑
11介导的顺式和/或反式信号传导。在根据本发明的各个方面的一些实施方案中,本文提供的药剂能够抑制il
‑
11介导的顺式信号传导。
[0364]
在一些实施方案中,相比于不存在药剂时(或存在适当对照药剂时)的信号传导水平,该药剂可能能够将il
‑
11介导的信号传导抑制为小于100%,例如,为99%或更小、95%或更小、90%或更小、85%或更小、80%或更小、75%或更小、70%或更小、65%或更小、60%或更小、55%或更小、50%或更小、45%或更小、40%或更小、35%或更小、30%或更小、25%或更小、20%或更小、15%或更小、10%或更小、5%或更小、或1%或更小之一。在一些实施方案中,相比于不存在药剂时(或存在适当对照药剂时)的信号传导水平,该药剂能够将il
‑
11介导的信号传导降低至小于1倍,例如,为≤0.99倍、≤0.95倍、≤0.9倍、≤0.85倍、≤0.8倍、≤0.75倍、≤0.7倍、≤0.65倍、≤0.6倍、≤0.55倍、≤0.5倍、≤0.45倍、≤0.4倍、≤0.35倍、≤0.3倍、≤0.25倍、≤0.2倍、≤0.15倍、≤0.1倍之一。
[0365]
在一些实施方案中,il
‑
11介导的信号传导可以是由il
‑
11与il
‑
11rα:gp130受体结合介导的信号传导。例如,可通过用il
‑
11处理表达il
‑
11rα和gp130的细胞,或通过刺激表达il
‑
11rα和gp130的细胞中il
‑
11的产生,来分析这种信号传导。
[0366]
例如,通过在人il
‑
11和药剂存在的情况下培养表达il
‑
11rα和gp130的ba/f3细胞,并测量3h
‑
胸苷向dna的掺入,可确定抑制il
‑
11介导的信号传导的药剂的ic
50
。在一些实施方案中,在此类测定中,药剂可表现出10μg/ml或更小,优选地≤5μg/ml、≤4μg/ml、≤3.5
μg/ml、≤3μg/ml、≤2μg/ml、≤1μg/ml、≤0.9μg/ml、≤0.8μg/ml、≤0.7μg/ml、≤0.6μg/ml或≤0.5μg/ml之一的ic
50
。
[0367]
在一些实施方案中,il
‑
11介导的信号传导可以是由il
‑
11:il
‑
11rα复合物与gp130结合介导的信号传导。在一些实施方案中,il
‑
11:il
‑
11rα复合物可以是可溶性的,例如il
‑
11rα的胞外结构域与il
‑
11的复合物,或可溶性il
‑
11rα同工型/片段与il
‑
11的复合物。在一些实施方案中,可溶性il
‑
11rα是il
‑
11rα的可溶性(分泌型)同工型,或者是细胞膜结合的il
‑
11rα的胞外结构域的蛋白水解切割的释放产物。
[0368]
在一些实施方案中,il
‑
11:il
‑
11rα复合物可以是细胞结合的,例如细胞膜结合的il
‑
11rα和il
‑
11的复合物。由il
‑
11:il
‑
11rα复合物与gp130结合介导的信号传导可通过用il
‑
11:il
‑
11rα复合物(例如,包含通过肽接头与il
‑
11rα的胞外结构域连接的il
‑
11的重组融合蛋白,例如超il
‑
11)处理表达gp130的细胞来分析。使用il
‑
11rα的片段(由结构域1至3组成的氨基酸残基1至317;uniprotkb:q14626)和il
‑
11(uniprotkb:p20809的氨基酸残基22至199)与20个氨基酸长的接头(seq id no:20)构建超il
‑
11。超il
‑
11的氨基酸序列示出在seq id no:21中。
[0369]
在一些实施方案中,药剂可能能够抑制由il
‑
11:il
‑
11rα复合物与gp130结合介导的信号传导,并且还能够抑制由il
‑
11与il
‑
11rα:gp130受体结合介导的信号传导。
[0370]
在一些实施方案中,药剂可能能够抑制il
‑
11介导的过程。
[0371]
在一些实施方案中,药剂可能能够抑制il
‑
11和/或il
‑
11rα的基因/蛋白表达。基因和/或蛋白质表达可如本文所述或通过本领域技术人员熟知的本领域方法来测量。
[0372]
在一些实施方案中,相比于不存在药剂时(或存在适当对照药剂时)的表达水平,该药剂可能能够将il
‑
11和/或il
‑
11rα的基因/蛋白质表达抑制为小于100%,例如,为99%或更小、95%或更小、90%或更小、85%或更小、80%或更小、75%或更小、70%或更小、65%或更小、60%或更小、55%或更小、50%或更小、45%或更小、40%或更小、35%或更小、30%或更小、25%或更小、20%或更小、15%或更小、10%或更小、5%或更小、或1%或更小之一。在一些实施方案中,相比于不存在药剂时(或存在适当对照药剂时)的表达水平,该药剂能够将il
‑
11和/或il
‑
11rα的基因/蛋白质表达抑制为小于1倍,例如,为≤0.99倍、≤0.95倍、≤0.9倍、≤0.85倍、≤0.8倍、≤0.75倍、≤0.7倍、≤0.65倍、≤0.6倍、≤0.55倍、≤0.5倍、≤0.45倍、≤0.4倍、≤0.35倍、≤0.3倍、≤0.25倍、≤0.2倍、≤0.15倍、≤0.1倍之一。
[0373]
肾损伤的治疗/预防
[0374]
本发明提供了用于治疗/预防肾损伤(例如,如本文所述)和与肾损伤相关的障碍、疾病或病症的方法和制品(药剂和组合物)。
[0375]
通过抑制il
‑
11介导的信号传导(即,拮抗il
‑
11介导的信号传导)来实现治疗。也就是说,本发明提供了通过在例如细胞、组织/器官/器官系统/受试者中抑制il
‑
11介导的信号传导来治疗/预防肾损伤和与肾损伤相关的障碍、疾病或病症。在一些实施方案中,根据本公开的对il
‑
11介导的信号传导的抑制包括对肾的细胞(例如,肾小管上皮细胞)中il
‑
11介导的信号传导的抑制。
[0376]
提供了能够抑制白介素11(il
‑
11)介导的信号传导的药剂,该药剂用于治疗或预防肾损伤和/或与肾损伤相关的障碍、疾病或病症的方法中。
[0377]
还提供了能够抑制白介素11(il
‑
11)介导的信号传导的药剂用于制备药物的用
途,该药物用于治疗或预防肾损伤和/或与肾损伤相关的障碍、疾病或病症的方法中。
[0378]
还提供了治疗或预防肾损伤和/或与肾损伤相关的障碍、疾病或病症的方法,该方法包括向需要治疗的受试者施用治疗有效量的能够抑制白介素11(il
‑
11)介导的信号传导的药剂。
[0379]
在一些实施方案中,本发明提供了疾病/病症中肾损伤相关病理的治疗/预防。也就是说,本发明提供了病理学上涉及肾损伤的疾病/病症的治疗/预防。本文描述了肾损伤相关病理。特别地,相关病理包括对近端、远端或两者的肾小管上皮细胞的损害。
[0380]
此外,本文证实了能够抑制白介素11(il
‑
11)介导的信号传导的药剂能够逆转肾损伤。也就是说,对il
‑
11介导的信号传导的抑制表明能够改善肾损伤后的肾功能。
[0381]
因此,本发明考虑采用il
‑
11介导的信号传导的拮抗剂来增强/改善肾功能受损(例如,由于肾损伤)的受试者的肾功能。
[0382]
能够抑制白介素11(il
‑
11)介导的信号传导的药剂可用于促进tec增殖,用于产生功能性肾组织。因此,本文提供了能够抑制白介素11(il
‑
11)介导的信号传导的药剂,该药剂用于促进肾小管上皮细胞(tec)的增殖、存活和/或功能,和/或肾组织的生长、维持和/或功能。
[0383]
本文提供了能够抑制白介素11(il
‑
11)介导的信号传导的药剂,该药剂用于再生肾小管上皮细胞(tec)和/或肾组织。
[0384]
由肾小管上皮细胞进行的上皮和/或acta向间充质细胞样表型的转化(本文也称为“emt”)与肾功能降低相关。tec进行的emt是由组织损伤后产生的可溶性因子诸如tgfb1诱导的。对il
‑
11介导的信号传导的拮抗在本文中显示为抑制tec进行的emt,并由此保护/改善肾功能。
[0385]
snail的表达与tec增殖能力的丧失以及emt有关。il
‑
11介导的信号传导在本文中被证实在上调snail表达中起重要作用。因此,本发明考虑采用il
‑
11介导的信号传导的拮抗剂来抑制snail(例如,在tec中)的表达。il
‑
11介导的信号传导的拮抗从snail介导的对tec增殖的抑制中释放tec。
[0386]
因此,本发明考虑采用il
‑
11介导的信号传导的拮抗剂来保持/增加肾中具有tec表型的细胞的数量/比例。tec表型可例如通过e
‑
钙粘蛋白表达来表征。本发明考虑采用il
‑
11介导的信号传导的拮抗剂来减少肾中具有间充质细胞样表型的细胞的数量/比例。间充质细胞样表型可例如通过snail和/或acta2表达来表征,任选地缺乏e
‑
钙粘蛋白表达。
[0387]
il
‑
11介导的信号传导的拮抗剂可用于保持/增加tec或肾组织的功能水平的方法中。例如,可通过评价这种活性的相关性来评价tec/肾组织功能。例如,可通过分析血清/血液中尿素和/或肌酸的水平(例如,血尿素氮),或通过监测白蛋白与肌酸的比率(acr)来评价tec/肾组织功能。il
‑
11介导的信号传导的拮抗剂可用于降低血清/血液中肌酸和/或尿素的水平或降低acr的方法中。
[0388]
本领域技术人员将清楚,本发明的治疗和预防效用基本上扩展到将受益于肾损伤和/或肾损伤相关病理的减轻的任何疾病/病症。本发明的治疗和预防效用扩展到患有肾损伤和/或与肾损伤相关的障碍、疾病或病症的任何受试者。本发明的治疗和预防效用还扩展到患有其中存在肾损伤相关病理的疾病的任何受试者。
[0389]
在一些实施方案中,本发明提供了由肾损伤引起/加剧的疾病/病症的治疗/预防。
在一些实施方案中,提供了对其中肾损伤提供不良预后的受试者的疾病/病症的治疗/预防。
[0390]
急性肾损伤的诊断和管理描述于rahman m等人,“急性肾损伤:诊断和管理指南”,am fam physician,2012年10月1日:86(7):631
‑
9。如其中所述,急性肾损伤的特征在于肾功能突然恶化,表现为血清肌酸酐水平升高,伴有或不伴有尿排出量减少。
[0391]
在一些实施方案中,待治疗/预防的肾损伤和/或与肾损伤相关的障碍、疾病或病症的特征可在于,例如与正常器官/组织/受试者(即,没有肾损伤或与肾损伤相关的障碍、疾病或病症)相比,受肾损伤和/或与肾损伤相关的障碍、疾病或病症影响的器官/组织/受试者中的以下一者或多者增加:il
‑
11和il
‑
11rα中的一者或多者的表达。
[0392]
在一些实施方案中,本发明提供了在例如如本文所述的与肾损伤相关的疾病/障碍/病症的背景下治疗/预防肾损伤。在一些实施方案中,本发明提供了肾损伤和与肾损伤相关的潜在疾病/障碍/病症的治疗/预防。例如,抑制il
‑
11介导的信号传导可用于拮抗il
‑
11在化疗相关的肾损伤中的作用,以及拮抗il
‑
11在癌症本身中的作用。
[0393]
根据本发明,肾损伤和/或与肾损伤相关的障碍、疾病或病症的治疗/预防可以是与il
‑
11上调相关的肾损伤和/或与肾损伤相关的障碍、疾病或病症,例如在其中疾病/障碍/病症的症状表现或可能发生的细胞或组织中il
‑
11的上调,或细胞外il
‑
11或il
‑
11rα的上调。
[0394]
与肾损伤相关的障碍、疾病或病症可影响任何组织或器官或器官系统。在一些实施方案中,疾病/障碍/病症可影响若干组织/器官/器官系统。在一些实施方案中,疾病/障碍/病症影响肾。
[0395]
在一些实施方案中,与肾损伤相关的障碍、疾病或病症影响以下的一者或多者:心血管系统、消化系统、排泄系统、呼吸系统、肾系统、生殖系统、循环系统、肌肉系统、内分泌系统、外分泌系统、淋巴系统、免疫系统、神经系统和/或骨骼系统。
[0396]
在一些实施方案中,本发明提供了治疗/预防急性肾损伤、肾毒性、药物诱导的肾损伤、药物诱导的急性肾损伤、药物诱导的肾毒性、顺铂诱导的肾损伤、顺铂诱导的急性肾损伤、顺铂诱导的肾毒性中的肾损伤相关病理。
[0397]
治疗可有效预防肾损伤和/或与肾损伤相关的障碍、疾病或病症的进展,例如减少/延迟/预防肾损伤和/或与肾损伤相关的障碍、疾病或病症的恶化,或减少/延迟/预防其发展。在一些实施方案中,治疗可使肾损伤和/或与肾损伤相关的障碍、疾病或病症的症状得到改善,例如严重程度的降低和/或逆转。在一些实施方案中,治疗可增加存活率。在一些实施方案中,治疗有效逆转肾损伤和/或与肾损伤相关的障碍、疾病或病症的影响和/或症状。
[0398]
预防可指预防肾损伤和/或与肾损伤相关的障碍、疾病或病症的发展,和/或预防肾损伤和/或与肾损伤相关的障碍、疾病或病症的恶化,例如,预防肾损伤和/或与肾损伤相关的障碍、疾病或病症进展到晚期或慢性阶段。
[0399]
在一些实施方案中,本发明提供了急性肾损伤(aki)、急性肾衰竭、急性肾病、慢性肾病、肾损害、药物诱导的肾损伤、肾小管坏死、急性肾小管坏死、自身免疫性肾损伤和癌症的治疗/预防。
[0400]
急性肾小管坏死是住院患者中最常见的内源性急性肾损伤类型(rahman m等人,
同上)。诱因通常是缺血性的(由于长期低血压)或肾毒性的(由于对肾小管细胞有毒的药剂)。由急性肾小管坏死引起的急性肾损伤通常不会随着血管内容积和流向肾的血流的充分充盈而改善。缺血性和肾毒性急性肾小管坏死均可随着时间的推移而消退,但可能需要临时的肾替代疗法,这取决于肾损伤的程度和先前存在的慢性肾病的存在。
[0401]
本文所指的“癌症”可以是任何不希望的细胞增殖(或通过不希望的细胞增殖表现出自身的任何疾病)、赘生物或肿瘤,或增加的不希望的细胞增殖、赘生物或肿瘤的风险或倾向。癌症可以是良性的或恶性的,并且可以是原发性的或继发性的(转移性的)。赘生物或肿瘤可以是细胞的任何异常生长或增殖,并且可位于任何组织中。组织的示例包括肾上腺、肾上腺髓质、肛门、阑尾、膀胱、血液、骨、骨髓、大脑、乳房、盲肠、中枢神经系统(包括或不包括大脑)、小脑、子宫颈、结肠、十二指肠、子宫内膜、上皮细胞(例如,肾上皮细胞)、胆囊、食管、神经胶质细胞、心脏、回肠、空肠、肾、泪腺、喉、肝、肺、淋巴、淋巴结(包括腹部淋巴结、腋窝淋巴结、颈部淋巴结、腹股沟淋巴结、纵隔淋巴结、盆腔淋巴结、主动脉周围淋巴结)、淋巴母细胞、上颌骨、纵隔、肠系膜、子宫肌层、鼻咽、网膜、口腔、卵巢、胰腺、腮腺、周围神经系统腹膜、胸膜、前列腺、唾液腺、乙状结肠、皮肤、小肠、软组织、脾、胃、睾丸、胸腺、甲状腺、舌、扁桃体、气管、子宫、外阴、白细胞。
[0402]
癌症可能属于特定类型。癌症类型的示例包括星形细胞瘤、癌(例如,腺癌、肝细胞癌、髓样癌、乳头状癌、鳞状细胞癌)、神经胶质瘤、淋巴瘤、髓母细胞瘤、黑色素瘤、骨髓瘤、脑膜瘤、神经母细胞瘤、肉瘤(例如,血管肉瘤、慢性肉瘤、骨肉瘤)。
[0403]
如本文所用,“癌症”可包括以下中的任一者或多者:急性淋巴细胞白血病(all)、急性髓性白血病(aml)、肾上腺皮质癌、肛门癌、膀胱癌、血癌、骨癌、脑瘤、乳腺癌、女性生殖系统癌、男性生殖系统癌、中枢神经系统淋巴瘤、宫颈癌、儿童横纹肌肉瘤、儿童肉瘤、慢性淋巴细胞白血病(cll)、慢性髓性白血病(cml)、结肠和直肠癌、结肠癌、子宫内膜肉瘤、食道癌、眼癌、胆囊癌、胃癌、胃肠道癌、毛细胞白血病、头颈癌、肝细胞癌、霍奇金病、下咽癌、卡波济氏肉瘤、肾癌、喉癌、白血病、白血病、白血病、肝癌、肺癌、恶性纤维组织细胞瘤、恶性胸腺瘤、黑色素瘤、间皮瘤、多发性骨髓瘤、骨髓瘤、鼻腔和鼻窦癌、鼻咽癌、神经系统癌、神经母细胞瘤、非霍奇金淋巴瘤、口腔癌、口咽癌、骨肉瘤、卵巢癌、胰腺癌、甲状旁腺癌、阴茎癌、咽癌、垂体瘤、浆细胞肿瘤、原发性中枢神经系统淋巴瘤、前列腺癌、直肠癌、呼吸系统、视网膜母细胞瘤、唾液腺癌、皮肤癌、小肠癌、软组织肉瘤、胃癌、胃癌、睾丸癌、甲状腺癌、泌尿系统癌、子宫肉瘤、阴道癌、血管系统、waldenstrom氏巨球蛋白血症和wilms瘤。
[0404]
根据本发明的各个方面,方法可包括以下的一者或多者(例如,在肾损伤的背景下):
[0405]
减少肾组织和/或肾细胞的坏死;
[0406]
减少肾和/或肾组织的纤维化;
[0407]
降低肾和/或肾组织的胶原含量和/或抑制肾和/或肾组织中的胶原沉积;
[0408]
增加/维持肾功能;
[0409]
增加/维持尿排出量;
[0410]
降低尿白蛋白/肌酸酐比率;
[0411]
降低血清肌酸酐水平;
[0412]
降低血清尿素水平;
[0413]
降低血清tgfβ1水平;
[0414]
增加/维持肾重量;
[0415]
增加/维持肾皮质体积;
[0416]
增加/维持体重;
[0417]
抑制肾小管上皮细胞的上皮
‑
间充质细胞转化;
[0418]
减少肾中acta2 ve细胞的数量/比例;
[0419]
降低肾细胞和/或肾/肾组织中snail的表达;以及
[0420]
增加/维持肾细胞对e
‑
钙粘蛋白的表达和/或肾/肾组织中e
‑
钙粘蛋白的表达。
[0421]
施用
[0422]
施用能够抑制il
‑
11介导的信号传导的药剂优选地为“治疗有效”或“预防有效”量,该量足以使患者获益。
[0423]
在一些实施方案中,可在肾损伤的诱因(例如,施用或服用肾毒性药物或暴露于肾损伤的环境来源)之前、同时或之后施用药剂。
[0424]
施用的实际量、施用的速率和疗程将取决于肾损伤的性质和严重程度以及药剂的性质。治疗处方,例如剂量决定等,在全科医生和其他医生的责任范围内,并且通常考虑待治疗的疾病/病症、个体受试者的状况、递送部位、施用方法和医生已知的其他因素。上述技术和方案的示例可见于《雷明顿药学》,第20版,(利平科特,威廉姆斯和威尔金斯出版社2000年出版)中。
[0425]
可提供多次剂量的药剂。一次或多次或每次剂量可伴随另一种治疗剂的同时或依次施用。
[0426]
多次剂量可由预定时间间隔分开,该时间间隔可被选择为1、2、3、4、5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20、21、22、23、24、25、26、27、28、29、30或31天,或1、2、3、4、5或6个月之一。例如,剂量可每7、14、21或28天(加或减3、2或1天)给予一次。
[0427]
在治疗应用中,能够抑制il
‑
11介导的信号传导的药剂优选地与一种或多种本领域技术人员熟知的其他药学上可接受的成分一起配制成药物或药品,其他药学上可接受的成分包括但不限于药学上可接受的载体、佐剂、赋形剂、稀释剂、填充剂、缓冲剂、防腐剂、抗氧化剂、润滑剂、稳定剂、增溶剂、表面活性剂(例如,润湿剂)、掩蔽剂、着色剂、调味剂和甜味剂。
[0428]
本文所用的术语“药学上可接受的”涉及化合物、成分、材料、组合物、剂型等,其在合理的医学判断范围内,适用于与所讨论的受试者(例如,人)的组织接触而没有过度的毒性、刺激、过敏反应或其他问题或并发症,与合理的收益/风险比相称。每种载体、佐剂、赋形剂等在与制剂的其他成分相容的意义上也必须是“可接受的”。
[0429]
合适的载体、佐剂、赋形剂等可见于标准药学教科书中,例如《雷明顿药学》,第18版,mack出版公司,宾夕法尼亚州伊斯顿,1990;以及《药用辅料手册》,第2版,1994。
[0430]
制剂可通过药学领域公知的任何方法来制备。此类方法包括将活性化合物与构成一种或多种辅助成分的载体结合的步骤。通常,通过将活性化合物与载体(例如,液体载体、细分的固体载体等)均匀且紧密地结合,然后必要时使产品成型来制备制剂。
[0431]
制剂可被制备用于局部、肠胃外、全身、静脉内、动脉内、肌内、鞘内、眼内、结膜内、皮下、口服或经皮施用途径(其可包括注射)。可注射制剂可包含无菌或等渗介质中的选定
药剂。可根据药剂和待治疗的疾病/障碍/病症来选择施用的制剂和方式。
[0432]
在一些情况下,施用如本文所述的制品(例如,药剂/组合物)以用于如本文所述的治疗,连同用于与肾损伤相关的疾病/障碍/病症的治疗。用于与肾损伤相关的疾病/障碍/病症的合适治疗是本领域已知的。组合物可单独施用或与其他治疗剂联合施用,同时或依次施用,具体取决于待治疗的疾病/障碍/病症。例如,制品可在治疗剂之前、同时或之后施用。制品和治疗剂可一起配制,例如配制于上述制剂中,或分开配制。
[0433]
il
‑
11和il
‑
11受体的检测
[0434]
本发明的一些方面和实施方案涉及检测从受试者获得的样品中il
‑
11或il
‑
11受体(例如,il
‑
11rα、gp130或含il
‑
11rα和/或gp130的复合物)的表达。
[0435]
在一些方面和实施方案中,本发明涉及il
‑
11或il
‑
11受体(作为编码相应il
‑
11或il
‑
11受体的蛋白质或寡核苷酸)表达的上调(过表达),并检测这种上调作为用能够抑制il
‑
11作用的药剂或用能够阻止或减少il
‑
11或il
‑
11受体表达的药剂治疗的适宜性的指标。
[0436]
上调的表达包括比给定类型的细胞或组织正常预期的表达水平更高水平的表达。上调可通过测量细胞或组织中相关因子的表达水平来确定。可比较来自受试者的细胞或组织样品中的表达水平和相关因子的参考表达水平,例如代表相同或对应细胞或组织类型的相关因子的正常表达水平的值或值的范围。在一些实施方案中,可通过检测对照样品中(例如,在健康受试者或同一受试者健康组织的对应细胞或组织中)il
‑
11或il
‑
11受体的表达来确定参考水平。在一些实施方案中,可从标准曲线或数据集获得参考水平。
[0437]
可定量表达水平用于绝对比较,或可进行相对比较。
[0438]
在一些实施方案中,当测试样品中的表达水平至少是参考水平的1.1倍时,可认为il
‑
11或il
‑
11受体(例如,il
‑
11rα、gp130或含il
‑
11rα和/或gp130的复合物)存在上调。更优选地,表达水平可选自参考水平的至少1.2倍、至少1.3倍、至少1.4倍、至少1.5倍、至少1.6倍、至少1.7倍、至少1.8倍、至少1.9倍、至少2.0倍、至少2.1倍、至少2.2倍、至少2.3倍、至少2.4倍、至少2.5倍、至少2.6倍、至少2.7倍、至少2.8倍、至少2.9倍、至少3.0倍、至少3.5倍、至少4.0倍、至少5.0倍、至少6.0倍、、至少7.0倍、至少8.0倍、至少9.0倍或至少10.0倍之一。
[0439]
表达水平可通过多种已知的体外测定技术中的一种来确定,例如基于pcr的测定、原位杂交测定、流式细胞术测定、免疫学或免疫组织化学测定。
[0440]
例如,合适的技术包括通过使样品与能够结合il
‑
11或il
‑
11受体的药剂接触并检测该药剂与il
‑
11或il
‑
11受体的复合物的形成来检测样品中il
‑
11或il
‑
11受体水平的方法。药剂可以是任何合适的结合分子,例如抗体、多肽、肽、寡核苷酸、适体或小分子,并且可任选地被标记以允许检测(例如,可视化)所形成的复合物。合适的标记及其检测手段是本领域技术人员熟知的,并且包括荧光标记(例如,荧光素、若丹明、曙红和ndb、绿色荧光蛋白(gfp)、稀土元素如铕(eu)、铽(tb)和钐(sm)的螯合物、四甲基若丹明、德克萨斯红、4
‑
甲基伞形酮、7
‑
氨基
‑4‑
甲基香豆素、cy3、cy5)、同位素标记、放射性同位素(例如,32p、33p、35s)、化学发光标记(例如,吖啶酯、鲁米诺、异鲁米诺)、酶(例如,过氧化物酶、碱性磷酸酶、葡萄糖氧化酶、β
‑
半乳糖苷酶、荧光素酶)、抗体、配体和受体。检测技术是本领域技术人员熟知的,并且可被选择以对应于标记药剂。合适的技术包括寡核苷酸标签的pcr扩增、质谱、
荧光或颜色的检测,例如在报告蛋白对底物的酶促转化后,或放射性的检测。
[0441]
测定可被配置为对样品中il
‑
11或il
‑
11受体的量进行定量。可将来自测试样品的il
‑
11或il
‑
11受体的定量的量与参考值进行比较,并且该比较用于确定测试样品是否含有比参考值更高或更低且达到选定的统计学显著性程度的il
‑
11或il
‑
11受体的量。
[0442]
对检测到的il
‑
11或il
‑
11受体定量可用于确定编码il
‑
11或il
‑
11受体的基因的上调或下调或扩增。在测试样品含有纤维化细胞的情况下,可将这种上调、下调或扩增与参考值进行比较以确定是否存在任何统计学显著差异。
[0443]
从受试者获得的样品可以是任何种类。生物样品可取自任何组织或体液,例如血液样品、血液衍生样品、血清样品、淋巴液样品、精液样品、唾液样品、滑液样品。血液衍生样品可以是患者血液的选定部分,例如,选定的含细胞部分或血浆或血清部分。样品可包括组织样品或活组织检查样品;或从受试者分离的细胞。样品可通过已知技术收集,诸如活组织检查或针抽吸。可储存和/或处理样品以用于随后确定il
‑
11表达水平。
[0444]
样品可用于确定接受样品采集的受试者中il
‑
11或il
‑
11受体的上调。
[0445]
在一些优选的实施方案中,样品可以是取自肾组织、心脏组织、内脏器官组织、呼吸系统器官组织或尿/肾系统组织的组织样品(例如,活组织检查样品)。样品可含有细胞。
[0446]
根据本发明,基于确定受试者具有上调的il
‑
11或il
‑
11受体(例如,il
‑
11rα、gp130或含il
‑
11rα和/或gp130的复合物)的表达水平,可选择受试者进行治疗/预防。il
‑
11或il
‑
11受体的上调表达可作为肾损伤和/或与肾损伤相关的障碍、疾病或病症的标志,适于用能够抑制il
‑
11介导的信号传导的药剂进行治疗。
[0447]
上调可在给定组织中或在来自给定组织的选定细胞中。优选的组织可以是肾/肾组织。il
‑
11或il
‑
11受体表达的上调也可在循环流体诸如血液或血液衍生样品中确定。上调可以是细胞外il
‑
11或il
‑
11rα的上调。在一些实施方案中,表达可局部或全身上调。
[0448]
选择后,可以给受试者施用能够抑制il
‑
11介导的信号传导的药剂。
[0449]
诊断和预后
[0450]
il
‑
11或il
‑
11受体(例如,il
‑
11rα、gp130或含il
‑
11rα和/或gp130的复合物)表达上调的检测也可用于诊断肾损伤和/或与肾损伤相关的障碍、疾病或病症从而鉴定有发展肾损伤和/或与肾损伤相关的障碍、疾病或病症的风险的受试者的方法,以及用于预后或预测受试者对用能够抑制il
‑
11介导的信号传导的药剂治疗的反应的方法。
[0451]“发展中”、“发展”和其他形式的“发展”可指障碍/疾病的发作,或障碍/疾病的持续或进展。
[0452]
在一些实施方案中,受试者可例如基于在受试者身体内或受试者身体的选定细胞/组织中存在指示肾损伤和/或与肾损伤相关的障碍、疾病或病症的其他症状而被怀疑具有或患有肾损伤和/或与肾损伤相关的障碍、疾病或病症,或者被认为处于发展肾损伤和/或与肾损伤相关的障碍、疾病或病症的风险中,例如,由于遗传倾向或暴露于已知为肾损伤和/或与肾损伤相关的障碍、疾病或病症的风险因素的环境条件。确定il
‑
11或il
‑
11受体表达的上调可确认诊断或疑似诊断,或可确认受试者处于发展肾损伤和/或与肾损伤相关的障碍、疾病或病症的风险中。该确定还可将肾损伤和/或与肾损伤或倾向相关的障碍、疾病或病症诊断为适于用能够抑制il
‑
11介导的信号传导的药剂治疗的肾损伤和/或与肾损伤或倾向相关的障碍、疾病或病症。
[0453]
因此,可提供一种为患有或疑似患有肾损伤和/或与肾损伤相关的障碍、疾病或病症的受试者提供预后的方法,该方法包括确定从该受试者获得的样品中il
‑
11或il
‑
11受体的表达是否上调,并且基于该确定,提供用能够抑制il
‑
11介导的信号传导的药剂治疗该受试者的预后。
[0454]
在一些方面,诊断方法或预后或预测受试者对用能够抑制il
‑
11介导的信号传导的药剂治疗的反应的方法可能不需要确定il
‑
11或il
‑
11受体的表达,但是可基于确定受试者中预测表达或活性上调的遗传因子。此类遗传因子可包括确定il
‑
11、il
‑
11rα和/或gp130中的遗传突变、单核苷酸多态性(snp)或基因扩增,它们与表达或活性的上调和/或il
‑
11介导的信号传导相关和/或预测表达或活性的上调和/或il
‑
11介导的信号传导。使用遗传因子预测对疾病状态的倾向或对治疗的反应是本领域已知的,例如参见petergut 2008;57:440
‑
442;wright等人,mol.cell.biol.,2010年3月,第30卷第6期,第1411
‑
1420页。
[0455]
遗传因子可通过本领域普通技术人员已知的方法进行测定,包括基于pcr的测定,例如定量pcr、竞争性pcr。通过确定(例如,在从受试者获得的样品中)遗传因子的存在,可确认诊断,和/或可将受试者分类为处于发展肾损伤和/或与肾损伤相关的障碍、疾病或病症的风险中,并且/或者可将受试者鉴定为适于用能够抑制il
‑
11介导的信号传导的药剂进行治疗。
[0456]
一些方法可包括确定与il
‑
11分泌相关或与对肾损伤和/或与肾损伤相关的障碍、疾病或病症的发展的易感性相关的一个或多个snp的存在。snp通常是双等位基因的,因此可使用本领域技术人员已知的许多常规测定中的一种测定容易地确定(例如,参见anthony j.brookes.snp的本质.gene,第234卷,第2期,1999年7月8日,第177
‑
186页;fan等人,“高度平行的snp基因分型”,cold spring harb symp quant biol 2003.68:69
‑
78;matsuzaki等人,“在高密度寡核苷酸阵列上使用单引物分析对10000多个snp进行平行基因分型”,genome res.2004.14:414
‑
425)。
[0457]
方法可包括确定在从受试者获得的样品中存在哪个snp等位基因。在一些实施方案中,确定次要等位基因的存在可能与增加的il
‑
11分泌或对肾损伤和/或与肾损伤相关的障碍、疾病或病症的发展的易感性相关。
[0458]
因此,在本发明的一个方面,提供了一种用于筛选受试者的方法,该方法包括:
[0459]
获取受试者的核酸样品;
[0460]
确定哪个等位基因存在于样品中的在wo 2017/103108 a1(以引用方式并入本文)的图33、图34或图35中列出的一个或多个snp或与r2≥0.8的所列snp之一连锁不平衡的snp的多态性核苷酸位置处。
[0461]
确定步骤可包括确定次要等位基因是否存在于样品中的所选多态性核苷酸位置处。它可包括确定是否存在0、1或2个次要等位基因。
[0462]
筛选方法可以是用于确定受试者对肾损伤和/或与肾损伤相关的障碍、疾病或病症的发展的易感性的方法或如本文所述的诊断或预后的方法,或形成该方法的一部分。
[0463]
该方法可进一步包括将受试者鉴定为对发展肾损伤和/或与肾损伤相关的障碍、疾病或病症具有易感性或增加的风险的步骤,例如,如果确定受试者在多态性核苷酸位置具有次要等位基因。该方法可进一步包括选择受试者用于用能够抑制il
‑
11介导的信号传
导的药剂进行治疗和/或向受试者施用能够抑制il
‑
11介导的信号传导的药剂,以便提供对受试者的肾损伤和/或与肾损伤相关的障碍、疾病或病症的治疗,或预防受试者的肾损伤和/或与肾损伤相关的障碍、疾病或病症的发展或进展的步骤。
[0464]
在一些实施方案中,诊断肾损伤和/或与肾损伤相关的障碍、疾病或病症从而鉴定处于发展肾损伤和/或与肾损伤相关的障碍、疾病或病症的风险的受试者的方法,以及预后或预测受试者对用能够抑制il
‑
11介导的信号传导的药剂治疗的反应的方法,采用不检测il
‑
11或il
‑
11受体或遗传因子的表达上调的指标。
[0465]
在一些实施方案中,诊断肾损伤和/或与肾损伤相关的障碍、疾病或病症从而鉴定处于发展肾损伤和/或与肾损伤相关的障碍、疾病或病症的风险的受试者的方法,以及预后或预测受试者对用能够抑制il
‑
11介导的信号传导的药剂治疗的反应的方法,基于检测、测量和/或鉴定以下一项或多项指标或进行以下分析之一:
[0466]
·
血清肌酸酐、血尿素和/或氮升高
[0467]
·
尿钠和肌酸酐水平
[0468]
·
尿排出量减少
[0469]
·
肾超声检查以确定肾小管阻塞的存在/不存在
[0470]
·
肾活检
[0471]
·
进行尿分析。
[0472]
实验室肾测试的参考水平可见于例如,rahman等人,同上,该文献全文据此以引用方式并入。
[0473]
诊断或预后的方法可在体外对从受试者获得的样品进行,或者在处理从受试者获得的样品之后进行。一旦收集了样品,就不需要患者在场来进行体外诊断或预后方法,因此该方法可以是不在人或动物身体上实施的方法。从受试者获得的样品可以是如上文所述的任何种类。
[0474]
其他诊断或预后测试可与本文所述的那些测试联合使用,以提高诊断或预后的准确性或证实通过使用本文所述的测试获得的结果。
[0475]
受试者
[0476]
受试者可以是动物或人。受试者优选地是哺乳动物,更优选地是人。受试者可以是非人哺乳动物,但更优选地是人。受试者可以是男性或女性。受试者可以是患者。患者可患有如本文所述的肾损伤和/或与肾损伤相关的障碍、疾病或病症。受试者可能已被诊断为患有需要治疗的肾损伤和/或与肾损伤相关的障碍、疾病或病症,可能被怀疑患有此类肾损伤和/或与肾损伤相关的障碍、疾病或病症,或者可能处于发展肾损伤和/或与肾损伤相关的障碍、疾病或病症的风险中。
[0477]
在根据本发明的实施方案中,受试者优选地是人受试者。在根据本发明的实施方案中,可根据基于肾损伤和/或与肾损伤相关的障碍、疾病或病症的某些标志的表征的方法选择受试者用于治疗。
[0478]
在一些实施方案中,受试者可以是正被施用药物或药品以治疗在肾组织中可能表现出或可能不表现出的疾病、病症或障碍的受试者。作为这种治疗的结果,例如副作用,受试者可能已经发展了药物诱导的肾损伤。受试者可基于已经发展出这种药物诱导的肾损伤而被选择用于根据本发明的治疗或预防性疗法。
[0479]
在一些实施方案中,受试者可能已经接受了采用化疗剂的治疗,或者可能正在接受采用化疗剂的治疗。受试者可能患有癌症、怀疑患有癌症、或正从癌症恢复或缓解,并且化疗剂的施用可构成受试者治疗的一部分。因此,受试者可以是患有化疗剂诱导的肾损伤、化疗剂诱导的急性肾损伤或化疗剂诱导的肾毒性的受试者。
[0480]
在一些实施方案中,受试者可能已经接受了采用顺铂的治疗,或者可能正在接受采用顺铂的治疗。受试者可能患有癌症、怀疑患有癌症、或正从癌症恢复或缓解,并且顺铂的施用可构成受试者治疗的一部分。因此,受试者可以是患有顺铂诱导的肾损伤、顺铂诱导的急性肾损伤或顺铂诱导的肾毒性的受试者。
[0481]
受试者可任选地接受间歇性或定期透析。
[0482]
序列同一性
[0483]
为了确定两个或更多个氨基酸或核酸序列之间的同一性百分比,成对和多序列比对可以本领域技术人员已知的多种方式实现,例如,使用公开可用的计算机软件,诸如clustalomega(j.2005,bioinformatics 21,951
‑
960)、t
‑
coffee(notredame等人,2000,j.mol.biol.(2000)302,205
‑
217)、kal ign(lassmann和sonnhammer,2005,bmc bioinformatics,6(298))和mafft(katoh和standley,2013,molecular biology and evolution,30(4)772
–
780)软件。当使用此类软件时,优选使用默认参数,例如用于空位罚分和扩展罚分。
[0484]
序列
[0485]
[0486]
[0487]
[0488][0489]
***
[0490]
本发明包括所描述的方面和优选特征的组合,除非这种组合是明显不允许的或明确避免的。
[0491]
在前面的描述中、或者在下面的权利要求中、或者在附图中公开,并且以其特定形
式或根据用于执行所公开功能的手段、或用于获得所公开结果的方法或过程来表达的特征,可视情况单独地或以这些特征的任意组合用于以其不同形式实现本发明。
[0492]
为了避免任何疑问,本文提供的任何理论解释都是为了提高读者的理解。本发明人不希望受这些理论解释中的任一者的束缚。
[0493]
本文所用的任何章节标题仅用于组织目的,并且不应被解释为限制所描述的主题。
[0494]
贯穿本说明书,包括随后的权利要求书,除非上下文另有要求,否则词语“包括”及其变型形式诸如“包含”和“含有”将被理解为暗示包括所陈述的整数或步骤或者整数或步骤的组,但不排除任何其他整数或步骤或者整数或步骤的组。
[0495]
应该注意的是,除非上下文清楚地指明,否则说明书和所附权利要求中所用的单数形式“一个”、“一种”和“所述”包括复数指代物。范围可在本文中表示为从“约”一个特定值和/或至“约”另一个特定值。当表示这样的范围时,另一个实施方案包括从一个特定值和/或至另一个特定值。类似地,当通过使用先行词“约”将值表示为近似值时,应当理解,特定值形成另一个实施方案。与数值相关的术语“约”是可选的,并且是指例如 /
‑
10%。
[0496]
可在体外、离体或体内执行本文公开的方法,或者产品可在体外、离体或体内存在。术语“体外”旨在包括在实验室条件下或在培养物中用材料、生物物质、细胞和/或组织进行的实验,而术语“体内”旨在包括用完整的多细胞生物体进行的实验和程序。“离体”是指在生物体外部存在或发生的事物,例如在人或动物体外,其可在取自生物体的组织(例如,整个器官)或细胞上。
[0497]
当本文公开了核酸序列时,也明确考虑了其反向互补序列。
[0498]
有关标准分子生物学技术,参见sambrook,j.,russel,d.w.《分子克隆,实验室手册》,第3版.2001,纽约冷泉港:冷泉港实验室出版社。
[0499]
现在将参照附图讨论本发明的方面和实施方案。其他方面和实施方案对于本领域的技术人员将显而易见。本文中提及的所有文件均以引用方式并入本文。虽然已经结合下面描述的示例性实施方案描述了本发明,但是当给出本公开时,许多等同的修改和变型对于本领域技术人员将是显而易见的。因此,上述本发明的示例性实施方案被认为是说明性的而非限制性的。在不脱离本发明的实质和范围的情况下,可对所描述的实施方案进行各种改变。
附图说明
[0500]
现在将参照附图讨论说明本发明原理的实施方案和实验。
[0501]
图1.显示中和抗il
‑
11抗体与igg对照抗体相比防止aki进展为ckd的显微照片。小鼠经受叶酸诱导的肾损伤(急性肾小管坏死(atn)和继发性纤维化的模型)并被施用igg对照、enx203(抗il
‑
11抗体)或enx209(抗il
‑
11ra抗体)。28天后收获肾并用于masson三色染色。两种抗体在防止胶原沉积方面都非常有效。
[0502]
图2a和图2b.显示中和抗il
‑
11抗体防止aki进展的图表。小鼠经受叶酸诱导的肾损伤,并被施用igg对照或抗il
‑
11抗体(enx203,ab1)或抗il
‑
11ra抗体(enx209,ab2)。在第28天,收集肾用于hpa胶原测定,并评估血清尿液(收集在代谢笼中)的尿白蛋白/肌酸酐比率。注意,第2天肾损伤标志在显示相同水平的初始肾损伤的处理组之间是相似的,但是接
受抗il
‑
11处理的小鼠基本上恢复了功能,而接受igg的小鼠功能恢复不太有效。(2a)显示肾胶原含量,而(2b)显示经受不同处理的小鼠在第28天的尿白蛋白/肌酸酐比率。
[0503]
图3.显示enx203和enx209对肾损伤反应和erk激活的剂量依赖性效果的图和图像。动物用叶酸处理,并在损伤前一小时注射抗体。28天后评估肾胶原含量。每两周用10mg/kg或20mg/kg的igg对照抗体处理动物。未观察到组间差异,将两组动物一起作图。叶酸的肾损伤模型非常严重(参见图4)。然而,即使在强化学刺激的情况下,每周两次剂量低至5mg/kg的enx203也是高度有效的(上图)。单独点表示生物学重复。数据显示为平均值
±
sd。抗体的每两周一次(biw.)和每三周一次(triw.)注射。监测纤维化肾中il
‑
11介导的erk激活作为靶标参与的读数(下图),本发明人能够证明每周两次1mg/kg的exn203的效果。
[0504]
图4a至图4c.显示enx203和enx209对(4a)血清肌酸酐水平、(4b)血清尿素水平和(4c)血清tgfb1水平的剂量依赖性效果的图。动物用叶酸处理,并在损伤前一小时注射抗体。28天后评估血清标记水平。每两周用10mg/kg或20mg/kg的igg对照抗体处理动物。未观察到组间差异,将两组动物一起作图。单独点表示生物学重复。数据显示为平均值
±
sd。抗体的每两周一次(biw.)和每三周一次(triw.)注射。
[0505]
图5a至图5c.显示用(5a)enx108a(igg1)、(5b)enx203或(5c)enx209处理对aki进展的效果的图。小鼠用叶酸处理,并且从1天前起也用给定浓度的抗体处理(每两周一次)。在肾损伤后21天测定肾胶原含量。数据点表示单个动物,所有数据是并行生成的,因此单个抗体可相互比较。对每种抗体绘制相同的基线和igg对照动物以便于数据解释。数据是平均值
±
sd;点表示每组动物。双尾dunnett检验,经校正的p值。
[0506]
图6a和图6b.显示成纤维细胞特异性敲除il11ra的小鼠被保护免受aki的图。在用叶酸处理肾损伤之前,用他莫昔芬处理动物以从col1a1 ve细胞中缺失il11ra1。21天后,用hpa测定评估(6a)胶原含量,并通过血清尿素水平确定(6b)肾功能。动物被保护达到与抗体处理期间相似的水平,表明il
‑
11活性在肾损伤和功能障碍的发病机制中对成纤维细胞的重要作用。sidak校正后的p值。
[0507]
图7a至图7f.涉及从aki后第3天起抗il
‑
11治疗效果的示意图、图和图像。(7a)叶酸施用和抗体处理的时间安排的示意图。(7b)接受抗il
‑
11治疗的小鼠在接受抗il
‑
11治疗后不久体重增加。(7c)在研究期结束时,与接受igg的小鼠相比,接受抗il
‑
11治疗的小鼠具有更高的肾重量、(7d)更少的肾胶原、(7e)正常的尿排出量和(7f)改善的总体形态。
[0508]
图8a至图8f.显示enx203处理逆转肾损伤和功能障碍并诱导肾再生的示意图、图和图像。(8a)叶酸施用和抗体处理的时间安排的示意图。确定了叶酸的肾损伤模型,并且动物在损伤后21天才处理。这导致肾功能严重降低和胶原含量增加。然后开始抗体处理,在处理的第3、6、9和12周后通过评价血清尿素水平和胶原含量进行肾功能分析。这表明,与第21天处理前的动物相比,经enx203处理的动物的(8b)胶原含量显著降低,并且(8c)肾功能改善。虽然肾含有较少的胶原,但是它们仍然(8d)体重增加,并且(8e)、(8f)看起来不那么凹凸不平且具有更健康的组织结构(肾的横截面,3只动物)。p值经多重检验进行校正,并且表明fa 21d组(dunnett检验)的稍后时间点之间的差异。数据显示为平均值
±
sd。
[0509]
图9.显示enx203处理降低了胶原含量并促进了正常肾实质和皮质体积的恢复的图像。对来自叶酸(fa)损伤后第21天(d21)的小鼠或对照小鼠的肾中段的masson三色染色,以及fa损伤后d21小鼠随后用igg或抗il
‑
11处理3、6、9或12周的小鼠肾中段的masson三色
染色。
[0510]
图10.显示来自图9中所示图像的肾皮质的更高放大率的图像。对来自叶酸(fa)损伤后第21天(d21)的小鼠或对照小鼠的肾皮质的masson三色染色,以及fa损伤后d21小鼠随后用igg或抗il
‑
11处理3、6、9或12周的小鼠肾皮质的masson三色染色。
[0511]
图11a和图11b.显示在确定的肾损伤后enx203处理会导致体重增加并导致尿acr逆转50%的图。建立叶酸的肾损伤模型,并且动物在损伤后21天才处理。然后开始抗体处理,并持续评估动物重量。(11a)enx203处理的动物一旦开始处理就开始恢复体重。(11b)与损伤后3周的起始水平相比,经12周的治疗后尿白蛋白:肌酸酐比率逆转了约50%。
[0512]
图12a和图12b.显示肾小管上皮细胞的tgfb1驱动的部分上皮
‑
间充质转化为il
‑
11依赖性的图。用tgfb1、il
‑
11(5ng/ml,24h)或tgfb1和抗体(2μg/ml,24h)刺激人原代肾小管上皮细胞。在operetta高内涵成像平台上监测(12a)acta2
ve
细胞和(12b)胶原表达的百分比。
[0513]
图13.涉及肾小管上皮细胞的tgfb1驱动的部分上皮
‑
间充质转化的图像。上图,用il
‑
11(2.5
‑
20ng/ml,24小时)刺激人原代肾小管上皮细胞。operetta高内涵成像用于使用若丹明
‑
鬼笔环肽来呈现肌动蛋白应力纤维形成。下图,细胞中胶原表达的可视化表示。
[0514]
图14a和图14b.显示通过肾小管上皮细胞(tec)表达至关重要的snail因子为il
‑
11依赖性的图象和图。在igg或抗il
‑
11抗体(enx203)存在时用il
‑
11或tgfb刺激原代人tec,并使用operetta成像平台检测snail或acta2基因的表达。(14a)il
‑
11和tgfb均诱导部分emt以及acta2和snail二者的表达。在抗il
‑
11抗体存在时,这种效果在tgfb刺激的细胞中被强烈抑制。(14b)根据图14a的显微照片定量acta ve细胞。
[0515]
图15.显示抗il
‑
11抗体处理阻止了在原代人tec中诱导snail的图像。用tgfb在抗il
‑
11抗体(enx203)存在或不存在时处理或用il
‑
11处理的原代人肾小管上皮细胞的蛋白质印迹。上图,tgfb(5ng/ml)对emt的主要调控基因snail的诱导依赖于il
‑
11信号传导,而单独的il
‑
11(5ng/ml)能够诱导snail表达。下图,通过gapdh对照蛋白证实的相等蛋白负荷。
[0516]
图16.显示再生肾中e
‑
钙粘蛋白的表达随着抗il
‑
11治疗而增加的图像。e
‑
钙粘蛋白表达是上皮细胞身份的典型标志,当细胞经历emt或部分emt时,e
‑
钙粘蛋白的表达会丢失。与il
‑
11驱动tec进入部分emt(pemt)的效果一致,叶酸损伤后d21小鼠和损伤后用igg处理12周的小鼠的肾的蛋白质印迹与对照相比具有较低的e
‑
钙粘蛋白水平,并且用抗il
‑
11处理逆转了这种效果。
[0517]
图17a和图17b.涉及在单侧输尿管梗阻(uuo)的肾损伤模型中抗il
‑
11抗体处理效果的图和条形图。进行uuo以诱导小鼠的物理肾损伤反应。一些动物在处理的第4、7和9天用enx203或igg对照抗体(20mg/kg)处理。(17a)enx203和igg对照处理动物的体重。(17b)手术后10天,使用hpa测定评估肾中的胶原含量。与用对照抗体处理的动物相比,用enx203治疗性抗体处理的动物具有显著降低的胶原含量。数据显示为平均值
±
sd。sidak校正后的p值。
[0518]
图18a至图18h.涉及在顺铂诱导的肾损伤模型中抗il
‑
11抗体处理效果的示意图和图。(18a)给小鼠施用顺铂(7mg/kg顺铂),每周一次,持续4周。对照组施用盐水。从第1周开始,每两周一次通过ip注射给小鼠施用10mg/kg x203或同种型匹配的igg对照抗体。8周后收获小鼠用于肾分析。(18b)通过hpa测定评估肾中的胶原含量。(18c至18h)如通过qpcr
确定的(18c)col3、(18d)纤连蛋白、(18e)mmp2、(18f)timp、(18g)ccl5和(18h)ccl2的rna表达。图显示相对于经盐水处理的小鼠中的表达,表达的倍数变化(fc)。
[0519]
实施例
[0520]
在以下实施例中,本发明人证实,在急性和慢性肾病模型中,抗il
‑
11治疗可通过广泛再生和逆转肾损害来改善肾损伤。
[0521]
实施例1:材料和方法
[0522]
1.1原代人肾近端小管上皮细胞
[0523]
培养和刺激条件
[0524]
1.将原代人肾近端小管上皮细胞(hrptec,pcs
‑
400
‑
010,atcc)在完全肾上皮细胞生长培养基(pcs
‑
400
‑
030和pcs
‑
400
‑
040,atcc)中于37℃和5%co2下生长和维持。hrptec培养基每2
‑
3天更新一次,细胞用标准胰蛋白酶消化技术以80%融合率传代。所有实验均在p3进行,在无血清肾上皮细胞培养基中进行相应刺激(24小时)之前,将细胞血清饥饿16小时。将经刺激的细胞与在相同条件(无血清肾上皮细胞培养基)下生长相同持续时间但没有刺激的未刺激细胞进行比较。
[0525]
operetta表型测定
[0526]
2.将hrptec以1
×
104细胞/孔的密度接种在96孔cellcarrier板(600550,perkinelmer)中。用指示浓度的il
‑
11(genscript)或tgf
‑
β1(phc 143b,bio
‑
rad)在存在和不存在2μg/ml抗il
‑
11(enx203)或igg同种型对照抗体的情况下刺激细胞24小时。在实验条件下,将细胞固定在4%多聚甲醛(pfa,28908,thermo fisher scientific)中,在pbs中用0.1%triton x
‑
100(t8787,sigma)透化。在pbs中用0.5%bsa(a7906,sigma)和0.1%tween
‑
20(170
‑
6531,bio
‑
rad)封闭非特异性结合位点。将细胞与一抗(1:500)(即,acta2(ab7817,abcam))、胶原i(34710,abcam)、snail(ab180714,abcam)一起孵育过夜(4c),然后与合适的alexafluor488偶联的二抗(山羊抗小鼠488,ab150113;和山羊抗兔488,ab150077,abcam)一起孵育1小时(1:1000,室温,黑暗)。将细胞在封闭液中用罗丹明
‑
鬼笔环肽(r415,thermo fisher scientific)和dapi(1μg/ml,d1306,thermo fisher scientific)复染。用operetta高内涵成像系统(1483,perkinelmer)扫描板并收集图像。从至少两个孔和每孔最少七个视野测定每种条件。使用harmony软件3.5.2版进行acta2 细胞的定量。用columbus 2.7.1版进行单位面积的胶原i荧光强度的测量。
[0527]
1.2蛋白质印迹
[0528]
3.对hrpte总蛋白提取物进行蛋白质印迹。将hrpte在含有蛋白酶和磷酸酶抑制剂(thermo scientifics)的放射免疫沉淀测定(ripa)缓冲液中裂解,然后离心以清除裂解物。通过bradford测定(bio
‑
rad)确定蛋白质浓度。通过sds
‑
page分离等量的蛋白质裂解物,将其转移至pvdf膜,并进行snail(3879,cst)和gapdh(2118,cst)的免疫印迹分析。使用ecl检测系统(pierce)和抗兔hrp(7074,cst)使蛋白可视化。
[0529]
1.3动物模型
[0530]
4.所有动物程序均根据singhealth机构动物护理和使用委员会(iacuc)获得批准并实施。所有小鼠均随意获得食物和水。
[0531]
化学诱导的小鼠急性肾损伤模型
[0532]
5.通过向10周龄雄性小鼠ip注射溶于溶媒(0.3m nahco3)的叶酸(200mg/kg)来诱
导肾损伤;对照小鼠仅被施用溶媒。fa后28天处死动物。给小鼠腹膜内注射抗il
‑
11抗体(enx203)、抗il
‑
11rα抗体(enx209)或相同浓度的igg同种型对照。图中概述了抗体疗法的处理持续时间和剂量。
[0533]
手术诱导的小鼠急性肾损伤模型
[0534]
6.对12周龄雄性小鼠进行单侧输尿管梗阻(uuo)手术。简而言之,小鼠通过ip注射氯胺酮(100mg/kg)/甲苯噻嗪(10mg/kg)被麻醉,并通过足底反射被确认进入全深度麻醉。然后在小鼠腹部左侧剃毛。用手术刀穿过皮肤作垂直切口,穿过腹膜作第二切口,露出肾。使用镊子,将肾置于表面,并在肾下方用手术丝将输尿管打结两次。将结扎的肾轻轻地放回到其正确的解剖位置,并加入无菌盐水以补充流失的液体。然后缝合切口。动物术后连续三天用抗生素恩诺沙星(15mg/kg,sc)和镇痛剂丁丙诺啡(0.1mg/kg,sc)处理。
[0535]
1.4比色测定和elisa
[0536]
7.使用尿素测定试剂盒(ab83362,abcam)测量小鼠血清中的血尿素氮(bun)水平。分别使用小鼠白蛋白elisa试剂盒(ab108792,abcam)和肌酸酐测定试剂盒(ab204537,abcam)测量尿白蛋白和肌酸酐水平。通过elisa测量血清tgfβ1水平。所有elisa和比色测定均根据制造商的方案进行。
[0537]
1.5组织学
[0538]
8.将肾组织在10%中性缓冲福尔马林(nbf)中于室温下固定48小时,脱水,包埋在石蜡块中,并以4μm切片。然后根据标准方案用masson三色法染色切片,并通过光学显微镜检查。
[0539]
实施例2:化学诱导的肾损伤模型中il
‑
11介导的信号传导的抑制效果的分析
[0540]
通过腹膜内(i.p.)注射溶于溶媒(0.3m nahco3)的叶酸(180mgkg
‑1)在10
‑
12周龄体重相似的同窝小鼠中化学诱导肾损伤;对照小鼠仅被施用溶媒。
[0541]
enx203(能够与小鼠il
‑
11(和人il
‑
11)结合并抑制il
‑
11介导的信号传导的抗体)或enx209(能够与小鼠il
‑
11(和人il
‑
11)结合并抑制il
‑
11介导的信号传导的抗体)在叶酸处理后一天施用,然后以20mg/kg的剂量每周施用3次。注射后28天对小鼠实施安乐死。
[0542]
enx203和enx209是il
‑
11介导的信号传导的拮抗剂。enx203是小鼠抗小鼠il
‑
11igg,并且描述于例如ng等人,sci transl med.(2019)11(511)pii:eaaw1237(也公开为ng等人,“il
‑
11是特发性肺纤维化的治疗靶点”,biorxiv336537;doi:https://doi.org/10.1101/336537)。enx203也称为“x203”。enx203包含根据wo 2019/238882 a1的seq id no:92的vh区(本公开的seq id no:22)和根据wo 2019/238882 a1的seq id no:94的vl区(本公开的seq id no:23)。enx209为小鼠抗小鼠il
‑
11rαigg,并且描述于例如widjaja等人,gastroenterology(2019)157(3):777
‑
792(也发表为widjaja等人,“il
‑
11中和疗法针对nash中肝星状细胞诱导的肝脏炎症和纤维化”,biorxiv 470062;doi:https://doi.org/10.1101/470062)。enx209也称为“x209”。enx209包含根据wo 2019/238884 a1的seq id no:7的vh区(本公开的seq id no:24)和根据wo 2019/238884 a1的seq id no:14的vl区(本公开的seq id no:25)。
[0543]
根据制造商的说明书,分别使用尿素测定试剂盒(ab83362,abcam)和肌酸酐测定试剂盒(ab65340,abcam)定量小鼠的尿素和肌酸酐的血浆水平。使用quickzyme总胶原测定试剂盒(quickzyme biosciences)基于羟脯氨酸的比色检测定量肾中总胶原的量。所有比
色测定均根据制造商的说明书进行。
[0544]
将组织石蜡包埋,并且将肾以3μm切片。对于石蜡切片,将组织在室温下在10%中性缓冲福尔马林(sigma
‑
aldrich)中固定24小时,脱水并包埋在石蜡中。对于冷冻切片,用tissue
‑
tek最佳切割温度化合物(vwr international)包埋新鲜解剖的器官。然后将冷冻模具冷冻在金属烧杯中,异戊烷在液氮中冷却,切片储存在
‑
80℃下。根据制造商的说明书,用masson三色染色试剂盒(ht15,sigma
‑
aldrich)将总胶原染色。用imagej软件(1.49版)捕获切片的图像并半定量确定蓝色染色区域。对于免疫组织化学法,将组织切片与抗acta2抗体(ab5694,abcam)一起温育。使用immpress hrp抗兔igg聚合物检测试剂盒(vector laboratories)以immpact dab过氧化物酶底物(vector laboratories)作为色原,使一抗染色可视化。然后用mayer苏木精(merck)复染切片。
[0545]
图1和图2显示,发现用抗il11抗体或抗il
‑
11rα抗体拮抗剂处理的小鼠具有显著减少的胶原染色。
[0546]
图2还显示,用抗il
‑
11抗体或抗il
‑
11rα抗体处理后,尿白蛋白/肌酸比率显著降低,表明肾损害水平降低。
[0547]
重要的是,化学诱导肾损害后第2天的尿素和肌酸的血清水平在处理组之间相似(数据未显示),然而接受拮抗剂il
‑
11处理的小鼠基本上恢复了功能,而接受igg的小鼠功能恢复不太有效。
[0548]
在单独的实验中,使用类似的叶酸诱导的肾损伤模型来评价il
‑
11介导的信号传导的拮抗剂治疗/预防肾损伤的治疗功效。如上所述,小鼠用叶酸处理,并在损伤前一小时施用抗体。28天后评估肾胶原含量。给动物每两周一次施用1mg/kg enx203、每两周一次5mg/kg enx203、每三周一次5mg/kg enx203、每两周一次10mg/kg enx203、每三周一次10mg/kg enx203、每三周一次20mg/kg enx203、每两周一次20mg/kg enx209,或者每两周一次10mg/kg或20mg/kg igg对照抗体。
[0549]
图3显示,用il
‑
11介导的信号传导的抗体拮抗剂处理以剂量依赖性方式降低了与叶酸诱导的肾损伤相关的胶原含量水平。甚至当enx203以5mg/kg每两周一次施用时,也观察到对胶原水平的影响。
[0550]
监测纤维化肾中il
‑
11介导的erk激活作为靶标参与的读数,本发明人证实了每周两次施用1mg/kg剂量的exn203的效果。
[0551]
在这些实验中还评价了肌酸、尿素和tgfβ1的血清水平,并且图4显示,用il
‑
11介导的信号传导的抗体拮抗剂处理以剂量依赖性方式降低了肾损伤的这些相关物的血清水平。同样,甚至当每两周一次施用5mg/kg enx203时也观察到血清中这些因子水平的降低。
[0552]
在进一步的实验中,使用类似的叶酸诱导的肾损伤模型来评价il
‑
11介导的信号传导的拮抗剂治疗/预防肾损伤的治疗功效。如上所述,小鼠用叶酸处理,并在损伤前一天施用抗体。21天后评估肾胶原含量。给动物每两周一次施用10mg/kg igg对照抗体,或者0.5mg/kg、1mg/kg、5mg/kg或10mg/kg的enx203、enx209或enx108a。结果示于图5中。
[0553]
enx108a是人抗人il
‑
11igg,能够与小鼠il
‑
11和人il
‑
11结合,并抑制il
‑
11介导的信号传导。enx108a描述于wo 2019/238882 a1中,并且包含根据wo 2019/238882a1的seq id no:8的vh区(本公开的seq id no:26)和根据wo2019/238882a1的seq id no:20的vl区(本公开的seq id no:27)。在本实施例中,enx108a以higg4(l248e、s241p)、λ轻链形式提供
(即,由具有seq id no:28所示氨基酸序列的重链和具有seq id no:29所示氨基酸序列的轻链形成)。
[0554]
在进一步的实验中,本发明人研究了il11ra1敲除在该急性化学诱导的肾损伤模型中的后果。响应于他莫昔芬而显示成纤维细胞特异性敲除il11ra1的cre
‑
lox小鼠用他莫昔芬处理以从col1a2阳性细胞中缺失il
‑
11ra1,随后如上所述经受叶酸诱导的肾损伤(或用溶媒处理)。21天后,用hpa测定评估胶原含量,并通过分析血清尿素水平确定肾功能。结果示于图6中。发现成纤维细胞中的il11ra1敲除保护小鼠免受叶酸诱导的肾损伤,这表明成纤维细胞中il
‑
11介导的传导在肾损伤和随之而来的功能障碍和继发性纤维化的病理中起重要作用。
[0555]
在另一个实验中,如上所述用叶酸处理小鼠,并且从第3天起每两周一次施用10mg/kg enx203。28天后评价体重、肾重量、肾胶原含量、尿排出量和总体肾形态。结果示于图7中。在研究结束时,与接受igg对照的小鼠相比,接受抗il
‑
11抗体治疗的小鼠具有增加的肾重量、更少的肾胶原、正常的尿排出量和改善的总体形态。
[0556]
本发明人在化学诱导的慢性肾损伤模型中进行了进一步的实验。简而言之,通过如上所述的叶酸处理在小鼠中诱导肾损伤,并且不处理21天。在通过叶酸处理诱导急性肾损伤后21天,已经形成慢性肾病,这通过血尿素氮增加约2.5倍(图8b)和尿中白蛋白与肌酸比率(acr)增加约2.9倍(图11,下图)来确定。肾已经损失了其初始质量的约33%(图8c),并且胶原水平升高约2.8倍(图8a)。
[0557]
从第21天起,用10mg/kg的enx203或igg对照每两周一次处理小鼠。在实验的指定日对小鼠实施安乐死,并评价肾胶原、血清尿素水平、肾重量和总体肾形态。结果示于图8中。用enx203处理与肾胶原水平降低(图8a)和血清尿素水平降低相关,到处理的第12周bun总体逆转51%(与igg的p<0.001;图8b)。
[0558]
重要的是,在经enx203处理的动物中肾重量随时间增加,而在经enx203处理的动物中肾胶原含量降低(图8c和8a)且血清尿素水平随时间降低(图8b)。这些结果表明,enx203处理不仅能抑制叶酸诱导的肾组织损伤反应,还能促进功能性肾组织的再生,逆转损伤表型。在第84天和第105天收获的经enx203处理的小鼠的肾也更接近健康的肾(图8d和图8e)。
[0559]
对来自小鼠的肾切片的组织学分析表明,enx203处理恢复了经受叶酸诱导的肾损伤的小鼠肾的正常肾实质(到第12周实质损失逆转54%(p<0.001))、皮质厚度和体积以及皮质形态(图9和图10)。
[0560]
在整个实验过程中还监测了该实验中小鼠的体重,并且发现enx203处理与经叶酸处理的小鼠体重向对照、未处理时水平的增加相关(图11,上图)。在实验的第21、84和105天,还监测了小鼠尿中的acr,结果如图11(下图)所示。发现用enx203处理导致经叶酸处理的小鼠中的尿acr显著降低(12周内降低约50%)。
[0561]
结果证实,il
‑
11介导的信号传导的拮抗可逆转肾纤维化并产生肾实质的广泛再生,这与肾损害的显著逆转相关。
[0562]
实施例3:研究il
‑
11介导的信号传导的拮抗剂抑制/逆转肾损伤的分子基础
[0563]
本发明人进行了进一步的研究以评价il
‑
11介导的信号传导在肾组织功能和损伤反应中的作用。
[0564]
肾小管上皮细胞向间充质细胞样表型的转化涉及对肾实质的损害和与肾损伤相关的功能障碍(参见,例如,lovisa等人,nat.med.(2015)21,998
–
1009),因此本发明人研究了il
‑
11介导的信号传导是否在tec的上皮
‑
间充质转化中起作用。
[0565]
用tgfb1、il
‑
11(5ng/ml,24h)或tgfb1 enx203(2μg/ml,24h)体外刺激人原代肾小管上皮细胞(tec),并使用operetta高内涵成像平台评价acta2
ve
细胞的百分比和胶原表达。
[0566]
结果示于图12中。发现tgfb1和il
‑
11均增加了表达acta2的tec的比例,并增加了这些细胞的胶原i表达。发现用enx203处理,tec响应于tgfb1/il
‑
11对acta2和胶原i的表达降低。
[0567]
在单独的实验中,用不同浓度的il
‑
11(2.5ng/ml、5ng/ml、10ng/ml)、tgfb1(5ng/ml)或tgfb1(5ng/ml) enx203(2μg/ml)刺激人原代tec 24小时,并且operetta高内涵成像用于使用若丹明
‑
鬼笔环肽(图13,上图)和胶原((图13,下图)来呈现肌动蛋白应力纤维形成。
[0568]
如上文所解释的,snail最近已表明是急性肾损伤后tec功能障碍的关键决定因素。它在tec中的表达与tec功能和增殖受损相关。对用不同浓度的il
‑
11(5ng/ml)、tgfb1(5ng/ml)、tgfb1(5ng/ml) enx203(2μg/ml)或tgfb1(5ng/ml) igg对照(2μg/ml)体外刺激24小时的人原代tec,使用operetta高内涵成像系统来分析acta2或snail的表达。
[0569]
结果示于图14中。发现用il
‑
11或tgfb1处理可诱导部分上皮细胞
‑
间充质细胞转化(emt),以及acta2和snail的表达。然而,enx203的存在强烈抑制acta2和snail的诱导。
[0570]
由细胞制备细胞裂解物,并通过蛋白质印迹分析snail表达。进行gapdh的单独蛋白质印迹作为蛋白质上样对照。结果示于图15中,证实snail的表达响应于tgfb1和il
‑
11而上调,并且tgfb介导的snail上调被enx203的存在完全阻止。
[0571]
因此发现tgfb1介导的snail诱导为il
‑
11依赖性的。
[0572]
本发明人通过对来自上述实验的小鼠肾组织的蛋白质裂解物的蛋白质印迹研究了上皮细胞身份的典型标记e
‑
钙粘蛋白的表达,其中通过如上所述的叶酸处理在小鼠中诱导肾损伤,随后从第21天开始每两周一次用10mg/kg的enx203或igg对照处理小鼠。
[0573]
结果示于图16中。发现叶酸诱导的肾损伤降低了e
‑
钙粘蛋白表达,同时发现用enx203处理恢复了e
‑
钙粘蛋白表达。
[0574]
实施例4:物理诱导的肾损伤模型中il
‑
11介导的信号传导的抑制效果的分析
[0575]
单侧输尿管梗阻(uuo)诱导小鼠急性肾损伤模型。简而言之,通过假手术或对一侧输尿管的输尿管梗阻来处理小鼠。
[0576]
小鼠在处理的第4、7和9天用enx203(在图17b中称为“3c6”)或igg对照抗体(20mg/kg)处理。在整个实验中监测小鼠的体重,并在uuo手术后10天使用hpa测定评估肾中的胶原含量。
[0577]
结果示于图17中。与经受uuo并用igg对照抗体处理的小鼠相比,用enx203处理的小鼠具有减少的肾胶原和增加的体重。
[0578]
实施例5:顺铂诱导的肾损伤模型中il
‑
11介导的信号传导的抑制效果的分析
[0579]
通过每周一次连续四周施用7mg/kg顺铂,在10周龄的c57bl/6j小鼠中诱导肾损伤。对照组不施用顺铂。
[0580]
从第1周开始,每两周一次通过ip注射给小鼠施用10mg/kg剂量的x203(能够与小鼠il
‑
11(和人il
‑
11)结合并抑制il
‑
11介导的信号传导的抗体)或同种型匹配的igg对照抗体,或盐水(对照)。8周后收获小鼠用于分析。
[0581]
使用quickzyme总胶原测定试剂盒(quickzyme biosciences)基于羟脯氨酸的比色检测定量肾中总胶原的量。结果示于图18b中。顺铂处理与肾中胶原含量的增加相关。来自施用中和抗il
‑
11抗体的经顺铂处理小鼠的肾的胶原含量低于来自施用igg对照抗体的经顺铂处理小鼠的肾。
[0582]
还通过qpcr分析了经受不同处理的小鼠的肾中col3、纤连蛋白、mmp2、timp、ccl5和ccl2的rna表达。
[0583]
简而言之,使用trizol(invitrogen)和rneasy微型试剂盒(qiagen)从速冻肾组织中提取总rna。使用iscript cdna合成试剂盒(biorad)进行pcr扩增。通过taqman(applied biosystems)或sybr green(qiagen)技术,使用steponeplus(applied biosystems)在40个循环内一式两份分析基因表达。将表达数据归一化为gapdh mrna表达,并计算相对于盐水处理的对照受试者中表达的倍数变化。
[0584]
结果示于图18c至图18h。顺铂处理与col3、纤连蛋白、mmp2、timp、ccl5和ccl2的表达增加相关。与来自施用igg对照抗体的经顺铂处理小鼠的肾相比,来自施用中和抗il
‑
11抗体的经顺铂处理小鼠的肾倾向于具有较低的col3、纤连蛋白、mmp2、timp、ccl5和ccl2表达。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。