1.本发明属于体外诊断领域,尤其是生物标志物在早期检测宫颈癌中的应用,具体地,所述生物标志物为krt1和scgb2a1。
背景技术:
2.宫颈癌(cervical cancer)是最常见的妇科恶性肿瘤。原位癌高发年龄为30~35岁,浸润癌为45~55岁,近年来其发病有年轻化的趋势。根据国家肿瘤中心公布的癌症统计数据,2015年我国的宫颈癌新发病例约为9.89万例,年死亡例数约为3.05万例,并且该数据呈逐年上升且发病年轻化的趋势(chen w,zheng r,baade p d,et al.cancer statistics in china 2015[j].ca cancer j clin,2016,66(2):115
‑
132)。宫颈癌的发生与多种因素密切相关,如早婚、早育、多产及性生活紊乱等,人乳头状瘤病毒(human papilloma virus,hpv)是绝大多数宫颈癌发生的病因,约99%的宫颈癌患者hpv筛查呈阳性,且hpv持续感染患者罹患宫颈癌的风险是hpv阴性者的250多倍。
[0003]
自明确hpv感染是宫颈癌发病的重要成因以来,研究学者们针对hpv感染诱发宫颈癌发病的机制展开了深入的研究,并开发出了针对宫颈癌的筛查诊断方法以及预防治疗策略,一定程度上改善了宫颈癌患者的生存和生活质量。目前临床上对于该病的诊断主要依靠巴氏涂片法、醋酸染色肉眼观察法(visual inspection with acetic acid,via)和碘染色肉眼观察法(visual inspection with lugol’s iodine,vili)、液基细胞学等方法,其中,采用巴氏涂片法造成的临床上假阴性者的受试者较多,敏感性只有43.1%;液基细胞学法虽是在巴氏涂片法的基础上进行了改进,但其阳性预测值仅为16%,且所述设备和检测耗材昂贵,不适用于推广应用;via和vili虽经济成本低廉、操作简单,但是受检测者主观因素的影响较大,容易造成误诊和漏诊。
[0004]
随着分子生物学技术的不断发展,涉及肿瘤发生的多种生物学过程中的多种分子,如核酸、蛋白质、糖类、脂类、小分子代谢物乃至血液中游离的肿瘤细胞,均可作为重要的肿瘤标志物,给临床预防、诊断和治疗提供明确的依据。虽然目前已经发现了一些宫颈癌相关的肿瘤标志物用于宫颈癌的临床预防中,但是这些已有的肿瘤标志物因在正常情况下组成性表达、或在非恶性肿瘤疾病中水平也升高,缺乏肿瘤特异性。因此,目前本领域仍亟待寻找肿瘤特异性抗原作为宫颈癌筛查的生物标志物用于临床宫颈癌的早期筛查诊断中,这也是最大限度地预防、降低宫颈癌发生的一条重要途径,从长远来看,对于维护全球女性的身心健康具有重要的意义。
技术实现要素:
[0005]
鉴于此,为了解决目前本领域存在的上述技术缺陷,本发明的目的是提供生物标志物在早期检测宫颈癌中的应用。
[0006]
为了实现本发明的上述目的,本发明采用了如下技术方案:
[0007]
第一方面,本发明提供了检测样本中生物标志物的试剂在制备诊断宫颈癌的产品
中的应用。
[0008]
进一步,所述生物标志物为krt1和scgb2a1。
[0009]
进一步,所述试剂选自:
[0010]
特异性扩增所述生物标志物的引物;或
[0011]
特异性识别所述生物标志物的探针。
[0012]
进一步,所述产品包括通过核酸杂交技术、核酸扩增技术、蛋白免疫技术、测序技术、色谱技术、质谱技术检测所述生物标志物的表达水平的试剂。
[0013]
进一步,所述核酸杂交技术是指互补的核苷酸序列(dna与dna、dna与rna、rna与rna等)通过watson
‑
crick碱基配对形成非共价键,从而形成稳定的同源或异源双链分子的过程,又称为核酸杂交。
[0014]
进一步,所述核酸扩增技术是指一大类技术方法的总称,目前核酸扩增技术包括常规pcr、实时荧光pcr、等温核酸扩增技术等,可将极微量的靶dna特异地扩增上百万倍,从而大大提高对dna分子的分析和检测能力,能检测单分子dna或对每10万个细胞中仅含1个靶dna分子的样品,具有敏感性高、特异性强、快速、简便等优点。
[0015]
进一步,所述蛋白免疫技术是指包括放射免疫测定、直接、间接或对比酶联免疫吸附测定、酶免疫测定、荧光免疫测定、蛋白质印迹法、免疫沉淀法、基于任何颗粒的免疫测定(例如:使用金颗粒、银颗粒或乳胶颗粒、磁性颗粒或量子点)对目标物进行检测的一类方法的统称,可在微量滴定板或条的形式中实施蛋白免疫法。
[0016]
进一步,所述测序技术包括(但不限于)一代测序、二代测序、三代测序,其中,一代测序也称sanger测序,是利用dna聚合酶合成反应的测序技术,一代测序是基于sanger方法的测序技术;二代测序基于大规模平行测序技术(massive parallel analysis,mps),它能同时完成测序模板互补链的合成和序列数据的获取;三代测序则基于单分子测序和大规模平行测序技术。
[0017]
进一步,所述色谱技术是指分离和分析复杂混合物中各个组分的方法,利用不同物质在由固定相和流动相构成的体系中具有不同的分配系数,当两相作相对运动时,这些物质随流动相一起运动,并在两相间进行反复多次的分配,从而使各物质达到分离。
[0018]
进一步,所述质谱技术是指利用电场和磁场将运动的离子(带电荷的原子、分子或分子碎片、有分子离子、同位素离子、碎片离子、重排离子、多电荷离子、亚稳离子、负离子和离子
‑
分子相互作用产生的离子)按它们的质荷比分离后进行检测的方法。测出离子准确质量即可确定离子的化合物组成。
[0019]
进一步,所述样本选自血液或组织。
[0020]
进一步,所述检测样本中的生物标志物是通过以下步骤进行的:
[0021]
(1)获取受试者的样本;
[0022]
(2)确定所述样本中生物标志物krt1和scgb2a1的表达水平。
[0023]
第二方面,本发明提供了一种早期诊断宫颈癌的产品。
[0024]
进一步,所述产品包括检测样本中生物标志物krt1和scgb2a1的试剂;
[0025]
优选地,所述产品包括芯片、试剂盒、试纸、高通量测序平台。
[0026]
进一步,所述检测样本中生物标志物krt1和scgb2a1的试剂包括检测样本中生物标志物krt1和scgb2a1 mrna表达水平的试剂、检测样本中生物标志物krt1和scgb2a1编码
的蛋白和/或多肽表达水平的试剂。
[0027]
进一步,所述检测样本中生物标志物krt1和scgb2a1 mrna表达水平的试剂包括特异性识别所述生物标志物的探针、特异性扩增所述生物标志物的引物。
[0028]
进一步,所述检测样本中生物标志物krt1和scgb2a1编码的蛋白和/或多肽表达水平的试剂包括特异性结合所述生物标志物的抗体、抗体片段、亲和性蛋白。
[0029]
进一步,所述试剂盒还包括使用说明书或标签、阳性对照物、阴性对照物、缓冲剂、助剂或溶剂。
[0030]
进一步,所述使用说明书或标签注明了所述试剂盒用于检测宫颈癌。
[0031]
进一步,所述芯片包括固相载体以及固定在固相载体的寡核苷酸探针。
[0032]
进一步,所述寡核苷酸探针包括用于检测所述生物标志物表达水平的针对所述生物标志物的寡核苷酸探针。
[0033]
本发明中所述的“引物”,是指包含5
‑
100个核苷酸的核酸片段,优选地,是指包含能起始酶促反应(例如,酶促扩增反应)的15
‑
30个核苷酸。
[0034]
本发明中所述的“探针”,是指包括至少5个核苷酸的核酸序列,例如,包含5
‑
100个核苷酸,其能在指定条件下与目标基因的表达产物或者该表达产物的扩增产物杂交形成复合物,杂交探针上还可以包括用于检测的标记物,所述标记物包括(但不限于)用于荧光定量pcr或荧光原位杂交的标记物。
[0035]
本发明中所述的引物或探针可以使用亚磷酰胺固相载体方法或其他公知的方法化学合成。这种核酸序列可以利用本领域中公知的多种手段来进行变形。这种变形的非限制性地包括甲基化、封装、天然核苷酸的一种以上的同源物的取代以及核苷酸之间的变形,例如,变形为不带电的连接体(诸如膦酸甲酯、磷酸三酯、氨基磷酸酯、氨基甲酸酯等)或带电的连接体(诸如硫代磷酸酯、二硫代磷酸酯等)。
[0036]
在本发明中,可通过优化步骤在一系列过程中确定使探针与cdna分子杂交的合适条件。该步骤由本领域普通技术人员通过一系列过程进行,以建立用于在实验室中使用的条件。例如,温度、成分浓度、杂交及洗涤时间、缓冲液成分及其ph以及离子强度等条件取决于探针的长度、gc量及靶核苷酸序列等各种因素。
[0037]
本发明中所述的“抗体”,是指针对抗原位点的特异性免疫球蛋白,本发明中的抗体是指与本发明中所述的生物标志物多肽和/或蛋白特异性结合的抗体,可以根据本领域中的常规方法来制造抗体,抗体的形式包括多克隆抗体或单克隆抗体、抗体片段(例如:fab、fab'、f(ab')2和fv片段)、单链fv(scfv)抗体、多特异性抗体(例如:双特异性抗体)、单特异性抗体、单价抗体、嵌合抗体、人源化抗体、人抗体、包含抗体的抗原结合位点的融合蛋白,以及包含抗原结合位点的任何其他修饰的免疫球蛋白分子,只要该抗体表现出所需的生物结合活性即可。
[0038]
本发明中所述的“多肽”,是指由氨基酸以肽键连接组成的化合物,包括多肽的全长或氨基酸片段,所述基因编码的多肽的表达水平,可以根据样本中总蛋白的量或管家基因所编码的多肽的量来标准化。
[0039]
本发明中所述的“表达水平”、“水平”,是指本发明中所述生物标志物的绝对量或相对量,可以通过多种技术确定本发明中所述生物标志物中任何一种的表达水平,特别地,可以通过使用本领域技术人员熟知的方法对本发明中所述生物标志物的绝对量或相对量
进行检测。
[0040]
本发明中所述的“样本”、“待测样本”,是指获自或衍生自目的个体(受试者)的生物试样,生物试样的供给源可以是新鲜、冷冻和/或保存的器官或组织样品或从活检或引物产生的固体组织;血液或任意血液组分。术语“样本”或“待测样本”包括在其获得后以任意方式操作过的生物样本,如通过试剂处理、稳定化、或针对某些成分(如蛋白质或多核苷酸)富集、或包埋在用于切片目的的半固体或固体基质中。在本发明的具体实施例中,将组织组分用作试样。
[0041]
本发明中所述的“生物标志物”,是指存在于或源自样品的任何可检测化合物,如蛋白质、肽、蛋白聚糖、糖蛋白、脂蛋白、碳水化合物、脂质、核酸(例如dna,诸如cdna或扩增的dna,或rna,诸如mrna)、有机或无机化学物质、天然或合成的聚合物、小分子(例如,代谢物)或上述任何物质的区分分子或区分片段。如这段内容中使用的“源自”是指检测时指示存在于样品中的特定分子的化合物。例如,特定cdna的检测可以指示样品中特定rna转录物的存在。作为另一个实例,特定抗体的检测或与特定抗体的结合可以指示样品中特定抗原(例如,蛋白质)的存在。在此,区分分子或片段是检测时指示以上鉴定的化合物的存在或丰度的分子或片段。生物标志物例如可以分离自样品、直接在样品中测量,或在样品中检测或测定。生物标志物可以例如是功能性的、部分功能性的或非功能性的。在本发明的具体实施例中,所述生物标志物为基因krt1和scgb2a1的联合。
[0042]
第三方面,本发明提供了一种早期诊断宫颈癌的系统。
[0043]
进一步,所述系统中包括用于输入生物标志物的表达水平的输入装置、用于输出宫颈癌诊断结果的输出装置,其中所述生物标志物为krt1和scgb2a1。
[0044]
进一步,所述系统中还包括计算装置,所述计算装置包括存储器和处理器;所述存储器中存储有计算机程序,所述处理器被配置为执行所述存储器中存储的计算机程序;
[0045]
优选地,所述系统中还包括生物标志物krt1和scgb2a1表达水平的检测装置;
[0046]
更优选地,所述检测装置包括实时定量pcr仪和实时定量pcr引物、高通量测序平台、检测芯片和芯片信号读取器;
[0047]
最优选地,所述实时定量pcr引物包括检测生物标志物表达水平的实时定量pcr引物;
[0048]
最优选地,所述实时定量pcr引物还包括内参引物,所述内参引物为检测gapdh或β
‑
actin的表达水平的实时定量pcr引物。
[0049]
最优选地,所述芯片包括检测生物标志物表达水平的探针;
[0050]
最优选地,所述芯片还包括内参探针,所述内参探针为检测gapdh或β
‑
actin的表达水平的探针。
[0051]
本发明中所述的生物标志物包括基因krt1和基因scgb2a1,以及其编码的蛋白及其同源物,突变,和同等型,所述生物标志物涵盖全长未加工的生物标志物,以及源自细胞中加工的任何形式的生物标志物,同时涵盖生物标志物的天然发生变体(例如剪接变体或等位变体)。gene id可在https://www.ncbi.nlm.nih.gov/gene/获得,本发明中所述的生物标志物的信息如下:
[0052]
基因krt1:全称为keratin 1,基因在染色体上的具体位置为12q13.13,gene id为3848;
[0053]
基因scgb2a1:全称为secretoglobin family 2a member 1,基因在染色体上的具体位置为11q12.3,gene id为4246。
附图说明
[0054]
以下,结合附图来详细说明本发明的实施方案,其中:
[0055]
图1显示基因krt1、基因scgb2a1在训练集中的差异表达的结果图,其中,a图:krt1,b图:scgb2a1;
[0056]
图2显示基因krt1、基因scgb2a1在验证集中的差异表达的结果图,其中,a图:krt1,b图:scgb2a1;
[0057]
图3显示基因krt1、基因scgb2a1在训练集中的roc曲线结果图,其中,a图:krt1,b图:scgb2a1;
[0058]
图4显示基因krt1 scgb2a1联合在训练集中的roc曲线结果图;
[0059]
图5显示基因krt1、基因scgb2a1在验证集中的roc曲线结果图,其中,a图:krt1,b图:scgb2a1;
[0060]
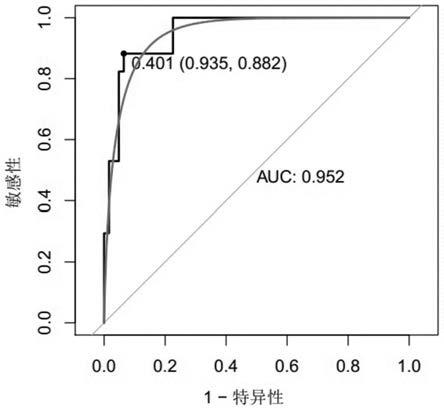
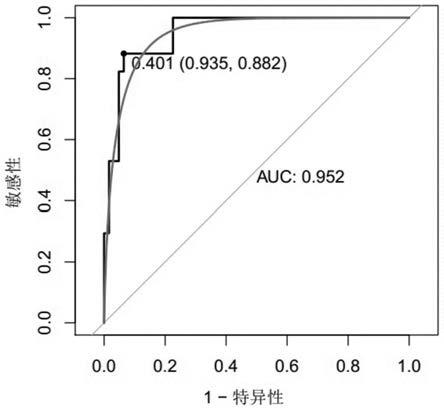
图6显示基因krt1 scgb2a1联合在验证集中的roc曲线结果图。
具体实施方式
[0061]
下面结合具体实施例,进一步阐述本发明,仅用于解释本发明,而不能理解为对本发明的限制。本领域的普通技术人员可以理解为:在不脱离本发明的原理和宗旨的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由权利要求及其等同物限定。下列实施例中未注明具体条件的实验方法,通常按照常规条件或按照厂商所建议的条件实施检测。
[0062]
实施例1筛选宫颈癌中差异表达的基因
[0063]
1、数据来源
[0064]
本研究中所采用的数据均来自于gene expression omnibus(geo)数据库,以“cervical cancer”为检索关键词,在geo数据库中进行检索,在排除细胞系或动物水平上的研究、以及单样本的研究后有两套数据集被纳入,分别为gse63514和gse39001;
[0065]
其中,gse63514来自gpl570平台,包含了28个宫颈癌患者的组织样本和24个正常的组织样本;gse39001数据集中包含两个平台的数据,分别是来自gpl201和gpl6244的数据,来自gpl201的数据中包含有43个宫颈癌患者的组织样本和12个正常的组织样本,来自gpl6244的数据中包含有19个宫颈癌患者的组织样本和5个正常的组织样本;
[0066]
将上述从geo数据库中下载的数据集gse63514作为训练集,样本量为case:normal=28:24;将上述从geo数据库中下载的数据集gse39001作为验证集,样本量为case:normal=62:17。
[0067]
2、数据预处理
[0068]
对上述从geo数据库下载的训练集和验证集的原始数据进行了标准化处理。其中,对于下载的数据集gse63514的基因表达矩阵文件,使用gpl平台注释文件对基因表达谱进行注释,将基因探针转换成gene symbol,其中多个探针对应同一个基因的,取平均值作为该基因的表达量;对于下载的数据集gse39001的基因表达矩阵文件,使用对应的gpl平台注
释文件对基因表达谱进行注释,将基因探针转换成gene symbol,其中多个探针对应同一个基因的取平均值,使用r包“sva”中的combat函数移除批次效应。
[0069]
3、差异表达分析
[0070]
使用r软件中的“limma”包分别对上述数据集gse63514和gse39001中经预处理的数据进行差异表达分析,其中,差异表达基因的筛选标准均为:|log2fc|>1.5,p.value<0.01。
[0071]
4、实验结果
[0072]
结果显示,筛选得到的训练集和验证集中的差异表达基因取交集后得到92个共有的表达趋势一致的差异表达基因,其中,筛选出的差异表达基因krt1和scgb2a1在训练集中的差异表达情况见表1和图1a
‑
b,在验证集中的差异表达情况见表2和图2a
‑
b,基因krt1、scgb2a1在宫颈癌中低表达,且差异具有统计学意义。
[0073]
表1基因在训练集中的差异表达结果
[0074]
基因log2fcaveexprtp.valueadj.p.valkrt1
‑
4.6704211.91365
‑
3.967560.000220.00170scgb2a1
‑
3.344695.73823
‑
3.179500.002500.01224
[0075]
表2基因在验证集中的差异表达结果
[0076]
基因log2fcaveexprtp.valueadj.p.valkrt1
‑
2.113175.49707
‑
4.707021.03e
‑
058.47e
‑
05scgb2a1
‑
2.712416.21911
‑
4.004440.000130.00079
[0077]
实施例2基因krt1和scgb2a1诊断效能的验证
[0078]
1、实验方法
[0079]
对实施例1中筛选出的在宫颈癌中差异表达的基因krt1和scgb2a1,使用r包“proc”(版本1.15.0)执行接收器工作特性(roc)分析,计算曲线下面积(auc)以评估基因krt1、基因scgb2a1、基因krt1 scgb2a1联合分别在训练集和验证集中对诊断宫颈癌的准确性,以及其敏感性和特异性。auc值的范围是0到1,其中,0.7是可接受的性能,而0.9是优异的性能;
[0080]
在判断单独指标在训练集和验证集中的诊断效能时,直接使用基因的表达量进行分析,选择youden指数最大的一点对应的水平作为其cutoff值,auc在0.5<auc<0.8的基因被用于联合分析;
[0081]
在判断指标联合在训练集和验证集中的诊断效能时,对各基因的表达水平进行logistics回归分析,通过拟合出的回归曲线计算出每个个体患病与否的概率,确定不同的概率划分阈值,根据确定的概率划分阈值,计算得出联合诊断方案的灵敏度、特异性以及准确性等。
[0082]
2、实验结果
[0083]
结果见表3
‑
4和图3
‑
6,结果显示基因组合krt1 scgb2a1对宫颈癌的诊断效能显著优于单个基因krt1、scgb2a1的诊断效能,基因组合krt1 scgb2a1在训练集和验证集中的auc值分别为0.905、0.952,敏感性和特异性分别为0.833和0.857、0.882和0.935,表明了基因组合krt1 scgb2a1具有较好的诊断效能,能够应用于宫颈癌的早期筛查诊断中。
[0084]
表3基因在训练集中的诊断效能结果
[0085]
基因auc敏感性特异性krt10.8020.5830.893scgb2a10.7800.9170.536krt1 scgb2a10.9050.8330.857
[0086]
表4基因在验证集中的诊断效能结果
[0087]
基因auc敏感性特异性krt10.7710.6470.806scgb2a10.7140.6470.855krt1 scgb2a10.9520.8820.935
[0088]
上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。