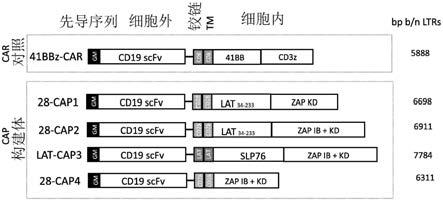
嵌合衔接子和激酶信号传导蛋白及其在免疫疗法中的用途
1.相关申请的交叉引用
2.本技术要求于2019年3月15日提交的美国临时申请号62/819,386的权益,其通过引用以其全文并入本文。
技术领域
3.本公开内容涉及嵌合衔接蛋白,其在一些实例中包括t细胞激活接头(lat)结构域,以及它们在免疫疗法中的用途。
4.政府支持致谢
5.本发明是由美国国立卫生研究院、国立癌症研究所在项目编号z01 bc 010304的政府支持下完成的。政府对本发明享有一定的权利。
背景技术:
6.嵌合抗原受体(car)是由肿瘤抗原特异性抗体片段组成的分子,其融合到跨膜结构域和t细胞信号传导部分。当在t细胞表面表达时,car介导与靶标的结合并激活t细胞,最终诱导靶细胞裂解。car正在成为治疗血液系统恶性肿瘤(包括非霍奇金淋巴瘤、b细胞急性淋巴细胞白血病和多发性骨髓瘤)的一种有前景的方法,并且也正在测试使用car治疗实体瘤。然而,t细胞耗竭仍是car
‑
t疗法中的挑战。
技术实现要素:
7.仍需要用于治疗实体瘤以及血液系统恶性肿瘤的有效免疫疗法。本文公开了可用于治疗癌症(包括血液恶性肿瘤和实体恶性肿瘤)的免疫疗法方法中的嵌合衔接蛋白(cap)。
8.公开了嵌合多肽(cap),包括(a)细胞外靶向结构域;(b)跨膜结构域;(c)细胞内t细胞激活接头(lat)结构域;和(d)细胞内zap70结构域,其中(a)
‑
(d)按n端到c端的顺序。在其他实施方案中,lat结构域被slp
‑
76结构域替换。在进一步的实施方案中,cap进一步包括细胞内信号传导结构域(例如41bb或cd28细胞内信号传导结构域),其是跨膜结构域的c端和lat或slp
‑
76结构域的n端。在一些实施方案中,嵌合多肽进一步包括铰链结构域(例如cd8或cd28铰链结构域),其是细胞外靶向结构域的c端和跨膜结构域的n端。在另外的实施方案中,嵌合多肽进一步包括信号序列结构域(例如gm
‑
csf信号序列),其是细胞外靶向结构域的n端。接头(例如,间隔区)可以存在于公开的cap的任何组件之间,例如,以实现cap的正确折叠和/或功能。
9.在另外的实施方案中,cap是嵌合多肽,包括(a)细胞外靶向结构域;(b)跨膜结构域;(c)细胞内zap70结构域,其中(a)
‑
(c)按n端到c端的顺序。在一些实施方案中,cap进一步包括41bb或cd28细胞内信号传导结构域,其在跨膜结构域的c端和zap70结构域的n端。在一些实施方案中,cap进一步包括铰链结构域,其是细胞外靶向结构域的c端和跨膜结构域的n端。在另外的实施方案中,cap进一步包括信号序列结构域,其是细胞外信号传导结构域
的n端。接头(例如,间隔区)可以存在于公开的cap的任何组件之间,例如,以实现cap的正确折叠和/或功能。
10.在一些实例中,细胞外靶向结构域是抗体、抗原结合结构域或scfv,其结合目标靶蛋白,例如肿瘤相关抗原(例如,癌细胞表达的抗原)。在非限制性实例中,细胞外靶向结构域结合cd19、cd22或bcma。在一些实例中,跨膜结构域是cd8跨膜结构域、cd28跨膜结构域或lat跨膜结构域。在另外的实例中,lat结构域是全长lat多肽,或是lat的氨基酸34
‑
233。在其他实例中,zap70结构域包括zap70激酶结构域(kd)、zap70结构域间b(ib)或其组合。
11.在一些实施方案中,本文公开的cap包括seq id no:5、7、9、16、17、19、21、23、25、27、29、31、33、35、37、39、41、43、45、47和49中任一项的氨基酸序列。
12.还公开了编码本文提供的cap的核酸分子。在一些实施方案中,cap包括seq id no:6、8、10、15、18、20、22、24、26、28、30、32、34、36、38、40、42、44、46、48和50中任一项的核酸序列。在另外的实施方案中,核酸分子被包括在表达载体(例如慢病毒或逆转录病毒载体)中。提供了表达cap的分离的细胞(例如t细胞或自然杀伤细胞),以及包括细胞和药学上可接受的载体的组合物。
13.进一步提供了治疗癌症(例如血液恶性肿瘤或实体瘤)受试者的方法。此类方法包括向受试者施用本文公开的分离的细胞或组合物。在一些实例中,细胞是表达cap的t细胞,例如自体t细胞。在其他实例中,细胞是表达cap的nk细胞,例如自体nk细胞。
14.从以下参照附图进行的详细描述中,本公开的前述和其他特征将变得更加明显。
附图说明
15.图1a
‑
1d是显示cd4 cap表征的一系列组图。图1a是包括cd4细胞外结构域(ed)和全长(fl)lat(cd4
‑
lat)或cd4
‑
ed、fllat和zap70激酶结构域(kd)(cd4
‑
cap)的基于lat的构建体的示意图。这些构建体包括cd4信号序列和lat tm结构域。表达tcrζ
‑
emerald的e6.1 jurkatt细胞在包被抗cd3抗体(hit3)的盖玻片上被激活(图1b)。表达cd4
‑
lat和grb2
‑
emerald(图1c)或cd4
‑
cap
‑
gfp(图1d)的e6.1 jurkatt细胞在包被抗cd4抗体(okt4)的盖玻片上被激活。
16.图2a和2b是显示在包被抗cd4抗体(okt4)的盖玻片(图2a)或包被抗cd45(左)或抗cd43(右)的盖玻片(图2b)上激活的表达cd4
‑
cap
‑
gfp的e6.1 jurkat t细胞中的微团簇的组图。
17.图3a和3b是显示在包被抗cd4抗体(okt4)的盖玻片上激活的表达tcrζ
‑
halo和cd4
‑
cap
‑
gfp(图3a)或zap70
‑
halo和cd4
‑
cap
‑
gfp(图3b)的e6.1 jurkat t细胞中的微团簇的组图。
18.图4a
‑
4c是显示在包被抗cd4抗体(okt4)的盖玻片上激活的表达cd4
‑
cap
‑
gfp和plcγ1
‑
halo(图4a)、slp76
‑
halo(图4b)或grb2
‑
halo(图4c)的e6.1 jurkat t细胞中微团簇形成的一系列组图。
19.图5a
‑
5b是抗cd19
‑
scfv
‑
lz cap(图5a)的示意图以及与raji b细胞(r)形成缀合物的表达cd19
‑
lz
‑
gfp和grb2
‑
scarlet的e6.1细胞(t)的复合dic图像(图5b)。
20.图6是显示示例性含slp76的cap构建体的示意图。
21.图7是显示另外的示例性cap构建体的示意图。
22.图8a
‑
8b是显示在激活的原代人t细胞中由指定的cap构建体(图7中所示)产生的细胞因子的图。转导或未转导的pbmc与nalm6或nalm6 cd19敲除肿瘤细胞或k562(不表达cd19)或k562 cd19(表达cd19)以1:1的比例共培养。24小时后通过elisa测量ifnγ(图8a)或il2(图8b)释放。
23.图9是显示由在原代人t细胞中表达的指定cap构建体(如图7所示)杀死肿瘤细胞的图。转导或未转导的pbmc与稳定表达荧光素酶的nalm6或nalm6 cd19敲除肿瘤细胞以指定的5:1或1:1比例共培养。4小时后,通过加入steady glo试剂(promega)检测发光。来自仅靶标孔(max cps)和仅靶标孔加1%tween
‑
20(min cps)的发光用于确定测定范围。特异性裂解百分比计算为:1
‑
(样品cps
‑
min cps)/(max cps
‑
min cps)。
24.图10a
‑
10c是显示另外的cap构建体的示意图。图10a显示了在lat结构域中仅包括所示酪氨酸的构建体。图10b显示了在zap70结构域中具有指定突变的构建体。图10c显示了cap2和cap4构建体的第二代版本。
25.序列表
26.本文或随附的序列表中列出的任何核酸和氨基酸序列使用核苷酸碱基和氨基酸的标准字母缩写显示,如37c.f.r.
§
1.822所定义。在至少一些情况下,仅显示每个核酸序列的一条链,但互补链被理解为包括在对显示链的任何引用中。
27.seq id no:1是cd4
‑
lat的氨基酸序列。cd4信号肽:氨基酸1
‑
25;cd4细胞外结构域:氨基酸1
‑
391;lat 2
‑
233全长:氨基酸393
‑
624。
28.seq id no:2是编码cd4
‑
lat的核酸序列。cd4信号肽:核苷酸1
‑
75;cd4细胞外结构域:核苷酸1
‑
1174;lat 2
‑
233全长:核苷酸1177
‑
1872。
29.seq id no:3是cd4
‑
cap的氨基酸序列。cd4信号肽:氨基酸1
‑
25;cd4细胞外结构域:氨基酸1
‑
391;lat全长2
‑
233:氨基酸393
‑
624;接头:氨基酸625
‑
645(包括zap
‑
70中的aa 318
‑
377
–
结构域间b的末端);zap70
‑
kd:氨基酸646
‑
911。
30.seq id no:4是编码cd4
‑
cap的核酸序列。cd4信号肽:核苷酸1
‑
75;cd4细胞外结构域:核苷酸1
‑
1174;lat全长2
‑
233:核苷酸1177
‑
1872;接头:核苷酸1876
‑
1935(接头包括zap
‑
70中的aa 318
‑
377
–
结构域间b的末端);zap70
‑
kd:核苷酸1936
‑
2724。
31.seq id no:5是抗cd19
‑
scfv
‑
lz的氨基酸序列。cd8信号肽:氨基酸1
‑
21;myc序列:氨基酸22
‑
31;抗cd19scfv:氨基酸32
‑
242;lat全长2
‑
233:氨基酸276
‑
507;接头:氨基酸508
‑
526(氨基酸509
‑
524是zap70氨基酸318
‑
333);zap70
‑
kd:氨基酸527
‑
789。
32.seq id no:6是编码抗cd19
‑
scfv
‑
lz的核酸序列。cd8信号肽:核苷酸1
‑
63;myc序列:核苷酸64
‑
93;抗cd19scfv:核苷酸94
‑
819;lat全长2
‑
233:核苷酸826
‑
1521;接头:核苷酸1522
‑
1578(核苷酸1525
‑
1572编码zap70氨基酸318
‑
333);zap70
‑
kd:核苷酸1579
‑
2367。
33.seq id no:7是lat
‑
cap1的氨基酸序列。gm
‑
csf信号肽:氨基酸1
‑
22;抗cd19scfv:氨基酸23
‑
267;lat全长2
‑
233:氨基酸271
‑
502(氨基酸271
‑
273,lat细胞外/铰链;氨基酸274
‑
295,lat tm;氨基酸296
‑
502,lat细胞内结构域);接头:氨基酸503
‑
521(氨基酸504
‑
519是zap70的氨基酸318
‑
333);zap70
‑
kd:氨基酸522
‑
784。
34.seq id no:8是编码lat
‑
cap1的核酸序列。gm
‑
csf信号肽:核苷酸1
‑
66;抗cd19scfv:核苷酸67
‑
801;lat全长2
‑
233:核苷酸811
‑
1506(核苷酸811
‑
819,lat细胞外/铰链;核苷酸820
‑
885,lat tm;核苷酸886
‑
1506,lat细胞内结构域);接头:核苷酸1507
‑
1563
(核苷酸1510
‑
1557编码zap70的氨基酸318
‑
333);zap70
‑
kd:核苷酸1564
‑
2352。
35.seq id no:9是lat
‑
cap2的氨基酸序列。gm
‑
csf信号肽:氨基酸1
‑
22;抗cd19scfv:氨基酸23
‑
267;lat全长2
‑
233:氨基酸271
‑
502(氨基酸271
‑
273,lat细胞外/铰链;氨基酸274
‑
295,lat tm;氨基酸296
‑
502,lat细胞内结构域);接头:氨基酸503
‑
521(氨基酸504
‑
519是zap70的氨基酸318
‑
333);zap70
‑
ib:氨基酸522
‑
604;zap70
‑
kd:氨基酸605
‑
867。
36.seq id no:10是编码lat
‑
cap2的核酸序列。gm
‑
csf信号肽:核苷酸1
‑
66;抗cd19scfv:核苷酸67
‑
801;lat全长2
‑
233:核苷酸811
‑
1506(核苷酸811
‑
819,lat细胞外/铰链;核苷酸820
‑
885,lat tm;核苷酸886
‑
1506,lat细胞内结构域);接头:核苷酸1507
‑
1563(核苷酸1510
‑
1557编码zap70的氨基酸318
‑
333);zap70
‑
ib:核苷酸1564
‑
1812;zap70
‑
kd:核苷酸1813
‑
2601。
37.seq id no:11是示例性cd8信号序列的氨基酸序列。
38.seq id no:12是示例性cd8信号序列的核酸序列。
39.seq id no:13是示例性slp
‑
76的核酸序列
40.seq id no:14是示例性slp
‑
76的氨基酸序列
41.seq id no:15是含有cap的示例性slp
‑
76的核酸序列。gm
‑
csf信号肽:核苷酸1
‑
66;抗cd19scfv:核苷酸67
‑
801;lat细胞外/铰链lat tm结构域:核苷酸811
‑
912(811
‑
819lat细胞外/铰链、820
‑
885lat tm、886
‑
912);全长slp
‑
76:核苷酸913
‑
2508,接头:核苷酸2509
‑
2565(核苷酸1510
‑
1557编码zap70的氨基酸318
‑
333);zap70
‑
kd:核苷酸2566
‑
3354。
42.seq id no:16是含有cap的示例性slp
‑
76的氨基酸序列。gm
‑
csf信号肽:氨基酸1
‑
22;抗cd19scfv:氨基酸23
‑
267;lat细胞外/铰链和lat tm结构域:氨基酸271
‑
301(aa271
‑
273:lat细胞外/铰链,aa274
‑
295:lat tm,aa296
‑
304:lat tm附近的氨基酸27
‑
25);全长slp76:氨基酸305
‑
836,接头:837
‑
855(aa 838
‑
853是zap70 aa 318
‑
333);zap70
‑
kd:氨基酸856
‑
1118。
43.seq id no:17是28
‑
cap1的氨基酸序列。gm
‑
csf信号肽aa 1
‑
22;抗cd19 scfv aa 23
‑
267;cd28铰链和tm aa 270
‑
335;lat 34
‑
233aa 336
‑
535;接头aa 536
‑
547;zap70激酶结构域aa 548
‑
810。
44.seq id no:18是28
‑
cap1的核酸序列。gm
‑
csf信号肽bp 1
‑
66;抗cd19 scfv bp 67
‑
801;cd28铰链和tm bp 808
‑
1005;lat 35
‑
233bp 1006
‑
1605;接头bp 1606
‑
1641;zap70激酶结构域bp 1642
‑
2430。
45.seq id no:19是28
‑
cap2的氨基酸序列。gm
‑
csf信号肽aa 1
‑
22;抗cd19 scfv aa 23
‑
267;cd28铰链和tm aa 270
‑
335;lat 35
‑
233aa 336
‑
534;接头aa 535
‑
539;zap70 ib和激酶结构域aa 540
‑
885;zap70 601
‑
619aa 886
‑
904。
46.seq id no:20是28
‑
cap2的核酸序列。gm
‑
csf信号肽bp 1
‑
66;抗cd19 scfv bp 67
‑
801;cd28铰链和tm bp 808
‑
1005;lat 35
‑
233bp 1006
‑
1602;接头bp 1603
‑
1617;zap70 ib和激酶结构域bp 1618
‑
2655;zap70 601
‑
619bp 2656
‑
2712。
47.seq id no:21是lat
‑
cap3的氨基酸序列。gm
‑
csf信号肽:氨基酸1
‑
22;抗cd19 scfv:氨基酸23
‑
267;lat 1
‑
35:氨基酸270
‑
303;slp76:氨基酸304
‑
835;zap70 ib和激酶结构域:氨基酸836
‑
1181。
48.seq id no:22是lat
‑
cap3的核酸序列。gm
‑
csf信号肽:核苷酸1
‑
66;抗cd19 scfv:核苷酸67
‑
801;lat 1
‑
35:核苷酸808
‑
909;slp76:核苷酸910
‑
2505;zap70 ib和激酶结构域:核苷酸2506
‑
3543。
49.seq id no:23是28
‑
cap4的氨基酸序列。gm
‑
csf信号肽aa 1
‑
22;抗cd19 scfv aa 23
‑
267;cd28铰链和tm aa 270
‑
335;接头aa 336
‑
340;zap70 ib和激酶结构域aa 341
‑
686;zap70 601
‑
619aa 687
‑
705。
50.seq id no:24是28
‑
cap4的核酸序列。gm
‑
csf信号肽bp 1
‑
66;抗cd19 scfv bp 67
‑
801;cd28铰链和tm bp 808
‑
1005;接头bp 1006
‑
1020;zap70 ib和激酶结构域bp 1021
‑
2058;zap70 601
‑
619 2059
‑
2115。
51.seq id no:25是8
‑
cap2的氨基酸序列。gm
‑
csf信号肽:氨基酸1
‑
22;抗cd19 scfv:氨基酸23
‑
267;cd8铰链和tm:氨基酸268
‑
336;lat 34
‑
233:氨基酸337
‑
535;接头:氨基酸536
‑
540;zap70 ib和激酶结构域:氨基酸541
‑
905。
52.seq id no:26是8
‑
cap2的核酸序列。gm
‑
csf信号肽:核苷酸1
‑
66;抗cd19 scfv:核苷酸67
‑
801;cd8铰链和tm:核苷酸802
‑
1008;lat 34
‑
233:核苷酸1009
‑
1605;接头:核苷酸1606
‑
1620;zap70 ib和激酶结构域:核苷酸1621
‑
2715。
53.seq id no:27是8
‑
cap4的氨基酸序列。gm
‑
csf信号肽:氨基酸1
‑
22;抗cd19 scfv:氨基酸23
‑
267;cd8铰链和tm:氨基酸268
‑
338;接头:氨基酸339
‑
343;zap70 ib和激酶结构域:氨基酸344
‑
365。
54.seq id no:28是8
‑
cap4的核酸序列。gm
‑
csf信号肽:核苷酸1
‑
66;抗cd19 scfv:核苷酸67
‑
801;cd8铰链和tm:核苷酸808
‑
1014;接头:核苷酸1015
‑
1029;zap70 ib和激酶结构域:核苷酸1030
‑
2124。
55.seq id no:29是8
‑
cap2 2ya的氨基酸序列。gm
‑
csf信号肽:氨基酸1
‑
22;抗cd19 scfv:氨基酸23
‑
267;cd8铰链和tm:氨基酸268
‑
336;lat 34
‑
233y132,y171:氨基酸337
‑
535;接头:氨基酸536
‑
540;zap70 ib和激酶结构域:氨基酸541
‑
905。
56.seq id no:30是8
‑
cap2 2ya的核酸序列。gm
‑
csf信号肽:核苷酸1
‑
66;抗cd19 scfv:核苷酸67
‑
801;cd8铰链和tm:核苷酸802
‑
1008;lat 34
‑
233y132,y171:核苷酸1009
‑
1605;接头:核苷酸1606
‑
1620;zap70 ib和激酶结构域:核苷酸1621
‑
2715。
57.seq id no:31是8
‑
cap2 2yb的氨基酸序列。gm
‑
csf信号肽:氨基酸1
‑
22;抗cd19 scfv:氨基酸23
‑
267;cd8铰链和tm:氨基酸268
‑
336;lat 34
‑
233y132,y191:氨基酸337
‑
535;接头:氨基酸536
‑
540;zap70 ib和激酶结构域:氨基酸541
‑
905。
58.seq id no:32是8
‑
cap2 2yb的核酸序列。gm
‑
csf信号肽:核苷酸1
‑
66;抗cd19 scfv:核苷酸67
‑
801;cd8铰链和tm:核苷酸802
‑
1008;lat 34
‑
233y132,y191:核苷酸1009
‑
1605;接头:核苷酸1606
‑
1620;zap70 ib和激酶结构域:核苷酸1621
‑
2715。
59.seq id no:33是8
‑
cap2 3ya的氨基酸序列。gm
‑
csf信号肽:氨基酸1
‑
22;抗cd19 scfv:氨基酸23
‑
267;cd8铰链和tm:氨基酸268
‑
336;lat 34
‑
233y132,y171,y191:氨基酸337
‑
535;接头:氨基酸536
‑
540;zap70 ib和激酶结构域:氨基酸541
‑
905。
60.seq id no:34是8
‑
cap2 3ya的核酸序列。gm
‑
csf信号肽:核苷酸1
‑
66;抗cd19 scfv:核苷酸67
‑
801;cd8铰链和tm:核苷酸802
‑
1008;lat 34
‑
233y132,y171,y191:核苷酸1009
‑
1605;接头:核苷酸1606
‑
1620;zap70 ib和激酶结构域:核苷酸1621
‑
2715。
61.seq id no:35是8
‑
cap2 3yb的氨基酸序列。gm
‑
csf信号肽:氨基酸1
‑
22;抗cd19 scfv:氨基酸23
‑
267;cd8铰链和tm:氨基酸268
‑
336;lat 34
‑
233y132,y171,y226:氨基酸337
‑
535;接头:氨基酸536
‑
540;zap70 ib和激酶结构域:氨基酸541
‑
905。
62.seq id no:36是8
‑
cap2 3yb的核酸序列。gm
‑
csf信号肽:核苷酸1
‑
66;抗cd19 scfv:核苷酸67
‑
801;cd8铰链和tm:核苷酸802
‑
1008;lat 34
‑
233y132,y171,y226:核苷酸1009
‑
1605;接头:核苷酸1606
‑
1620;zap70 ib和激酶结构域:核苷酸1621
‑
2715。
63.seq id no:37是8
‑
cap2 3yc的氨基酸序列。gm
‑
csf信号肽:氨基酸1
‑
22;抗cd19 scfv:氨基酸23
‑
267;cd8铰链和tm:氨基酸268
‑
336;lat 34
‑
233y132,y191,y226:氨基酸337
‑
535;接头:氨基酸536
‑
540;zap70 ib和激酶结构域:氨基酸541
‑
905。
64.seq id no:38是8
‑
cap2 3yc的核酸序列。gm
‑
csf信号肽:核苷酸1
‑
66;抗cd19 scfv:核苷酸67
‑
801;cd8铰链和tm:核苷酸802
‑
1008;lat 34
‑
233y132,y191,y226:核苷酸1009
‑
1605;接头:核苷酸1606
‑
1620;zap70 ib和激酶结构域:核苷酸1621
‑
2715。
65.seq id no:39是8
‑
cap4 zapas1的氨基酸序列。gm
‑
csf信号肽:氨基酸1
‑
22;抗cd19 scfv:氨基酸23
‑
267;cd8铰链和tm:氨基酸268
‑
338;接头:氨基酸339
‑
343;zap70 ib和激酶结构域m414a:氨基酸344
‑
365。
66.seq id no:40是8
‑
cap4 zapas1的核酸序列。gm
‑
csf信号肽:核苷酸1
‑
66;抗cd19 scfv:核苷酸67
‑
801;cd8铰链和tm:核苷酸808
‑
1014;接头:核苷酸1015
‑
1029;zap70 ib和激酶结构域m414a:核苷酸1030
‑
2124。
67.seq id no:41是8
‑
cap4 zapas2的氨基酸序列。gm
‑
csf信号肽:氨基酸1
‑
22;抗cd19 scfv:氨基酸23
‑
267;cd8铰链和tm:氨基酸268
‑
338;接头:氨基酸339
‑
343;zap70 ib和激酶结构域c405v,m414a:氨基酸344
‑
365。
68.seq id no:42是8
‑
cap4 zapas2的核酸序列。gm
‑
csf信号肽:核苷酸1
‑
66;抗cd19 scfv:核苷酸67
‑
801;cd8铰链和tm:核苷酸808
‑
1014;接头:核苷酸1015
‑
1029;zap70 ib和激酶结构域c405v,m414a:核苷酸1030
‑
2124。
69.seq id no:43是8
‑
41bb cap2的氨基酸序列。gm
‑
csf信号肽:氨基酸1
‑
22;抗cd19 scfv:氨基酸23
‑
267;cd8铰链和tm:氨基酸268
‑
336;41bb信号传导结构域:氨基酸337
‑
378;lat 35
‑
233:氨基酸379
‑
577;接头:氨基酸578
‑
582;zap70 ib和激酶结构域:氨基酸583
‑
947。
70.seq id no:44是8
‑
41bb cap2的核酸序列。gm
‑
csf信号肽:核苷酸1
‑
66;抗cd19 scfv:核苷酸67
‑
801;cd8铰链和tm:核苷酸802
‑
1008;41bb信号传导结构域:核苷酸1009
‑
1134;lat 35
‑
233:核苷酸1135
‑
1731;接头:核苷酸1732
‑
1746;zap70ib和激酶结构域:核苷酸1747
‑
2841。
71.seq id no:45是8
‑
28cap2的氨基酸序列。gm
‑
csf信号肽:氨基酸1
‑
22;抗cd19 scfv:氨基酸23
‑
267;cd8铰链和tm:氨基酸268
‑
336;cd28信号传导结构域:氨基酸337
‑
377;lat 35
‑
233:氨基酸378
‑
576;接头:氨基酸577
‑
581;zap70 ib和激酶结构域:氨基酸582
‑
946。
72.seq id no:46是8
‑
28cap2的核酸序列。gm
‑
csf信号肽:核苷酸1
‑
66;抗cd19 scfv:核苷酸67
‑
801;cd8铰链和tm:核苷酸802
‑
1008;cd28信号传导结构域:核苷酸1009
‑
1131;lat 35
‑
233:核苷酸1132
‑
1728;接头:核苷酸1729
‑
1743;zap70 ib和激酶结构域:核苷酸
genetics,genomics,proteomics and informatics,3
rd edition,springer,2008(isbn:1402067534),以及其他类似的参考文献。
83.除非另有说明,否则本文使用的所有技术和科学术语与本公开所属领域的普通技术人员通常理解的含义相同。除非上下文另有明确指示,否则单数术语“a”、“an”和“the”包括复数指示对象。“包括a或b”是指包括a、或b、或a和b。还应理解,对于核酸或多肽给出的所有碱基大小或氨基酸大小以及所有分子量或分子质量值是近似的,并提供说明。
84.尽管在本公开的实践或测试中可以使用与本文所述的那些方法和材料相似或等同的方法和材料,但下文描述了合适的方法和材料。本文提及的所有出版物、专利申请、专利和其他参考文献均通过引用以其全文并入,以及genbank登录号(用于2019年3月15日提供的序列)。如有冲突,以本说明书(包括术语解释)为准。此外,材料、方法和实施例仅是说明性的而不是限制性的。
85.为便于查阅本发明的各个实施方案,提供具体术语的以下解释:
86.抗体:包括至少一个可变区的多肽配体,该可变区识别并结合(例如特异性识别和特异性结合)抗原的表位。哺乳动物免疫球蛋白分子由重(h)链和轻(l)链组成,其各自均具有可变区,分别称为可变重(v
h
)区和可变轻(v
l
)区。v
h
区和v
l
区一起负责结合抗体识别的抗原。哺乳动物免疫球蛋白有五种主要的重链类别(或同种型),它们决定了抗体分子(igm、igd、igg、iga和ige)的功能活性。
87.抗体可变区包含“框架”区和高变区,称为“互补决定区”或“cdr”。cdr主要负责结合抗原表位。抗体的框架区用于在三维空间中定位和比对cdr。给定cdr的氨基酸序列边界可以使用许多熟知的编号方案中的任何一种而容易地确定,包括kabat等人描述的那些(具有免疫学意义的蛋白质序列,美国卫生和人类服务部,1991年;“kabat”编号方案),chothia等人(参见chothia and lesk,j mol biol 196:901
‑
917,1987;chothia et al.,nature 342:877,1989;和al
‑
lazikani et al.,(jmb 273,927
‑
948,1997;the“chothia”numbering scheme)和immunogenetics(imgt)数据库(参见lefranc,nucleic acids res29:207
‑
9,2001;“imgt”编号方案)。kabat和imgt数据库在线维护。
88.单链抗体(scfv)是一种基因工程分子,包含一个或更多个抗体的v
h
和v
l
结构域,它们通过合适的多肽接头连接为基因融合的单链分子(参见,例如,bird et al.,science,242:423
‑
426,1988;huston et al.,proc.natl.acad.sci.,85:5879
‑
5883,1988;ahmad et al.,clin.dev.immunol.,2012,doi:10.1155/2012/980250;marbry,idrugs,13:543
‑
549,2010)。scfv中v
h
结构域和v
l
结构域的分子内取向通常对scfv不是决定性的。因此,可以使用具有两种可能排列(v
h
‑
结构域
‑
接头结构域
‑
v
l
‑
结构域;v
l
‑
结构域
‑
接头结构域
‑
v
h
‑
结构域)的scfv。在dsfv中,v
h
和v
l
已发生突变以引入二硫键以稳定链的结合。还包括双抗体,它们是二价、双特异性抗体,其中v
h
和v
l
结构域在单条多肽链上表达,但是使用的接头太短,无法在同一链上的两个结构域之间配对,从而迫使结构域与另一条链的互补结构域配对并产生两个抗原结合位点(参见,例如,holliger et al.,proc.natl.acad.sci.,90:6444
‑
6448,1993;poljak et al.,structure,2:1121
‑
1123,1994)。
89.抗体还包括基因工程形式,例如嵌合抗体(例如人源化鼠抗体)和异源偶联抗体(例如双特异性抗体)。另见,pierce catalog and handbook,1994
‑
1995(pierce chemical co.,rockford,il);kuby,j.,immunology,3
rd ed.,w.h.freeman&co.,new york,1997。
90.分离的:“分离的”生物组分,例如核酸、蛋白质(包括抗体)或细胞器,已与该组分天然存在的环境(例如细胞)中的其他生物组分(即,其他染色体和染色体外dna和rna、蛋白质和细胞器)基本上分离或纯化。已“分离的”核酸和蛋白质包括通过标准纯化方法纯化的核酸和蛋白质。该术语还涵盖通过在宿主细胞中重组表达制备的核酸和蛋白质以及化学合成的核酸。
91.t细胞激活接头(lat):一种跨膜蛋白,其在tcr激活时被zap70磷酸化,并充当含有分子(例如grb2和plcγ1)的src同源2(sh2)的支架。产生的复合体随后充当支架,用于募集参与tcr信号传导的其他下游效应器。示例性人lat核酸和氨基酸序列在本文中公开并且还包括genbank登录号nm_001014989、nm_014387、nm_001014987和nm_001014988(核酸序列)以及np_001014989、np_055202、np_001014987和np_001014988(氨基酸序列)。
92.自然杀伤(nk)细胞:在不存在特定抗原刺激物且不受mhc类别限制的情况下杀死靶细胞的免疫系统细胞。靶细胞可以是肿瘤细胞或携带病毒的细胞。nk细胞的特点是存在cd56且不存在cd3表面标志物。nk细胞通常占正常外周血中单核细胞部分的约10%至15%。历史上,nk细胞最初是通过它们在没有既往免疫或激活的情况下溶解某些肿瘤细胞的能力来确定的。nk细胞被认为为病毒和肿瘤提供了“备用”保护机制,这些病毒和肿瘤可能通过下调mhc i类表达而逃避ctl应答。除了参与直接细胞毒性杀伤外,nk细胞还在细胞因子的产生中发挥作用,这对控制癌症和感染很重要。
93.在一些实例中,“修饰的nk细胞”是转导异源核酸(例如本文公开的一种或更多种核酸或载体)或表达一种或更多种异源蛋白质的nk细胞。术语“修饰的nk细胞”和“转导的nk细胞”在本文的一些实例中可互换使用。
94.纯化的:术语纯化的不要求绝对纯度;相反,它旨在作为相对术语。因此,例如,纯化的蛋白质或核酸制剂是其中蛋白质或核酸比蛋白质或核酸在其天然环境中(例如,在细胞内)更富集的制剂。在一个实施方案中,纯化制剂使得蛋白质或核酸占制剂的总蛋白质或核酸含量的至少50%。基本上纯化表示从其他蛋白质或细胞组分中纯化。基本上纯化的蛋白质或核酸的纯度至少为60%、70%、80%、90%、95%或98%。因此,在一个具体的非限制性实例中,基本上纯化的蛋白质或核酸90%不含其他组分。
95.重组体:具有非天然存在的序列或具有通过人工组合两个原本分离的序列片段(例如“嵌合”序列)制成的序列的核酸或蛋白质。这种人工组合可以通过化学合成或通过人工操作分离的核酸片段来实现,例如通过基因工程技术。
96.slp
‑
76:也称为淋巴细胞胞质蛋白2(lcp2)。一种在t细胞受体激活时磷酸化的衔接蛋白。示例性人slp
‑
76核酸和氨基酸序列在本文中公开并且还包括genbank登录号nm_005565(核酸序列)和np_005556(氨基酸序列)。
97.受试者:活的多细胞脊椎动物生物体,该类别包括人和兽医受试者,包括人和非人类哺乳动物。
98.t细胞:一种白细胞(淋巴细胞),其是免疫应答的重要介质。t细胞包括但不限于,cd4
t细胞和cd8
t细胞。cd4
t淋巴细胞是表面带有标志物(称为“分化簇4”(cd4))的免疫细胞。这些细胞,也称为辅助t细胞,有助于协调免疫应答,包括抗体应答和杀伤性t细胞应答。cd8
t细胞带有“分化簇8”(cd8)标志物。在一个实施方案中,cd8
t细胞是细胞毒性t淋巴细胞(cll)。在另一个实施方案中,cd8
细胞是抑制性t细胞。
99.可以通过细胞增殖和/或一种或更多种细胞因子(例如il
‑
2、il
‑
4、il
‑
6、ifnγ或tnfα)的表达或分泌的增加来检测激活的t细胞。cd8
t细胞的激活也可以通过响应抗原的细胞溶解活性的增加来检测。
100.在一些实例中,“修饰的t细胞”是转导异源核酸(例如本文公开的一种或更多种核酸或载体)或表达一种或更多种异源蛋白质的t细胞。术语“修饰的t细胞”和“转导的t细胞”在本文的一些实例中可互换使用。
101.转导的或转化的:转化的细胞是通过分子生物学技术将核酸分子引入其中的细胞。如本文所用,术语转导和转化涵盖可将核酸分子引入此类细胞的所有技术,包括用病毒载体转染、质粒载体的使用,以及通过电穿孔、脂质转染和粒子枪加速引入dna。
102.治疗或改善疾病:“治疗”是指在疾病或病理状况开始发展后减少或抑制其体征或症状的治疗干预,例如减少肿瘤大小或肿瘤负荷。“改善”是指疾病(例如癌症)的体征或症状的数量或严重程度减少。
103.载体:可以引入宿主细胞(例如,通过转染或转导),从而产生转化的宿主细胞的核酸分子。重组dna载体是具有重组dna的载体。载体可以包括允许其在宿主细胞中复制的核酸序列,例如复制起点。载体还可以包括一种或更多种选择标记基因和本领域已知的其他遗传元件。病毒载体是具有至少一些源自一种或更多种病毒的核酸序列的重组核酸载体。复制缺陷型病毒载体是由于至少一种复制必需基因功能缺陷而需要与复制所需的病毒基因组的一个或更多个区域互补的载体。
104.zap70:参与t细胞发育和激活的蛋白酪氨酸激酶。作为tcr介导的信号传导的一部分,zap70在tcr刺激后被酪氨酸磷酸化。示例性人zap70核酸和氨基酸序列在本文中公开并且还包括genbank登录号nm_001079和nm_207519(核酸序列)以及np_001070和np_997402(氨基酸序列)。
105.ii.嵌合衔接蛋白和核酸
106.本文公开了重组嵌合衔接蛋白(cap)和编码所述cap的核酸。在一些实施方案中,cap是嵌合多肽,包括(a)细胞外靶向结构域;(b)跨膜结构域;(c)用细胞内t细胞激活接头(lat)结构域或slp
‑
76结构域;和(d)细胞内zap70结构域,其中(a)
‑
(d)按n端到c端的顺序。在进一步的实施方案中,cap进一步包括细胞内信号传导结构域(例如41bb或cd28细胞内信号传导结构域),其是跨膜结构域的c端和lat或slp
‑
76结构域的n端。在一些实施方案中,cap进一步包括铰链结构域,其是细胞外靶向结构域的c端和跨膜结构域的n端。在另外的实施方案中,cap进一步包括信号序列结构域,其是细胞外信号传导结构域的n端。接头(例如,间隔区)可以存在于公开的cap的任何组件之间,例如,以实现cap的正确折叠和/或功能。
107.在另外的实施方案中,cap是嵌合多肽,包括(a)细胞外靶向结构域;(b)跨膜结构域;和(c)细胞内zap70结构域,其中(a)
‑
(c)按n端到c端的顺序。在一些实施方案中,cap进一步包括41bb或cd28细胞内信号传导结构域,其在跨膜结构域的c端和zap70结构域的n端。在一些实施方案中,cap进一步包括铰链结构域,其在细胞外靶向结构域的c端和跨膜结构域的n端。在另外的实施方案中,cap进一步包括信号序列结构域,其在细胞外信号传导结构域的n端。接头(例如,间隔区)可存在于公开的cap的任何组件之间,例如,实现正确折叠和/或cap的功能。
108.单独的组件以及示例性cap将在以下讨论。
109.a.细胞外区
110.公开的cap的细胞外区包括细胞外靶向结构域。在一些实施方案中,细胞外区还包括信号序列(例如信号序列和细胞外靶向结构域)。在其他实例中,细胞外区还包括信号序列和铰链结构域(例如信号序列、细胞外靶向结构域和铰链结构域)。在其他实施方案中,cap不包括信号序列,例如,当信号序列已经从cap细胞区切割时。
111.在一些实施方案中,细胞外靶向结构域是抗体的抗原结合结构域(例如单克隆抗体的抗原结合结构域),其特异性结合目标细胞(例如肿瘤细胞)表面上的靶蛋白。在一些实例中,抗原结合结构域可以包括v
h
和v
l
,它们分别包括v
h
和v
l
的hcdr1、hcdr2、hcdr3、lcdr1、lcdr2和lcdr3,其特异性结合靶蛋白。在其他实例中,抗原结合结构域可以是特异性结合靶蛋白的scfv。
112.在特定实施方案中,靶向结构域是结合目标靶标(例如肿瘤相关抗原)的抗原结合结构域或scfv。任何靶向结构域均可以插入本文所述的cap中。在一些实施方案中,靶向结构域结合在血液恶性肿瘤或实体瘤上表达的蛋白质。在一些非限制性实例中,靶向结构域结合cd19(例如结合cd19的scfv)。细胞外靶向结构域的示例性靶标和相应的恶性肿瘤如表1所示。
113.表1.示例性细胞外靶向结构域靶标和恶性肿瘤
114.115.116.117.[0118][0119]
因此,在一些实施方案中,细胞外靶向结构域结合以下项中的一种或更多种:cd19、cd22、b细胞成熟因子(bcma)、cd171、表皮生长因子受体变体iii(egfrviii)、白介素
‑
13受体α(il
‑
13ra)、间皮素、粘蛋白16、粘蛋白1、受体酪氨酸激酶样孤儿受体1(ror
‑
1)、前列腺干细胞抗原(psca)、cd33、前列腺特异性膜抗原(pmsa)、cd123、cd70、人表皮生长因子受体2(her2)、癌胚抗原(cea)、gptase激活蛋白(gap)、cd5、cd38、肝配蛋白a型受体2(epha2)、成纤维细胞激活蛋白α(fap)、神经节苷脂g2(gd2)、上皮细胞粘附分子(epcam)、cd133和磷脂酰肌醇蛋白聚糖3(gpc3)。该列表是非限制性的,也可以使用另外的细胞外靶向结构域。例如,细胞外结构域可以包括任何tcr,例如在白血病或淋巴瘤中克隆表达的tcr。
[0120]
在特定实例中,细胞外靶向区域是与cd19结合的scfv。在一些实例中,cd19 scfv的氨基酸序列与氨基酸序列seq id no:17的氨基酸23
‑
267具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成。在另外的实例中,cd19 scfv由与seq id no:18的核苷酸67
‑
801具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0121]
在一些实施方案中,cap的细胞外区包括信号序列结构域,例如,靶向结构域的n端,例如,以促进cap在细胞表面上的表达。在一些实例中,在细胞表面上表达cap后,可以将信号序列域从cap切割。因此,在一些实施方案中,cap缺乏信号序列域。
[0122]
信号序列结构域可以包括任何合适的信号肽序列。在一个非限制性实例中,信号肽结构域是人粒细胞
‑
巨噬细胞集落刺激因子(gm
‑
csf)信号序列,例如与seq id no:7的氨基酸1
‑
22具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在另外的实例中,gm
‑
csf信号序列由与seq id no:18的
核苷酸1
‑
66具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。在另外的实例中,信号肽结构域是cd8信号序列,例如与与seq id no:11具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,cd8信号序列由与seq id no:12具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。然而,可以利用本领域已知的其他信号序列。
[0123]
在一些实施方案中,公开的cap还包括铰链结构域,其在一些实例中是细胞外靶向结构域和跨膜区之间的间隔区。然而,在其他实施方案中,cap不包括铰链结构域。在其他实例中,铰链结构域是跨膜结构域的一部分。例如,在一些实例中,lat铰链结构域(其是三个氨基酸
‑
eea)可以作为lat tm结构域的一部分而被包括。cap的铰链结构域(如果被包括)是细胞外靶向结构域的c端和跨膜结构域的n端。在一些实例中,铰链结构域的长度为约3至250个氨基酸(例如长度为约3
‑
25、5
‑
30、10
‑
50、40
‑
80、60
‑
100、70
‑
120、90
‑
140、110
‑
150、125
‑
160、130
‑
180、150
‑
200、170
‑
225或210
‑
250个氨基酸)。在一些实例中,在靶向结构域和铰链结构域之间包括间隔区或接头,例如接头的长度为2
‑
4个氨基酸。
[0124]
在一些实施方案中,细胞外铰链结构域是cd28铰链结构域或cd8铰链结构域。在一些实例中,铰链结构域是与seq id no:17的氨基酸270
‑
308的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的cd28铰链结构域。在一些实例中,cd28铰链结构域由与seq id no:18的核苷酸808
‑
924具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。在其他实施方案中,铰链结构域是与seq id no:25的氨基酸266
‑
312的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的cd8铰链结构域。在一些实例中,cd8铰链结构域由与seq id no:26的核苷酸796
‑
936具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。在其他实例中,细胞外铰链结构域来自免疫球蛋白,例如iggl、igg4或igd铰链结构域。
[0125]
b.跨膜结构域
[0126]
公开的cap包括与铰链结构域(如果存在)(例如,铰链结构域的c端)和lat(例如,lat的n端)连接的跨膜结构域。在其他实例中,如果不存在铰链结构域,则跨膜与细胞外靶向结构域(例如,细胞外靶向结构域的c端)和lat结构域(例如,lat结构域的n端)连接。跨膜结构域可以来自任何膜结合蛋白或跨膜蛋白,或可以是合成的。本领域普通技术人员可以识别跨膜序列,例如使用跨膜结构域预测程序,例如tmpred(可在embnet.vital
‑
it.ch/software/tmpred_form.html获得)、tmhmm v.2.0(可在cbs.dtu.dk/services/tmhmm
‑
2.0/获得)和其他公开可获得的预测程序。
[0127]
在一些实施方案中,公开的cap的跨膜结构域是来自cd8、cd28、lat、cd3ε、cd45、cd4、cd5、cd8、cd9、cd 16、cd22、cd33、cd37、cd64、cd80、cd86、cd134、cd137或cd154的跨膜结构域。在其他实施方案中,跨膜结构域是来自t细胞受体(tcr)(例如tcrα、tcrβ或tcrζ链)的跨膜结构域。
[0128]
在具体实例中,跨膜结构域是cd8的跨膜结构域,例如与seq id no:25的氨基酸313
‑
336的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少
99%同一性,或包括其或由其组成的跨膜结构域。在一些实例中,cd8跨膜结构域由与seq id no:26的核苷酸937
‑
1008具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。在其他实例中,跨膜结构域是cd28的跨膜结构域,例如,与seq id no:17的氨基酸309
‑
335的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的跨膜结构域。在一些实例中,cd28跨膜结构域由与seq id no:18的核苷酸925
‑
1005具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0129]
在又其他实例中,跨膜结构域是lat的跨膜结构域,例如,与seq id no:15的氨基酸271
‑
295的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的跨膜结构域,其中前三个氨基酸是lat铰链结构域。在一些实例中,lat铰链和跨膜结构域由与seq id no:16的核苷酸811
‑
885具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0130]
在具体的非限制性实例中,当跨膜结构域来自cd8时,铰链结构域也来自cd8,或当跨膜结构域来自cd28时,铰链结构域也来自cd28。在其他实例中,跨膜结构域和铰链结构域可以来自不同的来源,例如来自cd8、cd28和lat中任一个的铰链结构域和跨膜结构域的组合。在一些非限制性实例中,跨膜结构域来自cd8并且铰链结构域来自cd28,跨膜结构域来自cd28并且铰链结构域来自cd8,或跨膜结构域来自lat并且铰链结构域来自cd8或cd28。
[0131]
c.lat结构域
[0132]
在一些实施方案中,公开的cap包括细胞内lat结构域,其是跨膜结构域的c端。在一些实例中,在tm结构域和lat结构域之间可以包括间隔区。当前的car使用cd3ζ作为信号传导结构域,具有不同的共刺激、跨膜、铰链和细胞外靶向结构域组合。lat充当许多关键信号传导和衔接分子的关键支架,这些分子参与tcr连接下游的tcr信号转导。tcr激活后,lat通过grb2和sos介导的交联机制形成独特的信号传导复合体。此外,lat复合体的募集受共刺激和抑制分子的动力学调节,其形成足以引起tcr激活非依赖的完全t细胞激活。因此,一方面,本文公开的cap与car的区别在于lat结构域替换cd3ζ作为信号传导结构域。
[0133]
lat结构域可以包括全部或部分lat蛋白。在一些实例中,cap包括全长lat、例如与lat的氨基酸2
‑
233(例如seq id no:5的氨基酸276
‑
507)的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。全长lat包括lat的细胞外结构域、tm结构域和细胞内结构域。在一些实例中,lat结构域由与seq id no:6的核苷酸826
‑
1521具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。在具体的非限制性实例中,lat结构域与lat的氨基酸34
‑
233(例如seq id no:17的氨基酸336
‑
535)具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成。在其他实例中,lat结构域编码lat的氨基酸34
‑
233并且是与seq id no:18的核苷酸1006
‑
1605具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸。氨基酸34
‑
233对应于lat的细胞内结构域,例如在cap构建体中使用来自其他来源的铰链和tm结构域时使用。
[0134]
在另外的实施方案中,lat结构域包括一个或更多个突变,例如提高蛋白质稳定性、表达和/或信号功能。在一个实例中,lat结构域包括k52r和/或k204r取代。参见,例如,美国专利号8,779,095,其通过引用并入本文。
[0135]
在其他实施方案中,lat结构域包括酪氨酸残基的一个或更多个突变。在一些实施方案中,lat结构域仅包括存在于野生型lat结构域中的十种胞质酪氨酸残基中的两种或三种。lat胞质结构域包含十种酪氨酸,lat功能不需要所有这些酪氨酸。四种膜远端酪氨酸残基y132、y171、y191和y226已被证明对tcr介导的信号传导最重要(例如,zhang et al.,j.biol.chem.275:23355
‑
23361,2000)。因此,具有完整的这四种膜远端酪氨酸中的两种或三种的lat突变体可能实现降低来自含有lat的cap的信号强度。因此,在一些实例中,cap包括其中六个或更多个(例如,6、7、8、9或10个)酪氨酸残基被苯丙氨酸取代的lat结构域。在一些实例中,lat结构域仅包括在lat结构域的氨基酸y132、y171、y191或y226处的酪氨酸(例如,分别对应于seq id no:25的氨基酸位置434、473、493和528),或其两个或更多个的组合,其中lat结构域中的其他酪氨酸残基被苯丙氨酸取代。在一些实例中,lat结构域在对应于seq id no:29的y434和y473的氨基酸处包括酪氨酸,lat结构域中的其他酪氨酸残基被苯丙氨酸取代。在其他实例中,lat结构域在对应于seq id no:31的y434和y493的氨基酸处包括酪氨酸,lat结构域中的其他酪氨酸残基被苯丙氨酸取代。在进一步的实例中,lat结构域在对应于seq id no:33的y434、y473和y493的氨基酸处包括酪氨酸,lat结构域中的其他酪氨酸残基被苯丙氨酸取代。在另外的实例中,lat结构域在对应于seq id no:528的y434、y473和y538的氨基酸处包括酪氨酸,lat结构域中的其他酪氨酸残基被苯丙氨酸取代。在其他实例中,lat结构域在对应于seq id no:37的y434、y493和y528的氨基酸处包括酪氨酸,lat结构域中的其他酪氨酸残基被苯丙氨酸取代。
[0136]
在其他实施方案中,lat结构域被slp
‑
76结构域替换。tcr激活后,zap
‑
70磷酸化slp
‑
76和lat,并且slp
‑
76和lat均参与t细胞信号传导。先前研究表明,lat的重要作用是将slp
‑
76及其相关分子募集到膜上,其是信号传导分子集中的地方。该研究表明lat胞质结构域可以被slp
‑
76替换(boerth et al.,j exp med 192(7):1047
‑
1058,2000)。因此,在本文所述的cap中包括slp
‑
76可以增强t细胞中的信号传导。
[0137]
因此,在一些实例中,本文所述的cap中的lat结构域被slp
‑
76结构域替换。包括slp
‑
76的示例性cap构建体(cap
‑
slp76构建体)如图6所示。在一些实例中,slp
‑
76结构域可以包括slp
‑
76蛋白的全部或部分。在一些实例中,cap包括全长slp
‑
76(不包括起始蛋氨酸),例如与seq id no:14的氨基酸2
‑
533或seq id no:16的氨基酸305
‑
836的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成。在一些实例中,slp
‑
76结构域由与seq id no:13的核苷酸4
‑
1602或seq id no:15的核苷酸913
‑
2508具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0138]
d.zap70结构域
[0139]
公开的cap还包括zap70蛋白的至少一部分。zap70结构域位于lat结构域的c端。zap70是蛋白酪氨酸激酶,在通过t细胞抗原受体刺激t细胞后,它在t细胞信号传导中起关键作用。激活的zap70使衔接子lat和slp
‑
76磷酸化,然后作为各种衔接子和酶的支架。这些信号传导分子共同导致t细胞激活。因此,lat和zap
‑
70激酶结构域的融合有望绕过tcr激
活。在一些实施方案中,包括zap
‑
70ib结构域是因为zap70 ib结构域包含在zap70活性调节中起作用的酪氨酸残基。
[0140]
在一些实例中,zap70结构域是zap70激酶结构域(kd)。在其他实例中,zap70结构域是zap70结构域间b(ib)结构域和zap70 kd。在一些实例中,zap70结构域包括zap70 kd,例如与seq id no:5的氨基酸527
‑
789的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,zap70 kd由与seq id no:6的核苷酸1579
‑
2367具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸编码。
[0141]
在其他实例中,zap70结构域包括zap70 ib,例如与seq id no:9的氨基酸522
‑
604的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,zap70 ib由与seq id no:10的核苷酸1564
‑
1812具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸编码。在一个非限制性实例中,cap包括zap70 ib和zap70 kd(例如,zap70 ib后接zap70 kd)。
[0142]
在另外的实施方案中,zap70结构域包括一个或更多个突变。类似物敏感(as)zap70突变体保留催化活性,但可以被小分子突变体特异性激酶抑制剂3
‑
mb
‑
pp1抑制(参见,例如,levin et al.,j.biol.chem.283:15419
‑
15430,2008)。这些突变的掺入实现在治疗过程中以可调和且可逆的方式对含有zap70的cap进行突变特异性、小分子介导的控制。在一个实例中,zap70结构域包括氨基酸取代m414a和/或c405v,对应于seq id no:27的氨基酸位置m503和c494。
[0143]
e.另外的组件
[0144]
在一些实施方案中,公开的cap包括lat结构域和zap70结构域之间的接头,例如,以保持cap的lat结构域和zap70结构域之间的灵活性。在一些实例中,接头可包括zap70蛋白的全部或部分,例如zap70的氨基酸318
‑
333。该序列是zap70 ib的一部分,可用于调节zap70 kd的激酶活性。在一些实例中,接头包括与seq id no:9的氨基酸5504
‑
519的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在其他实例中,接头由与seq id no:10的核苷酸1510
‑
1557具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸编码。其他接头包括肽接头(g3s)3、(g4s)3、(g4s)4、(g4s)5或(g4s)。也可以选择其他接头。
[0145]
在其他实施方案中,公开的cap包括一种或更多种另外的细胞内信号传导结构域(例如来自41bb、cd28、icos、cd27、dap10和dap12中的至少一种,或其两种或更多种的组合)。在一些实例中,另外的细胞内信号传导结构域是跨膜结构域的c端和lat结构域的n端。在其他实例中,cap不包括lat结构域并且另外的细胞内信号传导结构域是跨膜结构域的c端和zap70结构域的n端。在一些实例中,细胞内信号传导结构域是41bb细胞内信号传导结构域并且包括与seq id no:43的氨基酸337
‑
378的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在其他实例中,细胞内信号传导结构域是41bb细胞内信号传导结构域并且由与seq id no:44的核苷酸1009
‑
1134具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同
一性,或包括其或由其组成的核酸编码。在一些实例中,细胞内信号传导结构域是cd28细胞内信号传导结构域并且包括与seq id no:45的氨基酸337
‑
377的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,包括其或由其组成的氨基酸序列。在其他实例中,细胞内信号传导结构域是cd28细胞内信号传导结构域并且由与seq id no:46的核苷酸1009
‑
1131具有至少90%、至少95%、至少96%、至少97%、至少98%,或至少99%同一性,或包括其或由其组成的核酸编码。
[0146]
f.示例性cap多肽和核酸
[0147]
示例性cap多肽在本文中提供,例如图1a、5a、6、7和10a
‑
10c所示的那些。
[0148]
在一些实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd8铰链结构域、cd8跨膜结构域、lat 34
‑
233结构域以及zap70 ib和kd(称为8
‑
cap2)。在一些实例中,8
‑
cap2具有与氨基酸序列seq id no:25的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,8
‑
cap2由与seq id no:26的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0149]
在其他实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd28铰链结构域、cd28跨膜结构域、lat 34
‑
233结构域和zap70 kd(称为28
‑
cap1)。在一些实例中,28
‑
cap1具有与seq id no:17的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,28
‑
cap1由与seq id no:18的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%,或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0150]
在其他实施方式中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd28铰链结构域、cd28跨膜结构域、lat 34
‑
233结构域以及zap70 ib和kd(称为28
‑
cap2)。在一些实例中,28
‑
cap2具有与seq id no:19的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,28
‑
cap2由与seq id no:20的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0151]
在进一步的实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd8铰链、cd8 tm结构域、slp
‑
76 2
‑
533结构域和zap70 kd(称为8
‑
slp
‑
cap1)。在其他实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd8铰链、cd8 tm结构域、slp
‑
76 2
‑
533结构域、zap70 ib和zap70 kd(称为8
‑
slp
‑
cap2)。在另外的实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd28铰链、cd28 tm结构域、slp
‑
76 2
‑
533结构域和zap70 kd(称为28
‑
slp
‑
cap1)。在其他实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd28铰链、cd28 tm结构域、slp
‑
76 2
‑
533结构域、zap70 ib和zap70 kd(称为28
‑
slp
‑
cap2)。在进一步的实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、lat细胞外和tm结构域、slp
‑
76 2
‑
533结构域、zap70 ib和zap70 kd(称为lat
‑
slp
‑
cap2)。
[0152]
在其他实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、lat细胞外和tm结构域、slp
‑
76 2
‑
533结构域、zap70 ib和zap70 kd(称为lat
‑
slp
‑
cap1)。在一些实例中,lat
‑
slp76
‑
cap1具有与seq id no:15的氨基酸序列具有至少90%、至少
95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,lat
‑
slp76
‑
cap1由与seq id no:16的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的的核酸分子编码。
[0153]
在其他实施方案中,cap包括(按照n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、lat铰链和tm结构域、slp
‑
76 2
‑
533结构域、zap70 ib以及zap70 kd(称为lat
‑
cap3)。在一些实例中,lat
‑
cap3具有与seq id no:21的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,lat
‑
cap3由与seq id no:22的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0154]
在其他实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd28铰链和tm结构域、zap70 ib和zap70 kd(称为28
‑
cap4)。在一些实例中,28
‑
cap4具有与seq id no:23的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,28
‑
cap4由与seq id no:24的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0155]
在其他实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd8铰链结构域、cd8跨膜结构域、在位置y132和y171具有酪氨酸的lat 34
‑
233结构域、以及zap70 ib和kd(称为8
‑
cap2 2ya)。在一些实例中,8
‑
cap2 2ya具有与seq id no:29的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,8
‑
cap2 2ya由与seq id no:30的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0156]
在另外的实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd8铰链结构域、cd8跨膜结构域、在位置y132和y191具有酪氨酸的lat 34
‑
233结构域,以及zap70 ib和kd(称为8
‑
cap2 2yb)。在一些实例中,8
‑
cap2 2yb具有与seq id no:31的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,8
‑
cap2 2yb由与seq id no:32的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0157]
在进一步的实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd8铰链结构域、cd8跨膜结构域、在位置y132、y171和y191具有酪氨酸的lat 34
‑
233结构域,以及zap70 ib和kd(称为8
‑
cap2 3ya)。在一些实例中,8
‑
cap2 3ya具有与氨基酸序列seq id no:33的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,8
‑
cap2 3ya由与seq id no:34的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0158]
在一些实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd8铰链结构域、cd8跨膜结构域、在位置y132、y171和y226具有酪氨酸的lat 34
‑
233结构
域,以及zap70 ib和kd(称为8
‑
cap2 3yb)。在一些实例中,8
‑
cap2 3yb具有与seq id no:35的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,8
‑
cap2 3yb由与seq id no:36的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0159]
在其他实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd8铰链结构域、cd8跨膜结构域、在位置y132、y191和y226具有酪氨酸的lat 34
‑
233结构域、以及zap70 ib和kd(称为8
‑
cap2 3yc)。在一些实例中,8
‑
cap2 3yb具有与seq id no:37的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,8
‑
cap2 3yc由与seq id no:38的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0160]
在其他实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd8铰链结构域、cd8 tm结构域、zap70 ib和zap70 kd(称为8
‑
cap4)。在一些实例中,8
‑
cap4具有与seq id no:27的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,8
‑
cap4由与seq id no:28的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。在一些实例中,8
‑
cap4进一步包括zap70结构域中的m414a取代(称为8
‑
cap4 zapas1)。在一些实例中,8
‑
cap4 zapas1具有与seq id no:39的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,8
‑
cap4 zapas1由与seq id no:40的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。在其他实例中,8
‑
cap4进一步包括zap70结构域中的c405v和m414a取代(称为8
‑
cap4 zapas2)。在一些实例中,8
‑
cap4 zapas2具有与seq id no:41的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,8
‑
cap4 zapas2由与seq id no:42的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0161]
在还进一步的实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd8铰链结构域、cd8跨膜结构域、41bb信号传导结构域、lat 34
‑
233结构域、以及zap70 ib和kd(称为8
‑
41bb cap2)。在一些实例中,8
‑
41bb cap2具有与seq id no:43的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,8
‑
41bb cap2由与seq id no:44的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0162]
在另外的实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd8铰链结构域、cd8跨膜结构域、cd28信号传导结构域、lat 34
‑
233结构域、以及zap70 ib和kd(称为8
‑
28cap2)。在一些实例中,8
‑
28cap2具有与seq id no:45的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其
或由其组成的氨基酸序列。在一些实例中,8
‑
28cap2由与seq id no:46的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0163]
在其他实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd8铰链结构域、cd8跨膜结构域、41bb信号传导结构域、以及zap70 ib和kd(称为8
‑
41bb cap4)。在一些实例中,8
‑
41bb cap4具有与seq id no:47的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,8
‑
41bb cap4由与seq id no:48的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0164]
在另外的实施方案中,cap包括(按n端到c端的顺序)gm
‑
csf信号序列、抗cd19 scfv、cd8铰链结构域、cd8跨膜结构域、cd28信号传导结构域、以及zap70 ib和kd(称为8
‑
28 cap4)。在一些实例中,8
‑
28 cap2具有与seq id no:49的氨基酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的氨基酸序列。在一些实例中,8
‑
28cap4由与seq id no:50的核酸序列具有至少90%、至少95%、至少96%、至少97%、至少98%、或至少99%同一性,或包括其或由其组成的核酸分子编码。
[0165]
还提供了本文所述的cap或其结构域的功能变体,其保留了作为其变体的cap的生物活性或保留了特定结构域的生物活性。功能变体的氨基酸序列可以与亲本cap或结构域具有至少约80%、约85%、约90%、约91%、约92%、约93%、约94%、约95%、约96%、约97%、约98%、约99%或更多同一性。例如,可以在信号序列结构域、细胞外靶向结构域、铰链结构域、跨膜结构域、lat结构域和zap70结构域中的一种或更多种中进行取代。
[0166]
在一些实例中,功能变体包括具有至少一个保守氨基酸取代(例如最多10个保守氨基酸取代,例如1、2、3、4、5、6、7、8、9或10个保守取代)的亲本cap或结构域的氨基酸序列。在其他实例中,功能变体包括具有至少一个非保守氨基酸取代(例如最多10个非保守氨基酸取代,例如1、2、3、4、5、6、7、8、9或10个非保守取代)的亲本cap或结构域的氨基酸序列。在这种情况下,非保守氨基酸取代不干扰或抑制功能变体的生物活性。非保守氨基酸取代可增强功能变体的生物学活性,从而与亲本cap或结构域相比,功能变体的生物学活性增加。
[0167]
在一些实例中,cap或cap结构域可以包括一种或更多种合成氨基酸代替一种或更多种天然存在的氨基酸。此类合成氨基酸包括,例如,氨基环己烷羧酸、正亮氨酸、α
‑
氨基正癸酸、高丝氨酸、s
‑
乙酰氨基甲基
‑
半胱氨酸、反式
‑3‑
和反式
‑4‑
羟脯氨酸、4
‑
氨基苯丙氨酸、4
‑
硝基苯丙氨酸、4
‑
氯苯丙氨酸、4
‑
羧基苯丙氨酸、β
‑
苯丝氨酸、β
‑
羟基苯丙氨酸、苯基甘氨酸、α
‑
萘丙氨酸、环己基丙氨酸、二氢吲哚
‑2‑
羧酸、1,2,3,4
‑
四氢异喹啉
‑3‑
羧酸、氨基丙二酸,氨基丙二酸单酰胺、n'
‑
苄基
‑
n'
‑
甲基
‑
赖氨酸、ν',ν'
‑
二苄基
‑
赖氨酸、6
‑
羟基赖氨酸,鸟氨酸、α
‑
氨基环戊烷羧酸、α
‑
氨基环己烷羧酸、oc
‑
氨基环庚烷羧酸、
‑
(2
‑
氨基
‑2‑
降冰片烷)
‑
羧酸、γ
‑
二氨基丁酸、α,β
‑
二氨基丙酸、高苯丙氨酸和α
‑
叔丁基甘氨酸。cap可以被糖基化、酰胺化、羧化、磷酸化、酯化、n
‑
酰化、通过例如二硫键环化、或转化为酸加成盐和/或任选地二聚或聚合、或缀合。
[0168]
iii.表达嵌合衔接蛋白的细胞
[0169]
本文还提供了表达公开的cap的细胞(例如,免疫细胞)和包括表达公开的cap的细胞的组合物。在特定的实施方案中,组合物包括表达cap的细胞(例如t细胞或自然杀伤(nk)
细胞)和药学上可接受的载体。
[0170]
在一些实施方案中,编码公开的cap的核酸分子被包括在表达载体(例如病毒载体)中以用于在宿主细胞例如t细胞或nk细胞中表达。在一些实例中,表达载体包括与编码cap的核酸分子可操作地连接的启动子。另外的表达控制序列,例如一种或更多种增强子、转录和/或翻译终止子,以及起始序列也可以包括在表达载体中。
[0171]
公开的核酸可以在宿主细胞(例如细菌、植物、酵母、昆虫或哺乳动物细胞)中表达,例如,使用包括编码cap的核酸的表达载体。当宿主是真核生物时,可以使用dna转染方法,例如磷酸钙共沉淀、显微注射、电穿孔、插入包裹在脂质体中的质粒或病毒载体。真核细胞也可以用编码cap的多核苷酸序列和编码可选择表型如单纯疱疹胸苷激酶基因的第二核酸分子共转化。另一种方法是使用真核病毒载体,例如猿猴病毒40(sv40)、慢病毒或逆转录病毒,转导或转化真核细胞并表达cap(参见例如,病毒表达载体,springer出版社,muzyczka编辑,2011)。在一些实例中,此类表达系统用于在细胞例如293、cos、cho、hela或骨髓瘤细胞系中产生重组蛋白。
[0172]
在一些实施方案中,病毒载体用于表达cap。病毒载体包括但不限于猿猴病毒40、腺病毒、腺相关病毒(aav)、慢病毒载体和逆转录病毒,例如γ逆转录病毒。逆转录病毒载体提供了将基因转入真核细胞的高效方法。此外,逆转录病毒整合以受控方式进行,并导致每个细胞稳定整合一个或几个新遗传信息的副本。不受理论束缚,慢病毒载体优于源自癌逆转录病毒如鼠白血病病毒的载体,因为它们可以转导非增殖细胞,如肝细胞。它们还具有低免疫原性的另外的优势。在一个非限制性实例中,载体是慢病毒载体,例如具有ef1a启动子的pelns。其他示例性载体包括plv
‑
er1a
‑
ires
‑
neo、新霉素缺失或逆转录病毒载体mgsv。
[0173]
还提供了表达本文公开的cap的免疫细胞(例如t细胞或nk细胞)。免疫细胞用包括编码cap的核酸的表达载体转导或转化。在一些实例中,转导或转化的细胞是外周血淋巴细胞(例如,从受试者获得)、外周血单核细胞(例如,从受试者获得)、分离的t细胞(例如原代t细胞或从受试者获得的t细胞)、或分离的nk细胞(例如原代nk细胞或从受试者获得的nk细胞)。t细胞或nk细胞可以从受试者的样品(例如血液、血浆、骨髓、淋巴结或胸腺)中获得。在一些实例中,t细胞或nk细胞也从受试者的样品中富集、纯化和/或扩增,例如在用cap表达载体转导或转化之前和/或之后。在一些实例中,t细胞是cd3
t细胞,例如cd8
t细胞或cd4
t细胞。
[0174]
iv.免疫疗法的方法
[0175]
本文公开了利用cap治疗受试者的癌症(例如血液恶性肿瘤或实体瘤)的方法。在一些实施方案中,该方法包括向受试者施用组合物,该组合物包括表达cap(例如,用编码cap的载体转导的)的t细胞或nk细胞和药学上可接受的载体。在其他实例中,该方法包括向受试者施用药物组合物,该药物组合物包括编码cap的表达载体和药学上可接受的载体。cap的细胞外靶向结构域基于所治疗的癌症进行选择,例如,如表1所示。在一些实例中,受试者是人或兽医受试者。
[0176]
血液系统恶性肿瘤的实例包括白血病,包括急性白血病(例如11q23阳性急性白血病,急性淋巴细胞白血病(all),t细胞all,急性髓细胞白血病,急性髓系白血病(aml),以及成髓细胞、早幼粒细胞、粒单核细胞、单核细胞和红白血病)、慢性白血病(例如慢性髓细胞(粒细胞)白血病、慢性髓系白血病和慢性淋巴细胞白血病)、淋巴细胞白血病、真性红细胞
增多症、淋巴瘤、弥漫性大b细胞淋巴瘤、burkitt淋巴瘤、t细胞淋巴瘤、滤泡性淋巴瘤、套细胞淋巴瘤、霍奇金病、非霍奇金淋巴瘤、多发性骨髓瘤、waldenstrom巨球蛋白血症、重链疾病、骨髓增生异常综合征、毛细胞白血病和骨髓增生异常。
[0177]
实体瘤的实例包括肉瘤(例如纤维肉瘤、粘液肉瘤、脂肪肉瘤、软骨肉瘤、骨肉瘤和其他肉瘤)、滑膜瘤、间皮瘤、ewin肉瘤、平滑肌肉瘤、横纹肌肉瘤、结肠癌、结肠直肠癌、腹膜癌、食道癌、胰腺癌、乳腺癌(包括基底癌、导管癌和小叶乳腺癌)、肺癌、卵巢癌、前列腺癌、肝癌(包括肝细胞癌)、胃癌、鳞状细胞癌(包括头颈部鳞状细胞癌)、基底细胞癌、腺癌、汗腺癌、甲状腺髓样癌、甲状腺乳头状癌、嗜铬细胞瘤、皮脂腺癌、乳头状癌、乳头状腺癌、髓样癌、支气管癌、肝癌、胆管癌、绒毛膜癌、肾母细胞瘤、宫颈癌、输卵管癌,睾丸肿瘤、精原细胞瘤、膀胱癌(例如肾细胞癌)、黑色素瘤和cns肿瘤(例如神经胶质瘤、胶质母细胞瘤、星形细胞瘤、髓母细胞瘤、颅咽管瘤、室管膜瘤、松果体瘤、血管母细胞瘤、听神经瘤、少突胶质细胞瘤、脑膜瘤、成神经细胞瘤和)。实体瘤还包括肿瘤转移(例如,转移到肺、肝、脑或骨)。
[0178]
多种药学上可接受的载体(carrier)可用于本文提供的组合物中,例如,缓冲盐水等,用于将细胞或载体(vector)引入受试者。这些溶液是无菌的并且通常不含非期望物质。组合物可经灭菌。在一些实例中,组合物还包括药学上可接受的辅助物质,例如ph调节剂和缓冲剂、毒性调节剂和防腐剂,例如醋酸钠、氯化钠、氯化钾、氯化钙、乳酸钠等。这些制剂中的浓度可以变化,并且将主要基于流体体积、粘度、体重等根据所选择的特定给药模式和受试者的需要进行选择。
[0179]
待施用的组合物的精确量可由医师考虑患者(受试者)的年龄、体重、肿瘤大小、转移程度和状况的个体差异来确定。在一些实施方案中,包含表达本文所述cap的t细胞或nk细胞的药物组合物以约104至109个细胞/kg体重(例如,约104、105、106、107、108或109个细胞/kg),例如约104至106个细胞/kg、约105至107个细胞/kg、或约106至108个细胞/kg。示例性剂量为约105个细胞/kg至约109个细胞/kg,例如约106个细胞/kg、约5
×
106个细胞/kg、约107个细胞/kg、约5
×
107个细胞/kg、约108个细胞/kg、或约5
×
108个细胞/kg。修饰的t细胞或nk细胞群通常是肠胃外施用,例如静脉内施用;然而,也可以使用注射或输注至肿瘤或接近肿瘤(局部给药)或施用至腹腔。本领域技术人员可以确定合适的施用途径。
[0180]
在一些实例中,施用组合物(例如包括表达cap的t细胞或nk细胞的组合物)一次或多次,例如1、2、3、4、5、6、7、8、9或10次。该组合物可以通过静脉注射或输注施用。在一些实例中,每天、每周、每两个月或每月施用组合物。如果施用多剂,施用之间的时间可以是1、2、3、4、5、6、7、8、9、10、11、12、13、14天或更长时间。在一些非限制性实例中,组合物被配制用于静脉内施用并且多次施用。施用的数量和频率将取决于例如受试者的状况、受试者疾病的类型和严重程度等因素,尽管适当的剂量可以通过临床试验来确定。
[0181]
在一些实例中,cap修饰的t细胞或nk细胞能够在受试者体内持续存在和/或复制,导致长期持续存在,从而导致持续的肿瘤控制。在相同的实例中,向受试者施用t或nk细胞,或这些细胞的后代,在受试者体内持续至少4个月、5个月、6个月、7个月、8个月、9个月、10个月、11个月、12个月、13个月、14个月、15个月、16个月、17个月、18个月、19个月、20个月、21个月、22个月、23个月、或向受试者施用后数年。在其他实施方案中,在向受试者施用细胞后,细胞或其后代存在少于6个月、5个月、4个月、3个月、2个月或1个月,例如3周、3周、1周。
[0182]
在一个实施方案中,将cap引入细胞,例如t细胞或nk细胞,并且受试者接受细胞的
施用。在一些实施方案中,该方法包括从受试者分离t细胞或nk细胞,用编码cap的表达载体(例如慢病毒载体或逆转录病毒载体)转导或转化t细胞或nk细胞以产生修饰的t细胞或nk细胞,并将表达cap的修饰的t细胞或nk细胞施用于癌症受试者以进行治疗。t细胞或nk细胞可以是受体自体的或同种异体的(例如,分离和转化的t细胞或nk细胞不是来自被治疗的受试者)。在一些实例中,受试者可以在施用修饰的t细胞或nk细胞之前经历免疫抑制方案(例如,淋巴去除或部分淋巴去除)。免疫系统支持疗法(例如il
‑
2和/或g
‑
csf)也可以施用于受试者,例如以促进受试者中修饰细胞的扩增和/或支持嗜中性粒细胞的恢复。
[0183]
在一些实施方案中,可以通过任何方法获得包括淋巴细胞(例如pbmc)的细胞群,包括但不限于血液分离术(apheresis)。可以立即利用全部或部分细胞群,或者可以冷冻保存全部或部分细胞以备将来使用。当准备使用时,全部或部分细胞群被解冻(如果先前冷冻保存),并且t细胞或nk细胞在培养中被激活、富集和/或扩增。分离、激活和扩增t细胞或nk细胞的方法是本领域已知的(例如,wo 2018/006054和wo 2018/022646,其通过引用以其全文并入本文)。用包括cap的载体转导或转化细胞。在特定实例中,转导或转化约107‑
109个细胞(例如,约1
×
107、5
×
107、1
×
108、5
×
108或1
×
109个细胞)。转导或转化的t细胞或nk细胞可以离体扩增,并可以在扩增后以适当的剂量(例如,约106至10
12
个细胞)冷冻保存。在向受试者施用之前,将转导或转化的t细胞或nk细胞解冻(如果先前已冷冻)。在施用修饰的t细胞或nk细胞之前,受试者可以接受免疫抑制方案(例如,淋巴去除)。向受试者施用修饰的t细胞或nk细胞,例如通过输注。
[0184]
通过例如肿瘤大小、病变数量、肿瘤阶段、缓解率或其他标准等方法监测治疗疗效。在一些实例中,原发肿瘤或转移灶的大小减小(例如,如标准recist或irrecist标准所定义)表明受试者中的癌症受到抑制。在其他实例中,无进展生存期和/或总生存期(例如,1个月、3个月、6个月、9个月、12个月、18个月、2年或更长时间,例如1
‑
12个月、6
‑
18个月、1
‑
2年或更长)表明受试者的癌症受到抑制。在其他实例中,评估循环表达cap的t细胞或nk细胞的持续性、免疫细胞亚群的变化和t细胞的激活状态以及其他免疫决定因素中的一种或更多种,并在基线时评估临床结局(例如,在施用修饰细胞之前或之时)、治疗期间的不同时间点以及疾病进展时。
[0185]
在一些实例中,受试者还接受手术、化疗、放疗、免疫抑制剂和化学治疗剂中的一种或更多种治疗。示例性试剂包括但不限于烷化剂,例如氮芥(例如,苯丁酸氮芥、氯甲酸、环磷酰胺、异环磷酰胺和美法仑)、亚硝基脲(例如,卡莫司汀、福莫司汀、洛莫司汀和链脲佐菌素)、铂化合物(例如,卡铂、顺铂、奥沙利铂和bbr3464)、白消安、达卡巴嗪、氯乙胺、丙卡巴肼、替莫唑胺、噻替哌和乌拉莫司汀;抗代谢药,例如叶酸(例如,甲氨蝶呤、培美曲塞和雷替曲塞)、嘌呤(例如,克拉屈滨、氯法拉滨、氟达拉滨、巯嘌呤和硫鸟嘌呤)、嘧啶(例如,卡培他滨)阿糖胞苷、氟尿嘧啶和吉西他滨;植物生物碱,例如鬼臼(例如,依托泊苷和替尼泊苷)、紫杉烷(例如,多西他赛和紫杉醇)、长春花(例如,长春碱、长春新碱、长春地辛和长春瑞滨);细胞毒性/抗肿瘤抗生素,例如蒽环类抗生素(例如,柔红霉素、多柔比星、表柔比星、伊达比星、米托蒽醌和戊柔比星)、博来霉素、羟基脲和丝裂霉素;拓扑异构酶抑制剂,例如拓扑替康和伊立替康;单克隆抗体,例如阿仑单抗、贝伐珠单抗、西妥昔单抗、吉妥珠单抗、利妥昔单抗、帕尼单抗、阿替利珠单抗、阿维单抗、伊匹木单抗、奥法木单抗、纳武利尤单抗、帕博利珠单抗、利妥昔单抗、度伐单抗和曲妥珠单抗;光敏剂,例如氨基乙酰丙酸、氨基乙酰
technologies)、10%胎牛血清(life technologies)和1%青霉素
‑
链霉素(life technologies)中培养。对于瞬时转染,在成像前24小时,使用nucleofector kit v(lonza,货号vca
‑
1003),program x
‑
001,用2μg dna转染1
×
106个jurkat细胞。在成像之前,将jurkat细胞离心并重悬于成像缓冲液(20mm hepes ph 7.2、137mm nacl、5mm kcl、0.7mm na2hpo4、6mm d
‑
葡萄糖、2mm mgcl2、1mm cacl2、1%bsa)。
[0194]
k562cd19细胞系的生成:全长cd19的cdna购自invitrogen并克隆到msgv逆转录病毒骨架中。如下在瞬时逆转录病毒和慢病毒生产下所述制备含有逆转录病毒的上清液。用该上清液转导k562细胞(atcc),然后通过流式细胞术对表达cd19的细胞进行分选,以获得均匀表达高水平cd19的k562细胞群。
[0195]
瞬时逆转录病毒和慢病毒产生:为了瞬时产生逆转录病毒(cd19)和慢病毒(28z car和cap),293t细胞用表达car或cap的病毒载体以及包装质粒pspax2(addgene)和编码病毒包膜蛋白pvsv
‑
g(addgene)的质粒转染,使用lipofectamine 2000(invitrogen)。将转染的细胞在不含抗生素的dmem培养基(dmem,10%热灭活fbs)中在37℃下孵育6
‑
8小时。然后将用于转染的培养基更换为新鲜的dmem培养基(dmem,10%热灭活fbs,1%penn
‑
strep),并将细胞再孵育36
‑
48小时。从培养皿中取出含有逆转录病毒或慢病毒的上清液并离心以除去细胞碎片并用于转导实验。
[0196]
原代人t细胞的细胞培养和慢病毒转导:原代人外周血t细胞获自美国国立卫生研究院血库,没有供体标识符。通过ficoll密度梯度离心分离单核细胞。分离的细胞以1
×
106个细胞/ml的浓度重悬于含50ng/ml okt3和300iu/ml il
‑
2的t细胞培养基中(第0天)。细胞在75cm2培养瓶中培养,在37℃和5%co2下直立培养。在刺激的第2天,使用293t细胞瞬时产生的慢病毒上清液转导细胞。转导通过在28℃下以2000
×
g在纤维连接蛋白(retronectin)包被的板上对细胞进行2小时的自旋接种进行。在第3天重复慢病毒转导。细胞在37℃和5%co2中培养6天,处于指数生长期。在第6天,如下所述通过流式细胞术评估cd3、cd4、cd8和cd19的表达。
[0197]
活细胞成像:包被抗体的盖玻片的制备先前已有描述(bunnell et al.,sci.stke 2003:pl8,2003)。jurkat细胞被添加到hit3a或okt4抗体包被的8孔盖玻片室(lab
‑
tek,thermo fisher)中,并在成像缓冲液中成像。表达halo标记构建体的jurkat细胞在37℃下用100nm janelia fluor halo
‑
647配体标记30分钟。在完全培养基中洗涤3次后对细胞进行成像,然后重悬在成像缓冲液中。用于活细胞成像的所有腔室均包含成像缓冲液。活细胞的tirf图像使用nikon ti
‑
e倒置显微镜采集,使用100
×
sr apochromat tirf物镜(1.49数值孔径)和andor ixon ultra 897em电荷耦合器件相机(512
×
512像素,16μm像素)。以3秒/帧的速度采集延时图像
[0198]
免疫荧光成像:使jurkat t细胞在37℃下在成像缓冲液中粘附在hit3a抗体包被的盖玻片上2分钟,然后在4%(重量/体积)pfa溶液(电子显微镜科学)中固定30分钟。将样品在0.1%triton
‑
x
‑
100中透化3分钟,然后在由10%fbs(sigma
‑
aldrich)、0.01%叠氮化钠(sigma
‑
aldrich)、1
×
pbs组成的封闭溶液中在室温(rt)下孵育1小时。在1
×
pbs中洗涤3次后,细胞在rt下用封闭溶液(20μg/ml)中的抗磷酸酪氨酸或抗ptcr抗体染色1小时。细胞在pbs中洗涤3次,并使用tirf显微镜成像,如上详述。
[0199]
流式细胞术:在分离和如上所述用okt3和il
‑
2刺激后的第6天,通过流式细胞术评
估原代人pbmc上的细胞表面标志物。细胞用抗cd4
‑
apc、抗cd8
‑
fitc、抗cd3
‑
percp和抗cd19
‑
pe(ebiosciences)染色,以评估t细胞的百分比和特征。对于car或cap检测,添加生物素标记的多克隆山羊抗小鼠f(ab)2抗体(抗fab,jackson immunoresearch)以检测cd19 scfv。生物素标记的正常多克隆山羊igg抗体(jackson immunoresearch)作为同种型对照。将细胞在4℃下孵育25分钟并洗涤一次。将细胞悬浮在fac缓冲液(1
×
pbs、10%fbs、0.02%叠氮化钠)中并用正常小鼠igg(invitrogen)封闭。然后将细胞用藻红蛋白(pe)标记的链霉亲和素(bd pharmingen)染色。在bd lsrfortessa cell analyzer(bd biosciences)上进行流式细胞术采集,并使用flowjo(treestar,inc.)进行分析。
[0200]
il
‑
2和ifn
‑
γ酶联免疫吸附试验(elisa):将靶k562或k562cd19细胞洗涤并以1
×
106个细胞/ml悬浮在不含il
‑
2的t细胞培养基中。将每种靶细胞类型的1
×
105个靶细胞加入96孔圆底板(corning)的孔中。将效应t细胞培养物洗涤并以1
×
106个细胞/ml悬浮在不含il
‑
2的t细胞培养基中。在圆底96孔板的孔中,1
×
105个效应t细胞与1
×
10个靶细胞以200μl的总体积混合。此外,制备仅含有t细胞的孔。作为阳性对照,用板结合的抗cd3(10μg/ml)和抗cd28(1μg/ml)刺激t细胞。将板在37℃下孵育18
‑
20小时。孵育后,收集上清液,然后按照生产商的说明(r&d systems)进行il
‑
2或ifnγelisa测定。
[0201]
基于荧光素酶的杀伤测定:如图所示,将转导或未转导的pbmc与稳定表达荧光素酶的nalm6或nalm6 cd19敲除肿瘤细胞共培养,比例为5:1或1:1。4小时后,通过加入steady glo试剂(promega)检测发光。来自仅目标孔(max cps)和仅目标孔加1%tween
‑
20(min cps)的发光用于确定测定范围。特异性裂解百分比计算为:1
‑
(样品cps
‑
min cps)/(max cps
‑
min cps)。
[0202]
实施例2
[0203]
基于lat的cd4和cd19嵌合衔接蛋白的表征
[0204]
构建基于lat的嵌合衔接蛋白(cap)(图1a)。表达tcrζ
‑
emerald的e6.1jurkat t细胞在抗cd3抗体(hit3)包被的盖玻片上被激活。表达cd4
‑
lat和grb2
‑
emerald或cd4
‑
cap
‑
gfp的e6.1 jurkat t细胞在抗cd4抗体(okt4)包被的盖玻片上被激活,当细胞被激活时,观察到定义为微团簇的结构。微团簇不存在于抗cd4激活的cd4
‑
lat表达细胞中(图1c),但在表达cd4
‑
cap
‑
gfp的细胞中观察到(图1d),表明含有lat和zap70
‑
kd的嵌合分子可用于激活t细胞信号传导。
[0205]
表达cd4
‑
cap
‑
gfp的e6.1 jurkat t细胞在包被抗cd4抗体(okt4)的盖玻片上激活,固定并用抗磷酸酪氨酸(py)抗体(4g10)染色。py信号与cd4
‑
cap
‑
gfp信号共定位,表明这些微团簇是活动信号的位点(图2a)。cd4
‑
cap表达细胞没有在包被抗cd45或抗cd43抗体的盖玻片上形成微团簇(图2b),表明cd4
‑
cap
‑
gfp激活对cd4连接具有特异性。
[0206]
表达tcrζ
‑
halo和cd4
‑
cap
‑
gfp或zap70
‑
halo和cd4
‑
cap
‑
gfp的e6.1 jurkat在包被抗cd4抗体(okt4)的盖玻片上激活。tcrζ
‑
halo(图3a)和zap70
‑
halo(图3b)未定位于cd4
‑
cap
‑
gfp微团簇,表明cap的激活与tcr复合体无关。tcrζ和zap
‑
70通常被招募到抗cd3刺激下游的微团簇中,如图1所示。
[0207]
表达cd4
‑
cap
‑
gfp和plcγ1
‑
halo(图4a)、slp76
‑
halo(图4b)或grb2
‑
halo(图4c)的e6.1 jurkat t细胞在抗包被cd4抗体(okt4)的盖玻片上被激活。cd4
‑
cap
‑
gfp在抗cd4刺激后被招募到微团簇中。plcγ1
‑
halo、slp76
‑
halo和grb2
‑
halo信号蛋白也定位于cd4
‑
cap
‑
gfp微团簇。这表明lat相关信号复合体是在cap激活的t细胞中形成的。
[0208]
还产生抗cd19
‑
scfv
‑
lat
‑
zap70 kd构建体(图5a)。表达cd19
‑
lz
‑
gfp和grb2
‑
scarlet的e6.1细胞与raji b细胞形成缀合物(图5b)。包含cd19
‑
lz
‑
gfp和grb2
‑
scarlet的微团簇在缀合物中心附近形成,显示t细胞激活。
[0209]
实施例3
[0210]
cd19
‑
cap分子的进一步评价
[0211]
用cap1、cap2和cap3转导的pbmc(图7)在与nalm6和k652 cd19细胞以1:1的比例(图8a)共培养后释放大量干扰素γ,但在nalm6 cd19 ko和不表达cd19的k562细胞中也显示出高水平的抗原非依赖性细胞因子释放。相比之下,表达cap4的pbmc显示出低基础但高抗原诱导的干扰素γ释放,类似于41bbz对照。用cap2和cap4转导的pbmc在与k562 cd19表达细胞共培养后释放白细胞介素
‑
2,证明功能激活(图8b)。表达cap1、cap2、cap3和cap4的pbmc对nalm6 cd19 急性淋巴细胞白血病细胞显示出与41bbz car阳性对照相似的细胞溶解活性,其效应物:靶标比为5:1和1:1(图9)。
[0212]
实施例4
[0213]
cap疗效的体内评价
[0214]
本实施例描述了可用于在小鼠异种移植模型中体内评价一种或更多种公开的cap的疗效的方法。然而,本领域技术人员将理解偏离这些特定方法的方法也可用于检测cap的体内疗效。
[0215]
向nsg小鼠静脉或皮下注射表达荧光素酶的人淋巴瘤或白血病细胞系(包括naml6白血病细胞系),然后接受经过基因改造以表达cap构建体的人t细胞处理。空白转导的t细胞(例如设计为不起作用或对无关靶标具有特异性的构建体)用作阴性对照。一种或更多种经证实可对抗靶标恶性肿瘤的car用作阳性对照。使用xenogen ivis lumina(caliper life sciences)检测白血病负荷。
[0216]
实施例5
[0217]
用表达cd19
‑
cap的t细胞治疗白血病
[0218]
本实施例描述了可用于用cd19
‑
cap转导的t细胞治疗患有白血病的受试者的方法。然而,本领域技术人员将理解,偏离这些特定方法的方法也可用于成功治疗患有白血病的受试者。此外,类似的方法可用于治疗患有其他表达cap的t细胞和其他癌症的受试者。
[0219]
患有白血病(例如急性淋巴细胞白血病)的受试者接受血液分离术以收集外周血单核细胞。t细胞用包括cd19
‑
cap的逆转录病毒载体激活和转导,例如本文所述的那些(例如,seq id no:5
‑
10和15
‑
50)。转导的t细胞被扩增。在用转导的t细胞输注前2
‑
14天,受试者出现化疗诱导的淋巴耗竭。
[0220]
实施例6
[0221]
用表达cd19
‑
cap的nk细胞治疗b细胞淋巴瘤
[0222]
本实施例描述了可用于用cd19
‑
cap转导的nk细胞治疗患有b细胞淋巴瘤的受试者的方法。然而,本领域技术人员将理解偏离这些特定方法的方法也可用于成功治疗患有b细胞淋巴瘤的受试者。此外,类似的方法可用于治疗患有其他表达cap的nk细胞和其他癌症的受试者。
[0223]
患有b细胞淋巴瘤的受试者接受血液分离术以收集外周血单核细胞。nk细胞(例
如,cd56阳性/cd3阴性细胞)通过使用免疫磁珠方法的阳性和/或阴性选择从pbmc中分离。用包括cd19
‑
cap的逆转录病毒载体转导,例如本文所述的那些(例如,seq id no:5
‑
10和15
‑
50)。可将转导的nk细胞冷冻保存备用,或可配制用于施用于受试者(例如,在药学上可接受的载体中)。向受试者静脉内施用包括106至10
12
个扩增的nk细胞的组合物。
[0224]
鉴于可以应用本公开的原理的许多可能的实施方案,应当认识到,所示出的实施方案仅是实例并且不应被视为限制本发明的范围。相反,本发明的范围由以下权利要求限定。因此,我们要求将落入这些权利要求的范围和精神内的所有内容作为我们的发明。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。