1.本发明涉及体外诊断技术领域,具体涉及一种微流控芯片。
背景技术:
2.微流控芯片是微流控技术实现的主要平台,可以把生物、化学、医学分析过程的样品制备、反应、分离、检测等基本操作单元集成到一块很小的芯片上。通过微通道自动完成分析全过程,用以实现常规化学或生物实验室的各种功能。微流控芯片具有体积轻巧、使用样品及试剂量少,且反应速度快、可大量平行处理及可即用即弃等优点,在生物、化学、医学等领域有着的巨大潜力,近年来已经发展成为一个生物、化学、医学、流体、电子、材料、机械等学科交叉的崭新研究领域。
3.目前的微流控芯片一般采用盖片和基片键合的方式形成相应的流动区和反应区,对密封性技术要求极高,一旦键合的密封效果不好,就会出现液体样本泄露的问题,同时,微流控芯片涉及不同疾病标志物的检测,根据不同样本的检测需要,可能需要不同的反应时间,而且现有的微流控芯片由于其固有的结构特点,样本在微通道中的反应时间有限,这就存在当检测某些疾病标志物时,检测范围较窄的问题。
技术实现要素:
4.本发明的目的是针对现有技术的不足,提供一种微流控芯片,用于解决上述背景技术中提出的技术问题。
5.为实现上述目的,本发明的技术方案是这样实现的,一种微流控芯片,包括由基片和盖片围合形成的微通道,微通道通过样本加样孔注入样本流体,所述微通道的顶壁高度低于基片和盖片接触面的高度,样本流体在微通道的毛细作用力下向微通道的出口流动。
6.具体的,所述微通道通过向上的连接通道与扩展孔连通。
7.具体的,所述微通道通过倾斜向上的连接通道与扩展孔连通。
8.具体的,沿基片长度方向设置有凹槽,盖片下表面向凹槽方向凸出作为微通道的顶壁,与凹槽的底壁配合形成微通道。
9.具体的,所述扩展孔沿平行于微通道的长度方向延伸;或者所述扩展孔沿平行于微通道长度的方向间隔设置。
10.具体的,所述扩展孔单独设置在微通道侧边的一侧,或者同时位于微通道两侧边。
11.具体的,所述微流控芯片包括分别与微通道两端连通的进样区和废液区,所述进样区通过样本加样孔和缓冲液加样孔分别注入样本流体和缓冲液。
12.具体的,所述样本加样孔位于缓冲液加样孔和微通道之间。
13.具体的,所述微通道的出口连接废液区,所述废液区通过样本出口与外界连通,样本出口内嵌有可在样本出口内滑动的吸水性材料,样本出口至少具有两个端部,一个端部贴近微通道出口,另一个端部远离微通道出口。
14.具体的,所述扩展孔由盖片上开设的凹槽和基片围合而成;或者由基片上开设的
凹槽和盖片围合而成;或者所述扩展孔由盖片上开设的凹槽和基片上开设的凹槽共同围合而成。
15.通过上述技术方案得到的一种微流孔芯片,其有益效果是:1、有效防止微通道侧面漏液情况,使检测结果更精确,减少无效检测率与报废率。
16.2、倾斜的连接通道和扩展孔有利于排气,避免气泡堵塞微通道,使液体流动更顺畅。
17.3、通过样本加样孔和缓冲液加样孔的双孔设置,在微通道内反应完成后,缓冲液将推动反应废液快速流到废液区,缩减了整个微流控芯片的反应时间,同时可以对微通道内残留的荧光溶液进行冲洗,避免残留液体对检测结果造成干扰。
18.4、在样本出口设置可移动的吸水性材料,当流体样本在微通道发生反应时,吸水性材料与微通道断开,样本流体会滞留在微通道内,形成液相反应池,不仅可以增加反应时间,又使干式荧光反应转化成液相荧光反应,极大地增加反应的充分性,并提高检测结果的精密性,当反应完成后,移动吸水性材料,使吸水性材料与微通道出口连接,废液将被吸水性材料吸收到废液区,避免废液影响检测结果,吸水性材料的移动可根据样本于微通道内的反应情况进行控制,这种反应时间可控的方法,可进一步提高不同产品反应时间的灵活性,同时可以加快反应废液快速流至废液区,缩短检测时间。
附图说明
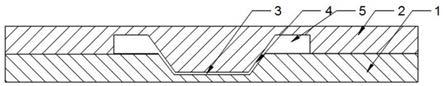
19.图1是本发明所述微流控芯片的其中一个实施例的剖面图。
20.图2是本发明所述微流控芯片的平面结构示意图。
21.图3是本发明所述微流控芯片的另一个实施例的剖面图。
22.图4是本发明所述微流控芯片的再一个实施例的剖面图。
23.图中,基片1;盖片2;微通道3;连接通道4;扩展孔5;进样区6;废液区7;样本出口8;吸水性材料9;样本加样孔10;缓冲液加样孔11;荧光标记区3a;质控区3b;检测区3c。
具体实施方式
24.需要说明的是,在不冲突的情况下,本发明中的实施例及实施例中的特征可以相互组合。
25.在本发明的描述中,需要理解的是,术语“中心”、“纵向”、“横向”、“上”、“下”、“前”、“后”、“左”、“右”、“竖直”、“水平”、“顶”、“底”、“内”、“外”等指示的方位或位置关系为基于附图所示的方位或位置关系,仅是为了便于描述本发明和简化描述,而不是指示或暗示所指的装置或元件必须具有特定的方位、以特定的方位构造和操作,因此不能理解为对本发明的限制。此外,术语“第一”、“第二”等仅用于描述目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”等的特征可以明示或者隐含地包括一个或者更多个该特征。在本发明的描述中,除非另有说明,“多个”的含义是两个或两个以上。
26.在本发明的描述中,需要说明的是,除非另有明确的规定和限定,术语“安装”、“相连”、“连接”、“设置”应做广义理解,例如,可以是固定连接,也可以是可拆卸连接,或一体地连接;可以是机械连接,也可以是电连接;可以是直接连接,也可以通过中间媒介间接连接,
可以是两个元件内部的连通。对于本领域的普通技术人员而言,可以通过具体情况理解上述术语在本发明中的具体含义。
27.本发明提供了一种微流控芯片,包括由基片1和盖片2围合形成的具有限定高度和宽度的微通道3,样本流体可在微通道3的毛细作用力下向微通道3的出口流动,所述微通道3的顶壁高度低于基片1和盖片2接触面的高度。
28.下面结合实施例及附图来对本发明进行详细说明。
29.图1所示的是本发明第一实施例的微流控芯片剖视图,所述微通道3由盖片2下表面和基片1上表面围合而成,所述基片1沿基片1长度方向设置有凹槽,盖片2下表面向凹槽方向凸出作为微通道3的顶壁,与凹槽的底壁配合形成可供样本流体流过并发生反应的微通道3。
30.如图2所示,所述微通道3内沿样本流体流动方向依次间隔设置有荧光标记区3a、检测区3c和质控区3b。
31.样本液体从进样孔注入芯片后在微通道3的毛细作用力下向微通道3出口方向流通,因微通道3的顶壁高度低于基片1和盖片2接触面的高度,只要保证样本液体的注入量,即可有效防止微通道3侧面漏液情况,使检测结果更精确,减少无效检测率与报废率,同时降低了对微流控芯片键合的工艺要求。
32.图3所示,所述微流控芯片中还包括扩展孔5,所述微通道3通过向上的连接通道4与扩展孔5连通,扩展孔5的高度高于微通道3的高度,所述扩展孔5由盖片2上开设的凹槽和基片1围合而成;或者由基片1上开设的凹槽和盖片2围合而成;或者由盖片2上开设的凹槽和基片1上开设的凹槽共同围合而成。
33.扩展孔5的设置可以减少样本流体流动过程中的气泡,所述扩展孔5既可以单独设置在微通道3侧边的一侧,也可以同时位于微通道3两侧边;既可以沿微通道3长度方向间隔设置,也可以连续设置。
34.图4所示的是本发明另一个较佳的实施例,与图3不同的是,形成微通道3的基片1上的凹槽和盖片2上的凸出部分横截面为梯形,即所述扩展孔5通过向上倾斜的连接通道4与扩展孔5连接,可以更好的排出样本流体流动过程中产生的气泡。
35.如图2所示,上述实施例中的芯片还包括分别与微通道3两端连通的进样区6和废液区7,进样区6、废液区的高度与微通道3高度一致,所述进样区6通过盖片2顶面设置的样本加样孔10和缓冲液加样孔11注入样本流体和缓冲液,其中样本加样孔10位于缓冲液加样孔11和微通道3之间,所述进样区6的宽度大于微通道3的宽度,进样区6和微通道3通过宽度逐渐收紧的弧形连接部连接。
36.样本流体反应完后,向缓冲液加入孔内加入缓冲液,缓冲液推动反应废液快速流到废液区7,可以冲刷微通道3内反应后的残留荧光溶液,避免微通道3内的残留液体对检测结果造成干扰,同时缩减了整个芯片检测操作的总体时间,满足poct即时检测、反应时间较快的市场需求。
37.所述废液区7通过基片1上设置的样本出口8与外界连通,样本出口8内嵌有可在样本出口8内滑动的吸水性材料9,样本出口8至少具有两个端部,一个端部贴近微通道3出口,另一个端部远离微通道3出口,分别使吸水性材料9与微通道3出口连接和远离微通道3出口。
38.所述吸水性材料9可采用聚酯纤维、吸水性树脂、吸水明胶、造纸木浆或其他具有吸水性特点的材料,所述吸水性材料9的规格可根据加入芯片的待检样本注入量进行调整,整体上保持吸水性材料9的吸水能力为待检样本注入量的2
‑
4倍,以避免吸水性材料9饱和,从而导致待检样本从样本出口8中泄露。
39.加样前,确认吸水性材料9位于样本出口8远离微通道3的一端,向样本加样孔10内加入定量的样本流体后,样本流体由加样区流入微通道3,并在毛细作用下向微通道3出口一端移动,此时缺少吸水性材料9的连接,样本流体滞留在微通道3内进行充分反应,待反应完全后,手动将吸水性材料9滑动至与微通道3出口连接,吸水性材料9与样本流体接触,将流入废液区7内的样本流体完全吸收,配合光学分析仪进行检测。
40.d二聚体(d
‑
dimer)主要用于血栓性疾病的检测,下面以定量检测血浆、全血中的d二聚体含量为例对本发明第二实施例中的微流控芯片和现有的微流控芯片进行对比实验。
41.1、材料准备 改进后d二聚体(d
‑
dimer)微流控芯片a与改进前的d二聚体(d
‑
dimer)微流控芯片b(相对于微流控芯片b中吸水性材料位于废液区中固定不动,微流控芯片a的废液区通过样本出口与外界连通,吸水性材料可滑移的嵌入样本出口内)均由山东迈微生物科技有限公司生产;d二聚体(d
‑
dimer)临床样本s1、s2,由相关医院获得;山东迈微生物科技有限公司生产的荧光免疫分析仪,计时器(如秒表)和移液器。
42.2、包被位点包被点二位于检测区3c,包被有d
‑
dimer抗体。
43.包被点四位于质控区3b,包被有二抗;荧光标记区3a固定有干燥的d
‑
dimer荧光标记配对抗体。
44.3、检测方法3.1改进后d二聚体(d
‑
dimer)微流控芯片改进后d二聚体(d
‑
dimer)微流控芯片a平放在实验台上,加样前吸水性材料9与微通道3为断开状态,将样本加入到微流控芯片样本加样孔10中,计时2min后,反方向移动吸水性材料9与微通道3连接,并在缓冲液加样孔11中加入15
µ
l缓冲液,3min后,芯片用荧光免疫分析仪进行判读,记录d
‑
dimer样本的检测结果。平行测定样本s1、s2,每个样本重复检测5次,计算各样本检测结果均值与原浓度值的相对偏差,并计算各样本检测结果的变异系数(cv)。
45.3.2改进前d二聚体(d
‑
dimer)微流控芯片 改进前d二聚体(d
‑
dimer)微流控芯片b平放在实验台上,将样本加入到微流控芯片中,5min后,芯片用荧光免疫分析仪进行判读,记录d
‑
dimer样本的检测结果。平行测定样本s1、s2,每个样本重复检测5次,计算各样本检测结果均值与原浓度值的相对偏差,并计算各样本检测结果的变异系数(cv)。
46.4、结果如表1所示,改进后d
‑
dimer微流控芯片的检测结果与原浓度值的相对偏差均不超过
±
5%,且cv均小于5%,改进前d
‑
dimer微流控芯片的检测结果与原浓度值的相对偏差均不超过
±
10%,且cv均小于10%,改进后的偏差与cv小于改进前的,表明改进后芯片检测结果更
精准、更均一。从检测点信号值可以看出,改进后的荧光信号值高于改进前的荧光信号值,表明反应更充分;表1 微流控芯片改进前后的样本检测结果上述技术方案仅体现了本发明技术方案的优选技术方案,本技术领域的技术人员对其中某些部分所可能做出的一些变动均体现了本发明的原理,属于本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。