生物合成糖蛋白群体
1.相关申请的交叉引用
2.本技术要求以下申请的权益:2020年4月17日提交的美国序列号63/011,959;2020年4月17日提交的美国序列号63/011,974;2020年4月17日提交的美国序列号63/011,985;2020年4月17日提交的美国序列号63/011,993;2020年4月17日提交的美国序列号63/011,991;2020年5月27日提交的美国序列号63/030,765;2020年5月27日提交的美国序列号63/030,787;2020年5月27日提交的美国序列号63/030,808;2020年5月27日提交的美国序列号63/030,823;2020年5月27日提交的美国序列号63/030,829;2020年7月29日提交的美国序列号63/058,354;2020年7月29日提交的美国序列号63/058,332;2020年7月29日提交的美国序列号63/058,369;2020年7月29日提交的美国序列号63/058,345;2020年7月29日提交的美国序列号63/058,351;2021年1月28日提交的美国序列号63/142,981;2021年1月28日提交的美国序列号63/142,982;2021年1月28日提交的美国序列号63/142,983;2021年1月28日提交的美国序列号63/142,985以及2021年1月28日提交的美国序列号63/142,987,这些申请中的每一篇申请全文以引用方式并入本文。
3.以电子方式提交的参考序列表
4.本技术包含序列表,该序列表作为ascii格式的序列表经由efs-web以电子方式递交,文件为
″
14620-451-228_seq_listing
″
并且创建日期为2021年4月3日,并且大小为343,588字节经由efs-web提交的该序列表是本说明书的一部分并且全文以引用方式并入本文。
1.技术领域
5.本文提供了具有增强的抗体依赖性细胞毒性(adcc)和增强的补体依赖性细胞毒性(cdc)的抗体。
2.
背景技术:
6.治疗性抗体可结合在免疫效应细胞(诸如自然杀伤(nk)细胞和巨噬细胞)上表达的fc受体,从而经由抗体依赖性细胞毒性(adcc)产生抗肿瘤活性。治疗性抗体还可活化补体依赖性细胞毒性(cdc)并实现抗肿瘤功效。本领域中需要具有增强的adcc和增强的cdc效应子两种功能的抗体。
3.
技术实现要素:
7.在一个方面,本文提供了一种抗体群体,其中少于80%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基;并且其中抗体群体包括fc区包含k338a和t437r突变或k248e和t437r突变(re突变)的抗体,其中氨基酸残基编号根据eu编号系统。在一些实施方案中,本文提供了一种抗体群体,该抗体群体包含k338a和t437r突变或k248e和t437r突变(re突变),其中少于80%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
8.在一些实施方案中,少于70%的经由其n297残基共价连接至抗体群体的低聚糖包
含核心岩藻糖残基。在一些实施方案中,少于60%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。在一些实施方案中,少于50%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。在一些实施方案中,少于40%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。在一些实施方案中,少于30%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。在一些实施方案中,少于20%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。在一些实施方案中,少于10%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
9.在一些实施方案中,通过在宿主细胞中表达编码抗体或其片段的多核苷酸来产生抗体,该宿主细胞不足以将岩藻糖添加到连接至抗体的低聚糖。
10.在一些实施方案中,宿主细胞具有降低的gdp-甘露糖4,6-脱水酶(gmd)活性或降低的α-1,6岩藻糖基转移酶活性。
11.在一些实施方案中,抗体群体具有增强的抗体依赖性细胞毒性(adcc)和增强的补体依赖性细胞毒性(cdc)两者。在一些实施方案中,抗体是igg1。
12.在一些实施方案中,抗体与hla-g结合。在一些实施方案中,抗体与cd37结合。在一些实施方案中,抗体与gprc5d结合。在一些实施方案中,抗体与klk2结合。在一些实施方案中,抗体与psma结合。在一些实施方案中,抗体与cd3结合。在一些实施方案中,抗体与bcma结合。
13.在一些实施方案中,抗体是单特异性抗体。在其他实施方案中,抗体是多特异性抗体(诸如psma
×
cd3双特异性抗体)。
14.在另一方面,本文提供了一种抗体群体,其中少于80%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基;并且其中抗体群体包括在其fc区中具有一个或多个突变以用于增加抗体的cdc活性的抗体。
15.在另一方面,本文提供了一种抗体群体,该抗体群体包括用于增加抗体的adcc活性的第一构件和用于增加抗体的cdc活性的第二构件。
16.在又一方面,本文提供了一种药物组合物,该药物组合物包含本文提供的抗体群体和药学上可接受的赋形剂。在另一方面,本文提供了一种药物组合物,该药物组合物包含抗体群体,其中少于80%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基;并且其中抗体群体包括在其fc区中具有一个或多个突变以用于增加抗体的cdc活性的抗体和药学上可接受的赋形剂。在另一方面,本文提供了一种药物组合物,该药物组合物包含:(a)抗体群体,该抗体群体包括用于增加抗体的adcc活性的第一构件和用于增加抗体的cdc活性的第二构件;和(b)药学上可接受的赋形剂。
17.在又一方面,本文提供了一种制备抗体群体的方法,该方法包括在宿主细胞中表达编码抗体或其片段的多核苷酸,该宿主细胞不足以将岩藻糖残基添加到经由n297残基连接至抗体的低聚糖,其中抗体群体包括fc区包含k338a和t437r突变或k248e和t437r突变(re突变)的抗体。
18.在一些实施方案中,宿主细胞具有降低的α-1,6岩藻糖基转移酶活性。在一些实施方案中,宿主细胞具有降低的gdp-甘露糖4,6-脱水酶活性。在一些实施方案中,编码α-1,6岩藻糖基转移酶的基因突变,以低于正常水平表达,或在宿主细胞中敲除。在一些实施方案中,编码gdp-甘露糖4,6-脱水酶的基因突变,以低于正常水平表达,或在宿主细胞中敲除。
19.在另一方面,本文提供了一种制备抗体群体的方法,该方法包括用于在抗体群体的fc区中引入k338a和t437r突变或k248e和t437r突变(re突变)的步骤;以及用于产生在经由n297残基连接至抗体的低聚糖中具有减少量的核心岩藻糖的抗体群体的步骤。
20.在另一方面,本文提供了一种制备抗体群体的方法,该方法包括执行以下功能的步骤:在宿主细胞中表达编码抗体或其片段的多核苷酸,该宿主细胞不足以将岩藻糖残基添加到经由n297残基连接至抗体的低聚糖,其中抗体群体包括fc区包含k338a和t437r突变或k248e和t437r突变(re突变)的抗体。
21.在另一方面,本文提供了一种制备抗体群体的方法,该方法包括用于执行以下功能的步骤:在抗体群体的fc区中引入k338a和t437r突变或k248e和t437r突变(re突变)的步骤;以及用于执行以下功能的步骤:产生在经由n297残基连接至抗体的低聚糖中具有减少量的核心岩藻糖的抗体群体。
22.在又一方面,本文提供了一种治疗受试者的疾病或障碍的方法,该方法包括向受试者施用本文提供的抗体群体。在一些实施方案中,抗体与抗原结合,并且其中疾病或障碍与抗原相关。在一些实施方案中,抗原是hla-g。在一些实施方案中,抗原是cd37。在一些实施方案中,该抗原是gprc5d。在一些实施方案中,该抗原是klk2。在一些实施方案中,该抗原是psma。在一些实施方案中,该抗原是cd3。在一些实施方案中,该抗原是bcma。在一些实施方案中,疾病或障碍为实体瘤癌症。在一些实施方案中,疾病或障碍选自:肾腺、胰腺或肺腺癌、非小细胞肺癌和卵巢癌。
23.在另一方面,本文提供了一种治疗受试者的疾病或障碍的方法,该方法包括向受试者施用抗体群体,其中少于80%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基;并且其中抗体群体包括在其fc区中具有一个或多个突变以用于增加抗体的cdc活性的抗体。
24.在另一方面,本文提供了一种治疗受试者的疾病或障碍的方法,该方法包括向受试者施用:(a)抗体群体,该抗体群体包括用于增加抗体的adcc活性的第一构件和用于增加抗体的cdc活性的第二构件;和(b)药学上可接受的赋形剂。
25.在又一方面,本文提供了一种调节宿主的免疫力的方法,该方法包括向宿主施用本文提供的抗体群体。在另一方面,本文提供了一种调节宿主的免疫力的方法,该方法包括向宿主施用抗体群体,其中少于80%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基;并且其中抗体群体包括在其fc区中具有一个或多个突变以用于增加抗体的cdc活性的抗体。在另一方面,本文提供了一种调节宿主的免疫力的方法,该方法包括施用抗体群体:该抗体群体包括用于增加抗体的adcc活性的第一构件和用于增加抗体的cdc活性的第二构件。
4.附图说明
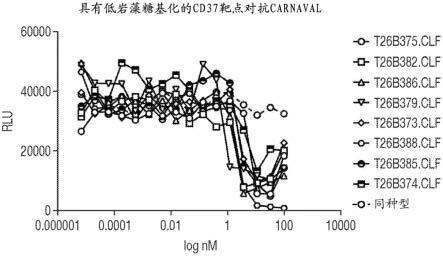
26.图1a、图1b、图1c、图1d、图1e、图1f、图1g和图1h描绘了具有低岩藻糖基化(图1a和图1b)、具有xencor突变(图1c和图1d)、具有re突变(图1e和图1f)以及具有低岩藻糖基化和re突变(图1g和1h)的不同类型的抗cd37抗体的对抗表达高水平的cd37(carnaval,图1a、图1c、图1e和图1g)和低水平的cd37(jeko-1,图1b、图1d、图1f和图1h)的靶细胞的cdc活性。如所指出的那样将靶细胞与滴定浓度的抗体一起温育30分钟。然后将幼兔血清添加到混合物
中至10%的最终浓度,以提供补体组分源。温育4小时后,通过添加cell titer-glo试剂(promega)并测量所得发光来测量细胞活力,并以相对发光单位(rlu)报告。
27.图2描绘了具有低岩藻糖基化的野生型和具有re突变的抗gprc5d抗体的对抗h929靶细胞的cdc活性。如所指出的那样将靶细胞与滴定浓度的抗体一起温育30分钟。然后将幼兔血清添加到混合物中至10%的最终浓度,以提供补体组分源。温育4小时后,通过添加cell titer-glo试剂(promega)并测量所得发光来测量细胞活力,并以相对发光单位(rlu)报告。
28.图3a、图3b、图3c、图3d和图3e示出了利用pbmc对vcap细胞的通过klk2抗体介导的体外adcc动力学杀伤。简而言之,将用nuclight red(essen bioscience)稳定转染的vcap细胞以每孔10,000个细胞接种在384孔板(perkin elmer viewplate)中的透明培养基(rpmi 1641 10%fbs,thermo fisher scientific)中,以允许细胞过夜粘附。用刚解冻的pbmc(hemcare,pb009c-3)进行adcc测定。对于pbmc作为效应细胞而言,每孔效应细胞与靶细胞的比率为34∶1。测试最终浓度在100nm至0.01nm范围的klk2抗体。在将效应细胞和抗体添加到靶细胞之后,在s3仪器(essen bioscience)下进行实时成像。用软件定量每个孔的总红色积分信号。基于一式四份的值,通过软件和prism(graphpad software)进行数据分析。将细胞杀伤的百分比计算为:(1-klk2 mab/无mab对照)
×
100%。
29.图4示出了在48小时通过pbmc对vcap的体外adcc剂量应答杀伤。在将效应细胞和抗体添加到靶细胞之后48小时生成剂量应答曲线。
30.图5a和图5b描绘了抗hla-g抗体mhgb732和mhgb738以及它们的具有低岩藻糖基化、具有re突变以及具有低岩藻糖基化和re突变的相应对应物的对抗jeg-3和rerf-lc-ad-1细胞的adcc活性。将溶解百分比与triton-x 100洗涤剂对jeg-3或rerf-lc-ad-1细胞的最大溶解进行比较,并且计算为(样品值-单独的靶标值)/(最大值-单独的靶标值)
×
100%。
31.图5c和图5d描绘了抗hla-g抗体mhgb732和mhgb738以及它们的具有低岩藻糖基化、具有re突变以及具有低岩藻糖基化和re突变的相应对应物的cdc活性。如所指出的那样,在37℃下将靶细胞与抗体一起温育30分钟。将15%-20%(储备浓度)的兔补体和热灭活补体添加到各孔中,分别至25μl/孔的体积。将混合物在37℃下温育4小时-12小时。通过添加cell titer-glo试剂(promega)并测量所得发光来测量靶细胞溶解,并以相对发光单位(rlu)报告。
32.图6a、图6b、图6c和图6d示出了对c42b细胞和lncap细胞的由具有低岩藻糖基化和re突变的抗psma抗体psmb896和psmb898介导的体外adcc剂量应答杀伤。具体地,图6a示出了在6小时利用pbmc对c42b细胞的由抗体介导的体外adcc剂量应答杀伤;图6b示出了在6小时利用pbmc对lncap细胞的由抗体介导的体外adcc剂量应答杀伤;图6c示出了在24小时利用nk细胞对c42b细胞的由抗体介导的体外adcc剂量应答杀伤;图6d示出了在24小时利用nk细胞对lncap细胞的由抗体介导的体外adcc剂量应答杀伤。在将效应细胞和抗体添加到靶细胞之后6小时或24小时生成剂量应答曲线。
5.具体实施方式
33.本公开部分地基于以下令人惊讶的发现:当少于80%的共价连接至抗体群体的低聚糖包含岩藻糖残基并且抗体的fc区包含k248e和t437r突变(re突变)时,抗体群体具有增强的adcc和增强的cdc两种活性。另外,低岩藻糖基化不会干扰re突变对增强cdc的作用,并且re突变不会干扰由低岩藻糖基化赋予的增强的adcc活性,如以下第7部分所展示。在一个方面,本文提供了一种抗体,该抗体在fc区中包含re突变并且在共价连接至抗体的fc区的低聚糖中不包含核心岩藻糖残基。在另一方面,本文提供了一种抗体群体,该抗体群体在fc区中包含re突变并且在共价连接至抗体的fc区的低聚糖中不包含核心岩藻糖残基。在一些实施方案中,本文提供了一种抗体群体,该抗体群体包含k248e和t437r突变(re突变),其中少于80%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。在一些实施方案中,少于70%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。在一些实施方案中,少于60%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。在一些实施方案中,少于50%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。在一些实施方案中,少于40%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。在一些实施方案中,少于30%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。在一些实施方案中,少于20%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。在一些实施方案中,少于10%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。在一些实施方案中,少于5%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
34.在某些实施方案中,在本公开中包括具有任何抗原结合结构或靶向任何抗原的任何抗体,只要抗体具有fc区即可。本公开中还包括包含本发明抗体的药物组合物及其制备方法和用途。
35.5.1定义
36.本文描述或引用的技术和程序包括本领域技术人员通常熟知的和/或使用常规方法通常采用的那些,诸如例如以下文献中描述的广泛利用的方法:molecular cloning:a laboratory manual(sambrook等人,第3版,2001);current protocols in molecular biology(ausubel等人编辑,2003);therapeutic monoclonal antibodies:from bench to clinic(an编辑,2009);monoclonal antibodies:methods and protocols(albitar编辑,2010);以及antibody engineering,第1卷和第2卷(kontermann和d
ü
bel编辑,第2版,2010)。
37.除非本文另有定义,否则本说明书中使用的技术和科学术语具有本领域普通技术人员通常理解的含义。出于解释本说明书的目的,将应用以下术语描述,并且只要适当,以单数使用的术语也将包括复数,反之亦然。在所阐述的术语的任何描述与以引用方式并入本文的任何文档冲突的情况下,将以下面所阐述的术语的描述为准。
38.术语
″
抗体
″
、
″
免疫球蛋白
″
或
″
ig
″
在本文中可互换使用,并且以最广泛的意义使用,并且具体地涵盖例如单克隆抗体(包括激动剂、拮抗剂、中和抗体、全长或完整的单克隆抗体)、具有多表位或单表位特异性的抗体组合物、多克隆或单价抗体、多价抗体以及由至少两种完整抗体形成的多特异性抗体(例如,双特异性抗体,只要它们表现出期望的生物活性即可),如下文所述。抗体可以是人的、人源化的、嵌合的和/或亲和力成熟的,以及来自其
他物种例如小鼠和兔等的抗体。术语
″
抗体
″
旨在包括免疫球蛋白多肽类别内的b细胞的多肽产物,其能够与特定分子抗原结合并且由两对相同的多肽链组成,其中每对具有一条重链(约50kda-70kda)和一条轻链(约25kda),每条链的每个氨基末端部分包括约100个至约130个或更多个氨基酸的可变区,并且每条链的每个羧基末端部分包括恒定区。参见例如,antibody engineering(borrebaeck编辑,第2版,1995);和kuby,immunology(第3版,1997)。在具体实施方案中,特异性分子抗原可被本文提供的抗体结合,包括多肽或表位。抗体还包括但不限于合成抗体、重组产生的抗体、羊驼抗体或其人源化变体、细胞内抗体和抗独特(抗id)抗体。如本文所用,术语
″
抗体
″
还包括具有fc区和上述任一者的功能性片段(例如,抗原结合片段)的任何结合分子,该功能性片段是指抗体重链或轻链多肽的一部分并保留该片段所源自的抗体的一部分或全部结合活性。功能性片段(例如,抗原结合片段)的非限制性示例包括单链fv(scfv)(例如,包括单特异性、双特异性等)、fab片段、f(ab
′
)片段、f(ab)2片段、f(ab
′
)2片段、二硫键连接的fv(dsfv)、fd片段、fv片段、双抗体、三抗体、四抗体和微抗体。具体地,本文提供的抗体包括免疫球蛋白分子和免疫球蛋白分子的免疫活性部分,例如,含有结合抗原的抗原结合位点的抗原结合结构域或分子(例如,抗体的一个或多个cdr)。此类抗体片段可见于例如harlow和lane,antibodies:a laboratory manual(1989);mol.biology and biotechnology:a comprehensive desk reference(myers编辑,1995);huston等人,1993,cell biophysics 22:189-224;pl
ü
ckthun和skerra,1989,meth.enzymol.178:497-515;和day,advanced immunochemistry(第2版,1990)。本文提供的抗体可以是免疫球蛋白分子的任何类别(例如igg、ige、igm、igd和iga)或任何亚类(例如igg1、igg2、igg3、igg4、iga1和iga2)。抗体可以是激动性抗体或拮抗性抗体。
39.″
抗原
″
是抗体可选择性结合的结构。靶抗原可以是多肽、碳水化合物、核酸、脂质、半抗原或其他天然存在的或合成的化合物。在一些实施方案中,靶抗原是多肽。在某些实施方案中,抗原与细胞缔合,例如,存在于细胞上或细胞中。
40.″
完整
″
抗体是包含抗原结合位点以及恒定结构域(cl)和至少重链恒定区ch 1、ch2和ch3的抗体。恒定区可包括人恒定区或其氨基酸序列变体。在某些实施方案中,完整抗体具有一种或多种效应子功能。
41.术语
″
结合(binds)
″
或
″
结合(binding)
″
是指分子之间的相互作用,包括例如形成复合物。相互作用可以是例如非共价相互作用,包括氢键、离子键、疏水相互作用和/或范德华相互作用。复合物还可包括通过共价键或非共价键、相互作用或力保持在一起的两个或多个分子的结合。抗体上的单个抗原结合位点和靶分子诸如抗原的单个表位之间的总非共价相互作用的强度是抗体或功能性片段对该表位的亲和力。结合分子(例如抗体)与单价抗原的解离速率(k
off
)与缔合速率(k
on
)的比率(k
off
/k
on
)为解离常数kd,其与亲和力成反比。kd值越低,抗体的亲和力越高。kd值随着抗体和抗原的不同复合物而变化,并且取决于k
on
和k
off
两者。本文提供的抗体的解离常数kd可使用本文提供的任何方法或本领域技术人员众所周知的任何其他方法来确定。一个结合位点处的亲和力并不总是反映抗体与抗原之间的相互作用的真实强度。当含有多个重复抗原决定簇的复合抗原(诸如多价抗原)与含有多个结合位点的抗体接触时,抗体与抗原在一个位点处的相互作用将增加在第二个位点处反应的概率。多价抗体与抗原之间的这种多重相互作用的强度称为亲合力。
42.与本文所述的抗体相关的术语,诸如
″
结合
″
、
″
特异性结合
″
和类似术语在本文中
也可互换使用,并且是指特异性结合抗原诸如多肽的抗原结合结构域的抗体。结合或特异性结合抗原的抗体或抗原结合结构域可与相关抗原交叉反应。在某些实施方案中,结合或特异性结合抗原的抗体或抗原结合结构域不与其他抗原交叉反应。结合或特异性结合抗原的抗体或抗原结合结构域可例如通过免疫测定、或本领域技术人员已知的其他技术来鉴定。在一些实施方案中,如使用实验技术诸如放射性免疫测定(ria)和酶联免疫吸附测定(elisa)确定的,当抗体或抗原结合结构域以比与任何交叉反应性抗原更高的亲和力结合抗原时,它结合或特异性结合抗原。典型地,特异性或选择性反应将为背景信号或噪声的至少两倍,并且可以是背景的10倍以上。参见例如fundamental immunology 332-36(paul编辑,第2版,1989年)有关结合特异性的讨论。在某些实施方案中,抗体或抗原结合结构域与
″
非靶
″
蛋白的结合程度小于抗体或抗原结合结构域与其特定靶抗原结合的约10%,例如,如通过荧光活化细胞分选(facs)分析或ria所确定的。关于诸如
″
特异性结合
″
、
″
特异性地结合
″
或
″
特异于
″
的术语意指与非特异性相互作用明显不同的结合。特异性结合可例如通过确定与对照分子的结合相比的分子的结合来测量,该对照分子通常是不具有结合活性的类似结构的分子。例如,特异性结合可通过与类似于靶的对照分子竞争来确定,例如过量的未标记靶。在这种情况下,如果标记靶与探针的结合被过量的未标记靶竞争性地抑制,则指示特异性结合。与抗原结合的抗体或抗原结合结构域包括能够以足够亲和力结合抗原的一种抗体或抗原结合结构域,使得抗体可用作例如靶向抗原的诊断剂或治疗剂。在某些实施方案中,与抗原结合的抗体或抗原结合结构域具有小于或等于1000nm、800nm、500nm、250nm、100nm、50nm、10nm、5nm、4nm、3nm、2nm、1nm、0.9nm、0.8nm、0.7nm、0.6nm、0.5nm、0.4nm、0.3nm、0.2nm或0.1nm的解离常数(kd)。在某些实施方案中,抗体或抗原结合结构域结合在来自不同物种(例如,在人和食蟹猕猴物种之间)的抗原中保守的抗原表位。
43.″
结合亲和力
″
通常是指分子(例如,结合蛋白诸如抗体)的单个结合位点与其结合配偶体(例如,抗原)之间的非共价相互作用的总和的强度。除非另外指明,否则如本文所用,
″
结合亲和力
″
是指内在结合亲和力,其反映结合对的成员(例如,抗体与抗原)之间的1∶1相互作用。结合分子x对其结合配偶体y的亲和力通常可由解离常数(kd)表示。亲和力可通过本领域已知的常见方法测量,包括本文所述的那些。低亲和力抗体通常缓慢结合抗原并且倾向于易于解离,而高亲和力抗体通常更快地结合抗原并且趋向于更长地保持结合。测量结合亲和力的多种方法是本领域已知的,其中的任何方法都可用于本公开的目的。具体的例示性实施方案包括以下。在一个实施方案中,
″
kd″
或
″
kd值
″
可通过本领域已知的测定例如通过结合测定来测量。kd可在ria中测量,例如用目的抗体及其抗原的fab版本进行(chen等人,j.mol biol,1999,293:865-81)。kd或kd值也可通过使用生物层干涉仪(bli)测量或者通过使用例如系统或通过吏用例如2000或3000的表面等离子共振(spr)测定测量。
″
结合速率
″
或
″
缔合的速率
″
或
″
缔合速率
″
或
″kon
″
也可用上述相同的生物层干涉测量法(bli)或表面等离子共振(spr)技术使用例如2000或3000系统来确定。
44.在某些实施方案中,抗体可包含
″
嵌合
″
序列,其中重链和/或轻链的一部分与来源于特定物种或属于特定抗体类别或亚类的抗体中的对应序列相同或同源,而链的剩余部分
与来源于另一物种或属于另一抗体类别或亚类的抗体中的对应序列相同或同源,只要它们表现出期望的生物活性即可(参见美国专利4,816,567;和morrison等人,proc.natl.acad.sci.usa,1984,81:6851-55)。
45.在某些实施方案中,抗体可包含非人(例如,鼠)抗体的
″
人源化
″
形式的部分,这些抗体是嵌合抗体并包括人免疫球蛋白(例如,受体抗体),其中天然cdr残基被来自非人物种诸如小鼠、大鼠、兔或非人灵长类动物(例如,供体抗体)的具有期望的特异性、亲和力和能力的对应cdr残基替换。在一些情况下,人免疫球蛋白的一个或多个fr区残基被对应的非人残基替换。此外,人源化抗体可包含受体抗体或供体抗体中没有的残基。进行这些修饰以进一步改善抗体性能。人源化抗体重链或轻链可包含一个或多个可变区,其中所有或基本上所有的cdr对应于非人免疫球蛋白的那些,并且所有或基本上所有的fr是人免疫球蛋白序列的那些。在某些实施方案中,人源化抗体将包含免疫球蛋白恒定区(fc)的至少一部分,通常是人免疫球蛋白的恒定区的至少一部分。对于更多细节,参见jones等人,nature,1986,321:522-25;riechmann等人,nature,1988,332:323-29;presta,curr.op.struct.biol.,1992,2:593-96;carter等人,proc.natl.acad.sci.usa,1992,89:4285-89;美国专利:6,800,738;6,719,971;6,639,055;6,407,213;和6,054,297。
46.在某些实施方案中,抗体可包含
″
完全人抗体
″
或
″
人抗体
″
的部分,其中这些术语在本文中可互换使用并且是指包含人可变区和例如人恒定区的抗体。在具体实施方案中,这些术语是指包含人来源的可变区和恒定区的抗体。在某些实施方案中,
″
完全人
″
抗体还可涵盖结合多肽并由核酸序列编码的抗体,该核酸序列是人种系免疫球蛋白核酸序列的天然存在的体细胞变体。术语
″
完全人抗体
″
包括具有对应于如kabat等人所述的人种系免疫球蛋白序列的可变区和恒定区的抗体(参见kabat等人(1991)sequences of proteins of immunological interest,第五版,u.s.department of health and human services,nih公开号91-3242)。
″
人抗体
″
是指具有与由人产生和/或已使用用于制备人抗体的任何技术制备的抗体的氨基酸序列相对应的氨基酸序列的抗体。人抗体的这一定义特别排除了包含非人抗原结合残基的人源化抗体。可使用本领域已知的各种技术来产生人抗体,包括噬菌体展示文库(hoogenboom和winter,j.mol.biol.,1991,227:381;marks等人,1991,j.mol.biol.,1991,222:581)和酵母展示文库(chao等人,nature protocols,2006,1:755-68)。也可用于制备人单克隆抗体的方法描述于cole等人,monoclonal antibodies and cancer therapy 77(1985);boerner等人,j.immunol.,1991,147(1):86-95;以及van dijk和van de winkel,curr.opin.pharmacol.,2001,5:368-74。人抗体可通过将抗原施用到转基因动物来制备,该转基因动物已被修饰以响应于抗原攻击而产生此类抗体,但其内源性基因座已被禁用,例如小鼠(参见例如,jakobovits,curr.opin.biotechnol.,1995,6(5):561-66;br
ü
ggemann和taussing,curr.opin.biotechnol.,1997,8(4):455-58;和关于xenomouse
tm
技术的美国专利6,075,181和6,150,584)。还参见例如li等人,proc.natl.acad.sci.usa,2006,103:3557-62关于经由人b细胞杂交瘤技术生成的人抗体。
47.在某些实施方案中,抗体可包含
″
重组人抗体
″
的部分,其中该短语包括通过重组手段制备、表达、产生或分离的人抗体,诸如使用转染到宿主细胞中的重组表达载体表达的抗体、从重组组合人抗体文库中分离的抗体、从人免疫球蛋白基因的转基因和/或转染色体的动物(例如,小鼠或牛)中分离的抗体(参见例如,taylor,l.d.等人,nucl.acids res.,
1992,20:6287-6295)或通过涉及将人免疫球蛋白基因序列剪接到其他dna序列的任何其他手段制备、表达、产生或分离的抗体。此类重组人抗体可具有衍生自人种系免疫球蛋白序列的可变区和恒定区(参见kabat,e.a.等人(1991)sequences of proteins of immunological interest,第五版,u.s.department of health and human services,nih公开号91-3242)。然而,在某些实施方案中,对此类重组人抗体进行体外诱变(或者,当使用针对人ig序列的转基因动物时,进行体内体细胞诱变),并且因此重组抗体的vh和vl区的氨基酸序列是这样的序列,其虽然衍生自人种系vh和vl序列并与之相关,但可能不天然存在于体内人抗体种系组库内。
48.在某些实施方案中,抗体可包含
″
单克隆抗体
″
的一部分,其中如本文所用的术语是指从基本上均一的抗体群体中获得的抗体,例如,除了可能以少量存在的天然存在的突变之外,组成群体的单个抗体是相同的,并且每个单克隆抗体通常将识别抗原上的单个表位。在具体实施方案中,如本文所用,
″
单克隆抗体
″
是由单个杂交瘤或其他细胞产生的抗体。术语
″
单克隆
″
不限于用于制备抗体的任何特定方法。例如,可用于本公开的单克隆抗体可通过首先由kohler等人,1975,nature 256:495描述的杂交瘤方法制备,或者可在细菌或真核动物或植物细胞中使用重组dna方法制备(参见例如,美国专利4,816,567)。
″
单克隆抗体
″
也可使用例如clackson等人,nature,1991,352:624-28和marks等人,j.mol.biol.,1991,222:581-97中描述的技术从噬菌体抗体文库中分离。用于制备克隆细胞系和由此表达的单克隆抗体的其他方法在本领域中是众所周知的。参见例如short protocols in molecular biology(ausubel等人编辑,第5版,2002)。
49.典型的4链抗体单元是由两条相同的轻(l)链和两条相同的重(h)链组成的异四聚体糖蛋白。在igg的情况下,4链单元通常为约150,000道尔顿。每条l链通过一个共价二硫键与h链连接,而两条h链根据h链同种型通过一个或多个二硫键彼此连接。每条h和l链还具有规则间隔的链内二硫键。每条h链在n-末端具有可变结构域(vh),随后是α链和γ链中的每一条的三个恒定结构域(ch)以及μ和ε同种型的四个ch结构域。每条l链在n-末端具有可变结构域(vl),随后在其另一端具有恒定结构域(cl)。vl与vh对准,并且cl与重链的第一恒定结构域(ch1)对准。据信特定的氨基酸残基在轻链和重链可变结构域之间形成界面。vh和vl的配对一起形成单个抗原结合位点。对于不同类别的抗体的结构和特性,参见例如basic and clinical immunology 71(stites等人编辑,第8版,1994);和immunobiology(janeway等人编辑,第5版,2001)。
50.如本文所用,术语
″
核心岩藻糖
″
、
″
核心岩藻糖残基
″
、
″
岩藻糖
″
或
″
岩藻糖残基
″
是指连接至asn-297-连接的n-低聚糖的第一glcnac的α1,6-键中的岩藻糖残基。ferrara等人,proc natl acad sci u s a,2011,108:12669-74。
″
岩心岩藻糖
″
、
″
核心岩藻糖残基
″
、
″
岩藻糖
″
和
″
岩藻糖残基
″
在本公开中可互换使用。
51.术语
″
fab
″
或
″
fab区
″
是指结合抗原的抗体区。常规igg通常包含两个fab区,每个fab区驻留在y形igg结构的两个臂中的一个臂上。每个fab区通常由重链和轻链中的每一者的一个可变区和一个恒定区构成。更具体地,fab区中重链的可变区和恒定区为vh和ch1区,并且fab区中的轻链的可变区和恒定区为vl和cl区。fab区中的vh、ch1、vl和cl可以各种方式布置以赋予根据本公开的抗原结合能力。例如,vh和ch 1区可在一个多肽上,并且vl和cl区可在单独的多肽上,类似于常规igg的fab区。另选地,vh、ch1、vl和cl区可全部在同一多
肽上并以不同的顺序取向,如下文部分更详细描述的。
52.术语
″
可变区
″
、
″
可变结构域
″
、
″
v区
″
或
″
v结构域
″
是指抗体的轻链或重链的一部分,其通常位于轻链或重链的氨基末端,并且在重链中具有约120至130个氨基酸的长度以及在轻链中具有约100至110个氨基酸的长度,并且用于每个特定抗体对其特定抗原的结合和特异性。重链的可变区可被称为
″
vh
″
。轻链的可变区可被称为
″
vl
″
。术语
″
可变
″
是指可变区的某些片段在抗体之间在序列上广泛不同的事实。v区介导抗原结合并限定特定抗体对其特定抗原的特异性。然而,可变性在可变区的110个氨基酸跨度上不是均匀分布的。相反,v区由较少可变(例如,相对不变)的称为框架区(fr)的约15-30个氨基酸的延伸组成,其被称为
″
高变区
″
的较大可变性(例如,极端可变性)的较短区域分开,该较短区域各自长约9-12个氨基酸。重链和轻链可变区各自包含四个fr,主要采用β片构型,由三个高变区连接,它们形成连接β折叠结构的环并且在一些情况下形成其部分。每条链中的高变区通过fr并与来自另一条链的高变区紧密靠近地保持在一起,有助于抗体的抗原结合位点的形成(参见例如,kabat等人,sequences of proteins of immunological interest(第5版,1991))。恒定区不直接参与抗体与抗原的结合,但表现出各种效应子功能,诸如抗体参与抗体依赖性细胞毒性(adcc)和补体依赖性细胞毒性(cdc)。不同抗体之间的可变区在序列上广泛不同。在具体实施方案中,可变区是人可变区。
53.术语
″
根据kabat的可变区残基编号
″
或
″
如kabat中的氨基酸位置编号
″
及其变型是指kabat等人(出处同上)中用于抗体编译的重链可变区或轻链可变区的编号系统。使用该编号系统,实际线性氨基酸序列可含有对应于可变结构域的fr或cdr的缩短或插入的更少或另外的氨基酸。例如,重链可变结构域可包括在残基52之后的单个氨基酸插入(根据kabat的残基52a)和在残基82之后的三个插入残基(例如,根据kabat的残基82a、82b和82c等)。通过在抗体序列的同源区与
″
标准
″
kabat编号序列比对,可确定给定抗体的kabat残基编号。当提及可变结构域中的残基(大约轻链的残基1-107和重链的残基1-113)时,通常使用kabat编号系统(例如,kabat等人,出处同上)。当提及免疫球蛋白重链恒定区中的残基时,通常使用
″
eu编号系统
″
或
″
eu索引
″
(例如,kabat等人中报道的eu索引,出处同上)。
″
如kabat中的eu索引
″
是指人igg1 eu抗体的残基编号。其他编号系统已由例如abm、chothia、contact、imgt和ahon描述。
54.当参考抗体使用时,术语
″
重链
″
是指约50-70kda的多肽链,其中氨基末端部分包括约120至130个或更多个氨基酸的可变区,并且羧基末端部分包括恒定区。基于重链恒定区的氨基酸序列,恒定区可以是五种不同类型中的一种类型(例如同种型),称为α(α)、δ(δ)、ε(ε)、γ(γ)和μ(μ)。不同的重链大小不同:α、δ和γ含有大约450个氨基酸,而μ和ε含有大约550个氨基酸。当与轻链结合时,这些不同类型的重链分别产生五种众所周知的类别(例如,同种型)的抗体,即iga、igd、ige、igg和igm,包括igg的四个亚类,即igg1、igg2、igg3和igg4。
55.当参考抗体使用时,术语
″
轻链
″
是指约25kda的多肽链,其中氨基末端部分包括约100至约110个氨基酸的可变区,并且羧基末端部分包括恒定区。轻链的近似长度为211至217个氨基酸。基于恒定结构域的氨基酸序列,存在两种不同类型,称为κ(κ)或λ(λ)。
56.如本文所用,术语
″
高变区
″
、
″
hvr
″
、
″
互补决定区
″
和
″
cdr
″
可互换使用。
″
cdr
″
是指免疫球蛋白(ig或抗体)vh β-片框架的非框架区内的三个高变区(h1、h2或h3)中的一个高
变区,或抗体vlβ-片框架的非框架区内的三个高变区(l1、l2或l3)中的一个高变区。因此,cdr是散布在框架区序列内的可变区序列。
57.cdr区是本领域技术人员众所周知的,并且已由众所周知的编号系统定义。例如,kabat互补决定区(cdr)是基于序列变异性的,并且是最常用的(参见例如,kabat等人,出处同上)。chothia相反是指结构环的位置(参见例如,chothia和lesk,j.mol.biol.,1987,196:901-17)。当使用kabat编号惯例编号时,chothia cdr-h 1环的末端在h32和h34之间变化,这取决于环的长度(这是因为kabat编号方案将插入置在h35a和h35b处;如果35a和35b都不存在,则环在32处结束;如果仅存在35a,则环在33处结束;如果35a和35b都存在,则环在34处结束)。abm高变区代表kabat cdr和chothia结构环之间的折衷,并被oxford molecular的abm抗体建模软件使用(参见例如antibody engineering,第2卷(kontermann和d
ü
bel编辑,第2版,2010)。
″
contact
″
高变区是基于对可获得的复杂晶体结构的分析。已经开发出来并被广泛采用的另一通用编号系统为immunogenetics(imgt)information(lafranc等人,dev.comp.immunol.,2003,27(1):55-77)。imgt是专门研究人和其他脊椎动物的免疫球蛋白(ig)、t细胞受体(tcr)和主要组织相容性复合物(mhc)的整合信息系统。在本文中,cdr根据氨基酸序列以及轻链或重链内的位置两者来引用。由于cdr在免疫球蛋白可变结构域结构内的
″
位置
″
在物种之间是保守的,并且存在于称为环的结构中,因此通过使用根据结构特征比对可变结构域序列的编号系统,cdr和构架残基容易鉴定。该信息可用于将来自一个物种的免疫球蛋白的cdr残基移植和替换到通常来自人抗体的受体框架中。honegger和pl
ü
ckthun开发了一个另外的编号系统(ahon),j.mol.biol.,2001,309:657-70)。编号系统之间的对应关系,包括例如kabat编号和imgt唯一编号系统,为本领域技术人员所熟知(参见例如kabat,出处同上;chothia和lesk,出处同上;martin,出处同上;lefranc等人,出处同上)。来自这些高变区或cdr中的每一者的残基在下文中指出。
58.表1.
[0059][0060]
给定cdr的边界可根据用于识别的方案而变化。因此,除非另有说明,否则给定抗体或其区域(诸如可变区)的术语
″
cdr
″
和
″
互补决定区
″
以及抗体或其区域的单独cdr(例如,cdr-h1、cdr-h2)应理解为涵盖如上文所述的任何已知方案所定义的互补决定区。在一些情况下,指定用于识别特定cdr或cdr的方案,诸如由kabat、chothia或contact方法定义的cdr。在其他情况下,给出了cdr的特定氨基酸序列。
[0061]
高变区可包括如下
″
扩展高变区
″
:vl中的24-36或24-34(l1)、46-56或50-56(l2)和89-97或89-96(l3),以及vh中的26-35或26-35a(h1)、50-65或49-65(h2)和93-102、94-102或95-102(h3)。
[0062]
术语
″
恒定区
″
或
″
恒定结构域
″
是指轻链和重链的羧基末端部分,其不直接参与抗体与抗原的结合,但表现出各种效应子功能,诸如与fc受体的相互作用。该术语是指免疫球蛋白分子的相对于免疫球蛋白的其他部分(包含抗原结合位点的可变区)具有更保守的氨基酸序列的部分。恒定区可包含重链的ch1、ch2和ch3区和轻链的cl区。
[0063]
术语
″
框架
″
或
″
fr
″
是指侧接cdr的那些可变区残基。fr残基存在于例如嵌合的、人源化的、人的结构域抗体、双价抗体、线性抗体和双特异性抗体中。fr残基是除高变区残基或cdr残基之外的那些可变结构域残基。vh和vl区中的每一者中通常存在四个fr区。vh中的fr区是vh fr1、vh fr2、vh fr3和vh fr4(或fr h1、fr h2、fr h3和fr h4)。vl中的fr区是vl fri、vl fr2、vl fr3和vl fr4(或fr l1、fr l2、fr l3和fr l4)。
[0064]
术语
″
fc区
″
在本文中用于定义免疫球蛋白重链的c-末端区域,包括例如天然序列fc区、重组fc区和变异fc区。尽管免疫球蛋白重链的fc区的边界可能变化,但人igg重链fc区通常被定义为从位置cys226的氨基酸残基或从pro230延伸到其羧基末端。fc区的c-末端赖氨酸(残基447根据eu编号系统)可例如在抗体的生产或纯化期间或通过重组工程化编码抗体重链的核酸来去除。因此,完整抗体的组合物可包括去除了所有k447残基的抗体群、没有去除k447残基的抗体群体、以及具有含和不合k447残基的抗体混合物的抗体群体。
″
功能性fc区
″
具有天然序列fc区的
″
效应子功能
″
。示例性
″
效应子功能
″
包括c1q结合;cdc;fc受体结合;adcc吞噬作用;细胞表面受体(例如,b细胞受体)的下调等。此类效应子功能通常需要fc区与结合区或结合结构域(例如,抗体可变区或结构域)组合,并且可使用本领域技术人员已知的各种测定来评估。
″
变体fc区
″
包括由于至少一个氨基酸修饰(例如,取代、添加或缺失)而与天然序列fc区的氨基酸序列不同的氨基酸序列。在某些实施方案中,变体fc区与天然序列fc区或亲本多肽的fc区相比具有至少一个氨基酸取代,例如,在天然序列fc区或亲本多肽的fc区中约一至约十个氨基酸取代,或约一至约五个氨基酸取代。本文的变体fc区可与天然序列fc区和/或亲本多肽的fc区具有至少约80%的同源性,或者与其具有至少约90%的同源性,例如与其具有至少约95%的同源性。
[0065]
当与抗原或抗体相关使用时,术语
″
变体
″
可以指与天然或未修饰序列相比包含一个或多个(诸如例如约1个至约25个、约1个至约20个、约1个至约15个、约1个至约10个、或约1个至约5个)氨基酸序列取代、缺失和/或添加的肽或多肽。例如,cd37变体可由对天然cd37的氨基酸序列的一种或多种(诸如例如,约1种至约25种、约1种至约20种、约1种至约15种、约1种至约10种或约1种至约5种)变化得到。同样以举例的方式,抗cd37抗体的变体可由对天然或先前未修饰抗cd37抗体的氨基酸序列的一种或多种(诸如例如,约1种至约25种、约1种至约20种、约1种至约15种、约1种至约10种或约1种至约5种)变化得到。变体可以是天然存在的,诸如等位基因或剪接变体,或者可以是人工构造的。多肽变体可由编码变体的相应核酸分子制备。在具体的实施方案中,cd37变体或抗cd37抗体变体至少分别保持cd37或抗cd37抗体功能活性。在具体的实施方案中,抗cd37抗体变体结合cd37和/或对cd37活性拮抗。在某些实施方案中,变体由核酸分子的编码cd37或抗cd37抗体vh或vl区或亚区诸如一个或多个cdr的单核苷酸多态性(snp)变体编码。
[0066]
术语
″
同一性
″
是指如通过比对和比较序列所确定的两个或更多个多肽分子或者两个或更多个核酸分子的序列之间的关系。相对于参考多肽序列的
″
氨基酸序列同一性百分比(%)
″
定义为候选序列中与参考多肽序列中的氨基酸残基相同的氨基酸残基的百分比,在比对序列并引入缺口(如果需要的话)以实现最大的序列同一性百分比之后,不考虑任何保守置换作为序列同一性的一部分。出于确定氨基酸序列同一性百分比的目的进行的比对可以本领域技术范围内的多种方式实现,例如使用可公开获得的计算机软件诸如blast、blast-2、align或megalign(dnastar,inc.)软件。本领域技术人员可确定用于比对序列的合适参数,包括在所比较序列的全长上实现最大比对所需的任何算法。
[0067]
氨基酸残基/位置的
″
修饰
″
是指一级氨基酸序列与起始氨基酸序列相比的变化,其中变化是由涉及所述氨基酸残基/位置的序列改变引起的。例如,典型的修饰包括残基被另一个氨基酸取代(例如保守或非保守取代)、与所述残基/位置相邻的一个或多个(例如,通常少于5个、4个或3个)氨基酸的插入和/或所述残基/位置的缺失。
[0068]
如本文所用,
″
表位
″
是本领域的术语,并且是指抗体可特异性结合的抗原的局部区域。表位可以是线性表位或构象、非线性或不连续表位。在多肽抗原的情况下,例如,表位可以是多肽的连续氨基酸(
″
线性
″
表位),或者表位可包含来自多肽的两个或更多个非连续区域的氨基酸(
″
构象
″
、
″
非线性
″
或
″
不连续
″
表位)。本领域技术人员将理解,一般来讲,线性表位可取决于或不取决于二级、三级或四级结构。例如,在一些实施方案中,抗体与一组氨基酸结合,而无论它们是否在天然三维蛋白质结构中折叠。在其他实施方案中,抗体需要构成表位的氨基酸残基表现出特定的构象(例如弯曲、扭曲、翻转或折叠)以便识别和结合表位。
[0069]
术语
″
多肽
″
、
″
肽
″
和
″
蛋白质
″
在本文中可互换使用,并且是指任何长度的氨基酸的聚合物。该聚合物可以是直链或支链的,其可包含经修饰的氨基酸,并且其可夹杂有非氨基酸。该术语还涵盖已被天然修饰或通过干预修饰的氨基酸聚合物;例如二硫键形成、糖基化、脂化、乙酰化、磷酸化或任何其他操作或修饰。该定义还包括例如含有一种或多种氨基酸类似物(包括但不限于非天然氨基酸)以及本领域已知的其他修饰的多肽。应当理解,因为本公开的多肽可基于抗体或免疫球蛋白超家族的其他成员,所以在某些实施方案中,
″
多肽
″
可作为单链或两个或更多个相关链出现。
[0070]
术语
″
载体
″
是指用于携带或包含核酸序列的物质,该核酸序列包括例如编码如本文所述的抗体的核酸序列,以便将核酸序列引入宿主细胞。适用的载体包括例如表达载体、质粒、噬菌体载体、病毒载体、附加体和人工染色体,其可包括可操作用于稳定整合到宿主细胞染色体中的选择序列或标记。另外,载体可包括一个或多个选择性标记基因和适当的表达控制序列。可包括的选择性标记基因例如提供对抗生素或毒素的抗性,补充营养缺陷,或提供不在培养基中的关键营养物。表达控制序列可包括本领域众所周知的组成型和诱导型启动子、转录增强子、转录终止子等。当两个或更多个核酸分子被共表达时(例如,抗体重链和轻链或抗体vh和vl两者),两种核酸分子都可被插入例如单个表达载体或单独的表达载体中。对于单个载体表达,编码核酸可操作地连接到一个共同表达控制序列或连接到不同的表达控制序列,诸如一个诱导型启动子和一个组成型启动子。将核酸分子引入宿主细胞可使用本领域众所周知的方法来确认。此类方法包括例如核酸分析,诸如mrna的northern印迹或聚合酶链反应(pcr)扩增、用于基因产物表达的免疫印迹或其他合适的分
析方法,以测试引入的核酸序列或其对应基因产物的表达。本领域技术人员应理解,核酸分子以足以产生期望产物的量表达,并且进一步理解,可使用本领域众所周知的方法优化表达水平以获得足够的表达。
[0071]
如本文所用,术语
″
宿主
″
是指动物,诸如哺乳动物(例如,人)。
[0072]
如本文所用,术语
″
宿主细胞
″
是指可用核酸分子转染的特定受试者细胞和此类细胞的后代或潜在后代。此类细胞的后代可与用核酸分子转染的亲本细胞不同,由于可在后代中发生的突变或环境影响或者由于核酸分子整合到宿主细胞基因组中。
[0073]
″
分离的核酸
″
是基本上与天然序列自然伴随的其他基因组dna序列以及蛋白质或复合物诸如核糖体和聚合酶分离的核酸,例如rna、dna或混合核酸。
″
分离的
″
核酸分子是与存在于该核酸分子的天然来源中的其他核酸分子分离的核酸分子。此外,
″
分离的
″
核酸分子,诸如cdna分子,当通过重组技术产生时可基本上不合其他细胞材料或培养基,或当化学合成时基本上不合化学前体或其他化学品。在一个具体实施方案中,分离或纯化编码如本文所述的抗体的一种或多种核酸分子。该术语涵盖已从其天然存在的环境中去除的核酸序列,并且包括重组或克隆的dna分离物和化学合成的类似物或通过异源系统生物合成的类似物。基本上纯的分子可包括该分子的分离形式。
[0074]
如在本文中可互换使用的
″
多核苷酸
″
、
″
核苷酸
″
或
″
核酸
″
是指任何长度的核苷酸的聚合物并且包括dna和rna。核苷酸可以是脱氧核糖核苷酸、核糖核苷酸、修饰的核苷酸或碱基和/或它们的类似物,或是可通过dna或rna聚合酶或通过合成反应掺入聚合物中的任何底物。多核苷酸可包含修饰的核苷酸,诸如甲基化核苷酸及其类似物。如本文所用,
″
寡核苷酸
″
是指短的、通常单链的合成多核苷酸,其长度通常但不一定少于约200个核苷酸。术语
″
寡核苷酸
″
和
″
多核苷酸
″
不是相互排斥的。以上针对多核苷酸的描述同样并且完全适用于寡核苷酸。产生本公开的抗体的细胞可包括亲本杂交瘤细胞,以及其中已引入编码抗体的核酸的细菌和真核宿主细胞。除非另有说明,否则本文所公开的任何单链多核苷酸序列的左侧末端是5
′
末端;双链多核苷酸序列的左侧方向被称为5
′
方向。新生rna转录物的5
′
至3
′
添加方向被称为转录方向;dna链上具有与rna转录物相同序列的序列区域,其在rna转录物的5
′
至5
′
端,被称为
″
上游序列
″
;dna链上具有与rna转录物相同序列的序列区域,其在rna转录物的3
′
至3
′
端,被称为
″
下游序列
″
。
[0075]
如本文所用,术语
″
药学上可接受的
″
意指在动物并且更具体地在人中使用的由联邦或州政府的监管机构批准的或在美国药典、欧洲药典或其他公认的药典中列出的。
[0076]
″
赋形剂
″
意指药学上可接受的材料、组合物或媒介物,诸如液体或固体填充剂、稀释剂、溶剂或包封材料。赋形剂包括例如包封材料或添加剂,诸如吸收促进剂、抗氧化剂、粘结剂、缓冲液、载体、包衣剂、着色剂、稀释剂、崩解剂、乳化剂、增量剂、填充剂、调味剂、保湿剂、润滑剂、香料、防腐剂、推进剂、释放剂、灭菌剂、甜味剂、增溶剂、润湿剂以及它们的混合物。术语
″
赋形剂
″
还可指稀释剂、佐剂(例如,弗氏佐剂(完全或不完全))或媒介物。
[0077]
在一些实施方案中,赋形剂是药学上可接受的赋形剂。药学上可接受的赋形剂的示例包括缓冲液,诸如磷酸盐、柠檬酸盐和其他有机酸;抗氧化剂,包括抗坏血酸;低分子量(例如,少于约10个氨基酸残基)多肽;蛋白质,诸如血清白蛋白、明胶或免疫球蛋白;亲水性聚合物,诸如聚乙烯吡咯烷酮;氨基酸,诸如甘氨酸、谷氨酰胺、天冬酰胺、精氨酸或赖氨酸;单糖、二糖和其他碳水化合物,包括葡萄糖、甘露糖或糊精;螯合剂,诸如edta;糖醇,诸如甘
露醇或山梨糖醇;成盐抗衡离子,诸如钠;和/或非离子表面活性剂,诸如tween
tm
、聚乙二醇(peg)和pluronics
tm
。药学上可接受的赋形剂的其他示例描述于remington和gennaro,remington
′
s pharmaceutical sciences(第18版,1990)中。
[0078]
在一个实施方案中,每种组分在与药物制剂的其他成分相容的意义上是
″
药学上可接受的
″
,并且适用于与人和动物的组织或器官接触而没有过度毒性、刺激、过敏反应、免疫原性或其他问题或并发症,与合理的益处/风险比相称。参见例如,lippincott williams&wilkins:philadelphia,pa,2005;handbook of pharmaceutical excipients,第6版;rowe等人编辑;the pharmaceutical press and the american pharmaceutical association:2009;handbook of pharmaceutical additives,第3版;ash和ash编辑;gower publishing company:2007;pharmaceutical preformulation and formulation,第2版;gibson编辑;crc press llc:boca raton,fl,2009。在一些实施方案中,药学上可接受的赋形剂在所采用的剂量和浓度下对暴露于其的细胞或哺乳动物无毒。在一些实施方案中,药学上可接受的赋形剂是ph缓冲水溶液。
[0079]
在一些实施方案中,赋形剂是无菌液体,诸如水和油,包括石油、动物、植物或合成来源诸如花生油、大豆油、矿物油、芝麻油等的那些。当静脉内施用组合物(例如,药物组合物)时,水是示例性赋形剂。盐水溶液和右旋糖水溶液以及甘油溶液也可用作液体赋形剂,尤其是用于注射溶液。赋形剂还可包括淀粉、葡萄糖、乳糖、蔗糖、明胶、麦芽、大米、面粉、白垩、硅胶、硬脂酸钠、单硬脂酸甘油酯、滑石、氯化钠、脱脂奶粉、甘油、丙烯、二醇、水、乙醇等。如果需要,组合物还可含有少量润湿剂或乳化剂或ph缓冲剂。组合物可采用溶液、悬浮液、乳液、片剂、丸剂、胶囊、粉末、缓释制剂等形式。口服组合物,包括制剂,可包含标准赋形剂,诸如药物级甘露醇、乳糖、淀粉、硬脂酸镁、糖精钠、纤维素、碳酸镁等。
[0080]
例如,包含药物化合物的组合物可含有抗体,例如以分离或纯化的形式与合适量的赋形剂一起。
[0081]
如本文所用,术语
″
有效量
″
或
″
治疗有效量
″
是指足以产生期望结果的本文提供的抗体或药物组合物的量。
[0082]
术语
″
受试者
″
和
″
患者
″
可互换使用。如本文所用,在某些实施方案中,受试者是哺乳动物,诸如非灵长类动物(例如,牛、猪、马、猫、狗、大鼠等)或灵长类动物(例如,猴和人)。在具体实施方案中,受试者是人。在一个实施方案中,受试者是被诊断患有病症或障碍的哺乳动物,例如人。在另一个实施方案中,受试者是具有发展病症或障碍的风险的哺乳动物,例如人。
[0083]
″
施用
″
(administer或administration)是指将存在于体外的物质注射或以其他方式物理递送至患者体内的动作,诸如通过粘膜、皮内、静脉内、肌内、皮下递送和/或本文所述或本领域已知的任何其他物理递送方法。
[0084]
如本文所用,术语
″
治疗
″
(treat、treatment和treating)是指由施用一种或多种疗法引起的疾病或病症的进展、严重程度和/或持续时间的减少或改善。治疗可通过评估是否已存在与潜在障碍相关的一种或多种症状的减少、减轻和/或缓解来确定,使得尽管患者可能仍然受到潜在障碍的折磨,但观察到患者的改善。术语
″
治疗
″
包括管理和改善疾病。术语
″
管理
″
(manage、managing和management)是指受试者从不一定导致疾病治愈的疗法中获得的有益效果。
[0085]
术语
″
预防
″
(prevention、preventing和prevention)是指降低疾病、障碍、病症或相关联症状发作(或复发)的可能性。
[0086]
术语
″
约
″
和
″
大约
″
意指在给定值或范围的20%内、15%内、10%内、9%内、8%内、7%内、6%内、5%内、4%内、3%内、2%内、1%内或更小。
[0087]
如本公开和权利要求书中所用,单数形式
″
一
″
、
″
一个
″
和
″
该
″
包括复数形式,除非上下文清楚表明并非如此。
[0088]
应当理解,在本文中用术语
″
包括
″
描述实施方案的任何地方,还提供了根据
″
由.....组成
″
和/或
″
基本上由......组成
″
描述的其他类似实施方案。还应理解,在本文中用短语
″
基本上由...组成
″
描述实施方案的任何地方,还提供了根据
″
由.....组成
″
描述的其他类似实施方案。
[0089]
如在短语诸如
″
a与b之间
″
或
″
a-b之间
″
中使用的术语
″
之间
″
是指包括a和b两者的范围。
[0090]
如在短语诸如
″
a和/或b
″
中使用的术语
″
和/或
″
在此旨在包括a和b两者;a或b;a(单独);和b(单独)。同样,如在短语诸如
″
a、b和/或c
″
中使用的术语
″
和/或
″
旨在涵盖以下实施方案中的每个实施方案:a、b和c;a、b或c;a或c;a或b;b或c;a和c;a和b;b和c;a(单独);b(单独);和c(单独)。
[0091]
5.2低岩藻糖基化
[0092]
抗体糖基化是一种类型的翻译后修饰,其可经由低聚糖通过两种类型的共价键一天冬酰胺残基上的键(n-低聚糖)或丝氨酸/苏氨酸残基上的键(o-低聚糖)添加到抗体中而发生(alter,g.等人,semin immunol.,2018,39:102-10)并且明显影响抗体的治疗性功能(walsh,g.和jefferis,r.,nat.biotechnol.,2006,24:1241-52;jefferis,r.,nat.rev.drug discov.,2009,8(3):226-34;dalziel,m.等人,science,2014,343(6166):1235681)。值得注意的是,所有igg抗体均在保守性asn-297残基上糖基化在其fc区中(alter g.等人,出处同上)。
[0093]
asn-297-连接的n-低聚糖由保守双天线核心结构(liu,l.,j pharm sci.,2015,104(6):1866-84)构成,该保守双天线核心结构由进一步连接至甘露糖的两个共价连接的n-乙酰基葡糖胺(glcnac)残基组成并以1,3-和1,6-支化方式连接至两个其他甘露糖残基(alter,g.等人,出处同上)。附加的单糖,包括两种半乳糖、岩藻糖、二等分glcnac和两种唾液酸(alter,g.等人,出处同上)可延伸核心结构,从而产生相当大的结构和功能不均匀性(jefferis,r.,biochem j.,1990,268(3):529-37;rudd,p.m.,science,2001,291(5512):2370-6;liu,l.,出处同上)。已经报道了用于igg asn-297连接的n-低聚糖的至少30种结构(糖型)(alter,g.等人,出处同上)。
[0094]
在哺乳动物细胞中表达的抗体通常是大于80%岩藻糖基化的(kamoda,s.等人,j chromatogra.,2004,1050(2):211-6;shinkawa,t.等人,j biol chem.,2003,278(5):3466-73)。例如,正常中国仓鼠卵巢(cho)细胞和hek293细胞将岩藻糖添加至igg抗体上的80%-98%asn-297-连接的n-低聚糖中(shields,r.l.等人,jbiol chem.,2002,277(30):26733-40)。
[0095]
在一个方面,本文提供了一种抗体,该抗体在连接至其fc区并且在fc区中具有re突变的低聚糖中不合岩藻糖。在另一方面,本文提供了一种抗体群体,该抗体群体在连接至
其fc区并且在fc区中具有re突变的低聚糖中不合岩藻糖。在又一方面,本文提供了一种抗体群体,其中少于80%的共价连接至抗体群体的低聚糖包含岩藻糖残基并且这些抗体的fc区包含k248e和t437r突变(re突变)。
[0096]
在一些实施方案中,少于70%的共价连接至抗体群体的低聚糖包含岩藻糖残基。在一些实施方案中,少于60%的共价连接至抗体群体的低聚糖包含岩藻糖残基。在一些实施方案中,少于50%的共价连接至抗体群体的低聚糖包含岩藻糖残基。在其他实施方案中,少于40%的共价连接至抗体群体的低聚糖包含岩藻糖残基。在另外的实施方案中,少于30%的共价连接至抗体群体的低聚糖包含岩藻糖残基。在另外的实施方案中,少于20%的共价连接至抗体群体的低聚糖包含岩藻糖残基。在另外的实施方案中,少于10%的共价连接至抗体群体的低聚糖包含岩藻糖残基。
[0097]
可使用本领域技术人员已知的标准技术例如质谱法来表征抗体上的asn297-连接的n-低聚糖(pereira,n.a.等人,出处同上;shields,r.l.等人,出处同上)。例如,在基质辅助激光解吸/电离飞行时间质谱(maldi-tof-ms)分析中,将50mg的igg抗体固定在multiscreen 96孔ip板(millipore)中的聚偏二氟乙烯膜上。然后使用50ml 0.1m dtt在rcm缓冲液(ph 8.6,3.2mm edta,360mm tris和8m尿素)中的溶液来还原蛋白质。接下来,将其在黑暗中在25℃下在含有0.1m碘乙酸的rcm缓冲液中温育30分钟,以便将由还原步骤产生的游离巯基基团羧甲基化。然后将膜结合的蛋白质在25℃下在1%聚乙烯吡咯烷酮360(sigma)的水溶液中温育1小时,并且通过三步法从蛋白质中裂解其低聚糖:在37℃下在ph为8.4的含有32个肽:n-糖苷酶f单位(new england biolabs,beverly,ma)的tris乙酸盐缓冲液(25ml)中温育3小时,添加1.5m乙酸(2.5ml)以降低ph,并在25℃下温育3小时(shields,r.l.等人,jbiol chem.,2001,276(9):6591-604)。
[0098]
在一些实施方案中,通过在宿主细胞中表达编码抗体或其片段的多核苷酸来产生本文提供的抗体,该宿主细胞不足以将岩藻糖添加到连接至抗体的低聚糖。
[0099]
在哺乳动物细胞中,fut8编码唯一的酶α-1,6岩藻糖基转移酶,该酶催化核心岩藻糖基化、gdp-岩藻糖残基经由α-1,6-键转移至最内glcnac(imai-nishiya,h.等人,bmc biotechnol.,2007,7:84)。低聚糖岩藻糖基化需要细胞内gdp-岩藻糖作为底物,细胞内gdp-岩藻糖经由从头途径或补救途径在细胞质中合成。在从头途径中,gdp-甘露糖4,6-脱水酶(gmd)介导由gdp-甘露糖合成gdp-4-酮-6-脱氧-甘露糖(gkdm),之后进行由gdp-酮-6-脱氧甘露糖3,5-表异构酶4-还原酶(fx)介导的gdp-岩藻糖的合成(imai-nishiya,h.等人,出处同上)。因此,已经发现,缺乏gmd酶的细胞系例如cho lec13细胞或由突变的fut8基因引起的α-1,6岩藻糖基转移酶活性降低的细胞系生成非岩藻糖基化抗体(pereira,n.a.等人,mabs,2018,10(5):693-711)。例如,具有大约10%(shields,r.l.等人,出处同上)或更少岩藻糖基化的抗体可始终在lec13细胞中产生(shields,r.l.等人,出处同上;kanda y.,biotechnol bioeng.,2006,94(4):680-8),而当将细胞在静态烧瓶中培养至汇合时可发生岩藻糖基化增加(pereira,n.a.等人,出处同上)。
[0100]
将二等分glcnac添加到低聚糖核心结构对岩藻糖基化产生空间位阻(alter,g.等人,出处同上)。因此,发现β-1,4-甘露糖基-糖蛋白4-β-n-乙酰葡糖氨基转移酶(gnt-iii,其催化将二等分glcnac添加到最内部甘露糖)的过表达显著减少fc岩藻糖基化(pereira,n.a.等人,出处同上)。
[0101]
此外,已经发现,灭活的golgi gdp-岩藻糖转运蛋白(gft)基因(slc35c1)例如在cho-gmt3细胞中产生非岩藻糖基化抗体(pereira,n.a.等人,出处同上)。使用岩藻糖基化的生物化学抑制剂例如岩藻糖类似物诸如2-氟岩藻糖和5-炔基岩藻糖也可生成非岩藻糖基化抗体(pereira,n.a.等人,出处同上)。哺乳动物细胞中的从头岩藻糖合成途径中的中间体gkdm可被细菌gdp-4-酮-6-脱氧甘露糖还原酶(rmd)还原成gdp-鼠李糖,从而避开岩藻糖生物合成途径。非岩藻糖基化抗体也可在其中细菌rmd在胞质溶胶中异源表达的细胞中生成(pereira,n.a.等人,出处同上)。
[0102]
在一些实施方案中,本文提供的抗体是通过在缺乏上述酶中的任何酶的宿主细胞中表达抗体来产生的。在一些实施方案中,宿主细胞具有降低的gdp-甘露糖4,6-脱水酶(gmd)活性。在一些实施方案中,宿主细胞具有降低的α-1,6岩藻糖基转移酶活性。
[0103]
5.3具有增强的效应子功能的fc突变
[0104]
本文提供的抗体在fc区中的位置248的赖氨酸(k248)(eu编号)处和位置437的苏氨酸(t437)(eu编号)处具有突变。不同igg亚型中位置248的赖氨酸(k248)(eu编号)和位置437的苏氨酸(t437)(eu编号)均为fc区中的保守残基(zhang,d.等人,出处同上)。发现fc突变t437r和k248e(eu编号)促进抗体在细胞表面结合抗原时低聚化,并具有增强的效应子功能(zhang,d.等人,出处同上)。发现t437r和k248e双突变(
″
re突变
″
)以剂量依赖性方式赋予不具有cdc活性的野生型iggl抗体cdc活性(zhang,d.等人,出处同上)。
[0105]
当提及免疫球蛋白重链恒定区中的残基时,通常使用
″
eu编号
″
或
″
eu索引
″
。它是指人igg1eu抗体的残基编号。它是通过将抗体序列与eu抗体序列进行比对(edelman,g.m.等人,proc natl acad sci u s a,1969,63(1):78-85;kabat等人,出处同上),使得与eu抗体中的残基同源的每个残基将具有与eu残基相同的残基编号而计算的。
[0106]
还已经发现,包含其他fc区突变例如s239d/i332e和s239d/i332e/a330l(eu编号)的抗体经由与fcγr增强的结合而表现出显著增强的adcc(lazar,g.a.等人,proc natl acad sci u s a,2006,103(11):4005-10)。
[0107]
5.4抗体依赖性细胞介导的细胞毒性(adcc)和补体依赖性细胞毒性(cdc)效应子功能
[0108]
本文提供的抗体的抗体群体具有增强的adcc活性和增强的cdc活性两者。
[0109]
治疗性抗体在效应细胞诸如自然杀伤(nk)细胞、巨噬细胞、单核吞噬细胞、中性粒细胞和嗜酸性粒细胞的细胞表面上结合fc受体(saunder,k.o.,front immunol.,2019,10:1296),从而产生重要的抗体依赖性效应子功能,诸如抗体依赖性细胞介导的细胞毒性(adcc)和抗体依赖性细胞介导的吞噬作用(adcp)。igg fc区的受体家族被称为fcγ受体(fcγr)(cohen-solal,j.f.,immunol lett.,2004,92(3):199-205),并且由以下构成:fcγri;fcyrii,包括亚型fcγriia、fcγriib和fcγriic;和fcγriii,包括亚型fcγriiia和fcγriiib(jefferis,r.和lund,j.,immunol lett.,2002,82(1-2):57-65)。
[0110]
在各种效应子功能中,已经发现adcc和adcp具有临床上显著的抗肿瘤功效。例如,发现adcc是曲妥珠单抗在体外的抗肿瘤功效,如通过nk细胞能够经由fcγriii受体(cd16)介导的adcc机制杀死曲妥珠单抗包被的肿瘤细胞所证实的(cooley,s.等人,exp hematol.,1999;27(10):1533-41;carson,w.e.等人,eur j immunol.,2001,31(10):3016-3025;kubo,m.等人,anticancer res.,2003,23(6a):4443-9);和在体内的抗肿瘤功效的重
要机制,如通过在曲妥珠单抗处理后肿瘤浸润物中nk细胞的数量增加所证实的(clynes,r.a.等人,nat med.,2000,6(4):443-6;amould,l.等人,br j cancer,2006,94(2):259-67)。另外,已经发现,巨噬细胞介导的adcp在曲妥珠单抗的抗肿瘤功效中很重要(shi,y.等人,j immunol.,2015,194(9):4379-86)。
[0111]
不具有或具有低岩藻糖基化的抗体因对fcγriiia结合的结合能力增强而示出显著增强的adcc活性,而cdc或抗原结合能力未发生任何可检测变化(okazaki,a.等人,j mol biol.,2004,336(5):1239-49;kanda,y.等人,glycobiology,2007,17(1):104-18)。抗体fc区的n-低聚糖对于与fcγr结合是必不可少的,fcγr参与抗体效应子功能(yamane-ohnuki,n.和satoh,m.,mabs,2009,1(3):230-6)。
[0112]
已经发现,在抗体fc区的n-低聚糖上不存在岩藻糖显著增强了抗体对免疫效应细胞诸如自然杀伤(nk)细胞和巨噬细胞上存在的fcγriiia受体的结合能力,从而产生抗肿瘤治疗效果(pereira,n.a.等人,出处同上)。fcγriiia受体经由与fc的铰链区和ch2结构域的相互作用接合fc区(radaev,s.等人,j biol chem.,2001,276:16469-77;sondermann,p.等人,nature,2000,406:267-73)。不存在岩藻糖因此消除空间位阻并增强fc-fcγriiia相互作用,导致效应子功能增强(pereira,n.a.等人,出处同上)。
[0113]
补体依赖性细胞毒性(cdc)是另一种重要的抗体效应子功能。在抗体依赖性经典补体活化途径中,补体c1q异源六聚化headpiece与低聚抗体复合物之间的结合引发蛋白水解补体级联(wang,g.等人,mol cell,2016,63:135-45;diebolder,c.a.等人,science,2014,343:1260-3),这导致靶细胞通过c3衍生的调理素(例如c3b)被调理并生成强效的炎症介质(c3a和c5a),最终导致在靶细胞膜上形成膜攻击复合物(mac)c5b-c9(reis,e.s.等人,nat rev immunol.,2018,18:5-18)。还已经发现,cdc例如在抗cd20 mab利妥昔单抗和抗cd38mab达雷木单抗中具有临床上显著的抗肿瘤功效(de weers,m.等人,j immunol.,2011年,186:1840-8;lokhorst,h.m.等人,nengl j med.,2015,373:1207-19;taylor,r.p.和lindorfer,m.a.,semin immuno1.,2016,28:309-16)。
[0114]
已经发现,有利于抗体低聚化的fc区中的突变(诸如re突变和e345r(eu编号))显著增强抗体cdc活性(diebolder,c.a.等人,出处同上;zhang,d.等人,出处同上)。
[0115]
在一些实施方案中,本发明抗体的adcc活性比具有正常岩藻糖基化的抗体高10%。在一些实施方案中,本发明抗体的adcc活性比具有正常岩藻糖基化的抗体高20%。在一些实施方案中,本发明抗体的adcc活性比具有正常岩藻糖基化的抗体高30%。在一些实施方案中,本发明抗体的adcc活性比具有正常岩藻糖基化的抗体高40%。在一些实施方案中,本发明抗体的adcc活性比具有正常岩藻糖基化的抗体高50%。在一些实施方案中,本发明抗体的adcc活性比具有正常岩藻糖基化的抗体高60%。在一些实施方案中,本发明抗体的adcc活性比具有正常岩藻糖基化的抗体高70%。在一些实施方案中,本发明抗体的adcc活性比具有正常岩藻糖基化的抗体高80%。在一些实施方案中,本发明抗体的adcc活性比具有正常岩藻糖基化的抗体高90%。在一些实施方案中,本发明抗体的adcc活性为具有正常岩藻糖基化的抗体的2倍以上。在一些实施方案中,本发明抗体的adcc活性为具有正常岩藻糖基化的抗体的3倍以上。在一些实施方案中,本发明抗体的adcc活性为具有正常岩藻糖基化的抗体的4倍以上。在一些实施方案中,本发明抗体的adcc活性为具有正常岩藻糖基化的抗体的5倍以上。在一些实施方案中,本发明抗体的adcc活性为具有正常岩藻糖基化的抗
体的6倍以上。在一些实施方案中,本发明抗体的adcc活性为具有正常岩藻糖基化的抗体的7倍以上。在一些实施方案中,本发明抗体的adcc活性为具有正常岩藻糖基化的抗体的8倍以上。在一些实施方案中,本发明抗体的adcc活性为具有正常岩藻糖基化的抗体的9倍以上。在一些实施方案中,本发明抗体的adcc活性为具有正常岩藻糖基化的抗体的10倍以上。
[0116]
在一些实施方案中,上述抗体还具有更高的cdc活性。在一些实施方案中,本发明抗体的cdc活性比不具有re突变的抗体高10%。在一些实施方案中,本发明抗体的cdc活性比不具有re突变的抗体高20%。在一些实施方案中,本发明抗体的cdc活性比不具有re突变的抗体高30%。在一些实施方案中,本发明抗体的cdc活性比不具有re突变的抗体高40%。在一些实施方案中,本发明抗体的cdc活性比不具有re突变的抗体高50%。在一些实施方案中,本发明抗体的cdc活性比不具有re突变的抗体高60%。在一些实施方案中,本发明抗体的cdc活性比不具有re突变的抗体高70%。在一些实施方案中,本发明抗体的cdc活性比不具有re突变的抗体高80%。在一些实施方案中,本发明抗体的cdc活性比不具有re突变的抗体高90%。在一些实施方案中,本发明抗体的cdc活性为不具有re突变的抗体的2倍以上。在一些实施方案中,本发明抗体的cdc活性为不具有re突变的抗体的3倍以上。在一些实施方案中,本发明抗体的cdc活性为不具有re突变的抗体的4倍以上。在一些实施方案中,本发明抗体的cdc活性为不具有re突变的抗体的5倍以上。在一些实施方案中,本发明抗体的cdc活性为不具有re突变的抗体的6倍以上。在一些实施方案中,本发明抗体的cdc活性为不具有re突变的抗体的7倍以上。在一些实施方案中,本发明抗体的cdc活性为不具有re突变的抗体的8倍以上。在一些实施方案中,本发明抗体的cdc活性为不具有re突变的抗体的9倍以上。在一些实施方案中,本发明抗体的cdc活性为不具有re突变的抗体的10倍以上。
[0117]
5.5抗hla-g抗体和相关分子
[0118]
在一个方面,本文提供了抗hla-g抗体。
[0119]
在一些实施方案中,抗体是mhgb732,其具有包含seq id no:172的氨基酸序列的vl和包含seq id no:174的氨基酸序列的vh。在一些实施方案中,抗体是mhgb738,其具有包含seq id no:173的氨基酸序列的vl和包含seq id no:175的氨基酸序列的vh。
[0120]
在一些实施方案中,本文提供了与hla-g结合的抗体,其中抗体包含:(i)vh,该vh包含分别具有seq id no:174的vh cdr1、vh cdr2和vh cdr3的氨基酸序列的vh cdr1、vh cdr2和vh cdr3;和(ii)vl,该vl包含分别具有seq id no:172的vl cdr1、vl cdr2和vl cdr3的氨基酸序列的vl cdr1、vl cdr2和vl cdr3。在一些实施方案中,本文提供了与hla-g结合的抗体,其中抗体包含:(i)vh,该vh包含分别具有seq id no:175的vh cdr1、vh cdr2和vh cdr3的氨基酸序列的vh cdr1、vh cdr2和vh cdr3;和(ii)vl,该vl包含分别具有seq id no:173的vl cdr1、vl cdr2和vl cdr3的氨基酸序列的vl cdr1、vl cdr2和vl cdr3。在一些实施方案中,本文提供了与hla-g结合的抗体,其中抗体包含:(i)vh,该vh包含分别具有seq id no:174的vh cdr1、vh cdr2和vh cdr3的氨基酸序列的vh cdr1、vh cdr2和vh cdr3;和(ii)vl,该vl包含分别具有seq id no:173的vl cdr1、vl cdr2和vl cdr3的氨基酸序列的vl cdr1、vl cdr2和vl cdr3。在一些实施方案中,本文提供了与hla-g结合的抗体,其中抗体包含:(i)vh,该vh包含分别具有seq id no:175的vh cdr1、vh cdr2和vh cdr3的氨基酸序列的vh cdr1、vh cdr2和vh cdr3;和(ii)vl,该vl包含分别具有seq id no:172的vl cdr1、vl cdr2和vl cdr3的氨基酸序列的vl cdr1、vl cdr2和vl cdr3。
id no:218)的氨基酸序列的vl cdr2和具有yhstpw(seq id no:219)的氨基酸序列的vl cdr3。
[0128]
在另一方面,本文提供了与hla-g结合的抗体,其中抗体包含:(i)vh,该vh包含具有gdsvssnraa(seq id no:220)的氨基酸序列的vh cdr1、具有tyyrskwyn(seq id no:221)的氨基酸序列的vh cdr2和具有arvrpgipfdy(seq id no:222)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有qsvlfssnnkny(seq id no:223)的氨基酸序列的vl cdr1、具有was(seq id no:224)的氨基酸序列的vl cdr2和具有qqyhstpwt(seq id no:225)的氨基酸序列的vl cdr3。
[0129]
在另一方面,本文提供了与hla-g结合的抗体,其中抗体包含:(i)vh,该vh包含具有gdsvssnraawn(seq id no:226)的氨基酸序列的vh cdr1、具有rtyyrskwynd(seq id no:227)的氨基酸序列的vh cdr2和具有vrpgipfdy(seq id no:228)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有kssqsvlfssnnknyla(seq id no:229)的氨基酸序列的vl cdr1、具有wastres(seq id no:230)的氨基酸序列的vl cdr2和具有qqyhstpwt(seq id no:231)的氨基酸序列的vl cdr3。
[0130]
在一些实施方案中,抗体包含具有seq id no:174的氨基酸序列的vh。在一些实施方案中,抗体包含具有seq id no:172的氨基酸序列的vl。在一些实施方案中,抗体包含vh,该vh包含与seq id no:174的氨基酸序列具有至少95%同一性的氨基酸序列。在一些实施方案中,抗体包含vl,该vl包含与seq id no:172的氨基酸序列具有至少95%同一性的氨基酸序列。
[0131]
在一些实施方案中,抗体包含具有seq id no:175的氨基酸序列的vh。在一些实施方案中,抗体包含具有seq id no:173的氨基酸序列的vl。在一些实施方案中,抗体包含vh,该vh包含与seq id no:175的氨基酸序列具有至少95%同一性的氨基酸序列。在一些实施方案中,抗体包含vl,该vl包含与seq id no:173的氨基酸序列具有至少95%同一性的氨基酸序列。
[0132]
在又一方面,本文提供了与上述其抗体中的一者竞争的抗体。此类抗体还可结合与上述抗体中的一者或重叠表位相同的表位。与上述抗体竞争或结合相同表位的抗体预期表现出类似的功能特性。
[0133]
在某些实施方案中,本文所述的抗体包含相对于上述抗体具有某些百分比同一性的氨基酸序列,并包括以下第7部分中描述的示例性抗体。
[0134]
两个序列(例如,氨基酸序列或核酸序列)之间的同一性百分比的测定可使用数学算法来完成。用于比较两个序列的数学算法的优选非限制性示例为karlin和altschul,proc.natl.acad.sci.u.s.a.,1990,87:2264-8的算法,如karlin和altschul,proc.natl.acad.sci.u.s.a.,1993,90:5873-7中那样进行修改。此类算法并入altschul等人,j.mol.biol.,1990,215:403的nblast和xblast程序中。可用nblast核苷酸程序参数集进行blast核苷酸检索,例如,对于评分=100,字长=12,以获得与本文所述的核酸分子同源的核苷酸序列。可用xblast程序参数集进行blast蛋白质检索,例如,对于得分50,字长=3,以获得与本文所述的蛋白质分子同源的氨基酸序列。为了获得用于比较目的的空位比对,可如altschul等人,nucleic acids res.,1997,25:3389-402中所述利用空位blast。另选地,可使用psi blast执行检测分子之间的距离关系(id.)的迭代检索。当利用blast、空
位blast和psi blast程序时,可使用相应程序(例如xblast和nblast)的默认参数(参见例如,万维网上的国家生物技术信息中心(ncbi),ncbi.nlm.nih.gov)。用于比较序列的数学算法的另一优选非限制性示例为myers和miller,1988,cabios 4:1117的算法。此类算法并入align程序(版本2.0)中,其是gcg序列比对软件包的一部分。当利用align程序比较氨基酸序列时,可使用pam120权重残基表、空位长度罚分12、空位罚分4。
[0135]
两个序列之间的同一性百分比可使用与上述那些类似的技术来确定,允许或不允许空位。在计算百分比同一性时,通常仅计数精确匹配。
[0136]
在某些实施方案中,本文提供的抗体包含与seq id no:174的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区以及/或者与seq id no:172的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区,其中抗体与hla-g结合。
[0137]
在某些实施方案中,本文提供的抗体包含与seq id no:175的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区以及/或者与seq id no:173的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区,其中抗体与hla-g结合。
[0138]
在某些实施方案中,本文提供的抗体包含与seq id no:174的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区以及/或者与seq id no:173的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区,其中抗体与hla-g结合。
[0139]
在某些实施方案中,本文提供的抗体包含与seq id no:175的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区以及/或者与seq id no:172的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区,其中抗体与hla-g结合。
[0140]
在一些实施方案中,本文提供了一种抗体,该抗体包含上述抗hla-g抗体的vh、vl或cdr序列并且还包含具有re突变但不具有岩藻糖残基的fc区。
[0141]
在一些实施方案中,本文提供的抗hla-g抗体包含具有re突变并且不具有岩藻糖残基的fc区。
[0142]
本领域技术人员已知的标准技术可用于在编码本文提供的分子的核苷酸序列中引入突变,包括例如导致氨基酸突变的定点诱变和pcr介导的诱变。
[0143]
在一些实施方案中,谷氨酸被本文提供的抗体的fc区的位置248的赖氨酸(k248e)(eu编号)取代。在一些实施方案中,精氨酸被本文提供的抗体的fc区的位置437的苏氨酸(t437r)(eu编号)取代。在一些实施方案中,谷氨酸被本文提供的抗体的fc区的位置248的赖氨酸取代并且精氨酸被位置437的苏氨酸(k248e/t437r)(eu编号)取代。
[0144]
在一些实施方案中,本文提供的抗体包含重链,该重链包含t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含k248e突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含k338a突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含k248e/t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含k338a/t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:182的氨基酸序列但具有t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链
包含seq id no:182的氨基酸序列但具有k248e突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:182的氨基酸序列但具有k338a突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:182的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:182的氨基酸序列但具有k338a/t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:183的氨基酸序列但具有t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:183的氨基酸序列但具有k248e突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:183的氨基酸序列但具有k338a突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:183的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:183的氨基酸序列但具有k338a/t437r突变。在一些实施方案中,抗体是mhgb752,其包含重链,该重链包含seq id no:182的氨基酸序列但具有k248e和t437r突变(re突变)。在一些实施方案中,抗体是mhgb758,其包含重链,该重链包含seq id no:183的氨基酸序列但具有k248e和t437r突变(re突变)。在一些实施方案中,本文提供的抗体(包括上述抗hla-g抗体)不是岩藻糖基化的。
[0145]
可使用本领域技术人员已知的标准技术来生成本文提供的抗体,其中重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。例如,已经发现,缺乏gmd酶(例如cho lec13细胞)的、由突变的fut8基因引起的α-1,6岩藻糖基转移酶活性降低的、β-1,4-甘露糖基-糖蛋白4-β-n-乙酰葡糖氨基转移酶(gnt-iii)过表达的、golgi gdp-岩藻糖转运蛋白(gft)基因slc35c1灭活的(例如,cho-gmt3细胞)、细菌rmd异源表达的或者使用岩藻糖基化的生物化学抑制剂(例如,岩藻糖类似物诸如2-氟岩藻糖和5-炔基岩藻糖)的哺乳动物细胞系产生在重链上的asn-297-连接的n-低聚糖上不具有岩藻糖残基的抗体(pereira,n.a.等人,出处同上;shields,r.l.等人,出处同上;kanda y.,出处同上)。
[0146]
在一些实施方案中,抗体包含重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是mhgb732.clf,其具有包含seq id no:180的氨基酸序列的轻链和包含seq id no:182的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是mhgb738.clf,其具有包含seq id no:181的氨基酸序列的轻链和包含seq id no:183的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:182的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:183的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含k248e、k338a、t437r、k248e/t437r或k338a/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:182的氨基酸序列并包含k248e、k338a、t437r、k248e/t437r或k338a/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:183的氨基酸序列并包含k248e、k338a、t437r、k248e/t437r或k338a/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。
[0147]
5.6抗cd37抗体和相关分子
[0148]
在一些实施方案中,本文提供了抗cd37抗体。在一些实施方案中,本文提供的抗体包含具有下表5和下表6中的vl和vh序列中所含的vl、vh或cdr的氨基酸序列的vl、vh或cdr。
[0149]
在一些实施方案中,抗体是t26b373、t26b459或t26b608,其具有包含seq id no:1的氨基酸序列的vl和包含seq id no:9的氨基酸序列的vh。在一些实施方案中,抗体是t26b374、t26b460或t26b611,其具有包含seq id no:2的氨基酸序列的vl和包含seq id no:10的氨基酸序列的vh。在一些实施方案中,抗体是t26b375、t26b461或t26b612,其具有包含seq id no:3的氨基酸序列的vl和包含seq id no:11的氨基酸序列的vh。在一些实施方案中,抗体是t26b379、t26b462或t26b615,其具有包含seq id no:4的氨基酸序列的vl和包含seq id no:12的氨基酸序列的vh。在一些实施方案中,抗体是t26b382、t26b463或t26b613,其具有包含seq id no:5的氨基酸序列的vl和包含seq id no:13的氨基酸序列的vh。在一些实施方案中,抗体是t26b385、t26b464或t26b610,其具有包含seq id no:6的氨基酸序列的vl和包含seq id no:14的氨基酸序列的vh。在一些实施方案中,抗体是t26b386、t26b465或t26b614,其具有包含seq id no:7的氨基酸序列的vl和包含seq id no:15的氨基酸序列的vh。在一些实施方案中,抗体是t26b388、t26b466或t26b609,其具有包含seq id no:8的氨基酸序列的vl和包含seq id no:16的氨基酸序列的vh。
[0150]
在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:1的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:9的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:1的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:10的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:1的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:11的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:1的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:12的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:1的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:13的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:1的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:14的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:1的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:15的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:1的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:16的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:2的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:9的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:2的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:10的
氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:2的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:11的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:2的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:12的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:2的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:13的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:2的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:14的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:2的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:15的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:2的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:16的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:3的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:9的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:3的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:10的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:3的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:11的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:3的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:12的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:3的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:13的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:3的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:14的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:3的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:15的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:3的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:16的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:4的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:9的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:4的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:10
的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:4的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:11的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:4的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:12的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:4的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:13的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:4的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:14的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:4的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:15的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:4的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:16的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:5的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:9的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:5的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:10的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:5的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:11的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:5的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:12的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:5的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:13的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:5的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:14的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:5的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:15的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:5的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:16的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:6的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:9的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:6的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:10
的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:6的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:11的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:6的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:12的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:6的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:13的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:6的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:14的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:6的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:15的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:6的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:16的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:7的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:9的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:7的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:10的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:7的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:11的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:7的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:12的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:7的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:13的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:7的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:14的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:7的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:15的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:7的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:16的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:8的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:9的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:8的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:10
的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:8的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:11的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:8的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:12的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:8的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:13的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:8的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:14的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:8的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:15的氨基酸序列的vh中所含的cdr的氨基酸序列。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:8的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:16的氨基酸序列的vh中所含的cdr的氨基酸序列。
[0151]
在又一方面,本文提供了与上述其抗体中的一者竞争的抗体。此类抗体还可结合与上述抗体中的一者或重叠表位相同的表位。与上述抗体竞争或结合相同表位的抗体预期表现出类似的功能特性。例示的抗原结合蛋白包括具有本文提供的vl区和vh区的那些,包括表5和表6中的那些。
[0152]
在某些实施方案中,本文所述的抗体包含相对于上述抗体具有某些百分比同一性的氨基酸序列,并包括以下第7部分中描述的示例性抗体。
[0153]
两个序列(例如,氨基酸序列或核酸序列)之间的同一性百分比的测定可使用数学算法来完成。用于比较两个序列的数学算法的优选非限制性示例为karlin和altschu1,proc.natl.acad.sci.u.s.a.,1990,87:2264-8的算法,如karlin和altschul,proc.natl.acad.sci.u.s.a.,1993,90:5873-7中那样进行修改。此类算法并入altschul等人,j.mol.biol.,1990,215:403的nblast和xblast程序中。可用nblast核苷酸程序参数集进行blast核苷酸检索,例如,对于评分=100,字长=12,以获得与本文所述的核酸分子同源的核苷酸序列。可用xblast程序参数集进行blast蛋白质检索,例如,对于得分50,字长=3,以获得与本文所述的蛋白质分子同源的氨基酸序列。为了获得用于比较目的的空位比对,可如altschul等人,nucleic acids res.,1997,25:3389-402中所述利用空位blast。另选地,可使用psi blast执行检测分子之间的距离关系(id.)的迭代检索。当利用blast、空位blast和psi blast程序时,可使用相应程序(例如xblast和nblast)的默认参数(参见例如,万维网上的国家生物技术信息中心(ncbi),ncbi.nlm.nih.gov)。用于比较序列的数学算法的另一优选非限制性示例为myers和miller,1988,cabios 4:1117的算法。此类算法并入align程序(版本2.0)中,其是gcg序列比对软件包的一部分。当利用align程序比较氨基酸序列时,可使用pam120权重残基表、空位长度罚分12、空位罚分4。
[0154]
两个序列之间的同一性百分比可使用与上述那些类似的技术来确定,允许或不允许空位。在计算百分比同一性时,通常仅计数精确匹配。
[0155]
在某些实施方案中,本文提供的抗体包含与seq id no:1的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:9的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:1中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:9中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:1的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:10的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:1中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:10中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:1的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:11的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:1中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:11中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:1的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:12的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:1中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:12中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:1的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:13的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:1中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:13中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:1的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:14的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含
与seq id no:1中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:14中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:1的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:15的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:1中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:15中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:1的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:16的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:1中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:16中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:2的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:9的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:2中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:9中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:2的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:10的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:2中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:10中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:2的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:11的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:2中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:11中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:2的氨基酸序列具有至
少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:12的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:2中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:12中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:2的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:13的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:2中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:13中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:2的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:14的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:2中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:14中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:2的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:15的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:2中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:15中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:2的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:16的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:2中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:16中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:3的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:9的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:3中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至
no:15的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:3中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:15中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:3的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:16的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:3中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:16中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:4的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:9的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:4中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:9中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:4的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:10的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:4中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:10中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:4的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:11的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:4中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:11中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:4的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:12的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:4中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:12中所含的cdr的氨基酸
序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:4的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:13的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:4中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:13中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:4的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:14的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:4中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:14中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:4的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:15的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:4中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:15中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:4的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:16的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:4中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:16中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:5的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:9的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:5中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:9中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:5的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:10的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性
的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:5中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:10中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:5的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:11的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:5中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:11中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:5的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:12的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:5中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:12中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:5的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:13的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:5中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:13中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:5的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:14的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:5中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:14中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:5的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:15的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:5中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:15中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体
与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:5的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:16的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:5中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:16中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:6的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:9的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:6中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:9中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:6的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:10的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:6中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:10中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:6的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:11的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:6中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:11中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:6的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:12的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:6中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:12中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:6的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:13的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含
与seq id no:6中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:13中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:6的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:14的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:6中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:14中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:6的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:15的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:6中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:15中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:6的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:16的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:6中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:16中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:7的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:9的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:7中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:9中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:7的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:10的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:7中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:10中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:7的氨基酸序列具有至
少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:11的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:7中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:11中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:7的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:12的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:7中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:12中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:7的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:13的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:7中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:13中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:7的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:14的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:7中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:14中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:7的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:15的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:7中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:15中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:7的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:16的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:7中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或
至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:16中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:8的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:9的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:8中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:9中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:8的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:10的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:8中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:10中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。
[0156]
在某些实施方案中,本文提供的抗体包含与seq id no:8的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:11的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:8中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:11中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:8的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:12的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:8中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:12中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:8的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:13的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:8中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:13中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:8的氨基酸序列具有至
少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:14的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:8中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:14中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:8的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:15的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:8中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:15中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含与seq id no:8的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:16的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与cd37结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:8中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:16中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与cd37结合。
[0157]
在一些实施方案中,本文提供了一种抗体,该抗体包含上述抗cd37抗体的vh、vl或cdr序列并且还包含具有re突变但不具有岩藻糖残基的fc区。在一些实施方案中,抗体是t26b459,其具有包含seq id no:37的氨基酸序列的轻链和包含seq id no:53的氨基酸序列的重链。在一些实施方案中,抗体是t26b460,其具有包含seq id no:38的氨基酸序列的轻链和包含seq id no:54的氨基酸序列的重链。在一些实施方案中,抗体是t26b461,其具有包含seq id no:39的氨基酸序列的轻链和包含seq id no:55的氨基酸序列的重链。在一些实施方案中,抗体是t26b462,其具有包含seq id no:40的氨基酸序列的轻链和包含seq id no:56的氨基酸序列的重链。在一些实施方案中,抗体是t26b463,其具有包含seq id no:41的氨基酸序列的轻链和包含seq id no:57的氨基酸序列的重链。在一些实施方案中,抗体是t26b464,其具有包含seq id no:42的氨基酸序列的轻链和包含seq id no:58的氨基酸序列的重链。在一些实施方案中,抗体是t26b465,其具有包含seq id no:43的氨基酸序列的轻链和包含seq id no:59的氨基酸序列的重链。在一些实施方案中,抗体是t26b466,其具有包含seq id no:44的氨基酸序列的轻链和包含seq id no:60的氨基酸序列的重链。在一些实施方案中,抗体包含重链,该重链包含seq id no:45的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,抗体包含重链,该重链包含seq id no:46的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,抗体包含重链,该重链包含seq id no:47的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,抗体包含重链,该重链包含seq id no:48的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,抗体包含重
链,该重链包含seq id no:49的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,抗体包含重链,该重链包含seq id no:50的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,抗体包含重链,该重链包含seq id no:51的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,抗体包含重链,该重链包含seq id no:52的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,抗体包含重链,该重链包含seq id no:53的氨基酸序列。在一些实施方案中,抗体包含重链,该重链包含seq id no:54的氨基酸序列。在一些实施方案中,抗体包含重链,该重链包含seq id no:55的氨基酸序列。在一些实施方案中,抗体包含重链,该重链包含seq id no:56的氨基酸序列。在一些实施方案中,抗体包含重链,该重链包含seq id no:57的氨基酸序列。在一些实施方案中,抗体包含重链,该重链包含seq id no:58的氨基酸序列。在一些实施方案中,抗体包含重链,该重链包含seq id no:59的氨基酸序列。在一些实施方案中,抗体包含重链,该重链包含seq id no:60的氨基酸序列。
[0158]
在一些实施方案中,抗体包含重链,该重链包含seq id no:61的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,抗体包含重链,该重链包含seq id no:62的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,抗体包含重链,该重链包含seq id no:63的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,抗体包含重链,该重链包含seq id no:64的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,抗体包含重链,该重链包含seq id no:65的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,抗体包含重链,该重链包含seq id no:66的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,抗体包含重链,该重链包含seq id no:67的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,抗体包含重链,该重链包含seq id no:68的氨基酸序列但具有k248e/t437r突变。
[0159]
在一些实施方案中,抗体是t26b373.clf,其具有包含seq id no:37的氨基酸序列的轻链和包含seq id no:45的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是t26b374.clf,其具有包含seq id no:38的氨基酸序列的轻链和包含seq id no:46的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是t26b375.clf,其具有包含seq id no:39的氨基酸序列的轻链和包含seq id no:47的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是t26b379.clf,其具有包含seq id no:40的氨基酸序列的轻链和包含seq id no:48的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是t26b382.clf,其具有包含seq id no:41的氨基酸序列的轻链和包含seq id no:49的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是t26b385.clf,其具有包含seq id no:42的氨基酸序列的轻链和包含seq id no:50的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是t26b386.clf,其具有包含seq id no:43的氨基酸序列的轻链和包含seq id no:51的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是t26b388.clf,其具有包含seq id no:44的氨基酸序列的轻链和包含seq id no:52的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上
不包含岩藻糖残基。在一些实施方案中,抗体是t26b459.clf,其具有包含seq id no:37的氨基酸序列的轻链和包含seq id no:53的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是t26b460.clf,其具有包含seq id no:38的氨基酸序列的轻链和包含seq id no:54的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是t26b461.clf,其具有包含seq id no:39的氨基酸序列的轻链和包含seq id no:55的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是t26b462.clf,其具有包含seq id no:40的氨基酸序列的轻链和包含seq id no:56的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是t26b463.clf,其具有包含seq id no:41的氨基酸序列的轻链和包含seq id no:57的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是t26b464.clf,其具有包含seq id no:42的氨基酸序列的轻链和包含seq id no:58的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是t26b465.clf,其具有包含seq id no:43的氨基酸序列的轻链和包含seq id no:59的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是t26b466.clf,其具有包含seq id no:44的氨基酸序列的轻链和包含seq id no:60的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:45的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:46的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:47的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:48的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:49的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:50的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:51的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:52的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:53的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:54的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:55的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:56的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:57的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:58的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:59的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩
藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:60的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:61的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:62的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:63的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:64的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:65的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:66的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:67的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:68的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:45的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:46的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:47的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:48的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:49的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:50的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:51的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:52的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:53的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:54的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:55的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:56的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:57的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:58的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:59的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重
链包含seq id no:60的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:61的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:62的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:63的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:64的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:65的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:66的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:67的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:68的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。
[0160]
5.7抗gprc5d抗体和相关分子
[0161]
在其他实施方案中,本文提供了抗gprc5d抗体。在一些实施方案中,本文提供的抗体包含具有表13中的vl和vh序列中所含的vl、vh或cdr的氨基酸序列的vl、vh或cdr。
[0162]
在一些实施方案中,抗体是gc5b747或gc5b752,其具有包含seq id no:33的氨基酸序列的vl和包含seq id no:34的氨基酸序列的vh。在一些实施方案中,抗体包含:vl,该vl包含cdr,该cdr具有包含seq id no:33的氨基酸序列的vl中所含的cdr的氨基酸序列;和vh,该vh包含cdr,该cdr具有包含seq id no:34的氨基酸序列的vh中所含的cdr的氨基酸序列。
[0163]
在又一方面,本文提供了与上述其抗体中的一者竞争的抗体。此类抗体还可结合与上述抗体中的一者或重叠表位相同的表位。与上述抗体竞争或结合相同表位的抗体预期表现出类似的功能特性。例示的抗原结合蛋白包括具有本文提供的vl区和vh区的那些,包括表13中的那些。
[0164]
在某些实施方案中,本文所述的抗体包含相对于上述抗体具有某些百分比同一性的氨基酸序列,并包括以下第7部分中描述的示例性抗体。
[0165]
两个序列(例如,氨基酸序列或核酸序列)之间的同一性百分比的测定可使用数学算法来完成。用于比较两个序列的数学算法的优选非限制性示例为karlin和altschul,proc.natl.acad.sci.u.s.a.,1990,87:2264-8的算法,如karlin和altschul,proc.natl.acad.sci.u.sa.,1993,90:5873-7中那样进行修改。此类算法并入altschul等人,j.mol.biol.,1990,215:403的nblast和xblast程序中。可用nblast核苷酸程序参数集进行blast核苷酸检索,例如,对于评分=100,字长=12,以获得与本文所述的核酸分子同源的核苷酸序列。可用xblast程序参数集进行blast蛋白质检索,例如,对于得分50,字长=3,以获得与本文所述的蛋白质分子同源的氨基酸序列。为了获得用于比较目的的空位比
对,可如altschul等人,nucleic acids res.,1997,25:3389-402中所述利用空位blast。另选地,可使用psi blast执行检测分子之间的距离关系(id.)的迭代检索。当利用blast、空位blast和psi blast程序时,可使用相应程序(例如xblast和nblast)的默认参数(参见例如,万维网上的国家生物技术信息中心(ncbi),ncbi.nlm.nih.gov)。用于比较序列的数学算法的另一优选非限制性示例为myers和miller,1988,cabios 4:1117的算法。此类算法并入align程序(版本2.0)中,其是gcg序列比对软件包的一部分。当利用align程序比较氨基酸序列时,可使用pam120权重残基表、空位长度罚分12、空位罚分4。
[0166]
两个序列之间的同一性百分比可使用与上述那些类似的技术来确定,允许或不允许空位。在计算百分比同一性时,通常仅计数精确匹配。
[0167]
在某些实施方案中,本文提供的抗体包含与seq id no:33的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区以及/或者与seq id no:34的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区,其中抗体与gprc5d结合。在某些实施方案中,本文提供的抗体包含vl区,该vl区包含与seq id no:33中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr;和/或vh区,该vh区包含与seq id no:34中所含的cdr的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的cdr,其中抗体与gprc5d结合。
[0168]
在一些实施方案中,谷氨酸被本文提供的抗体的fc区的位置248的赖氨酸(k248e)(eu编号)取代。在一些实施方案中,精氨酸被本文提供的抗体的fc区的位置437的苏氨酸(t437r)(eu编号)取代。在一些实施方案中,谷氨酸被本文提供的抗体的fc区的位置248的赖氨酸取代并且精氨酸被位置437的苏氨酸(k248e/t437r)(eu编号)取代。
[0169]
在一些实施方案中,抗体是gc5b747,其具有包含seq id no:101的氨基酸序列的轻链和包含seq id no:102的氨基酸序列的重链。在一些实施方案中,抗体是gc5b752,其具有包含seq id no:101的氨基酸序列的轻链和包含seq id no:103的氨基酸序列的重链。在一些实施方案中,抗体包含重链,该重链包含seq id no:102的氨基酸序列并包含k248e、t437r或k248e/t437r突变。在一些实施方案中,抗体包含重链,该重链包含seq id no:103的氨基酸序列。
[0170]
在一些实施方案中,本文提供的抗体在fc区中不包含岩藻糖。在一些实施方案中,抗体是gc5b747.clf,其具有包含seq id no:101的氨基酸序列的轻链和包含seq id no:102的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是gc5b752.clf,其具有包含seq id no:101的氨基酸序列的轻链和包含seq id no:103的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:102的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:103的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。
[0171]
在一些实施方案中,本文提供的抗体包含k248e/t437r突变并且在fc区中不具有岩藻糖基化。在一些实施方案中,抗体是gc5b752.clf,其具有包含seq id no:101的氨基酸序列的轻链和包含seq id no:103的氨基酸序列的重链,该重链在其asn-297-连接的n-低
聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:102的氨基酸序列并包含k248e、t437r或k248e/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:103的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。
[0172]
5.8抗klk2抗体和相关分子
[0173]
在一个方面,本文提供了抗klk2抗体。
[0174]
在一些实施方案中,抗体是kl2b870,其具有包含seq id no:108的氨基酸序列的vl和包含seq id no:107的氨基酸序列的vh。在一些实施方案中,本文提供了与klk2结合的抗体,其中抗体包含:(i)vh,该vh包含分别具有seq id no:107的vh cdr1、vh cdr2和vh cdr3的氨基酸序列的vh cdr1、vh cdr2和vh cdr3;和(ii)vl,该vl包含分别具有seq id no:108的vl cdr1、vl cdr2和vl cdr3的氨基酸序列的vl cdr1、vl cdr2和vl cdr3。在一些实施方案中,vh cdr1、vh cdr2、vh cdr3、vl cdr1、vl cdr2和vl cdr3序列根据kabat编号系统。在一些实施方案中,vh cdr1、vh cdr2、vh cdr3、vl cdr1、vl cdr2和vl cdr3序列根据chothia编号系统。在一些实施方案中,vh cdr1、vh cdr2、vh cdr3、vl cdr1、vl cdr2和vl cdr3序列根据示例性编号系统。在一些实施方案中,vh cdr1、vh cdr2、vh cdr3、vl cdr1、vl cdr2和vl cdr3序列根据contact编号系统。在一些实施方案中,vh cdr1、vh cdr2、vh cdr3、vl cdr1、vl cdr2和vl cdr3序列根据imgt编号系统。在一些实施方案中,vh cdr1、vh cdr2、vh cdr3、vl cdr1、vl cdr2和vl cdr3序列根据abm编号系统。
[0175]
在另一方面,本文提供了与klk2结合的抗体,其中抗体包含:(i)vh,该vh包含具有ggsissyyws(seq id no:109)的氨基酸序列的vh cdr1、具有yiyysgstnynpslks(seq id no:110)的氨基酸序列的vh cdr2和具有ttifgvvtpnfyygmdv(seq id no:111)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有rasqgissyla(seq id no:112)的氨基酸序列的vl cdr1、具有aastlqs(seq id no:113)的氨基酸序列的vl cdr2和具有qqlnsyplt(seq id no:114)的氨基酸序列的vl cdr3。在另一方面,本文提供了与klk2结合的抗体,其中抗体包含:(i)vh,该vh包含具有ggsissyy(seq id no:115)的氨基酸序列的vh cdr1、具有iyysgst(seq id no:116)的氨基酸序列的vh cdr2和具有agttifgvvtpnfyygmdv(seq id no:117)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有qgissy(seq id no:118)的氨基酸序列的vl cdr1、具有aas(seq id no:119)的氨基酸序列的vl cdr2和具有qqlnsyplt(seq id no:120)的氨基酸序列的vl cdr3。在另一方面,本文提供了与klk2结合的抗体,其中抗体包含:(i)vh,该vh包含具有syyws(seq id no:121)的氨基酸序列的vh cdr1、具有yiyysgstnynpslks(seq id no:122)的氨基酸序列的vh cdr2和具有ttifgvvtpnfyygmdv(seq id no:123)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有rasqgissyla(seq id no:124)的氨基酸序列的vl cdr1、具有aastlqs(seq id no:125)的氨基酸序列的vl cdr2和具有qqlnsyplt(seq id no:126)的氨基酸序列的vl cdr3。在另一方面,本文提供了与klk2结合的抗体,其中抗体包含:(i)vh,该vh包含具有ggsissy(seq id no:127)的氨基酸序列的vh cdr1、具有ysg(seq id no:128)的氨基酸序列的vh cdr2和具有tifgvvtpnfyygmd(seq id no:129)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有sqgissy(seq id no:130)的氨基酸序列的vl cdr1、具有aas(seq id no:131)的氨基酸序列的vl cdr2和具有lnsypl(seq id no:132)的氨基酸序列的vl cdr3。在另一方面,本文提
供了与klk2结合的抗体,其中抗体包含:(i)vh,该vh包含具有ggsissy(seq id no:127)的氨基酸序列的vh cdr1、具有yysgs(seq id no:168)的氨基酸序列的vh cdr2和具有tifgvvtpnfyygmd(seq id no:129)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有rasqgissy(seq id no:169)的氨基酸序列的vl cdr1、具有aastlqs(seq id no:170)的氨基酸序列的vl cdr2和具有qqlnsyplt(seq id no:171)的氨基酸序列的vl cdr3。在另一方面,本文提供了与klk2结合的抗体,其中抗体包含:(i)vh,该vh包含具有ssyyws(seq id no:133)的氨基酸序列的vh cdr1、具有wigyiyysgstn(seq id no:134)的氨基酸序列的vh cdr2和具有agttifgvvtpnfyygmd(seq id no:135)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有ssylawy(seq id no:136)的氨基酸序列的vl cdr1、具有fliyaastlq(seq id no:137)的氨基酸序列的vl cdr2和具有qqlnsypl(seq id no:138)的氨基酸序列的vl cdr3。在另一方面,本文提供了与klk2结合的抗体,其中抗体包含:(i)vh,该vh包含具有ggsissyyws(seq id no:139)的氨基酸序列的vh cdr1、具有yiyysgstn(seq id no:140)的氨基酸序列的vh cdr2和具有ttifgvvtpnfyygmdv(seq id no:141)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有rasqgissyla(seq id no:142)的氨基酸序列的vl cdr1、具有aastlqs(seq id no:143)的氨基酸序列的vl cdr2和具有qqlnsyplt(seq id no:144)的氨基酸序列的vl cdr3。在一些实施方案中,抗体包含具有seq id no:107的氨基酸序列的vh。在一些实施方案中,抗体包含具有seq id no:108的氨基酸序列的vl。在一些实施方案中,抗体包含vh,该vh包含与seq id no:107的氨基酸序列具有至少95%同一性的氨基酸序列。在一些实施方案中,抗体包含vl,该vl包含与seq id no:108的氨基酸序列具有至少95%同一性的氨基酸序列。
[0176]
在又一方面,本文提供了与上述其抗体中的一者竞争的抗体。此类抗体还可结合与上述抗体中的一者或重叠表位相同的表位。与上述抗体竞争或结合相同表位的抗体预期表现出类似的功能特性。
[0177]
在某些实施方案中,本文所述的抗体包含相对于上述抗体具有某些百分比同一性的氨基酸序列,并包括以下第7部分中描述的示例性抗体。
[0178]
两个序列(例如,氨基酸序列或核酸序列)之间的同一性百分比的测定可使用数学算法来完成。用于比较两个序列的数学算法的优选非限制性示例为karlin和altschul,proc.natl.acad.sci.u.s.a.,1990,87∶2264-8的算法,如karlin和altschul,proc.natl.acad.sci.u.s.a.,1993,90:5873-7中那样进行修改。此类算法并入altschul等人,j.mol.biol.,1990,215:403的nblast和xblast程序中。可用nblast核苷酸程序参数集进行blast核苷酸检索,例如,对于评分=100,字长=12,以获得与本文所述的核酸分子同源的核苷酸序列。可用xblast程序参数集进行blast蛋白质检索,例如,对于得分50,字长=3,以获得与本文所述的蛋白质分子同源的氨基酸序列。为了获得用于比较目的的空位比对,可如altschul等人,nucleic acids res.,1997,25:3389-402中所述利用空位blast。另选地,可使用psi blast执行检测分子之间的距离关系(id.)的迭代检索。当利用blast、空位blast和psi blast程序时,可使用相应程序(例如xblast和nblast)的默认参数(参见例如,万维网上的国家生物技术信息中心(ncbi),ncbi.nlm.nih.gov)。用于比较序列的数学算法的另一优选非限制性示例为myers和miller,1988,cabios 4:1117的算法。此类算法并入align程序(版本2.0)中,其是gcg序列比对软件包的一部分。当利用align程序比较氨基
酸序列时,可使用pam120权重残基表、空位长度罚分12、空位罚分4。
[0179]
两个序列之间的同一性百分比可使用与上述那些类似的技术来确定,允许或不允许空位。在计算百分比同一性时,通常仅计数精确匹配。
[0180]
在某些实施方案中,本文提供的抗体包含与seq id no:107的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区以及/或者与seq id no:108的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区,其中抗体与klk2结合。
[0181]
在一些实施方案中,本文提供了一种抗体,该抗体包含上述抗klk2抗体的vh、vl或cdr序列并且还包含具有re突变但不具有岩藻糖残基的fc区。在一些实施方案中,本文提供的抗klk2抗体包含具有re突变并且不具有岩藻糖残基的fc区。
[0182]
本领域技术人员已知的标准技术可用于在编码本文提供的分子的核苷酸序列中引入突变,包括例如导致氨基酸突变的定点诱变和pcr介导的诱变。
[0183]
在一些实施方案中,谷氨酸被本文提供的抗体的fc区的位置248的赖氨酸(k248e)(eu编号)取代。在一些实施方案中,精氨酸被本文提供的抗体的fc区的位置437的苏氨酸(t437r)(eu编号)取代。在一些实施方案中,谷氨酸被本文提供的抗体的fc区的位置248的赖氨酸取代并且精氨酸被位置437的苏氨酸(k248e/t437r)(eu编号)取代。
[0184]
在一些实施方案中,本文提供的抗体包含重链,该重链包含t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含k248e突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含k338a突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含k248e/t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含k338a/t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:155的氨基酸序列但具有t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:155的氨基酸序列但具有k248e突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:155的氨基酸序列但具有k338a突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:155的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:155的氨基酸序列但具有k338a/t437r突变。在一些实施方案中,抗体是kl2b870,其包含重链,该重链包含seq id no:155的氨基酸序列但具有k248e和t437r突变(re突变)。
[0185]
在一些实施方案中,本文提供的抗体(包括上述抗klk2抗体)不是岩藻糖基化的。可使用本领域技术人员已知的标准技术来生成本文提供的抗体,其中重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。例如,已经发现,缺乏gmd酶(例如cho lec13细胞)的、由突变的fut8基因引起的α-1,6岩藻糖基转移酶活性降低的、β-1,4-甘露糖基-糖蛋白4-β-n-乙酰葡糖氨基转移酶(gnt-iii)过表达的、golgi gdp-岩藻糖转运蛋白(gft)基因slc35c1灭活的(例如,cho-gmt3细胞)、细菌rmd异源表达的或者使用岩藻糖基化的生物化学抑制剂(例如,岩藻糖类似物诸如2-氟岩藻糖和5-炔基岩藻糖)的哺乳动物细胞系产生在重链上的asn-297-连接的n-低聚糖上不具有岩藻糖残基的抗体(pereira,n.a.等人,出处同上;shields,r.l.等人,出处同上;kanda y.,出处同上)。
[0186]
在一些实施方案中,抗体包含重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是kl2b872.clf,其具有包含seq id no:146的氨基
酸序列的轻链和包含seq id no:155的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是kl2b870.clf,其具有包含seq id no:146的氨基酸序列的轻链和包含seq id no:153的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:155的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:155的氨基酸序列并包含k248e、k338a、t437r、k248e/t437r或k338a/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。
[0187]
5.9抗psma抗体和相关分子
[0188]
在一个方面,本文提供了抗psma抗体。
[0189]
在一些实施方案中,抗体是psmb896,其具有包含seq id no:232的氨基酸序列的vl和包含seq id no:233的氨基酸序列的vh。在一些实施方案中,抗体是psmb898,其具有包含seq id no:232的氨基酸序列的vl和包含seq id no:234的氨基酸序列的vh。
[0190]
在一些实施方案中,本文提供了与psma结合的抗体,其中抗体包含:(i)vh,该vh包含分别具有seq id no:233的vh cdr1、vh cdr2和vh cdr3的氨基酸序列的vh cdr1、vh cdr2和vh cdr3;和(ii)vl,该vl包含分别具有seq id no:232的vl cdr1、vl cdr2和vl cdr3的氨基酸序列的vl cdr1、vl cdr2和vl cdr3。在一些实施方案中,本文提供了与psma结合的抗体,其中抗体包含:(i)vh,该vh包含分别具有seq id no:234的vh cdr1、vh cdr2和vh cdr3的氨基酸序列的vh cdr1、vh cdr2和vh cdr3;和(ii)vl,该vl包含分别具有seq id no:232的vl cdr1、vl cdr2和vl cdr3的氨基酸序列的vl cdr1、vl cdr2和vl cdr3。在一些实施方案中,vh cdr1、vh cdr2、vh cdr3、vl cdrl、vl cdr2和vl cdr3序列根据kabat编号系统。在一些实施方案中,vh cdr1、vh cdr2、vh cdr3、vl cdr1、vl cdr2和vl cdr3序列根据chothia编号系统。在一些实施方案中,vh cdr1、vh cdr2、vh cdr3、vl cdr1、vl cdr2和vl cdr3序列根据imgt编号系统。在一些实施方案中,vh cdr1、vh cdr2、vh cdr3、vl cdr1、vl cdr2和vl cdr3序列根据abm编号系统。
[0191]
在另一方面,本文提供了与psma结合的抗体,其中抗体包含:(i)vh,该vh包含具有syams(seq id no:244)的氨基酸序列的vh cdr1、具有aisggigstyyadsvkg(seq id no:245)的氨基酸序列的vh cdr2和具有dgvgatpyyfdy(seq id no:246)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有sgsssniginyvst(seq id no:247)的氨基酸序列的vl cdr1、具有dnnkrps(seq id no:248)的氨基酸序列的vl cdr2和具有gtwdsslsavv(seq id no:249)的氨基酸序列的vl cdr3。在另一方面,本文提供了与psma结合的抗体,其中抗体包含:(i)vh,该vh包含具有syams(seq id no:250)的氨基酸序列的vh cdr1、具有aisggsgstyyadsvkg(seq id no:251)的氨基酸序列的vh cdr2和具有dgvgatpyyfdy(seq id no:252)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有sgsssniginyvs(seq id no:253)的氨基酸序列的vl cdr1、具有dnnkrps(seq id no:254)的氨基酸序列的vl cdr2和具有gtwdsslsavv(seq id no:255)的氨基酸序列的vl cdr3。在另一方面,本文提供了与psma结合的抗体,其中抗体包含:(i)vh,该vh包含具有gftfssyams(seq id no:256)的氨基酸序列的vh cdr1、具有aisggigsty(seq id no:257)的氨基酸序列的vh cdr2和具有dgvgatpyyfdy(seq id no:258)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有
sgsssniginyvs(seq id no:259)的氨基酸序列的vl cdr1、具有dnnkrps(seq id no:260)的氨基酸序列的vl cdr2和具有gtwdsslsavv(seq id no:261)的氨基酸序列的vl cdr3。在另一方面,本文提供了与psma结合的抗体,其中抗体包含:(i)vh,该vh包含具有gftfssyams(seq id no:262)的氨基酸序列的vh cdr1、具有aisggsgsty(seq id no:263)的氨基酸序列的vh cdr2和具有dgvgatpyyfdy(seq id no:264)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有sgsssniginyvs(seq id no:265)的氨基酸序列的vl cdr1、具有dnnkrps(seq id no:266)的氨基酸序列的vl cdr2和具有gtwdsslsavv(seq id no:267)的氨基酸序列的vl cdr3。在另一方面,本文提供了与psma结合的抗体,其中抗体包含:(i)vh,该vh包含具有gftfssy(seq id no:268)的氨基酸序列的vh cdr1、具有sggigs(seq id no:269)的氨基酸序列的vh cdr2和具有gvgatpyyfd(seq id no:270)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有sssniginy(seq id no:271)的氨基酸序列的vl cdr1、具有dnn(seq id no:272)的氨基酸序列的vl cdr2和具有wdsslsav(seq id no:273)的氨基酸序列的vl cdr3。在另一方面,本文提供了与psma结合的抗体,其中抗体包含:(i)vh,该vh包含具有gftfssy(seq id no:274)的氨基酸序列的vh cdr1、具有sggsgs(seq id no:275)的氨基酸序列的vh cdr2和具有gvgatpyyfd(seq id no:276)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有ssssniginy(seq id no:277)的氨基酸序列的vl cdr1、具有dnn(seq id no:278)的氨基酸序列的vl cdr2和具有wdsslsav(seq id no:279)的氨基酸序列的vl cdr3。在另一方面,本文提供了与psma结合的抗体,其中抗体包含:(i)vh,该vh包含具有syams(seq id no:280)的氨基酸序列的vh cdr1、具有aisggigstyyadsvkg(seq id no:281)的氨基酸序列的vh cdr2和具有dgvgatpyyfdy(seq id no:282)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有sgsssniginyvs(seq id no:283)的氨基酸序列的vl cdr1、具有dnnkrps(seq id no:284)的氨基酸序列的vl cdr2和具有gtwdsslsavv(seq id no:285)的氨基酸序列的vl cdr3。在另一方面,本文提供了与psma结合的抗体,其中抗体包含:(i)vh,该vh包含具有syams(seq id no:286)的氨基酸序列的vh cdr1、具有aisggsgstyyadsvkg(seq id no:287)的氨基酸序列的vh cdr2和具有dgvgatpyyfdy(seq id no:288)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有sgsssniginyvs(seq id no:289)的氨基酸序列的vl cdr1、具有dnnkrps(seq id no:290)的氨基酸序列的vl cdr2和具有gtwdsslsavv(seq id no:291)的氨基酸序列的vl cdr3。
[0192]
在一些实施方案中,抗体包含具有seq id no:233的氨基酸序列的vh。在一些实施方案中,抗体包含具有seq id no:232的氨基酸序列的vl。在一些实施方案中,抗体包含vh,该vh包含与seq id no:233的氨基酸序列具有至少95%同一性的氨基酸序列。在一些实施方案中,抗体包含vl,该vl包含与seq id no:232的氨基酸序列具有至少95%同一性的氨基酸序列。
[0193]
在一些实施方案中,抗体包含具有seq id no:234的氨基酸序列的vh。在一些实施方案中,抗体包含具有seq id no:232的氨基酸序列的vl。在一些实施方案中,抗体包含vh,该vh包含与seq id no:234的氨基酸序列具有至少95%同一性的氨基酸序列。在一些实施方案中,抗体包含vl,该vl包含与seq id no:232的氨基酸序列具有至少95%同一性的氨基酸序列。
[0194]
在又一方面,本文提供了与上述其抗体中的一者竞争的抗体。此类抗体还可结合
与上述抗体中的一者或重叠表位相同的表位。与上述抗体竞争或结合相同表位的抗体预期表现出类似的功能特性。
[0195]
在某些实施方案中,本文所述的抗体包含相对于上述抗体具有某些百分比同一性的氨基酸序列,并包括以下第7部分中描述的示例性抗体。
[0196]
两个序列(例如,氨基酸序列或核酸序列)之间的同一性百分比的测定可使用数学算法来完成。用于比较两个序列的数学算法的优选非限制性示例为karlin和altschul,proc.natl.acad.sci.u.s.a.,1990,87:2264-8的算法,如karlin和altschul,proc.natl.acad.sci.u.s.a.,1993,90:5873-7中那样进行修改。此类算法并入altschul等人,j.mol.biol.,1990,215:403的nblast和xblast程序中。可用nblast核苷酸程序参数集进行blast核苷酸检索,例如,对于评分=100,字长=12,以获得与本文所述的核酸分子同源的核苷酸序列。可用xblast程序参数集进行blast蛋白质检索,例如,对于得分50,字长=3,以获得与本文所述的蛋白质分子同源的氨基酸序列。为了获得用于比较目的的空位比对,可如altschul等人,nucleic acids res.,1997,25:3389-402中所述利用空位blast。另选地,可使用psi blast执行检测分子之间的距离关系(id.)的迭代检索。当利用blast、空位blast和psi blast程序时,可使用相应程序(例如xblast和nblast)的默认参数(参见例如,万维网上的国家生物技术信息中心(ncbi),ncbi.nlm.nih.gov)。用于比较序列的数学算法的另一优选非限制性示例为myers和miller,1988,cabios 4:1117的算法。此类算法并入align程序(版本2.0)中,其是gcg序列比对软件包的一部分。当利用align程序比较氨基酸序列时,可使用pam120权重残基表、空位长度罚分12、空位罚分4。
[0197]
两个序列之间的同一性百分比可使用与上述那些类似的技术来确定,允许或不允许空位。在计算百分比同一性时,通常仅计数精确匹配。
[0198]
在某些实施方案中,本文提供的抗体包含与seq id no:233的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区以及/或者与seq id no:232的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区,其中抗体与psma结合。在某些实施方案中,本文提供的抗体包含与seq id no:234的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区以及/或者与seq id no:232的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区,其中抗体与psma结合。
[0199]
在一些实施方案中,本文提供了一种抗体,该抗体包含上述抗psma抗体的vh、vl或cdr序列并且还包含具有re突变但不具有岩藻糖残基的fc区。在一些实施方案中,本文提供的抗psma抗体包含具有re突变并且不具有岩藻糖残基的fc区。
[0200]
本领域技术人员已知的标准技术可用于在编码本文提供的分子的核苷酸序列中引入突变,包括例如导致氨基酸突变的定点诱变和pcr介导的诱变。
[0201]
在一些实施方案中,谷氨酸被本文提供的抗体的fc区的位置248的赖氨酸(k248e)(eu编号)取代。在一些实施方案中,精氨酸被本文提供的抗体的fc区的位置437的苏氨酸(t437r)(eu编号)取代。在一些实施方案中,谷氨酸被本文提供的抗体的fc区的位置248的赖氨酸取代并且精氨酸被位置437的苏氨酸(k248e/t437r)(eu编号)取代。
[0202]
在一些实施方案中,本文提供的抗体包含重链,该重链包含t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含k248e突变。在一些实施方案中,本文提供
的抗体包含重链,该重链包含k338a突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含k248e/t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含k338a/t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:242的氨基酸序列但具有t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:242的氨基酸序列但具有k248e突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:242的氨基酸序列但具有k338a突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:242的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:242的氨基酸序列但具有k338a/t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:243的氨基酸序列但具有t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:243的氨基酸序列但具有k248e突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:243的氨基酸序列但具有k338a突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:243的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:243的氨基酸序列但具有k338a/t437r突变。在一些实施方案中,抗体是psmb896,其包含重链,该重链包含seq id no:242的氨基酸序列但具有k248e和t437r突变(re突变)。在一些实施方案中,抗体是psmb898,其包含重链,该重链包含seq id no:243的氨基酸序列但具有k248e和t437r突变(re突变)。
[0203]
在一些实施方案中,本文提供的抗体(包括上述抗psma抗体)不是岩藻糖基化的。可使用本领域技术人员已知的标准技术来生成本文提供的抗体,其中重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。例如,已经发现,缺乏gmd酶(例如cho lec13细胞)的、由突变的fut8基因引起的α-1,6岩藻糖基转移酶活性降低的、β-1,4-甘露糖基-糖蛋白4-β-n-乙酰葡糖氨基转移酶(gnt-iii)过表达的、golgi gdp-岩藻糖转运蛋白(gft)基因slc35c1灭活的(例如,cho-gmt3细胞)、细菌rmd异源表达的或者使用岩藻糖基化的生物化学抑制剂(例如,岩藻糖类似物诸如2-氟岩藻糖和5-炔基岩藻糖)的哺乳动物细胞系产生在重链上的asn-297-连接的n-低聚糖上不具有岩藻糖残基的抗体(pereira,n.a.等人,出处同上;shields,r.l.等人,出处同上;kanda y.,出处同上)。
[0204]
在一些实施方案中,抗体包含重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是psmb896.clf,其具有包含seq id no:241的氨基酸序列的轻链和包含seq id no:242的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体是psmb898.clf,其具有包含seq id no:241的氨基酸序列的轻链和包含seq id no:243的氨基酸序列的重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:242的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:243的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:242的氨基酸序列并包含k248e、k338a、t437r、k248e/t437r或k338a/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:243的氨基酸序列并包含k248e、k338a、t437r、k248e/t437r或k338a/t437r
突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。
[0205]
5.10抗bcma抗体和相关分子
[0206]
在一个方面,本文提供了抗bcma抗体。
[0207]
在一些实施方案中,抗体是bcmb519,其具有包含seq id no:299的氨基酸序列的vl和包含seq id no:298的氨基酸序列的vh。在一些实施方案中,本文提供了与bcma结合的抗体,其中抗体包含:(i)vh,该vh包含分别具有seq id no:298的vh cdr1、vh cdr2和vh cdr3的氨基酸序列的vh cdr1、vh cdr2和vh cdr3;和(ii)vl,该vl包含分别具有seq id no:299的vl cdr1、vl cdr2和vl cdr3的氨基酸序列的vl cdrl、vl cdr2和vl cdr3。在一些实施方案中,vh cdr1、vh cdr2、vh cdr3、vl cdr1、vl cdr2和vl cdr3序列根据kabat编号系统。在一些实施方案中,vh cdr1、vh cdr2、vh cdr3、vl cdr1、vl cdr2和vl cdr3序列根据chothia编号系统。在一些实施方案中,vh cdr1、vh cdr2、vh cdr3、vl cdr1、vl cdr2和vl cdr3序列根据示例性编号系统。在一些实施方案中,vh cdr1、vh cdr2、vh cdr3、vl cdr1、vl cdr2和vl cdr3序列根据contact编号系统。在一些实施方案中,vh cdr1、vh cdr2、vh cdr3、vl cdr1、vl cdr2和vl cdr3序列根据imgt编号系统。在一些实施方案中,vh cdr1、vh cdr2、vh cdr3、vl cdr1、vl cdr2和vl cdr3序列根据abm编号系统。
[0208]
在另一方面,本文提供了与bcma结合的抗体,其中抗体包含:(i)vh,该vh包含具有gftfssya(seq id no:292)的氨基酸序列的vh cdr1、具有isgsggst(seq id no:293)的氨基酸序列的vh cdr2和具有akdegyssghyygmdv(seq id no:294)的氨基酸序列的vh cdr3;和(ii)vl,该vl包含具有qsisssf(seq id no:295)的氨基酸序列的vl cdr1、具有gas(seq id no:296)的氨基酸序列的vl cdr2和具有qhygsspmyt(seq id no:297)的氨基酸序列的vl cdr3。
[0209]
在一些实施方案中,抗体包含具有seq id no:298的氨基酸序列的vh。在一些实施方案中,抗体包含具有seq id no:299的氨基酸序列的vl。在一些实施方案中,抗体包含vh,该vh包含与seq id no:298的氨基酸序列具有至少95%同一性的氨基酸序列。在一些实施方案中,抗体包含vl,该vl包含与seq id no:299的氨基酸序列具有至少95%同一性的氨基酸序列。
[0210]
在又一方面,本文提供了与上述其抗体中的一者竞争的抗体。此类抗体还可结合与上述抗体中的一者或重叠表位相同的表位。与上述抗体竞争或结合相同表位的抗体预期表现出类似的功能特性。
[0211]
在某些实施方案中,本文所述的抗体包含相对于上述抗体具有某些百分比同一性的氨基酸序列,并包括以下第7部分中描述的示例性抗体。
[0212]
两个序列(例如,氨基酸序列或核酸序列)之间的同一性百分比的测定可使用数学算法来完成。用于比较两个序列的数学算法的优选非限制性示例为kar1in和altschu1,proc.natl.acad.sci.u.s.a.,1990,87:2264-8的算法,如karlin和altschul,proc.natl.acad.sci.u.s.a.,1993,90:5873-7中那样进行修改。此类算法并入altschul等人,j.mol.biol.,1990,215:403的nblast和xblast程序中。可用nblast核苷酸程序参数集进行blast核苷酸检索,例如,对于评分=100,字长=12,以获得与本文所述的核酸分子同源的核苷酸序列。可用xblast程序参数集进行blast蛋白质检索,例如,对于得分50,字长=3,以获得与本文所述的蛋白质分子同源的氨基酸序列。为了获得用于比较目的的空位比
对,可如altschul等人,nucleic acids res.,1997,25:3389-402中所述利用空位blast。另选地,可使用psi blast执行检测分子之间的距离关系(id.)的迭代检索。当利用blast、空位blast和psi blast程序时,可使用相应程序(例如xblast和nblast)的默认参数(参见例如,万维网上的国家生物技术信息中心(ncbi),ncbi.nlm.nih.gov)。用于比较序列的数学算法的另一优选非限制性示例为myers和miller,1988,cabios 4:11 17的算法。此类算法并入align程序(版本2.0)中,其是gcg序列比对软件包的一部分。当利用align程序比较氨基酸序列时,可使用pam120权重残基表、空位长度罚分12、空位罚分4。
[0213]
两个序列之间的同一性百分比可使用与上述那些类似的技术来确定,允许或不允许空位。在计算百分比同一性时,通常仅计数精确匹配。
[0214]
在某些实施方案中,本文提供的抗体包含与seq id no:298的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vh区以及/或者与seq id no:299的氨基酸序列具有至少80%、至少85%、至少90%、至少95%或至少98%序列同一性的vl区,其中抗体与bcma结合。
[0215]
在一些实施方案中,本文提供了一种抗体,该抗体包含上述抗bcma抗体的vh、vl或cdr序列并且还包含具有re突变但不具有岩藻糖残基的fc区。
[0216]
在一些实施方案中,本文提供的抗bcma抗体包含具有re突变并且不具有岩藻糖残基的fc区。
[0217]
本领域技术人员已知的标准技术可用于在编码本文提供的分子的核苷酸序列中引入突变,包括例如导致氨基酸突变的定点诱变和pcr介导的诱变。
[0218]
在一些实施方案中,谷氨酸被本文提供的抗体的fc区的位置248的赖氨酸(k248e)(eu编号)取代。在一些实施方案中,精氨酸被本文提供的抗体的fc区的位置437的苏氨酸(t437r)(eu编号)取代。在一些实施方案中,谷氨酸被本文提供的抗体的fc区的位置248的赖氨酸取代并且精氨酸被位置437的苏氨酸(k248e/t437r)(eu编号)取代。
[0219]
在一些实施方案中,本文提供的抗体包含重链,该重链包含t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含k248e突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含k338a突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含k248e/t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含k338a/t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:300的氨基酸序列但具有t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:300的氨基酸序列但具有k248e突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:300的氨基酸序列但具有k338a突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:300的氨基酸序列但具有k248e/t437r突变。在一些实施方案中,本文提供的抗体包含重链,该重链包含seq id no:300的氨基酸序列但具有k338a/t437r突变。
[0220]
在一些实施方案中,本文提供的抗体(包括上述抗bcma抗体)不是岩藻糖基化的。可使用本领域技术人员已知的标准技术来生成本文提供的抗体,其中重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。例如,已经发现,缺乏gmd酶(例如cho lec13细胞)的、由突变的fut8基因引起的α-1,6岩藻糖基转移酶活性降低的、β-1,4-甘露糖基-糖蛋白4-β-n-乙酰葡糖氨基转移酶(gnt-iii)过表达的、golgi gdp-岩藻糖转运蛋白(gft)基因
slc35c1灭活的(例如,cho-gmt3细胞)、细菌rmd异源表达的或者使用岩藻糖基化的生物化学抑制剂(例如,岩藻糖类似物诸如2-氟岩藻糖和5-炔基岩藻糖)的哺乳动物细胞系产生在重链上的asn-297-连接的n-低聚糖上不具有岩藻糖残基的抗体(pereira,n.a.等人,出处同上;shields,r.l.等人,出处同上;kanda y.,出处同上)。
[0221]
在一些实施方案中,抗体包含重链,该重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:300的氨基酸序列并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,抗体包含重链,该重链包含seq id no:300的氨基酸序列并包含k248e、k338a、t437r、k248e/t437r或k338a/t437r突变并在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。
[0222]
5.11其他示例性抗体
[0223]
在一些实施方案中,本文提供的抗体包含具有某些已知抗体中所含的vl、vh或cdr的氨基酸序列的vl、vh或cdr,其中抗体包含具有re突变并且不具有岩藻糖基化的fc区。此类示例性已知抗体包括但不限于reopro(阿昔单抗)、humira(阿达木单抗)、hyrimoz(阿达木单抗-adaz)、cyltezo(阿达木单抗-adbm)、abrilada(阿达木单抗-afzb)、amjevita(阿达木单抗-atto)、hadlima(阿达木单抗-bwwd)、campath/lemtrada(阿仑单抗)、praluent(阿莫罗布单抗)、tecentriq(阿特珠单抗)、bavencio(阿维鲁单抗)、simulect(巴利昔单抗)、benlysta(贝利木单抗)、benlysta(贝利木单抗)、fasenra(贝那利珠单抗)、avastin(贝伐珠单抗)、mvasi(贝伐珠单抗-awwb)、zirabev(贝伐珠单抗-bvzr)、zinplava(贝洛托舒单抗)、blincyto(博纳吐单抗)、siliq(布达鲁单抗)、beovu(布西珠单抗-dbll)、crysvita(布罗索尤单抗-twza)、ilaris(卡那单抗)、cablivi(卡拉西单抗-yhdp)、libtayo(西米普利单抗-rwlc)、erbitux(西妥昔单抗)、adakveo(立赞利珠单抗-tmca)、zenapax(达克珠单抗)、zinbryta(达克珠单抗)、darzalex(达雷木单抗)、prolia/xgeva(地诺单抗)、unituxin(达妥昔单抗)、dupixent(度普利尤单抗)、imfinzi(德瓦鲁单抗)、soliris(依库丽单抗)、empliciti(埃罗妥珠单抗)、gamifant(依帕伐单抗-lzsg)、hemlibra(艾美赛珠单抗-kxwh)、vyepti(依普奈珠单抗-jjmr)、aimovig(依瑞奈尤单抗-aooe)、repatha(依洛尤单抗)、ajovy(瑞玛奈珠单抗-vfrm)、emgality(伽奈珠单抗-gnlm)、simponi(戈利木单抗)、simponi aria(戈利木单抗)、tremfya(古塞库单抗)、trogarzo(伊巴利珠单抗-uiyk)、praxbind(依达赛珠单抗)、remicade(英夫利西单抗)、renflexis(英夫利西单抗-abda)、avsola(英夫利西单抗-axxq)、inflectra(英夫利西单抗-dyyb)、ixifi(英夫利西单抗-qbtx)、yervoy(伊匹木单抗)、sarclisa(伊沙妥昔单抗-irfc)、taltz(依奇珠单抗)、takhzyro(拉那芦人单抗-flyo)、nucala(美泊利珠单抗)、nucala(美泊利珠单抗)、poteligeo(莫格利珠单抗-kpkc)、tysabri(那他珠单抗)、portrazza(耐昔妥珠单抗)、opdivo(纳武利尤单抗)、anthim(奥比妥昔单抗)、gazyva(奥比妥珠单抗)、ocrevus(奥瑞组单抗)、arzerra(奥法木单抗)、lartruvo(奥拉单抗)、xolair(奥马珠单抗)、synagis(帕利珠单抗)、vectibix(帕尼单抗)、keytruda(派姆单抗)、perjeta(帕妥珠单抗)、cyramza(雷莫芦单抗)、lucentis(兰尼单抗)、ultomiris(雷夫利珠单抗-cwvz)、raxibacumab(雷昔库单抗)、cinqair(瑞利珠单抗)、skyrizi(瑞莎珠单抗-rzaa)、rituxan(利妥昔单抗)、truxima(利妥昔单抗-abbs)、ruxience(利妥昔单抗-pvvr)、evenity(罗莫单抗-aqqg)、kevzara(沙利鲁单抗)、cosentyx(苏金单抗)、sylvant(司妥昔单抗)、tepezza(替妥木单
抗-trbw)、ilumya(替拉珠单抗-asmn)、actemra(托珠单抗)、actemra(托珠单抗)、herceptin(曲妥珠单抗)、kanjinti(曲妥珠单抗-anns)、ogivri(曲妥珠单抗-dkst)、ontruzant(曲妥珠单抗-dttb)、herzuma(曲妥珠单抗-pkrb)、trazimera(曲妥珠单抗-qyyp)、stelara(优特克单抗)、stelara(优特克单抗)和entyvio(维多珠单抗)。用于引入re突变和减少岩藻糖基化的方法更详细地描述于本文提供的其他部分中并且在本领域中是众所周知的。
[0224]
5.12多核苷酸
[0225]
在某些实施方案中,本公开涵盖编码本文所述抗体的多核苷酸。术语
″
编码多肽的多核苷酸
″
涵盖仅包含多肽的编码序列的多核苷酸以及包含附加的编码和/或非编码序列的多核苷酸。本公开的多核苷酸可以是rna形式或dna形式。dna包括cdna、基因组dna和合成dna;并且可以是双链或单链的,并且如果是单链,可以是编码链或非编码(反义)链。
[0226]
在某些实施方案中,多核苷酸包含与有助于例如多肽从宿主细胞表达和分泌的多核苷酸在同一阅读框中融合的多肽的编码序列(例如,前导序列,其充当用于控制多肽的转运的分泌序列)。多肽可具有被宿主细胞裂解以形成多肽的
″
成熟
″
形式的前导序列。
[0227]
在某些实施方案中,多核苷酸包含与标记或标签序列在同一阅读框中融合的多肽的编码序列。例如,在一些实施方案中,标记序列是由载体提供的六组氨酸标签,其允许在细菌宿主的情况下有效纯化与标记物融合的多肽。在一些实施方案中,标记物与其他亲和标签一起使用。
[0228]
在某些实施方案中,本文提供的多核苷酸选自下表17中列出的多核苷酸。在某些实施方案中,本文提供的多核苷酸选自下表20和下表22中列出的多核苷酸。在某些实施方案中,本文提供的多核苷酸选自下表26中列出的多核苷酸。
[0229]
在某些实施方案中,本文提供的多核苷酸选自下表9-表12中列出的多核苷酸。在某些实施方案中,本文提供的多核苷酸选自下表15和下表16中列出的多核苷酸。在某些实施方案中,本文提供的多核苷酸选自下表2中列出的多核苷酸。
[0230]
表2.示例性小鼠抗体的多核苷酸序列
[0231]
[0232][0233]
在一些实施方案中,多核苷酸包含seq id no:69的轻链核苷酸序列和/或seq id no:77的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:70的轻链核苷酸序列和/或seq id no:78的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:71的轻链核苷酸序列和/或seq id no:79的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:72的轻链核苷酸序列和/或seq id no:80的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:73的轻链核苷酸序列和/或seq id no:81的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:74的轻链核苷酸序列和/或seq id no:82的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:75的轻链核苷酸序列和/或seq id no:83的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:76的轻链核苷酸序列和/或seq id no:84的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:69的轻链核苷酸序列和/或seq id no:85的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:70的轻链核苷酸序列和/或seq id no:86的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:71的轻链核苷酸序列和/或seq id no:87的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:72的轻链核苷酸序列和/或seq id no:88的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:73的轻链核苷酸序列和/或seq id no:89的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:74的轻链核苷酸序列和/或seq id no:90的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:75的轻链核苷酸序列和/或seq id no:91的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:76的轻链核苷酸序列和/或seq id no:92的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:69的轻链核苷酸序列和/或seq id no:93的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:76的轻链核苷酸序列和/或seq id no:94的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:74的轻链核苷酸序列和/或seq id no:95的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:70的轻链核苷酸序列和/或seq id no:96的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:71的轻链核苷酸序列和/或seq id no:97的重链核
苷酸序列。在一些实施方案中,多核苷酸包含seq id no:73的轻链核苷酸序列和/或seq id no:98的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:75的轻链核苷酸序列和/或seq id no:99的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:72的轻链核苷酸序列和/或seq id no:100的重链核苷酸序列。
[0234]
在一些实施方案中,多核苷酸包含seq id no:104的轻链核苷酸序列和/或seq id no:105的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:104的轻链核苷酸序列和/或seq id no:106的重链核苷酸序列。
[0235]
在一些实施方案中,多核苷酸包含seq id no:161的轻链核苷酸序列和/或seq id no:160的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:161的轻链核苷酸序列和/或seq id no:162的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:161的轻链核苷酸序列和/或seq id no:163的重链核苷酸序列。
[0236]
在一些实施方案中,多核苷酸包含seq id no:180的轻链核苷酸序列和/或seq id no:182的重链核苷酸序列。在一些实施方案中,多核苷酸包含seq id no:181的轻链核苷酸序列和/或seq id no:183的重链核苷酸序列。
[0237]
本公开还涉及本文所述的多核苷酸的变体,其中该变体编码例如多肽的片段、类似物和/或衍生物。在某些实施方案中,本公开提供了一种多核苷酸,其包括具有与编码包含本文所述抗体的多肽的多核苷酸至少约80%相同、至少约85%相同、至少约90%相同、至少约95%相同并且在一些实施方案中至少约96%、97%、98%或99%相同的核苷酸序列的多核苷酸。
[0238]
如本文所用,短语
″
具有与参考核苷酸序列至少例如95%
″
相同
″
的核苷酸序列的多核苷酸
″
旨在意指该多核苷酸的核苷酸序列与参考序列相同,不同的是该多核苷酸序列可包括参考核苷酸序列的每100个核苷酸至多五个点突变。换句话讲,为了获得具有与参考核苷酸序列至少95%相同的核苷酸序列的多核苷酸,参考序列中至多5%的核苷酸可缺失或被另一核苷酸取代,或者可将参考序列中总核苷酸的至多5%的核苷酸数目可插入参考序列中。参考序列的这些突变可发生在参考核苷酸序列的5
′
或3
′
末端位置或那些末端位置之间的任何位置,或者单独散布在参考序列的核苷酸中,或者散布在参考序列内的一个或多个连续组中。
[0239]
多核苷酸变体可在编码区、非编码区或两者中含有改变。在一些实施方案中,多核苷酸变体含有产生沉默取代、添加或缺失但不改变所编码的多肽的特性或活性的改变。在一些实施方案中,多核苷酸变体包含沉默取代,其不导致多肽的氨基酸序列的改变(由于遗传密码的简并性)。多核苷酸变体可出于各种原因产生,例如,为了优化特定宿主的密码子表达(即,将人mrna中的密码子改变为细菌宿主诸如大肠杆菌(e.coli)的优选密码子)。在一些实施方案中,多核苷酸变体在序列的非编码区或编码区中包含至少一个沉默突变。
[0240]
在一些实施方案中,产生多核苷酸变体以调节或改变所编码的多肽的表达(或表达水平)。在一些实施方案中,产生多核苷酸变体以增加所编码的多肽的表达。在一些实施方案中,产生多核苷酸变体以降低所编码的多肽的表达。在一些实施方案中,多核苷酸变体与亲本多核苷酸序列相比具有增加的所编码的多肽的表达。在一些实施方案中,多核苷酸变体与亲本多核苷酸序列相比具有降低的所编码的多肽的表达。
[0241]
在某些实施方案中,本公开提供了一种多核苷酸,其包含与选自表9-12、15、16、
20、22和26中列出的多核苷酸的多核苷酸至少约80%相同、至少约85%相同、至少约90%相同、至少约95%相同并且在一些实施方案中至少约96%、97%、98%或99%相同的核苷酸序列。
[0242]
在某些实施方案中,本文提供的多核苷酸还包含在表9-12、15、16、20、22和26中列出的vh和/或vl序列之前的一个或多个信号序列。
[0243]
在某些实施方案中,分离多核苷酸。在某些实施方案中,多核苷酸是基本上纯的。
[0244]
还提供了包含本文所述的多核苷酸的载体和细胞。在一些实施方案中,表达载体包含多核苷酸分子。在一些实施方案中,宿主细胞包含表达载体,该表达载体包含多核苷酸分子。在一些实施方案中,宿主细胞包含一种或多种包含多核苷酸分子的表达载体。在一些实施方案中,宿主细胞包含多核苷酸分子。在一些实施方案中,宿主细胞包含一种或多种多核苷酸分子。本文提供的载体的构建在以下第7部分中举例说明。
[0245]
5.13多克隆和单克隆抗体
[0246]
在一些实施方案中,本文提供的抗体群体包括多克隆抗体。制备多克隆抗体的方法是技术人员已知的。可例如通过免疫剂以及(如果需要)佐剂的一次或多次注射来提升哺乳动物中的多克隆抗体。通常,将通过多次皮下或腹膜内注射将免疫剂和/或佐剂注射在哺乳动物中。免疫剂可包括多肽(如hla-g、cd37、gprc5d、klk2、psma或bcma或它们的片段)或其融合蛋白。可能有用的是将免疫剂缀合到已知在被免疫的哺乳动物中具有免疫原性的蛋白质或将哺乳动物用蛋白质和一种或多种佐剂免疫。此类免疫原性蛋白质的示例包括但不限于钥孔虫戚血蓝蛋白、血清白蛋白、牛甲状腺球蛋白和大豆胰蛋白酶抑制剂。可采用的佐剂的示例包括ribi、cpg、poly(i:c)、弗氏完全佐剂和mpl-tdm佐剂(单磷酰基脂质a、合成海藻糖二杆菌分枝菌酸酯)。在无不当实验的情况下,本领域的技术人员可选择免疫方案。然后可从哺乳动物取血,并且测定血清的例如抗hla-g、抗cd37、抗gprc5d、抗klk2抗体、抗psma或抗bcma滴度。如果需要,可将哺乳动物提升,直到抗体滴度增加或稳定为止。附加地或另选地,可从免疫动物获得淋巴细胞以用于融合和制备来自杂交瘤的单克隆抗体,如下所述。
[0247]
在一些实施方案中,本文提供的抗体包括单克隆抗体。可使用首先由kohler等人,nature,1975,256:495-7描述的杂交瘤方法来制备单克隆抗体,或者可通过重组dna方法制备单克隆抗体(参见例如,美国专利4,816,567)。
[0248]
在杂交瘤方法中,如上所述将小鼠或其他合适的宿主动物诸如仓鼠免疫,以引发产生或能够产生与用于免疫的蛋白质特异性结合的抗体的淋巴细胞。另选地,可在体外将淋巴细胞免疫。免疫后,分离出淋巴细胞,并且然后使用合适的融合剂(诸如聚乙二醇)将淋巴细胞与骨髓瘤细胞系融合以形成杂交瘤细胞(goding,monoclonal antibodies:principles and practice 59-103(1986))。
[0249]
将由此制备的杂交瘤细胞接种并培养在合适的培养基中,在某些实施方案中,该培养基含有抑制未融合的亲本骨髓瘤细胞(也被称为融合配偶体)的生长或存活的一种或多种物质。例如,如果亲本骨髓瘤细胞缺乏酶次黄嘌呤鸟嘌呤转磷酸核糖基酶(hgprt或hprt),则用于杂交瘤的选择性培养基通常将包含次黄嘌呤、氨基蝶呤和胸苷(hat培养基),其防止缺乏hgprt的细胞生长。
[0250]
示例性融合配偶体骨髓瘤细胞是有效地融合、通过所选的抗体生成细胞支持抗体
的稳定高水平产生并且对针对未融合亲本细胞进行选择的选择性培养基敏感的那些。示例性骨髓瘤细胞系是鼠骨髓瘤细胞系,诸如sp-2和衍生物,例如可从美国典型培养物保藏中心(manassas,va)获得的x63-ag8-653细胞以及源自可从索尔克研究所细胞配送中心(san diego,ca)获得的mopc-21和mpc-11小鼠肿瘤的那些。另外已经描述人骨髓瘤和小鼠-人异质骨髓瘤细胞系用于产生人单克隆抗体(kozbor,immunol.,1984,133:3001-05;以及brodeur等人,monoclonal antibody production techniques and applications,1987,51-63)。
[0251]
测定其中培养杂交瘤细胞以用于产生针对抗原的单克隆抗体的培养基。通过免疫沉淀或通过体外结合测定诸如ria或elisa来确定由杂交瘤细胞产生的单克隆抗体的结合特异性。可例如通过munson等人,anal.biochem.,1980,107:220-39中描述的斯卡查德分析来确定单克隆抗体的结合亲和力。
[0252]
一旦鉴定出产生期望的特异性、亲和力和/或活性的抗体的杂交瘤细胞,就可通过有限稀释程序对克隆进行亚克隆,并且通过标准方法培养(goding,出处同上)。用于此目的的合适的培养基包括例如dmem或rpmi-1640培养基。此外,例如,通过将细胞腹腔注射到小鼠中,杂交瘤细胞可在体内作为动物的腹水瘤培养。
[0253]
通过常规抗体纯化程序诸如例如亲和色谱法(例如,使用蛋白a或蛋白g-琼脂糖)或离子交换色谱法、羟基磷灰石色谱法、凝胶电泳、渗析等将由亚克隆分泌的单克隆抗体与培养基、腹水或血清适当地分离。
[0254]
使用常规程序(例如,通过使用能够与编码鼠抗体的重链和轻链的基因特异性结合的寡核苷酸探针)将编码单克隆抗体的dna容易地分离和测序。杂交瘤细胞可用作此类dna的来源。在分离之后,可将dna置于表达载体中,然后将这些表达载体转染到宿主细胞诸如不以另外的方式产生抗体蛋白质的大肠杆菌细胞、猿猴cos细胞、中国仓鼠卵巢(cho)细胞或骨髓瘤细胞中,以实现单克隆抗体在重组宿主细胞中的合成。有关编码抗体的dna在细菌中重组表达的综述文章包括skerra等人,curr.opinion in immunol.,1993,5∶256-62以及pl
ü
ckthun,immunol.revs.,1992,130:151-88。
[0255]
在一些实施方案中,(例如,在hla-g、cd37、gprc5d、klk2、psma或bcma上)结合表位的抗体包含由这样的核苷酸序列编码的vh结构域的氨基酸序列和/或vl结构域的氨基酸序列:该核苷酸序列与(1)编码本文所述的vh和/或vl结构域中的任一者的核苷酸序列的互补序列在严格条件下(例如,在约45℃下在6
×
氯化钠/柠檬酸钠(ssc)中与过滤器结合的dna杂交,然后在约50℃-65℃下在0.2
×
ssc/0.1%sds中洗涤一次或多次)、在高度严格条件下(例如,在约45℃下在6
×
ssc中与过滤器结合的核酸杂交,然后在约68℃下在0.1
×
ssc/0.2%sds中洗涤一次或多次)或在本领域技术人员已知的其他严格杂交条件下杂交(参见例如,current protocols in molecular biology,第i卷,6.3.1-6.3.6和2.10.3(ausubel等人编辑,1989))。
[0256]
在另一个实施方案中,单克隆抗体可从使用例如antibody phage display:methods and protocols(o
′
brien和aitken编辑,2002)中所述的技术生成的抗体噬菌体文库中分离。在噬菌体展示方法中,功能性抗体结构域展示在噬菌体颗粒的表面上,这些噬菌体颗粒携带编码功能性抗体结构域的多核苷酸序列。可用于制备本文所述抗体的噬菌体展示方法的示例包括以下中所公开的那些:brinkman等人,j.immunol.methods,1995,182:
41-50;ames等人,j.immunol.methods,1995,184:177-86;kettleborough等人,eur.j.immunol.,1994,24:952-8;persic等人,gene,1997,187:9-18;burton等人,advances in immunology,1994,57:191-280;pct申请pct/gb91/o1 134;国际公布wo 90/02809、wo 91/10737、wo 92/01047、wo 92/18619、wo 93/11236、wo 95/15982、wo 95/20401和wo 97/13844;以及美国专利5,698,426、5,223,409、5,403,484、5,580,717、5,427,908、5,750,753、5,821,047、5,571,698、5,427,908、5,516,637、5,780,225、5,658,727、5,733,743和5,969,108。
[0257]
原则上,通过筛选含有噬菌体的噬菌体文库来选择合成的抗体克隆,这些噬菌体展示与噬菌体外壳蛋白融合的抗体可变区(fv)的各种片段。针对期望的抗原筛选此类噬菌体文库。表达能够与期望抗原结合的fv片段的克隆被吸附到抗原,并因此与文库中的非结合克隆分离。然后将结合克隆从抗原中洗脱出,并且可通过附加的抗原吸附/洗脱循环将结合克隆进一步富集。
[0258]
可变结构域可在功能上作为单链fv(scfv)片段(其中vh和vl通过柔性短肽共价连接)或作为fab片段(其中它们各自与恒定结构域融合并且非共价地相互作用)展示在噬菌体上,如例如在winter等人,1994,ann.rev.immunol.12:433-55中所述。
[0259]
通过pcr将vh和vl基因的组库单独克隆,并且在噬菌体文库中随机重组,然后可搜索抗原结合克隆,如在winter等人,出处同上中所述。来自免疫源的文库无需构建杂交瘤即可提供针对免疫原的高亲和力抗体。另选地,可克隆原初组库以在无任何免疫的情况下向广泛的非自体抗原以及自体抗原提供单一来源的人抗体,如griffiths等人,embo j,1993,12:725-34所述。最后,也可通过克隆来自干细胞的未重排v-基因片段并且使用含有随机序列的pcr引物来合成制备原始文库,用于编码高度可变的cdr3区并在体外完成重排,如例如hoogenboom和winter,j.mol.biol.,1992,227:381-88所述。
[0260]
文库的筛选可通过本领域已知的各种技术来实现。例如,hla-g、cd37、gprc5d、klk2、psma或bcma(例如,hla-g、cd37、gprc5d、klk2、psma或bcma多肽、片段或表位)可用于涂覆吸附板的孔,在附连于吸附板的宿主细胞上表达或用于细胞分选,缀合至生物素以用链霉亲和素包被的小珠捕获,或在任何其他方法中用于平移展示文库。可如bass等人,proteins,1990,8:309-14和wo 92/09690中所述通过使用长洗涤和单价噬菌体展示,以及如marks等人,biotechnol.,1992,10:779-83中所述通过使用低涂覆密度的抗原来促进具有慢离解动力学(例如,良好结合亲和力)的抗体的选择。
[0261]
可通过以下方式获得抗体:设计合适的抗原筛选程序以选择目的噬菌体克隆,然后使用vh和/或vl序列(例如,fv序列)或来自目的噬菌体克隆的vh和vl序列的各种cdr序列以及kabat等人,出处同上中所述的合适的恒定区(例如fc)序列(包括包含k248e、t437r或k248e/t437r突变的序列)来构建全长抗体克隆。
[0262]
本文所述的抗体还可例如包括嵌合抗体。嵌合抗体是其中抗体的不同部分来源于不同免疫球蛋白分子的分子。例如,嵌合抗体可含有与人抗体的恒定区融合的小鼠或大鼠单克隆抗体的可变区。用于产生嵌合抗体的方法是本领域已知的。参见例如,morrison,science,1985,229:1202;oi等人,1986,biotechniques 4:214;gillies等人,1989,j.immunol.methods125:191-202;以及美国专利5,807,715、4,816,567、4,816,397和6,331,415。
[0263]
使用诸如本文所述的那些技术产生的抗体可使用众所周知的标准技术分离。例如,可通过常规免疫球蛋白纯化程序诸如例如蛋白a-琼脂糖、羟基磷灰石色谱法、凝胶电泳、透析或亲和色谱法将抗体与例如培养基、腹水、血清、细胞溶解物、合成反应材料等适当地分离。如本文所用,
″
分离的
″
或
″
纯化的
″
抗体基本上不含来自抗体所来源于的细胞或组织源的细胞物质或其他蛋白质,或当化学合成时基本上不含化学前体或其他化学物质。
[0264]
在一些具体的实施方案中,使用以下第7部分中举例说明的方法生成单克隆抗体。
[0265]
5.14人源化抗体
[0266]
在一些实施方案中,本文提供的抗体可为人源化抗体。人源化抗体可包含人框架区和人恒定区序列。例如,人源化抗体可包含人恒定区序列。在某些实施方案中,人源化抗体可选自任何类别的免疫球蛋白,包括igm、igg、igd、iga和ige以及任何同种型,包括iggl、igg2、igg3和igg4(例如,igg4和igg4无效体的变体)。在某些实施方案中,人源化抗体可包含κ或λ轻链恒定序列。
[0267]
人源化抗体可使用本领域已知的多种技术来产生,包括但不限于cdr移植(欧洲专利ep 239,400;国际公布号wo 91/09967;和美国专利号5,225,539、5,530,101和5,585,089)、镶面或表面重修(欧洲专利号ep 592,106和ep 519,596;padlan,molecular immunology,1991,28(4/5):489-498;studnicka等人,protein engineering,1994,7(6):805-814;以及roguska等人,proc.natl.acad.sci.usa,1994,91:969-73)、链改组(美国专利5,565,332)和例如以下文献中公开的技术:美国专利6,407,213、美国专利5,766,886、wo 93/17105;tan等人,j.immunol.,2002,169:1119-25;caldas等人,protein eng.,2000,13(5):353-60;morea等人,methods,2000,20(3):267-79;baca等人,j.biol.chem.,1997,272(16):10678-84;roguska等人,protein eng.,1996年,9(10):895904;couto等人,cancer res.,1995,55(23增刊):5973s-5977s;couto等人,cancer res.,1995,55(8):1717-22;sandhu,j.s.,gene,1994,150(2):409-10;以及pedersen等人,j.mol.biol.,1994,235(3):959-73。还可参见美国专利公布us 2005/0042664a1(2005年2月24日),这些文献中的每一篇全文以引用的方式并入本文。
[0268]
用于人源化非人抗体的各种方法是本领域已知的。例如,人源化抗体可具有从非人来源引入其中的一个或多个氨基酸残基。这些非人氨基酸残基通常称为
″
输入
″
残基,其通常取自
″
输入
″
可变结构域。人源化可例如按照jones等人,1986,nature 321:522-5;riechmann等人,nature,1988,332:323-7;以及verhoeyen等人,science,1988,239:1534-6的方法,通过用高变区序列取代人抗体的对应序列进行。
[0269]
在一些情况下,人源化抗体通过cdr移植构建,其中亲本非人(例如,啮齿动物)抗体的六个cdr的氨基酸序列移植到人抗体框架上。例如,padlan等人确定cdr中仅约三分之一的残基实际上接触抗原,并且将这些残基称为
″
特异性决定残基
″
或sdr(padlan等人,faseb j.,1995,9:133-9)。在sdr接枝技术中,仅sdr残基被接枝到人抗体框架上(参见例如,kashmiri等人,methods,2005,36:25-34)。
[0270]
用于制备人源化抗体的人可变结构域(轻链和重链两者)的选择对于降低抗原性很重要。例如,根据所谓的
″
最佳拟合
″
方法,针对已知人可变结构域序列的整个文库筛选非人(例如,啮齿动物)抗体的可变结构域的序列。可选择最接近啮齿动物的人序列作为人源化抗体的人框架(sims等人,j.immunol.,1993,151:2296-308;以及chothia等人,
j.mol.biol.,1987,196:901-17)。另一种方法使用来源于特定轻链或重链亚组的所有人抗体的共有序列的特定框架。相同的框架可用于几种不同的人源化抗体(carter等人,proc.natl.acad.sci.usa,1992,89:4285-89;以及presta等人,j.immunol.,1993,151:2623-32)。在一些情况下,框架源自最丰富的人亚类vl6亚组i(vl6i)和vh亚组iii(vhiii)的共有序列。在另一种方法中,人类种系基因用作框架区的来源。
[0271]
在基于cdr的比较的另选范例中,称为超人源化,fr同源性是不相关的。所述方法由非人序列与功能性人种系基因组库的比较组成。然后选择对鼠序列进行编码相同或紧密相关正则结构的那些基因。接着,在与非人抗体共享规范结构的基因中,选择在cdr内具有最高同源性的基因作为fr供体。最后,将非人cdr接枝到这些fr上(参见例如,tan等人,j.immunol.,2002,169:1119-25)。
[0272]
通常还期望抗体被人源化,同时保留其对抗原的亲和力和其他有利的生物特性。为了实现这个目标,根据一个方法,人源化抗体使用亲本和人源化序列的三维模型通过亲本序列和各种概念上的人源化产物的分析过程进行制备。三维免疫球蛋白模型通常是可用的并且是为本领域的技术人员所熟悉的。举例说明且显示所选候选免疫球蛋白序列的可能三维构象结构的计算机程序是可用的。这些包括例如wam(whitelegg和rees,protein eng.,2000,13:819-24)、modeller(sali和blundell,j.mol.biol.,1993,234:779-815)和swiss pdb viewer(guex和peitsch,electrophoresis,1997,18:2714-23)。这些展示的检测使得能分析在候选免疫球蛋白序列的功能发挥中残基的可能作用,例如分析影响候选免疫球蛋白与其抗原结合的能力的残基。以这种方式,可以从受体和输入序列中选择和组合fr残基,从而能实现所需抗体特征,诸如对靶抗原的增加的亲和力。通常,高变区残基直接且基本上大多数涉及影响抗原结合。
[0273]
用于抗体人源化的另一种方法是基于称为人类链含量(hsc)的抗体人源性的度量。该方法将小鼠序列与人种系基因的组库进行比较,并且差异被评分为hsc。然后通过使其hsc最大化而不是使用全局同一性测量来人源化靶序列,以生成多种不同人源化变体(lazar等人,mol.immunol.,2007,44:1986-98)。
[0274]
除了上述方法之外,经验方法还可以用于生成和选择人源化抗体。这些方法包括基于生成人源化变体的大基因库和使用富集技术或高通量筛选技术选择最佳克隆的方法。抗体变体可从噬菌体、核糖体和酵母展示文库中分离以及通过细菌菌落筛选分离(参见例如,hoogenboom,nat.biotechnol.,2005,23:1105-16;dufner等人,trends biotechnol.,2006,24:523-9;feldhaus等人,nat.biotechnol.,2003,21∶163-70;以及schlapschy等人,protein eng.des.sel.,2004,17:847-60)。
[0275]
在fr文库方法中,在fr中的特定位置处引入残基变体的集合,随后筛选文库以选择最佳支持移植cdr的fr。待取代的残基可包括一些或所有被鉴定为可能有助于cdr结构的
″
vernier
″
残基(参见例如,foote和winter,j.mol.biol.,1992,224:487-99),或通过baca等人,j.biol.chem.,1997,272:10678-84鉴定的更有限的靶残基组。
[0276]
在fr改组中,将完整fr与非人cdr组合,而不是产生所选残基变体的组合文库(参见例如,dall
′
acqua等人,methods,2005,36:43-60)。可在两步法:第一步人源化vl,然后人源化vh中筛选用于结合的文库。另选地,可使用一步fr改组方法。已证实这种方法比两步筛选更有效,因为所得抗体表现出改进的生物化学和物理化学性质,包括增强的表达、增加的
亲和力和热稳定性(参见例如,damschroder等人,mol.immunol.,2007,44:3049-60)。
[0277]
″
人源改造
″
方法基于实验鉴定必需的最小特异性决定簇(msd),并且基于将非人片段顺序替换到人fr文库中并评估结合。其开始于非人vh和vl链的cdr3区,并且将非人抗体的其他区逐渐替换为人fr,包括vh和vl两者的cdr1和cdr2。该方法通常导致表位保留和鉴定具有不同人v-区段cdr的多个亚类的抗体。人源改造允许分离与人种系基因抗体91%-96%同源的抗体(参见例如,alfenito,cambridge healthtech institute
′
s third annual pegs,the protein engineering summit,2007)。
[0278]
″
人类工程化
″
方法涉及通过对抗体的氨基酸序列进行特异性改变来改变非人抗体或抗体片段诸如小鼠或嵌合抗体或抗体片段,以便产生在人类中具有降低的免疫原性的修饰抗体,该抗体仍然保留原始非人抗体的所需结合特性。通常,该技术涉及将非人(例如,小鼠)抗体的氨基酸残基分类为
″
低风险
″
、
″
中等风险
″
或
″
高风险
″
残基。使用整体风险/回报计算来执行分类,该整体风险/回报计算评估针对取代将影响所得抗体折叠的风险进行特定取代(例如针对人类中的免疫原性)的预测益处。可通过将来自非人抗体可变区的氨基酸序列与特定或共有人抗体序列的相应区域进行比对来选择在非人(例如,小鼠)抗体序列的给定位置(例如,低或中等风险)处待被取代的特定人氨基酸残基。非人序列中的低或中度风险位置处的氨基酸残基可以根据比对来取代人抗体序列中的对应残基。用于制造人类工程化蛋白质的技术更详细地描述于以下中:studnicka等人,protein engineering,1994,7:805-14;美国专利号5,766,886;5,770,196;5,821,123;和5,869,619;以及pct公开wo 93/11794。
[0279]
可以使用例如复合人抗体
tm
技术(antitope ltd.,cambridge,united kingdom)产生复合人抗体。为了产生复合人抗体,以避免t细胞表位的方式从多个人抗体可变区序列的片段设计可变区序列,从而使所得抗体的免疫原性最小化。此类抗体可包含人恒定区序列,例如人轻链和/或重链恒定区。
[0280]
去免疫抗体是其中已经去除t细胞表位的抗体。已经描述了用于制备去免疫抗体的方法(参见例如,jones等人,methods mol biol.,2009,525:405-23;和de groot等人,cell.immunol.,2006,244:148-153)。去免疫抗体包含t细胞表位耗竭的可变区和人恒定区。简而言之,克隆抗体的vh和vl,并且随后通过在t细胞增殖测定中测试来源于抗体的vh和vl的重叠肽来鉴定t细胞表位。经由电子方法鉴定t细胞表位以鉴定与人mhc ii类结合的肽。将突变引入vh和vl中以消除与人mhc ii类的结合。然后利用突变的vh和vl来生成去免疫抗体。
[0281]
5.15抗体变体
[0282]
在一些实施方案中,设想了本文所提供的抗体的氨基酸序列修饰。例如,可能期望改善抗体的结合亲和力和/或其他生物特性,包括但不限于特异性、热稳定性、表达水平、效应子功能、糖基化(例如,岩藻糖基化)、降低的免疫原性或溶解度。因此,除本文所述的抗体之外,预期可制备抗体变体。例如,可通过将适当的核苷酸变化引入编码dna和/或通过合成期望的抗体或多肽来制备抗体变体。本领域技术人员将理解,氨基酸变化可改变抗体的翻译后过程,诸如改变糖基化位点的数量或位置或改变膜锚固特征。
[0283]
在一些实施方案中,本文提供的抗体例如通过将任何类型的分子共价连接至抗体而被化学修饰。抗体衍生物可包括已经例如通过糖基化、乙酰化、聚乙二醇化、磷酸化、酰胺
化、通过已知保护/封闭基团的衍生化、蛋白水解裂解、与细胞配体或其他蛋白质的连接等被化学修饰的抗体。许多化学修饰中的任一种化学修饰可通过已知技术进行,这些技术包括但不限于特异性化学裂解、乙酰化、配制、衣霉素的代谢合成等。另外,抗体可含有一种或多种非典型氨基酸。
[0284]
变体可以是编码抗体或多肽的一个或多个密码子的取代、缺失或插入,这导致氨基酸序列与天然序列抗体或多肽相比发生变化。氨基酸取代可以是用具有类似结构和/或化学特性的一个氨基酸替换另一个氨基酸的结果,诸如用丝氨酸替换亮氨酸,例如,保守氨基酸替换。本领域技术人员已知的标准技术可用于在编码本文提供的分子的核苷酸序列中引入突变,包括例如导致氨基酸取代的定点诱变和pcr介导的诱变。插入或缺失可任选地在约1至5个氨基酸的范围内。在某些实施方案中,取代、缺失或插入包括相对于原始分子少于25个氨基酸取代、少于20个氨基酸取代、少于15个氨基酸取代、少于10个氨基酸取代、少于5个氨基酸取代、少于4个氨基酸取代、少于3个氨基酸取代或少于2个氨基酸取代。在具体实施方案中,取代是在一个或多个预测的非必需氨基酸残基处进行的保守氨基酸取代。所允许的变体可通过系统地对序列中的氨基酸进行插入、缺失或取代并针对全长或成熟天然序列所表现出的活性测试所得变体来确定。
[0285]
氨基酸序列插入包括长度范围从一个残基到含有一百个或更多个残基的多肽的氨基和/或羧基末端融合物,以及单个或多个氨基酸残基的序列内插入。末端插入的示例包括具有n-末端甲硫氨酰残基的抗体。抗体分子的其他插入变体包括抗体的n-末端或c-末端与酶(例如,对于抗体导向的酶前药疗法来说)或多肽的融合物,这延长了抗体的血清半衰期。
[0286]
″
保守氨基酸取代
″
是其中氨基酸残基被具有带类似电荷的侧链的氨基酸残基替换的取代。本领域已经定义了具有带类似电荷的侧链的氨基酸残基家族。这些家族包括具有碱性侧链(例如,赖氨酸、精氨酸、组氨酸)、酸性侧链(例如,天冬氨酸、谷氨酸)、不带电荷的极性侧链(例如,甘氨酸、天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸、酪氨酸、半胱氨酸)、非极性侧链(例如,丙氨酸、缬氨酸、亮氨酸、异亮氨酸、脯氨酸、苯丙氨酸、甲硫氨酸、色氨酸)、β-支链侧链(例如,苏氨酸、缬氨酸、异亮氨酸)和芳族侧链(例如,酪氨酸、苯丙氨酸、色氨酸、组氨酸)的氨基酸。另选地,突变可沿编码序列的全部或部分诸如通过饱和诱变随机引入,并且可筛选所得突变体的生物活性以鉴定保留活性的突变体。在诱变后,可表达所编码的蛋白质,并且可确定蛋白质的活性。
[0287]
抗体的生物特性中的基本修饰是通过选择取代而实现的,这些取代对维持(a)多肽主链在取代区域中的结构,例如,作为折叠或螺旋构象;(b)分子在靶位点处的电荷或疏水性;或(c)侧链的本体的效果显著不同。另选地,(例如,在具有相似特性和/或侧链的氨基酸基团内)可进行保守取代,以便维持或不显著改变特性。氨基酸可根据其侧链特性的相似性来分组(参见例如,lehninger,biochemistry 73-75(第2版1975)):(1)非极性:ala(a)、val(v)、leu(l)、ile(i)、pro(p)、phe(f)、trp(w)、met(m);(2)不带电荷极性:gly(g)、ser(s)、thr(t)、cys(c)、tyr(y)、asn(n)、gln(q);(3)酸性:asp(d)、glu(e);和(4)碱性:lys(k)、arg(r)、his(h)。
[0288]
另选地,天然存在的残基可基于常见的侧链特性分成几组:(1)疏水性:正亮氨酸、met、ala、val、leu、ile;(2)中性亲水:cys、ser、thr、asn、gln;(3)酸性:asp、glu;(4)碱性:
his、lys、arg;(5)影响链取向的残基:gly、pro;和(6)芳族:trp、tyr、phe。
[0289]
非保守取代需要将这些类别中的一个类别的成员交换为另一类别。也可将此类经取代的残基引入保守取代位点或引入剩余(非保守)位点。
[0290]
因此,在一个实施方案中,与hla-g、cd37、gprc5d、klk2、psma或bcma表位结合的抗体包含与本文所述抗体的氨基酸序列,例如以下第7部分中所述的抗体至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列。
[0291]
在一个实施方案中,与hla-g、cd37、gprc5d、klk2、psma或bcma表位结合的抗体包含与本文所述抗体的氨基酸序列至少35%相同的氨基酸序列。在一个实施方案中,与hla-g、cd37、gprc5d、klk2、psma或bcma表位结合的抗体包含与本文所述抗体的氨基酸序列至少40%相同的氨基酸序列。在一个实施方案中,与hla-g、cd37、gprc5d、klk2、psma或bcma表位结合的抗体包含与本文所述抗体的氨基酸序列至少45%相同的氨基酸序列。在一个实施方案中,与hla-g、cd37、gprc5d、klk2、psma或bcma表位结合的抗体包含与本文所述抗体的氨基酸序列至少50%相同的氨基酸序列。在一个实施方案中,与hla-g、cd37、gprc5d、klk2、psma或bcma表位结合的抗体包含与本文所述抗体的氨基酸序列至少55%相同的氨基酸序列。在一个实施方案中,与hla-g、cd37、gprc5d、klk2、psma或bcma表位结合的抗体包含与本文所述抗体的氨基酸序列至少60%相同的氨基酸序列。在一个实施方案中,与hla-g、cd37、gprc5d、klk2、psma或bcma表位结合的抗体包含与本文所述抗体的氨基酸序列至少65%相同的氨基酸序列。在一个实施方案中,与hla-g、cd37、gprc5d、klk2、psma或bcma表位结合的抗体包含与本文所述抗体的氨基酸序列至少70%相同的氨基酸序列。在一个实施方案中,与hla-g、cd37、gprc5d、klk2、psma或bcma表位结合的抗体包含与本文所述抗体的氨基酸序列至少75%相同的氨基酸序列。在一个实施方案中,与hla-g、cd37、gprc5d、klk2、psma或bcma表位结合的抗体包含与本文所述抗体的氨基酸序列至少80%相同的氨基酸序列。在一个实施方案中,与hla-g、cd37、gprc5d、klk2、psma或bcma表位结合的抗体包含与本文所述抗体的氨基酸序列至少90%相同的氨基酸序列。在一个实施方案中,与hla-g、cd37、gprc5d、klk2、psma或bcma表位结合的抗体包含与本文所述抗体的氨基酸序列至少95%相同的氨基酸序列。在一个实施方案中,与hla-g、cd37、gprc5d、klk2、psma或bcma结合的抗体包含与本文所述抗体的氨基酸序列至少99%相同的氨基酸序列。
[0292]
在一些实施方案中,本文提供了与cd37表位结合并包含vl区、vh区、轻链和/或重链的抗体,该vl区包含与表3中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列,该vh区包含与表6中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列,该轻链包含与表7中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列,该重链包含与表8中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列。
[0293]
在一些实施方案中,本文提供了与cd37表位结合并包含vl区的抗体,该vl区包含与表5中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vl区的抗体,该vl区包含与表5中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vl区的抗体,该vl区包含与表5中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vl区的抗体,该vl区包含与表5中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vl区的抗体,该vl区包含与表5中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vl区的抗体,该vl区包含与表5中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vl区的抗体,该vl区包含与表5中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vl区的抗体,该vl区包含与表5中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vl区的抗体,该vl区包含与表5中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vl区的抗体,该vl区包含与表5中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vl区的抗体,该vl区包含与表5中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vl区的抗体,该vl区包含与表5中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vl区的抗体,该vl区包含与表5中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vl区的抗体,该vl区包含与表5中提供的氨基酸序列至少99%相同的氨基酸序列。
[0294]
在一些实施方案中,本文提供了与cd37表位结合并包含vh区的抗体,该vh区包含与表6中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vh区的抗体,该vh区包含与表6中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vh区的抗体,该vh区包含与表6中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vh区的抗体,该vh区包含与表6中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vh区的抗体,该vh区包含与表6中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vh区的抗体,该vh区包含与表6中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vh区的抗体,该vh区包含与表6中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vh区的抗体,该vh区包含与表6中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vh区的抗体,该vh区包含与表6中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vh区的抗体,该vh区包含与表6中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vh区的抗体,该vh区包含与表6中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案
中,本文提供了与cd37表位结合并包含vh区的抗体,该vh区包含与表6中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vh区的抗体,该vh区包含与表6中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含vh区的抗体,该vh区包含与表6中提供的氨基酸序列至少99%相同的氨基酸序列。
[0295]
在一些实施方案中,本文提供了与cd37表位结合并包含轻链的抗体,该轻链包含与表7中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含轻链的抗体,该轻链包含与表7中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含轻链的抗体,该轻链包含与表7中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含轻链的抗体,该轻链包含与表7中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含轻链的抗体,该轻链包含与表7中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含轻链的抗体,该轻链包含与表7中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含轻链的抗体,该轻链包含与表7中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含轻链的抗体,该轻链包含与表7中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含轻链的抗体,该轻链包含与表7中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含轻链的抗体,该轻链包含与表7中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含轻链的抗体,该轻链包含与表7中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含轻链的抗体,该轻链包含与表7中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含轻链的抗体,该轻链包含与表7中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含轻链的抗体,该轻链包含与表7中提供的氨基酸序列至少99%相同的氨基酸序列。
[0296]
在一些实施方案中,本文提供了与cd37表位结合并包含重链的抗体,该重链包含与表8中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含重链的抗体,该重链包含与表8中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含重链的抗体,该重链包含与表8中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含重链的抗体,该重链包含与表8中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含重链的抗体,该重链包含与表8中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含重链的抗体,该重链包含与表8中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含重链的抗体,该重链包含与表8中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含重链的抗体,该重链包含与表8中提供的氨基酸序列至少70%
相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含重链的抗体,该重链包含与表8中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含重链的抗体,该重链包含与表8中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含重链的抗体,该重链包含与表8中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含重链的抗体,该重链包含与表8中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含重链的抗体,该重链包含与表8中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与cd37表位结合并包含重链的抗体,该重链包含与表8中提供的氨基酸序列至少99%相同的氨基酸序列。
[0297]
在又一个实施方案中,与cd37表位结合的抗体包含与下表5和下表6中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的vl cdr和/或vh cdr氨基酸序列。
[0298]
在又一个实施方案中,与cd37表位结合的抗体包含与表5和表6中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少35%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与cd37表位结合的抗体包含与表5和表6中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少40%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与cd37表位结合的抗体包含与表5和表6中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少45%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与cd37表位结合的抗体包含与表5和表6中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少50%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与cd37表位结合的抗体包含与表5和表6中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少55%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与cd37表位结合的抗体包含与表5和表6中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少60%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与cd37表位结合的抗体包含与表5和表6中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少65%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与cd37表位结合的抗体包含与表5和表6中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少70%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与cd37表位结合的抗体包含与表5和表6中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少75%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与cd37表位结合的抗体包含与表5和表6中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少80%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与cd37表位结合的抗体包含与表5和表6中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少85%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与cd37表位结合的抗体包含与表5和表6中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少90%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与cd37表位结合的抗体包含与表5和表6中的vl和vh
序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少95%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与cd37表位结合的抗体包含与表5和表6中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少99%相同的vl cdr和/或vh cdr氨基酸序列。
[0299]
在一些实施方案中,本文提供了与gprc5d表位结合并包含vl区、vh区、轻链和/或重链的抗体,该vl区包含与表13中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列,该vh区包含与表13中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列,该轻链包含与表14中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列,该重链包含与表14中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列。
[0300]
在一些实施方案中,本文提供了与gprc5d表位结合并包含vl区的抗体,该vl区包含与表13中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vl区的抗体,该vl区包含与表13中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vl区的抗体,该vl区包含与表13中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vl区的抗体,该vl区包含与表13中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vl区的抗体,该vl区包含与表13中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vl区的抗体,该vl区包含与表13中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vl区的抗体,该vl区包含与表13中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vl区的抗体,该vl区包含与表13中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vl区的抗体,该vl区包含与表13中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vl区的抗体,该vl区包含与表13中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vl区的抗体,该vl区包含与表13中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vl区的抗体,该vl区包含与表13中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vl区的抗体,该vl区包含与表13中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vl区的抗体,该vl区包含与表13中提供的氨基酸序列至少99%相同的氨基酸序列。
[0301]
在一些实施方案中,本文提供了与gprc5d表位结合并包含vh区的抗体,该vh区包含与表13中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供
了与gprc5d表位结合并包含vh区的抗体,该vh区包含与表13中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vh区的抗体,该vh区包含与表13中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vh区的抗体,该vh区包含与表13中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vh区的抗体,该vh区包含与表13中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vh区的抗体,该vh区包含与表13中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vh区的抗体,该vh区包含与表13中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vh区的抗体,该vh区包含与表13中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vh区的抗体,该vh区包含与表13中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vh区的抗体,该vh区包含与表13中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vh区的抗体,该vh区包含与表13中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vh区的抗体,该vh区包含与表13中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vh区的抗体,该vh区包含与表13中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含vh区的抗体,该vh区包含与表13中提供的氨基酸序列至少99%相同的氨基酸序列。
[0302]
在一些实施方案中,本文提供了与gprc5d表位结合并包含轻链的抗体,该轻链包含与表14中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含轻链的抗体,该轻链包含与表14中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含轻链的抗体,该轻链包含与表14中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含轻链的抗体,该轻链包含与表14中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含轻链的抗体,该轻链包含与表14中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含轻链的抗体,该轻链包含与表14中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含轻链的抗体,该轻链包含与表14中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含轻链的抗体,该轻链包含与表14中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含轻链的抗体,该轻链包含与表14中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含轻链的抗体,该轻链包含与表14中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含轻链的抗体,该轻链包含与表14中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含轻链的抗体,该轻链包含与表14中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方
案中,本文提供了与gprc5d表位结合并包含轻链的抗体,该轻链包含与表14中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含轻链的抗体,该轻链包含与表14中提供的氨基酸序列至少99%相同的氨基酸序列。
[0303]
在一些实施方案中,本文提供了与gprc5d表位结合并包含重链的抗体,该重链包含与表14中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含重链的抗体,该重链包含与表14中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含重链的抗体,该重链包含与表14中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含重链的抗体,该重链包含与表14中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含重链的抗体,该重链包含与表14中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含重链的抗体,该重链包含与表14中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含重链的抗体,该重链包含与表14中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含重链的抗体,该重链包含与表14中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含重链的抗体,该重链包含与表14中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含重链的抗体,该重链包含与表14中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含重链的抗体,该重链包含与表14中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含重链的抗体,该重链包含与表14中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含重链的抗体,该重链包含与表14中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与gprc5d表位结合并包含重链的抗体,该重链包含与表14中提供的氨基酸序列至少99%相同的氨基酸序列。
[0304]
在又一个实施方案中,与gprc5d表位结合的抗体包含与下表13中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的vl cdr和/或vh cdr氨基酸序列。
[0305]
在又一个实施方案中,与gprc5d表位结合的抗体包含与表13中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少35%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与gprc5d表位结合的抗体包含与表13中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少40%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与gprc5d表位结合的抗体包含与表13中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少45%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与gprc5d表位结合的抗体包含与表13中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少50%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与gprc5d表位结合的抗体包含与表13中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少55%相同的vl cdr和/或vh cdr氨基
酸序列。在又一个实施方案中,与gprc5d表位结合的抗体包含与表13中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少60%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与gprc5d表位结合的抗体包含与表13中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少65%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与gprc5d表位结合的抗体包含与表13中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少70%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与gprc5d表位结合的抗体包含与表13中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少75%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与gprc5d表位结合的抗体包含与表13中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少80%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与gprc5d表位结合的抗体包含与表13中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少85%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与gprc5d表位结合的抗体包含与表13中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少90%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与gprc5d表位结合的抗体包含与表13中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少95%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与gprc5d表位结合的抗体包含与表13中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少99%相同的vl cdr和/或vh cdr氨基酸序列。
[0306]
在一个实施方案中,与klk2表位结合的抗体包含与本文所述抗体的氨基酸序列至少35%相同的氨基酸序列。在一个实施方案中,与klk2表位结合的抗体包含与本文所述抗体的氨基酸序列至少40%相同的氨基酸序列。在一个实施方案中,与klk2表位结合的抗体包含与本文所述抗体的氨基酸序列至少45%相同的氨基酸序列。在一个实施方案中,与klk2表位结合的抗体包含与本文所述抗体的氨基酸序列至少50%相同的氨基酸序列。在一个实施方案中,与klk2表位结合的抗体包含与本文所述抗体的氨基酸序列至少55%相同的氨基酸序列。在一个实施方案中,与klk2表位结合的抗体包含与本文所述抗体的氨基酸序列至少60%相同的氨基酸序列。在一个实施方案中,与klk2表位结合的抗体包含与本文所述抗体的氨基酸序列至少65%相同的氨基酸序列。在一个实施方案中,与klk2表位结合的抗体包含与本文所述抗体的氨基酸序列至少70%相同的氨基酸序列。在一个实施方案中,与klk2表位结合的抗体包含与本文所述抗体的氨基酸序列至少75%相同的氨基酸序列。在一个实施方案中,与klk2表位结合的抗体包含与本文所述抗体的氨基酸序列至少80%相同的氨基酸序列。在一个实施方案中,与klk2表位结合的抗体包含与本文所述抗体的氨基酸序列至少90%相同的氨基酸序列。在一个实施方案中,与klk2表位结合的抗体包含与本文所述抗体的氨基酸序列至少95%相同的氨基酸序列。在一个实施方案中,与klk2结合的抗体包含与本文所述抗体的氨基酸序列至少99%相同的氨基酸序列。
[0307]
在一些实施方案中,本文提供了与klk2表位结合并包含vl区、vh区、轻链和/或重链的抗体,该vl区包含与表19中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列,该vh区包含与表19中提供的氨基酸序列至少
35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列,该轻链包含与表21中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列,该重链包含与表21中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列。
[0308]
在一些实施方案中,本文提供了与klk2表位结合并包含vl区的抗体,该vl区包含与表19中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vl区的抗体,该vl区包含与表19中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vl区的抗体,该vl区包含与表19中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vl区的抗体,该vl区包含与表19中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vl区的抗体,该vl区包含与表19中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vl区的抗体,该vl区包含与表19中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vl区的抗体,该vl区包含与表19中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vl区的抗体,该vl区包含与表19中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vl区的抗体,该vl区包含与表19中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vl区的抗体,该vl区包含与表19中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vl区的抗体,该vl区包含与表19中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vl区的抗体,该vl区包含与表19中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vl区的抗体,该vl区包含与表19中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vl区的抗体,该vl区包含与表19中提供的氨基酸序列至少99%相同的氨基酸序列。
[0309]
在一些实施方案中,本文提供了与klk2表位结合并包含vh区的抗体,该vh区包含与表19中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vh区的抗体,该vh区包含与表19中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vh区的抗体,该vh区包含与表19中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vh区的抗体,该vh区包含与表19中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vh区的抗体,该vh区包含与表19中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vh区的抗体,该vh区包含与表19中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vh区的抗
体,该vh区包含与表19中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vh区的抗体,该vh区包含与表19中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vh区的抗体,该vh区包含与表19中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vh区的抗体,该vh区包含与表19中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vh区的抗体,该vh区包含与表19中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vh区的抗体,该vh区包含与表19中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vh区的抗体,该vh区包含与表19中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含vh区的抗体,该vh区包含与表19中提供的氨基酸序列至少99%相同的氨基酸序列。
[0310]
在一些实施方案中,本文提供了与klk2表位结合并包含轻链的抗体,该轻链包含与表21中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含轻链的抗体,该轻链包含与表21中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含轻链的抗体,该轻链包含与表21中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含轻链的抗体,该轻链包含与表21中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含轻链的抗体,该轻链包含与表21中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含轻链的抗体,该轻链包含与表21中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含轻链的抗体,该轻链包含与表21中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含轻链的抗体,该轻链包含与表21中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含轻链的抗体,该轻链包含与表21中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含轻链的抗体,该轻链包含与表21中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含轻链的抗体,该轻链包含与表21中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含轻链的抗体,该轻链包含与表21中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含轻链的抗体,该轻链包含与表21中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含轻链的抗体,该轻链包含与表21中提供的氨基酸序列至少99%相同的氨基酸序列。
[0311]
在一些实施方案中,本文提供了与klk2表位结合并包含重链的抗体,该重链包含与表21中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含重链的抗体,该重链包含与表21中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含重链的抗体,该重链包含与表21中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提
供了与klk2表位结合并包含重链的抗体,该重链包含与表21中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含重链的抗体,该重链包含与表21中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含重链的抗体,该重链包含与表21中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含重链的抗体,该重链包含与表21中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含重链的抗体,该重链包含与表21中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含重链的抗体,该重链包含与表21中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含重链的抗体,该重链包含与表21中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含重链的抗体,该重链包含与表21中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含重链的抗体,该重链包含与表21中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含重链的抗体,该重链包含与表21中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与klk2表位结合并包含重链的抗体,该重链包含与表21中提供的氨基酸序列至少99%相同的氨基酸序列。
[0312]
在又一个实施方案中,与klk2表位结合的抗体包含与下表19中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的vl cdr和/或vh cdr氨基酸序列。
[0313]
在又一个实施方案中,与klk2表位结合的抗体包含与表19中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少35%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与klk2表位结合的抗体包含与表19中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少40%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与klk2表位结合的抗体包含与表19中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少45%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与klk2表位结合的抗体包含与表19中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少50%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与klk2表位结合的抗体包含与表19中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少55%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与klk2表位结合的抗体包含与表19中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少60%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与klk2表位结合的抗体包含与表19中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少65%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与klk2表位结合的抗体包含与表19中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少70%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与klk2表位结合的抗体包含与表19中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少75%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,
与klk2表位结合的抗体包含与表19中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少80%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与klk2表位结合的抗体包含与表19中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少85%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与klk2表位结合的抗体包含与表19中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少90%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与klk2表位结合的抗体包含与表19中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少95%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与klk2表位结合的抗体包含与表19中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少99%相同的vl cdr和/或vh cdr氨基酸序列。
[0314]
在一些实施方案中,本文提供了与hla-g表位结合并包含vl区、vh区、轻链和/或重链的抗体,该vl区包含与表24中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列,该vh区包含与表24中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列,该轻链包含与表25中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列,该重链包含与表25中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列。
[0315]
在一些实施方案中,本文提供了与hla-g表位结合并包含vl区的抗体,该vl区包含与表24中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vl区的抗体,该vl区包含与表24中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vl区的抗体,该vl区包含与表24中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vl区的抗体,该vl区包含与表24中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vl区的抗体,该vl区包含与表24中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vl区的抗体,该vl区包含与表24中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vl区的抗体,该vl区包含与表24中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vl区的抗体,该vl区包含与表24中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vl区的抗体,该vl区包含与表24中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vl区的抗体,该vl区包含与表24中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vl区的抗体,该vl区包含与表24中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vl区的抗体,该vl区包含与
表24中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vl区的抗体,该vl区包含与表24中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vl区的抗体,该vl区包含与表24中提供的氨基酸序列至少99%相同的氨基酸序列。
[0316]
在一些实施方案中,本文提供了与hla-g表位结合并包含vh区的抗体,该vh区包含与表24中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vh区的抗体,该vh区包含与表24中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vh区的抗体,该vh区包含与表24中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vh区的抗体,该vh区包含与表24中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vh区的抗体,该vh区包含与表24中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vh区的抗体,该vh区包含与表24中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vh区的抗体,该vh区包含与表24中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vh区的抗体,该vh区包含与表24中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vh区的抗体,该vh区包含与表24中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vh区的抗体,该vh区包含与表24中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vh区的抗体,该vh区包含与表24中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vh区的抗体,该vh区包含与表24中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vh区的抗体,该vh区包含与表24中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含vh区的抗体,该vh区包含与表24中提供的氨基酸序列至少99%相同的氨基酸序列。
[0317]
在一些实施方案中,本文提供了与hla-g表位结合并包含轻链的抗体,该轻链包含与表25中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含轻链的抗体,该轻链包含与表25中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含轻链的抗体,该轻链包含与表25中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含轻链的抗体,该轻链包含与表25中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含轻链的抗体,该轻链包含与表25中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含轻链的抗体,该轻链包含与表25中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含轻链的抗体,该轻链包含与表25中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含轻链的抗体,该轻链包含与表25中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合
并包含轻链的抗体,该轻链包含与表25中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含轻链的抗体,该轻链包含与表25中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含轻链的抗体,该轻链包含与表25中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含轻链的抗体,该轻链包含与表25中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含轻链的抗体,该轻链包含与表25中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含轻链的抗体,该轻链包含与表25中提供的氨基酸序列至少99%相同的氨基酸序列。
[0318]
在一些实施方案中,本文提供了与hla-g表位结合并包含重链的抗体,该重链包含与表25中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含重链的抗体,该重链包含与表25中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含重链的抗体,该重链包含与表25中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含重链的抗体,该重链包含与表25中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含重链的抗体,该重链包含与表25中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含重链的抗体,该重链包含与表25中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含重链的抗体,该重链包含与表25中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含重链的抗体,该重链包含与表25中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含重链的抗体,该重链包含与表25中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含重链的抗体,该重链包含与表25中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含重链的抗体,该重链包含与表25中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含重链的抗体,该重链包含与表25中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含重链的抗体,该重链包含与表25中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与hla-g表位结合并包含重链的抗体,该重链包含与表25中提供的氨基酸序列至少99%相同的氨基酸序列。
[0319]
在又一个实施方案中,与hla-g表位结合的抗体包含与下表24中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的vl cdr和/或vh cdr氨基酸序列。
[0320]
在又一个实施方案中,与hla-g表位结合的抗体包含与表24中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少35%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与hla-g表位结合的抗体包含与表24中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少40%相同的vl cdr和/或vh cdr氨基酸
序列。在又一个实施方案中,与hla-g表位结合的抗体包含与表24中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少45%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与hla-g表位结合的抗体包含与表24中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少50%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与hla-g表位结合的抗体包含与表24中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少55%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与hla-g表位结合的抗体包含与表24中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少60%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与hla-g表位结合的抗体包含与表24中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少65%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与hla-g表位结合的抗体包含与表24中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少70%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与hla-g表位结合的抗体包含与表24中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少75%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与hla-g表位结合的抗体包含与表24中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少80%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与hla-g表位结合的抗体包含与表24中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少85%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与hla-g表位结合的抗体包含与表24中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少90%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与hla-g表位结合的抗体包含与表24中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少95%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与hla-g表位结合的抗体包含与表24中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少99%相同的vl cdr和/或vh cdr氨基酸序列。
[0321]
在一些实施方案中,本文提供了与psma表位结合并包含vl区、vh区、轻链和/或重链的抗体,该vl区包含与表28中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列,该vh区包含与表28中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列,该轻链包含与表30中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列,该重链包含与表30中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列。
[0322]
在一些实施方案中,本文提供了与psma表位结合并包含vl区的抗体,该vl区包含与表28中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vl区的抗体,该vl区包含与表28中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vl区的抗体,该vl区
包含与表28中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vl区的抗体,该vl区包含与表28中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vl区的抗体,该vl区包含与表28中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vl区的抗体,该vl区包含与表28中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vl区的抗体,该vl区包含与表28中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vl区的抗体,该vl区包含与表28中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vl区的抗体,该vl区包含与表28中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vl区的抗体,该vl区包含与表28中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vl区的抗体,该vl区包含与表28中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vl区的抗体,该vl区包含与表28中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vl区的抗体,该vl区包含与表28中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vl区的抗体,该vl区包含与表28中提供的氨基酸序列至少99%相同的氨基酸序列。
[0323]
在一些实施方案中,本文提供了与psma表位结合并包含vh区的抗体,该vh区包含与表28中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vh区的抗体,该vh区包含与表28中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vh区的抗体,该vh区包含与表28中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vh区的抗体,该vh区包含与表28中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vh区的抗体,该vh区包含与表28中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vh区的抗体,该vh区包含与表28中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vh区的抗体,该vh区包含与表28中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vh区的抗体,该vh区包含与表28中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vh区的抗体,该vh区包含与表28中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vh区的抗体,该vh区包含与表28中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vh区的抗体,该vh区包含与表28中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vh区的抗体,该vh区包含与表28中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vh区的抗体,该vh区包含与表28中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含vh区的抗体,该vh区包含与表28
中提供的氨基酸序列至少99%相同的氨基酸序列。
[0324]
在一些实施方案中,本文提供了与psma表位结合并包含轻链的抗体,该轻链包含与表30中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并且包含轻链的抗体,所述轻链包含与表30中提供的氨基酸序列至少40%一致的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并且包含轻链的抗体,所述轻链包含与表30中提供的氨基酸序列至少45%一致的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并且包含轻链的抗体,所述轻链包含与表30中提供的氨基酸序列至少50%一致的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并且包含轻链的抗体,所述轻链包含与表30中提供的氨基酸序列至少55%一致的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并且包含轻链的抗体,所述轻链包含与表30中提供的氨基酸序列至少60%一致的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并且包含轻链的抗体,所述轻链包含与表30中提供的氨基酸序列至少65%一致的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并且包含轻链的抗体,所述轻链包含与表30中提供的氨基酸序列至少70%一致的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并且包含轻链的抗体,所述轻链包含与表30中提供的氨基酸序列至少75%一致的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并且包含轻链的抗体,所述轻链包含与表30中提供的氨基酸序列至少80%一致的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并且包含轻链的抗体,所述轻链包含与表30中提供的氨基酸序列至少85%一致的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并且包含轻链的抗体,所述轻链包含与表30中提供的氨基酸序列至少90%一致的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并且包含轻链的抗体,所述轻链包含与表30中提供的氨基酸序列至少95%一致的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含轻链的抗体,该轻链包含与表30中提供的氨基酸序列至少99%相同的氨基酸序列。
[0325]
在一些实施方案中,本文提供了与psma表位结合并包含重链的抗体,该重链包含与表30中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含重链的抗体,该重链包含与表30中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含重链的抗体,该重链包含与表30中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含重链的抗体,该重链包含与表30中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含重链的抗体,该重链包含与表30中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含重链的抗体,该重链包含与表30中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含重链的抗体,该重链包含与表30中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含重链的抗体,该重链包含与表30中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含重链的抗体,该重链包含与表30中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含重链的抗体,该重链包含与表30中提供的氨
基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含重链的抗体,该重链包含与表30中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含重链的抗体,该重链包含与表30中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含重链的抗体,该重链包含与表30中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与psma表位结合并包含重链的抗体,该重链包含与表30中提供的氨基酸序列至少99%相同的氨基酸序列。
[0326]
在又一个实施方案中,与psma表位结合的抗体包含与下表28中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的vl cdr和/或vh cdr氨基酸序列。
[0327]
在又一个实施方案中,与psma表位结合的抗体包含与表28中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少35%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与psma表位结合的抗体包含与表28中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少40%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与psma表位结合的抗体包含与表28中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少45%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与psma表位结合的抗体包含与表28中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少50%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与psma表位结合的抗体包含与表28中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少55%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与psma表位结合的抗体包含与表28中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少60%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与psma表位结合的抗体包含与表28中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少65%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与psma表位结合的抗体包含与表28中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少70%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与psma表位结合的抗体包含与表28中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少75%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与psma表位结合的抗体包含与表28中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少80%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与psma表位结合的抗体包含与表28中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少85%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与psma表位结合的抗体包含与表28中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少90%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与psma表位结合的抗体包含与表28中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少95%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与psma表位结合的抗体包含与表28中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少99%相同的vl cdr和/或vh cdr氨基酸序列。
[0328]
在一些实施方案中,本文提供了与bcma表位结合并包含vl区和vh区的抗体,该vl区包含与表33中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列,该vh区包含与表33中提供的氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的氨基酸序列。
[0329]
在一些实施方案中,本文提供了与bcma表位结合并包含vl区的抗体,该vl区包含与表33中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vl区的抗体,该vl区包含与表33中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vl区的抗体,该vl区包含与表33中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vl区的抗体,该vl区包含与表33中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vl区的抗体,该vl区包含与表33中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vl区的抗体,该vl区包含与表33中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vl区的抗体,该vl区包含与表33中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vl区的抗体,该vl区包含与表33中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vl区的抗体,该vl区包含与表33中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vl区的抗体,该vl区包含与表33中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vl区的抗体,该vl区包含与表33中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vl区的抗体,该vl区包含与表33中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vl区的抗体,该vl区包含与表33中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vl区的抗体,该vl区包含与表33中提供的氨基酸序列至少99%相同的氨基酸序列。
[0330]
在一些实施方案中,本文提供了与bcma表位结合并包含vh区的抗体,该vh区包含与表33中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vh区的抗体,该vh区包含与表33中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vh区的抗体,该vh区包含与表33中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vh区的抗体,该vh区包含与表33中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vh区的抗体,该vh区包含与表33中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vh区的抗体,该vh区包含与表33中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vh区的抗体,该vh区包含与表33中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案
中,本文提供了与bcma表位结合并包含vh区的抗体,该vh区包含与表33中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vh区的抗体,该vh区包含与表33中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vh区的抗体,该vh区包含与表33中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vh区的抗体,该vh区包含与表33中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vh区的抗体,该vh区包含与表33中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vh区的抗体,该vh区包含与表33中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含vh区的抗体,该vh区包含与表33中提供的氨基酸序列至少99%相同的氨基酸序列。
[0331]
在一些实施方案中,本文提供了与bcma表位结合并包含重链的抗体,该重链包含与表34中提供的氨基酸序列至少35%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含重链的抗体,该重链包含与表34中提供的氨基酸序列至少40%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含重链的抗体,该重链包含与表34中提供的氨基酸序列至少45%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含重链的抗体,该重链包含与表34中提供的氨基酸序列至少50%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含重链的抗体,该重链包含与表34中提供的氨基酸序列至少55%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含重链的抗体,该重链包含与表34中提供的氨基酸序列至少60%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含重链的抗体,该重链包含与表34中提供的氨基酸序列至少65%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含重链的抗体,该重链包含与表34中提供的氨基酸序列至少70%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含重链的抗体,该重链包含与表34中提供的氨基酸序列至少75%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含重链的抗体,该重链包含与表34中提供的氨基酸序列至少80%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含重链的抗体,该重链包含与表34中提供的氨基酸序列至少85%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含重链的抗体,该重链包含与表34中提供的氨基酸序列至少90%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含重链的抗体,该重链包含与表34中提供的氨基酸序列至少95%相同的氨基酸序列。在一些实施方案中,本文提供了与bcma表位结合并包含重链的抗体,该重链包含与表34中提供的氨基酸序列至少99%相同的氨基酸序列。
[0332]
在又一个实施方案中,与bcma表位结合的抗体包含与下表33中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少35%、至少40%、至少45%、至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少95%或至少99%相同的vl cdr和/或vh cdr氨基酸序列。
[0333]
在又一个实施方案中,与bcma表位结合的抗体包含与表33中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少35%相同的vl cdr和/或vh cdr氨基酸
序列。在又一个实施方案中,与bcma表位结合的抗体包含与表33中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少40%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与bcma表位结合的抗体包含与表33中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少45%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与bcma表位结合的抗体包含与表33中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少50%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与bcma表位结合的抗体包含与表33中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少55%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与bcma表位结合的抗体包含与表33中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少60%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与bcma表位结合的抗体包含与表33中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少65%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与bcma表位结合的抗体包含与表33中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少70%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与bcma表位结合的抗体包含与表33中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少75%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与bcma表位结合的抗体包含与表33中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少80%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与bcma表位结合的抗体包含与表33中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少85%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与bcma表位结合的抗体包含与表33中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少90%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与bcma表位结合的抗体包含与表33中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少95%相同的vl cdr和/或vh cdr氨基酸序列。在又一个实施方案中,与bcma表位结合的抗体包含与表33中的vl和vh序列中所含的vl cdr氨基酸序列和/或vh cdr氨基酸序列至少99%相同的vl cdr和/或vh cdr氨基酸序列。
[0334]
5.16多价抗体
[0335]
相比于二价抗体,多价抗体可被表达抗体所结合的抗原的细胞更快地内化(和/或分解代谢)。本公开的抗体可以是具有三个或更多个抗原结合位点的多价抗体(其不是igm类别的)(例如,四价抗体),其可通过重组表达编码抗体的多肽链的核酸容易地产生。多价抗体可包含二聚化结构域和三个或更多个抗原结合位点。在某些实施方案中,二聚化结构域包含fc区或铰链区(或者由其组成)。在这种情况下,抗体将包含fc区和fc区的三个或更多个抗原结合位点氨基末端。在某些实施方案中,多价抗体包含三个至约八个抗原结合位点(或由其组成)。在一个此类实施方案中,多价抗体包含四个抗原结合位点(或由其组成)。多价抗体包含至少一条多肽链(例如,两条多肽链),其中多肽链包含两个或更多个可变结构域。例如,多肽链可包含vd1-(x1)n-vd2-(x2)n-fc,其中vd1是第一可变结构域,vd2是第二可变结构域,fc是fc区的一条多肽链,x1和x2表示氨基酸或多肽,并且n为0或1。例如,多肽链可包含:vh-ch1-柔性接头-vh-ch1-fc区链;或vh-ch1-vh-ch1-fc区链。本文的多价抗体还可包含至少两个(例如,四个)轻链可变结构域多肽。本文的多价抗体可例如包含约两
个至约八个轻链可变结构域多肽。本文设想的轻链可变结构域多肽包含轻链可变结构域,并且任选地还包含cl结构域。
[0336]
5.17多特异性抗体
[0337]
多特异性抗体诸如双特异性抗体是对至少两个不同抗原具有结合特异性的单克隆抗体。在某些实施方案中,可基于本文提供的抗体的序列,例如,本文提供的vl和vh序列中所含的cdr序列来构建多特异性抗体。在某些实施方案中,本文提供的多特异性抗体是双特异性抗体。在某些实施方案中,双特异性抗体是小鼠嵌合的人或人源化抗体。用于制备多特异性抗体的方法是本领域已知的,诸如通过两个免疫球蛋白重链-轻链对的共表达,其中两条重链具有不同的特异性(参见例如,milstein和cuello,nature,1983,305:537-40)。有关生成多特异性抗体(例如,双特异性抗体)的详细信息,参见例如,bispecific antibodies(kontermann编辑,2011)。
[0338]
5.18制备抗体的方法
[0339]
在又一方面,本文提供了用于制备本文提供的各种抗体的方法。
[0340]
在一些实施方案中,本文提供的与抗原(例如,hla-g、cd37、gprc5d、klk2、psma或bcma)结合的抗体(例如,本文提供的全长抗体、抗体的重链和/或轻链,或其突变体)的重组表达需要构建含有编码抗体的多核苷酸的表达载体。一旦已经获得编码本文提供的抗体分子或者抗体的重链或轻链的多核苷酸,就可通过基因合成(参见例如,zhang,d.等人,出处同上)和/或定点诱变(clynes,r.a.等人,nature medicine,2000,6(4):443-6)生成在全长抗体或其重链中包含k248e、t437r或k248e/t437r突变的此类多核苷酸的变体。在一些实施方案中,包含k248e/t437r突变的多核苷酸包含seq id no:85、86、87、88、89、90、91、92、106、160中的任一者的重链核苷酸序列。
[0341]
用于产生抗体分子的载体可通过重组dna技术使用本领域众所周知的技术产生。因此,本文描述了通过表达含有抗体编码核苷酸序列的多核苷酸来制备蛋白质的方法。本领域技术人员众所周知的方法可用于构建含有抗体编码序列和适当转录和翻译控制信号的表达载体。在一些实施方案中,这些方法为例如体外重组dna技术、合成技术和体内基因重组。在一些实施方案中,这些表达载体是可复制载体,其包含可操作地连接至启动子的编码本文提供的抗体分子或者抗体的重链或轻链的核苷酸序列。在一些实施方案中,这些载体可包含编码抗体分子的恒定区的核苷酸序列(参见例如,国际公布wo 86/05807和wo 89/01036;和美国专利5,122,464)并且可将抗体的可变结构域克隆到此类载体中以表达整条重链、整条轻链或整条重链和轻链两者。
[0342]
在一些实施方案中,通过常规技术将表达载体转移到宿主细胞中,然后通过常规技术培养经转染的细胞以产生本文提供的抗体。在一些实施方案中,宿主细胞含有可操作地连接至异源启动子的编码本文提供的抗体或其重链或轻链的多核苷酸。在用于表达双链抗体的某些实施方案中,编码重链和轻链两者的载体可在宿主细胞中共表达以表达整个免疫球蛋白分子,如下所详述。
[0343]
可利用多种宿主表达载体系统来表达本文提供的抗体分子(参见例如,美国专利5,807,715)。此类宿主表达系统代表了可产生并随后纯化目的编码序列的媒介物,而且也代表了在经适当的核苷酸编码序列转化或转染时可原位表达本文提供的抗体分子的细胞。在一些实施方案中,这些宿主表达系统是用含有抗体编码序列的重组噬菌体dna、质粒dna
或粘粒dna表达载体转化的微生物诸如细菌(例如,大肠杆菌和枯草芽孢杆菌(b.subtilis))。在一些实施方案中,这些宿主表达系统是用含有抗体编码序列的重组酵母表达载体转化的酵母(例如,毕赤酵母属(saccharomyces pichia))。在一些实施方案中,这些宿主表达系统是用含有抗体编码序列的重组病毒表达载体感染的昆虫细胞系统(例如,杆状病毒);用含有抗体编码序列的重组病毒表达载体(例如,花椰菜花叶病毒、camv、烟草花叶病毒、tmv)感染或用重组质粒表达载体(例如,ti质粒)转化的植物细胞系统。在一些实施方案中,这些宿主表达系统是包含重组表达构建体的哺乳动物细胞系统(例如,cos、cho、bhk、293、ns0和3t3细胞),这些重组表达构建体含有源自哺乳动物细胞的基因组(例如,金属硫蛋白启动子)或源自哺乳动物病毒(例如,腺病毒晚期启动子;牛痘病毒7.5k启动子)的启动子。在一些实施方案中,这些宿主表达系统是细菌细胞(诸如大肠杆菌)或真核细胞(尤其是对于整个重组抗体分子的表达),其可用于表达重组抗体分子。在一些实施方案中,哺乳动物细胞(诸如中国仓鼠卵巢细胞(cho))与载体(诸如来自人巨细胞病毒的主要中间早期基因启动子元件)结合是用于抗体的有效表达系统(foecking等人,gene,1986,45:101;和cockett等人,bio/technology,1990,8:2)。在一些实施方案中,本文提供的抗体在cho细胞中产生。在一些实施方案中,编码本文提供的与hla-g、cd37、gprc5d、klk2、psma或bcma抗原免疫特异性结合的抗体的核苷酸序列的表达是由组成型启动子、诱导型启动子或组织特异性启动子调控的。
[0344]
在细菌系统中,根据旨在用于表达抗体分子的用途,可有利地选择许多表达载体。例如,当要产生大量此类抗体时,为了生成抗体分子的药物组合物,可能期望指导表达易于纯化的高水平融合蛋白产物的载体。此类载体包括但不限于大肠杆菌表达载体pur278(ruther等人,embo,1983,12:1791),其中可将抗体编码序列与lac z编码区同框地单独连接到载体中,使得产生融合蛋白;pin载体(inouye&inouye,nucleic acids res.,1985,13:3101-3109;van heeke&schuster,j.biol.chem.,1989,24:5503-9);等。pgex载体还可用于表达外来多肽作为与谷胱甘肽5-转移酶(gst)的融合蛋白。在一些实施方案中,此类融合蛋白是可溶的并且可通过与基质谷胱甘肽琼脂糖珠吸附和结合,然后在游离谷胱甘肽存在下洗脱而容易地从溶解细胞中纯化。在一些实施方案中,pgex载体被设计成包括凝血酶或因子xa蛋白酶裂解位点,使得克隆的靶基因产物可从gst部分释放。
[0345]
在一些实施方案中,苜蓿银纹夜蛾(autographa californica)核多角体病毒(acnpv)用作在昆虫系统中表达外来基因的载体。在一些实施方案中,病毒在秋粘虫(spodoptera frugiperda)细胞中生长。在一些实施方案中,可将抗体编码序列单独地克隆到病毒的非必需区(例如多角体蛋白基因)中并且置于acnpv启动子(例如,多角体蛋白启动子)的控制下。
[0346]
在一些实施方案中,病毒载体,例如,基于烟草花叶病毒(tmv)的病毒载体用于植物细胞中,并且通过农杆菌属(agrobacterium)被系统地递送到植物体的多个部分以共表达多种目的抗体(giritch,a.等人,proc.natl.acad.sci.usa,2006,103(40):14701-6)。在一些实施方案中,使用植物细胞作为表达系统导致抗体的生产速度和产率以及合成哺乳动物型复合物n-低聚糖的能力显著增加(loos,a.和steinkellner,h.,arch biochem biophys.,2012,526-172(2):167-73)。
[0347]
在哺乳动物宿主细胞中,可利用许多基于病毒的表达系统。在一些实施方案中,在
将腺病毒用作表达载体的情况下,可将目的抗体编码序列连接到腺病毒转录/翻译控制复合物,例如晚期启动子和三联前导序列。在一些实施方案中,然后该嵌合基因可通过体外或体内重组插入在腺病毒基因组中。在一些实施方案中,插入病毒基因组的非必需区(例如,el或e3区)将得到活的并能够在感染的宿主中表达抗体分子的重组病毒(参见例如,logan&shenk,proc.natl.acad.sci.usa,1984,8(1):355-9)。在一些实施方案中,对于所插入的抗体编码序列的有效翻译也可能需要特定的起始信号。在一些实施方案中,这些信号包括atg起始密码子和相邻序列。在一些实施方案中,起始密码子必须与期望的编码序列的阅读框相同,以确保整个插入物的翻译。在一些实施方案中,这些外源翻译控制信号和起始密码子可以是天然和合成两者的多种来源。在一些实施方案中,可通过包含适当的转录增强子元件、转录终止子等来增强表达效率(参见例如,bittner等人,methods in enzymol.,1987,153:51-544)。
[0348]
在一些实施方案中,可选择调节所插入的序列的表达或以期望的特定方式修饰和加工基因产物的宿主细胞株。蛋白质产物的此类修饰(例如,糖基化,包括岩藻糖基化)和加工(例如,裂解)对于蛋白质的功能可能是重要的。不同的宿主细胞具有用于蛋白质和基因产物的翻译后加工和修饰的特征性和特异性机制。可选择适当的细胞系或宿主系统以确保对所表达的外来蛋白的正确修饰和加工。为此,可以使用具有用于基因产物的初级转录物的适当加工、糖基化和磷酸化的细胞机制的真核宿主细胞。此类哺乳动物宿主细胞包括但不限于cho、very、bhk、hela、cos、mdck、293、3t3、w138、bt483、hs578t、htb2、bt2o和t47d、ns0(不内源性地产生任何免疫球蛋白链的鼠骨髓瘤细胞系)、crl7o3o和hss78bst细胞。在一些实施方案中,本文提供的完全人单克隆抗体在哺乳动物细胞(诸如cho细胞)中产生。
[0349]
可使用本领域技术人员已知的标准技术来生成本文提供的抗体,其中重链在其asn-297-连接的n-低聚糖上不包含岩藻糖残基。在一些实施方案中,缺乏gmd酶的细胞(例如,cho lec13细胞)用于生成在重链上的asn-297-连接的n-低聚糖上不具有岩藻糖残基的抗体。在一些实施方案中,由突变的或灭活的fut8基因引起的α-1,6岩藻糖基转移酶活性降低的细胞(例如,大鼠杂交瘤yb2/0细胞系)用于生成在重链上的asn-297-连接的n-低聚糖上不具有岩藻糖残基的抗体。在一些实施方案中,β-1,4-甘露糖基-糖蛋白4-β-n-乙酰葡糖氨基转移酶(gnt-iii)过表达的细胞用于生成在重链上的asn-297-连接的n-低聚糖上不具有岩藻糖残基的抗体。在一些实施方案中,golgi gdp-岩藻糖转运蛋白(gft)基因slc35c1灭活的细胞(例如,cho-gmt3细胞)用于生成在重链上的asn-297-连接的n-低聚糖上不具有岩藻糖残基的抗体。在一些实施方案中,细菌rmd异源表达的细胞用于生成在重链上的asn-297-连接的n-低聚糖上不具有岩藻糖残基的抗体。在一些实施方案,岩藻糖基化的生物化学抑制剂(例如,岩藻糖类似物诸如2-氟岩藻糖和5-炔基岩藻糖)用于表达系统中以产生在重链上的asn-297-连接的n-低聚糖上不具有岩藻糖残基的抗体(pereira,n.a.等人,出处同上;shields,r.l.等人,出处同上;kanda y.,出处同上)。在一些实施方案,α1,3-岩藻糖基转移酶(fuct)和β1,2-木糖基转移酶(xylt)被破坏的植物细胞用于生成在重链上的asn-297-连接的n-低聚糖上不具有岩藻糖残基的抗体(pereira,n.a.等人,出处同上)。在一些实施方案,使用化学酶促重建来生成在重链上的asn-297-连接的n-低聚糖上不具有岩藻糖残基的抗体(pereira,n.a.等人,出处同上)。例如,外切糖苷酶诸如岩藻糖苷酶可用于去除在抗体的重链上的asn-297-连接的n-低聚糖上的岩藻糖(pereira,n.a.等人,出处同上)。
[0350]
对于重组蛋白的长期、高产率生产,可利用稳定表达。例如,可对稳定表达抗体分子的细胞系进行工程化。不使用含有病毒复制起点的表达载体,而是用由适当表达控制元件(例如,启动子、增强子、序列、转录终止子、聚腺苷酸化位点等)控制的dna和选择性标记物转化宿主细胞。外来dna引入之后,可允许工程化细胞在富集培养基中生长1-2天,然后转换到选择培养基。在一些实施方案中,重组质粒中的选择性标记物赋予选择抗性,并且允许细胞将质粒稳定整合到其染色体中并长成集落,继而可将其克隆和扩增成细胞系。该方法可有利地用于工程化表达抗体分子的细胞系。此类工程化细胞系可特别用于筛选和评估与抗体分子直接或间接相互作用的组合物。
[0351]
可使用许多选择系统,包括但不限于单纯疱疹病毒胸苷激酶(wigler等人,cell,1977,11:223)、次黄嘌呤鸟嘌呤磷酸核糖转移酶(szybalska&szybalski,proc.natl.acad.sci.usa,1992,48:202)和腺嘌呤磷酸核糖转移酶(lowy等人,cell,1980,22:8-17)基因可分别用于tk-、hgprt-或aprt-细胞。此外,抗代谢物抗性可用作以下基因的选择基础:dhfr,其赋予对甲氨蝶呤的抗性(wigler等人,natl.acad.sci.usa,1980,77:357o
′
hare等人,proc.natl.acad.sci.usa,1981,78:1527);gpt,其赋予对霉酚酸的抗性(mulligan&berg,proc.natl.acad.sci.usa,1981,78:2072);neo,其赋予对氨基糖苷g-418的抗性(wu和wu,biotherapy,1991,3:87-95;tolstoshev,ann.rev.pharmacol.toxicol.,1993,32:573-96;mulligan,science,1993,260:926-32;以及morgan和anderson,ann.rev.biochem.,1993,62:191-217);和hygro,其赋予对潮霉素的抗性(santerre等人,gene,1984,30:147)。重组dna技术领域中通常已知的方法可常规地应用于选择期望的重组克隆,并且此类方法描述于例如ausubel等人(编辑),current protocols in molecular biology,john wiley&sons,ny(1993);kriegler,gene transfer and expression,a laboratory manual,stockton press,ny(1990);以及第12章和第13章,dracopoli等人(编辑),current protocols in human genetics,john wiley&sons,ny(1994);colberre-garapin等人,j.mol.biol.,1981,150:1,这些文献全文以引用方式并入本文。
[0352]
抗体分子的表达水平可通过载体扩增来提高(综述参见bebbington和hentschel,the use of vectors based on gene amplification for the expression of cloned genes in mammalian cells in dna cloning,第3卷(academic press,new york,1987))。在一些实施方案中,表达抗体的载体系统中的标记物可扩增,并且宿主细胞的培养物中存在的抑制剂水平的增加将增加标记物基因的拷贝数和抗体的产生,因为扩增区域与抗体基因相关联(crouse等人,1983,mol.cell.biol.)3:257)。
[0353]
宿主细胞可与本文提供的两种表达载体:编码重链来源多肽的第一载体和编码轻链来源多肽的第二载体共转染。两种载体可含有相同的选择性标记物,其使得能够相等地表达重链和轻链多肽。另选地,可使用编码并能够表达重链和轻链多肽两者的单个载体。在此类情况下,轻链应放置在重链之前,以避免过量的无毒重链(proudfoot,nature,1986,322:52;以及kohler,proc.natl.acad.sci.usa,1980,77:2197-9)。重链和轻链的编码序列可包含cdna或基因组dna。
[0354]
一旦通过重组表达产生了本文提供的抗体分子,其就可通过本领域已知的用于纯化免疫球蛋白分子的任何方法,例如通过色谱法(例如,离子交换、亲和(特别是通过蛋白a后对特定抗原的亲和)和尺寸柱色谱法)、离心、差异溶解度或通过用于纯化蛋白质的任何
controlled release,第2卷,115-38(1984))。受控释放系统例如通过langer,出处同上论述。本领域技术人员已知的任何技术可用于产生包含一种或多种如本文所述的抗体的持续释放制剂(参见例如,美国专利4,526,938,pct公开wo 91/05548和wo 96/20698,ning等人,radiotherapy&oncology,1996,39:179-89;song等人,pda j.ofpharma.sci.&tech.,1995,50:372-97;cleek等人,pro.int’l.symp.control.rel.bioact.mater.,1997,24:853-4;以及lam等人,proc.int’l.symp.control rel.bioact.mater.,1997,24:759-60)。
[0362]
5.20使用、施用和投配的方法
[0363]
在一个方面,本文提供了一种增强抗体的adcc和/或cdc活性的方法。
[0364]
在一些实施方案中,本文提供的抗hla-g抗体、抗cd37抗体、抗gprc5d抗体、抗klk2抗体、抗psma抗体或抗bcsma抗体的adcc活性通过测量由效应细胞例如nk细胞、巨噬细胞、单核吞噬细胞、中性粒细胞或嗜酸性粒细胞介导的靶细胞死亡的百分比来确定。例如,内源性表达hla-g、cd37的靶细胞可装载有细胞标记试剂batda,该细胞标记试剂在细胞死亡时释放并且在形成荧光螯合物后可在细胞培养上清液中检测到。在此类情况下,将抗hla-g抗体或抗cd37抗体添加到batda标记的靶细胞中。可在50∶1的效应细胞与靶细胞比率(e∶t比率)下将培养过夜的效应细胞例如外周血单核细胞(pbmc)以5,000个细胞/孔添加到靶细胞中。在一些实施方案中,将效应细胞和靶细胞混合物在37℃下温育4小时。可将batda螯合物底物铕(iii)螯合物以1∶10的比率添加到混合物中。所释放的batda的量可通过测量在615nm处的发射荧光来确定。在一些实施方案中,使用含有与triton-x 100洗涤剂混合的batda标记的靶细胞的孔来确定100%靶细胞死亡的荧光信号。
[0365]
又如,将用nuclight red(essen bioscience)稳定转染的vcap细胞以每孔10,000个细胞接种在384孔板(perkin elmer viewplate)中的透明培养基(rpmi 1641 10%fbs,thermo fisher scientific)中,以允许细胞过夜粘附。可用刚解冻的pbmc(hemcare,pb009c-3)进行adcc测定。对于pbmc作为效应细胞而言,每孔效应细胞与靶细胞的比率可为34∶1。在一些实施方案中,测试最终浓度在100nm至0.01nm范围的klk2抗体。在将效应细胞和抗体添加到靶细胞之后,可在s3仪器(essen bioscience)下进行实时成像。可用软件定量每个孔的总红色积分信号。基于一式四份的值,可通过软件和prism(graphpad software)进行数据分析。在一些实施方案中,将细胞杀伤的百分比计算为:(1-klk2 mab/无mab对照)
×
100%。
[0366]
又如,将用gfp稳定转染的c42b和lncap细胞以每孔9,000个细胞接种在384孔板(perkin elmer viewplate)中的透明培养基(rpmi1641 10%fbs,thermo fisher scientific)中,以允许细胞过夜粘附。可通过robosep
tm
细胞分离仪器用刚解冻的pbmc(hemcare,pb009c-3)或从冷冻pbmc分离的nk细胞进行adcc测定。所分离的nk细胞可立即使用或用低剂量il-2(1ng/ml,miltenyi biotec)准备过夜。对于pbmc而言,每孔效应细胞与靶细胞的比率可为34∶1,对于所分离的nk细胞而言,每孔效应细胞与靶细胞的比率可为5∶1。在一些实施方案中,测试最终浓度在100nm至0.01nm范围的抗psma抗体。在将效应细胞和抗体添加到靶细胞之后,可在s3仪器(essen bioscience)下进行实时成像。可
用软件定量每个孔的总gfp积分信号。基于一式四份的值,可通过软件和prism(graphpad software)进行数据分析。可将细胞杀伤的百分比计算为:(1-psma mab/无mab对照)
×
100%。
[0367]
又如,将用gfp稳定转染的c42b和lncap细胞以每孔9,000个细胞接种在384孔板(perkin elmer viewplate)中的透明培养基(rpmi 1641 10%fbs,thermo fisher scientific)中,以允许细胞过夜粘附。可通过roboseptm细胞分离仪器用刚解冻的pbmc(hemcare,pb009c-3)或从冷冻pbmc分离的nk细胞进行adcc测定。所分离的nk细胞可立即使用或用低剂量il-2(1ng/ml,miltenyi biotec)准备过夜。对于pbmc而言,每孔效应细胞与靶细胞的比率可为34∶1,对于所分离的nk细胞而言,每孔效应细胞与靶细胞的比率可为5∶1。在一些实施方案中,测试最终浓度在100nm至0.01nm范围的抗bcma抗体。在将效应细胞和抗体添加到靶细胞之后,可在s3仪器(essen bioscience)下进行实时成像。可用软件定量每个孔的总gfp积分信号。基于一式四份的值,可通过软件和prism(graphpad software)进行数据分析。可将细胞杀伤的百分比计算为:(1-bcma mab/无mab对照)
×
100%。
[0368]
在一些实施方案中,本文提供的抗体经由adcc引起至少10%靶细胞死亡。在一些实施方案中,本文提供的抗体经由adcc引起至少20%靶细胞死亡。在一些实施方案中,本文提供的抗体经由adcc引起至少30%靶细胞死亡。在一些实施方案中,本文提供的抗体经由adcc引起至少40%靶细胞死亡。在一些实施方案中,本文提供的抗体经由adcc引起至少50%靶细胞死亡。在一些实施方案中,本文提供的抗体经由adcc引起至少60%靶细胞死亡。在一些实施方案中,本文提供的抗体经由adcc引起至少70%靶细胞死亡。在一些实施方案中,本文提供的抗体经由adcc引起至少80%靶细胞死亡。在一些实施方案中,本文提供的抗体经由adcc引起至少90%靶细胞死亡。在一些实施方案中,本文提供的抗体经由adcc引起至少95%靶细胞死亡。
[0369]
在一些实施方案中,本文提供的抗hla-g抗体、抗cd37抗体、抗gprc5d抗体、抗klk2抗体、抗psma抗体或抗bcsma抗体的cdc活性通过测量靶细胞死亡的百分比来确定。例如,可将内源性表达hla-g、cd37、gprc5d、klk2、psma或bcma的靶细胞在具有10%胎牛血清(fbs)的dmem培养基中培养。在一些实施方案中,将抗体添加到靶细胞中并在37℃下与幼兔血清一起温育30分钟,然后添加到靶细胞中至10%的最终浓度,以提供cdc的补体组分源。在一些实施方案中,将此类混合物在37℃下温育4小时。可将100μl celltiter-glo试剂(promega)添加到混合物中,然后在室温下温育10分钟。可通过用tecan spark读取器测量发光来确定靶细胞活力。因此,可将靶细胞死亡确定为100%与靶细胞活力之间的差异。
[0370]
在一些实施方案中,本文提供的抗体经由cdc引起至少10%靶细胞死亡。在一些实施方案中,本文提供的抗体经由cdc引起至少20%靶细胞死亡。在一些实施方案中,本文提供的抗体经由cdc引起至少30%靶细胞死亡。在一些实施方案中,本文提供的抗体经由cdc引起至少40%靶细胞死亡。在一些实施方案中,本文提供的抗体经由cdc引起至少50%靶细胞死亡。在一些实施方案中,本文提供的抗体经由cdc引起至少60%靶细胞死亡。在一些实施方案中,本文提供的抗体经由cdc引起至少70%靶细胞死亡。在一些实施方案中,本文提供的抗体经由cdc引起至少80%靶细胞死亡。在一些实施方案中,本文提供的抗体经由cdc
引起至少90%靶细胞死亡。在一些实施方案中,本文提供的抗体经由cdc引起至少95%靶细胞死亡。
[0371]
在一些实施方案中,本文提供的抗体增强了至少约2倍的adcc活性。在一些实施方案中,本文提供的抗体增强了至少约5倍的adcc活性。在一些实施方案中,本文提供的抗体增强了至少约10倍的adcc活性。在一些实施方案中,本文提供的抗体增强了至少约20倍的adcc活性。在一些实施方案中,本文提供的抗体增强了至少约30倍的adcc活性。在一些实施方案中,本文提供的抗体增强了至少约40倍的adcc活性。在一些实施方案中,本文提供的抗体增强了至少约50倍的adcc活性。在一些实施方案中,本文提供的抗体增强了至少约60倍的adcc活性。在一些实施方案中,本文提供的抗体增强了至少约70倍的adcc活性。在一些实施方案中,本文提供的抗体增强了至少约80倍的adcc活性。在一些实施方案中,本文提供的抗体增强了至少约90倍的adcc活性。在一些实施方案中,本文提供的抗体增强了至少约100倍的adcc活性。在一些实施方案中,本文提供的抗体增强了至少约200倍的adcc活性。在一些实施方案中,本文提供的抗体增强了至少约500倍的adcc活性。
[0372]
在一些实施方案中,本文提供的抗体增强了至少约2倍的cdc活性。在一些实施方案中,本文提供的抗体增强了至少约5倍的cdc活性。在一些实施方案中,本文提供的抗体增强了至少约10倍的cdc活性。在一些实施方案中,本文提供的抗体增强了至少约20倍的cdc活性。在一些实施方案中,本文提供的抗体增强了至少约30倍的cdc活性。在一些实施方案中,本文提供的抗体增强了至少约40倍的cdc活性。在一些实施方案中,本文提供的抗体增强了至少约50倍的cdc活性。在一些实施方案中,本文提供的抗体增强了至少约60倍的cdc活性。在一些实施方案中,本文提供的抗体增强了至少约70倍的cdc活性。在一些实施方案中,本文提供的抗体增强了至少约80倍的cdc活性。在一些实施方案中,本文提供的抗体增强了至少约90倍的cdc活性。在一些实施方案中,本文提供的抗体增强了至少约100倍的cdc活性。在一些实施方案中,本文提供的抗体增强了至少约200倍的cdc活性。在一些实施方案中,本文提供的抗体增强了至少约500倍的cdc活性。
[0373]
在一些实施方案中,本文提供的抗体增强了至少约2倍的adcc和cdc活性两者。在一些实施方案中,本文提供的抗体增强了至少约5倍的adcc和cdc活性两者。在一些实施方案中,本文提供的抗体增强了至少约10倍的adcc和cdc活性两者。在一些实施方案中,本文提供的抗体增强了至少约20倍的adcc和cdc活性两者。在一些实施方案中,本文提供的抗体增强了至少约30倍的adcc和cdc活性两者。在一些实施方案中,本文提供的抗体增强了至少约40倍的adcc和cdc活性两者。在一些实施方案中,本文提供的抗体增强了至少约50倍的adcc和cdc活性两者。在一些实施方案中,本文提供的抗体增强了至少约60倍的adcc和cdc活性两者。在一些实施方案中,本文提供的抗体增强了至少约70倍的adcc和cdc活性两者。在一些实施方案中,本文提供的抗体增强了至少约80倍的adcc和cdc活性两者。在一些实施方案中,本文提供的抗体增强了至少约90倍的adcc和cdc活性两者。在一些实施方案中,本文提供的抗体增强了至少约100倍的adcc和cdc活性两者。在一些实施方案中,本文提供的抗体增强了至少约200倍的adcc和cdc活性两者。在一些实施方案中,本文提供的抗体增强了至少约500倍的adcc和cdc活性两者。
[0374]
在另一方面,本文提供了一种治疗受试者的疾病或障碍的方法,该方法包括向受试者施用有效量的本文提供的抗体。在一个实施方案中,疾病或障碍为hla-g介导的疾病或
障碍。在一个实施方案中,疾病或障碍为cd37介导的疾病或障碍。在一个实施方案中,疾病或障碍为gprc5d介导的疾病或障碍。在一个实施方案中,疾病或障碍为klk2介导的疾病或障碍。在一个实施方案中,疾病或障碍为psma介导的疾病或障碍。在一个实施方案中,疾病或障碍为bcma介导的疾病或障碍。在一些实施方案中,疾病或障碍选自:影响关节、皮肤、肾脏、肝脏、肠、心脏、肺、肌肉、胃、脾、胰腺、胆囊、膀胱、阑尾、胸腺、大脑、食道、眼或耳的癌症、自体免疫疾病、炎性疾病、心血管疾病、遗传疾病、血液病和/或肺病,其中疾病或障碍任选地选自:类风湿性关节炎、大疱性类天疱疮、盘状皮肤狼疮、荨麻疹性血管炎、亨-舍二氏紫癜、iga肾病、特应性皮炎(特应性湿疹)、牛皮癣(寻常型银屑病)、皮脂溢性湿疹、哮喘、蛋白尿肾脏疾病、肝脏疾病、狼疮性肾炎、多肌炎、皮肌炎、钙调神经蛋白抑制剂引起的肾毒性、肌强直性营养不良、心功能障碍和衰竭、alport综合征、溃疡性结肠炎、克隆氏病、皮肤血管炎、恶病质和炎症性肠病,并且其中任选地疾病或障碍与纤维化相关并任选地选自组织纤维化、特发性肺间质纤维化、间质性肺疾病、硬皮病(系统性硬化病)、癌症、癌症相关恶病质、肌肉萎缩、瘢痕瘤、包涵体肌炎和组织重建(参见例如,heider,k.h.等人,blood,2011,118(15):4159-68;carosella,e.d.等人,adv.immunol.,2015,127:33-144;stathis,s.等人,invest new drugs,2018,36(5):869-76;stilgenbauer,s.等人,leukemia,2019,33:2531-5;gomes,r.g.等人,hum.immunol.,2018,79(6):477-84;moroso,v.等人,transplantation,2015,99(12):2514-22;lazarte,j.等人,hum.immunol.,2018,79(8):587-93;rached,m.r.等人,eur j obstet gynecol reprod biol.,2019,235:36-41;koc,a.等人,adv clin exp med.,2018,27(9):1233-7;ribeyre,c.等人,front immunol.,2018,9:278;smith,e.l.等人,sci transl med.,2019,11(485):eaau7746;kodama,t.等人,mol cancer ther.,2019,18(9):1555-64;cohen,y.等人,hematology,2013,18(6):348-51)。
[0375]
本文还提供了一种治疗疾病或障碍的方法,其中将一种或多种治疗剂与本文提供的抗体组合施用给受试者。
[0376]
在另一方面,本文提供了本文提供的抗体在制造用于治疗受试者的疾病或障碍的药物中的用途。
[0377]
在另一方面,本文提供了本文提供的药物组合物在制造用于治疗受试者的疾病或障碍的药物中的用途。
[0378]
在一个具体的实施方案中,本文提供了一种用于预防和/或治疗疾病或病症的包含本文提供的抗体的组合物。在一个实施方案中,本文提供了一种用于预防疾病或病症的组合物,其中组合物包含本文提供的抗体。在一个实施方案中,本文提供了一种用于治疗疾病或病症的组合物,其中组合物包含本文提供的抗体。在一些实施方案中,疾病或病症为hla-g介导的疾病。在一些实施方案中,疾病或病症为cd37介导的疾病。在一些实施方案中,疾病或病症为gprc5d介导的疾病。在一些实施方案中,疾病或病症为klk2介导的疾病。在一个实施方案中,疾病或病症为psma介导的疾病。在一个实施方案中,疾病或病症为bcma介导的疾病。在一些实施方案中,疾病或障碍选自:影响关节、皮肤、肾脏、肝脏、肠、心脏、肺、肌肉、胃、脾、胰腺、胆囊、膀胱、阑尾、胸腺、大脑、食道、眼或耳的癌症、自体免疫疾病、炎性疾病、心血管疾病、遗传疾病、血液病和/或肺病,其中疾病或障碍任选地选自:类风湿性关节炎、大疱性类天疱疮、盘状皮肤狼疮、荨麻疹性血管炎、亨-舍二氏紫癜、iga肾病、特应性皮
炎(特应性湿疹)、牛皮癣(寻常型银屑病)、皮脂溢性湿疹、哮喘、蛋白尿肾脏疾病、肝脏疾病、狼疮性肾炎、多肌炎、皮肌炎、钙调神经蛋白抑制剂引起的肾毒性、肌强直性营养不良、心功能障碍和衰竭、alport综合征、溃疡性结肠炎、克隆氏病、皮肤血管炎、恶病质和炎症性肠病,并且其中任选地疾病或障碍与纤维化相关并任选地选自组织纤维化、特发性肺间质纤维化、间质性肺疾病、硬皮病(系统性硬化病)、癌症、癌症相关恶病质、肌肉萎缩、瘢痕瘤、包涵体肌炎和组织重建。
[0379]
在某些实施方案中,受试者是对其有需要的受试者。在一些实施方案中,受试者患有疾病或病症。在其他实施方案中,受试者具有罹患疾病或病症的风险。在一些实施方案中,施用导致疾病或病症的预防、管理、治疗或改善。
[0380]
在一个实施方案中,本文提供了一种用于预防和/或治疗疾病或病症的症状的组合物,其中组合物包含本文提供的抗体。在一个实施方案中,本文提供了一种用于预防疾病或病症的症状的组合物,其中组合物包含本文提供的抗体。在一个实施方案中,本文提供了一种用于治疗疾病或病症的症状的组合物,其中组合物包含本文提供的抗体。在一些实施方案中,疾病或病症是hla-g介导的疾病、cd37介导的疾病、gprc5d介导的疾病、klk2介导的疾病、psma介导的疾病和/或bcma介导的疾病。在一些实施方案中,疾病或障碍选自:影响关节、皮肤、肾脏、肝脏、肠、心脏、肺、肌肉、胃、脾、胰腺、胆囊、膀胱、阑尾、胸腺、大脑、食道、眼或耳的癌症、自体免疫疾病、炎性疾病、心血管疾病、遗传疾病、血液病和/或肺病,其中疾病或障碍任选地选自:类风湿性关节炎、大疱性类天疱疮、盘状皮肤狼疮、荨麻疹性血管炎、亨-舍二氏紫癜、iga肾病、特应性皮炎(特应性湿疹)、牛皮癣(寻常型银屑病)、皮脂溢性湿疹、哮喘、蛋白尿肾脏疾病、肝脏疾病、狼疮性肾炎、多肌炎、皮肌炎、钙调神经蛋白抑制剂引起的肾毒性、肌强直性营养不良、心功能障碍和衰竭、alport综合征、溃疡性结肠炎、克隆氏病、皮肤血管炎、恶病质和炎症性肠病,并且其中任选地疾病或障碍与纤维化相关并任选地选自组织纤维化、特发性肺间质纤维化、间质性肺疾病、硬皮病(系统性硬化病)、癌症、癌症相关恶病质、肌肉萎缩、瘢痕瘤、包涵体肌炎和组织重建。
[0381]
在某些实施方案中,受试者是对其有需要的受试者。在一些实施方案中,受试者患有疾病或病症。在其他实施方案中,受试者具有罹患疾病或病症的风险。在一些实施方案中,施用导致疾病或病症的症状的预防或治疗。
[0382]
在另一个实施方案中,本文提供了一种预防和/或治疗受试者的疾病或病症的方法,该方法包括施用有效量的本文提供的抗体。在一个实施方案中,本文提供了一种预防受试者的疾病或病症的方法,该方法包括施用有效量的本文提供的抗体。在一个实施方案中,本文提供了一种治疗受试者的疾病或病症的方法,该方法包括施用有效量的本文提供的抗体。在一些实施方案中,疾病或病症是hla-g介导的疾病、cd37介导的疾病、gprc5d介导的疾病、klk2介导的疾病、psma介导的疾病和/或bcma介导的疾病。在一些实施方案中,疾病或障碍选自:影响关节、皮肤、肾脏、肝脏、肠、心脏、肺、肌肉、胃、脾、胰腺、胆囊、膀胱、阑尾、胸腺、大脑、食道、眼或耳的癌症、自体免疫疾病、炎性疾病、心血管疾病、遗传疾病、血液病和/或肺病,其中疾病或障碍任选地选自:类风湿性关节炎、大疱性类天疱疮、盘状皮肤狼疮、荨麻疹性血管炎、亨-舍二氏紫癜、iga肾病、特应性皮炎(特应性湿疹)、牛皮癣(寻常型银屑病)、皮脂溢性湿疹、哮喘、蛋白尿肾脏疾病、肝脏疾病、狼疮性肾炎、多肌炎、皮肌炎、钙调神经蛋白抑制剂引起的肾毒性、肌强直性营养不良、心功能障碍和衰竭、alport综合征、溃疡
性结肠炎、克隆氏病、皮肤血管炎、恶病质和炎症性肠病,并且其中任选地疾病或障碍与纤维化相关并任选地选自组织纤维化、特发性肺间质纤维化、间质性肺疾病、硬皮病(系统性硬化病)、癌症、癌症相关恶病质、肌肉萎缩、瘢痕瘤、包涵体肌炎和组织重建。
[0383]
在某些实施方案中,受试者是对其有需要的受试者。在一些实施方案中,受试者患有疾病或病症。在其他实施方案中,受试者具有罹患疾病或病症的风险。在一些实施方案中,施用导致疾病或病症的预防或治疗。
[0384]
在另一个实施方案中,本文提供了一种预防和/或治疗受试者的疾病或病症的症状的方法,该方法包括施用有效量的本文提供的抗体。在一个实施方案中,本文提供了一种预防受试者的疾病或病症的症状的方法,该方法包括施用有效量的本文提供的抗体。在一个实施方案中,本文提供了一种治疗受试者的疾病或病症的症状的方法,该方法包括施用有效量的本文提供的抗体。在一些实施方案中,疾病或病症是hla-g介导的疾病、cd37介导的疾病、gprc5d介导的疾病、klk-2介导的疾病、psma介导的疾病和/或bcma介导的疾病。在一些实施方案中,疾病或障碍选自:影响关节、皮肤、肾脏、肝脏、肠、心脏、肺、肌肉、胃、脾、胰腺、胆囊、膀胱、阑尾、胸腺、大脑、食道、眼或耳的癌症、自体免疫疾病、炎性疾病、心血管疾病、遗传疾病、血液病和/或肺病,其中疾病或障碍任选地选自:类风湿性关节炎、大疱性类天疱疮、盘状皮肤狼疮、荨麻疹性血管炎、亨-舍二氏紫癜、iga肾病、特应性皮炎(特应性湿疹)、牛皮癣(寻常型银屑病)、皮脂溢性湿疹、哮喘、蛋白尿肾脏疾病、肝脏疾病、狼疮性肾炎、多肌炎、皮肌炎、钙调神经蛋白抑制剂引起的肾毒性、肌强直性营养不良、心功能障碍和衰竭、alport综合征、溃疡性结肠炎、克隆氏病、皮肤血管炎、恶病质和炎症性肠病,并且其中任选地疾病或障碍与纤维化相关并任选地选自组织纤维化、特发性肺间质纤维化、间质性肺疾病、硬皮病(系统性硬化病)、癌症、癌症相关恶病质、肌肉萎缩、瘢痕瘤、包涵体肌炎和组织重建。
[0385]
在某些实施方案中,受试者是对其有需要的受试者。在一些实施方案中,受试者患有疾病或病症。在其他实施方案中,受试者具有罹患疾病或病症的风险。在一些实施方案中,施用导致疾病或病症的症状的预防或治疗。
[0386]
本文还提供了通过向受试者施用有效量的本文提供的抗体或包含本文提供的抗体的药物组合物来预防和/或治疗疾病或病症的方法。在一个方面,抗体是基本上纯化的(即,基本上不合限制其效果或产生不期望的副作用的物质)。施用疗法的受试者可以是哺乳动物,诸如非灵长类动物(例如,牛、猪、马、猫、狗、大鼠等)或灵长类动物(例如,猴(诸如食蟹猕猴)或人)。在一个实施方案中,受试者是人。在另一个实施方案中,受试者是患有疾病或病症的人。
[0387]
各种递送系统是已知的并且可用于施用预防性或治疗性药剂(例如,本文提供的抗体),包括但不限于包封在脂质体、微粒、微胶囊、能够表达抗体/受体介导的胞吞的重组细胞中(参见例如,wu和wu,j.biol.chem.,1987 262:4429-4432)、核酸作为逆转录病毒或其他载体的一部分的构建等。施用预防性或治疗性药剂(例如,本文提供的抗体)或药物组合物的方法包括但不限于肠胃外施用(例如,皮内、肌内、腹膜内、静脉内和皮下)、硬膜外施用和粘膜施用(例如,鼻内和口服途径)。在一个具体的实施方案中,预防性或治疗性药剂(例如,本文提供的抗体)或药物组合物经鼻内、肌内、静脉内或皮下施用。预防性或治疗性药剂或组合物可通过任何便利的途径施用,例如通过输注或推注、通过上皮层或粘膜层(例
of pharmaceutical sci&technol.,1995,50:372-97;cleek等人,pro.int’l.symp.control.rel.bioact.mater.,1997,24:853-54;以及lam等人,proc.int’l.symp.control rel.bioact.mater.,1997,24:759-60,这些文献中的每一篇全文均以引用方式并入本文。
[0391]
在一个具体的实施方案中,在本文提供的组合物是编码预防性或治疗性药剂(例如,本文提供的抗体)的核酸的情况下,核酸可通过以下方式在体内施用以促进其编码的预防性或治疗性药剂的表达:例如,通过使用逆转录病毒载体(参见美国专利4,980,286)或通过直接注射或通过使用微粒轰击(例如,基因枪;biolistic,dupont)将核酸构建为适当核酸表达载体的一部分并且施用以使其变成细胞内的,或通过用脂质或细胞表面受体或转染剂涂覆,或通过将核酸与已知进入细胞核的同源框样肽连接施用(参见例如,joliot等人,proc.natl.acad.sci.usa,1991,88:1864-8)等。另选地,核酸可在细胞内引入并且并入宿主细胞dna内以通过同源重组而表达。
[0392]
在一个具体的实施方案中,本文提供的组合物包含本文提供的一种、两种或更多种抗体。在另一个实施方案中,本文提供的组合物包含本文提供的一种、两种或更多种抗体以及除本文提供的抗体之外的预防性或治疗性药剂。在一个实施方案中,已知预防性或治疗性药剂可用于或已经用于或目前用于预防、管理、治疗和/或改善疾病或病症。除了预防性或治疗性药剂之外,本文提供的组合物还可包含赋形剂。
[0393]
本文提供的组合物包括可用于制备单位剂型的可用于制造药物组合物(例如,适于施用给受试者或患者的组合物)的原料药物组合物。在一个实施方案中,本文提供的组合物是药物组合物。此类组合物包含预防或治疗有效量的一种或多种预防性或治疗性药剂(例如,本文提供的抗体或其他预防性或治疗性药剂)和药学上可接受的赋形剂。药物组合物可被配制成适于向受试者施用的途径。
[0394]
在一个具体的实施方案中,术语
″
赋形剂
″
还可指稀释剂、佐剂(例如,弗氏佐剂(完全或不完全))或媒介物。药物赋形剂可以是无菌的液体,诸如水和油,包括那些衍生自石油、动物、植物的油或合成的油,诸如花生油、大豆油、矿物油、芝麻油等。当静脉内施用药物组合物时,水是示例性赋形剂。盐水溶液和右旋糖水溶液以及甘油溶液也可用作液体赋形剂,尤其是用于注射溶液。合适的药物赋形剂包括但不限于淀粉、葡萄糖、乳糖、蔗糖、明胶、麦芽、大米、面粉、白垩、硅胶、硬脂酸钠、单硬脂酸甘油酯、滑石、氯化钠、脱脂奶粉、甘油、丙烯、二醇、水、乙醇等。如果需要,组合物还可含有少量润湿剂或乳化剂或ph缓冲剂。这些组合物可采用溶液、悬浮液、乳液、片剂、丸剂、胶囊、粉末、缓释制剂等形式。口服制剂可包含标准赋形剂,诸如药物级甘露醇、乳糖、淀粉、硬脂酸镁、糖精钠、纤维素、碳酸镁等。合适的药物赋形剂的示例描述于remington
′
s pharmaceutical sciences(1990)mack publishing co.,easton,pa中。此类组合物将含有预防或治疗有效量的本文提供的抗体,诸如纯化形式,以及合适量的赋形剂以便提供用于适当施用于患者的形式。制剂应与施用方式相适应。
[0395]
在一个实施方案中,根据常规程序将组合物配制为适于向人类静脉内施用的药物组合物。在一些实施方案中,用于静脉内施用的组合物是无菌等渗缓冲水溶液。在必要时,组合物还可包含增溶剂和局部麻醉剂诸如利多卡因,以减轻注射部位处的疼痛。然而,此类组合物可通过除静脉内施用之外的途径施用。
[0396]
本文提供的组合物的成分可在指示活性剂的量的气密密封容器诸如安瓿或小袋
中单独提供或以单位剂型混合在一起,例如,作为干燥冻干粉末或无水浓缩物。在组合物通过输注施用的情况下,可使用含有无菌药物级水或盐水的输注瓶来分配组合物。在组合物通过注射施用的情况下,可提供无菌注射用水或盐水的安瓿,使得可在施用之前混合成分。
[0397]
本文提供的抗体可包装在指示抗体的量的气密密封容器诸如安瓿或小袋中。在一个实施方案中,抗体作为干燥灭菌的冻干粉末或无水浓缩物在气密密封容器中提供并且可例如用水或盐水重构至适当浓度以施用于受试者。冻干抗体可在其原始容器中储存在2℃至8℃之间,并且抗体可在重构后12小时内,诸如在6小时内、5小时内、3小时内或1小时内施用。在另选的实施方案中,本文提供的抗体在指示抗体的量和浓度的气密密封容器中以液体形式提供。
[0398]
本文提供的组合物可被配制为中性或盐形式。药学上可接受的盐包括但不限于由阴离子形成的那些,诸如衍生自盐酸、磷酸、乙酸、草酸、酒石酸等的那些;以及由阳离子形成的那些,诸如衍生自钠、钾、铵、钙、氢氧化铁、异丙胺、三乙胺、2-乙氨基乙醇、组氨酸、普鲁卡因等的那些。
[0399]
有效预防和/或治疗疾病或病症的预防性或治疗性药剂(例如,本文提供的抗体)或本文提供的组合物的量可通过标准临床技术确定。此外,可任选地采用体外测定来帮助确定最佳剂量范围。在一些实施方案中,在制剂中待采用的精确剂量也将取决于施用途径以及疾病或病症的严重程度,并且应该根据医生的判断和每个患者的情况来决定。
[0400]
有效剂量可通过源自体外或动物模型测试体系的剂量响应曲线来推导。
[0401]
在某些实施方案中,向患者施用一定剂量的本文提供的抗体的途径是鼻内、肌内、静脉内、皮下或它们的组合,但是本文所述的其他途径也是可接受的。每个剂量可以或可以不通过相同的施用途径施用。在一些实施方案中,本文提供的抗体可经由多种施用途径同时或随后施用至本文提供的相同或不同抗体的其他剂量。
[0402]
在某些实施方案中,本文提供的抗体预防性或治疗性地施用于受试者。本文提供的抗体可预防性或治疗性地施用于受试者,以便防止、减轻或改善疾病或其症状。
[0403]
为了简洁起见,本文使用某些缩写。一个示例是表示氨基酸残基的单字母缩写。氨基酸及其对应的三字母和单字母缩写如下:
[0404]
丙氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
ala
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(a)
[0405]
精氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
arg
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(r)
[0406]
天冬酰胺
ꢀꢀꢀꢀꢀꢀꢀ
asn
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(n)
[0407]
天冬氨酸
ꢀꢀꢀꢀꢀꢀꢀ
asp
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(d)
[0408]
半胱氨酸
ꢀꢀꢀꢀꢀꢀꢀ
cys
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(c)
[0409]
谷氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
glu
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(e)
[0410]
谷氨酰胺
ꢀꢀꢀꢀꢀꢀꢀ
gln
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(q)
[0411]
甘氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
gly
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(g)
[0412]
组氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
his
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(h)
[0413]
异亮氨酸
ꢀꢀꢀꢀꢀꢀꢀ
ile
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ(i)[0414]
亮氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
leu
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(l)
[0415]
赖氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
lys
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(k)
[0416]
甲硫氨酸
ꢀꢀꢀꢀꢀꢀꢀ
met
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(m)
[0417]
苯丙氨酸
ꢀꢀꢀꢀꢀꢀꢀ
phe
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(f)
[0418]
脯氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
pro
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(p)
[0419]
丝氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
ser
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(s)
[0420]
苏氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
thr
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(t)
[0421]
色氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
trp
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(w)
[0422]
酪氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
tyr
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(y)
[0423]
缬氨酸
ꢀꢀꢀꢀꢀꢀꢀꢀꢀ
val
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(v)
[0424]
本文使用肯定语言来描述多个实施方案而总体上公开本发明。本发明还具体地包括其中完全或部分排除特定主题诸如物质或材料、方法步骤和条件、方案、程序、测定或分析的实施方案。因此,即使本发明通常不是按照本发明不包括的内容来表达的,但本文仍然公开了未明确包括在本发明中的方面。
[0425]
已描述了本发明的多个实施方案。然而,应当理解,在不脱离本发明的精神和范围的情况下,可进行各种修改。因此,以下实施例旨在说明而非限制权利要求书中描述的发明的范围。
[0426]
6.实施方案
[0427]
本发明提供了以下非限制性实施方案。
[0428]
在一组实施方案(a组实施方案)中,提供了:
[0429]
a1.一种抗体群体,
[0430]
(i)其中少于80%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基;并且
[0431]
(ii)其中抗体群体包括fc区包含k338a和t437r突变或k248e和t437r突变(re突变)的抗体,
[0432]
其中氨基酸残基编号根据eu编号系统,并且其中抗体群体中任选的每种抗体包含re突变。
[0433]
a2.根据实施方案a1所述的抗体群体,其中少于70%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0434]
a3.根据实施方案a1所述的抗体群体,其中少于60%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0435]
a4.根据实施方案a1所述的抗体群体,其中少于50%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0436]
a5.根据实施方案a1所述的抗体群体,其中少于40%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0437]
a6.根据实施方案a1所述的抗体群体,其中少于30%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0438]
a7.根据实施方案a1所述的抗体群体,其中少于20%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0439]
a8.根据实施方案a1所述的抗体群体,其中少于10%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0440]
a9.根据实施方案a1至a8中任一项所述的抗体群体,其中通过在宿主细胞中表达
编码抗体或其片段的多核苷酸来产生抗体,该宿主细胞不足以将岩藻糖添加到连接至抗体的低聚糖。
[0441]
a10.根据实施方案a9所述的抗体群体,其中宿主细胞具有降低的gdp-甘露糖4,6-脱水酶(gmd)活性或降低的α-1,6岩藻糖基转移酶活性。
[0442]
a11.根据实施方案a1至a10中任一项所述的抗体群体,其中抗体群体具有增强的抗体依赖性细胞毒性(adcc)和增强的补体依赖性细胞毒性(cdc)两者。
[0443]
a12.根据实施方案a1至a11中任一项所述的抗体群体,其中抗体是igg1。
[0444]
a13.根据实施方案a1至a12中任一项所述的抗体群体,其中抗体与hla-g结合,其中抗体任选地如以上第5.5部分中所述。
[0445]
a14.根据实施方案a13所述的抗体群体,其中与hla-g结合的抗体包含seq id no:180的轻链核苷酸序列和seq id no:182的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变),或包含seq id no:181的轻链核苷酸序列和seq id no:183的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变)。
[0446]
a15.根据实施方案a1至a12中任一项所述的抗体群体,其中抗体与cd37结合,其中抗体任选地如以上第5.6部分中所述。
[0447]
a16.根据实施方案a15所述的抗体群体,其中与cd37结合的抗体包含seq id no:69的轻链核苷酸序列和seq id no:85的重链核苷酸序列、seq id no:70的轻链核苷酸序列和seq id no:86的重链核苷酸序列、seq id no:71的轻链核苷酸序列和seq id no:87的重链核苷酸序列、seq id no:72的轻链核苷酸序列和seq id no:88的重链核苷酸序列、seq id no:73的轻链核苷酸序列和seq id no:89的重链核苷酸序列、seq id no:74的轻链核苷酸序列和seq id no:90的重链核苷酸序列、seq id no:75的轻链核苷酸序列和seq id no:91的重链核苷酸序列或seq id no:76的轻链核苷酸序列和seq id no:92的重链核苷酸序列。
[0448]
a17.根据实施方案a1至a12中任一项所述的抗体群体,其中抗体与gprc5d结合,其中抗体任选地如以上第5.7部分中所述。
[0449]
a18.根据实施方案a17所述的抗体群体,其中与gprc5d结合的抗体包含seq id no:104的轻链核苷酸序列和seq id no:106的重链核苷酸序列。
[0450]
a19.根据实施方案a1至a12中任一项所述的抗体群体,其中抗体与klk2结合,其中抗体任选地如以上第5.8部分中所述。
[0451]
a20.根据实施方案a19所述的抗体群体,其中与klk2结合的抗体包含seq id no:161的轻链核苷酸序列和seq id no:160的重链核苷酸序列、seq id no:161的轻链核苷酸序列和seq id no:162的重链核苷酸序列或seq id no:161的轻链核苷酸序列和seq id no:163的重链核苷酸序列。
[0452]
a21.根据实施方案a1至a12中任一项所述的抗体群体,其中抗体与psma结合,其中抗体任选地如以上第5.9部分中所述。
[0453]
a22.根据实施方案a21所述的抗体群体,其中与psma结合的抗体包含seq id no:241的轻链核苷酸序列和seq id no:242的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变),或包含seq id no:241的轻链核苷酸序列和seq id no:243的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变)。
[0454]
a23.根据实施方案a1至a12中任一项所述的抗体群体,其中抗体与bcma结合,其中抗体任选地如以上第5.10部分中所述。
[0455]
a24.一种抗体群体,
[0456]
(i)其中少于80%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基;并且
[0457]
(ii)其中抗体群体包括在其fc区中具有一个或多个突变以用于增加抗体的cdc活性的抗体。
[0458]
a25.一种抗体群体,该抗体群体包括用于增加抗体的adcc活性的第一构件和用于增加抗体的cdc活性的第二构件。
[0459]
在另一组实施方案(b组实施方案)中,提供了:
[0460]
b1.一种药物组合物,所述药物组合物包含:
[0461]
(a)抗体群体,
[0462]
(i)其中少于80%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基;并且
[0463]
(ii)其中抗体群体包括fc区包含k338a和t437r突变或k248e和t437r突变(re突变)的抗体,
[0464]
其中氨基酸残基编号根据eu编号系统,和
[0465]
(b)药学上可接受的赋形剂。
[0466]
b2.根据实施方案b1所述的药物组合物,其中少于70%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0467]
b3.根据实施方案b1所述的药物组合物,其中少于60%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0468]
b4.根据实施方案b1所述的药物组合物,其中少于50%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0469]
b5.根据实施方案b1所述的药物组合物,其中少于40%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0470]
b6.根据实施方案b1所述的药物组合物,其中少于30%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0471]
b7.根据实施方案b1所述的药物组合物,其中少于20%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0472]
b8.根据实施方案b1所述的药物组合物,其中少于10%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0473]
b9.根据实施方案b1至b8中任一项所述的药物组合物,其中通过在宿主细胞中表达编码抗体或其片段的多核苷酸来产生抗体,该宿主细胞不足以将岩藻糖添加到连接至抗体的低聚糖。
[0474]
b10.根据实施方案b9所述的药物组合物,其中宿主细胞具有降低的gdp-甘露糖4,6-脱水酶(gmd)活性或降低的α-1,6岩藻糖基转移酶活性。
[0475]
b11.根据实施方案b1至b10中任一项所述的药物组合物,其中抗体群体具有增强的抗体依赖性细胞毒性(adcc)和增强的补体依赖性细胞毒性(cdc)两者。
[0476]
b12.根据实施方案b1至b11中任一项所述的药物组合物,其中抗体是igg1。
[0477]
b13.根据实施方案b1至b12中任一项所述的药物组合物,其中抗体与hla-g结合,其中抗体任选地如以上第5.5部分中所述。
[0478]
b14.根据实施方案b13所述的药物组合物,其中与hla-g结合的抗体包含seq id no:180的轻链核苷酸序列和seq id no:182的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变),或包含seq id no:181的轻链核苷酸序列和seq id no:183的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变)。
[0479]
b15.根据实施方案b1至b12中任一项所述的药物组合物,其中抗体与cd37结合,其中抗体任选地如以上第5.6部分中所述。
[0480]
b16.根据实施方案b15所述的药物组合物,其中与cd37结合的抗体包含seq id no:69的轻链核苷酸序列和seq id no:85的重链核苷酸序列、seq id no:70的轻链核苷酸序列和seq id no:86的重链核苷酸序列、seq id no:71的轻链核苷酸序列和seq id no:87的重链核苷酸序列、seq id no:72的轻链核苷酸序列和seq id no:88的重链核苷酸序列、seq id no:73的轻链核苷酸序列和seq id no:89的重链核苷酸序列、seq id no:74的轻链核苷酸序列和seq id no:90的重链核苷酸序列、seq id no:75的轻链核苷酸序列和seq id no:91的重链核苷酸序列或seq id no:76的轻链核苷酸序列和seq id no:92的重链核苷酸序列。
[0481]
b17.根据实施方案b1至b12中任一项所述的药物组合物,其中抗体与gprc5d结合,其中抗体任选地如以上第5.7部分中所述。
[0482]
b18.根据实施方案b17所述的药物组合物,其中与gprc5d结合的抗体包含seq id no:104的轻链核苷酸序列和seq id no:106的重链核苷酸序列。
[0483]
b19.根据实施方案b1至b12中任一项所述的药物组合物,其中抗体与klk2结合,其中抗体任选地如以上第5.8部分中所述。
[0484]
b20.根据实施方案b19所述的药物组合物,其中与klk2结合的抗体包含seq id no:161的轻链核苷酸序列和seq id no:160的重链核苷酸序列、seq id no:161的轻链核苷酸序列和seq id no:162的重链核苷酸序列或seq id no:161的轻链核苷酸序列和seq id no:163的重链核苷酸序列。
[0485]
b21.根据实施方案b1至b12中任一项所述的药物组合物,其中抗体与psma结合,其中抗体任选地如以上第5.9部分中所述。
[0486]
b22.根据实施方案b21所述的药物组合物,其中与psma结合的抗体包含seq id no:241的轻链核苷酸序列和seq id no:242的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变),或包含seq id no:241的轻链核苷酸序列和seq id no:243的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变)。
[0487]
b23.根据实施方案b1至b12中任一项所述的药物组合物,其中抗体与bcma结合,其中抗体任选地如以上第5.10部分中所述。
[0488]
b24.一种药物组合物,所述药物组合物包含:
[0489]
(a)抗体群体,
[0490]
(i)其中少于80%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基;并且
[0491]
(ii)其中抗体群体包括在其fc区中具有一个或多个突变以用于增加抗体的cdc活性的抗体,和
[0492]
(b)药学上可接受的赋形剂。
[0493]
b25.一种药物组合物,所述药物组合物包含:
[0494]
(a)抗体群体,该抗体群体包括用于增加抗体的adcc活性的第一构件和用于增加抗体的cdc活性的第二构件;和
[0495]
(b)药学上可接受的赋形剂。
[0496]
在另一组实施方案(c组实施方案)中,提供了:
[0497]
c1.一种制备抗体群体的方法,该方法包括在宿主细胞中表达编码抗体或其片段的多核苷酸,该宿主细胞不足以将岩藻糖残基添加到经由n297残基连接至抗体的低聚糖,其中抗体群体包括fc区包含k338a和t437r突变或k248e和t437r突变(re突变)的抗体。
[0498]
c2.根据实施方案c1所述的方法,其中宿主细胞具有降低的α-1,6岩藻糖基转移酶活性。
[0499]
c3.根据实施方案c1所述的方法,其中宿主细胞具有降低的gdp-甘露糖4,6-脱水酶活性。
[0500]
c4.根据实施方案c1所述的方法,其中编码α-1,6岩藻糖基转移酶的基因突变,以低于正常水平表达,或在宿主细胞中敲除。
[0501]
c5.根据实施方案c1所述的方法,其中编码gdp-甘露糖4,6-脱水酶的基因突变,以低于正常水平表达,或在宿主细胞中敲除。
[0502]
c6.根据实施方案c1至c5中任一项所述的方法,其中少于80%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0503]
c7.根据实施方案c1至c5中任一项所述的方法,其中少于70%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0504]
c8.根据实施方案c1至c5中任一项所述的方法,其中少于60%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0505]
c9.根据实施方案c1至c5中任一项所述的方法,其中少于50%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0506]
c10.根据实施方案c1至c5中任一项所述的方法,其中少于40%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0507]
c11.根据实施方案c1至c5中任一项所述的方法,其中少于30%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0508]
c12.根据实施方案c1至c5中任一项所述的方法,其中少于20%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0509]
c13.根据实施方案c1至c5中任一项所述的方法,其中少于10%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0510]
c14.根据实施方案c1至c13中任一项所述的方法,其中抗体群体具有增强的抗体依赖性细胞毒性(adcc)和增强的补体依赖性细胞毒性(cdc)两者。
[0511]
c15.根据实施方案c1至c14中任一项所述的方法,其中抗体是igg1。
[0512]
c16.根据实施方案c1至c15中任一项所述的方法,其中抗体与hla-g结合,并且其
中抗体任选地如第5.5部分中所述。
[0513]
c17.根据实施方案c16所述的方法,其中与hla-g结合的抗体包含seq id no:180的轻链核苷酸序列和seq id no:182的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变),或包含seq id no:181的轻链核苷酸序列和seq id no:183的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变)。
[0514]
c18.根据实施方案c1至c14中任一项所述的方法,其中抗体与cd37结合,其中抗体任选地如第5.6部分中所述。
[0515]
c19.根据实施方案c18所述的方法,其中与cd37结合的抗体包含seq id no:69的轻链核苷酸序列和seq id no:85的重链核苷酸序列、seq id no:70的轻链核苷酸序列和seq id no:86的重链核苷酸序列、seq id no:71的轻链核苷酸序列和seq id no:87的重链核苷酸序列、seq id no:72的轻链核苷酸序列和seq id no:88的重链核苷酸序列、seq id no:73的轻链核苷酸序列和seq id no:89的重链核苷酸序列、seq id no:74的轻链核苷酸序列和seq id no:90的重链核苷酸序列、seq id no:75的轻链核苷酸序列和seq id no:91的重链核苷酸序列或seq id no:76的轻链核苷酸序列和seq id no:92的重链核苷酸序列。
[0516]
c20.根据实施方案c1至c14中任一项所述的方法,其中抗体与gprc5d结合,其中抗体任选地如第5.7部分中所述。
[0517]
c21.根据实施方案c20所述的方法,其中与gprc5d结合的抗体包含seq id no:104的轻链核苷酸序列和seq id no:106的重链核苷酸序列。
[0518]
c22.根据实施方案c1至c14中任一项所述的方法,其中抗体与klk2结合,其中抗体任选地如第5.8部分中所述。
[0519]
c23.根据实施方案c22所述的方法,其中与klk2结合的抗体包含seq id no:161的轻链核苷酸序列和seq id no:160的重链核苷酸序列、seq id no:161的轻链核苷酸序列和seq id no:162的重链核苷酸序列或seq id no:161的轻链核苷酸序列和seq id no:163的重链核苷酸序列。
[0520]
c24.根据实施方案c1至c14中任一项所述的方法,其中抗体与psma结合,其中抗体任选地如第5.9部分中所述。
[0521]
c25.根据实施方案c24所述的方法,其中与psma结合的抗体包含seq id no:241的轻链核苷酸序列和seq id no:242的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变),或包含seq id no:241的轻链核苷酸序列和seq id no:243的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变)。
[0522]
c26.根据实施方案c1至c14中任一项所述的方法,其中抗体与bcma结合,并且其中抗体任选地如第5.10部分中所述。
[0523]
c27.一种制备抗体群体的方法,该方法包括:
[0524]
(i)用于在抗体群体的fc区中引入k338a和t437r突变或k248e和t437r突变(re突变)的步骤;以及
[0525]
(ii)用于产生在经由n297残基连接至抗体的低聚糖中具有减少量的核心岩藻糖的抗体群体的步骤。
[0526]
c28.一种制备抗体群体的方法,该方法包括执行以下功能的步骤:在宿主细胞中表达编码抗体或其片段的多核苷酸,该宿主细胞不足以将岩藻糖残基添加到经由n297残基
连接至抗体的低聚糖,其中抗体群体包括fc区包含k338a和t437r突变或k248e和t437r突变(re突变)的抗体。
[0527]
c29.一种制备抗体群体的方法,该方法包括:
[0528]
(i)用于执行以下功能的步骤:在抗体群体的fc区中引入k338a和t437r突变或k248e和t437r突变(re突变);以及
[0529]
(ii)用于执行以下功能的步骤:产生在经由n297残基连接至抗体的低聚糖中具有减少量的核心岩藻糖的抗体群体。
[0530]
在又一组实施方案(d组实施方案)中,提供了:
[0531]
d1.一种治疗受试者的疾病或障碍的方法,该方法包括向受试者施用抗体群体。
[0532]
(i)其中少于80%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基;并且
[0533]
(ii)其中抗体群体包括fc区包含k338a和t437r突变或k248e和t437r突变(re突变)的抗体,
[0534]
其中氨基酸残基编号根据eu编号系统。
[0535]
d2.根据实施方案d1所述的方法,其中少于70%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0536]
d3.根据实施方案d1所述的方法,其中少于60%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0537]
d4.根据实施方案d1所述的方法,其中少于50%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0538]
d5.根据实施方案d1所述的方法,其中少于40%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0539]
d6.根据实施方案d1所述的方法,其中少于30%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0540]
d7.根据实施方案d1所述的方法,其中少于20%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0541]
d8.根据实施方案d1所述的方法,其中少于10%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0542]
d9.根据实施方案d1至d8中任一项所述的方法,其中通过在宿主细胞中表达编码抗体或其片段的多核苷酸来产生抗体,该宿主细胞不足以将岩藻糖添加到连接至抗体的低聚糖。
[0543]
d10.根据实施方案d9所述的方法,其中宿主细胞具有降低的gdp-甘露糖4,6-脱水酶(gmd)活性或降低的α-1,6岩藻糖基转移酶活性。
[0544]
d11.根据实施方案d1至d10中任一项所述的方法,其中抗体群体具有增强的抗体依赖性细胞毒性(adcc)和增强的补体依赖性细胞毒性(cdc)两者。
[0545]
d12.根据实施方案d1至d11中任一项所述的方法,其中抗体是igg1。
[0546]
d13.根据实施方案d1至d12中任一项所述的方法,其中抗体与hla-g结合,其中抗体任选地如第5.5部分中所述。
[0547]
d14.根据实施方案d13所述的方法,其中与hla-g结合的抗体包含seq id no:180
的轻链核苷酸序列和seq id no:182的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变),或包含seq id no:181的轻链核苷酸序列和seq id no:183的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变)。
[0548]
d15.根据实施方案d1至d12中任一项所述的方法,其中抗体与cd37结合,并且其中抗体任选地如第5.6部分中所述。
[0549]
d16.根据实施方案d15所述的方法,其中与cd37结合的抗体包含seq id no:69的轻链核苷酸序列和seq id no:85的重链核苷酸序列、seq id no:70的轻链核苷酸序列和seq id no:86的重链核苷酸序列、seq id no:71的轻链核苷酸序列和seq id no:87的重链核苷酸序列、seq id no:72的轻链核苷酸序列和seq id no:88的重链核苷酸序列、seq id no:73的轻链核苷酸序列和seq id no:89的重链核苷酸序列、seq id no:74的轻链核苷酸序列和seq id no:90的重链核苷酸序列、seq id no:75的轻链核苷酸序列和seq id no:91的重链核苷酸序列或seq id no:76的轻链核苷酸序列和seq id no:92的重链核苷酸序列。
[0550]
d17.根据实施方案d1至d12中任一项所述的方法,其中抗体与gprc5d结合,其中抗体任选地如第5.7部分中所述。
[0551]
d18.根据实施方案d17所述的方法,其中与gprc5d结合的抗体包含seq id no:104的轻链核苷酸序列和seq id no:106的重链核苷酸序列。
[0552]
d19.根据实施方案d1至d12中任一项所述的方法,其中抗体与klk2结合,其中抗体任选地如第5.8部分中所述。
[0553]
d20.根据实施方案d19所述的方法,其中与klk2结合的抗体包含seq id no:161的轻链核苷酸序列和seq id no:160的重链核苷酸序列、seq id no:161的轻链核苷酸序列和seq id no:162的重链核苷酸序列或seq id no:161的轻链核苷酸序列和seq id no:163的重链核苷酸序列。
[0554]
d21.根据实施方案d1至d12中任一项所述的方法,其中抗体与psma结合,并且其中抗体任选地如第5.9部分中所述。
[0555]
d22.根据实施方案d21所述的方法,其中与psma结合的抗体包含seq id no:241的轻链核苷酸序列和seq id no:242的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变),或包含seq id no:241的轻链核苷酸序列和seq id no:243的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变)。
[0556]
d23.根据实施方案d1至d12中任一项所述的方法,其中抗体与bcma结合,并且其中抗体任选地如第5.10部分中所述。
[0557]
d24.根据实施方案d1至d11中任一项所述的方法,其中抗体与抗原结合,并且其中疾病或病症与抗原相关。
[0558]
d25.根据实施方案d24所述的方法,其中抗原是hla-g。
[0559]
d26.根据实施方案d24所述的方法,其中抗原是cd37。
[0560]
d27.根据实施方案d24所述的方法,其中抗原是gprc5d。
[0561]
d28.根据实施方案d24所述的方法,其中抗原是klk2。
[0562]
d29.根据实施方案d24所述的方法,其中抗原是psma。
[0563]
d30.根据实施方案d24所述的方法,其中抗原是bcma。
[0564]
d31.根据实施方案d24至d30中任一项所述的方法,其中疾病或障碍为实体瘤癌
症。
[0565]
d32.根据实施方案d24至d30中任一项所述的方法,其中疾病或障碍选自:肾腺、胰腺或肺腺癌、非小细胞肺癌和卵巢癌。
[0566]
d33.一种治疗受试者的疾病或障碍的方法,该方法包括向受试者施用抗体群体。
[0567]
(i)其中少于80%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基;并且
[0568]
(ii)其中抗体群体包括在其fc区中具有一个或多个突变以用于增加抗体的cdc活性的抗体。
[0569]
d34.一种治疗受试者的疾病或障碍的方法,该方法包括向受试者施用:(a)抗体群体,该抗体群体包括用于增加抗体的adcc活性的第一构件和用于增加抗体的cdc活性的第二构件;和(b)药学上可接受的赋形剂。
[0570]
在又一组实施方案(e组实施方案)中,提供了:
[0571]
e1.一种调节宿主的免疫力的方法,该方法包括向宿主施用抗体群体,
[0572]
(i)其中少于80%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基;并且
[0573]
(ii)其中抗体群体包括fc区包含k338a和t437r突变或k248e和t437r突变(re突变)的抗体,
[0574]
其中氨基酸残基编号根据eu编号系统。
[0575]
e2.根据实施方案e1所述的方法,其中少于70%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0576]
e3.根据实施方案e1所述的方法,其中少于60%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0577]
e4.根据实施方案e1所述的方法,其中少于50%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0578]
e5.根据实施方案e1所述的方法,其中少于40%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0579]
e6.根据实施方案e1所述的方法,其中少于30%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0580]
e7.根据实施方案e1所述的方法,其中少于20%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0581]
e8.根据实施方案e1所述的方法,其中少于10%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基。
[0582]
e9.根据实施方案e1至e8中任一项所述的方法,其中通过在宿主细胞中表达编码抗体或其片段的多核苷酸来产生抗体,该宿主细胞不足以将岩藻糖添加到连接至抗体的低聚糖。
[0583]
e10.根据实施方案e9所述的方法,其中宿主细胞具有降低的gdp-甘露糖4,6-脱水酶(gmd)活性或降低的α-1,6岩藻糖基转移酶活性。
[0584]
e11.根据实施方案e1至e10中任一项所述的方法,其中抗体群体具有增强的抗体依赖性细胞毒性(adcc)和增强的补体依赖性细胞毒性(cdc)两者。
[0585]
e12.根据实施方案e1至e11中任一项所述的方法,其中抗体是igg1。
[0586]
e13.根据实施方案e1至e12中任一项所述的方法,其中抗体与hla-g结合,并且其中抗体任选地如第5.5部分中所述。
[0587]
e14.根据实施方案e13所述的方法,其中与hla-g结合的抗体包含seq id no:180的轻链核苷酸序列和seq id no:182的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变),或包含seq id no:181的轻链核苷酸序列和seq id no:183的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变)。
[0588]
e15.根据实施方案e1至e12中任一项所述的方法,其中抗体与cd37结合,并且其中抗体任选地如第5.6部分中所述。
[0589]
e16.根据实施方案e15所述的方法,其中与cd37结合的抗体包含seq id no:69的轻链核苷酸序列和seq id no:85的重链核苷酸序列、seq id no:70的轻链核苷酸序列和seq id no:86的重链核苷酸序列、seq id no:71的轻链核苷酸序列和seq id no:87的重链核苷酸序列、seq id no:72的轻链核苷酸序列和seq id no:88的重链核苷酸序列、seq id no:73的轻链核苷酸序列和seq id no:89的重链核苷酸序列、seq id no:74的轻链核苷酸序列和seq id no:90的重链核苷酸序列、seq id no:75的轻链核苷酸序列和seq id no:91的重链核苷酸序列或seq id no:76的轻链核苷酸序列和seq id no:92的重链核苷酸序列。
[0590]
e17.根据实施方案e1至e12中任一项所述的方法,其中抗体与gprc5d结合,并且其中抗体任选地如第5.7部分中所述。
[0591]
e18.根据实施方案e17所述的方法,其中与gprc5d结合的抗体包含seq id no:104的轻链核苷酸序列和seq id no:106的重链核苷酸序列。
[0592]
e19.根据实施方案e1至e12中任一项所述的方法,其中抗体与klk2结合,并且其中抗体任选地如第5.8部分中所述。
[0593]
e20.根据实施方案e19所述的方法,其中与klk2结合的抗体包含seq id no:161的轻链核苷酸序列和seq id no:160的重链核苷酸序列、seq id no:161的轻链核苷酸序列和seq id no:162的重链核苷酸序列或seq id no:161的轻链核苷酸序列和seq id no:163的重链核苷酸序列。
[0594]
e21.根据实施方案e1至e12中任一项所述的方法,其中抗体与psma结合,并且其中抗体任选地如第5.9部分中所述。
[0595]
e22.根据实施方案e21所述的方法,其中与psma结合的抗体包含seq id no:241的轻链核苷酸序列和seq id no:242的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变),或包含seq id no:241的轻链核苷酸序列和seq id no:243的重链核苷酸序列,但具有k338a和t437r突变或k248e和t437r突变(re突变)。
[0596]
e23.根据实施方案e1至e12中任一项所述的方法,其中抗体与bcma结合,并且其中抗体任选地如第5.10部分中所述。
[0597]
e24.一种调节宿主的免疫力的方法,该方法包括施用抗体群体,
[0598]
(i)其中少于80%的经由其n297残基共价连接至抗体群体的低聚糖包含核心岩藻糖残基;并且
[0599]
(ii)其中抗体群体包括在其fc区中具有一个或多个突变以用于增加抗体的cdc活性的抗体。
[0600]
e25.一种调节宿主的免疫力的方法,该方法包括施用抗体群体:该抗体群体包括用于增加抗体的adcc活性的第一构件和用于增加抗体的cdc活性的第二构件。
[0601]
7.实施例
[0602]
以下是对在研究中使用的各种方法和材料的描述。它们被提出以便为本领域普通技术人员提供如何制造和使用本发明的完整公开和描述,并且不旨在限制发明人认为其发明的范围,也不旨在表示执行以下实验并且是可以执行的所有实验。应当理解,不一定要执行以现在时态书写的示例性描述,而是可执行这些描述以生成与本发明的教导相关联的数据等。已努力确保关于所使用的数字(例如量、百分比等)的准确性,但应考虑一些实验误差和偏差。
[0603]
实施例1-抗hla-g抗体的adcc和cdc功能分析
[0604]
在本研究中测试了抗hla-g抗体及其具有修饰的恒定区的变体(即,低岩藻糖基化的并且/或者具有k248e和t437r(re)突变,并且这些抗体汇总在下表3中。
[0605]
表3.抗hla-g抗体及其变体
[0606][0607]
具有正常和低岩藻糖基化的抗体的adcc功能分析
[0608]
测试具有正常和低岩藻糖基化的抗hla-g抗体在内源性表达hla-g的绒毛膜癌细胞系jeg-3中介导经由adcc的肿瘤细胞杀伤的能力。简而言之,将jeg-3细胞装载batda一细胞死亡后释放并在形成荧光螯合物之后可在细胞培养上清液中检测到的细胞标记试剂。将抗hla-g抗体添加到batda标记的jeg-3细胞中。可在50∶1的效应细胞与靶细胞比率(e∶t比率)下将培养过夜的外周血单核细胞(pbmc)以5,000个细胞/孔添加到jeg-3细胞中。将混合物在37℃下温育4小时。将batda螯合物底物铕(iii)螯合物以1∶10的比率添加到混合物中。所释放的batda的量通过测量在615nm处的发射荧光来确定。使用含有与triton-x 100洗涤剂混合的batda标记的靶细胞的孔来确定100%肿瘤细胞杀伤的荧光信号。
[0609]
抗hla-g抗体在缺乏岩藻糖基化的中国仓鼠卵巢(cho)细胞中表达以产生具有小于10%岩藻糖基化的抗体。具有不结合fc受体的fc区的野生型抗体的修饰版本作为包含l234a、l235a和d265s突变的阴性对照生成。测试具有正常和低岩藻糖基化的野生型抗体的群体在50∶1的效应细胞:靶细胞比率下诱导基于nk细胞的adcc对抗任一种jeg-3细胞的能力。
[0610]
包含re突变的抗体的cdc功能分析
[0611]
测试具有re突变的抗hla-g抗体在绒毛膜癌细胞系jeg-3或腺癌细胞系rerf-lc-ad-1中介导经由cdc的肿瘤细胞杀伤的能力。简而言之,将jeg-3细胞在具有10%胎牛血清(fbs)的dmem培养基中培养,并将rerf-lc-ad-1在具有10%fbs的rpmi培养基中培养。将抗
体添加到靶细胞中并在37℃下温育30分钟。然后将幼兔血清添加到靶细胞中至10%的最终浓度,以提供cdc的补体组分源。将混合物在37℃下温育4小时。将100μl celltiter-glo试剂(promega)添加到混合物中,然后在室温下温育10分钟。通过用tecan spark读取器测量发光来确定靶细胞活力,并以相对发光单位(rlu)报告。
[0612]
具有正常和低岩藻糖基化并包含re突变的抗体的adcc和cdc功能分析
[0613]
包含re突变的抗体在缺乏岩藻糖基化的cho细胞中表达以产生具有小于10%岩藻糖基化的抗体。测试具有正常和低岩藻糖基化的抗体介导对抗细胞的cdc的能力。
[0614]
还测试具有re突变和低岩藻糖基化的抗体的adcc活性。简而言之,将抗体添加到已经预填装有batda的jeg-3细胞中。可在50∶1的效应细胞与靶细胞比率(e∶t比率)下将培养过夜的外周血单核细胞(pbmc)以5,000个细胞/孔添加到jeg-3细胞中。将混合物在37℃下温育4小时。将铕(iii)螯合物以1∶10的比率添加到混合物中。所释放的batda的量通过测量在615nm处的发射荧光来确定。使用含有与triton-x100洗涤剂混合的batda标记的靶细胞的孔来确定100%肿瘤细胞杀伤的荧光信号。
[0615]
实施例2—抗cd37抗体的cdc功能分析
[0616]
测试八种不同类型的抗cd37抗体(表2)在细胞系carnaval(其表达高水平的cd37)和jeko-1(其表达较低水平的cd37)中介导经由cdc的肿瘤细胞杀伤的能力。简而言之,对于每种类型的抗cd37抗体,生成具有低岩藻糖基化的抗体(即,分别为t26b375.clf、t26b382.clf、t26b386.clf、t26b379.clf、t26b373.clf、t26b388.clf、t26b385.clf和t26b374.clf)、包含s239d/i332e(xencor)突变的抗体(即,分别为t26b612、t26b613、t26b614、t26b615、t26b608、t26b609、t26b610和t26b611)、包含re突变的抗体(即,分别为t26b461、t26b463、t26b465、t26b462、t26b459、t26b466、t26b464和t26b460)和包含re突变并具有低岩藻糖基化的抗体(即,分别为t26b461.clf、t26b463.clf、t26b465.clf、t26b462.clf、t26b459.clf、t26b466.clf、t26b464.clf和t26b460.clf)。将抗cd37抗体添加到carnaval靶细胞中并在37℃下温育30分钟。然后将幼兔血清添加到靶细胞中至10%的最终浓度,以提供cdc的补体组分源。将混合物在37℃下温育4小时。将100μl celltiter-glo试剂(promega)添加到混合物中,然后在室温下温育10分钟。通过用tecan spark读取器测量发光来确定靶细胞活力,并以相对发光单位(rlu)报告。
[0617]
抗cd37抗体及其具有修饰的恒定区的变体汇总于下表4中。
[0618]
表4.抗cd37抗体及其变体
[0619][0620][0621]
具有低岩藻糖基化的抗cd37抗体表现出对抗carnaval细胞但不对抗jeko-1细胞
的cdc活性(图1a和图1b)。这些抗体中的xencor突变显著消除其对抗carnaval细胞的cdc活性(图1c)。re突变进一步增加这些抗体对抗carnaval细胞的cdc效力,同时赋予这些抗体对抗jeko-1细胞的cdc活性(图1e和1f)。重要的是,与具有正常岩藻糖基化的抗体(图1e和1f)相比,当使用具有低岩藻糖基化的抗体(图1g和图1h)时,通过re突变对cdc活性的增强不受影响。
[0622]
总之,这些结果表明re突变的cdc增强特征不依赖于靶标。这些结果还表明,虽然发现s239d/i332e突变提高抗体的adcc活性(lazar,g.a.等人,出处同上),但它们对cdc产生负面影响。相反,re突变可增强抗体的cdc活性。这种增强不受抗体的低岩藻糖基化的影响,抗体的低岩藻糖基化可增强其adcc活性。
[0623]
示例性抗cd37抗体的vl和vh氨基酸序列汇总于下表5和表6中。
[0624]
表5.示例性抗cd37抗体的vl氨基酸序列
[0625]
[0626]
[0627][0628]
表6.示例性抗cd37抗体的vh氨基酸序列
[0629]
[0630]
[0631][0632]
示例性抗cd37抗体的轻链和重链的完整氨基酸序列汇总于下表7和表8中。
[0633]
表7.示例性抗cd37抗体的轻链的完整氨基酸序列
[0634]
[0635]
[0636]
[0637][0638]
表8.示例性抗cd37抗体的重链的完整氨基酸序列
[0639]
[0640]
[0641]
[0642]
[0643]
[0644]
[0645][0646]
示例性抗cd37抗体的vl和vh核苷酸序列汇总于下表9和表10中。
[0647]
表9.示例性抗cd37抗体的vl核苷酸序列
[0648]
[0649]
[0650]
[0651]
[0652][0653]
表10.示例性抗cd37抗体的vh核苷酸序列
[0654]
[0655]
[0656]
[0657]
[0658]
[0659][0660]
示例性抗cd37抗体的轻链和重链的完整核苷酸序列汇总于下表11和表12中。
[0661]
表11.示例性抗cd37抗体的轻链的完整核苷酸序列
[0662]
[0663]
[0664]
[0665]
[0666]
[0667]
[0668]
[0669]
[0670][0671]
表12.示例性抗cd37抗体的重链的完整核苷酸序列
[0672]
[0673]
[0674]
[0675]
[0676]
[0677]
[0678]
[0679]
[0680]
[0681]
[0682]
[0683]
[0684]
[0685]
[0686]
[0687]
[0688][0689]
实施例3—抗gprc5d抗体的cdc功能分析
[0690]
为了进一步证实fc区中re突变的cdc增强特征是突变的一般特性,在表达gprc5d的第三靶细胞系h929中研究了re突变的影响。简而言之,将具有低岩藻糖基化的野生型igg1抗体gc5b747.clf及其具有re突变的对应物gc5b752.clf添加到h929靶细胞中并在37℃下温育30分钟。然后将幼兔血清添加到靶细胞中至10%的最终浓度,以提供cdc的补体组分源。将混合物在37℃下温育4小时。将100μl celltiter-glo试剂(promega)添加到混合物中,然后在室温下温育10分钟。通过用tecan spark读取器测量发光来确定靶细胞活力,并以相对发光单位(rlu)报告。
[0691]
野生型gc5b747.clf抗体不表现出对抗h929细胞的任何cdc活性,而包含re突变的gc5b752.clf抗体表现出对抗h929细胞的显著增强的cdc活性(图2)。
[0692]
这些结果表明,fc区中的re突变在多个靶细胞系上始终增强抗体的cdc活性。因此,这种cdc增强不是靶标特异性现象,而是可应用以通常增强fc效应子功能的re突变的一般特征。
[0693]
示例性抗gprc5d抗体的vl和vh氨基酸序列汇总于下表13中。
[0694]
表13.示例性抗gprc5d抗体的vl和vh氨基酸序列
[0695]
[0696][0697]
示例性抗gprc5d抗体的轻链和重链的完整氨基酸序列汇总于下表14中。
[0698]
表14.示例性抗gprc5d抗体的轻链和重链的完整氨基酸序列
[0699][0700]
示例性抗gprc5d抗体的vl和vh核苷酸序列汇总于下表15中。
[0701]
表15.示例性抗gprc5d抗体的vl和vh核苷酸序列
[0702][0703][0704]
示例性抗gprc5d抗体的轻链和重链的完整核苷酸序列汇总于下表16中。
[0705]
表16.示例性抗gprc5d抗体的轻链和重链的完整核苷酸序列
[0706]
[0707]
[0708][0709]
实施例4-抗klk2抗体的生成
[0710]
使用转基因小鼠和转基因大鼠表达人免疫球蛋白基因座来生成抗体
[0711]
含有嵌合人/大鼠igh基因座(包含22个人vh,全部的人d和jh片段以天然构型连接至大鼠ch基因座)连同完全人igl基因座(连接至jκ-cκ的12个vκ和连接至jλ-cλ的16个vλ)(参见例如,osbom等人,j immunol,2013,190(4):1481-90)。因此,大鼠表现出大
鼠免疫球蛋白的表达降低,并且响应于免疫,引入的人重链和轻链转基因经历类别转换和体细胞突变以生成具有完全人可变区的高亲和力嵌合人/大鼠igg单克隆抗体。国际公布wo14/093908中描述了的制备和用途以及由这些大鼠携带的基因组修饰。
[0712]
小鼠生成具有与人ch1和cl结构域连接的人可变结构域、嵌合人/小鼠铰链区和小鼠fc区的抗体。ablexis κ小鼠和λ小鼠品系通过如下所示其重链中的哪些重链是人或小鼠来区分。由κ小鼠产生的抗体缺乏源自小鼠vh、dh和jh外显子以及小鼠vκ、jκ和cκ外显子的序列。内源性小鼠igλ在κ小鼠中有活性。在该品系中人igκ链占原初组库的大约90%-95%,并且小鼠igλ链占原初组库的大约5%-10%。由λ小鼠产生的抗体缺乏源自小鼠vh、dh和jh外显子以及小鼠vλ、jλ和cλ外显子的序列。内源性小鼠igκ在λ小鼠中有活性。人igλ链占原初组库的大约40%,并且小鼠igr链占原初组库的大约60%。国际公布wo11/123708中描述了的制备和用途以及由这些大鼠携带的基因组修饰。
[0713]
将小鼠和大鼠用可溶性全长klk2蛋白质(人激肽释放酶-26-his蛋白质,具有氨基酸序列vpliegrivggwecekhsqpwqvavyshgwahcggvlvhpqwvltaahclkknsqvwlgrhnlfepedtgqrvpvshsfphplynmsllkhqslrpdedsshdlmllrlsepakitdvvkvlglptqepalgttcyasgwgsiepeeflrprslqcvslhysekvtefmlcaglwtggkdtcggdsggplvcngvlqgitswgpepcalpekpavytkvvhyrkwikdtiaanphhhhhh(seq id no:167))免疫。
[0714]
从淋巴结中提取小鼠和大鼠的淋巴细胞并按队列进行融合。合并细胞并针对cd138表达进行分选。使用可溶性hklk2抗原以高通量微型化msd格式进行杂交瘤筛选。将大约大于300份样品鉴定为klk2结合剂。使用biacore
tm
8k spr系统,通过单循环动力学方法测量大于300份抗hklk2上清液样品与人klk2蛋白质的结合。另外,测试上清液样品与人klk3蛋白质的结合,并通过流式细胞术测试上清液样品与表达klk2的细胞系vcap和阴性对照细胞系du145的结合。
[0715]
在vh-vl和vl-vh两种取向中,使选定的结合剂经受scfv转化并测试热稳定性。以vh-接头-vl的取向生成二元组合scfv文库,其中可变区中的一个可变区包含组合文库的序列,另一个可变区包含亲本kl2b30 vh或vl的序列。使用具有ggsegkssgsgseskstggs(seq id no:166)的序列的接头来缀合vh/vl区。工程化scfv在大肠杆菌中克隆并表达。通过elisa测试由上清液得到的scfv与人klk2的结合,并将这种结合与kl2b30抗体的结合进行比较。将表现出与kl2b30的结合亲和力相当的结合亲和力的任何新变体合并,并在55℃、60℃和65℃下将大肠杆菌培养物上清液温育10分钟之后进一步测试与人klk2的结合。在55℃、60℃和65℃下温育后保持与hu11b6相当的结合和提高的热稳定性的分子以两个取向(vh-接头-vl;vl-接头-vh)矩阵化并且转化为哺乳动物scfv以如下所述进一步表征。
[0716]
由于小鼠免疫活动生成kl2b30并且其以fab格式、mab格式、vh-接头-vl取向的scfv格式或vl-接头-vh取向的scfv格式表达,并且如下所述进一步分析。使用seq id no:166的接头序列来缀合vh/vl区。
[0717]
kl2b30抗体及其变体的序列汇总于下表17中。
[0718]
表17.kl2b30抗体和变体的氨基酸和核苷酸序列
[0719]
[0720]
[0721]
[0722]
[0723][0724]
实施例5-抗klk2抗体的生物物理表征
[0725]
抗klk2抗体的亲和力和热稳定性
[0726]
通过表面等离子体共振(spr)测量选定hklk2抗体对可溶性hklk2的亲和力。spr是一种无标签技术,用于通过测量复合物形成和解离时的质量变化来研究两个结合配偶体之间的相互作用的强度。在涂覆有抗fc抗体的传感器芯片上捕获抗体,接着以各种浓度和指定的缔合和解离时间注射可溶性hk2。解离后,用适当的溶液再生表面以准备进行下一相互作用。通过将传感器图拟合到1∶1langmuir模型来提取动力学信息(结合速率和解离速率常数)。将结合亲和力(kd)报告为速率常数比率(k
off
/k
on
)。经测量,kl2b30 fab(klcb80)抗体的kd值为0.460nm。
[0727]
使用自动prometheus仪器,通过差示扫描荧光测定法(nanodsf)确定热稳定性。使用nanodsf测量在磷酸盐缓冲盐水(ph 7.4)中0.5mg/ml的浓度下分子的tm。通过将样品从384孔样品板装载到24孔毛细管中来进行测量。对每个样品执行重复运行。热扫描范围为20℃至95℃,速率为1.0℃/分钟。在330nm和350nm的发射波长下监测固有色氨酸和酪氨酸荧光,并且将f350nm/f330nm比率相对于温度绘图以生成拆解曲线。经测量,kl2b30 fab(klcb80)抗体的tm为>70℃。
[0728]
表位定位
[0729]
通过氢-氘交换质谱法(hdx-ms)确定kl2b30抗体上的表位。人klk2抗原用于表位定位实验。
[0730]
简而言之,将纯化的klk2抗原在氧化氘标记缓冲液中与和不与抗klk2抗体一起温育。在不同时间点通过添加8m尿素、1m tcep(ph 3.0)淬灭氢-氘交换(hdx)混合物。在室温下使淬灭的样品通过用缓冲液a(1%乙腈、0.1%fa的h2o溶液)平衡的600μl/min的固定胃蛋白酶/fpxiii柱。将胃蛋白酶片段装载到具有缓冲液a的600μl/min的反相阱柱上并且脱盐1分钟(600μl缓冲液a)。将脱盐片段通过c18柱在20分钟内以8%至35%缓冲液b(95%乙腈、5%h2o、0.0025%tfa)的线性梯度,以100μl/min分离,并且通过质谱法分析。使用ltq
tm orbitrap fusion lumos质谱仪(thermo fisher scientific)进行质谱分析,其中毛细管温度为275℃、分辨率150,000且质量范围(m/z)300-1,800。使用biopharma finder 3.0(thermo fisher scientific)在hdx实验之前进行非氘化样品的肽鉴定。使用hdexaminer 2.5版(sierra analytics,modesto,ca)从hdx实验的ms原始数据文件中提取质心值。
[0731]
将hklk2抗体kl2b30与可溶性hklk2蛋白质一起温育产生氢交换和整体保护的不同模式。将保护的区段定位到hklk2抗原的序列上以可视化结合表位。kl2b30与(i)具有kvtef(seq id no:164)的序列的残基174-178和(ii)具有hyrkw(seq id no:165)的序列的残基230-234的共同序列结合。
[0732]
抗klk2抗体的效应子功能分析
[0733]
生成抗klk2抗体及其具有修饰的恒定区(即,具有l234a/l235a/d265s突变、低岩藻糖基化和/或具有k248e和t437r(re)突变)的变体,并且测试其在脊椎前列腺癌(vcap)细胞系中介导经由adcc的肿瘤细胞杀伤的能力,并且这些抗体汇总在下表18中。
[0734]
表18.抗klk2抗体及其变体
[0735][0736][0737]
将亲本抗体kl2b30在其fc区中进行修饰以引入l234a、l235a和d265s突变(aas突变),这产生不结合fc受体的fc区。所得的kl2b871作为阴性对照生成。将kl2b30抗体在其fc区中进行修饰以引入k248e和t437r突变(re突变),并且所得抗体是kl2b870。kl2b870和kl2b872抗体在缺乏岩藻糖基化的细胞中表达以产生具有低岩藻糖基化的抗体(例如,在缺乏岩藻糖基化的中国仓鼠卵巢细胞中表达这些抗体会产生具有小于10%岩藻糖基化的抗体),它们分别被指定为kl2b870.clf和kl2b872.clf(参见表18)。
[0738]
将用nuclight red(essen bioscience)稳定转染的vcap细胞以每孔10,000个细胞接种在384孔板(perkin elmer viewplate)中的透明培养基(rpmi 1641 10%fbs,thermo fisher scientific)中,以允许细胞过夜粘附。用刚解冻的pbmc(hemcare,pb009c-3)进行adcc测定。对于pbmc作为效应细胞而言,每孔效应细胞与靶细胞的比率为34∶1。测试最终浓度在100nm至0.01nm范围的klk2抗体。在将效应细胞和抗体添加到靶细胞之后,在s3仪器(essen bioscience)下进行实时成像(图3a-图3e)。用软件定量每个孔的总红色积分信号。基于一式四份的值,通过软件和prism(graphpad software)进行数据分析。将细胞杀伤的百分比计算为:(1-klk2 mab/无mab对照)
×
100%。
[0739]
klk2抗体通过pbmc表现出对vcap细胞明显的剂量依赖性adcc活性。动力学表明,在添加效应细胞和抗体之后adcc活性立即开始并且随时间推移继续(图4)。klkb870.clf和klkb872.clf抗体以大约89%和85%细胞杀伤表现出最高的adcc活性,然后是klkb870(大约73%)。具有aas突变的igg1抗体klkb87未表现出任何adcc活性(图4)。在某个时间点生成
的剂量-响应曲线(在将效应细胞和抗体添加到靶细胞中之后48小时)表明,对于具有低岩藻糖基化的抗体klkb870.clf,杀伤ec50为大约354pm。正常岩藻糖基化抗体klkb870的ec50为大约1nm(表18)。
[0740]
kl2b870、kl2b871和kl2b872抗体的vh和vl氨基酸序列汇总于下表19中。
[0741]
表19.抗klk2抗体的vh和vl氨基酸序列
[0742][0743]
kl2b870、kl2b871和kl2b872抗体的vh和vl核苷酸序列汇总于下表20中。
[0744]
表20.抗klk2抗体的vh和vl核苷酸序列
[0745]
[0746]
[0747][0748]
kl2b870、kl2b871和kl2b872抗体的轻链和重链的完整氨基酸序列汇总于下表21中。
[0749]
表21.抗klk2抗体的重链和轻链氨基酸序列
[0750]
[0751]
[0752][0753]
kl2b870、kl2b871和kl2b872抗体的轻链和重链的完整核苷酸序列汇总于下表22中。
[0754]
表22.抗klk2抗体的重链和轻链核苷酸序列
[0755]
[0756]
[0757]
[0758][0759]
[0760]
实施例6-特异性抗hla-g抗体的adcc和cdc功能分析
[0761]
为了测试抗hla-g抗体在内源性表达hla-g的绒毛膜癌细胞系jeg-3(atcc htb-36)中介导经由adcc的肿瘤细胞杀伤的能力,将抗体添加到用可单向地穿透到细胞中的batda染料(perkin elmer目录号c136-100)标记的jeg-3细胞中。在细胞溶解时,染料被释放到含有铕的溶液中,铕与染料反应以形成荧光螯合物,可测量该荧光螯合物的荧光信号。在50:1的e:t比率下将培养过夜的pbmc以5,000个细胞/孔添加到jeg-3细胞中,并将混合物在37℃下温育4小时。将细胞混合物以1∶10添加到铕溶液中,在室温下温育15分钟,并监测610nm处的荧光以确定信号。使用含有与triton-x 100洗涤剂混合的batda标记的靶细胞的孔来确定100%杀伤的荧光信号。
[0762]
由于抗hla-g abs可表现出体外adcc,因此研究了这种活性是否可增强。若干项研究表明,由于与fc受体的亲和力结合较高,具有小于10%的末端岩藻糖基化fc区的抗体表现出增强的效应子功能。因此,在低岩藻糖中国仓鼠卵巢(cho)宿主中生成抗hla-g抗体mhgb732和mhgb738,以产生具有小于10%岩藻糖基化的抗体(mhgb732.clf和mhgb738.clf)(表23,图5a-图5d)。作为阴性对照,生成具有不能结合fc受体的fc区的mhgb738的版本,并且该抗体被称为mhgb745。
[0763]
测试正常岩藻糖和低岩藻糖抗体诱导对抗jeg-3细胞(图5a)或对抗rerf-lc-ad-1细胞(人肺腺癌细胞系,jcrb1020)(图5b)的基于nk细胞的adcc的能力。通过在cho细胞中用低表达水平的岩藻糖基转移酶表达编码重链和轻链的构建体来生成具有低岩藻糖基化的抗体,从而产生具有小于10%岩藻糖基化的抗体。
[0764]
如上所述进行adcc活性测定。效应细胞与靶细胞的比率示于图5a和图5b中。mhgb745和同种型对照均不在测定中诱导adcc。两种igg1抗体mhgb732和mhgb738可诱导adcc,而具有低岩藻糖基化的fc区的相同抗体表现出大约10倍增强的adcc活性。这表明,可通过使用具有低岩藻糖基化的抗体来获得adcc增强。
[0765]
接下来,测试这些抗体介导cdc的能力(图5c和图5d)。简而言之,在含有10%fbs的dmem(jeg-3)或rpmi(rerf-lc-ad-1)中运行测定。将抗体添加到靶细胞中并在37℃下温育30分钟。温育后,将15%-20%(储备浓度)的兔补体(cedarlane目录号cl3441-s)和热灭活补体添加到各孔中,分别至25μl/孔的体积。将混合物在37℃下温育4小时-12小时。通过添加100μl celltitre-glo(promega目录号g9242)试剂,然后在室温下温育10分钟来检测细胞溶解。使用tecan酶标仪监测发光。两种igg1抗体mhgb732和mhgb738不介导cdc。由于igg1抗体不能介导cdc,因此将其可变区克隆到具有显示特异性增强cdc活性的k248e和t437r突变(re突变)的igg1 fc中。具有与其igg1对应物相同的可变区的这些抗体可介导cdc活性。作为对照,在cdc活性测定中也测试了抗hla-g抗体mhgb665。检查了在具有低岩藻糖基化的抗体中re fc变体是否会影响adcc活性增强,以及具有低岩藻糖基化的fc区是否会影响re fc变体的cdc活性。在低岩藻糖宿主(具有小于10%的岩藻糖基化)中产生的具有re突变的抗体mhgb752和mhgb758具有与具有低岩藻糖基化的igg1抗体mhgb732和mhgb738相同的adcc活性(图5a和图5b)。类似地,在低岩藻糖宿主中产生的具有re突变的抗体与在正常岩藻糖宿主中产生的相同抗体具有相同的cdc活性(图5c和图5d)。
[0766]
抗体mhgb732和mhgb738及其具有修饰的恒定区的变体汇总于下表23中。
[0767]
表23.抗体mhgb732和mhgb738及其变体
[0768][0769][0770]
示例性抗hla-g抗体的vl和vh氨基酸序列汇总于下表24中。
[0771]
表24.示例性抗hla-g抗体的vl和vh氨基酸序列
[0772][0773]
示例性抗hla-g抗体的轻链和重链的完整氨基酸序列汇总于下表25中。
[0774]
表25.示例性抗hla-g抗体的轻链和重链的完整氨基酸序列
[0775]
[0776][0777]
示例性抗hla-g抗体的轻链和重链的完整核苷酸序列汇总于下表26中。
[0778]
表26.示例性抗hla-g抗体的轻链和重链的完整核苷酸序列
[0779]
[0780]
[0781][0782]
实施例7-抗psma抗体的adcc功能分析
[0783]
将抗psma抗体psmb896和psmb898在其fc区中进行修饰以引入k248e和t437r突变(re突变)。具有re突变的抗psma抗体在缺乏岩藻糖基化的细胞中表达以产生具有低岩藻糖基化的抗体。psmb896的所得抗体是psmb952;psmb898的所得抗体是psmb956。测定psmb952和psmb956的结合和热稳定性。结果表明,低岩藻糖基化和re突变不会影响psmb896和psmb898抗体的这些生物物理特征。
[0784]
将用gfp稳定转染的c42b和lncap细胞以每孔9,000个细胞接种在384孔板(perkin elmer viewplate)中的透明培养基(rpmi 1641 10%fbs,thermo fisher scientific)中,以允许细胞过夜粘附。通过robosep
tm
细胞分离仪器用刚解冻的pbmc(hemcare,pb009c-3)或从冷冻pbmc分离的nk细胞进行adcc测定。所分离的nk细胞立即使用或用低剂量il-2(1ng/ml,miltenyi biotec)准备过夜。对于pbmc而言,每孔效应细胞与靶细胞的比率为34:1,对于所分离的nk细胞而言,每孔效应细胞与靶细胞的比率为5:1。测试最终浓度在1o0nm至0.01nm范围的psmb952和psmb956抗体。在将效应细胞和抗体添加到靶细胞之后,在s3仪器(essen bioscience)下进行实时成像。用软件定量每个孔的总gfp积分信号。基于一式四份的值,通过软件和prism(graphpad software)进行数据分析。将细胞杀伤的百分比计算为:(1-psma mab/无mab对照)
×
100%。
[0785]
psmb952和psmb956抗体通过效应细胞表现出对c42b和lncap细胞明显的剂量依赖性adcc活性(图6a-图6d)。动力学表明,在添加效应细胞和抗体之后adcc活性立即开始并且随时间推移继续。对于pbmc,最大adcc活性为约97%,对于纯化的nk细胞为40%-50%。
[0786]
在某些时间点(对于pbmc为6小时,对于nk细胞为24小时)生成的剂量-响应曲线示出,杀伤ec50处于10-10
~10-11
m的范围内(表27)。
[0787]
表27.在6小时通过pbmc和在24小时通过nk细胞对c42b和lncap细胞的体外adcc杀伤ec50(m)
[0788]
靶细胞效应细胞psmb952psmb956c42bpbmc3.51e-0104.231e-010lncappbmc2.011e-0101.519e-010c42bnk2.453e-0119.956e-012lncapnk4.585e-0113.579e-011
[0789]
示例性抗psma抗体的vh和vl氨基酸序列汇总于下表28中。
[0790]
表28.示例性抗psma抗体的vh和vl氨基酸序列
[0791][0792][0793]
示例性抗psma抗体的vh和vl核苷酸序列汇总于下表29中。
[0794]
表29.示例性抗psma抗体的vh和vl核苷酸序列
[0795][0796][0797]
示例性抗psma抗体的轻链和重链的完整氨基酸序列汇总于下表30中。
[0798]
表30.示例性抗psma抗体的重链和轻链氨基酸序列
[0799][0800][0801]
示例性抗psma抗体的轻链和重链的完整核苷酸序列汇总于下表31中。
[0802]
表31.示例性抗psma抗体的重链和轻链核苷酸序列
[0803]
[0804]
[0805]
[0806][0807]
实施例8-双特异性psma
×
cd3抗体的adcc和cdc功能分析
[0808]
将示例性双特异性psma
×
cd3抗体在其fc区中进行修饰以引入re突变(k248e和t437r突变)。具有re突变的双特异性psma
×
cd3抗体在缺乏岩藻糖基化的细胞中表达以产生具有低岩藻糖基化的抗体。测定所得抗体的结合和热稳定性。
[0809]
将用gfp稳定转染的c42b和lncap细胞以每孔9,000个细胞接种在384孔板(perkin elmer viewplate)中的透明培养基(rpmi 1641 10%fbs,thermo fisher scientific)中,以允许细胞过夜粘附。通过robosep
tm
细胞分离仪器用刚解冻的pbmc(hemcare,pb009c-3)或从冷冻pbmc分离的nk细胞进行adcc测定。所分离的nk细胞立即使用或用低剂量il-2(1ng/ml,miltenyi biotec)准备过夜。对于pbmc而言,每孔效应细胞与靶细胞的比率为34:1,对于所分离的nk细胞而言,每孔效应细胞与靶细胞的比率为5:1。测试最终浓度在100nm至0.01nm范围的具有低岩藻糖基化和re突变的双特异性psma
×
cd3抗体。在将效应细胞和抗体添加到靶细胞之后,在s3仪器(essen bioscience)下进行实时成像。用软件定量每个孔的总gfp积分信号。基于一式四份的值,通过软件和prism(graphpad software)进行数据分析。将细胞杀伤的百分比计算为:(1-psma mab/无mab对照)
×
100%。
[0810]
接下来,测试这些抗体介导cdc的能力。简而言之,在含有10%fbs的dmem(jeg-3)或rpmi(rerf-lc-ad-1)中运行测定。将抗体添加到靶细胞中并在37℃下温育30分钟。温育后,将15%-20%(储备浓度)的兔补体(cedarlane目录号cl3441-s)和热灭活补体添加到各孔中,分别至25μl/孔的体积。将混合物在37℃下温育4小时-12小时。通过添加100μl celltitre-glo(promega目录号g9242)试剂,然后在室温下温育10分钟来检测细胞溶解。使用tecan酶标仪监测发光。
[0811]
实施例9-抗bcma抗体的adcc和cdc功能分析
[0812]
将示例性抗bcma抗体bcmb519在其fc区中进行修饰以引入re突变(k248e和t437r突变)。具有re突变的抗bcma抗体在缺乏岩藻糖基化的细胞中表达以产生具有低岩藻糖基化的抗体。测定所得抗体的结合和热稳定性。
[0813]
将用gfp稳定转染的c42b和lncap细胞以每孔9,000个细胞接种在384孔板(perkin elmer viewplate)中的透明培养基(rpmi 1641 10%fbs,thermo fisher scientific)中,以允许细胞过夜粘附。通过roboseptm细胞分离仪器用刚解冻的pbmc(hemcare,pb009c-3)或从冷冻pbmc分离的nk细胞进行adcc测定。所分离的nk细胞立即使用或用低剂量il-2(1ng/ml,miltenyi biotec)准备过夜。对于pbmc而言,每孔效应细胞与靶细胞的比率为34:1,对于所分离的nk细胞而言,每孔效应细胞与靶细胞的比率为5:1。测试最终浓度在100nm至0.01nm范围的具有低岩藻糖基化和re突变的抗bcma抗体。在将效应细胞和抗体添加到靶细胞之后,在s3仪器(essen bioscience)下进行实时成像。用软件定量每个孔的总gfp积分信号。基于一式四份的值,通过软件和prism(graphpad software)进行数据分析。将细胞杀伤的百分比计算为:(1-bcma mab/无mab对照)
×
100%。
[0814]
接下来,测试这些抗体介导cdc的能力。简而言之,在含有10%fbs的dmem(jeg-3)或rpmi(rerf-lc-ad-1)中运行测定。将抗体添加到靶细胞中并在37℃下温育30分钟。温育后,将15%-20%(储备浓度)的兔补体(cedarlane目录号cl3441-s)和热灭活补体添加到各孔中,分别至25μl/孔的体积。将混合物在37℃下温育4小时-12小时。通过添加100μl celltitre-glo(promega目录号g9242)试剂,然后在室温下温育10分钟来检测细胞溶解。使用tecan酶标仪监测发光。
[0815]
示例性抗bcma抗体(bcmb519)的vh cdr和vl cdr氨基酸序列示于下表32中。
[0816]
表32.示例性抗bcma抗体的cdr氨基酸序列
[0817][0818]
示例性抗bcma抗体(bcmb519)的vh和vl氨基酸序列汇总于下表33中。
[0819]
表33.示例性抗bcma抗体的vh和vl氨基酸序列
[0820][0821]
示例性抗bcma抗体(bcmb519)的重链的完整氨基酸序列汇总于下表34中。
[0822]
表34.示例性抗bcma抗体的重链氨基酸序列
[0823]
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。