1.本发明属于医药技术领域,涉及玫瑰烷型二萜类化合物及制备、药物组合物和抗肿瘤应用,具体公开了从月腺大戟中提取分离的四个具有相同的二萜母核的玫瑰烷型二萜类化合物euphebracteolatin c、euphebracteolatin d、euphebracteolatin e和euphebracteolatin f及其在制备抗肿瘤药物中的应用。
背景技术:
2.癌症是当前全球共同面对的持续性公共卫生挑战,作为全球第二大常见的死亡原因,癌症预计将成为21世纪人口预期寿命增长的最主要障碍。近几十年来,最常见的癌症有肺癌、肝癌、胃癌、食管癌和乳腺癌,其对公众健康构成严重威胁,经济负担沉重。
3.目前,临床上对于癌症主要的治疗手段有手术切除、放射治疗和化学药物治疗;但均存在一些局限性,如复发率高、药物耐受及各种不良反应,可谓“伤敌一千,自损八百”。中医药对癌症的治疗有着悠久的历史, 也是当今中医防治重大疾病的一个特色和优势。从中药中寻找抗癌活性明显且副作用小的天然化合物是行之有效的途径。
4.月腺大戟为中药狼毒的来源之一,始载于《神农本草经》,其以根入药,味辛,性平,归肝、脾经,具有逐水祛痰,破积杀虫的功效,临床用于治疗乳腺癌、肝癌等恶性肿瘤。现代研究表明,月腺大戟具有抗肿瘤、抗炎等作用,其中二萜类化合物具有良好的抗肿瘤作用。因此,从月腺大戟中寻找抗肿瘤活性的二萜类化合物具有重要的现实价值。
技术实现要素:
5.针对现有技术所存在的不足,本发明公开了玫瑰烷型二萜类化合物及制备、药物组合物和抗肿瘤应用,具体公开了从月腺大戟中提取的四个具有相同的二萜母核的玫瑰烷型二萜类化合物euphebracteolatin c、euphebracteolatin d、euphebracteolatin e和euphebracteolatin f及其在制备抗肿瘤药物中的应用。
6.为实现上述目的,本发明的技术方案如下:一种玫瑰烷型二萜类化合物,其是具有如下式i、ii、iii、ⅳ所示的结构:所示的结构:iiiiiiii
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀⅳ
。
7.本发明另一方面还提供了上述玫瑰烷型二萜类化合物的制备方法,所述玫瑰烷型二萜类化合物是从月腺大戟中提取分离获得。
8.在上述技术方案中,所述玫瑰烷型二萜类化合物的制备方法,包括以下步骤:s1、取干燥的月腺大戟,加入溶剂回流提取,合并提取液后浓缩,得浸膏;s2、将浸膏加入到8-12倍质量的水中混悬后,分别用石油醚、二氯甲烷和乙酸乙酯萃取,二氯甲烷萃取物和乙酸乙酯萃取物舍弃,将石油醚萃取物经硅胶柱色谱,使用石油醚-乙酸乙酯洗脱,收集馏分后利用硅胶薄层层析检识,合并依次得到馏分a、b、c、d、e、f、g、h和i;s3、将馏分b经硅胶柱色谱,使用石油醚-乙酸乙酯梯度洗脱,收集得到8个馏分b1~b8,将馏分b6经ods柱色谱,使用甲醇-水梯度洗脱,收集到60-70个馏分后,利用硅胶薄层层析检识,合并为10个馏分j1~j10,将馏分j5经sephadex lh-20凝胶柱色谱,使用二氯甲烷-甲醇梯度洗脱,收集到50-60个馏分后,利用硅胶薄层色谱检识,合并为5个馏分k1~k5;s4、以甲醇-水为流动相,采用hplc法,利用c
18
色谱柱在馏分k3中制备得到结构式如式i、iii和ⅳ所示的玫瑰烷型二萜类化合物,以乙腈-水为流动相,采用hplc法,利用c
18
色谱柱在馏分j6中制备得到结构式如式ii所示的玫瑰烷型二萜类化合物。
9.在本发明的具体实施方式中,步骤s4中,在hplc法分离馏分k3时所用的流动相中,根据化合物的极性,结合其分离度等因素,甲醇和水的体积比为(55:45)-(60:40),且结构式如式i、iii和ⅳ所示的玫瑰烷型二萜类化合物的保留时间分别为37-38 min、39-41 min和42-45 min。
10.在本发明的具体实施方式中,步骤s4中,在hplc法分离馏分j6时所用的流动相中,乙腈和水的体积比为(45:55)-(50:50),且结构式如式ii所示的玫瑰烷型二萜类化合物的保留时间为36-38 min。
11.在本发明的具体实施方式中,步骤s3中,将馏分b经硅胶柱色谱时,使用体积比为(100:0)-(0:100)的石油醚-乙酸乙酯进行梯度洗脱。
12.在本发明的具体实施方式中,步骤s3中,将馏分b6经ods柱色谱时,根据化合物的极性,结合其分离度等因素,使用体积比为(30:70)-(100:0)的甲醇-水进行梯度洗脱。
13.在本发明的具体实施方式中,步骤s3中,将馏分j5经sephadex lh-20凝胶柱色谱时,使用体积比为(100:0)-(0:100)的二氯甲烷-甲醇进行梯度洗脱。
14.在本发明的具体实施方式中,步骤s2中,将石油醚萃取物经硅胶柱色谱时,使用体积比为(100:0)-(0:100)的石油醚-乙酸乙酯进行洗脱。
15.在本发明的具体实施方式中,步骤s1中,所述溶剂为88-98 v%的乙醇水溶液,且其加入质量为月腺大戟的8-10倍,回流提取的次数为2-3次,每次提取1-3h。
16.本发明又一方面还提供了含有上述玫瑰烷型二萜类化合物的药物组合物。
17.具体地,在上述技术方案中,所述药物组合物的剂型为片剂、胶囊剂、颗粒剂、口服液、糖浆剂、膏剂、冲剂、滴丸或微丸。
18.具体地,在上述技术方案中,所述药物组合物还包括药效学上可接受的载体或赋形剂。也就是说,含有作为活性成份的本发明的玫瑰烷型二萜类化合物和常规药物赋形剂或辅剂或载体的药物组合物亦包含在本发明内。
19.本发明再一方面还提供了上述玫瑰烷型二萜类化合物或上述药物组合物在制备
抗肿瘤药物中的应用。
20.本发明与现有技术相比,具有以下优点:(1)本发明提供了一种目前尚未见报道的玫瑰烷型二萜类化合物,并进一步提供了一种操作简单可行、重现性好、提取纯度高的从月腺大戟中提取获得该玫瑰烷型二萜类化合物的方法;(2)试验结果表明,本发明所提供的玫瑰烷型二萜类化合物对乳腺癌细胞t47d和mcf-7、肝癌细胞hepg2和非小细胞肺癌细胞a549均具有明显的杀伤作用,尤其是对乳腺癌细胞t47d具有显著活性,可用于开发抗肿瘤类药物,尤其针对临床化疗阶段药物。
附图说明
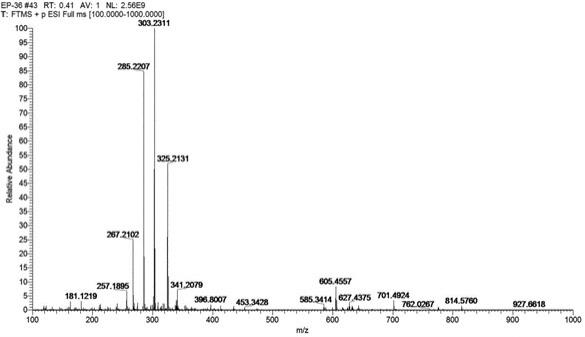
21.图1为本发明实施例1所制得的化合物1的hr-esi-ms谱;图2为本发明实施例1所制得的化合物1的1h nmr谱(600mhz,cdcl3);图3为本发明实施例1所制得的化合物1的
13
c nmr谱(150mhz,cdcl3);图4为本发明实施例1所制得的化合物1的hmbc谱;图5为本发明实施例1所制得的化合物1的noesy谱;图6为本发明实施例1所制得的化合物2的hr-esi-ms谱;图7为本发明实施例1所制得的化合物2的1h nmr谱(600mhz,cdcl3);图8为本发明实施例1所制得的化合物2的
13
c nmr谱(150 mhz,cdcl3);图9为本发明实施例1所制得的化合物2的hmbc谱;图10为本发明实施例1所制得的化合物2的noesy谱;图11为本发明实施例1所制得的化合物3的hr-esi-ms谱;图12为本发明实施例1所制得的化合物3的1h nmr谱(600mhz,cdcl3);图13为本发明实施例1所制得的化合物3的
13
c nmr谱(150 mhz,cdcl3);图14为本发明实施例1所制得的化合物3的hmbc谱;图15为本发明实施例1所制得的化合物3的noesy谱;图16为本发明实施例1所制得的化合物4的hr-esi-ms谱;图17为本发明实施例1所制得的化合物4的1h nmr谱(500mhz,cdcl3);图18为本发明实施例1所制得的化合物4的
13
c nmr谱(125 mhz,cdcl3);图19为本发明实施例1所制得的化合物4的hmbc谱;图20为本发明实施例1所制得的化合物4的noesy谱。
具体实施方式
22.为了使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步详细说明。
23.应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
24.实施例中,如无特别说明,所用手段均为本领域常规的手段。
25.本文中所用的术语“包含”、“包括”或其任何其它变形,意在覆盖非排它性的包括。例如,包含所列要素的组合物、步骤、方法、制品或装置不必仅限于那些要素,而是可以包括未明确列出的其它要素或此种组合物、步骤、方法、制品或装置所固有的要素。
26.实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可通过正规渠道商购买得到的常规产品。
27.在本文中所披露的范围的端点和任何值都不限于该精确的范围或值,这些范围或值应当理解为包含接近这些范围或值的值。对于数值范围来说,各个范围的端点值之间、各个范围的端点值和单独的点值之间,以及单独的点值之间可以彼此组合而得到一个或多个新的数值范围,这些数值范围应被视为在本文中具体公开。
28.此外,下面所描述的本发明各个实施方式中所涉及到的技术特征只要彼此之间未构成冲突就可以相互组合。
29.实施例1一种玫瑰烷型二萜类化合物的制备方法,包括如下步骤:s1、称取干燥的月腺大戟67 kg,加入质量为月腺大戟的10倍(670 kg)的95 v%的乙醇水溶液作为溶剂回流提取3次,每次提取2 h,合并提取液后浓缩,得到6.47 kg浸膏;s2、将浸膏(6.47 kg)加入到10倍质量的水(64.7 kg)中混悬后,分别用混悬液1.5倍量体积的石油醚、二氯甲烷和乙酸乙酯进行萃取,且各萃取剂分别萃取两次,得到1500 g石油醚萃取物、250 g乙酸乙酯萃取物(舍弃)和520 g二氯甲烷萃取物(舍弃),将石油醚萃取物经硅胶柱色谱,使用体积比为100︰0、90︰10、80︰20、70︰30、60︰40、50︰50、40︰60、30︰70、20︰80、10︰90和0︰100的石油醚-乙酸乙酯进行洗脱,每500 ml体积为1个馏分,共收集到50个馏分,利用硅胶薄层层析检识,合并依次得到馏分a、b、c、d、e、f、g、h和i;s3、将馏分b经硅胶柱色谱,使用体积比为100︰0、90︰10、80︰20、70︰30、60︰40、50︰50、40︰60、30︰70、20︰80、10︰90、0︰100的石油醚-乙酸乙酯梯度洗脱,共收集得到8个馏分b1~b8;将馏分b6经ods柱色谱,使用体积比为30︰70、40︰60、50︰50、60︰40、70︰30、80︰20、90︰10、100︰0的甲醇-水梯度洗脱,收集到68个馏分后,利用硅胶薄层层析检识,合并为10个馏分j1~j10;将馏分j5经sephadex lh-20凝胶柱色谱,使用体积比为100︰0、90︰10、80︰20、70︰30、60︰40、50︰50、40︰60、30︰70、20︰80、10︰90、0︰100的二氯甲烷-甲醇梯度洗脱,收集到55个馏分后,利用硅胶薄层色谱检识,合并为5个馏分k1~k5;s4、利用hplc法,以体积比为(55:45)-(60:40)的甲醇-水(最优选为56︰44)为流动相在馏分k3中制备得到化合物1(t
r = 37-38 min)、3(t
r = 39-41 min)、4(t
r = 42-45 min),以体积比为(45:55)-(50:50)的乙腈-水(最优选为48︰52)为流动相在馏分j6中制备得到化合物2(t
r = 36-38 min)。
30.对比例1本发明对比例1提供了一种玫瑰烷型二萜类化合物的制备方法,其步骤与实施例1类似,区别仅在于,步骤s3中,将馏分b6经ods柱色谱时,使用体积比为15:85的甲醇-水进行洗脱。
31.结果显示,无法制备得到化合物1-4。
32.对比例2本发明对比例2提供了一种玫瑰烷型二萜类化合物的制备方法,其步骤与实施例1类似,区别仅在于,步骤s4中,在hplc法分离馏分k3时所用的流动相中,甲醇和水的体积比为35:65。
33.结果显示,无法制备得到化合物1-4。
34.实施例2本发明实施例提供了实施例1所制得的化合物1的物理性质和检测数据,具体如下:白色粉末,易溶于三氯甲烷、甲醇; 105.13 (c 0.10,meoh)。
35.uv谱中(未示出),λ
max = 204 nm (meoh),提示为玫瑰烷型二萜类化合物的特征吸收;ir谱中(未示出),3442 cm-1
提示该结构含有羟基,1595 cm-1
提示该结构含有碳碳双键;根据高分辨质谱(hr-esi-ms,图1)m/z 303.2311[m h]
(计算值303.2319),推测其分子量为302,结合1h-nmr(图2)、
13
c-nmr谱(图3),确定其分子式为 c
20h30
o2,计算其不饱和度为6。
[0036]1h nmr (600 mhz, cdcl3) 谱(图2)显示,在低场区含有4 个烯氢信号 [δ
h 5.84 (1h, dd, j = 17.5, 10.8 hz), 5.59 (1h, dt, j = 5.3, 2.5 hz), 4.99 (1h, dd, j = 17.5, 1.2 hz), 4.90 (1h, dd, j = 10.8, 1.2 hz)];高场区存在4 个单峰甲基信号[δ
h 1.04, 0.96, 0.87,0.74 (each 3h, s)]。
[0037]
13
c nmr (150 mhz, cdcl3) 谱(图3)显示共有20 个碳信号,包括4 个甲基碳信号(δ
c 23.9, 23.0, 22.0, 13.1),5 个亚甲基碳信号(δ
c 37.3, 35.4, 32.4, 32.0, 31.1),2个次甲基碳信号(δ
c 48.5, 43.1),1个连氧碳信号(δ
c 74.6),4个烯氢碳信号(δ
c 150.3, 145.4 118.2, 109.7),1 个羰基碳信号(δ
c 213.5)以及3 个余下的季碳信号(δ
c 37.8, 35.6, 36.9)。
[0038]1h nmr、
13
c nmr的信号归属如下表所示。
positionδh(multi,jinhz)δcpositionδh(multi,jinhz)δc15.59(dt,j=5.3,2.5)118.2111.69(dd,j=13.6,3.9)1.77(ddd,j=13.6,4.2,3.0)35.422.00(m)2.40(dtd,j=17.3,5.3,2.5)32.0121.31(m)1.49(dd,j=13.6,4.2)32.433.60(dd,j=10.4,6.0)74.61335.6436.9141.43(m)1.61(dd,j=3.6,2.6)31.152.59(d,j=3.7)43.1155.84(dd,j=17.5,10.8)150.362.16(dd,j=18.8,13.8)2.53(dd,j=18.8,4.9)37.3164.90(dd,j=10.8,1.2)4.99(dd,j=17.5,1.2)109.77213.5170.96(s)22.082.61(d,j=3.6hz)48.5181.04(s)23.9937.8190.74(s)13.110145.4200.87(s)23.0
[0039]
结合1h nmr和
13
c nmr谱图,推测化合物1可能含有1个羰基,2对双键,推测余下的3个不饱和度为3个环所占有,此外,还可能含有1个与氧相连的碳信号和4个甲基;结合以上信息,推测该化合物1可能为一个玫瑰烷型二萜化合物。
[0040]
在hmbc谱(图4)中,可观察到h-5 (δ
h 2.59), h-6 (δ
h 2.16, 2.53), h-8 (δ
h 2.61), h-14 (δ
h 1.43)和c-7 (δ
c 213.5)之间的相关,推测羰基在c-7位;此外,h
3-17 (δ
h 0.96)与c-12 (δ
c 32.4)、c-13 (δ
c 35.6)、c-14 (δ
c 31.1)、c-15 (δ
c 150.3)之间的远程相关,h
3-18 (δ
h 1.04)与c-3 (δ
c 74.6)、c-4 (δ
c 36.9)、c-5 (δ
c 43.1)、c-19 (δ
c 13.1)之间的远程相关,h
3-19 (δ
h 0.74)与c-3 (δ
c 74.6)、c-4 (δ
c 36.9)、c-5 (δ
c 43.1)、c-18 (δ
c 23.9)之间的远程相关,h
3-20 (δ
h 0.87)与c-8 (δ
c 48.5)、c-9 (δ
c 37.8)、c-10 (δ
c 145.4)、c-11 (δ
c 35.4)之间的远程相关,可推测该结构中甲基的位置分别在c-17,c-18,c-19和c-20位。
[0041]
在noesy谱(图5)中,h-3 (δ
h 3.60)与h-5 (δ
h 2.59)、h-8 (δ
h 2.61)、h
3-18 (δ
h 1.04)具有noe相关,h-8 (δ
h 2.61)与h
3-17 (δ
h 0.96)具有noe相关,因此确定了化合物的相对构型,即h-3、h-5、h-8、h
3-18朝向一个平面为α构型,3-oh、h-15、h
3-19和h
3-20在另一个平面,为β构型。
[0042]
综上所述,确定了化合物1(euphebracteolatin c)的结构如下:。
[0043]
实施例3本发明实施例提供了实施例1所制得的化合物2的物理性质和检测数据,具体如下:白色粉末,易溶于三氯甲烷、甲醇; 13.99 (c0.10,meoh)。
[0044]
uv谱中(未示出),λ
max = 203 nm (meoh),提示为玫瑰烷型二萜类化合物的特征吸收;ir谱中(未示出),3442 cm-1
提示该结构含有羟基,1595 cm-1
提示该结构含有碳碳双键;根据高分辨质谱(hr-esi-ms,图6)m/z269.1893[m h-h2o]
,(计算值269.1900),推测其分子量为286,结合1h-nmr(图7)、
13
c-nmr谱(图8),确定其分子式为 c
19h26
o2,计算其不饱和度为7。
[0045]1h nmr (600 mhz, cdcl3)谱(图7)显示,在低场区存在5个烯氢信号[δh: 7.08 (1h, d, j = 8.3 hz), 6.65 (1h, d, j = 8.3 hz), 5.87 (1h, dd, j = 17.5, 10.7 hz), 4.97 (1h, dd, j = 17.5, 1.3 hz), 4.90 (1h, dd, j = 10.7, 1.3 hz)];存在两个与氧相连的氢信号[δh: 3.78 (1h, d, j = 11.0 hz), 3.63 (1h, d, j = 11.0 hz)];高场区含有2个单峰甲基氢信号[δ
h 2.13, 1.04 (each 3h, s)]。
[0046]
13
c nmr (150mhz, cdcl3)谱(图8)显示共有19个碳信号,包括2个甲基碳信号(δ
c 22.9, 11.3),5个亚甲基碳信号(δ
c 39.9, 32.7, 28.5, 27.1, 25.4),1个次甲基碳信号(δ
c 36.0),1个连氧碳信号(δ
c 63.6),8个烯氢碳信号(δ
c 152.1, 150.9, 137.3, 135.1, 123.9, 122.9, 112.3, 109.3),以及2个季碳信号(δ
c 40.9, 36.5)。
[0047]1h nmr、
13
c nmr的信号归属如下表所示。
positionδh(multi,jinhz)δcpositionδh(multi,jinhz)δc17.08(d,j=8.3)123.9111.46(dd,j=13.6,3.9)2.42(m)28.526.65(d,j=8.3)112.3121.42(d,j=3.3)1.65(d,j=4.0)32.73 152.113 36.54 122.9141.28(m)1.53(t,j=13.3)39.95 137.3155.87(dd,j=17.5,10.7)150.962.77(m)27.1164.90(dd,j=10.7,1.3)4.97(dd,j=17.5,1.3)109.371.62(m)1.83(ddt,j=13.3,9.9,6.6)25.4171.04(s)22.981.92(tt,j=13.3,3.4)36.0192.13(s)11.39 40.9203.63(d,j=11.0)3.78(d,j=11.0)63.610 135.1
ꢀꢀꢀ
[0048]
结合1h nmr 和
13
c nmr谱图,推测化合物2可能含有1个苯环和1 对末端双键,推测余下的2 个不饱和度为2 个环所占有;结合上述谱图数据,推测该化合物2可能为一个芳香玫瑰烷型二萜化合物。
[0049]
在hmbc谱(图9)中,可观察到h
2-20 (δ
h 3.78, 3.63)与c-8 (δ
c 36.0)、 c-9 (δ
c 40.9)、c-10 (δ
c 135.1)、c-11 (δ
c 28.5) 的远程相关,证明了羟基与c-20位相连;此外,h-15 (δ
h 5.87)与c-12 (δ
c 32.7)、c-13 (δ
c 36.5)、c-14 (δ
c 39.9)、c-17 (δ
c 22.9) 的远程相关,h
2-16 (δ
h 4.90 , 4.97)与c-13 (δ
c 36.5)、c-15 (δ
c 150.9) 的远程相关,证明了c-15位和c-16位之间双键的存在;h
3-17 (δ
h 1.04)与c-12 (δ
c 32.7)、c-13 (δ
c 36.5)、c-14 (δ
c 39.9)、c-15 (δ
c 150.9)的远程相关,h
3-19 (δ
h 2.13)与c-3 (δ
c 152.1)、c-4 (δ
c 122.9)、c-5 (δ
c 137.3)的远程相关,证明了c-17位和c-19位甲基的存在。
[0050]
在noesy谱(图10)中,h-8 (δ
h 1.92)和h
3-17 (δ
h 1.04)具有noe相关,h-15 (δ
h 5.87)和h
2-10 (δ
h 3.63, 3.78)具有noe相关;因此,确定了化合物2的相对构型,即h-8和h
3-17朝向同一个平面,为α构型,h-15和h
2-20朝向另一个平面,为β构型。
[0051]
综上所述,确定了化合物2(euphebracteolatin d)的结构如下:。
[0052]
实施例4本发明实施例提供了实施例1所制得的化合物3的物理性质和检测数据,具体如下:白色粉末,易溶于三氯甲烷、甲醇; 27.58(c 0.10,meoh)。
[0053]
uv (meoh)谱图(未示出)中λ
max = 204nm提示该化合物3为二萜类化合物,ir 谱图中(未示出)3442 cm
−1提示该结构含有羟基,1595 cm
−1提示该结构含有碳碳双键。根据高分辨质谱(hr-esi-ms,图11)m/z269.1893 [m h-h2o]
,(计算值269.1900),推测其分子量为286,确定其分子式为 c
19h26
o2,计算其不饱和度为7。
[0054]1h nmr (600 mhz, cdcl3)谱(图12)显示,在低场区存在5个烯氢信号[δh: 7.08 (1h, d, j = 8.5 hz), 6.67 (1h, d, j = 8.5 hz), 5.92 (1h, dd, j = 17.5, 10.7 hz), 5.02 (1h, dd, j = 17.5, 1.3 hz), 4.93 (1h, dd, j = 10.7, 1.3 hz)];存在1个与氧相连的氢信号[δh: 4.16 (1h, m)];高场区有3个甲基信号[δh: 2.14 (3h, s), 1.26 (3h, s), 1.03 (3h, s)]。
[0055]
13
c nmr (150mhz, cdcl3)谱(图13)显示共有19个碳信号,包括3个甲基碳信号(δ
c 24.1, 22.9, 11.5),4个亚甲基碳信号(δ
c 36.9, 36.7, 36.3, 33.0),1个次甲基碳信号(δ
c 40.2),1个连氧碳信号(δ
c 71.0),8个烯氢碳信号(δ
c 151.4, 150.9, 139.9, 132.7, 122.9, 122.1, 113.1, 109.4),以及2个季碳信号(δ
c 36.0, 36.0)。。
[0056]1h nmr、
13
c nmr的信号归属如下表所示。
positionδh(multi,jinhz)δcpositionδh(multi,jinhz)δc17.08(d,j=8.5)122.9111.62(d,j=3.5)1.99(dt,j=12.8,3.5)36.326.67(d,j=8.5)113.1121.40(m)1.74(d,j=3.9)33.03 151.413 36.04 122.1141.23(s)1.94(d,j=13.2)36.75 132.7155.92(dd,j=17.5,10.7)150.962.85(d,j=18.2)3.15(dd,j=18.2,6.6)36.9164.93(dd,j=10.7,1.3)5.02(dd,j=17.5,1.3)109.474.16(m)71.0171.03(s)22.981.81(dt,j=13.5,2.7)40.2192.14(s)11.5
9 36.0201.26(s)24.110 139.9
ꢀꢀꢀ
[0057]
结合1h nmr和
13
c nmr谱图,推测该化合物3可能含有1个苯环和1 对末端双键,推测余下的2个不饱和度为2个环所占有;结合上述谱图数据,推测该化合物3可能为一个芳香玫瑰烷型二萜化合物。
[0058]
在hmbc谱(图14)中,可观察到h-7 (δ
h 4.16)与c-5 (δ
c 132.7)、c-8 (δ
c 40.2)、c-11 (δ
c 36.3)的远程相关,证明了羟基与c-7位相连;此外,h
3-17 (δ
h 1.03)与c-12 (δ
c 33.0)、c-14 (δ
c 36.7)、c-15 (δ
c 150.9)的远程相关,h
3-19 (δ
h 2.14)与c-3 (δ
c 151.4)、c-4 (δ
c 122.1)、c-5 (δ
c 132.7)的远程相关,h
3-20 (δ
h 1.26)与c-8 (δ
c 40.2)、c-10 (δ
c 139.9)、c-11 (δ
c 36.3)的远程相关,证明了c-17位、c-19位和c-20位甲基的存在。
[0059]
在noesy谱(图15)中,h-8 (δ
h 3.38)与h-7 (δ
h 4.16)、h
3-17 (δ
h 1.08) 具有noe相关,h-15 (δ
h 5.92)与h
3-20 (δ
h 1.26)具有noe相关;因此,确定了化合物3的相对构型,7位氢、8位氢和17位甲基在同一平面上,为α位取代,15位氢与17 位甲基在另一平面,为β取代。
[0060]
综上所述,确定了化合物3(euphebracteolatin e)的结构如下:。
[0061]
实施例5本发明实施例提供了实施例1所制得的化合物4的物理性质和检测数据,具体如下:白色粉末,易溶于三氯甲烷、甲醇;-69.98(c 0.10,meoh)。
[0062]
uv (meoh)图谱(未示出)中λ
max = 206nm提示该化合物4为二萜类化合物,ir 谱图中(未示出)3442 cm
−1提示该结构含有羟基。根据高分辨质谱(hr-esi-ms,图16)m/z269.1892 [m h-h2o]
,(计算值269.1900),推测其分子量为286,确定其分子式为 c
19h26
o2,计算其不饱和度为7。
[0063]1h nmr (500 mhz, cdcl3)谱(图17)显示,在低场区存在5个烯氢信号[δ
h 7.09 (1h, d, j = 8.5 hz), 6.75 (1h, d, j = 8.5 hz), 5.88 (1h, dd, j = 17.5, 10.7 hz), 4.98 (1h, dd, j = 17.5, 1.3 hz), 4.90 (1h, dd, j = 10.7, 1.3 hz)];存在1个与氧相连的氢信号[δ
h 4.93 (1h, dd, j = 4.3, 1.7 hz)];高场区有3个甲基信号[δ
h 2.34, 1.08, 0.96 (each 3h, s)]。
[0064]
13
c nmr (125 mhz, cdcl3)谱(图18)显示共有19个碳信号,包括3个甲基碳信号(δ
c 23.2, 21.2, 11.3),4个亚甲基碳信号(δ
c 39.2, 35.4, 33.9, 33.1),1个次甲基碳信号(δ
c 31.1),1个连氧碳信号(δ
c 65.4),8个烯氢碳信号(δ
c 152.2, 151.1, 141.1, 136.0, 123.7, 123.4, 115.3, 109.1),以及2个季碳信号(δ
c 37.2, 36.7)。
[0065]1h nmr、
13
c nmr的信号归属如下表所示。
positionδh(multi,jinhz)δcpositionδh(multi,jinhz)δc17.089(d,j=8.5)123.4111.65(m)2.06(d,j=12.6)33.926.75(d,j=8.5)115.3121.72(d,j=3.9)1.42(dd,j=13.2,2.9)33.13 152.213 36.7
4 123.7141.22(m)1.51(d,j=13.2)39.25 136.0155.88(dd,j=17.5,10.7)151.164.93(dd,j=4.3,1.7)65.4164.90(dd,j=10.7,1.3)4.98(dd,j=17.5,1.3)109.171.69(t,j=2.2)1.92(td,j=13.7,4.3)35.4171.08(s)23.282.17(m)31.1192.34(s)11.39 37.2200.96(s)21.210 141.1
ꢀꢀꢀ
[0066]
结合1h nmr和
13
c nmr谱图,推测该化合物4可能含有1个苯环和1 对末端双键,推测余下的2个不饱和度为2个环所占有;结合上述谱图数据,推测该化合物4可能为一个芳香玫瑰烷型二萜化合物。
[0067]
在hmbc谱(图19)中,可观察到h-6 (δ
h 4.93)和c-4 (δ
c 123.7)、c-5 (δ
c 136.0)、c-10 (δ
c 141.1)的远程相关,证明了羟基与 c-6 位相连;此外,h
3-17 (δ
h 1.08)与c-12 (δ
c 33.1)、c-14 (δ
c 39.2)、c-15 (δ
c 151.1)的远程相关,h
3-19 (δ
h 2.34)与c-3 (δ
c 152.2)、c-4 (δ
c 123.7)、c-5 (δ
c 136.0)的远程相关,h
3-20 (δ
h 0.96)与c-8 (δ
c 31.1)、c-9 (δ
c 37.2)、c-10 (δ
c 141.1)的远程相关,证明c-17位、c-19位和c-20位甲基的存在。
[0068]
在noesy谱(图20)中,h-15 (δ
h 5.88)与h-6 (δ
h 4.93)、h
3-20 (δ
h 0.96) 具有noe相关,h-8 (δ
h 5.92)与h
3-17 (δ
h 1.08)具有noe相关;因此,确定了化合物4的相对构型,6位氢、15位氢和20位甲基在同一平面上,为α位取代,6位羟基、8位氢与17 位甲基在另一平面,为β取代。
[0069]
综上所述,确定了化合物4(euphebracteolatin f)的结构如下:。
[0070]
试验例本试验例公开了化合物1-4(euphebracteolatin c、euphebracteolatin d、euphebracteolatin e和euphebracteolatin f)的抗肿瘤活性试验。
[0071]
1、实验材料和仪器受试品:实施例1所制得的化合物1(euphebracteolatin c)、化合物2(euphebracteolatin d)、化合物3(euphebracteolatin e)和化合物4(euphebracteolatin f);实验细胞株及来源:肝癌细胞hepg2、乳腺癌细胞mcf-7和非小细胞肺癌细胞a549,均购自中国科学院细胞典藏库(上海)。
[0072]
2、实验方法2.1药物处理化合物euphebracteolatin c、euphebracteolatin d、euphebracteolatine和euphebracteolatin f,使用dmso溶解,配成浓度为0.01m的母液,储存于-20℃;临用时将其稀释为200、100、50、25、12.5、6.25、3.125 μm进行实验。
[0073]
选取顺铂(cisplatin)作为阳性对照药,按上述方法参照给药组配制成相应浓度的溶液;同时,设置dmso对照组和不含细胞的空白组。
[0074]
2.2 cck-8法的测定方法
取对数生长期的细胞,调整适当的细胞密度,接种于96孔板内,100 μl/well,培养于37℃、5% co2的培养箱内;培养24 h后,将药物稀释为200、100、50、25、12.5、6.25、3.125 μm五个浓度,100 μl/well,作用24 h。分设空白组、给药组,每组设6个复孔;再避光加入cck-8试剂10 μl,1.5h后利用酶标仪检测450 nm处吸光度值(a);最后以空白组a值为100%,计算各组细胞抑制率。
[0075]
细胞增殖抑制率(%)= [(a
对照-a
样品
)/ (a
对照-a
空白
)]
×
100%。
[0076]
2.3统计方法全部资料采用spss(13.0)统计软件进行检验分析;各组数据用均值
±
标准误(mean
±
s.e.)表示,采用one-way anova评价整体性差异,并进行dunnett 或dunnett’s t3 检验进行组间比较。
[0077]
3、实验结果表1 化合物对肿瘤细胞的ic
50
从表1的结果可以看出,化合物1-4(euphebracteolatin c、euphebracteolatin d、euphebracteolatine和euphebracteolatin f)作用24h之后对四种细胞株均具有较好的抑制作用,特别是对乳腺癌细胞t47d具有显著活性,其活性优于阳性药顺铂(cisplatin)。
[0078]
综上,本发明所述的玫瑰烷型二萜类化合物对肝癌细胞hepg2、乳腺癌细胞t47d和mcf-7及非小细胞肺癌细胞a549均具有明显的抑制作用,可用于开发抗肿瘤类药物,尤其针对临床化疗阶段药物。
[0079]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。
[0080]
应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。