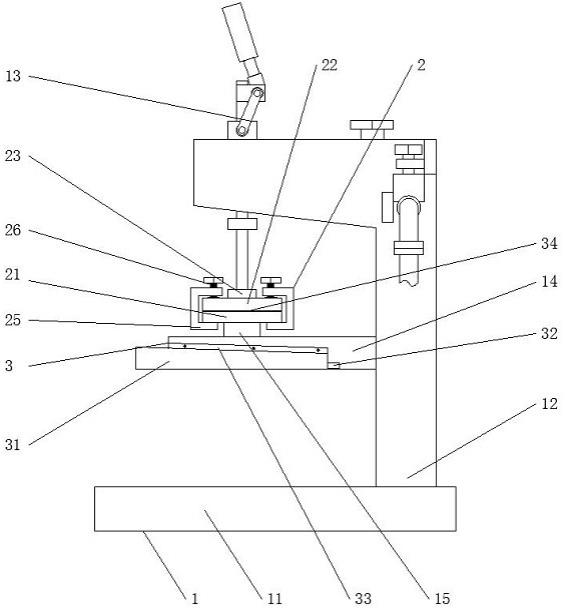
1.本发明属于传感器技术领域,尤其是涉及一种用于冠状病毒核酸检测的微电极及其制备方法与应用。
背景技术:
2.冠状病毒遗传物质是单条rna链,通过检测其rna序列中独一无二的特征序列,即可确定是否属于冠状病毒感染。目前,冠状病毒核酸的检测方法主要是作为金标准的普通聚酶链式反应及荧光定量聚酶链式反应,但这类检测方法对仪器、操作人员的专业性以及实验室环境都提出了很高的要求,且操作过程复杂,检测时间较长,容易出现假阴性结果,因此迫切需要开发简单高效、特异性高的冠状病毒核酸的检测方法。冠状病毒传染性强,传播速度快。由于冠状病毒是单链rna病毒,所以其变异速度快,因而导致症状更加不明显,更容易形成隐匿传播,导致更多的人患病。因此,需要建立快速检测确诊方法对阻断病毒传播和对疫情防控具有重要的作用。
技术实现要素:
3.本发明提供一种用于冠状病毒核酸检测的微电极及其制备方法与应用,从而克服了普通聚合酶链式反应及荧光定量聚合酶链式反应方法在冠状病毒核酸检测方面的不足。
4.本发明实现了准确定量检测冠状病毒核酸的目的,与目前检测病毒核酸所使用的普通聚合酶链式反应及荧光定量聚合酶链式反应方法相比,检测时间短,灵敏度高,特异性好,具有良好的应用前景。
5.本发明的目的可以通过以下技术方案来实现:
6.本发明提供一种用于冠状病毒核酸检测的微电极,该微电极包括绝缘衬底、制备于绝缘衬底上的微电极及导线,所述微电极包含工作电极,对电极和参比电极,在所述工作电极表面完全覆盖石墨烯,所述工作电极表面的石墨烯修饰固定dna探针;所述dna探针能够直接与待测冠状病毒核酸序列或能够和待测冠状病毒核酸特征序列逆转录后的dna通过碱基互补配对结合在一起,使dna探针上的电化学标签接触到所述微电极表面的石墨烯,发生氧化还原反应,产生电化学信号。基于是否出现电化学信号来实现检测冠状病毒核酸是否存在的目的。
7.在本发明的一个实施方式中,所述dna探针是在dna单链或三维核酸纳米结构上添加一条或多条用于与冠状病毒核酸序列互补配对的检测链以及位于检测链顶端的电化学标签,其中,三维核酸纳米结构通过寡核苷酸链互补配对自组装而成。
8.在本发明的一个实施方式中,所述冠状病毒核酸特征序列为编码非结构蛋白基因(orf1ab)、编码刺蛋白基因(s)、编码核壳蛋白基因(n)或编码包膜蛋白基因(e)中的一种或多种。
9.在本发明的一个实施方式中,所述电化学标签选自亚甲基蓝、二茂铁或普鲁士蓝中的一种或多种。
10.在本发明的一个实施方式中,在检测链与三维核酸纳米结构之间增加一段不与冠状病毒核酸序列或冠状病毒核酸序列逆转录后的dna配对的核酸单链,用以保证检测链可以多个自由度转动。
11.在本发明的一个实施方式中,所述dna探针通过共价键连接到所述工作电极表面的石墨烯。
12.在本发明的一个实施方式中,所述冠状病毒是在系统分类学中属套式病毒目,冠状病毒科,冠状病毒属的病毒,其基因组为线性单股正链的rna。
13.在本发明的一个实施方式中,所述工作电极、对电极和导线选自金属单质材料、导电硅化物、碳化物或导电高分子材料,其中金属单质材料包括金、银、铜、钛;所述参比电极为银/氯化银。
14.在本发明的一个实施方式中,所述工作电极表面完全覆盖有石墨烯,工作电极尺寸小于800微米。
15.在本发明的一个实施方式中,工作电极图案为中心对称图形,包括圆形、圆角正方形、圆角八边形,保证在工作电极表面电场的均一性。
16.在本发明的一个实施方式中,所述绝缘衬底采用二氧化硅材质。
17.在本发明的一个实施方式中,所述石墨烯为单层石墨烯。
18.本发明进一步提供用于冠状病毒核酸检测的微电极的制备方法,包括以下步骤:
19.步骤1:在绝缘衬底表面制备工作电极、参比电极、对电极和导线;
20.步骤2:将石墨烯转移到微电极表面,并利用光刻技术将石墨烯进行图案化,使石墨烯完全覆盖工作电极,将覆盖在对电极和参比电极表面的石墨烯去除,得到待修饰器件;
21.步骤3:将待修饰器件上加入连接分子溶液中0.5~2小时,使连接分子吸附到石墨烯表面,同时合成dna探针;
22.步骤4:在微电极上制造微量液体容器;
23.步骤5:在液体容器中加入dna探针溶液,使dna探针通过共价键与连接分子连接,静置2-10(优选为8-10)小时使dna探针修饰在石墨烯表面;
24.步骤6:修饰完成后,取出dna探针溶液,加入含镁离子的缓冲液,在常温下保存器件,得到所述用于冠状病毒核酸检测的微电极。
25.在本发明的一个实施方式中,步骤4中,所述微量液体容器的容量为20微升到1000微升,优选为80微升到100微升。
26.在本发明的一个实施方式中,步骤6中,所述缓冲液可以选择为含浓度为12.5mm镁离子的tm缓冲液。
27.另外,对于制备得到的所述用于冠状病毒核酸检测的微电极,在测试前,通过在工作电极上施加负电压,检测时,在微量液体容器里面加入待测样本,使其能够接触并覆盖工作电极表面的石墨烯,通过检测电化学电流变化实现冠状病毒核酸的高灵敏度检测。本发明还提供一种用于冠状病毒核酸检测的微电极非疾病诊断治疗目的的应用方法,
28.在测试前,微电极分别与电化学测试装置的接口进行电气连接,通过在工作电极上施加负电压,检测时,在微量液体容器里面加入待测样本,使其能够接触并覆盖工作电极表面的石墨烯,通过检测电化学电流变化实现冠状病毒核酸的高灵敏度检测。
29.在本发明的一个实施方式中,根据dna探针电化学标签的氧化还原电位设置相应
的电化学检测参数,包括电压扫描起始电压,终止电压,步进电压,脉冲电压;起始电压和终止电压根据电化学标签的氧化还原电位分别加减0.3伏特到0.5伏特,步进电压为0.005伏特到0.01伏特,脉冲电压为0.03伏特到0.08伏特。在测试前,通过在工作电极上施加-0.9伏特到-0.1伏特的负电压,使所述dna探针上的检测链以及电化学标签远离石墨烯,降低噪声。
30.在本发明的一个实施方式中,检测时,在电化学微电极的微量液体容器中,加入待测溶液,使得修饰在电化学微电极上的dna探针与待测溶液中的冠状病毒核酸序列或冠状病毒核酸逆转录后得到的dna互补配对结合;
31.在加入检测样本并孵育5到30分钟后,通过控制负电压的大小,调整施加排斥电场的强弱,将已与冠状毒核酸结合的检测链和未与冠状病毒核酸结合的检测链进行区分,使未与冠状病毒核酸结合的检测链顶端远离石墨烯,同时使与冠状病毒核酸结合的检测链顶端靠近石墨烯,提升检测灵敏度和精度;
32.检测过程中的电化学响应作为核酸检测的信号,即在电化学标签氧化还原电位附近出现氧化还原电流峰就可以判定为核酸阳性,在电化学标签氧化还原电位附近未出现氧化还原电流峰就可以判定为核酸阴性;
33.最后通过实时检测氧化还原电流的变化,通过浓度公式计算出冠状病毒核酸的浓度。
34.在本发明的一个实施方式中,出现氧化还原电流峰的标志为大于电化学标签氧化还原电位
±
0.2伏特所对应电流平均值的120%,包括120%。
35.在本发明的一个实施方式中,未出现氧化还原电流峰的标志为小于电化学标签氧化还原电位
±
0.2伏特所对应电流平均值的120%,不包括120%。
36.在本发明的一个实施方式中,在微量液体容器里面加入的待测样本为冠状病毒核酸样本。所述冠状病毒核酸样本是由采样的病毒标本处理后提取得到的,具体方法为:在病毒样本的采集管中抽取适量病毒标本,放入核酸提取试剂盒,接着将试剂盒放入自动或半自动核酸提取仪,从试剂盒中提取出冠状病毒核酸样本。
37.所述待测冠状病毒核酸序列逆转录后得到的dna序列,具体方法为:将提取出的冠状病毒核酸用逆转录试剂盒逆转录处理,处理方法为,使用逆转录试剂盒处理后加热退火,加热温度20~30摄氏度保持5~20分钟,随后加热温度35~45摄氏度保持1~2.5小时,最后80~90摄氏度保持2~10分钟,得到逆转录后的dna序列。
38.本发明中的微电极,是一种通过检测电化学电流信号变化的传感器件,具有高灵敏度和高选择性以及实时检测等优点。
39.与现有技术相比,本发明的优点在于:构建了一种用于冠状病毒核酸检测的微电极,作为一种新的方法来检测冠状病毒核酸,其原理为,通过设计合成各种不同结构的dna探针与冠状病毒核酸序列或冠状病毒核酸基因的逆转录dna序列互补杂交引起电化学电流的变化来实现实时检测,通过控制负电压的大小,调整施加排斥电场的强弱,提升灵敏度和准确度,同时具有操作简便、特异性好、响应时间短、可集成化、低成本等优点。
附图说明
40.图1是本发明实施例1中电化学微电极表面示意图以及与电化学测试装置连接示
意图;
41.图2是本发明实施例1中由样本提取的新型冠状病毒sars-cov-2核酸的差分脉冲伏安法电流响应曲线;
42.图3是本发明实施例5中由样本提取的新型冠状病毒sars-cov-2核酸的方波伏安法电流响应曲线。
具体实施方式
43.下面结合附图和具体实施例对本发明进行详细说明。
44.实施例1
45.本实施例提供一种具体的用于冠状病毒核酸检测的微电极及其制备方法与非疾病诊断治疗目的的应用
46.首先,首先通过热蒸镀技术制备铬/金(5/40纳米)导线、工作电极(圆形,半径200微米)和对电极(环绕工作电极)以及银(40纳米)电极(位于工作电极左侧),随后通过滴涂法在银电极上获得银/氯化银参比电极,最终得到电化学微电极。
47.利用化学气相沉积法在25微米厚的铜箔上制备单层石墨烯,采用化学刻蚀法将制得的石墨烯转移到电化学微电极表面。
48.采用紫外光刻法以及氧等离子刻蚀技术制备图案化电极,然后,将石墨烯电化学微电极浸泡到苯甲酸n-羟基琥珀酰亚胺酯溶液中0.5~2小时后,用超纯水冲洗干净,该分子一端的芘基团通过π-π堆叠作用吸附到电化学微电极表面。
49.制作微量液体容器放置在石墨烯工作电极上,微量液体容器的容量大约为400-500微升。
50.设计一种基于dna四面体纳米结构探针,该dna四面体纳米结构顶端上有一条用于与新型冠状病毒sars-cov-2核酸结合的检测链,检测链顶端为亚甲基蓝,在检测链与三维核酸纳米结构之间增加一段不与冠状病毒核酸序列配对的核酸单链,保证检测链可以多个自由度转动。该探针由四条dna单链通过碱基互补配对自组装而成,合成该dna探针的方法是将dna混合液加热到95摄氏度保持5分钟,随后在1分钟内匀速降温至15摄氏度,最后置于4摄氏度保存。随后,将该dna探针溶液置于微量液体容器中,dna探针底座上连接的氨基可以与n-羟基琥珀酰亚胺基团结合将dna探针固定在石墨烯电化学微电极表面的界面上,所需时间约为8-10小时,随后用超纯水冲洗干净。
51.将样本进行处理提取病毒核酸,提取方法为在样本的采集管中抽取200微升的样本,放入核酸提取试剂盒,接着将试剂盒放入自动或半自动核酸提取仪,提取得到新型冠状病毒sars-cov-2核酸置于4摄氏度保存。
52.在测试前,通过在工作电极上施加-0.7伏特的电压保持dna探针上的检测链以及电化学标签远离石墨烯,降低噪声。设置可以使亚甲基蓝产生反应的电化学测试参数,初始电压-0.6伏特,终止电压-0.2伏特,步进电压0.005伏特,脉冲电压0.05伏特。加入80微升待测溶液,使得修饰在电化学微电极上的dna探针与待测溶液中的冠状病毒核酸序列互补配对结合。在加入检测样本并完成孵育30分钟后,通过控制负电压的大小,调整施加排斥电场的强弱,将已与冠状毒核酸结合的检测链和未与冠状病毒核酸结合的检测链进行区分,使未与冠状病毒核酸结合的检测链顶端远离石墨烯,同时使与冠状病毒核酸结合的检测链顶
端靠近石墨烯,提升检测灵敏度和精度,最低检测浓度为5拷贝数/微升。
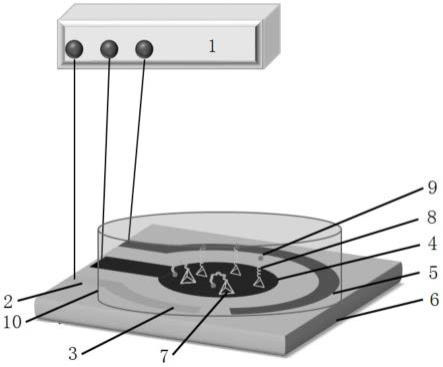
53.图1是实施例1中电化学微电极表面示意图以及与电化学测试装置连接示意图。
54.图1中,电化学测试装置1通过导线2和参比电极3、工作电极4、对电极5相连接,其中,导线2、参比电极3、工作电极4、对电极5都制备于绝缘衬底6上,在所述工作电极4表面完全覆盖石墨烯,所述工作电极4表面的石墨烯修饰固定dna探针7;其中,所述dna探针7是在三维核酸纳米结构上添加多条用于与冠状病毒核酸序列互补配对的检测链8以及位于检测链8顶端的电化学标签9,其中,三维核酸纳米结构通过寡核苷酸链互补配对自组装而成。微量液体容器10放置在石墨烯工作电极4上,微量液体容器的容量大约为80-100微升。
55.图2是实施例1中由样本提取的新型冠状病毒sars-cov-2核酸的差分脉冲伏安法电流响应曲线。
56.实施例2
57.本实施例提供一种具体的用于冠状病毒核酸检测的微电极及其制备方法与非疾病诊断治疗目的的应用
58.首先,首先通过热蒸镀技术制备铬/金(5/40纳米)导线、工作电极(圆角正方形,长和宽均为300微米)和对电极(环绕工作电极)以及银(40纳米)电极(位于工作电极左侧),随后通过滴涂法在银电极上获得银/氯化银参比电极,最终得到电化学微电极。
59.利用化学气相沉积法在25微米厚的铜箔上制备单层石墨烯,采用化学刻蚀剥离法将制得的石墨烯转移到电化学微电极表面。
60.采用紫外光刻法以及氧等离子刻蚀技术制备图案化电极,然后,将石墨烯电化学微电极浸泡到苯甲酸n-羟基琥珀酰亚胺酯溶液中0.5~2小时后,用超纯水冲洗干净,该分子一端的芘基团通过π-π堆叠作用吸附到电化学微电极表面。
61.制作微量液体容器放置在石墨烯工作电极上,微量液体容器的容量大约为100-200微升。
62.设计一种基于dna棱柱的纳米结构,在dna棱柱的三个顶端分别有用于sars病毒核酸检测的编码非结构蛋白基因(orf1ab)、编码刺蛋白基因(s)和编码核壳蛋白基因(n)逆转录dna结合的检测链,检测链顶端修饰有亚甲基蓝,在检测链与三维核酸纳米结构之间增加一段不与冠状病毒核酸序列逆转录后的dna配对的核酸单链,保证检测链可以多个自由度转动。该探针由九条dna单链通过碱基互补配对自组装而成,合成该dna探针的方法是将dna混合液加热到95摄氏度保持5分钟,随后在1分钟内匀速降温至15摄氏度,最后置于4摄氏度保存。然后,将该dna探针溶液置于微量液体容器中,dna探针底座上连接的氨基可以与n-羟基琥珀酰亚胺基团结合将dna探针固定在石墨烯电化学微电极表面的界面上,所需时间约为8-10小时,随后用超纯水冲洗干净。
63.将样本进行处理提取病毒核酸,将提取出的sars病毒核酸用逆转录试剂盒逆转录处理,处理方法为,使用逆转录试剂盒处理后加热退火,加热温度20~30摄氏度保持5~20分钟,随后加热温度35~45摄氏度保持1~2.5小时,最后80~90摄氏度保持2~10分钟,提取得到sars病毒核酸逆转录后得到的dna序列置于4摄氏度保存。
64.在测试前,通过在工作电极上施加-0.8伏特的电压保持dna探针上的检测链以及电化学标签远离石墨烯,降低噪声。设置可以使亚甲基蓝产生反应的电化学测试参数,使用方波伏安法,初始电压-0.7伏特,终止电压-0.1伏特,步进电压0.005伏特,脉冲电压0.05伏
特。加入150微升待测溶液,使得修饰在电化学微电极上的dna探针与待测溶液中的冠状病毒核酸序列逆转录后得到的dna互补配对结合。在加入检测样本并完成孵育30分钟后,通过控制负电压的大小,调整施加排斥电场的强弱,将已与逆转录后得到的dna结合的检测链和未与逆转录后得到的dna结合的检测链进行区分,使未与逆转录后得到的dna结合的检测链顶端远离石墨烯,同时使与逆转录后得到的dna结合的检测链顶端靠近石墨烯,提升检测灵敏度和精度。最终该款微电极对标本提取的sars病毒核酸具有高灵敏度响应,检测限为0.5拷贝数/微升。
65.实施例3
66.本实施例提供一种具体的用于冠状病毒核酸检测的微电极及其制备方法与非疾病诊断治疗目的的应用
67.首先,首先通过热蒸镀技术制备铬/金(5/40纳米)导线、工作电极(圆角八边形,长和宽均为400微米)和对电极(环绕工作电极)以及银(40纳米)电极(位于工作电极左侧),随后通过滴涂法在银电极上获得银/氯化银参比电极,最终得到电化学微电极。
68.利用化学气相沉积法在25微米厚的铜箔上制备单层石墨烯,采用电化学剥离法将制得的石墨烯转移到电化学微电极表面。
69.采用紫外光刻法以及氧等离子刻蚀技术制备图案化电极,然后,将石墨烯电化学微电极浸泡到苯甲酸n-羟基琥珀酰亚胺酯溶液中0.5~2小时后,用超纯水冲洗干净,该分子一端的芘基团通过π-π堆叠作用吸附到电化学微电极表面。
70.制作微量液体容器放置在石墨烯工作电极上,微量液体容器的容量大约为500-1000微升。
71.设计一种基于dna正方体结构,在dna正方体的四个顶点分别有用于检测中东呼吸综合症病毒的编码非结构蛋白基因(orf1ab)、编码包膜蛋白基因(e)、编码刺蛋白基因(s)和编码核壳蛋白基因(n)结合的检测链,检测链顶端修饰有二茂铁,在检测链与三维核酸纳米结构之间增加一段不与冠状病毒核酸序列逆转录后的dna配对的核酸单链,保证检测链可以多个自由度转动。该探针由十二条dna单链通过碱基互补配对自组装而成,合成该dna探针的方法是将dna混合液加热到95摄氏度保持5分钟,随后在1分钟内匀速降温至15摄氏度,最后置于4摄氏度保存。然后,将该dna探针溶液置于微量液体容器中,dna探针底座上连接的氨基可以与n-羟基琥珀酰亚胺基团结合将dna探针固定在石墨烯电化学微电极表面的界面上,所需时间约为8-10小时,随后用超纯水冲洗干净。
72.将样本进行处理提取病毒核酸,提取方法为在样本的采集管中抽取200微升的样本,放入核酸提取试剂盒,接着将试剂盒放入自动或半自动核酸提取仪,提取得到中东呼吸综合症病毒核酸,将提取出的冠状病毒核酸用逆转录试剂盒逆转录处理,处理方法为,使用逆转录试剂盒处理后加热退火,加热温度20~30摄氏度保持5~20分钟,随后加热温度35~45摄氏度保持1~2.5小时,最后80~90摄氏度保持2~10分钟,提取得到中东呼吸综合症病毒核酸逆转录后得到的dna序列置于4摄氏度保存。
73.在测试前,通过在工作电极上施加
‑‑
0.4伏特的电压保持dna探针上的检测链以及电化学标签远离石墨烯,降低噪声。设置可以使二茂铁产生反应的电化学测试参数,使用差分脉冲伏安法,初始电压0伏特,终止电压0.6伏特,步进电压0.005伏特,脉冲电压0.05伏特。加入800微升待测溶液,使得修饰在电化学微电极上的dna探针与待测溶液中的冠状病
毒核酸逆转录后得到的dna互补配对结合。在加入检测样本并完成孵育30分钟后,通过控制负电压的大小,调整施加排斥电场的强弱,将已与逆转录后得到的dna结合的检测链和未与逆转录后得到的dna结合的检测链进行区分,使未与逆转录后得到的dna结合的检测链顶端远离石墨烯,同时使与逆转录后得到的dna结合的检测链顶端靠近石墨烯,提升检测灵敏度和精度。最终该款微电极对标本提取的中东呼吸综合症病毒核酸具有高灵敏度响应,检测限为0.1拷贝数/微升。
74.实施例4
75.本实施例提供一种具体的用于冠状病毒核酸检测的微电极及其制备方法与非疾病诊断治疗目的的应用
76.首先,首先通过喷墨打印技术制备金(1000纳米)导线、工作电极(圆形,半径为400微米)和对电极(环绕工作电极)以及银/氯化银参比电极,最终得到电化学微电极。
77.利用化学气相沉积法在25微米厚的铜箔上制备单层石墨烯,采用化学刻蚀法将制得的石墨烯转移到电化学微电极表面。
78.采用紫外光刻法以及氧等离子刻蚀技术制备图案化电极,然后,将石墨烯电化学微电极浸泡到苯甲酸n-羟基琥珀酰亚胺酯溶液中0.5~2小时后,用超纯水冲洗干净,该分子一端的芘基团通过π-π堆叠作用吸附到电化学微电极表面。
79.制作微量液体容器放置在石墨烯工作电极上,微量液体容器的容量大约为10-50微升。
80.设计一种基于dna十二面体结构,在dna正方体的四个顶点分别有用于sars病毒核酸检测的编码非结构蛋白基因(orf1ab)、编码包膜蛋白基因(e)、编码刺蛋白基因(s)和编码核壳蛋白基因(n)结合的检测链,检测链顶端修饰有普鲁士蓝,在检测链与三维核酸纳米结构之间增加一段不与冠状病毒核酸序列配对的核酸单链,保证检测链可以多个自由度转动。该探针由十二条dna单链通过碱基互补配对自组装而成,合成该dna探针的方法是将dna混合液加热到95摄氏度保持5分钟,随后在1分钟内匀速降温至15摄氏度,最后置于4摄氏度保存。然后,将该dna探针溶液置于微量液体容器中,dna探针底座上连接的氨基可以与n-羟基琥珀酰亚胺基团结合将dna探针固定在石墨烯电化学微电极表面的界面上,所需时间约为8-10小时,随后用超纯水冲洗干净。
81.将样本进行处理提取病毒核酸,提取方法为在样本的采集管中抽取200微升的样本,放入核酸提取试剂盒,接着将试剂盒放入自动或半自动核酸提取仪,提取得到sars病毒核酸置于4摄氏度保存。在测试前,通过在工作电极上施加-0.5伏特的电压保持dna探针上的检测链以及电化学标签远离石墨烯,降低噪声。设置可以使普鲁士蓝产生反应的电化学测试参数,使用方波伏安法,初始电压0伏特,终止电压0.6伏特,步进电压0.005伏特,脉冲电压0.05伏特。加入40微升待测溶液,使得修饰在电化学微电极上的dna探针与待测溶液中的冠状病毒核酸序列互补配对结合。在加入检测样本并完成孵育30分钟后,通过控制负电压的大小,调整施加排斥电场的强弱,将已与冠状毒核酸结合的检测链和未与冠状病毒核酸结合的检测链进行区分,使未与冠状病毒核酸结合的检测链顶端远离石墨烯,同时使与冠状病毒核酸结合的检测链顶端靠近石墨烯,提升检测灵敏度和精度。最终该款微电极对标本提取的sars病毒核酸具有高灵敏度响应,检测限为0.1拷贝数/微升。
82.实施例5
83.本实施例提供一种具体的用于冠状病毒核酸检测的微电极及其制备方法与非疾病诊断治疗目的的应用
84.首先,首先通过喷墨打印技术制备铬/金(5/40纳米)导线、叉指电极(长度1000微米宽度20微米)以及银/氯化银参比电极(位于叉指电极下方),最终得到电化学微电极。
85.利用化学气相沉积法在25微米厚的铜箔上制备单层石墨烯,采用化学刻蚀法将制得的石墨烯转移到电化学微电极表面。
86.采用紫外光刻法以及氧等离子刻蚀技术制备图案化电极,然后,将石墨烯电化学微电极浸泡到苯甲酸n-羟基琥珀酰亚胺酯溶液中0.5~2小时后,用超纯水冲洗干净,该分子一端的芘基团通过π-π堆叠作用吸附到电化学微电极表面。
87.制作微量液体容器放置在石墨烯工作电极上,微量液体容器的容量大约为80-100微升。
88.设计一种基于dna四面体纳米结构探针,该dna四面体纳米结构顶端上有一条用于与新型冠状病毒sars-cov-2核酸结合的检测链,检测链顶端为亚甲基蓝,在检测链与三维核酸纳米结构之间增加一段不与冠状病毒核酸序列配对的核酸单链,保证检测链可以多个自由度转动。该探针由四条dna单链通过碱基互补配对自组装而成,合成该dna探针的方法是将dna混合液加热到95摄氏度保持5分钟,随后在1分钟内匀速降温至15摄氏度,最后置于4摄氏度保存。随后,将该dna探针溶液置于微量液体容器中,dna探针底座上连接的氨基可以与n-羟基琥珀酰亚胺基团结合将dna探针固定在石墨烯电化学微电极表面的界面上,所需时间约为8-10小时,随后用超纯水冲洗干净。
89.将样本进行处理提取病毒核酸,提取方法为在样本的采集管中抽取200微升的样本,放入核酸提取试剂盒,接着将试剂盒放入自动或半自动核酸提取仪,提取得到新型冠状病毒sars-cov-2核酸置于4摄氏度保存。
90.在测试前,通过在工作电极上施加-0.7伏特的电压保持dna探针上的检测链以及电化学标签远离石墨烯,降低噪声。设置可以使亚甲基蓝产生反应的电化学测试参数,使用方波伏安法,初始电压-0.7伏特,终止电压-0.1伏特,步进电压0.005伏特,脉冲电压0.05伏特。加入80微升待测溶液,使得修饰在电化学微电极上的dna探针与待测溶液中的冠状病毒核酸序列互补配对结合。在加入检测样本并完成孵育30分钟后,通过控制负电压的大小,调整施加排斥电场的强弱,将已与冠状毒核酸结合的检测链和未与冠状病毒核酸结合的检测链进行区分,使未与冠状病毒核酸结合的检测链顶端远离石墨烯,同时使与冠状病毒核酸结合的检测链顶端靠近石墨烯,提升检测灵敏度和精度。最终该款微电极对标本提取的新型冠状病毒sars-cov-2核酸具有高灵敏度响应,检测限为0.05拷贝数/微升。
91.图3是实施例5中由样本提取的新型冠状病毒sars-cov-2核酸的方波伏安法电流响应曲线。
92.实施例6
93.本实施例提供一种具体的用于冠状病毒核酸检测的微电极及其制备方法与非疾病诊断治疗目的的应用
94.首先,首先通过喷墨打印技术制备铬/金(5/40纳米)导线、叉指电极(长度1000微米宽度20微米)以及银/氯化银参比电极(位于叉指电极下方),最终得到电化学微电极。
95.利用化学气相沉积法在25微米厚的铜箔上制备单层石墨烯,采用化学刻蚀法将制
得的石墨烯转移到电化学微电极表面。
96.采用紫外光刻法以及氧等离子刻蚀技术制备图案化电极,然后,将石墨烯电化学微电极浸泡到苯甲酸n-羟基琥珀酰亚胺酯溶液中0.5~2小时后,用超纯水冲洗干净,该分子一端的芘基团通过π-π堆叠作用吸附到电化学微电极表面。
97.制作微量液体容器放置在石墨烯工作电极上,微量液体容器的容量大约为200-300微升。
98.设计一种基于dna四面体纳米结构探针,该dna四面体纳米结构顶端上有一条用于与中东呼吸综合症病毒核酸结合的检测链,检测链顶端为亚甲基蓝,在检测链与三维核酸纳米结构之间增加一段不与冠状病毒核酸序列配对的核酸单链,保证检测链可以多个自由度转动。该探针由四条dna单链通过碱基互补配对自组装而成,合成该dna探针的方法是将dna混合液加热到95摄氏度保持5分钟,随后在1分钟内匀速降温至15摄氏度,最后置于4摄氏度保存。随后,将该dna探针溶液置于微量液体容器中,dna探针底座上连接的氨基可以与n-羟基琥珀酰亚胺基团结合将dna探针固定在石墨烯电化学微电极表面的界面上,所需时间约为8-10小时,随后用超纯水冲洗干净。
99.将样本进行处理提取病毒核酸,提取方法为在样本的采集管中抽取200微升的样本,放入核酸提取试剂盒,接着将试剂盒放入自动或半自动核酸提取仪,提取得到中东呼吸综合症病毒核酸置于4摄氏度保存。
100.在测试前,通过在工作电极上施加-0.7伏特的电压保持dna探针上的检测链以及电化学标签远离石墨烯,降低噪声。设置可以使亚甲基蓝产生反应的电化学测试参数,使用方波伏安法,初始电压-0.7伏特,终止电压-0.1伏特,步进电压0.005伏特,脉冲电压0.05伏特。加入200微升待测溶液,使得修饰在电化学微电极上的dna探针与待测溶液中的冠状病毒核酸序列互补配对结合。在加入检测样本并完成孵育30分钟后,通过控制负电压的大小,调整施加排斥电场的强弱,将已与冠状毒核酸结合的检测链和未与冠状病毒核酸结合的检测链进行区分,使未与冠状病毒核酸结合的检测链顶端远离石墨烯,同时使与冠状病毒核酸结合的检测链顶端靠近石墨烯,提升检测灵敏度和精度。最终该款微电极对标本提取的中东呼吸综合症病毒核酸具有高灵敏度响应,检测限为0.05拷贝数/微升。
101.基于以上实施例1-6方案检测的病毒以及检测的定性结果如表1所示。
102.表1实施例1-6方案检测的病毒以及检测的定性结果
[0103][0104]
通过以上实施例,证实了本发明能够准确定量检测冠状病毒核酸,与目前检测病毒核酸所使用的普通聚合酶链式反应及荧光定量聚合酶链式反应方法相比,本发明提供的
技术方案检测时间短,灵敏度高,特异性好,具有良好的应用前景。
[0105]
上述的对实施例的描述是为便于该技术领域的普通技术人员能理解和使用发明。熟悉本领域技术的人员显然可以容易地对这些实施例做出各种修改,并把在此说明的一般原理应用到其他实施例中而不必经过创造性的劳动。因此,本发明不限于上述实施例,本领域技术人员根据本发明的揭示,不脱离本发明范畴所做出的改进和修改都应该在本发明的保护范围之内。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。