1.本发明涉及含氟嘧啶化合物及其制造方法。
背景技术:
2.一直以来,报道了含氟嘧啶化合物具有各种生物活性。其中,关于在嘧啶环2位具有咪唑环等作为取代基的化合物,有望在医药/农药领域中使用。
3.更具体而言,在非专利文献1中公开了在嘧啶环2位具有咪唑环的化合物。非专利文献1报道了在嘧啶环2位具有1-甲基咪唑基、在嘧啶环5位具有2,4,6-三氟苯基的化合物具有人结肠癌细胞(colo205细胞)的增殖抑制活性。
4.另一方面,作为在嘧啶环5位具有三氟甲基、在4位和6位具有取代基的嘧啶化合物的合成法,例如已知有非专利文献2~4中公开的方法。具体而言,非专利文献2分别报道了使用三氟甲烷亚磺酸钠(langlois试剂)的合成法;非专利文献3中报道了使用三氟乙酸衍生物的合成法;非专利文献4中报道了使用了三氟甲磺酸酐的合成法。
5.在先技术文献
6.非专利文献
7.非专利文献1:生物有机与药物化学(bioorganic&medicinal chemistry),2009年,第17卷,第111~118页;
8.非专利文献2:四面体(tetrahedron),2016年,第72卷,第3250~3255页;
9.非专利文献3:acs催化(acs catalysis),2018年,第8卷,第2839~2843页;
10.非专利文献4:德国应用化学(angewandte chemie international edition),2018年,第57卷,第6926~6929页。
技术实现要素:
11.发明要解决的问题
12.然而,以往,从反应性和选择性的方面出发,制造在嘧啶环5位具有含氟取代基、在2位具有杂环作为取代基、在4位和6位具有取代基的含氟嘧啶化合物是困难的,没有报道这样的含氟嘧啶化合物。期望该含氟嘧啶化合物具有各种生物活性,期望确立在嘧啶环4位和6位具有取代基、在2位具有杂环作为取代基的新型含氟嘧啶化合物及其制造方法。
13.在非专利文献2所报道的制造方法中,由于导入三氟甲基时的位置选择性低,因此对于取代有杂环的嘧啶化合物这样的具有多个杂环的底物,存在三氟甲基导入效率降低或三氟甲基的导入变困难的可能。此外,相对于底物,不仅使用3倍量langlois试剂作为三氟甲基化剂,而且还使用底物3倍量的有害乙酸锰(iii)水合物作为氧化剂,因此也需要考虑环境上的问题。
14.考虑到:对通过非专利文献3和4中报道的制造方法得到的化合物进行进一步的修饰/衍生化,由此转化为该含氟嘧啶化合物。然而,有时无法避免工序数增加导致的复杂化和效率降低,或者该含氟嘧啶化合物的制造本身困难。此外,需要在钌络合物催化剂存在下
进行光照射,在非专利文献3中,需要相对于底物使用2.5~3倍量的三氟甲基化剂,在非专利文献4中,由于需要相对于底物使用3倍量的三氟甲基化剂,因此认为不适于实用。
15.解决问题的手段
16.因此,本发明人得到如下见解:通过使特定的原料反应,能够在嘧啶环上两个氮原子之间的2位导入规定的唑类结构,从而完成了本发明。即,本发明提供在以往未知的、在嘧啶环4位和6位具有取代基、2位具有唑类结构作为取代基的新型含氟嘧啶化合物、以及能够简易地制造该含氟嘧啶化合物的制造方法。
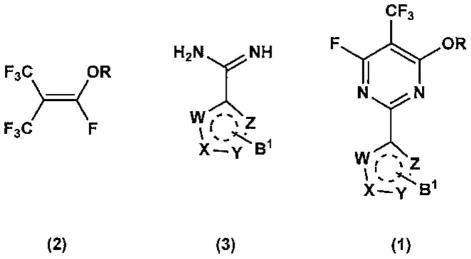
17.本发明的实施方式所述的含氟嘧啶化合物由下述通式(1)表示。
18.[化学式1]
[0019][0020]
上述通式(1)中,
[0021]
r表示碳原子数为1~12的烃基,
[0022]
b1表示氢原子、卤素原子、碳原子数为1~10的烃基、-c
nf2n 1
(n为1~10的整数)、硝基、硼酸基、-oa1、-soma1(m为0~3的整数)、-na1a2、-cooa1或-cona1a2,
[0023]
w、x、y和z各自独立地表示cv或n,其中,w、x、y和z中的至少一个为n,n可以具有取代基,
[0024]
v表示氢原子、卤素原子、碳原子数为1~10的烃基、-c
nf2n 1
(n为1~10的整数)、硝基、硼酸基、-oa1、-soma1(m为0~3的整数)、-na1a2、-cooa1或-cona1a2,
[0025]
a1和a2各自独立地表示氢原子、或碳原子数为1~10的烃基。
[0026]
本发明的实施方式所述的含氟嘧啶化合物的制造方法包括:
[0027]
通过使下述通式(2)所示的氟异丁烯衍生物与下述通式(3)所示的化合物或其盐反应而得到下述通式(1)的含氟嘧啶化合物的工序,
[0028]
[化学式2]
[0029][0030]
上述通式(1)~(3)中,
[0031]
r表示碳原子数为1~12的烃基,
[0032]
b1表示氢原子、卤素原子、碳原子数为1~10的烃基、-c
nf2n 1
(n为1~10的整数)、硝
基、硼酸基、-oa1、-soma1(m为0~3的整数)、-na1a2、-cooa1或-cona1a2,
[0033]
w、x、y和z各自独立地表示cv或n,其中,w、x、y和z中的至少一个为n,n可以具有取代基,
[0034]
v表示氢原子、卤素原子、碳原子数为1~10的烃基、-c
nf2n 1
(n为1~10的整数)、硝基、硼酸基、-oa1、-soma1(m为0~3的整数)、-na1a2、-cooa1或-cona1a2,
[0035]
a1和a2各自独立地表示氢原子、或碳原子数为1~10的烃基。
[0036]
本发明的其它实施方式所述的含氟嘧啶化合物的制造方法包括:
[0037]
通过使下述通式(4)所示的氟异丁烷衍生物与下述通式(3)所示的化合物或其盐反应而得到下述通式(1)的含氟嘧啶化合物的工序,
[0038]
[化学式3]
[0039][0040]
上述通式(1)、(3)或(4)中,
[0041]
q表示卤素原子、-oa1、-soma1(m为0~3的整数)或-na1a2,
[0042]
r表示碳原子数为1~12的烃基,
[0043]
b1表示氢原子、卤素原子、碳原子数为1~10的烃基、-c
nf2n 1
(n为1~10的整数)、硝基、硼酸基、-oa1、-soma1(m为0~3的整数)、-na1a2、-cooa1或-cona1a2,
[0044]
w、x、y和z各自独立地表示cv或n,其中,w、x、y和z中的至少一个为n,n可以具有取代基,
[0045]
v表示氢原子、卤素原子、碳原子数为1~10的烃基、-c
nf2n 1
(n为1~10的整数)、硝基、硼酸基、-oa1、-soma1(m为0~3的整数)、-na1a2、-cooa1或-cona1a2,
[0046]
a1和a2各自独立地表示氢原子、或碳原子数为1~10的烃基。
[0047]
在本发明的一个实施方式中,所述r是碳原子数为1~10的烷基。
[0048]
发明效果
[0049]
根据本发明,可以提供一种在嘧啶环4位和6位具有取代基、在2位具有唑类结构的新型含氟嘧啶化合物、以及能够简单地制造该含氟嘧啶化合物的制造方法。
具体实施方式
[0050]
以下,对本发明的实施方式进行详细说明。然而,本发明的范围并不局限于以下说明的具体例。
[0051]
(含氟嘧啶化合物)
[0052]
本实施方式中的含氟嘧啶化合物由下述通式(1)所示,在嘧啶环4位、5位和6位上分别具有特定的取代基(-or、-cf3、-f),在2位具有唑类结构。嘧啶环与具有规定的唑类结构的取代基键合,具体而言,存在于嘧啶环上两个氮原子之间的碳原子与存在于唑类结构
中的碳原子键合。即,存在于唑类结构中的氮原子与存在于嘧啶环上两个氮原子之间的碳原子未直接键合。
[0053]
[化学式4]
[0054][0055]
r只要是碳原子数为1~12的由碳原子和氢原子构成的烃基就不受到特别限定,可以举出链状烃基、芳香族烃基、脂环式烃基等。链状烃基只要总碳原子数为1~12就不受到特别限定,可以为直链状烃基,也可以为分支的链状烃基。r为芳香族烃基的情况下,芳香族烃基只要总碳原子数为6~12就不受到特别限定,可以为具有取代基的芳香族烃基,也可以为不具有取代基的芳香族烃基。此外,芳香族烃基可以具有稠合多环结构。r为脂环式烃基时,脂环式烃基只要总碳原子数为3~12就不受到特别限定,可以为具有取代基的脂环式烃基,也可以为不具有取代基的脂环式烃基。此外,脂环式烃基可以具有桥环结构。
[0056]
作为链状烃基,可以举出:甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、戊基、己基、庚基、辛基、壬基、癸基、十一烷基、十二烷基等烷基;
[0057]
乙烯基、丙烯基、丁烯基、戊烯基、己烯基、庚烯基、辛烯基、壬烯基、癸烯基、十一碳烯基、十二碳烯基等烯基;
[0058]
乙炔基、丙炔基、丁炔基、戊炔基、己炔基、庚炔基、丁炔基、壬炔基、癸炔基、十一炔基、十二炔基等炔基等。
[0059]
作为芳香族烃基,可举出苯基、萘基。
[0060]
作为脂环式烃基,可举出饱和或不饱和的环状烃基,作为环状烃基的示例,可举出环丙基、环丁基、环己基、环戊基、金刚烷基、降冰片基等。
[0061]
r优选为碳原子数为1~10的烷基。通过使r为碳原子数为1~10的烷基,可以容易地制备作为含氟嘧啶化合物原料的通式(2)的氟代异丁烯衍生物和通式(4)的氟异丁烷衍生物。
[0062]
b1表示氢原子、卤素原子、碳原子数为1~10的烃基、-c
nf2n 1
(n为1~10的整数)、硝基、硼酸基、-oa1、-soma1(m为0~3的整数)、-na1a2、-cooa1或-cona1a2,优选表示氢原子、卤素原子、碳原子数为1~10的烃基、-c
nf2n 1
、硝基、-oa1、-soma1或-cooa1。
[0063]
b1中,卤素原子为f、cl、br或i,优选为f或cl。
[0064]
b1中,碳原子数为1~10的烃基只要是由碳原子和氢原子构成的烃基就不受到特别限定,例如在上述r中可以是碳原子数为1~10的烃基。
[0065]
b1中,-c
nf2n 1
只要是由碳原子和氟原子构成的全氟烷基就不受到特别限定,可以为直链状,也可以为支链状。另外,n为1~10的整数,优选为1~3的整数。
[0066]
b1中,-oa1、-soma1中所含的a1表示氢原子、或碳原子数为1~10的烃基。在a1表示碳原子数为1~10的烃基的情况下,例如在上述r中可以是碳原子数为1~10的烃基。此外,m为
0~3的整数,优选为0~2的整数。
[0067]
b1中,-na1a2中所含的a1和a2各自独立地表示氢原子、或碳原子数为1~10的烃基。a1和a2各自可以相同,也可以不同。a1和a2表示碳原子数为1~10的烃基的情况下,例如在上述r中可以是碳原子数为1~10的烃基。
[0068]
b1中,-cooa1中所含的a1表示氢原子、或碳原子数为1~10的烃基。在a1表示碳原子数为1~10的烃基的情况下,例如在上述r中可以是碳原子数为1~10的烃基。
[0069]
b1中,-cona1a2中所含的a1和a2各自独立地表示氢原子、或碳原子数为1~10的烃基。a1和a2各自可以相同,也可以不同。a1和a2表示碳原子数为1~10的烃基的情况下,例如在上述r中可以是碳原子数为1~10的烃基。
[0070]
w、x、y和z各自独立地表示cv或n。其中,w、x、y和z中的至少一个为n,n可以具有取代基。即,w、x、y和z中的至少一个为取代或未取代的n。w、x、y和z中的至少一个为cv时,v表示氢原子、卤素原子、碳原子数为1~10的烃基、-c
nf2n 1
(n为1~10的整数)、硝基、硼酸基、-oa1、-soma1(m为0~3的整数)、-na1a2、-cooa1或-cona1a2,优选表示氢原子、卤素原子、碳原子数为1~10的烃基、-c
nf2n 1
、硝基、-oa1、-soma1或-cooa1。w、x、y和z中的至少两个优选为取代或未取代的n。n具有取代基的情况下,作为取代基,优选为碳原子数为1~20的烃基,例如举出甲基、乙基、正丙基、异丙基、正丁基、异丁基、仲丁基、叔丁基、苯基、苄基、三苯基甲基。这样的烃基只要是由碳原子和氢原子构成的烃基就不受到特别限定,例如在上述r中也可以为碳原子数为1~10的烃基。
[0071]
v中,卤素原子为f、cl、br或i,优选为f或cl。
[0072]
v中,碳原子数为1~10的烃基只要是由碳原子和氢原子构成的烃基就不受到特别限定,例如在上述r中可以是碳原子数为1~10的烃基。
[0073]
v中,-c
nf2n 1
只要是由碳原子和氟原子构成的全氟烷基就不受到特别限定,可以为直链状,也可以为支链状。另外,n为1~10的整数,优选为1~3的整数。
[0074]
v中,-oa1、-soma1中所含的a1表示氢原子、或碳原子数为1~10的烃基。在a1表示碳原子数为1~10的烃基的情况下,例如在上述r中可以是碳原子数为1~10的烃基。此外,m为0~3的整数,优选为0~2的整数。
[0075]
v中,-na1a2中所含的a1和a2各自独立地表示氢原子、或碳原子数为1~10的烃基。a1和a2各自可以相同,也可以不同。a1和a2表示碳原子数为1~10的烃基的情况下,例如在上述r中可以是碳原子数为1~10的烃基。
[0076]
v中,-cooa1中所含的a1表示氢原子、或碳原子数为1~10的烃基。在a1表示碳原子数为1~10的烃基的情况下,例如在上述r中可以是碳原子数为1~10的烃基。
[0077]
v中,-cona1a2中所含的a1和a2各自独立地表示氢原子、或碳原子数为1~10的烃基。a1和a2各自可以相同,也可以不同。a1和a2表示碳原子数为1~10的烃基的情况下,例如在上述r中可以是碳原子数为1~10的烃基。
[0078]
本实施方式中的含氟嘧啶化合物在嘧啶环2位上具有特定的取代基(咪唑基等唑类结构)、在嘧啶环4位、5位和6位上具有特定的取代基(-or、-cf3、-f),因此从结构扩展性的观点出发可以具有优异的效果,特别是能够期待所期望的生物活性(例如,各种细胞的增殖抑制活性)。此外,在唑类结构具有取代基的情况下,可以对本实施方式中的含氟嘧啶化合物赋予进一步的特性。此外,嘧啶环4位和6位上的取代基为不同的基团(-or和-f),因此
能够容易地对非对称的结构进行衍生化,也能够期待作为中间体而使用。更具体而言,通过在酸性条件下使含氟嘧啶化合物反应,能够对-or进行修饰而得到衍生物。此外,通过在碱性条件下使含氟嘧啶化合物反应,能够对-f进行修饰而得到衍生物。本实施方式中的含氟嘧啶化合物在例如有机半导体、液晶等电子材料领域中是有用的。
[0079]
(含氟嘧啶化合物的制造方法)
[0080]
本实施方式中的含氟嘧啶化合物的制造方法包括:(a)通过使下述通式(2)所示的氟异丁烯衍生物与下述通式(3)所示的化合物或其盐反应而得到下述通式(1)的含氟嘧啶化合物的工序,
[0081]
[化学式5]
[0082][0083]
上述通式(1)~(3)中,
[0084]
r表示碳原子数为1~12的烃基,
[0085]
b1表示氢原子、卤素原子、碳原子数为1~10的烃基、-c
nf2n 1
(n为1~10的整数)、硝基、硼酸基、-oa1、-soma1(m为0~3的整数)、-na1a2、-cooa1或-cona1a2,
[0086]
w、x、y和z各自独立地表示cv或n,其中,w、x、y和z中的至少一个为n,n可以具有取代基,
[0087]
v表示氢原子、卤素原子、碳原子数为1~10的烃基、-c
nf2n 1
(n为1~10的整数)、硝基、硼酸基、-oa1、-soma1(m为0~3的整数)、-na1a2、-cooa1或-cona1a2,
[0088]
a1和a2各自独立地表示氢原子、或碳原子数为1~10的烃基。
[0089]
通式(2)中,r与上述通式(1)的化合物中定义的相同,通式(3)中,b1、w、x、y和z各自与上述通式(1)的化合物中定义的相同。
[0090]
上述通式(2)中的r优选表示碳原子数为1~10的烷基。通式(2)中的r例如可以为上述通式(1)中的r中碳原子数为1~10的烷基。
[0091]
通式(2)所示的氟异丁烯衍生物与通式(3)所示的化合物之间的上述(a)的反应以下述反应式(a)表示。
[0092]
[化学式6]
[0093]
[0094]
在上述反应式(a)中,上述通式(3)的化合物可以各自为盐的形态。在通式(3)的化合物为盐的形态的情况下,例如可以举出构成通式(3)化合物的脒基的氨基部分(-nh2)和亚氨基部分(=nh)中的至少一个部分被阳离子化而成为(-nh
3
)和(=nh
2
)并与抗衡离子形成盐的形态。抗衡离子只要为1价阴离子则不受到特别限定,例如可以举出f-、cl-、br-、i-等卤化物离子。
[0095]
在本实施方式中的含氟嘧啶化合物的制造方法中,例如可以在卤化氢捕获剂的存在下一步进行上述(a)的反应。因此,可以简单地得到上述通式(1)的含氟嘧啶化合物。另外,在上述(a)的反应中,在通式(2)所示的氟异丁烯衍生物与通式(3)化合物的脒基之间形成环状的嘧啶结构。在该嘧啶结构2位存在来自通式(3)化合物中唑类结构的基团。此外,在该嘧啶结构4位、5位和6位分别存在来自氟异丁烯衍生物的-or、cf3和f。
[0096]
卤化氢捕获剂是具有捕获氟化氢(hf)的功能的物质,所述氟化氢(hf)由在上述(a)的反应式中来自通式(3)化合物中的脒基的氢原子和来自通式(2)的氟异丁烯衍生物的氟原子形成。作为卤化氢捕获剂,可以使用氢氧化钠、氢氧化钾、氢氧化钙、碳酸钠、碳酸钾、氟化钠和氟化钾等无机化合物;吡啶、三乙胺、二异丙基乙胺、二氮杂双环壬烯、二氮杂双环十一碳烯、甲基三氮杂双环癸烯和二氮杂双环辛烷等有机氮衍生物。
[0097]
得到上述(a)的含氟嘧啶化合物的工序可以在氟化物离子捕获剂的存在下进行。优选地,在作为氟化物离子捕获剂的锂、钠、镁、钾、钙或四甲基铵的阳离子与三氟乙酸、七氟丁酸、甲磺酸、乙磺酸、苯磺酸、甲苯磺酸、三氟甲磺酸、九氟丁磺酸、双(三氟甲磺酰)亚胺、双(九氟丁磺酰)亚胺、n,n-六氟丙烷-1,3-二磺酰亚胺、四苯基硼酸、四[3,5-双(三氟甲基)苯基]硼酸或四(五氟苯基)硼酸的阴离子的盐的存在下,将上述通式(2)所示的氟异丁烯衍生物与上述通式(3)所示的化合物或其盐进行反应。其中,优选使用钾盐或钠盐,更优选使用钠盐。认为来自氟化物离子捕获剂的阳离子在反应中捕获从通式(2)所示的氟异丁烯衍生物游离的氟离子,作为针对有机溶剂的溶解性低的盐而析出,由此促进反应,能够以高收率得到上述通式(1)所示的含氟嘧啶化合物。
[0098]
上述(a)的反应时的反应温度优选为0~100℃、更优选为5~50℃、进一步优选为10~20℃。上述(a)的反应时的反应时间优选为0.5~48小时、更优选为1~36小时、进一步优选为2~12小时。
[0099]
作为在上述(a)的反应中使用的溶剂,可以举出四氢呋喃、单甘醇二甲醚、二甘醇二甲醚、三甘醇二甲醚、四甘醇二甲醚、乙腈、二甲基甲酰胺、二甲基乙酰胺、甲基吡咯烷酮、二甲基亚乙基脲、四甲基脲、二甲基亚砜和环丁砜等非质子性极性溶剂,或者,水等质子性极性溶剂与二氯甲烷、甲苯及二乙醚等非水溶性溶剂的二相类溶剂等。另外,作为上述(a)的反应的催化剂,可以任意使用苄基三乙基氯化铵等季铵盐卤化物、季鏻卤化物、冠醚类等。
[0100]
其它实施方式中的含氟嘧啶化合物的制造方法包括:(b)通过使下述通式(4)所示的氟异丁烷衍生物与下述通式(3)所示的化合物或其盐反应,得到下述通式(1)的含氟嘧啶化合物的工序,
[0101]
[化学式7]
[0102][0103]
上述通式(1)、(3)或(4)中,
[0104]
q表示卤素原子、-oa1、-soma1(m为0~3的整数)或-na1a2,
[0105]
r表示碳原子数为1~12的烃基,
[0106]
b1表示氢原子、卤素原子、碳原子数为1~10的烃基、-c
nf2n 1
(n为1~10的整数)、硝基、硼酸基、-oa1、-soma1(m为0~3的整数)、-na1a2、-cooa1或-cona1a2,
[0107]
w、x、y和z各自独立地表示cv或n,其中,w、x、y和z中的至少一个为n,n可以具有取代基,
[0108]
v表示氢原子、卤素原子、碳原子数为1~10的烃基、-c
nf2n 1
(n为1~10的整数)、硝基、硼酸基、-oa1、-soma1(m为0~3的整数)、-na1a2、-cooa1或-cona1a2,
[0109]
a1和a2各自独立地表示氢原子、或碳原子数为1~10的烃基。
[0110]
通式(4)中,r与上述通式(1)的化合物中定义的相同,卤素原子、-oa1、-soma1(m为0~3的整数)和-na1a2与上述通式(1)的化合物中定义的相同。
[0111]
上述通式(1)和(4)中的r优选表示碳原子数为1~10的烷基。通式(4)中的r例如可以为上述通式(1)中的r中碳原子数为1~10的烷基。
[0112]
通式(4)所示的氟异丁烷衍生物与通式(3)所示的化合物之间的上述(b)的反应以下述反应式(b)表示。
[0113]
[化学式8]
[0114][0115]
在上述反应式(b)中,通式(3)的化合物可以分别为盐的形态。在通式(3)的化合物为盐的形态的情况下,例如可以举出构成通式(3)化合物的脒基的氨基部分(-nh2)和亚氨基部分(=nh)中的至少一个部分被阳离子化而成为(-nh
3
)和(=nh
2
)并与抗衡离子形成盐的形态。抗衡离子只要为1价阴离子则不受到特别限定,例如可以举出f-、cl-、br-、i-等卤化物离子。
[0116]
在其它实施方式中的含氟嘧啶化合物的制造方法中,例如,可以在一步进行上述(b)的反应。因此,可以简单地得到上述通式(1)的含氟嘧啶化合物。另外,在上述(b)的反应中,在通式(4)所示的氟异丁烷衍生物与通式(3)化合物的脒基之间形成环状的嘧啶结构。
在该嘧啶结构2位上存在来自通式(3)的化合物中唑类结构的基团。另外,在该嘧啶结构的4位、5位和6位上分别存在来自氟异丁烷衍生物的-or、cf3和f。
[0117]
上述(b)的反应时的反应温度优选为0~100℃、更优选为5~50℃、进一步优选为10~20℃。上述(b)的反应时的反应时间优选为0.5~48小时、更优选为1~36小时、进一步优选为4~24小时。在上述(b)的反应中,可以使用与上述(a)同样的卤化氢捕获剂。
[0118]
作为在上述(b)的反应中使用的溶剂,可以举出四氢呋喃、单甘醇二甲醚、二甘醇二甲醚、三甘醇二甲醚、四甘醇二甲醚、乙腈、二甲基甲酰胺、二甲基乙酰胺、甲基吡咯烷酮、二甲基亚乙基脲、四甲基脲、二甲基亚砜和环丁砜等非质子性极性溶剂,或者,水等质子性极性溶剂与二氯甲烷、甲苯和二乙醚等非水溶性溶剂的两相类溶剂等。此外,作为上述(b)的反应的催化剂,可以任意使用苄基三乙基氯化铵等季铵盐卤化物、季鏻卤化物、冠醚类等。
[0119]
以上,对本发明的实施方式进行了说明,但本发明并不限定于上述实施方式,包含本发明的概念以及权利要求书所包含的所有方式,能够在本发明的范围内进行各种改变。
[0120]
实施例
[0121]
以下,对本发明的实施例进行说明,但本发明只要不超出其主旨,就不局限于这些例子。另外,只要没有特别提及,则室温是指20℃
±
5℃的范围内。
[0122]
(实施例1)
[0123]
6-氟-4-甲氧基-2-(2-(1-甲基咪唑基))-5-(三氟甲基)嘧啶的制备
[0124]
在冰水冷却下,向乙腈10g中加入1-甲基-2-脒基咪唑盐酸盐2g(12mmol)、1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯3g(14mmol)。接着,以内温不超过10℃的方式滴加二异丙基乙胺8g(62mmol)与乙腈10g的混合溶液,升温至室温。约16小时后,减压蒸馏除去乙腈,接着溶解于乙酸乙酯进行柱纯化,得到下述式(5)所示的化合物(化学式:c
10
h8f4n4o,分子量:276.19g/mol)0.7g。得到的化合物的分离收率为20%。
[0125]
[化学式9]
[0126][0127]
分析结果如下所示。
[0128]
质谱(ci,m/z):276([m]
)
[0129]1h-nmr(300mhz,cdcl3)δppm:7.30(d,1h),7.12(d,1h),4.25(s,3h),4.18(s,3h)
[0130]
19
f-nmr(300mhz,c6f6)δppm:-58.5(d,3f),-60.3(dd,1f)
[0131]
(实施例2)
[0132]
代替实施例1的1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯而使用了1,1,1,3,3-五氟-3-甲氧基-2-(三氟甲基)-丙烷的6-氟-4-甲氧基-2-(2-(1-甲基咪唑基))-5-(三氟甲基)嘧啶的制备
[0133]
在冰水冷却下,向乙腈10g中加入1-甲基-2-脒基咪唑盐酸盐2g(12mmol)、1,1,1,3,3-五氟-3-甲氧基-2-(三氟甲基)-丙烷3g(14mmol)。接着,以内温不超过10℃的方式滴加
二异丙基乙胺10g(78mmol)与乙腈10g的混合溶液,升温至室温。约16小时后,减压蒸馏除去乙腈,接着溶解于乙酸乙酯,进行柱纯化。得到的化合物的分析结果与实施例1的产物相同。
[0134]
另外,在实施例2中,虽然未计算所得的化合物的分离收率,但预测在体系中从1,1,1,3,3-五氟-3-甲氧基-2-(三氟甲基)-丙烷生成1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯的过程中可能产生的副产物会引起杂质的种类及其量的增加。因此,与对应的实施例2的制法相比较,认为实施例1的制法得到的产物的分离收率高。
[0135]
(实施例3)
[0136]
6-氟-4-甲氧基-2-[3-(1-甲基-1h-吡唑基)]-5-(三氟甲基)嘧啶的制备
[0137]
将1-甲基-1h-吡唑-3-羧酰亚胺酰胺盐酸盐0.5g(2.9mmol)溶解于乙腈29ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.7g(3.3mmol)和二异丙基乙胺1.9g(14.7mmol),在室温下搅拌23.8小时。搅拌后,将反应液进行柱纯化,得到下述式(6)所示的化合物(化学式:c
10
h8f4n4o,分子量:276.19g/mol)0.2g(0.6mmol)。得到的化合物的分离收率为21.8%。
[0138]
[化学式10]
[0139][0140]
分析结果如下所示。
[0141]
质谱(apci,m/z):277.1([m h]
)
[0142]1h-nmr(400mhz,cdcl3)δppm:7.46(d,j=2.5hz,1h),7.06(d,j=2.1hz,1h),4.22(s,3h),2.05(s,3h)
[0143]
(实施例4)
[0144]
6-氟-4-甲氧基-2-[4-(1-甲基-1h-吡唑基)]-5-(三氟甲基)嘧啶的制备
[0145]
将1-甲基-1h-吡唑-4-羧酰亚胺酰胺盐酸盐的粗纯化物0.4g(2.3mmol)溶解于乙腈23ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.6g(2.8mmol)和二异丙基乙胺1.6g(12.4mmol),在室温下搅拌23小时。搅拌后,将反应液进行柱纯化,得到下述式(7)所示的化合物(化学式:c
10
h8f4n4o,分子量:276.19g/mol)0.05g(0.2mmol)。得到的化合物的两步收率为4.0%。
[0146]
[化学式11]
[0147][0148]
分析结果如下所示。
[0149]
质谱(apci,m/z):277.1([m h]
)
[0150]1h-nmr(400mhz,cdcl3)δppm:8.15(s,1h),8.11(s,1h),4.16(s,3h),3.98(s,3h)
[0151]
(实施例5)
[0152]
6-氟-4-甲氧基-2-[5-(1-甲基-1h-吡唑基)]-5-(三氟甲基)嘧啶的制备
[0153]
将1-甲基-1h-吡唑-5-羧酰亚胺酰胺盐酸盐0.4g(2.2mmol)溶解于乙腈22ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.5g(2.4mmol)和二异丙基乙胺1.5g(12.6mmol),在室温下搅拌22.5小时。搅拌后,将反应液进行柱纯化,得到下述式(8)所示的化合物(化学式:c
10
h8f4n4o,分子量:276.19g/mol)0.2g(0.8mmol)。得到的化合物的分离收率为34.7%。
[0154]
[化学式12]
[0155][0156]
分析结果如下所示。
[0157]
质谱(apci,m/z):277.5([m h]
)
[0158]1h-nmr(400mhz,cdcl3)δppm:7.54(d,j=2.1hz,1h),7.18(d,j=2.1hz,1h),4.36(s,3h),4.19(s,3h)
[0159]
(实施例6)
[0160]
6-氟-4-甲氧基-2-[2-(1-甲基-1h-吡咯基)]-5-(三氟甲基)嘧啶的制备
[0161]
将1-甲基-1h-吡咯-2-羧酰亚胺酰胺盐酸盐的粗纯化物0.3g溶解于乙腈10ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.2g和二异丙基乙胺0.4g,在室温下搅拌23小时。搅拌后,将反应液进行柱纯化,得到下述式(9)所示的化合物(化学式:c
11
h9f4n3o,分子量:275.21g/mol)的粗纯化物。
[0162]
[化学式13]
[0163][0164]
分析结果如下所示。
[0165]
质谱(apci,m/z):275.8([m]
)
[0166]
(实施例7)
[0167]
6-氟-4-甲氧基-2-(1-甲基-1h-1,2,3-三唑-4-基)-5-(三氟甲基)嘧啶的制备
[0168]
将1-甲基-1h-1,2,3-三唑-4-羧酰亚胺酰胺盐酸盐0.4g(2.2mmol)溶解于乙腈22ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.6g(2.8mmol)和二异丙基乙胺1.5g(11.6mmol),在室温下搅拌21.3小时。搅拌后,将反应液进行柱纯化,得到下述式
(10)所示的化合物(化学式:c9h7f4n5o,分子量:277.18g/mol)0.4g(1.4mmol)。得到的化合物的分离收率为69.4%。
[0169]
[化学式14]
[0170][0171]
分析结果如下所示。
[0172]
质谱(apci,m/z):277.7([m]
)
[0173]1h-nmr(400mhz,cdcl3)δppm:8.29(s,1h),4.25(s,1h),4.21(s,3h)
[0174]
(实施例8)
[0175]
6-氟-4-甲氧基-2-(1-甲基-1h-1,2,3-三唑-5-基)-5-(三氟甲基)嘧啶的制备
[0176]
将1-甲基-1h-1,2,3-三唑-5-羧酰亚胺酰胺盐酸盐0.3g(1.9mmol)溶解于乙腈18ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.5g(2.4mmol)和二异丙基乙胺1.2g(9.3mmol),在室温下搅拌23小时。搅拌后,将反应液进行柱纯化,得到下述式(11)所示的化合物(化学式:c9h7f4n5o,分子量:277.18g/mol)0.3g(1.0mmol)。得到的化合物的分离收率为52.3%。
[0177]
[化学式15]
[0178][0179]
分析结果如下所示。
[0180]
质谱(apci,m/z):277.7([m]
)
[0181]1h-nmr(400mhz,cdcl3)δppm:8.43(s,1h),4.50(s,3h),4.22(s,3h)
[0182]
(实施例9)
[0183]
6-氟-4-甲氧基-2-(1-甲基-1h-1,2,4-三唑-5-基)-5-(三氟甲基)嘧啶的制备
[0184]
将1-甲基-1h-1,2,4-咪唑-5-羧酰亚胺酰胺盐酸盐0.3g(1.8mmol)溶解于乙腈18ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.4g(1.9mmol)和二异丙基乙胺1.2g(9.3mmol),在室温下搅拌19.3小时。搅拌后,将反应液进行柱纯化,得到下述式(12)所示的化合物(化学式:c9h7f4n5o,分子量:277.18g/mol)0.07g(0.3mmol)。得到的化合物的分离收率为14.3%。
[0185]
[化学式16]
[0186][0187]
分析结果如下所示。
[0188]
质谱(apci,m/z):277.7([m]
)
[0189]1h-nmr(400mhz,cdcl3)δppm:8.06(s,1h),4.40(s,3h),4.28(s,3h)
[0190]
(实施例10)
[0191]
2-(5-氯-1-甲基-1h-咪唑-2-基)-6-氟-4-甲氧基-5-(三氟甲基)嘧啶的制备
[0192]
将5-氯-1-甲基-1h-咪唑-2-羧酰亚胺酰胺盐酸盐0.3g(1.3mmol)溶解于乙腈13ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.3g(1.4mmol)和二异丙基乙胺0.9g(7.0mmol),在室温下搅拌23小时。搅拌后,将反应液进行柱纯化,得到下述式(13)所示的化合物(化学式:c
10
h7clf4n4o,分子量:310.64g/mol)。
[0193]
[化学式17]
[0194][0195]
分析结果如下所示。
[0196]
质谱(apci,m/z):310.0([m]
)
[0197]1h-nmr(400mhz,cdcl3)δppm:7.27(s,1h),4.24(s,3h),4.13(s,3h)
[0198]
(实施例11)
[0199]
6-氟-4-甲氧基-2-[2-(甲磺酰基)-1-甲基-1h-咪唑-4-基]-5-(三氟甲基)嘧啶的制备
[0200]
将2-(甲磺酰基)-1-甲基-1h-咪唑-4-羧酰亚胺酰胺盐酸盐0.3g(1.5mmol)溶解于乙腈19.4ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.5g(2.4mmol)和二异丙基乙胺1.3g(10.1mmol),在室温下搅拌17小时。搅拌后,将反应液进行柱纯化,得到下述式(14)所示的化合物(化学式:c
11h10
f4n4o3s,分子量:354.28g/mol)0.3g(0.9mmol)。得到的化合物的分离收率为66.3%。
[0201]
[化学式18]
[0202][0203]
分析结果如下所示。
[0204]
质谱(apci,m/z):354.0([m]
)
[0205]1h-nmr(400mhz,cdcl3)δppm:7.89(s,1h),4.21(s,3h),4.09(s,3h),3.53(s,3h)
[0206]
(实施例12)
[0207]
6-氟-4-甲氧基-2-(1-苯基-1h-咪唑-4-基)-5-(三氟甲基)嘧啶的制备
[0208]
将1-苯基-1h-咪唑-4-羧酰亚胺酰胺盐酸盐的粗纯化物0.3g溶解于乙腈12.4ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.3g(1.4mmol)和二异丙基乙胺0.8g(6.2mmol),在室温下搅拌14小时。搅拌后,将反应液进行柱纯化,得到下述式(15)所示的化合物(化学式:c
15h10
f4n4o,分子量:338.27g/mol)0.03g(0.07mmol)。
[0209]
[化学式19]
[0210][0211]
分析结果如下所示。
[0212]
质谱(apci,m/z):339.1([m h]
)
[0213]1h-nmr(400mhz,cdcl3)δppm:8.21(d,j=1.2hz,1h),7.98(d,j=1.2hz,1h),7.44-7.57(m,5h),4.25(s,3h)
[0214]
(实施例13)
[0215]
6-氟-4-甲氧基-5-(三氟甲基)-2-(1-三苯基甲基-1h-咪唑-4-基)嘧啶的制备
[0216]
将1-(三苯基甲基)咪唑-4-羧酰亚胺酰胺盐酸盐的粗纯化物0.3g(0.7mmol)溶解于乙腈7.3ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.2g(0.9mmol)和二异丙基乙胺0.5g(3.9mmol),在室温下搅拌15.8小时。搅拌后,将反应液进行柱纯化,得到下述式(16)所示的化合物(化学式:c
28h20
f4n4o,分子量:504.49g/mol)0.02g(0.04mmol)。
[0217]
[化学式20]
[0218][0219]
分析结果如下所示。
[0220]
质谱(apci,m/z):504.2([m]
)
[0221]1h-nmr(400mhz,cdcl3)δppm:7.83(s,1h),7.57(s,1h),7.36-7.38(m,9h),7.15-7.18(m,6h),4.18(s,3h)
[0222]
(实施例14)
[0223]
6-氟-2-(1-甲基-3-硝基-1h-吡唑-5-基)-4-甲氧基-5-(三氟甲基)嘧啶的制备
[0224]
将1-甲基-3-硝基-1h-吡唑-5-羧酰亚胺酰胺盐酸盐的粗纯化物0.3g溶解于乙腈15ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.3g(1.4mmol)和二异丙基乙胺1.0g(7.7mmol),在室温下搅拌13.4小时。搅拌后,将反应液进行柱纯化,得到下述式(17)所示的化合物(化学式:c
10
h7f4n5o3,分子量:321.19g/mol)0.1g(0.3mmol)。
[0225]
[化学式21]
[0226][0227]
分析结果如下所示。
[0228]
质谱(apci,m/z):321.3([m]-)
[0229]1h-nmr(400mhz,cdcl3)δppm:7.73(s,1h),4.46(s,1h),4.22(s,3h)
[0230]
(实施例15)
[0231]
6-氟-2-[1-甲基-5-(甲硫基)-1h-吡唑-3-基]-4-甲氧基-5-(三氟甲基)嘧啶的制备
[0232]
将1-甲基-5-(甲硫基)-1h-吡唑-3-羧酰亚胺酰胺盐酸盐0.5g(2.0mmol)溶解于乙腈10ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.5g(2.4mmol)和二异丙基乙胺1.3g(10.1mmol),在室温下搅拌24.4小时。搅拌后,将反应液进行柱纯化,得到下述式(18)所示的化合物(化学式:c
11h10
f4n4os,分子量:322.28g/mol)0.3g(0.9mmol)。得到的化合物的分离收率为47.3%。
[0233]
[化学式22]
[0234][0235]
分析结果如下所示。
[0236]
质谱(apci,m/z):354.0([m meoh]-)
[0237]1h-nmr(400mhz,cdcl3)δppm:7.04(s,1h),4.22(s,3h),4.01(s,3h),2.49(s,3h)
[0238]
(实施例16)
[0239]
6-氟-4-甲氧基-2-[3-甲氧基-1-甲基-1h-吡唑-4-基]-5-(三氟甲基)嘧啶的制备
[0240]
将3-甲氧基-1-甲基-1h-吡唑-4-羧酰亚胺酰胺盐酸盐的粗产物0.2g溶解于乙腈12ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.3g(1.4mmol)和二异丙基乙胺0.3g(6.2mmol),在室温下搅拌14.7小时。搅拌后,将反应液进行柱纯化,得到下述式(19)所示的化合物(化学式:c
11h10
f4n4o2,分子量:306.22g/mol)的粗纯化物。
[0241]
[化学式23]
[0242][0243]
分析结果如下所示。
[0244]
质谱(apci,m/z):306.7([m]
)
[0245]1h-nmr(400mhz,cdcl3)δppm:7.96(s,1h),4.14(s,3h),4.02(s,3h),3.81(s,3h)
[0246]
(实施例17)
[0247]
6-氟-4-甲氧基-2-(4-碘-1-甲基-1h-吡咯基-2-基)-5-(三氟甲基)嘧啶的制备
[0248]
将4-碘-1-甲基-1h-吡咯-2-羧酰亚胺酰胺盐酸盐的粗纯化物0.1g溶解于乙腈6ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.2g和二异丙基乙胺0.4g,在室温下搅拌15.8小时。搅拌后,将反应液进行柱纯化,得到下述式(20)所示的化合物(化学式:c
11
h8f4in3o,分子量:401.10g/mol)的粗纯化物。
[0249]
[化学式24]
[0250]
[0251]
分析结果如下所示。
[0252]
质谱(apci,m/z):403.5([m]-)
[0253]
(实施例18)
[0254]
4-[6-氟-4-甲氧基-5-(三氟甲基)嘧啶-2-基]-1-甲基-1h-吡咯-2-羧酸甲酯的制备
[0255]
将4-甲脒基-1-甲基-1h-吡咯-2-羧酸甲酯盐酸盐(methyl 4-carbamimidoyl-1-methyl-1h-pyrrole-2-carboxylate hydrochloride)0.2g(0.9mmol)溶解于乙腈9.2ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.2g(0.9mmol)和二异丙基乙胺0.6g(4.6mmol),在室温下搅拌14.8小时。搅拌后,将反应液进行柱纯化,得到下述式(21)所示的化合物(化学式:c
13h11
f4n3o3,分子量:333.24g/mol)的粗纯化物。
[0256]
[化学式25]
[0257][0258]
分析结果如下所示。
[0259]
质谱(apci,m/z):333.6([m]
)
[0260]1h-nmr(400mhz,cdcl3)δppm:7.66(d,j=1.5hz,1h),7.60(d,j=1.8hz,1h),4.16(s,3h),4.00(s,3h),3.86(s,3h)
[0261]
(实施例19)
[0262]
6-氟-4-甲氧基-2-[1-甲基-5-(三氟甲基)-1h-1,2,3-三唑-4-基]-5-(三氟甲基)嘧啶的制备
[0263]
将1-甲基-5-(三氟甲基)-1h-1,2,3-三唑-4-羧酰亚胺酰胺盐酸盐0.2g(1.1mmol)溶解于乙腈10ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.3g(1.4mmol)和二异丙基乙胺0.7g(5.4mmol),在室温下搅拌15.7小时。搅拌后,将反应液进行柱纯化,得到下述式(22)所示的化合物(化学式:c
10
h6f7n5o,分子量:345.18g/mol)0.2g(0.6mmol)。得到的化合物的分离收率为64.1%。
[0264]
[化学式26]
[0265][0266]
分析结果如下所示。
[0267]
质谱(apci,m/z):345.8([m]-)
[0268]1h-nmr(400mhz,cdcl3)δppm:4.34(q,j=1.7hz,3h),4.19(s,3h)
[0269]
(实施例20)
[0270]
6-氟-4-甲氧基-2-(1,5-二甲基-1h-1,2,4-三唑-3-基)-5-(三氟甲基)嘧啶的制备
[0271]
将1,5-二甲基-1h-1,2,4-三唑-3-羧酰亚胺酰胺盐酸盐0.3g(1.5mmol)溶解于乙腈15ml中,加入1,3,3,3-四氟-1-甲氧基-2-(三氟甲基)-1-丙烯0.4g(1.9mmol)和二异丙基乙胺1.0g(7.7mmol),在室温下搅拌18.5小时。搅拌后,将反应液进行柱纯化,得到下述式(23)所示的化合物(化学式:c
10
h9f4in5o,分子量:291.21g/mol)的粗纯化物。
[0272]
[化学式27]
[0273][0274]
分析结果如下所示。
[0275]
质谱(apci,m/z):291.7([m]
)。
再多了解一些
本文用于创业者技术爱好者查询,仅供学习研究,如用于商业用途,请联系技术所有人。