1.本发明涉及新型冠状病毒的核酸检测试剂盒及新型冠状病毒的核酸检测方法,属于医疗临床上新型冠状肺炎诊断的技术领域。
背景技术:
2.新型冠状病毒肺炎(covid-19、或称sars-cov-2等),是以发热干咳等症状为主要表现的急性呼吸系统疾病。该病毒主要会导致患者出现发热、乏力、干咳等初期症状,随后表现为呼吸困难,严重者出现急性呼吸窘迫综合征以及代谢性酸中毒等。另外,现有的一些呼吸道病原体诸如急性呼吸综合征冠状病毒(sars-cov)、中东呼吸综合征冠状病毒 (mers-cov)等等,它们同样威胁人类健康安全。
3.新型冠状病毒是一种rna病毒,即遗传物质是rna(核糖核酸),病毒蛋白衣壳将 rna包裹在其中。目前新型冠状病毒的检测方法一般为核酸检测,方法主要采用实时荧光 pcr法,这种方法的优势是特异性好且准确率较高,但是该方法操作复杂,检测时间较长,实验条件苛刻需要专门实验室。其次,还有基于胶体金法快速筛查冠状病毒的检测试纸,虽然该方法的检测时间可缩短到十分钟,然而通常而言,胶体金法的敏感度和特异性相对于核酸检测更弱,很难将新型冠状病毒和其他冠状病毒鉴别出来。
技术实现要素:
4.为了克服现有技术的不足,本发明的目的是采用一种无核酸扩增的信号放大方法。具体来说,本发明提供了一种新型冠状病毒的核酸检测试剂盒及新型冠状病毒的核酸检测方法。
5.一方面,本发明提供了一种新型冠状病毒的核酸检测试剂盒,包括: pna探针溶液;用于修饰pna探针的氨基化的磁性纳米颗粒胶体;dna探针溶液;用于修饰dna探针的au纳米颗粒胶体;以及病毒保存液。
6.本发明中,首先制备(znmn)fe2o4@sio2磁性纳米颗粒和金纳米颗粒;使用两段分别于新冠病毒核酸核壳蛋白基因互补的肽核酸探针和核酸探针,并修饰于两种纳米颗粒表面,制备得双纳米颗粒探针。配置一系列浓度梯度新冠病毒核壳蛋白基因的标准溶液,双纳米颗粒探针在新冠病毒核壳蛋白基因存在时,与核壳蛋白基因发生耦合,经过多次磁分离得到分离产物,根据电感耦合等离子发射光谱质谱仪测定磁分离产物的金元素浓度,从而得到金元素和新冠病毒核壳蛋白基因的标准曲线。对待测溶液测定时,双纳米颗粒探针加入待测溶液反应后磁分离,分离产物通过电感耦合等离子发射光谱质谱仪测定金元素浓度,根据金元素和新冠病毒核壳蛋白基因的标准曲线,计算确定待测样品中新冠病毒核酸
浓度来达到检测目的。
7.本发明中,pna探针和dna探针的序列可根据不同新冠病毒的碱基对进行设计(例如covid-19或其变异德尔塔株、以及现有的sars-cov-2、sars-cov、mers-cov等都同样适用)。如果新型冠状病毒发生变异,重新设计探针序列就行。例如,所述pna探针的序列包括:cys-gly-aa tctg tcaa;所述dna探针的序列包括: aaaaaaaaaaaaaaaaaaaatttt gcagcagcaa。
8.较佳的,所述pna探针用量为6~15nmol。
9.较佳的,所述dna探针用量为25~40nmol。
10.较佳的,所述氨基化的磁性纳米颗粒胶体中磁性纳米颗粒的组成为 zn
0.4
mn
0.6
fe2o4@sio2,浓度为0.1~0.5mg/ml,粒径范围为25nm~40nm。
11.较佳的,所述au纳米颗粒胶体的浓度为0.02~0.1mg/ml,au纳米颗粒的粒径范围为3nm~10nm。
12.较佳的,所述氨基化的磁性纳米颗粒胶体的体积为160~220ul。
13.较佳的,所述au纳米颗粒胶体的体积为160~220ul。
14.较佳的,所述病毒保存液为hank
‘
液、或含有bsa、hepes、氨基酸、甘油的混合液(可通过市售购买获得)。
15.另一方面,本发明还提供了一种检测新型冠状病毒的双纳米探针,包括:氨基化的磁性纳米颗粒修饰的pna探针和au纳米颗粒修饰的dna探针;其中,氨基化的磁性纳米颗粒通过酰胺反应修饰在pna探针的一端;au纳米颗粒通过静电吸附修饰在dna探针中腺嘌呤的一端。
16.较佳的,所述氨基化的磁性纳米颗粒的组成为zn
0.4
mn
0.6
fe2o4@sio2,粒径范围为25 nm~40nm,负载量为10~30wt%。
17.较佳的,所述au纳米颗粒的粒径范围为3nm~10nm,负载量为10~30wt%。
18.较佳的,氨基化的磁性纳米颗粒修饰的pna探针和au纳米颗粒修饰的dna探针分别和新冠病毒核壳蛋白基因各一半序列碱基互补配对;通过电感耦合等离子体质谱光谱仪来检测金元素信号强度,根据金元素浓度以确定病毒含量。
19.再一方面,本发明还提供了一种采用新型冠状病毒的核酸检测试剂盒分析和检测新型冠状病毒的方法,包括:(1)将pna探针溶液、edc/nhs试剂、和用于修饰pna探针的氨基化的磁性纳米颗粒胶体混合,进行酰胺反应,得到氨基化的磁性纳米颗粒修饰的pna探针溶液;(2)将dna探针溶液和用于修饰dna探针的au纳米颗粒胶体混合,得到au纳米颗粒修饰的dna探针溶液;(3)将新冠病毒检测样分散在病毒保存液中,得到新冠病毒n gene溶液;(4)将氨基化的磁性纳米颗粒修饰的pna探针溶液和au纳米颗粒修饰的dna探针溶液加入到新冠病毒n gene溶液中,然后进行多次磁性分离,得到复合物溶液;(5)在复合物溶液中加入王水使得磁性纳米颗粒和au纳米颗粒充分溶解,得到待检测溶液;(6)采用电感耦合等离子体质谱光谱仪分析和检测待检测溶液中au元素的浓度,从而实现新冠病毒的分析和检测。
20.较佳的,金元素浓度(y)(pg/ml)和新冠病毒n gene浓度(x)(ng/ml)之间的关系为y=172.6x。
21.有益效果:该方法通过探针的磁性纳米颗粒和金纳米颗粒,与新冠病毒核壳蛋白基因互补配对,通过磁分离得到复合物,通过电感耦合等离子体质谱光谱仪分析测定出磁分离复合物中金元素浓度,经过金元素和核壳蛋白基因的标准曲线计算并确定待测新冠核酸浓度达到检测目的。相比传统pcr核酸检测方法,本方法无需核酸扩增过程,大大缩短检测时间,且检测限低,灵敏度和特异性高,实现在无需核酸扩增的前提下,达到放大信号检测新冠核酸的目的,可以更好地辅助目前新冠病毒检测工作。而且,王水可以最大限度灭活病毒提高了检测安全性,同时将金纳米颗粒消化成离子状态,提高icp-ms对金元素的检测准确性。
附图说明
22.图1为实施例1所得的zn
0.4
mn
0.6
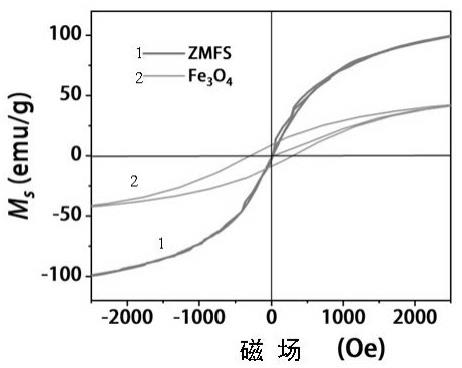
fe2o4@sio2磁性纳米颗粒(简称为zmfs)的tem照片;图2为实施例1所得的zmfs对比fe3o4纳米颗粒的磁滞回线;图3为实施例1所得的金纳米颗粒(简称为aunp)的tem照片;图4为实施例1所测得的zmfs,zmfs-nh2和zmfs-pna的zeta电位图;图5为实施例1所测得的aunp和aunp-dna的紫外可见吸收光谱图;图6为实施例1所测得的au与新冠病毒核壳蛋白基因(简称为n gene)的标准曲线;图7中表1为本方法对比pcr法对新冠核酸样本的检测结果。
具体实施方式
23.以下通过下述实施方式进一步说明本发明,应理解,下述实施方式仅用于说明本发明,而非限制本发明。
24.在本公开中,基于双纳米探针的无扩增新型冠状病毒核酸检测方法主要原理为:双纳米探针(修饰有磁性纳米颗粒的pna探针和修饰有金纳米颗粒的dna探针)耦合策略是一种基于核苷酸序列通过watson-crick碱基配对形成稳定杂交链的分子杂交技术,使用与新型冠状病毒核壳蛋白基因碱基配对的两段探针。该技术通过分别修饰pna探针和dna 探针的磁性纳米颗粒和金纳米颗粒与新型冠状病毒核酸杂交,经磁性分离将核壳蛋白基因阳性的核酸片段分离出来,由电感耦合等离子体质谱光谱仪测定分离产物的金元素信号,再根据预先测定的金元素与新冠病毒核壳蛋白基因标准曲线计算出核壳蛋白基因浓度。
25.在可选的实施方式中,修饰磁性纳米颗粒的肽核酸探针和和修饰有金纳米颗粒的 dna探针,两段探针分别与新冠病毒核壳蛋白基因各一半序列碱基互补配对。使用的磁性纳米颗粒为zn
0.4
mn
0.6
fe2o4@sio2纳米颗粒,其粒径范围可为20~40nm,负载量可为10~ 30%。使用的金纳米颗粒粒径范围可为3~10nm,负载量可为10~30%。
26.检测样品中的病毒核酸加入后,核酸会和修饰有肽核酸探针的磁性纳米颗粒结合,也和修饰有dna探针的金纳米颗粒结合,结合的量和样品中的病毒的量呈比例,经过磁分离,将复合体分离出来,由电感耦合等离子体质谱光谱仪来检测金元素信号强度,根据金元素浓度来确定病毒含量。
27.根据金元素浓度来确定病毒含量。具体来说,根据配置一系列不同浓度梯度的新
冠核酸溶液,加入修饰探针的磁性纳米颗粒和金纳米颗粒并与新冠病毒核壳蛋白基因耦合,通过电感耦合等离子体质谱光谱仪分析磁分离产物中的金元素浓度,得到金元素和新冠病毒核壳蛋白基因的标准曲线,根据标准曲线可以计算出待测样品中新冠病毒核酸浓度。
28.下面进一步例举实施例以详细说明本发明。同样应理解,以下实施例只用于对本发明进行进一步说明,不能理解为对本发明保护范围的限制,本领域的技术人员根据本发明的上述内容作出的一些非本质的改进和调整均属于本发明的保护范围。下述示例具体的工艺参数等也仅是合适范围中的一个示例,即本领域技术人员可以通过本文的说明做合适的范围内选择,而并非要限定于下文示例的具体数值。
29.实施例1基于双纳米探针的无扩增新型冠状病毒核酸检测方法,包括以下:双纳米探针耦合策略是一种基于核苷酸序列通过watson-crick碱基配对形成稳定杂交链的分子杂交技术,使用与新型冠状病毒核壳蛋白基因碱基配对的两段探针肽核酸(简称为pna)和dna,分别修饰于磁性纳米颗粒zn
0.4
mn
0.6
fe2o4@sio2(简称为zmfs)和金纳米颗粒(简称为aunp)表面;该技术通过修饰探针的磁性纳米颗粒和金纳米颗粒与新型冠状病毒核酸杂交,经磁性分离将核壳蛋白基因阳性的核酸片段分离出来,由电感耦合等离子体质谱光谱仪(简称icp-ms)测定分离产物的金元素信号,再根据预先测定的金元素与新冠病毒核壳蛋白基因标准曲线计算出核壳蛋白基因浓度。
30.该技术选用约25-40nm左右的zmfs作为磁性纳米颗粒,由图1可知,选用的 zmfs粒径均一,形貌规整,平均粒径约为30nm。由图2可知,选用的zmfs对比常用的 fe3o4纳米颗粒,其饱和磁化强度大于传统fe3o4纳米颗粒,达到约100emu/g。
31.该技术选用粒径大小约为3-10nm的aunp,由图3可知,选用的aunp形貌均匀,粒径大小约为5nm。
32.该技术选用的pna探针和dna探针序列分别与新冠病毒核壳蛋白基因各一半序列碱基互补配对。其中,pna探针(用量为10nmol)通过酰胺反应(edc/nhs介导(中文名称是1-乙基-(3-二甲基氨基丙基)碳酰二亚胺/n-羟基丁二酰亚胺),浓度分别为0.2 mg/ml和0.4mg/ml)修饰于aptes氨基化的zmfs(胶体,体积为200ul,浓度为0.1 mg/ml11%负载量)。由图4可知,修饰pna探针的zmfs相对于氨基化的zmfs其电位有所降低,说明pna探针的成功修饰。dna探针(修饰腺嘌呤,用量为30nmol)静电吸附于aunp表面(超声混合,体积为200ul,浓度为0.05mg/ml,约25wt%负载量)。由图5可知,对比aunp,修饰dna探针的aunp在267nm处有吸收峰,此处即对应dna 探针吸收波长,说明dna探针成功修饰于aunp。
33.选用病毒保存液(厂家北京友康生物科技股份有限公司和型号mt0501-7-3),将购买得到假病毒核酸(厂家深圳菁良基因科技有限公司和型号gw-crbm001-1),配置一系列浓度梯度的新冠核酸n gene溶液(calculated n gene),浓度范围为0.33-3300ng/ml (例如,0.33、3.3ng/ml、33ng/ml、330ng/ml、3300ng/ml)。将双纳米颗粒探针分别加入不同浓度梯度的新冠核酸n gene溶液中,随后进行磁性分离。一共进行三次磁分离,每次磁分离后加入无rnase水重新分散复合物,每次磁分离时间约为1min(其中磁性分离次数和加入无rnase水的量与后续金元素和n gene没关系,只是为了充分洗去双纳米探针耦合过程中,非特异性耦合的金纳米颗粒,增加检测结果可靠性)。将磁分离的复合物用王水充分消化,并由
icp-ms测定各样本中的金元素浓度,从而绘制出金元素浓度和新冠病毒ngene的标准曲线,由图5所示,标准曲线拟合良好,金元素(y)和新冠病毒n gene(x) 之间的关系为y=172.6x,相关度达0.9973,理论检测限可低至0.12ng/ml。
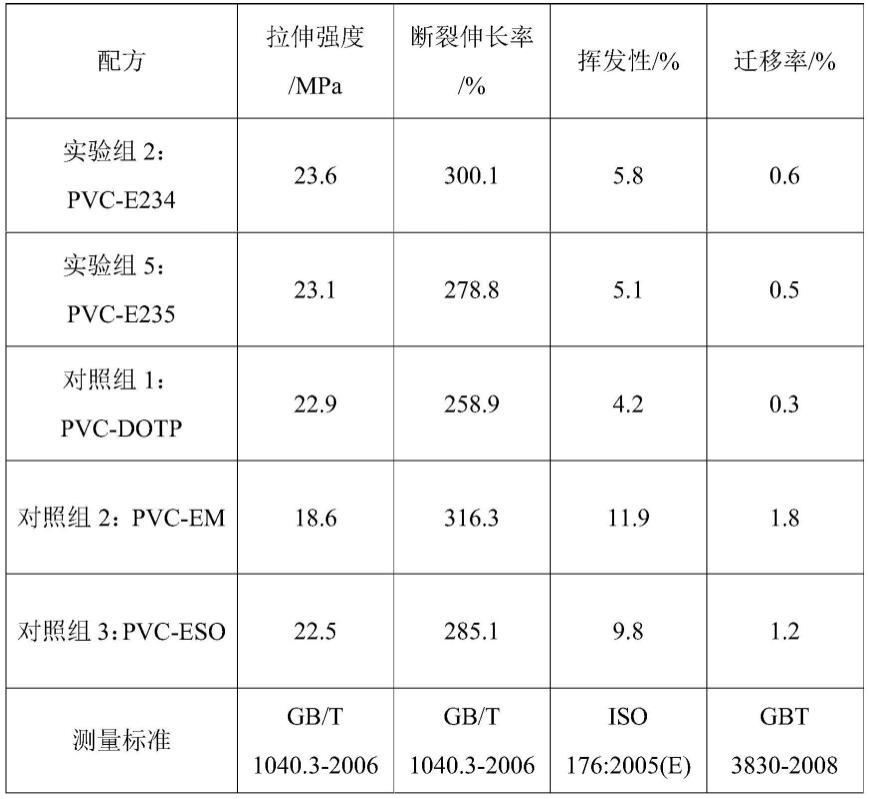
34.根据测定的标准曲线,对此常用的qrt-pcr法,本方法在灵敏度和准确度方面优良。由图7所示,对于前9个样本(no.1至no.9)含有不同浓度的新冠病毒n基因,范围为0.99至10.48ng/μl,本方法检测结果与qrt-pcr相符,说明本方法检测结果的准确性。样品10-18是通过稀释样品1-9获得的,样品1-9的n基因的浓度大大降低,范围从1.51到14.08ng/ml。这些高度稀释的样本中的n基因无法通过qrt-pcr检测到,但与此形成鲜明对比的是,即使浓度低至1.51ng/ml,表明与qrt-pcr相比,本方法对病毒基因检测具有很高的灵敏度。
35.以上描述说明了本发明的基本原理和主要特征,以及本发明的有点。为了安全考虑,虽然没有采用对真病毒covid-19或其变异德尔塔株等进行测试,但本行业技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中的描述只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都要包含于要求保护的本发明范围内。本发明要求保护范围由所附的权利要求书及其等效物界定。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。