1.本发明涉及串联合成嘧啶螺吲哚酮类化合物的方法,属于有机化学中的合成技术领域。
背景技术:
2.3,3-二取代的吲哚酮类化合物是重要的生物活性分子骨架,例如氨甲达林(i)、双醋酚汀(ii)、利诺吡啶(iii)等药物已经被人们大量使用,表现出了良好的药物效果。串联heck反应是构筑吲哚酮类化合物的重要方法,祝介平课题组报道了钯催化的n-芳基丙烯酰胺的分子内不对称heck还原反应,用联硼-水作为氢化物的来源,还原c(sp3)-pd中间体,以高产率和对映选择性合成了3,3-二取代的吲哚酮类化合物。lu课题组报道了通过pd/cu协同催化不对称heck/sonogashira偶联反应,合成含有四元立体中心和三氟甲基化中心的手性吲哚酮类化合物。
3.嘧啶类化合物广泛存在于医药中间体和感光剂的原料中,例如:5-氟脲嘧啶类化合物可用于抗肿瘤、抗癌药物中,对胃癌、乳腺癌和肠癌都具有很好的治疗效果,很多修饰过嘧啶类化合物还具有杀虫、杀菌和除草活性。根据药物化学中优势结构组合概念,将嘧啶和吲哚酮进行结构组合有望得到良好生物活性新结构。
技术实现要素:
4.为了解决上述技术问题,本发明公开了一种结构新颖嘧啶吲哚酮类化合物,并提供了钯催化串联合成吲哚螺嘧啶类化合物的方法。采用取代丙炔酸化合物或末端炔烃为炔基化试剂2,在pd(pph3)4作用下,与n-邻碘苯基脲嘧啶-5-甲酰胺1通过串联heck/炔基化反应得到嘧啶螺吲哚酮类化合物3。该方法以良好收率得到含有两个连续立体中心的嘧啶螺吲哚酮类化合物,为嘧啶螺吲哚酮类化合物的合成提供了一种温和、简便、高效的途径。
5.本发明首先提供了一种结构新颖嘧啶吲哚酮类化合物,结构如下:
[0006][0007]
其中:r选自c1-c6烷基、三(c1-c3烷基)硅基、苯基、取代苯基、萘基、取代萘基,所述取代指卤素、c1-c4烷基、c1-c4烷氧基、c1-c4烷氧羰基中的一种或多种。
[0008]
本发明所述钯催化串联合成吲哚螺嘧啶类化合物的方法,包括如下操作:以n-邻碘苯基脲嘧啶-5-甲酰胺1和丙炔酸类化合物2为原料,在钯催化剂/手性亚磷酰胺配体催化下,碱性条件下反应,得到嘧啶螺吲哚酮化合物3。反应方程式如下:
[0009][0010]
其中:r选自c1-c6烷基、三(c1-c3烷基)硅基、苯基、取代苯基、萘基、取代萘基,所述取代指卤素、c1-c4烷基、c1-c4烷氧基、c1-c4烷氧羰基中的一种或多种。
[0011]
进一步地,在上述技术方案中,所述钯催化剂选自pd(pph3)2cl2、pd2(dba)3、pdcl2(ch3cn)2、pd(oac)2、pd(pph3)4或pdcl2(dppf)。
[0012]
进一步地,在上述技术方案中,所述碱选自kf、cs2co3或csf。
[0013]
进一步地,在上述技术方案中,所述反应在有机溶剂中进行;有机溶剂选自甲苯、四氢呋喃或乙腈;优选有机溶剂为甲苯。
[0014]
进一步地,在上述技术方案中,所述n-邻碘苯基脲嘧啶-5-甲酰胺1、丙炔酸类化合物2、钯催化剂、有机膦配体与碱摩尔比为1:1-2:0.05-0.1:0.05-0.1:2-3。
[0015]
进一步地,在上述技术方案中,反应温度选自100-150℃。
[0016]
进一步地,在上述技术方案中,整个反应过程需要惰性气体保护下操作,惰性气体优选氮气。
[0017]
进一步地,得到嘧啶螺吲哚酮化合物3,采用叔丁醇钾和dmf中可进一步衍生得到衍生产物4,结构如下:
[0018][0019]
发明有益效果:
[0020]
1、以n-邻碘苯基脲嘧啶-5-甲酰胺1与丙炔酸类化合物2为原料,通过heck/炔基化串联反应,一步得到嘧啶螺吲哚酮类化合物3,同时具有手性季碳中心,结构新颖,未见公开资料报道。
[0021]
2、反应产物对映选择性高,反应收率和对映选择性最高分别可达82%和75%ee;产物经过进一步衍生,得到嘧啶螺吲哚酮产物4。
附图说明
[0022]
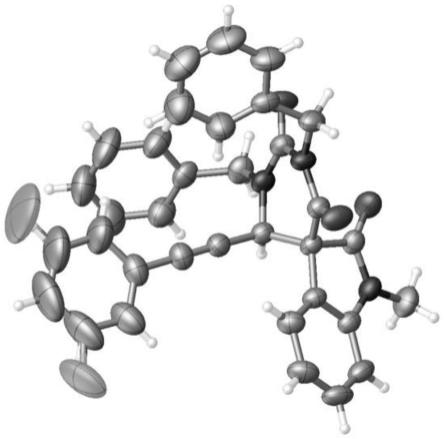
图1为实施例9中化合物3ai单晶x衍射谱图。
具体实施方式
[0023]
实施例1
[0024]
以n-邻碘苯基脲嘧啶-5-甲酰胺1a与苯丙炔酸化合物2a反应生成嘧啶螺吲哚酮化
合物3aa为例,进行反应条件优化,反应方程式如下:
[0025][0026]a1a(0.1mmol),2a(0.2mmol),pd(pph3)4(10mol%),碱(2.0eq),1.0ml溶剂,氮气保护下140℃反应6小时;b核磁收率。
[0027]
在反应条件筛选过程中,首先考察了溶剂对反应影响(entries 1-2)。同时考察了不同碱、溶剂、温度对反应的影响,最终确定甲苯为最佳反应溶剂,140℃为最佳反应温度,kf为最佳碱。
[0028]
反应条件考察操作(以entry 10为例):氮气保护下,将n-邻碘苯基脲嘧啶-5-甲酰胺1a(0.1mmol,1.0eq)、苯丙炔酸化合物2a(0.2mmol,2.0eq)、kf(0.2mmol,2.0eq)和pd(pph3)4(10mol%)加入schlenk管中,螺纹胶塞密封,注射器室温下加入干燥甲苯(1.0ml)然后反应转移至140℃搅拌6h。反应完成,二氯甲烷5ml稀释反应混合物,通过短硅胶柱过滤,dcm/meoh(20:1,20ml)洗涤。滤液经真空浓缩得到粗产物,再经制备薄层色谱纯化(pe/ea=2/1)得到淡黄色固体产物3aa,收率78%。m.p.83.2-83.4℃,tlc:rf=0.5(pe/ea=2:1)1h nmr(400mhz,cdcl3)δ7.42-7.21(m,15h),7.10-7.02(m,3h),6.87-6.84(m,1h),5.25-5.07(m,3h),4.71(s,1h),4.56(d,j=14.8hz,1h),3.16(s,3h).
13
c nmr(100mhz,cdcl3)δ170.3,165.2,152.9,144.6,137.3,135.8,131.9,130.3,129.4,129.1,128.7,128.6,128.5,128.4,128.1,127.4,125.7,124.3,123.1,121.1,108.8,88.5,81.1,58.3,51.2,50.3,45.4,26.7.hrms(esi):calcd for c
34h27
n3nao3(m na)
requires m/z 548.1945,found m/z 548.1937.
[0029]
实施例2:
[0030][0031]
氮气保护下,在schlenk管中依次加入n-邻碘苯基脲嘧啶-5-甲酰胺1a(0.1mmol,1.0eq)、苯丙炔酸化合物2b(0.2mmol,2.0eq)、pd(pph3)4(10mol%)和kf(0.2mmol,2.0eq),螺纹橡胶塞密封,注射器将1.0ml干燥甲苯打入反应管中,随后放在140℃下搅拌6小时。反应结束,dcm/meoh=15/1为洗脱剂,将反应液快速通过短硅胶柱,滤液经真空浓缩得到粗产品。硅胶柱色谱纯化,得到黄色糖浆状3ab,收率82%。tlc:rf=0.5(pe/ea=2:1);1h nmr(600mhz,cdcl3)δ7.43-7.38(m,2h),7.38-7.32(m,4h),7.32-7.18(m,7h),7.06(d,j=8.4hz,2h),7.03(td,j=7.8,1.2hz,1h)6.99-6.97(m,2h),6.85(d,j=7.8hz,1h),5.30-5.05(m,3h),4.70(s,1h),4.55(d,j=15.0hz,1h),3.16(s,3h),2.33(s,3h).
13
c nmr(150mhz,cdcl3)δ170.3,165.2,152.9,144.6,137.3,135.8,131.9,130.3,129.4,129.1,128.7,128.5,128.5,128.3,128.0,127.4,125.7,124.3,123.1,121.1,108.8,88.5,81.1,58.3,51.2,50.3,45.4,26.9,21.6.hrms(esi):calcd for c
35h29
n3nao3(m na)
requires m/z 562.2101,found m/z 562.2103.
[0032]
实施例3:
[0033][0034]
氮气保护下,在schlenk管中依次加入n-邻碘苯基脲嘧啶-5-甲酰胺1a(0.1mmol,1.0eq)、苯丙炔酸化合物2c(0.2mmol,2.0eq)、pd(pph3)4(10mol%)和kf(0.2mmol,2.0eq),螺纹橡胶塞密封,注射器将1.0ml干燥甲苯打入反应管中,放在140℃下搅拌6小时。反应结束,dcm/meoh=15/1为洗脱剂,将反应液快速通过短硅胶柱,滤液经真空浓缩得到粗产品。硅胶柱色谱纯化,得到黄色固体3ac,收率43%。m.p.189.2-191.4℃,tlc:rf=0.7(pe/ea=2:1),1h nmr(400mhz,cdcl3)δ7.45-7.20(m,12h),7.24-7.23(m,2h),7.06-7.02(m,3h),6.87(d,j=7.6hz,1h),5.27-5.06(m,3h),4.73(s,1h),4.53(d,j=14.8hz,1h),3.16(s,3h),1.29(s,9h).
13
c nmr(100mhz,cdcl3)δ170.4,165.3,152.9,152.9,144.7,137.3,135.9,131.7,130.3,129.1,128.7,128.5,128.4,128.0,127.4,125.6,125.5,124.4,123.1,118.1,108.8,88.8,80.4,58.5,51.2,50.2,45.4,35.0,31.2,26.8.hrms(esi):calcd for c
38h35
n3nao3(m na)
requires m/z 604.2571,found m/z 604.2565.
[0035]
实施例4:
[0036]
[0037]
氮气保护下,在schlenk管中依次加入n-邻碘苯基脲嘧啶-5-甲酰胺1a(0.1mmol,1.0eq)、苯丙炔酸化合物2d(0.2mmol,2.0eq)、pd(pph3)4(10mol%)和kf(0.2mmol,2.0eq),螺纹橡胶塞密封,注射器将1.0ml干燥甲苯打入反应管中,放在140℃下搅拌6小时。反应结束,dcm/meoh=15/1为洗脱剂,将反应液快速通过短硅胶柱,溶液经真空浓缩得到粗产品。硅胶柱色谱纯化,得到褐色固体3ad,收率78%。m.p.175.4-176.3℃,tlc:rf=0.5(pe/ea=2:1),1h nmr(600mhz,cdcl3)δ7.45-7.19(m,16h),7.04(td,j=7.2,1.2hz,1h),6.98-6.97(m,2h),6.86(d,j=7.8hz,1h),5.21
–
5.11(m,3h),4.68(s,1h),4.56(d,j=15.0hz,1h),3.16(s,3h).
13
c nmr(151mhz,cdcl3)δ170.1,165.0,152.8,144.5,137.2,135.6,135.6,133.0,130.3,129.0,128.8,128.6,128.5,128.3,128.0,127.4,125.6,124.2,123.0,119.4,108.7,87.2,82.1,58.2,51.1,50.3,45.3,26.7hrms(esi):calcd for c
34h29
cln3nao3(m na)
requires m/z 582.1555,found m/z 582.1555.
[0038]
实施例5:
[0039][0040]
氮气保护下,在schlenk管中依次加入n-邻碘苯基脲嘧啶-5-甲酰胺1a(0.1mmol,1.0eq)、苯丙炔酸化合物2e(0.2mmol,2.0eq)、pd(pph3)4(10mol%)和kf(0.2mmol,2.0eq),螺纹橡胶塞密封,注射器将1.0ml干燥甲苯打入反应管中,放在140℃下搅拌6小时。反应结束,dcm/meoh=15/1为洗脱剂,将反应液快速通过短硅胶柱,溶液经真空浓缩得到粗产品。硅胶柱色谱纯化得到黄色固体3ae,收率65%。m.p.195.9-196.1℃,tlc:rf=0.5(pe/ea=2:1),1h nmr(600mhz,cdcl3)δ7.45-7.20(m,14h),7.04(td,j=7.8,0.6hz,1h),6.92-6.90(m,2h),6.86(d,j=7.8hz,1h),5.21-5.11(m,3h),4.67(s,1h),4.56(d,j=15.0hz,1h),3.17(s,3h).
13
c nmr(151mhz,cdcl3)δ170.1,164.9,152.8,144.5,137.2,135.6,133.2,131.8,130.3,129.0,128.6,128.5,128.3,128.0,127.4,125.6,124.2,123.8,123.0,119.8,108.7,87.2,82.3,58.1,51.1,50.3,45.3,26.7;hrms(esi):calcd for c
34h26
brn3nao3(m na)
requires m/z 626.1050,found m/z 626.1042.
[0041]
实施例6:
[0042][0043]
氮气保护下,在schlenk管中依次加入n-邻碘苯基脲嘧啶-5-甲酰胺1a(0.1mmol,1.0eq)、苯丙炔酸化合物2f(0.2mmol,2.0eq)、pd(pph3)4(10mol%)和kf(0.2mmol,2.0eq),螺纹橡胶塞密封,注射器将1.0ml干燥甲苯打入反应管中,放在140℃下搅拌6小时。反应结束,dcm/meoh=15/1为洗脱剂,将反应液快速通过短硅胶柱,溶液经真空浓缩得到粗产品。硅胶柱色谱纯化得到深棕色固体3af,收率68%。m.p.155.3-154.2℃,tlc:rf=0.5(pe/ea
=2:1).1h nmr(600mhz,cdcl3)δ7.43-7.36(m,3h),7.36-7.31(m,3h),7.32-7.26(m,4h),7.24-7.18(m,2h),7.06-7.03(m,3h),6.97-6.94(m,2h),6.86(d,j=7.8hz,1h),5.34-4.94(m,3h),4.68(s,1h),4.55(d,j=14.4hz,1h),3.17(s,3h).
13
c nmr(150mhz,cdcl3)δ170.3,165.1,163.2(d,j
c-f
=249.0hz),152.9,144.6,137.3,135.8,133.9(d,j
c-f
=8.8hz),130.4,129.1,128.7,128.6,128.4,128.1,127.5,125.7,124.3,123.1,117.2(d,j
c-f
=3.3hz),115.9(d,j
c-f
=22.1hz),108.8,87.4,81.0,58.3,51.2,50.4,45.4,26.9.hrms(esi):calcd for c
34h26
fn3na o3(m na)
requires m/z 566.1850,found m/z 566.1854.
[0044]
实施例7:
[0045][0046]
氮气保护下,在schlenk管中依次加入n-邻碘苯基脲嘧啶-5-甲酰胺1a(0.1mmol,1.0eq)、苯丙炔酸化合物2g(0.2mmol,2.0eq)、pd(pph3)4(10mol%)和kf(0.2mmol,2.0eq),螺纹橡胶塞密封,注射器将1.0ml干燥甲苯打入反应管中,放在140℃下搅拌6小时。反应结束,dcm/meoh=15/1为洗脱剂,将反应液快速通过短硅胶柱,溶液经真空浓缩得到粗产品。硅胶柱色谱纯化得到黄色固体3ag,收率86%。m.p.146.5-147.1℃,tlc:rf=0.5(pe/ea=2:1),1h nmr(400mhz,cdcl3)δ7.42-7.14(m,12h),7.04(td,j=11.4,1.8hz,1h),6.92-6.83(m,2h),6.69(dt,j=11.4,1.8hz,1h),6.59-6.58(m,1h),5.34-4.97(m,3h),4.72(s,1h),4.55(d,j=15.2hz,1h),3.76(s,3h),3.17(s,3h).
13
c nmr(100mhz,cdcl3)δ170.2,165.3,159.3,152.9,144.6,135.7,130.2,129.5,129.0,128.6,128.5,128.2,127.9,127.3,125.6,124.3,124.3,123.0,116.8,115.6,108.7,80.7,58.3,55.3,51.1,50.2,45.3,26.7.hrms(esi):calcd for c
35h29
n3nao4(m na)
requires m/z 578.2050,found m/z 578.2047.
[0047]
实施例8:
[0048][0049]
氮气保护下,在schlenk管中依次加入n-邻碘苯基脲嘧啶-5-甲酰胺1a(0.1mmol,1.0eq)、苯丙炔酸化合物2h(0.2mmol,2.0eq)、pd(pph3)4(10mol%)和kf(0.2mmol,2.0eq),螺纹橡胶塞密封,注射器将1.0ml干燥甲苯打入反应管中,放在140℃下搅拌6小时。反应结束,dcm/meoh=15/1为洗脱剂,将反应液快速通过短硅胶柱,溶液经真空浓缩得到粗产品硅胶柱色谱纯化得到黄色固体3ah,收率46%。m.p.152.8-153.1℃ tlc:rf=0.5(pe/ea=2:1)1h nmr(600mhz,cdcl3)δ7.47-7.23(m,14h),7.18(t,j=1.8hz,1h),7.13(t,j=7.8hz,1h),7.06(t,j=7.8hz,1h),7.00(d,j=1.8hz,1h),5.20-5.09(m,3h),4.66(s,1h),4.56(d,j=14.4hz,1h),3.17(s,3h).
13
c nmr(151mhz,cdcl3)δ170.0,164.9,152.7,144.5,
137.2,135.6,134.5,132.5,130.3,130.3,129.9,129.0,128.7,128.5,128.3,128.0,127.4,125.7,124.1,123.1,122.9,122.2,108.8,86.6,82.5,58.0,51.1,50.4,45.4,26.8.hrms(esi):calcd for c
34h26
brn3nao3(m na)
requires m/z 626.1050,found m/z 626.1042.
[0050]
实施例9:
[0051][0052]
氮气保护下,在schlenk管中依次加入n-邻碘苯基脲嘧啶-5-甲酰胺1a(0.1mmol,1.0eq)、苯丙炔酸化合物2i(0.2mmol,2.0eq)、pd(pph3)4(10mol%)和kf(0.2mmol,2.0eq),螺纹橡胶塞密封,注射器将1.0ml干燥甲苯打入反应管中,放在140℃下搅拌6小时。反应结束,dcm/meoh=15/1为洗脱剂,将反应液快速通过短硅胶柱,溶液经真空浓缩得到粗产品。硅胶柱色谱纯化得到黄色固体3ai,收率51%。m.p.182.4-182.6℃,tlc:rf=0.5(pe/ea=2:1),1h nmr(600mhz,cdcl3)δ7.42-7.21(m,12h),7.06-7.02(m,2h),6.88-6.86(m,2h),6.74-6.72(m,1h),5.22-5.09(m,3h),4.68(s,1h),4.56(d,j=15.0hz,1h),3.17(s,3h).
13
c nmr(150mhz,cdcl3)δ170.2,165.0,162.3(d,j
c-f
=247.3hz),152.9,144.6,137.3,135.8,130.4,130.2(d,j
c-f
=8.3hz),129.1,128.8,128.6,128.4,128.1,127.8(d,j
c-f
=3.4hz),127.5,125.7,124.2,123.2,122.8(d,j
c-f
=9.8hz),118.7(d,j
c-f
=23.1hz),116.9(d,j
c-f
=21.0hz),108.8,87.0,82.1,58.2,51.2,50.5,45.5,26.9.hrms(esi):calcd for c
34h26
fn3nao3(m na)
requires m/z 566.1850,found m/z 566.1844.
[0053]
实施例10:
[0054][0055]
氮气保护下,在schlenk管中依次加入n-邻碘苯基脲嘧啶-5-甲酰胺1a(0.1mmol,1.0eq)、苯丙炔酸化合物2j(0.2mmol,2.0eq)、pd(pph3)4(10mol%)和kf(0.2mmol,2.0eq),螺纹橡胶塞密封,注射器将1.0ml干燥甲苯打入反应管中。将反应管放在140℃下搅拌6小时。反应结束,dcm/meoh=15/1为洗脱剂,将反应液快速通过短硅胶柱,溶液经真空浓缩得到粗产品。硅胶柱色谱纯化得到黄色固体3aj,收率67%。m.p.146.1-147.1℃,tlc:rf=0.5(pe/ea=2:1)1h nmr(400mhz,cdcl3)δ7.43-7.29(m,7h),7.27-7.17(m,4h),7.12-7.07(m,3h),7.02(td,j=11.4,1.8hz,1h),6.85(d,j=7.6hz,1h),5.32(d,j=14.8hz,1h),5.11(dd,j=14.0,31.2hz,2h),4.90(s,1h),4.57(d,j=14.8hz,1h),3.18(s,3h),1.97(s,3h).
13
c nmr(100mhz,cdcl3)δ170.5,165.3,152.9,144.7,140.6,137.2,135.9,132.5,130.3,129.6,129.4,128.9,128.7,128.6,128.5,127.9,127.5,125.7,125.3,124.5,123.1,120.9,109.0,58.6,51.3,50.1,45.4,26.8,20.3.hrms(esi):calcd for c
35h29
n3nao3(m
na)
requires m/z 562.2101,found m/z 562.2103.
[0056]
实施例11:
[0057][0058]
氮气保护下,在schlenk管中依次加入n-邻碘苯基脲嘧啶-5-甲酰胺1a(0.1mmol,1.0eq)、苯丙炔酸化合物2k(0.2mmol,2.0eq)、pd(pph3)4(10mol%)和kf(0.2mmol,2.0eq),螺纹橡胶塞密封,注射器将1.0ml干燥甲苯打入反应管中,放在140℃下搅拌6小时。反应结束后,用dcm/meoh=15/1为洗脱剂,将反应液快速通过短硅胶柱,溶液经真空浓缩得到粗产品。硅胶柱色谱纯化,得到黄色固体3ak,收率85%。m.p.134.6-135.2℃,tlc:rf=0.5(pe/ea=2:1)1h nmr(400mhz,cdcl3)δ7.90-7.75(m,2h),7.49-7.17(m,17h),7.08(td,j=11.4,1.2hz,1h),6.89(d,j=7.6hz,1h),5.37(d,j=15.2hz,1h),5.20-5.06(m,3h),4.64(d,j=14.8hz,1h),3.16(s,3h).
13
c nmr(100mhz,cdcl3)δ170.6,165.3,152.9,144.8,137.1,135.9,133.1,132.9,131.4,130.3,129.9,128.9,128.7,128.5,128.4,128.3,128.0,127.4,127.1,126.6,125.5,125.1,125.1,124.5,123.1,118.6,109.1,87.0,85.0,58.7,51.4,50.1,45.4,26.8.hrms(esi):calcd for c
38h30
n3o3(m h)
requires m/z 576.2282,found m/z 576.2277.
[0059]
实施例12:
[0060][0061]
在0℃下,向化合物3(44.1mg,0.1mmol)/dmf(1ml)溶液中加入t-buok(10mg,0.1mmol),然后在室温下搅拌反应。通过tlc监测反应。反应结束,水和乙酸乙酯萃取,饱和食盐水溶液洗涤,无水硫酸镁干燥,减压浓缩,将其通过柱色谱法纯化得到产品4,收率61%。tlc:rf=0.5(pe/ea=2:1),1h nmr(600mhz,cdcl3)7.46(d,j=7.2hz,2h),7.33(t,j=7.2hz,2h),7.28-7.22(m,4h),7.18-7.09(m,9h),7.00(d,j=7.2hz,1h),6.84(t,j=7.2hz,1h),6.77-6.71(m,3h),6.55(s,1h),5.15(dd,j=24.6,13.8hz,2h),4.99(d,j=15.0hz,1h),4.73(d,j=15.0hz,1h),3.09(s,3h).
13
c nmr(150mhz,cdcl3)δ194.9,170.1,164.7,150.9,143.7,137.0,136.3,132.6,130.0,128.9,128.6,128.6,128.4,128.3,127.7,127.7,127.5,127.5,123.9,123.2,111.5,109.0,108.8,50.5,45.9,29.8,26.9.hrms(esi):calcd for c
34h27
n3nao3(m na)
requires m/z 548.1945,found m/z 548.1949.
[0062]
以上实施例描述了本发明的基本原理、主要特征及优点。本行业的技术人员应该了解,本发明不受上述实例的限制,上述实例和说明书中描述的只是说明本发明的原理,在不脱离本发明原理的范围下,本发明还会有各种变化和改进,这些变化和改进均落入本发
明保护的范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。
