基于数字pcr一步法检测血液中登革热、寨卡病毒的方法
技术领域
1.本发明涉及生物试剂领域,尤其涉及利用生物试剂定性定量检测现有病毒的方法技术领域,具体涉及基于数字pcr一步法检测血液中登革热、寨卡病毒的方法。
背景技术:
2.登革病毒(dengue virus,denv)和寨卡病毒(zika virus,zikv均是蚊虫媒介传播的黄病毒科、黄病毒属病毒,均属于单正链rna病毒,全长约11kb。登革热病毒包括四个血清型,常引起登革热,甚至发展为登革出血热及登革休克综合征,广泛分布于热带和亚热带地区,发热、头痛、全身肌肉及关节痛等为其主要临床特征。寨卡病毒病是寨卡病毒引起的,临床表现为轻微发热、红疹(多数为斑丘疹)、头痛、关节痛以及结膜炎等,也会引起小头畸形、格林巴利综合症以及其他胎儿中枢神经系统畸形。who曾将寨卡病毒感染及其相关新生儿小头畸形等神经系统疾病列为“国际关注的突发公共卫生事件”。
3.数字pcr(digital pcr,dpcr)技术是一种全新的核酸定量方法,通过将普通pcr的指数信号转化为数字信号,从而对样本中的病毒达到绝对定量效果。数字pcr主要是将总的模板pcr反应体系进行分液,分配为许多单独的pcr反应,使其在许多反应室中进行pcr扩增;pcr扩增完后,通过检测每个反应的荧光信号的有或无来计算模板的拷贝数,最后通过泊松分布的统计学处理,得到样品中病毒dna或rna的浓度。相比较于实时荧光定量pcr技术,数字pcr不需要建立标准曲线,并对低浓度的临床样本定量检测。现有的数字pcr需要先提取样本核酸过程,传统数字pcr一般是先进行样本核酸提取,再接着进行反转录,反转录后构建数字pcr反应体系。
技术实现要素:
4.为了解决现有数字pcr技术存在需要进行核算提取、转录的问题,本技术提供基于数字pcr一步法检测血液中登革热、寨卡病毒的方法,能够广泛的捕捉寨卡病毒和登革热病毒并进行定量检测。
5.为了达到上述目的,本技术所采用的技术方案为:
6.基于数字pcr一步法检测血液中登革热、寨卡病毒的方法,具体由以下步骤组成:
7.步骤stp100,取90ul待检测的血液样本y0,10ul的pcr反应液a混合,自然反应10min后获得血液样本y1;其中,pcr反应液a由10mg/ml莎梵婷,2%的sds(m/v),0.1%的np-40(v/v)和150mmol/l的mgcl2组成;
8.步骤stp200,取25ul步骤stp100中获得的血液样本y1并向血液样本y1中分别按照15:6:4的比例加入pcr反应液b、pcr反应液c、pcr反应液d,同时加入乳化剂振荡摇匀获得血液样本y2;
9.其中,pcr反应液b由5mmol/l mg cl2,ph=8.3,33mmol/l的tris-hcl,0.66mmol/l的dgtp,0.66mmol/l的datp 0.66mmol/l的dctp,0.4mmol/l的dttp和0.66mmol/l的dutp组成;
10.pcr反应液c由80u/ul反转录酶、8u/ul的taq dna聚合酶、0.08的mdtt、ph=7.4,4mmol/l的tris-hcl;40mmol/l的nacl;16u/ml的rnase inhibitor组成;
11.pcr反应液d由登革热引物对:引物-f:seq id no:1,引物-r:seq id no:2和探针:seq id no:5;以及寨卡病毒引物对:引物-f:seq id no:3,引物-r:seq id no:4和探针:seq id no:6组成;
12.乳化剂为体积比为6:4的硅油和16烷烃混合物,再加入4%的em90 2%的tritonx-100和2%的吐温-20混合摇匀获得;
13.步骤stp300,将血液样本y2加入微滴式数字pcr仪生成微滴进行pcr扩增并输出检测结果;其中,pcr扩增程序如下:
14.①
逆转录,温度为37℃,时间保持30min,反应循环数为1次;
15.②
预变性,温度为95℃,时间保持10min,反应循环数为1次;
16.③
变性,温度为95℃,时间保持30s,反应循环数为40次;
17.④
退火,温度为55℃,时间保持15s,反应循环数为40次;
18.⑤
延伸,温度为72℃,时间保持40s,反应循环数为40次;
19.⑥
灭活,温度为98℃,时间保持10min,反应循环数为1次;
20.⑦
hold,温度为4℃,时间保持 ∞min,反应循环数为1次。
21.有益效果:
22.1、本发明克服了数字pcr需要先提取样本核酸过程,传统数字pcr需要先进行样本核酸提取,再接着进行反转录,反转录后构建数字pcr反应体系需要繁琐操作,检测流程复杂的问题,本发明直接利用pcr反应体系与待测样本混合即可利用现有的数字pcr仪进行一步检测,过程简单,操作简便。
23.2、本发明克服了乳化剂与扩增试剂形成油滴后,不能在同一反应体系中先反转录再扩增的技术难题,本方案利用pcr扩增反应液a中的np40作用与乳化剂相结合,有效形成液滴具有大小均一、热稳定性好、不易产生气泡、不易挥发、不抑制扩增的油包水形态。
24.3、本发明设定的pcr程序中利用扩增反应体系中处于37℃作用的逆转录反应体系,直接进行rna逆转录反应,反应30分钟,结束后执行数字pcr反应,本方案是将扩增体系中的引物退火温度设置在55度,低于55度便不会存在pcr退火阶段,故扩增体系可以先进行逆转录,逆转录结束后可进行数字pcr过程。
附图说明
25.为了更清楚地说明本技术实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本技术的一些实施例,对于本领域技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
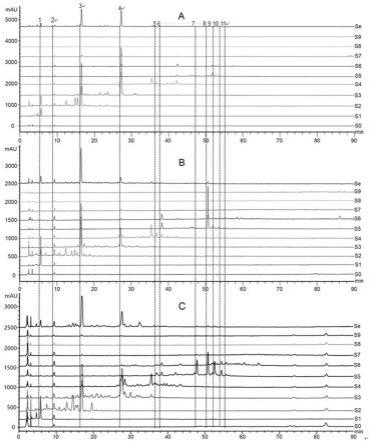
26.图1是实施例1中带登革热病毒阳性质控品样本检测结果。
27.图2是实施例1中带寨卡病毒阳性质控品样本检测结果。
28.图3是实施例1中纯阴性样本检测结果。
具体实施方式
29.为使本技术实施例的目的、技术方案和优点更加清楚,下面将结合本技术实施例中的附图,对本技术实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例是本技术一部分实施例,而不是全部的实施例。通常在此处附图中描述和示出的本技术实施例的组件可以以各种不同的配置来布置和设计。
30.因此,以下对在附图中提供的本技术的实施例的详细描述并非旨在限制要求保护的本技术的范围,而是仅仅表示本技术的选定实施例。基于本技术中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本技术保护的范围。
31.实施例1:
32.本实施例利用市售质控品分别进行实验检测,本实施例采用的质控品为阳性血浆样本,本实施例采用型号为qx200微滴式数字pcr仪,具体检测方法如下:
33.基于数字pcr一步法检测血液中登革热、寨卡病毒的方法,具体由以下步骤组成:
34.步骤stp100,取90ul待检测的血液样本y0,10ul的pcr反应液a混合,自然反应10min后获得血液样本y1;其中,pcr反应液a由10mg/ml莎梵婷,2%的sds(m/v),0.1%的np-40(v/v)和150mmol/l的mgcl2组成;
35.步骤stp200,取25ul步骤stp100中获得的血液样本y1并向血液样本y1中分别按照15:6:4的比例加入pcr反应液b、pcr反应液c、pcr反应液d,同时加入乳化剂振荡摇匀获得血液样本y2;
36.其中,pcr反应液b由5mmol/l mg cl2,ph=8.3,33mmol/l的tris-hcl,0.66mmol/l的dgtp,0.66mmol/l的datp 0.66mmol/l的dctp,0.4mmol/l的dttp和0.66mmol/l的dutp组成;
37.pcr反应液c由80u/ul反转录酶、8u/ul的taq dna聚合酶、0.08的mdtt、ph=7.4,4mmol/l的tris-hcl;40mmol/l的nacl;16u/ml的rnase inhibitor组成;
38.pcr反应液d由登革热引物对:引物-f:seq id no:1,引物-r:seq id no:2和探针:seq id no:5;以及寨卡病毒引物对:引物-f:seq id no:3,引物-r:seq id no:4和探针:seq id no:6组成;本实施例中分别选取登革病毒的ns5区域、寨卡病毒基因ns1蛋白序列引物探针的靶序列。详见表1-表2所示:
39.本实施例中所述引物具体如表1所示:
[0040][0041][0042]
表1
[0043]
本实施例中探针具体如表2所示:
[0044][0045]
表2
[0046]
乳化剂为体积比为6:4的硅油和16烷烃混合物,再加入4%的em90 2%的tritonx-100和2%的吐温-20混合摇匀获得;
[0047]
步骤stp300,将血液样本y2加入微滴式数字pcr仪生成微滴进行pcr扩增并输出检测结果;其中,pcr扩增程序如下:
[0048]
①
逆转录,温度为37℃,时间保持30min,反应循环数为1次;
[0049]
②
预变性,温度为95℃,时间保持10min,反应循环数为1次;
[0050]
③
变性,温度为95℃,时间保持30s,反应循环数为40次;
[0051]
④
退火,温度为55℃,时间保持15s,反应循环数为40次;
[0052]
⑤
延伸,温度为72℃,时间保持40s,反应循环数为40次;
[0053]
⑥
灭活,温度为98℃,时间保持10min,反应循环数为1次;
[0054]
⑦
hold,温度为4℃,时间保持 ∞min,反应循环数为1次。
[0055]
本实施例中,所述乳化剂采用硅油为主要成分,具有非极性不溶于水、不易挥发、性质稳定、对pcr扩增无抑制作用、轻质油运动粘度较低等优点,同时,通过添加合适比例14~16烷烃降低运动粘度,再添加合适的表面活性剂em90属硅酮表面活性剂,硅氧烷链上接聚氧乙烯醚链,以peg作为亲水基,聚硅氧烷作为亲油基,tritonx-100非离子型表面活性剂,最终,使用本发明油相组合物来制备液滴,所得液滴具有大小均一、热稳定性好、不易产生气泡、不易挥发、不抑制扩增等优点。
[0056]
本实施例中通过调节莎梵婷/np-40的浓度,有效避免对pcr扩增的影响,传统核酸提取试剂中的胍盐等强去垢剂物质会抑制pcr扩增,本体系中的莎梵婷/np-40柔和去垢剂通过浓度的调节对pcr反应影响极低,故可以放置扩增试剂a中,用于核酸免提取过程。同时,本实施例采用的乳化剂与扩增试剂形成油滴后,解决了不能在同一反应体系中先反转录再扩增的技术难题,本方案利用pcr扩增反应液a中的np40作用与乳化剂相结合,有效形成液滴具有大小均一、热稳定性好、不易产生气泡、不易挥发、不抑制扩增的油包水形态,同时利用扩增反应体系中处于37℃作用的逆转录反应体系,直接进行rna逆转录反应,反应30分钟,结束后执行数字pcr反应,本方案是将扩增体系中的引物退火温度设置在55度,低于55度便不会存在pcr退火阶段,故扩增体系可以先进行逆转录,逆转录结束后可进行数字pcr过程。
[0057]
按照上述检测方法,分别取带有登革热病毒和寨卡病毒的质控品进行检测,获得检测结果如图1和图2所示;同时,按照相同的程序设定,增加一组纯阴性样本进行检测,获得检测结果如图3所示。由上可知,本发明提供的pcr反应体系和程序设定依靠现有数字pcr仪器和本发明提供的引物、探针能够广泛捕捉登革热病毒和寨卡病毒。相较于现有技术而言,省略了裂解、提取、逆转录等流程,在保证精准检测目的的前提下,效率大大提高了检测效率。
[0058]
以上所述仅为本技术的优选实施例而已,并不用于限制本技术,对于本领域的技术人员来说,本技术可以有各种更改和变化。凡在本技术的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本技术的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。