胎儿染色体非整倍体多重数字pcr检测的引物、探针及其试剂盒和应用
技术领域
1.本发明属于产前诊断技术领域,特别涉及一种胎儿染色体非整倍体pcr检测的引物、探针及其试剂盒和应用,尤其涉及一种胎儿染色体非整倍体多重数字pcr检测的引物、探针及其试剂盒和应用。
背景技术:
2.在众多染色体异常疾病中,染色体非整倍体导致的残疾及生活障碍尤为明显。目前最常见的染色体疾病是21三体综合症(唐氏综合症),其新生儿发病率为1/700-1/600。除唐氏综合症之外,13三体综合症(帕陶综合症)的活婴发病率为1/2000,女性多于男性,患儿母亲平均生育年龄为31岁。18三体综合症(爱德华氏综合症)的活婴发病率为1/4000,女性多见患者母亲平均生育年龄为34岁。目前,产前的胎儿非整倍检测,主要通过基于血清学检测的唐氏筛查进行初筛,风险较高的孕妇也可采用羊水穿刺方法获取细胞,进而采用细胞生物学的方法进行核型分析,这一流程被视为金标准,但因其有创性,对孕妇宫内感染、早产及流产存在一定的风险,限制其广泛应用于临床。此外,细胞遗传学诊断也存在耗时长、培养难度高以及不能检测较小的染色体结构畸变等缺点。因此,基于高通量测序的无创产前诊断技术(nipt)开始在临床上开展应用,目前已被广泛用于高龄产妇的三体筛查及遗传病检测中;通过抽取孕妇血液,对血液中的游离dna进行处理分析来判断染色体异常情况,其主要缺点在于需要专业的操作人员对样本进行复杂的建库操作,该操作容易导致信息丢失造成假阴性或假阳性的问题、ngs设备成本以及使用成本昂贵以及后续分析方式复杂等问题,具有检测成本较高,耗时较长,操作复杂需要专业的操作员等原因,也限制了其临床应用,目前只有比较专业的临床检验机构例如医学检验所等进行检测,普通临床实验室难以进行实验操作和数据分析。因此需要一种更简便、成本低廉的方法用于无创产前筛查领域。
3.数字pcr技术是通过将微量样品作大倍数稀释和分液,直至每个样品中所含有的待测分子数不会超过1个拷贝,再将所有样品在相同条件下进行pcr扩增,并对发生了扩增反应的样品逐个进行计数的一种技术。数字pcr是一种核酸分子绝对定量技术,可以dna拷贝数进行精确定量分析。现有基于多重数字pcr平台的检测方案(例如,一种用于检测胎儿染色体非整倍体的试剂盒、引物和探针序列及检测方法-cn105695567b、一种从母体外周血检测胎儿非整倍体染色体的方法及其试剂盒-cn108342455a等)主要缺点在于部分方案设计检测靶标区域不足,需要通过增加样本投入量的方法提高检出率,以及设计方法基于常规pcr设计方案,即每个检测靶标区域需要一对引物和一条探针的方式,其缺点在于探针成本高。因而,期望能够提供一种基于多重数字pcr检测方法,可以非侵入性、高灵敏度、高准确性地鉴定胎儿染色体非整倍体的试剂盒和方法,以便于临床的推广引用。
技术实现要素:
4.本发明的目的是提供一种胎儿染色体非整倍体多重数字pcr检测的引物、探针及其试剂盒和应用,克服了ngs技术平台耗时长、成本高和技术操作要求高,以及常规多重数字pcr需要设计和使用多条检测探针导致的成本高,设计难度高等缺点;本发明可使用但不限于使用孕周5~8周的宫颈脱落细胞或其他含有胎儿dna的样本,避免有创取样导致的流产情况,是一种操作简单、成本低、时效快且准确度高的试剂盒及检测方法,可用于多重数字pcr平台检测胎儿染色体拷贝数变异现象。
5.为此,本发明技术方案如下:
6.第一方面,本发明提供一种胎儿染色体非整倍体多重数字pcr检测的引物和探针,包括:
7.用于检测第21号染色体非整倍体的seq id no.1-40所示核苷酸序列的引物和seq id no.121所示核苷酸序列的探针;
8.用于检测第18号染色体非整倍体的seq id no.41-80所示核苷酸序列的引物和seq id no.122所示核苷酸序列的探针;
9.用于检测第13号染色体非整倍体的seq id no.81-120所示核苷酸序列的引物和seq id no.123所示核苷酸序列的探针。
10.为保证较高的检测信号同时提高检测准确性,本发明最终在13、18和21号染色体上分别筛选出了20个待测靶标区域以及设计对应的引物探针,这些待测靶标区域的特征如下:
11.(1)待测靶标区域引物结合区不包含已知常见的snp位点,保证引物不受snp位点影响而导致结合效率不一致;
12.(2)待测靶标区域不发生常见的cnv(copy number variations,即基因拷贝数变异),正常细胞内拷贝数一致;
13.(3)同一染色体相邻两个待测靶标区域间隔大于10000bp,保证各待测靶标区域互相独立工作且所述20个待测靶标区域均匀的分布于待测染色体;
14.(4)同一染色体待测靶标区域内至少有连续10个碱基序列一致,这段序列存在但不限于存在于该染色体,其他染色体待测靶标区域不存在该相同序列;同一染色体待测靶标区域内连续10个碱基一致的区域即为探针结合区,这样做打破了常规pcr设计一对引物对应一个探针的设计方案,解决了探针修饰昂贵的问题同时减少考虑探针相互作用的问题;
15.(5)gc含量为40-60%且无重复序列,保证待测靶标区域扩增效率尽可能一致;
16.(6)待测靶标区域长度为60-100bp,较短的待测靶标区域长度能确保在短的退火时间内充分得到扩增同时也兼容胎儿游离dna检测;
17.另外,本发明筛选扩增效率一致且阴性阳性微滴明显分离的引物,最终选定的chr21、chr18、chr13非整倍体检测用引物和探针序列如表1所示。
18.表1引物和探针序列
19.20.21.22.[0023][0024]
优选的,所述探针的5’端连接荧光报告基团,3’端淬灭基团连接;
[0025]
优选的,所述探针加入了lna修饰和/或mgb修饰,用以提高探针结合效率,同时保证探针退火温度高于引物的退火温度;
[0026]
优选的,用于检测21号染色体的探针5’端标记为fam荧光修饰,3’端标记为bhq1淬灭修饰;
[0027]
优选的,用于检测18号染色体的探针5’端标记为hex荧光修饰,3’端标记为bhq1淬灭修饰;
[0028]
优选的,用于检测13号染色体的探针5’端标记为rox荧光修饰,3’端标记为bhq2淬灭修饰。
[0029]
第二方面,本发明提供如第一方面所述的引物和探针在制备胎儿染色体非整倍体多重数字pcr检测的试剂盒中的应用。
[0030]
第三方面,本发明提供一种胎儿染色体非整倍体多重数字pcr检测的试剂盒,包括如第一方面所述的引物和探针。
[0031]
优选的,所述试剂盒还包括pcr反应液;所述pcr反应液至少包括无核酸酶水、缓冲液buffer和taq酶。
[0032]
第四方面,本发明提供一种胎儿染色体非整倍体多重数字pcr检测的方法,至少包括以下步骤:
[0033]
1)对待测样品进行处理,提取脱落细胞dna或血浆游离dna;
[0034]
2)利用本发明所述的试剂盒以及所述提取的dna(即提取的脱落细胞dna或血浆游离dna),配制多重数字pcr扩增反应液;
[0035]
3)将所述反应液置于多重数字pcr设备中,生成液滴并进行pcr扩增、拍照以及数据分析;
[0036]
4)分别获得fam、hex和rox荧光通道检测结果,分别计算提取的dna中21、18和13号染色体的拷贝数比值,通过统计学方法判定胎儿是否存在13、18或21号染色体非整倍体疾病。
[0037]
优选的,步骤1)所述待测样品为含有胎儿dna的样品,优选为孕周5-8周的孕妇宫颈脱落细胞。
[0038]
优选的,步骤2)所述多重数字pcr扩增反应液中,每对所述引物的终浓度为100-400nm,例如可以是100nm、125nm、150nm、175nm、200nm、225nm、250nm、275nm、300nm、325nm、350nm、375nm、400nm或所述范围内的所有取值,由于篇幅的限制不再赘述;所述探针的终浓
度为100-400nm,例如可以是100nm、125nm、150nm、175nm、200nm、225nm、250nm、275nm、300nm、325nm、350nm、375nm、400nm或所述范围内的所有取值,由于篇幅的限制不再赘述;
[0039]
优选的,按总体积25ul计算,所述多重数字pcr扩增反应液配方包括:缓冲液buffer12.5ul、taq酶0.6ul、无核酸酶水5-7ul和提取的dna1-2.5ul。
[0040]
优选的,步骤3)所述多重数字pcr程序为:
[0041]
95℃预变性10分钟;45个循环94℃变性10秒,58-60℃退火延伸1分钟;98℃酶灭活5分钟;35℃保温。其中,退火温度可以是58℃、58.2℃、58.4℃、58.6℃、58.8℃、59℃、59.2℃、59.4℃、59.6℃、59.8℃、60℃或所述范围内的所有取值,由于篇幅的限制不再赘述;
[0042]
优选的,为了提高检测的准确性,检测判定的参照对象是同一检测样本的其他两个染色体的检测结果,步骤4)所述判定的方法为:
[0043]
阴性样本的判定:当13、18或21号染色体各自与其他两个染色体的拷贝数比例为0.95-1.05(例如可以是0.95、0.96、0.97、0.98、0.99、1.00、1.01、1.02、1.03、1.04、1.05或所述范围内的所有取值,由于篇幅的限制不再赘述)时,则检测样本不存在13、18或21号染色体的拷贝数变异情况;
[0044]
阳性样本的判定:当13、18或21号染色体各自与其他两个染色体的拷贝数比例为1.05-1.5(例如可以是1.05、1.06、1.07、1.08、1.09、1.10、1.11、1.12、1.13、1.14、1.15、1.20、1.25、1.30、1.35、1.40、1.45、1.50或所述范围内的所有取值,由于篇幅的限制不再赘述)时,则检测样本存在13、18或21号染色体的拷贝数变异情况。
[0045]
与现有技术相比,本发明提供的胎儿染色体非整倍体多重数字pcr检测的引物、探针及其试剂盒的检测过程耗时短,使用至少60对引物同时检测13、18和21号染色体,避免因样本质量问题及扩增过程中碱基突变产生的检测误差。本发明的检测成本低,不需要复杂的数据分析,能准确的测定检测样本染色体拷贝数情况。
附图说明
[0046]
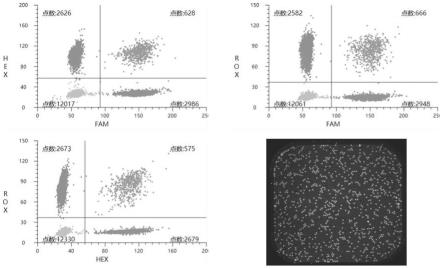
图1为实施例1中含30%的21三体dna的混合dna在检测平台a的检测结果图。
[0047]
图2为实施例2中含20%的21三体dna的混合dna在检测平台a的检测结果图。
[0048]
图3为实施例3中含10%的21三体dna的混合dna在检测平台a的检测结果图。
[0049]
图4为实施例4中含5%的21三体dna的混合dna在检测平台a的检测结果图。
[0050]
图5为实施例5中含2.5%的21三体dna的混合dna在检测平台a的检测结果图。
[0051]
图6为实施例6中含0%的21三体dna的混合dna在检测平台a的检测结果图。
[0052]
图7为实施例7中含30%的18三体dna的混合dna在检测平台a的检测结果图。
[0053]
图8为实施例8中含20%的18三体dna的混合dna在检测平台a的检测结果图。
[0054]
图9为实施例9中含10%的18三体dna的混合dna在检测平台a的检测结果图。
[0055]
图10为实施例10中含5%的18三体dna的混合dna在检测平台a的检测结果图。
[0056]
图11为实施例11中含2.5%的18三体dna的混合dna在检测平台a的检测结果图。
[0057]
图12为实施例12中含0%的18三体dna的混合dna在检测平台a的检测结果图。
[0058]
图13为实施例13中含30%的13三体dna的混合dna在检测平台a的检测结果图。
[0059]
图14为实施例14中含20%的13三体dna的混合dna在检测平台a的检测结果图。
[0060]
图15为实施例15中含10%的13三体dna的混合dna在检测平台a的检测结果图。
[0061]
图16为实施例16中含5%的13三体dna的混合dna在检测平台a的检测结果图。
[0062]
图17为实施例17中含2.5%的13三体dna的混合dna在检测平台a的检测结果图。
[0063]
图18为实施例18中含0%的13三体dna的混合dna在检测平台a的检测结果图。
[0064]
图19为实施例1~6含不同比例21三体dna的混合dna在检测平台a的数据分析图。
[0065]
图20为实施例7~12含不同比例18三体dna的混合dna在检测平台a的数据分析图。
[0066]
图21为实施例13~18含不同比例13三体dna的混合dna在检测平台a的数据分析图。
[0067]
图22为实施例1中含30%的21三体dna的混合dna在检测平台b的检测结果图。
[0068]
图23为实施例7中含30%的18三体dna的混合dna在检测平台b的检测结果图。
[0069]
图24为实施例13中含30%的13三体dna的混合dna在检测平台b的检测结果图。
[0070]
图25为实施例1、7和13在检测平台b的数据分析图。
具体实施方式
[0071]
下面详细描述本发明的实施例,所述实施例的示例在附图中示出,其中自始至终相同或类似的标号表示相同或类似的元件或具有相同或类似功能的元件。下面通过参考附图描述的实施例是示例性的,旨在用于解释本发明,而不能理解为对本发明的限制。
[0072]
在本说明书的描述中,参考术语“一个实施例”、“一些实施例”、“示例”、“具体示例”、或“一些示例”等的描述意指结合该实施例或示例描述的具体特征、结构、材料或者特点包含于本发明的至少一个实施例或示例中。在本说明书中,对上述术语的示意性表述不必须针对的是相同的实施例或示例。而且,描述的具体特征、结构、材料或者特点可以在任何的一个或多个实施例或示例中以合适的方式结合。此外,本领域的技术人员可以将本说明书中描述的不同实施例或示例进行接合和组合。
[0073]
pcr反应体系的配制
[0074]
按表2配方制备数字pcr平台a反应体系(1个反应)。按表3配方制备数字pcr平台b反应体系(1个反应)。
[0075]
表2数字pcr平台a反应液配方表
[0076][0077]
表3数字pcr平台b反应液配方表
[0078][0079][0080]
实施例1-18
[0081]
使用已验证为13、18和21号三体综合征的样本dna和验证为无13、18和21号三体综合征的样本dna,所述样本均采购于coriell institute,通过qubit进行浓度定量,将两种dna稀释至相同浓度,并按不同比例进行混合。含30%、20%、10%、5%、2.5%和0%的21三体dna,标记为实施例1、实施例2、实施例3、实施例4、实施例5和实施例6;含30%、20%、10%、5%、2.5%和0%的18三体dna,标记为实施例7、实施例8、实施例9、实施例10、实施例11和实施例12;含30%、20%、10%、5%、2.5%和0%的13三体dna,标记为实施例13、实施例14、实施例15、实施例16、实施例17和实施例18,用来模拟不同三体胎儿细胞含量的样本。
[0082]
其中,表2和表3中的dna即为实施例1-18的dna,按上述表格配制完反应液后,涡旋混匀、离心后备用。
[0083]
检测平台a的检测方法及结果
[0084]
检测平台a为北京达微生物科技有限公司检测平台。将实施例1-18的各25ul反应液置于北京达微生物科技有限公司数字pcr液滴发生装置,并在液滴生成芯片内加入8ml液滴生成油,启动液滴生成程序,生成液滴数约为1.8-2万个;
[0085]
待液滴生成完毕后,取出芯片,按要求贴上芯片专用封口膜,之后转移至芯片pcr仪进行扩增;
[0086]
北京达微生物科技有限公司数字pcr的反应条件是:95℃预变性10分钟;45个循环94℃变性10秒,58℃退火延伸1分钟;98℃酶灭活5分钟;35℃保温;
[0087]
反应结束后使用北京达微生物科技有限公司数字pcr荧光阅读仪进行拍照获取原始数据;
[0088]
使用北京达微生物科技有限公司数字pcr数据分析系统进行结果分析,获得所测样本21号染色体、18号染色体和13号染色体检测结果(分别为fam、hex和rox荧光通道检测结果),该平台各实施例检测结果和比例计算结果示于图1-图21。由图1-图6可知,含不同比例21号三体综合征样本的实施例1-6的检测效果稳定,各阳性微滴簇和阴性微滴簇明显区分;由图19和表4(分别为a平台21三体样本参比检测数据及其分析图)可知,随着异常样本的百分比增加,计算所得的比例随之提高,与预期比例结果有良好的相关性;由图7-图12可
知,含不同比例18号三体综合征样本的实施例7-12的检测效果稳定,各阳性微滴簇和阴性微滴簇明显区分;由图20和表5(分别为a平台18三体样本参比检测数据及其分析图)可知,随着异常样本的百分比增加,计算所得的比例随之提高,与预期比例结果有良好的相关性;由图13-图18可知,含不同比例13号三体综合征样本的实施例13-18的检测效果稳定,各阳性微滴簇和阴性微滴簇明显区分;由图21和表6(分别为a平台13三体样本参比检测数据分析图)可知,随着异常样本的百分比增加,计算所得的比例随之提高,与预期比例结果有良好的相关性。
[0089]
检测平台b的检测方法及结果
[0090]
检测平台b为苏州锐讯生物科技有限公司检测平台。将上述实施例1、实施例7和实施例13的各25ul反应液置于苏州锐讯生物科技有限公司数字pcr液滴发生芯片样本孔内,并在液滴生成芯片油相孔中加入75ul液滴生成油,最后在样本孔上方加入10ul密封油,启动液滴生成程序和pcr程序,生成液滴数约为1.3-1.5万个;
[0091]
所述苏州锐讯生物科技有限公司数字pcr的反应条件是:95℃预变性10分钟;45个循环94℃变性10秒,58℃退火延伸1分钟;98℃酶灭活5分钟;35℃保温;
[0092]
反应结束后使用苏州锐讯生物科技有限公司数字pcr荧光阅读仪进行拍照及数据分析,获得所测样本21号染色体、18号染色体和13号染色体检测结果(分别为fam、hex和rox荧光通道检测结果),该平台各实施例检测结果和比例计算结果示于表7-9以及图22-图25。由图22可知含30%比例21号三体综合征样本的实施例1的检测效果稳定,各阳性微滴簇和阴性微滴簇明显区分;由图23可知含30%比例18号三体综合征样本的实施例7的检测效果稳定,各阳性微滴簇和阴性微滴簇明显区分;由图24可知含30%比例13号三体综合征样本的实施例13的检测效果稳定,各阳性微滴簇和阴性微滴簇明显区分。由表7-9和图25可知,使用相同的检测体系,实施例1、7和13在检测平台b的检测效果稳定且与检测平台a检测结果一致均接近预期检测结果。
[0093]
从上述结果可以看出,本发明的胎儿染色体非整倍体多重数字pcr检测的引物、探针及其试剂盒和应用,克服了ngs技术平台耗时长、成本高和技术操作要求高,以及常规多重数字pcr需要设计和使用多条检测探针导致的成本高,设计难度高等缺点;本发明可使用但不限于使用孕周5~8周的宫颈脱落细胞或其他含有胎儿dna的样本,避免有创取样导致的流产情况,是一种操作简单、成本低、时效快且准确度高的试剂盒及检测方法,可用于至少2种数字pcr平台的多重数字pcr平台检测胎儿染色体拷贝数变异现象。
[0094]
表4 t21样本参比测试结果
[0095][0096]
*p<0.05 **p<0.01
[0097]
表5 t18样本参比测试结果
[0098][0099]
*p<0.05 **p<0.01
[0100]
表6 t13样本参比测试结果
[0101][0102]
*p<0.05 **p<0.01
[0103]
表7实施例1测试结果
[0104][0105]
表8实施例7测试结果
[0106][0107]
表9实施例13测试结果
[0108][0109]
应该注意到并理解,在不脱离后附的权利要求所要求的本发明的精神和范围的情况下,能够对上述详细描述的本发明做出各种修改和改进。因此,要求保护的技术方案的范围不受所给出的任何特定示范教导的限制。
[0110]
申请人声明,以上内容是结合具体的优选实施方式对本发明所作的进一步详细说明,不能认定本发明的具体实施只局限于这些说明。对于本发明所属技术领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干简单推演或替换,都应当视为属于本发明的保护范围。
[0111]
序列表
[0112]
[0113]
[0114]
[0115][0116]
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。