1.本发明涉及微生物学,具体涉及肠道微生物及其作为心脏移植免疫排斥或耐受的诊断标志物或治疗靶标。
背景技术:
2.心脏移植是治疗晚期心力衰竭、终末期冠状动脉疾病等的一种有效方案。心脏移植挽救了许多终末期心脏病患者的生命,但移植后免疫排斥反应仍然是心脏移植患者长期生存的主要问题。
3.目前颈静脉心内膜心肌活检是临床检验心脏移植排斥反应的主要方式,存在检验后并发症多、诊断费用高、缺乏早期诊断等局限性。免疫抑制治疗是目前预防和治疗心脏移植免疫排斥反应的主要手段,临床通常使用三联疗法来预防和控制移植排斥反应,但免疫抑制方案常常达不到理想的治疗效果。免疫抑制不足可能导致排斥反应,而过度免疫抑制可能导致感染、恶性肿瘤和慢性肾脏疾病等其他并发症。因此,诊断和治疗免疫排斥反应是心脏移植患者长期生存的关键。
4.肠道微生物在宿主免疫系统的稳态中起关键调控作用。肠道微生物在心脏移植患者移植前后存在差异,可作为心脏移植免疫反应的诊断标志物。肠道微生物诊断可弥补目前临床诊断心脏移植排斥反应的不足,可早期且无创诊断心脏移植排斥反应。肠道微生物诊断样本量需求少,采样无需安排专业人员。另外,肠道微生物诊断效率高,可一次性完成大量样本的检测。肠道微生物治疗可能成为诱导心脏移植免疫耐受的潜在治疗方式,有希望解决当前心脏移植免疫抑制治疗长期生存率低的问题。
技术实现要素:
5.针对上述技术的不足,本发明的目的之一在于提供一种心脏移植免疫排斥反应的肠道微生物标志物,能够无创检测、快速识别,目的之二在于提供心脏移植免疫耐受诱导的潜在治疗靶标。
6.为实现上述目的,本发明采用如下技术方案实现:
7.s1获取心脏移植患者移植前后的粪便样本。
8.s2提取不同粪便样本的dna并对相应粪便样本中的肠道微生物进行16srrna测定、宏基因组测序和分析。
9.s3根据种属相对丰度差异筛选出心脏移植患者移植前后显著丰度差异的微生物,并作为心脏移植免疫排斥或免疫耐受的标志物。
10.s3所述的心脏移植免疫排斥或免疫耐受的标志物包括:faecalibacterium prausnitzii、roseburia inulinivorans。
11.s2所述16srrna测定包括使用引物进行16s序列扩增和对16srrna的v3-v4区进行测序。
12.s2所述16srrna测定和宏基因组测序包括在illuminanovaseq平台上进行dna文库
测序。
13.本发明的有益效果是,在揭示心脏移植患者移植前后肠道微生物中厚壁菌门相对丰度的基础上,首次公开了faecalibacteriumprausnitzii、roseburiainulinivorans作为心脏移植患者免疫排斥反应的诊断标志物,可用于心脏移植患者免疫排斥反应的早期发现,为诱导心脏移植患者免疫耐受提供肠道微生物治疗靶标。
附图说明
14.图1:心脏移植患者肠道微生物chao1-α多样性分析
15.图2:心脏移植患者肠道微生物shannon-α多样性分析
16.图3:心脏移植患者肠道微生物upgmacluster-β多样性分析
17.图4:心脏移植患者丰度差异显著的肠道微生物菌门
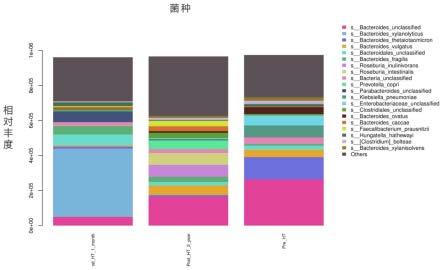
18.图5:心脏移植患者丰度差异显著的肠道微生物菌种
具体实施方式
19.下面通过具体实施例,并结合附图,对本发明作进一步的阐述。所述实施例仅用于对本发明进行说明,而非对本发明保护范围的限制。实施例中所用方法如未注明条件,均为常规实验条件。下列实施例中所需要的材料、试剂或仪器,如无特殊说明均可通过商业途径获得。
20.实施例心脏移植患者肠道微生物分析
21.(1)粪便样本收集
22.提供书面知情同意书给心脏移植受者,收集不同时间点(心脏移植前1周内和心脏移植手术期间(≤1月),心脏移植早期(1月~3月),心脏移植后中期(3月~12月),心脏移植后后期(1年~2年)),以及收集发生不良事件(如发热、腹泻、再次手术、acr和感染)时的粪便样本。由患者自行采集2-5g粪便样品放入装有10-15ml粪便保存液的采集管中,摇晃至充分混匀后储存在-80
°
冰箱内。
23.(2)粪便样本中dna提取
24.首先将每个样品(20mg)解冻并悬浮在5.0ml磷酸盐缓冲盐水(pbs;ph7.2)中。为了除去粪便颗粒,在4℃下以100g离心15min。将得到的上清液在4℃下以13000g离心10min。然后将其悬浮在1.5ml丙酮中洗涤3次。为了除去粪便中潜在的pcr抑制剂,每种制剂在4℃下以13000g离心10min。弃去上清液,使用粪便dna提取试剂盒处理沉淀,并根据制造商的说明使用旋转柱纯化dna。
25.(3)dna文库构建和测序
26.将提取到的微生物dna样品送到基因测序公司,在illuminanovaseq平台上进行dna文库测序。用16s全长通用引物对纯化后的dna进行pcr扩增,电泳检测pcr产物,将扩增的dna样品送到基因测序公司对16srrna的v3-v4区进行测序。
27.(4)数据分析
28.使用qiime和r软件对rawdata进行质量过滤、修剪、去复制和嵌合序列过滤,得到cleandata。cleandata以97%的相似性聚集到操作分类单元中,与分类数据库对齐。通过r计算样本内的α-多样性,分析样本间的β-多样性。
29.样本的α多样性由chao1(如图1)、goods_coverage、observedspecies、shannon(如图2)和simpson指数描述,β多样性通过距离矩阵比较样本间的相似性,结果由主坐标分析、upgmacluster(如图3)、nmds、pcoa、anosim、adonis描述。
30.(5)结果
31.本发明人研究发现,心脏移植后2年与心脏移植前1周比较,心脏移植患者的肠道微生物多样性增加(图1和2),组间多样性差异减小(图3),厚壁菌门丰度显著增加(图4)。心脏移植后1个月与心脏移植前1周比较,组间多样性差异较大(图3),厚壁菌门丰度显著增加(图4)。因此,厚壁菌门可作为心脏移植免疫反应的标志物。与心脏移植前1周比较,心脏移植后1个月减少但心脏移植后2年增加的厚壁菌门包含phascolarctobacterium faecium、phascolarctobacterium unclassified、phascolarctobacterium succinatutens、phascolarctobacterium sp.cag:207、clostridium sp.af36-18bh、clostridium aldenense,这些厚壁菌可作为心脏移植免疫排斥反应的标志物,也是心脏移植免疫耐受的治疗靶标。与心脏移植前1周比较,心脏移植后1个月增加且心脏移植后2年增加的厚壁菌门包含roseburia inulinivorans、roseburia intestinalis、faecalibacterium prausnitzii、clostridiales unclassified、roseburia unclassified、clostridium unclassified、faecalibacterium sp.marseille-p9312、firmicutes unclassified、faecalibacterium unclassified、eubacterium rectale、roseburia hominis、eubacterium eligens、lachnospiraceae unclassified、clostridium symbiosum、flavonifractor plautii、ruminococcus unclassified、ruminococcus torques、megasphaera unclassified、oscillospiraceae unclassified、uncultured clostridium sp.、clostridium leptum、streptococcus unclassified、tyzzerella nexilis、streptococcus salivarius、bacillus anthracis、ruminococcus gnavus、lawsonibacter asaccharolyticus、clostridium amygdalinum、clostridiumsp.pi-s10-a1b,这些厚壁菌可作为心脏移植免疫耐受的标志物或治疗靶标。心脏移植后1个月和2年faecalibacterium prausnitzii、clostridiales unclassified的丰度显著增加,而roseburia inulinivorans、roseburia intestinalis、roseburia unclassified变化不明显,所以roseburia inulinivorans、roseburia intestinalis、roseburia unclassified丰度的增加与心脏移植患者的长期生存率密切相关(图5)。
32.因此,所述肠道微生物能够作为心脏移植患者免疫排斥或耐受的生物标志物,心脏移植免疫排斥反应的标志物同时也可作为心脏移植免疫耐受的治疗靶标。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。