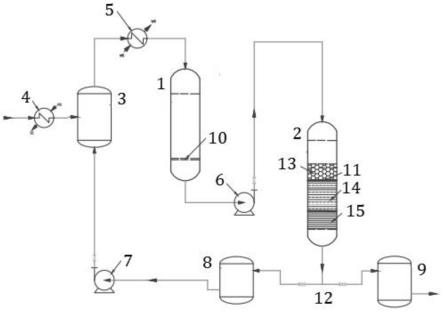
1.本发明涉及一种硫醚类独脚金内酯衍生物及其制备方法与调节植物生长的应用,属于植物生长调节剂领域。
背景技术:
2.独脚金内酯(strigolactones,sls)是一类新型植物激素,是一类以异戊二烯为基本单元的倍半萜烯化合物,其骨架结构由一个三环的内酯通过一个烯醇醚骨架与一个甲基丁烯羟酸内酯环连接而成,在高等植物中广泛存在。1966,cook等人从棉花根系分泌物中分离鉴定出一种可以诱导根茎寄生植物独脚金种子萌发的物质strigol,后来被命名为独脚金醇,经进一步试验探究,独脚金醇可以刺激独脚金(strigaspp.)、列当(orobanchespp.)种子的萌发。1972年,科学家成功解析了独脚金醇的结构。在随后的几十年中,从玉米,高粱和藜等多种粮食作物和经济作物中也分离得到独脚金醇以及其他结构十分相似并且可以诱导独脚金种子萌发的物质,例如高粱内醇(sorgolactone),黑蒴醇(alectrol),列当醇(orobanchol)等。
3.直到2005年,独角金内酯对寄主植物的生物学功能才被证明。akiyama等人发现独脚金内酯是一种植物源信号,能促进丛枝真菌(arbuscularmycorrhizal,am)菌丝的分枝。丛枝真菌在与植物共生关系中能传递矿物营养,提高磷肥的吸收,促进植物的生长。特别是在磷肥有限的田间生长的植物根系分泌物对丛枝真菌的刺激更大。2008年,gomez-roldan和umehara发现独脚金内酯以及它的衍生物作为一个新的植物激素抑制植物分枝是植物生物学的一个重大突破。这项发现使植物激素又多了一位重要成员,也使独脚金内酯的研究成为植物学界研究的热点。其中用于调控植物分枝的独脚金内酯类似物结构也成为研究的热门。
4.但植物中独脚金内酯含量极低,收集寄主植物根系分泌的生产方法不适宜于独脚金内酯的批量生产。此外,由于独脚金内酯的结构和立体化学结构复杂,其人工合成也正在经受挑战。因此高效低成本的独脚金内酯类似物成为研究的热门。目前,应用被认为最有效的和应用最广泛sls类似物是gr24,现有的gr24合成路线步骤繁琐、收率低,生产成本高,限制了其在农业生产中的大规模推广和应用。
5.因此,结构简单、稳定性好、生物活性高的独脚金内酯功能类似物的设计和合成研究迫在眉睫。
技术实现要素:
6.本发明的目的是提供一种硫醚类独脚金内酯衍生物及其制备方法与其在调节植物生长中的应用。
7.本发明提供的硫醚类独脚金内酯衍生物,其结构通式如式ⅰ所示,
[0008][0009]
式ⅰ中,r1表示单取代或多取代(具体可为二取代或三取代),r1可独立地选自:c
1-c6的烷基(具体可为甲基)、卤素(具体可为氯、溴、氟)、硝基和c
1-c6的烷氧基(具体可为甲氧基)中的一种或多种;r2为3-甲基或2-甲基。
[0010]
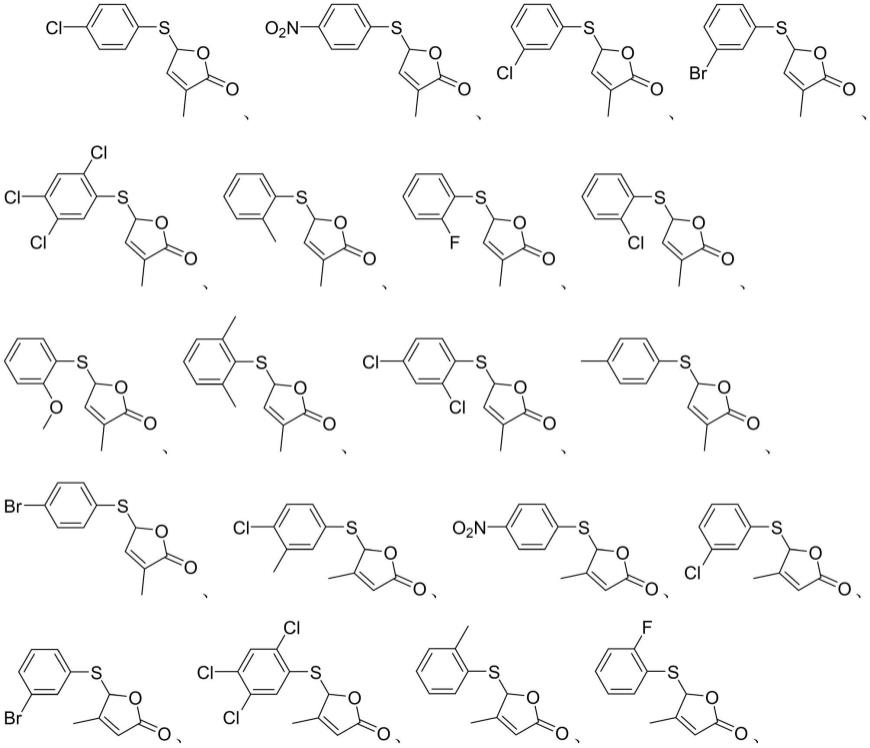
上述式i所示化合物具体可为如下化合物中的任意一种:
[0011][0012][0013]
上述式ⅰ所示化合物通过包括如下步骤的方法制备得到:
[0014]
式a所示化合物和式b所示化合物在溶剂和催化剂存在下进行硫醚化反应,得到式
ⅰ
所示化合物;
[0015][0016]
式a和式b中,r1和r2的定义与前述式i中的相同;
[0017]
上述方法中,所述硫醚化反应的条件为:以对甲苯磺酸为催化剂,甲苯为溶剂,回流条件下,使得式a所示化合物的巯基与式b所示化合物的羟基发生反应得到式ⅰ所示化合物。
[0018]
其中,式a所示化合物与式b所示化合物摩尔比可为:1:0.8-1.2。
[0019]
所述硫醚化反应的时间可为12-20h,具体可为15h。
[0020]
其中,式b所示化合物可直接购买或由式c所示化合物和环化试剂在催化剂、溶剂和酸存在下进行环化反应制得,
[0021][0022]
所述环化反应的条件为:以甲基丙二酸为环化试剂,水为溶剂,浓硫酸为酸,回流条件下,使得式c所示化合物发生环化反应得到式b所示化合物;
[0023]
式c所示化合物与甲基丙二酸的摩尔比可为:1:0.5-0.8;
[0024]
式c所示化合物与浓硫酸摩尔比可为:1:0.02%-0.08%;
[0025]
所述环化反应的时间可为15-20h,具体可为16h。
[0026]
上述式i所示化合物在调节植物生长活性中的应用及式ⅰ化合物作为植物生长调节剂的应用,也属于本发明的保护范围。
[0027]
具体的,所述调节植物生长活性为诱导寄生植物的种子萌发、调控植物根系生长和根瘤菌的形成以及抑制植物的分枝和侧芽的生长中至少一种;
[0028]
所述植物生长调节剂为用于诱导寄生植物的种子萌发、调控植物根系生长和根瘤菌的形成以及抑制植物的分枝和侧芽的生长中至少一种的调节剂;
[0029]
所述植物为寄生植物或涉及分蘖或涉及分枝的植物,具体可为小麦、水稻、独脚金或列当。
[0030]
所述调节植物生长活性为促进向日葵列当和锁阳种子萌发、抑制小麦分蘖及促进棉花叶片衰老(脱叶)中的至少一种。
[0031]
本发明还提供一种植物生长调节剂,所述植物生长调节剂含有上述式i所示化合物。
[0032]
本发明提供的式i所示硫醚类化合物,结构简单,稳定性好,具有优良的植物生长调节活性,制备方法简单可行,利于大规模生产应用。
具体实施方式
[0033]
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
[0034]
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
[0035]
本发明提供硫醚类独脚金内酯衍生物及其制备方法与其在调节植物生长中的应用。
[0036]
所述硫醚类独脚金内酯衍生物,其结构通式如式ⅰ所示,
[0037][0038]
式ⅰ中,r1表示单取代或多取代(具体可为二取代或三取代),r1可独立地选自:c
1-c6的烷基(具体可为甲基)、卤素(具体可为氯、溴、氟)、硝基和c
1-c6的烷氧基(具体可为甲氧基)中的一种或多种;r2为3-甲基或2-甲基。
[0039]
上述式i所示化合物在调节植物生长活性中的应用及式ⅰ化合物作为植物生长调节剂的应用,也属于本发明的保护范围。
[0040]
具体的,所述调节植物生长活性为诱导寄生植物的种子萌发、调控植物根系生长和根瘤菌的形成以及抑制植物的分枝和侧芽的生长中至少一种;
[0041]
所述植物生长调节剂为用于诱导寄生植物的种子萌发、调控植物根系生长和根瘤菌的形成以及抑制植物的分枝和侧芽的生长中至少一种的调节剂;
[0042]
所述植物为寄生植物或涉及分蘖或涉及分枝的植物,具体可为小麦、水稻、独脚金或列当;
[0043]
本发明还提供一种植物生长调节剂,所述植物生长调节剂含有上述式i所示化合物。
[0044]
本发明提供的式i所示硫醚类化合物,结构简单,稳定性好,具有优良的植物生长调节活性,制备方法简单可行,利于大规模生产应用。
[0045]
下述实施例中所用5-羟基-4-甲基-2-(5h)-呋喃酮可从公开商业途径(商品名:4-甲基-5-羟基呋喃-2-酮,厂家:上海麦克林生化科技有限公司)获得,所用5-羟基-3-甲基-2-(5h)-呋喃酮可按照如下反应式制得:
[0046][0047]
具体步骤如下:
[0048]
称取甲基丙二酸10g(84.68mmol)和乙二醛17.82g(40%水溶液,0.123mol)加入到250ml圆底烧瓶中,加入水100ml,磁力搅拌使其溶解,搅拌下缓慢加入浓h2so41.12ml(0.021mmol),加热回流进行反应。tlc[v
石油醚
﹕v
乙酸乙酯
=3﹕2]监测反应,16h后反应结束,乙酸乙酯萃取30ml
×
3,合并有机相,无水硫酸钠干燥,抽滤,减压浓缩,经柱层析纯化,v
石油醚
﹕v
乙酸乙酯
=2:1,得到5-羟基-3-甲基-2-(5h)-呋喃酮,为黄色固体,收率:51.97%。
[0049]
实施例1、化合物11的制备
[0050]
称取1g5-羟基-3-甲基-2-(5h)-呋喃酮1g(8.76mmol)于250ml圆底烧瓶中,加入甲苯30m磁力搅拌使其溶解,加入对甲苯磺酸一水合物0.045g(0.26mmol),再加入2,4-二氯苯
硫酚1.57g(8.76mmol),80℃下加热回流进行反应。tlc[v
石油醚
﹕v
乙酸乙酯
=5﹕1]检测反应,15h后反应结束。减压蒸馏,除去甲苯,乙酸乙酯萃取10ml
×
3,合并有机相,无水硫酸钠干燥,减压浓缩,柱层析,v
石油醚
﹕v
乙酸乙酯
=10:1。总收率:42.70%。
[0051]
实施例2、化合物15的制备
[0052]
称取1g5-羟基-4-甲基-2-(5h)-呋喃酮1g(8.76mmol)于250ml圆底烧瓶中,加入甲苯30ml磁力搅拌使其溶解,加入对甲苯磺酸一水合物0.045g(0.26mmol),再加入对硝基苯硫酚1.36g(8.76mmol),80℃下加热回流进行反应。tlc[v
石油醚
﹕v
乙酸乙酯
=5﹕1]检测反应,15h后反应结束。减压蒸馏,除去甲苯,乙酸乙酯萃取10ml
×
3,合并有机相,无水硫酸钠干燥,减压浓缩,柱层析,v
石油醚
﹕v
乙酸乙酯
=10:1。总收率:44.65%。
[0053]
参照实施例1和2提供的制备方法,替换相应取代基,可制得表1中的其他归属式ⅰ的化合物。
[0054]
上述化合物1至化合物9的理化数据均见表1,结构式及结构确证数据均见表2。
[0055]
表1、化合物1-26的理化数据
[0056]
化合物分子式状态收率(%)1c
11
h9clo2s黄色固体46.312c
11
h9no4s黄色固体39.693c
11
h9clo2s黄色固体46.034c
11
h9bro2s黄色油状液体41.785c
11
h7cl3o2s黄色油状液体39.126c
12h12
o2s黄色油状液体40.397c
11
h9fo2s黄色固体37.728c
11
h9clo2s黄色固体40.099c
12h12
o3s黄色油状液体41.6810c
13h14
o2s黄色油状液体40.8211c
11
h8cl2o2s白色固体42.7012c
12h12
o2s黄色固体38.7813c
11
h9bro2s黄色固体40.3314c
11
h9clo2s白色固体43.3515c
11
h9no4s黄色固体44.6516c
11
h9clo2s白色固体45.5417c
11
h9bro2s白色固体45.9418c
11
h7cl3o2s白色固体42.9619c
12h12
o2s黄色油状液体39.0420c
11
h9fo2s黄色固体38.5221c
11
h9clo2s黄色油状液体43.3122c
12h12
o3s黄色油状液体39.6723c
13h14
o2s白色固体43.8624c
11
h8cl2o2s黄色油状液体41.8325c
12h12
o2s黄色固体43.08
26c
11
h9bro2s黄色固体42.62
[0057]
表2、化合物1-9化学结构及1hnmr,
13
c-nmr和hrms数据
[0058]
[0059]
[0060]
[0061][0062]
实施例3、化合物促进向日葵列当种子萌发的生物活性测定
[0063]
将向日葵列当种子依次用70%(v/v)乙醇和0.5%次氯酸钠分别消毒1min和15min。然后用无菌水冲洗数次次,在超净工作台中自然晾干。将滤纸放入培养皿(直径d=9cm)中,并加入1ml无菌水中。在滤纸上放置三张直径d=13mm的玻璃纤维滤纸,并在玻璃纤维滤纸上滴加测试溶液。所有试验以gr24rac为阳性对照,以乙醇为阴性对照,其中,gr24rac为(2’r)和(2’s)的外消旋异构体混合物,每个处理设置6个重复。每一张玻璃纤维滤纸上放置30-80颗向日葵列当种子,然后在25-26℃的黑暗条件下培养。10d时以胚根出芽数计数。用sigmaplot11.0软件生成gr24和活性化合物的剂量-反应曲线和有效浓度(ec
50
)值。
[0064]
表3、化合物促进向日葵列当种子萌发的有效浓度
[0065]
[0066][0067]
由表3可知,阳性对照gr24的ec
50
值为9.067-8
mol/l,化合物1、4、10、12、18、21、22、26的ec
50
值与之相当,活性也与之相当,化合物3、7、8、11、13、17、23、24和25的ec
50
值分别为9.707e-9
mol/l、8.382e-9
mol/l、9.924e-9
mol/l、9.672e-9
mol/l、7.838e-9
mol/l、1.313e-9
mol/l、6.289e-9
mol/l、1.223e-9
mol/l和2.207e-9
mol/l,均比阳性对照gr24的ec
50
值小一个数量级,化合物14和19的ec
50
值分别为2.805e-10
和2.856e-10
,均比阳性对照gr24的ec
50
值小两个数量级,可见化合物1、3、4、7、8、10、11、12、13、14、17、18、19、21、22、23、24、25、26的促进向日葵列当种子萌发的活性好于阳性对照gr24,化合物14、19的活性最好。
[0068]
实施例4、化合物对小麦分蘖的影响
[0069]
挑选大小整齐饱满的小麦种子400粒,用10%的h2o2水溶液300ml浸泡15min,消毒后用大量无菌水冲洗种子,以便去除残留的h2o2,用300ml无菌水浸泡24h催芽,将催芽后的小麦种子进行播种。幼苗长至两叶一心时叶面分别喷施清水、2μmgr24和本发明提供的式ⅰ所示化合物(如化合物7),每间隔7天进行1次施药,连续施药3次。小麦幼苗长至四叶一心时开始进行分蘖数调查,每10天调查1次,连续调查3个月。
[0070]
表4、化合物对小麦分蘖的影响
[0071]
[0072][0073]
与清水对照相比,化合物2、4、19、22、26和gr24在施药初期对小麦分蘖的抑制效果不明显,随着小麦的生长,逐渐表现出对分蘖的抑制活性。而化合物6、11、14、18、20、24、25在施药初期即表现出很好的抑制分蘖活性,且持效期最好,由此可见,化合物具有很好的抑制小麦分蘖的活性。
[0074]
实施例5、化合物对锁阳种子萌发的生物活性测定
[0075]
将锁阳种子用70%(v/v)乙醇消毒30s,再用0.5%次氯酸钠消毒15min,然后用无菌水冲洗数次,在超净工作台中自然晾干。称取7gagar,加去离子水定容到一千毫升。将配制的培养液分装入锥形瓶内,98ml灭菌后备用。将已合成出的化合物用乙醇溶解,配置浓度为10-4
mol/l的供试母液,溶解度不好的化合物通过加热溶解,并过微孔滤膜过滤,备用。向备用的液体培养基中,加入供试母液混匀,制成10-6
mol/l含毒液体培养基(60℃),后将其倒入玻璃培养皿中,冷却后用于进一步的平板培养。
[0076]
将液体培养基倒入培养皿(直径d=9cm)中,所有试验以gr24rac为阳性对照,以乙醇为阴性对照,每个处理设置6个重复。每个培养皿中分别放置30-40颗锁阳种子,然后在25-26℃的黑暗条件下培养。15天时以胚根出芽数计数,计算发芽率。
[0077][0078]
实验结果发现,在药物浓度为10-6
mol/l时化合物1、8、11、17对锁阳种子具有一定的促进萌发的效果,但是对肉苁蓉并没有任何刺激作用。萌发效果不好的原因,猜测可能是由于肉苁蓉种子对合成出的药物不敏感,或者是种子对10-6
mol/l浓度下的药物不敏感。
[0079]
实施例6、化合物对棉花落叶的影响
[0080]
挑选大小整齐饱满的棉花种子100粒,用10%的h2o2水溶液300ml浸泡15min,消毒后用大量无菌水冲洗种子,以便去除残留的h2o2,用300ml无菌水浸泡24h催芽,将催芽后的棉花种子进行播种。棉花幼苗长至五叶一心时叶面分别喷施清水、乙烯利、25μmgr24、25μmgr24和乙烯利的混合溶液、25μm合成的化合物和乙烯利的混合溶液,每天观察棉花叶片的状态。
[0081][0082]
目前,机械化也已经成为棉花种植的主要方式,脱叶剂等化学产品跟机械化相结合也正在帮助棉农获得更优质的棉花。化合物1、8、11、19、21、22、23、25与乙烯利混合叶面喷施,可以明显促进乙烯利对棉花的脱叶作用,效果与gr24相当。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。