1.本公开涉及一种用于制备阿洛酮糖的组合物及使用所述组合物的方法。
背景技术:
2.为了糖类的稳定储存和分配,已经对用于制备糖类的前体的开发(利用)进行了研究。例如,国际专利公开号wo 2012-113405 a1公开了一种用于制备高纯度母乳寡糖组分的前体组合物,其难以通过化学或酶促方法合成或纯化。然而,没有关于用于制备阿洛酮糖的前体组合物的研究,阿洛酮糖是一种作为低热量糖类而近来受到关注的材料。
3.鉴于此技术背景,本发明人已发现,新型化合物可用作制备阿洛酮糖的前体,从而完成本公开。
技术实现要素:
4.本公开的一个目的是提供一种用于制备阿洛酮糖的新型组合物以及使用所述新型组合物制备阿洛酮糖的方法。
附图说明
5.图1示出了在制备阿洛酮糖的过程中产生的二糖的hplc色谱图,如通过尺寸排阻柱(biorad aminex hpx-87c)分析的;
6.图2示出了通过尺寸排阻柱从制备阿洛酮糖过程中产生的二糖中获得的混合物形式的d1和d2的hplc色谱图,如通过正相柱(ymc pack polyamine ii)分析的;
7.图3示出了作为阿洛酮糖二糖的d1的立体结构;和
8.图4示出了阿洛酮糖的结构及其编号的碳原子。
具体实施方式
9.下面将详细描述本公开。同时,本公开中公开的每个描述和实施方案也可以应用于其他描述和实施方案。也就是说,本公开中公开的各种要素的所有组合都落入本公开的范围内。此外,本公开的范围不受以下具体描述的限制。
10.此外,本领域技术人员将认识到或能够仅使用常规实验来确定本文描述的公开内容的特定实施方案的许多等同方案。此外,这些等同方案应被解释为落入本公开之内。
11.本公开的一个方面提供一种新型阿洛酮糖前体。
12.本公开的阿洛酮糖前体可以包括阿洛酮糖二糖。本公开的阿洛酮糖前体可以具有阿洛酮糖二糖的结构。
13.本公开的“阿洛酮糖二糖”是指“其中两个阿洛酮糖分子通过糖苷键连接而成的化合物”。术语“阿洛酮糖二糖”可称为“阿洛酮糖二聚体”或“二糖阿洛酮糖”。
14.具体地,所述阿洛酮糖二糖可以是其中两个阿洛酮糖分子通过糖苷键连接的化合
物,所述糖苷键将所述两个阿洛酮糖分子中的一个阿洛酮糖分子的c2位置处的羟基连接至另一个阿洛酮糖分子的c1至c6位置中的任意一个位置处的羟基。
15.具体地,阿洛酮糖二糖可以是其中两个阿洛酮糖分子中的至少一个分子为环状阿洛酮糖的化合物,其中环状阿洛酮糖c2位置处的羟基通过糖苷键与另一个阿洛酮糖分子的c1至c6位置中的任意一个位置处的羟基连接。糖苷键可以是一个糖苷键至两个糖苷键,特别地是一个糖苷键。
16.在一个实施方案中,糖苷键可以是环状阿洛酮糖的c2位置处的羟基与另一阿洛酮糖的c6位置处的羟基之间的糖苷键。
17.在一个实施方案中,在阿洛酮糖前体中,两个阿洛酮糖分子中的一个分子是呋喃阿洛酮糖的形式,而另一个分子是吡喃阿洛酮糖的形式。在一个实施方案中,阿洛酮糖前体可以是由下式1表示的化合物。
18.[式1]
[0019][0020]
在一个实施方案中,本公开的阿洛酮糖前体可以是命名为2-(羟甲基)-2-((3,4,5-三羟基-5-(羟甲基)四氢呋喃-2-基)甲氧基)四氢-2h-吡喃-3,4,5-三醇的化合物,更具体地是命名为(2s,3r,4r,5r)-2-(羟甲基)-2-(((2r,3s,4r)-3,4,5-三羟基-5-(羟甲基)四氢呋喃-2-基)甲氧基)四氢-2h-吡喃-3,4,5-三醇的化合物,但不限于此。
[0021]
根据呋喃阿洛酮糖的形式,(2s,3r,4r,5r)-2-(羟甲基)-2-(((2r,3s,4r)-3,4,5-三羟基-5-(羟甲基)四氢呋喃-2-基)甲氧基)四氢-2h-吡喃-3,4,5-三醇可统称为命名为6-o-β-d-吡喃阿洛酮糖基-α-d-呋喃阿洛酮糖或6-o-β-d-吡喃阿洛酮糖基-β-d-呋喃阿洛酮糖的化合物。
[0022]
(2s,3r,4r,5r)-2-(羟甲基)-2-(((2r,3s,4r)-3,4,5-三羟基-5-(羟甲基)四氢呋喃-2-基)甲氧基)四氢-2h-吡喃-3,4,5-三醇可以是命名为(2s,3r,4r,5r)-2-(羟甲基)-2-(((2r,3s,4r,5s)-3,4,5-三羟基-5-(羟甲基)四氢呋喃-2-基)甲氧基)四氢-2h-吡喃-3,4,5-三醇的化合物,或命名为(2s,3r,4r,5r)-2-(羟甲基)-2-(((2r,3s,4r,5r)-3,4,5-三羟基-5-(羟甲基)四氢呋喃-2-基)甲氧基)四氢-2h-吡喃-3,4,5-三醇的化合物,但不限于此。
[0023]
具体地,式1的化合物可以以下式2和/或式3的两种形式存在。
[0024]
[式2]
[0025][0026]
[式3]
[0027][0028]
式2的化合物可命名为6-o-β-d-吡喃阿洛酮糖基-α-d-呋喃阿洛酮糖,式3的化合物可命名为6-o-β-d-吡喃阿洛酮糖基-β-d-呋喃阿洛酮糖。
[0029]
本公开的阿洛酮糖前体可通过加热转化为阿洛酮糖。
[0030]
加热可以在60℃或更高且100℃或更低的温度进行,更具体地,在60℃或更高且95℃或更低、65℃或更高且95℃或更低、70℃或更高和95℃或更低的温度进行,但不限于此。
[0031]
加热可以进行长于0小时至108小时或更短,并且具体地进行10分钟、20分钟、30分钟、40分钟、50分钟、1小时、2小时、3小时、4小时、5小时、6小时、7小时、8小时、9小时、10小时、11小时或12小时或更长的时间,但不限于此。
[0032]
当本发明的阿洛酮糖前体转化为阿洛酮糖时,基于100重量份的初始阿洛酮糖前体,其20重量份或更多可以转化为阿洛酮糖。具体而言,基于100重量份的初始阿洛酮糖前体,阿洛酮糖前体的20重量份、25重量份、30重量份、35重量份、40重量份、45重量份、50重量份、55重量份、60重量份、65重量份重量、70重量份、75重量份、80重量份、90重量份、95重量份或99重量份或更多,或100重量份(即所有阿洛酮糖前体)可以转化为阿洛酮糖,但不限于此。
[0033]
同时,转换可以进行长于0小时至108小时或更短,具体地进行10分钟、20分钟、30分钟、40分钟、50分钟、1小时、2小时、3小时、4小时、5小时、6小时、7小时、8小时、9小时、10小时、11小时或12小时或更长,但不限于此。
[0034]
当本公开的阿洛酮糖前体转化为阿洛酮糖时,基于100重量份的总组合物,产生的除目标阿洛酮糖以外的副产物的量可以为10重量份或更少,具体为10重量份、9重量份、8重
量份、7.5重量份、7重量份、6.5重量份、6重量份、5.5重量份、5重量份、4.5重量份、4重量份、3.5重量份、3重量份、2.5重量份、2重量份、1.5重量份或1重量份或更少,或者,基于100重量份的总组合物,它可以是0重量份,即不会产生副产物,但不限于此。
[0035]
本公开的另一方面提供阿洛酮糖二糖作为阿洛酮糖前体的用途。
[0036]
本公开的又一方面提供一种包含阿洛酮糖二糖的阿洛酮糖前体组合物。
[0037]
本发明的又一方面提供阿洛酮糖二糖在制备阿洛酮糖中的用途。
[0038]
本发明的又一方面提供一种用于制备阿洛酮糖的组合物,所述组合物包含阿洛酮糖二糖。
[0039]
本发明的又一方面提供一种制备阿洛酮糖的方法,所述方法包括加热阿洛酮糖二糖。
[0040]
如上所述,本公开的阿洛酮糖二糖可以转化为阿洛酮糖,因此阿洛酮糖二糖可以应用于阿洛酮糖的制备。阿洛酮糖二糖、前体和加热与上述相同。
[0041]
本发明的又一方面提供一种制备阿洛酮糖的方法,所述方法包括加热包含阿洛酮糖二糖的组合物。
[0042]
如上所述,本公开的阿洛酮糖二糖可转化为阿洛酮糖,因此包含阿洛酮糖二糖的组合物可应用于阿洛酮糖的制备。阿洛酮糖二糖、前体和加热与上述相同。
[0043]
阿洛酮糖二糖的加热可将阿洛酮糖二糖转化为阿洛酮糖或可产生阿洛酮糖,但不限于此。
[0044]
所述组合物可以包含糖类。具体地,所述组合物还可以包含阿洛酮糖,但不限于此。
[0045]
关于包含阿洛酮糖二糖的组合物中阿洛酮糖二糖的含量,基于100重量份的组合物中包含的总糖类,阿洛酮糖二糖的含量可以大于0重量份且为15重量份或更少。具体地,基于100重量份的总糖类,阿洛酮糖二糖的含量可以超过0.0001重量份、超过0.001重量份、超过0.01重量份、超过0.1重量份、或超过0.15重量份并且为15重量份或更少,和/或,基于100重量份的总糖类,阿洛酮糖二糖的含量可以为15重量份或更少、13重量份或更少、11重量份或更少的量、10重量份或更少、9重量份或更少、8重量份或更少、7重量份或更少、6重量份或更少、5重量份或更少、4重量份或更少、3重量份或更少、2重量份或更少、或1重量份或更少且超过0重量份,但不限于此。
[0046]
所述组合物可以是食品组合物。
[0047]
食品组合物包括任何食品而没有限制,只要其中可以使用阿洛酮糖即可。具体地,食品组合物可以包括普通食品组合物、保健食品组合物和药用(或患者)食品组合物,但不限于此。具体地,本公开的食品组合物可以是饮料(例如碳酸饮料、果汁饮料、果/蔬饮料、膳食纤维饮料、碳酸水、混合谷物粉、茶、咖啡等)、酒精饮料、烘焙产品、酱料(例如番茄酱、烧烤酱等)、乳制品(例如发酵奶、加工奶等)、加工肉类(例如火腿、香肠、牛肉干等)、巧克力糖果、口香糖、糖果、果冻、冰淇淋、糖浆、调料、零食(例如曲奇、薄脆饼干、饼干等)、果脯(例如水果制品、蜜饯、红参汁、红参切片等)、代餐食品(例如冷冻食品、蒸煮袋、家庭代餐(hmr)等)或加工食品。然而,这只是示例,食品组合物不限于此。
[0048]
本公开的食品组合物可以包含另外的成分,例如各种调味剂、天然碳水化合物等。上述天然碳水化合物可以包括单糖例如葡萄糖、果糖和阿洛酮糖,二糖例如麦芽糖和蔗糖,
多糖例如糊精和环糊精,以及糖醇例如木糖醇、山梨糖醇和赤藓糖醇。作为甜味剂,可以使用天然甜味剂例如奇异果甜蛋白和甜叶菊提取物,合成甜味剂例如三氯蔗糖、糖精、阿斯巴甜等。
[0049]
除上述成分外,本公开的食品组合物还可包含各种营养补充剂、维生素、矿物质、调味剂、着色剂、果胶及其盐、海藻酸及其盐、有机酸、保护性胶体增稠剂、ph调节剂、稳定剂、防腐剂、甘油、醇类、碳酸饮料中使用的碳酸化剂等。此外,本公开的食品组合物可以包含用于制备天然果汁、果汁饮料和蔬菜饮料的水果闪蒸物。这些成分可以单独使用或组合使用。食品组合物中通常包含的物质可以由本领域普通技术人员适当地选择和添加,并且基于100重量份的本公开的食品组合物,添加剂的比例可以选择为,0.001重量份至1重量份,或0.01重量份至0.20重量份的范围,但不限于此。
[0050]
本公开的又一方面提供了一种提高食品的质量稳定性的方法,所述方法包括加热包含阿洛酮糖二糖的食品组合物。
[0051]
食品可以是包含阿洛酮糖的食品。
[0052]“提高质量稳定性”是指抑制在分销、储存、加工过程中可能发生的任何变性和随之发生的质量劣化,或者降低已经发生的变性和质量劣化的程度。具体地,变性可以包括其中阿洛酮糖变为不同于阿洛酮糖的物质或其物理性质发生变化的现象,例如结晶、褐变、氧化/还原反应等。
[0053]
当阿洛酮糖或包含其的组合物长期储存时,由于诸如阿洛酮糖的结晶等变性,食品质量可能劣化。然而,当将本公开的阿洛酮糖前体添加到食品中时,通过加热阿洛酮糖前体在所需时间获得阿洛酮糖,因此其可用于提高食品的质量稳定性。
[0054]
食品与上述相同。
[0055]
在下文中,将参考实施例和实验例更详细地描述本公开。然而,这些实施例和实验例仅用于说明目的,本公开的范围不受这些实施例和实验例的限制。
[0056]
实施例1.阿洛酮糖前体的分离
[0057]
根据us 2018-0327796 a1中公开的阿洛酮糖制备工艺,通过hplc分离出一种新型物质。
[0058]
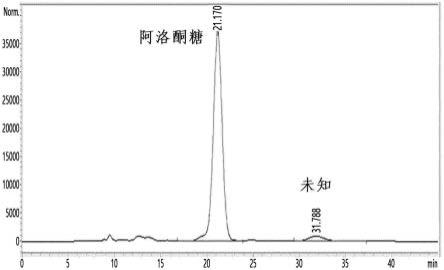
详细而言,在下表1的hplc色谱分析条件下,确认生成了目标二糖成分,并且从粗品溶液中生成了除阿洛酮糖以外的新型(未知)物质,如图1所示。在21.1分钟鉴定出阿洛酮糖,在31.7分钟鉴定出新型物质。
[0059]
[表1]
[0060]
设备agilent technologies 1200系列柱biorad aminex hpx-87c(7.8mm
×
300mm,9μm)洗脱液水流速0.6ml/分钟温度80℃ri池温度30℃
[0061]
为了分离生成的新型物质,在表2的条件下使用hplc和正相柱精确分离新型物质。
[0062]
[表2]
[0063][0064][0065]
结果,确认了在表1的hplc条件下显示为一个峰的物质在表2的分离条件下作为两个单独的峰被观察到(图2)。将在22.5分钟鉴定出峰的物质命名为d1,将在17.7分钟鉴定出的峰的另一种物质命名为d2。
[0066]
通过esi-ms、1h nmr和
13
c nmr进一步分析d1。
[0067]
主要的6-o-β-d-吡喃阿洛酮糖基-α-d-呋喃阿洛酮糖为白色无定形粉末,esi-ms m/z 365[m na] ;1h nmr(850mhz,d2o)δh 3.44(1h,d,j=12.0hz),3.47(1h,d,j=12.0hz),3.56(1h,dd,j=11.0hz,5.0hz),3.60(1h,d,j=12.0hz),3.62(1h,dd,j=11.0hz,2.5hz),3.70(1h,br d,j=12.5hz),3.75(1h,d,j=12.0hz),3.75(1h,br ma),3.82(1h,br d,j=12.5hz),3.84(1h,br s),3.92(1h,t,j=3.0hz),3.97(1h,d,j=5.5hz),4.09(1h,t,j=5.5hz),4.13(1h,br m)[d2o信号δh 4.70];
13
c nmr信号sbδc 57.6,60.4,62.9,64.7,64.9,69.1,68.9,70.2,70.3,81.2,101.8,103.4。
[0068]
次要的6-o-β-d-吡喃阿洛酮糖基-β-d-呋喃阿洛酮糖为白色无定形粉末,esi-ms m/z 365[m na] ;1h nmr(850mhz,d2o)δh 3.49(1h,d,j=13.0hz),3.73(1h,d,j=13.0hz),3.58(1h,ma),3.68(1h,dd,j=11.0,2.5hz),3.62(1h,ma),3.71(1h,br d,j=12.0hz),3.82(1h,br d,j=12.0hz),3.76(1h,br ma),3.78(1h,ma),3.87(1h,br s),3.98(1h,t,j=3.0hz),3.95(1h,d,j=4.5hz),4.00(1h,br m),4.34(1h,dd,j=8.0hz,4.5hz)[d2o信号δh 4.70];
13
c nmr信号sbδc57.7,61.4,62.2,64.7,64.8,69.0,69.2,70.8,74.4,80.8,101.8,105.9。
[0069]
结果,确认了d1是两个阿洛酮糖分子连接而成的新型化合物,具有下式1的结构。
[0070]
[式1]
[0071][0072]
还确认了,d1具有主要形式和次要形式两种类型(图3),主要形式6-o-β-d-吡喃阿洛酮糖基-α-d-呋喃阿洛酮糖具有下式2的结构,次要形式6-o-β-d-吡喃阿洛酮糖基-β-d-呋喃阿洛酮糖具有下式3的结构。
[0073]
[式2]
[0074][0075]
[式3]
[0076][0077]
将式2的化合物(6-o-β-d-吡喃阿洛酮糖基-α-d-呋喃阿洛酮糖)命名为化合物a,将式3的化合物(6-o-β-d-吡喃阿洛酮糖基-β-d-呋喃阿洛酮糖)命名为化合物b。
[0078]
此外,确认了,d2与式1的化合物具有结构异构体关系,是一种新型阿洛酮糖二糖,其中阿洛酮糖的c2位置(根据图4的碳编号)处的羟基与另一个阿洛酮糖分子的c1至c6位置中的任一位置处的羟基通过糖苷键连接。
[0079]
在以下实验中,进行实验以检查新型化合物d1和d2是否可以用作阿洛酮糖前体。
[0080]
实施例2.使用阿洛酮糖前体生产阿洛酮糖
[0081]
实施例2-1:阿洛酮糖二糖的加热转化反应比较
[0082]
将不含杂质的超纯水加入到实施例1中分离的两种二糖d1和d2中,制备浓度为1%(w/w)的样品,然后将其分别用于实验例1和2。为了根据加热条件比较分解反应,选择了由1分子葡萄糖和1分子果糖组成的糖(cj cheiljedang,纯度为99%或更高),这是最常见的二糖(二聚体)。同样地,向其中加入超纯水,制备浓度为1%(w/w)的样品,然后将其用于比较例1。
[0083]
将每个制备的样品置于密封玻璃瓶中,并在已预热至70℃、80℃、90℃或95℃的水浴(daihan science)中加热。每隔12小时收集加热的样品并取样,并在表1的条件下使用hplc分析其变化。所有实验重复进行三次,结果如下表3所示。
[0084]
[表3]
[0085][0086]
*不同的字符a、b和c表示实验例1、实验例2和比较例1在横向上的显著差异(p《0.05)。
[0087]
*单糖和二糖的%表示基于分析的糖的总重量的重量比(%,w/w),将其他归类为其他糖。
[0088]
结果,在相同的热损害(温度、时间)水平下,d1显示出显著高的向单糖的转化率,其次是d2和糖。
[0089]
具体而言,在最高温度条件95℃下,约74%的d1在12小时后转化为目标成分阿洛酮糖(单糖),在24小时后其98%或更多转化,确认产生阿洛酮糖。相反,约58%的d2在12小时后转化,在24小时后其89%转化。23%和40%的糖转化为单糖,这是相对微不足道的。
[0090]
基本上,实验例1-2和比较例1都显示了相同的模式,即随着加热温度越高和加热
时间越长,更多的二糖分解并转化为单糖。其中,在实验例1中,二糖(d1)向单糖(阿洛酮糖)的转化明显加快,转化后的单糖纯度保持在较高水平,证实转化效率高。
[0091]
特别地,与阿洛酮糖二糖d2相比,d1表现出更快的阿洛酮糖转化和高纯度结果。
[0092]
实施例2-2:阿洛酮糖前体在包含阿洛酮糖的食品模型中的利用
[0093]
通过将二糖d1添加到包含阿洛酮糖作为主要成分的食品模型中来检查混合物中存在的前体(而不是单独的前体)是否也转化为目标成分。
[0094]
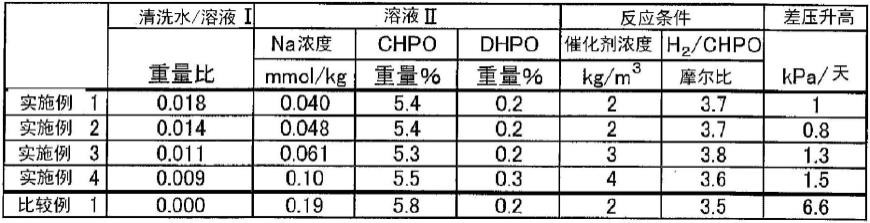
具体而言,通过将杂质最少的纯阿洛酮糖晶体(cj cheiljedang,纯度为99.8%或更高)和先前分离的二糖中的d1溶解在纯净水中来制备饮料模型(实验例3)。将制备的实验例3在95℃热处理约1小时,这是常见的饮料加工条件之一。在表1的条件下,通过hplc检查添加到实验例3中的二糖在热处理前后是否转化为阿洛酮糖。各样品的详细组成比和加热前后的变化如下表4所示。同样,所有实验重复进行三次。
[0095]
[表4]
[0096][0097]
结果,在向阿洛酮糖添加作为阿洛酮糖前体的d1的实验例3中,显示d1被转化为目标成分阿洛酮糖,阿洛酮糖的纯度提高。具体地,实验例3显示,在热处理后,以基于总固体含量为约4.7%的比例包含的d1降低至约1.5%(-3.2%)的比例,而目标成分阿洛酮糖增加了相应的量。
[0098]
换言之,d1在一般加工(加热)条件下转化为目标成分阿洛酮糖,同时没有产生意外产物,表明d1作为前体具有合适的性质。
[0099]
此外,由于作为前体的d1接收热能,因此可以预期抑制由于暴露于过度热损害导致的有用成分阿洛酮糖的变性(损失)的积极效果。
[0100]
实施例2-3:根据温度和固体浓度条件比较前体利用率
[0101]
在不同的温度和固体浓度条件下,检查了d1向阿洛酮糖的转化特性。以与先前测试的实施例2-2相同的方式将分离的前体d1添加到纯阿洛酮糖单糖中,并使用纯化水调节固体浓度。制备的实验例4至6的详细组成示于下表5和6中。
[0102]
首先,比较在40℃、60℃和80℃的改变温度条件下加热24小时时d1的转化率(表5)。
[0103]
[表5]
[0104][0105]
*与相同样品的初始制备相比,不同字符a、b和c表示在纵向上的显著差异(p《0.05)。
[0106]
与之前的实验一样,确认了,d1在所有温度条件下都转化为所需成分阿洛酮糖,阿洛酮糖的纯度提高。特别地,确认了d1在60℃-80℃加热时几乎转化为阿洛酮糖。
[0107]
接下来,通过在10%和30%(w/w,g/100g)的改变固体浓度,比较在高温(121℃)加热短时间(15分钟)时d1的转化率(表6)。
[0108]
[表6]
[0109][0110]
*与相同样品的初始制备相比,不同字符a、b和c表示在纵向上的显著差异(p《0.05)。
[0111]
与之前的实验一样,确认了,当在所有浓度条件下加热时,d1都转化为所需成分阿洛酮糖,阿洛酮糖的纯度提高。特别地,确认了总固体含量越低,甚至在热处理后,d1向阿洛酮糖的转化效率会相对较高。
[0112]
通过这些实验过程,证实了本公开的阿洛酮糖二糖作为前体转化为阿洛酮糖的效率很高,阿洛酮糖是一种有益于消费者的高附加值材料。
[0113]
特别地,确认了最终的目标材料阿洛酮糖是通过简单的加热反应(正常加工水平)而不是复杂的转化反应生成的,它具有防止阿洛酮糖在不存在意外杂质的情况下受到过度热损害的潜力。基于这种效果,预期d1可用作能够提高和保持食品和饮料产品中阿洛酮糖纯度的前体。
[0114]
基于以上描述,本领域技术人员将理解,本公开可以以不同的具体形式实施而不改变其技术精神或本质特征。在这点上,应理解,上述实施方案不是限制性的,而是在所有方面都是说明性的。本公开的范围由所附权利要求而不是由其之前的描述来定义,因此落入权利要求的范围和界限内的所有改变和修改,或这种范围和界限的等同方案,旨在被所述权利要求涵盖。
[0115]
本发明的效果
[0116]
本公开的阿洛酮糖前体可以简单地转化为阿洛酮糖,并且向阿洛酮糖以外的物质的转化水平低。因此,阿洛酮糖前体可用于改善包含阿洛酮糖的食品组合物的质量稳定性。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。