1.本发明涉及一种微针的制备方法,尤其涉及一种一氧化氮释放性聚离子液体抗真菌微针及其制备方法和应用,属于微针技术领域。
背景技术:
2.由真菌引起的皮肤感染极其顽固,危害着全球数以百万计人类的健康。皮肤角质层阻碍了抗真菌药物的转运,同时真菌容易增殖,甚至在皮下形成生物膜,引起炎症和皮下真菌脓肿。
3.真菌生物膜是一种高度动态的固定真菌群落,其自产的细胞外聚合物(eps)保护了病原菌免受外来抗菌药物的侵袭,使细菌更难以被杀死。此外,传统抗真菌药物的使用促进了耐药真菌的出现,同时也增加了真菌耐药性,导致抗真菌治疗成为一项具有挑战性的任务。临床应用中对于脓肿伤口通常使用伤口处敷料,防止伤口扩散和进一步的伤口感染。然而,对于脓肿伤口最有效的治疗方法是精准递送真菌物质至伤口处,杀死伤口处的病原菌,并促进伤口处皮肤的恢复。
4.因此,迫切需要开发无抗生素和具有精确递送效果的治疗策略以有效治疗真菌引起的皮肤感染。
技术实现要素:
5.为了解决上述技术问题,本发明的目的在于提供一种医用敷料,其具有抗真菌、抑制真菌生物膜,同时对脓肿伤口处的真菌及真菌生物膜有良好的杀灭及抑制作用。
6.为了实现上述技术目的,本发明提供了一种一氧化氮释放性聚离子液体抗真菌微针的制备方法,包括如下步骤:
7.以和1-乙烯基咪唑反应,得到离子液体1,n为独立地选自2-5的整数;
8.将离子液体1与反应2-4天(优选3天),得到离子液体2;其中,n为2-3的整数;
9.以离子液体2,丙烯酸羟乙酯作为单体,hcpk作为光引发剂,pegda作为交联剂以及水在微针模具里进行共聚反应,脱模,得到共聚物;
10.将共聚物在一氧化氮气氛下反应2-4小时,得到一氧化氮释放性聚离子液体抗真菌微针。
11.在本发明的一具体实施方式中,(优选2-溴乙醇)与1-乙烯基咪唑的投料摩尔比为1:1。离子液体1与的投料摩尔比为1:1。
12.在本发明的一具体实施方式中,离子液体2与丙烯酸羟乙酯的投料摩尔比为3:7-12;离子液体2与丙烯酸羟乙酯的混合物与水的质量比为4:6-6:4,hcpk的重量占总重量的
1%-2%,pegda的重量占总重量的2.5%-5%。这里需要说明的是,总重量是指离子液体2,丙烯酸羟乙酯作为单体,hcpk作为光引发剂,pegda作为交联剂和水的总重量。
13.在本发明的一具体实施方式中,pegda的分子量为400-1000;优选pegda的分子量为400、600或1000。
14.在本发明的一具体实施方式中,共聚反应的具体步骤为:
15.通过在紫外线照射下聚合混合溶液30-50分钟,然后脱模并在室温下真空干燥18-24小时,得到所述共聚物。
16.在本发明的一具体实施方式中,紫外线照射的波长为365nm。
17.在本发明的一具体实施方式中,将共聚物与过量的一氧化氮在密闭系统中反应2-4小时以得到一氧化氮释放性聚离子液体抗真菌微针。
18.为了实现上述技术目的,本发明还提供了一种一氧化氮释放性聚离子液体抗真菌微针,其是通过本发明的上述制备方法制备得到的。
19.为了实现上述技术目的,本发明又提供了一种医用敷料,该医用敷料是由本发明的一氧化氮释放性聚离子液体抗真菌微针制备得到的。
20.本发明一氧化氮释放性聚离子液体抗真菌微针,其制备方法是将可释放一氧化氮的聚离子液体与微针的方法结合,采用离子液体和一氧化氮进行。离子液体聚合物近年来在抗菌材料应用领域成为研究热点,由于离子液体诱导的亲水-疏水相互作用和静电引力的膜破坏机制导致了细菌裂解死亡。一氧化氮可代替传统抗生素进行抗菌治疗,并且不易诱导微生物产生耐药性。由于其反应副产物(如过氧亚硝酸盐和三氧化二氮)可发挥亚硝化作用,一氧化氮在体外和体内均显示出对细菌、真菌和生物膜抑制和消除作用,最终导致微生物死亡。一氧化氮还具有消炎、促进胶原沉积和促血管生成的作用。微针是一种无痛且精确的递送系统,具有可调针头长度的微针可以无痛地在皮肤表皮最外层产生短暂的孔道以精准输送药物,广泛用于生物医学领域。
21.本发明一氧化氮释放性聚离子液体抗真菌微针的制备方法,将可释放一氧化氮的聚离子液体与微针的方法结合,制备得到的基于可释放一氧化氮的聚离子液体的抗真菌微针可以用作医用敷料。该医用敷料能够抗真菌、抑制真菌生物膜,敷在伤口表面可以隔绝外界异物及微生物侵入伤口,同时对脓肿伤口处的真菌及真菌生物膜有良好的杀灭及抑制作用;抗炎,促进胶原沉积和促血管生成;适用于不同大小、形状及所在部位的脓肿创面;无过敏和耐药性、安全性高;制备和使用方便。
附图说明
22.图1为实施例1中微针用作医用敷料的抗菌测试效果图。
23.图2为实施例1中微针用作医用敷料的细胞毒性图。
24.图3为实施例1中微针用作医用敷料的抑制生物膜生长的测试效果图。
25.图4为实施例2中微针用作医用敷料的抗菌测试效果图。
26.图5为实施例3中微针用作医用敷料的抗菌测试效果图。
27.图6为实施例4中微针用作医用敷料的抗菌测试效果图。
28.图7为实施例5中微针用作医用敷料的抗菌测试效果图。
具体实施方式
29.本发明提供一氧化氮释放性聚离子液体抗真菌微针的制备方法,包括如下步骤:
30.以2-溴乙醇和1-乙烯基咪唑为单体进行反应(具体步骤为:在20℃下搅拌等摩尔的2-溴乙醇和1-乙烯基咪唑的混合物48小时,将反应所得溶液用乙酸乙酯和乙醚洗涤3次,然后用旋转蒸发仪在30℃下干燥4小时)得到离子液体1。
31.将离子液体1与在20℃下搅拌72小时,所得混合物在-70℃冰冻2小时后用冷冻干燥机处理24小时,得到离子液体2。
32.将离子液体2,丙烯酸羟乙酯,hcpk,pegda进行共聚反应(具体步骤为,以离子液体2,丙烯酸羟乙酯作为单体,hcpk作为光引发剂,pegda作为交联剂以及去离子水在微针模具里进行共聚反应,脱模,用去离子水洗涤三次,干燥)得到基于聚离子液体的微针;离子液体2与丙烯酸羟乙酯的投料摩尔比为3:7-12,离子液体2与丙烯酸羟乙酯混合物与去离子水的质量比为4:6,hcpk占总重量的1%-2%,pegda占总重量的2.5%-5%。
33.将聚离子液体微针在过量一氧化氮气氛下反应4小时,得到一氧化氮释放性聚离子液体抗真菌微针。
34.本的如上制备方法制备得到的一氧化氮释放性聚离子液体抗真菌微针,可以用作医用敷料。
35.实施例1
36.本实施例提供了一种一氧化氮释放性聚离子液体抗真菌微针,其制备方法包括以下步骤:
37.(a)以2-溴乙醇和1-乙烯基咪唑为单体进行反应(具体步骤为:在20℃下搅拌等摩尔的2-溴乙醇和1-乙烯基咪唑的混合物48小时,将反应所得溶液用乙酸乙酯和乙醚洗涤3次,然后用旋转蒸发仪在30℃下干燥4小时)得到离子液体1。
38.(b)将离子液体1与在20℃下搅拌72小时,所得混合物在-70℃冰冻2小时后用冷冻干燥机处理24小时,得到离子液体2。
39.(c)将离子液体2,丙烯酸羟乙酯,hcpk,pegda进行共聚反应(具体步骤为,以离子液体2,丙烯酸羟乙酯作为单体,hcpk作为光引发剂,pegda作为交联剂以及去离子水在微针模具里进行共聚反应,脱模,用去离子水洗涤三次,干燥)得到基于聚离子液体的微针;离子液体2与丙烯酸羟乙酯的投料摩尔比为3:7,离子液体2与丙烯酸羟乙酯混合物与去离子水的质量比为4:6,hcpk占总重量的1%,pegda占总重量的2.5%。
40.将上述制备得到的微针用作医用敷料,并且进行抗菌测试、细胞毒性测试、抑制生物膜的生长(结晶紫染色)测试、溶血测试。
41.具体的测试方法如下:
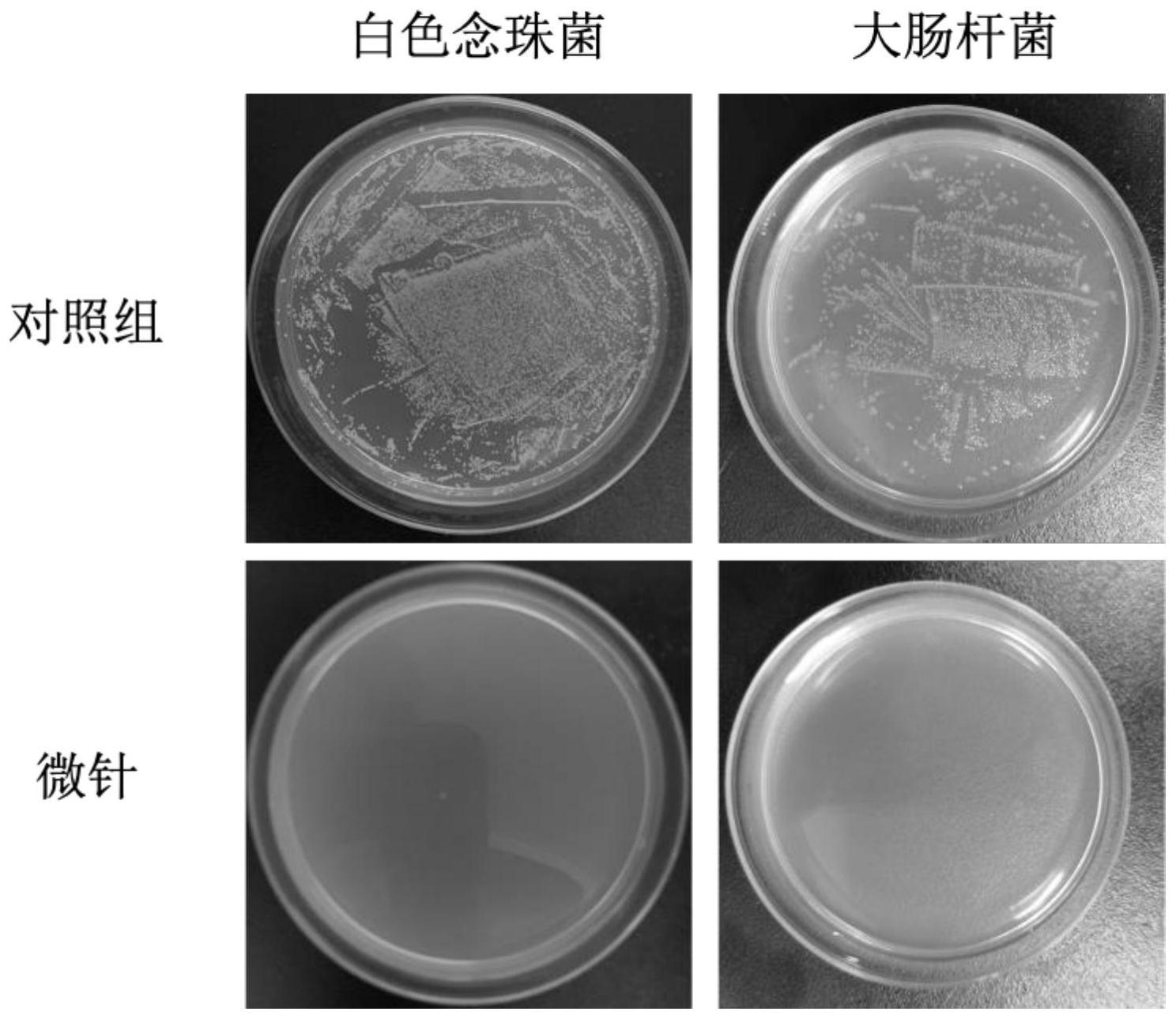
42.1、抗菌测试:测试微针分别对白色念珠菌、大肠杆菌的抗菌性。
43.取面积为1
×
1cm2的微针作为医用敷料样品为实验组、pet膜作为对照组,在实验组和对照组表面分别滴加od=0.1的菌液(白色念珠菌和大肠杆菌)培养2小时后涂板,再培养24小时后计数。
44.实施例1的抗菌性如图1所示,说明微针对白色念珠菌和大肠杆菌均具有优异的抗
菌性。
45.2、溶血测试:
46.将新鲜人血(3ml)以1500rpm离心15分钟并用pbs洗涤直至上清液透明。用pbs将红细胞沉淀物稀释至2vol%。将灭菌的微针的医用敷料样品和pet膜(面积:1
×
1cm2)浸入稀释的血液(每管5ml)溶液中,并分别在37℃下孵育3小时。在将处理过的稀释血液样品以1500rpm离心15分钟后,将100μl的上清液转移到96孔板中。通过用酶标仪记录od
576nm
来评估血红蛋白释放的量。pbs中的红细胞和2%triton分别用作阴性和阳性对照。
47.实施例1的溶血率如表1所示,说明本产品没有明显的溶血效应。
48.表1为实施例1中微针用作医用敷料的溶血测试结果。
49.材料对照组微针溶血率(%)0%2.14%
50.3、细胞毒性测试:利用mtt(3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐)法对医用敷料对老鼠皮肤成纤维细胞的毒性进行测试。
51.将老鼠皮肤成纤维细胞(1
×
104cfu/ml)用10%胎牛血清培养基在24孔板中培养48h,分别取1
×
1cm2微针作为医用敷料样品和pet膜加入到人类皮肤成纤维细胞溶液中37℃下培养24h后分别取0.1ml mtt溶液(5g/l pbs溶液)滴加至孔板中再培养,4h后将孔板中上清液移除,并加入0.75ml dmso来溶解甲瓒晶体用酶标仪测试其od
490nm
值来表征甲瓒的释放量,平行实验3次,测试老鼠皮肤成纤维细胞的相对生长速率。
52.实施例1的细胞毒性如图2所示,说明微针对老鼠成纤维细胞均不具有明显的细胞毒性。
53.4、抑制生物膜的生长(结晶紫染色)测试:
54.分别取面积为1
×
1cm2的微针作为医用敷料样品为实验组、pet膜作为对照组,在实验组和对照组表面分别滴加od=0.1的白色念珠菌,在37℃的培养箱下培养24小时。将培养基吸掉,并且用pbs洗涤3次,用95%乙醇作用15分钟,风干乙醇后,加入质量分数为0.1%的结晶紫溶液作用15分钟,用无菌水洗涤3次,最后使用33%醋酸溶解和生物膜作用的结晶紫,用酶标仪测试其od
490nm
值来表征生物膜的量。
55.实施例1的生物膜抑制效果如图3所示,说明本产品对生物膜的生长具有明显的抑制作用。
56.4、溶血测试:
57.将新鲜人血(3ml)以1500rpm离心15分钟并用pbs洗涤直至上清液透明。用pbs将红细胞沉淀物稀释至2vol%。将灭菌的微针的医用敷料样品和pet膜(面积:1
×
1cm2)浸入稀释的血液(每管5ml)溶液中,并分别在37℃下孵育3小时。在将处理过的稀释血液样品以1500rpm离心15分钟后,将100μl的上清液转移到96孔板中。通过用酶标仪记录od
576nm
来评估血红蛋白释放的量。pbs中的红细胞和2%triton分别用作阴性和阳性对照。生物膜抑制效果如表1所示,说明本产品没有明显的溶血效应。
58.实施例2
59.本实施例提供了一种一氧化氮释放性聚离子液体抗真菌微针,其制备方法与实施例1中的基本一致,不同的是:
60.步骤(b)中,所述n为2。实施例2的抗菌性如图4所示,说明微针对白色念珠菌和大
肠杆菌均具有优异的抗菌性。微针组细胞存活率为68%,残存生物膜基质量为38%。
61.实施例3
62.本实施例提供了一种一氧化氮释放性聚离子液体抗真菌微针,其制备方法与实施例1中的基本一致,不同的是:
63.步骤(c)中,离子液体2与丙烯酸羟乙酯的投料摩尔比为3:12。实施例3的抗菌性如图5所示,说明微针对白色念珠菌和大肠杆菌均具有优异的抗菌性。微针组细胞存活率为63%,残存生物膜基质量为27%。
64.实施例4
65.本实施例提供了一种一氧化氮释放性聚离子液体抗真菌微针,其制备方法与实施例1中的基本一致,不同的是:
66.步骤(c)中,hcpk占总重量的2%。实施例4的抗菌性如图6所示,说明微针对白色念珠菌和大肠杆菌均具有优异的抗菌性。微针组细胞存活率为78%,残存生物膜基质量为20%。
67.实施例5
68.本实施例提供了一种一氧化氮释放性聚离子液体抗真菌微针,其制备方法与实施例1中的基本一致,不同的是:
69.步骤(c)中,pegda占总重量的5%。实施例5的抗菌性如图7所示,说明微针对白色念珠菌和大肠杆菌均具有优异的抗菌性。微针组细胞存活率为77%,残存生物膜基质量为33%。
70.对比例1
71.本实施例提供了一种一氧化氮释放性聚离子液体抗真菌微针,其制备方法与实施例1中的基本一致,不同的是:
72.2-溴乙醇与1-乙烯基咪唑的投料摩尔比为2:1。微针组细胞存活率为37%,残存生物膜基质量为78%。
73.上述实施例只为说明本发明的技术构思及特点,其目的在于让熟悉此项技术的人士能够了解本发明的内容并据以实施,并不能以此限制本发明的保护范围。凡根据本发明精神实质所作的等效变化或修饰,都应涵盖在本发明的保护范围之内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。