1.本发明涉及微生物领域,特别是涉及一株解木聚糖拟杆菌及其在制备酒精性肝病治疗或预防产品中的应用。
背景技术:
2.酒精性肝病(ald)已被确定为世界范围内最常见的肝病之一。根据世界卫生组织最新估计,2016年报告了3000000例与酒精相关的死亡,占全球疾病的5.1%。据报道,酒精可以抑制线粒体β-氧化,增加脂肪酸合成,并在肝脏中积累脂肪酸,从而导致脂质代谢稳态的紊乱。ald也是许多肝病的根本原因,包括酒精性脂肪性肝炎(ash)和肝细胞癌(hcc)。ash是ald的晚期,以慢性肝损伤、炎症和纤维化为特征,最终可发展为hcc。已知的药物如皮质类固醇和己酮可可碱(tnf-α抑制剂)通常用于治疗ash,但它们不能降低6个月患者的死亡率。因此,迫切需要寻找一种新的预防和/或治疗ald的可行方法。
3.2001年联合国粮农组织和世界卫生组织对益生菌的定义:益生菌是活的微生物,当摄入到足够多的数量时,对宿主产生健康益处。现在认为益生菌发挥健康益处主要有两个方面:第一,益生菌在肠道内可以和致病菌互作,来抵御致病菌对肠道黏膜的粘附,也会直接影响黏膜免疫。第二,益生菌的代谢产物也会对宿主产生影响,进而能够抑制病原菌的入侵,增加肠道的屏障功能,抑制炎症反应和调节免疫反应。最后益生菌能够达到维持和改善健康,以及降低某些疾病风险的作用。
4.近年来,肠道微生物群在代谢性疾病领域引起了越来越多的关注。肠道细菌的研究使我们认识到,肠道里边还有很多有益的细菌,这些有益的细菌也可以发展成益生菌,也可以发展成药物,即提出了活体生物药(live biotherapeutic,lbps)的概念。2016年fda和cber颁布了活体生物药的指南,将活体生物药定义为具有以下特征的一种生物活性产品:(1)含有活的生物体,如细菌。(2)用于预防、处理、治疗人类疾病或适应症。(3)不是疫苗,不能作为疫苗使用。首先lbps不同于传统的一代益生菌如乳杆菌和双歧杆菌,有160余年的应用历史,它没有应用历史,它是基于微生物纯培养、测序等技术发展而发现的对人体有潜在益处的新的微生物(包括转基因微生物)。除了应用历史,两者在应用场景上存在显著差异,一代益生菌常以奶制品食品或食品补充剂的形式出现,但lbps是以肠道菌群、肠屏障功能、免疫状态评估为基础,针对明确的临床适应症的应用。
5.解木聚糖拟杆菌(bacteroides xylanisolvens)是一种革兰氏阴性严格厌氧菌,对氧气极其敏感,只能在完全无氧的环境中生长良好。可代谢木聚糖等多糖,也可代谢半纤维素、木糖等小分子糖。解木聚糖拟杆菌是人体正常肠道菌之一,但丰度较低。解木聚糖拟杆菌的碳水化合物利用系统显著地优于其他拟杆菌种,能够在不同的碳源环境下高质量地存活。因此,解木聚糖拟杆菌所具有的免疫调节作用及强大的环境适应力正是微生物学家寻找的新一代益生元、益生菌所必备的特性之一。
技术实现要素:
6.本发明的目的是提供一株解木聚糖拟杆菌及其在制备酒精性肝病治疗或预防产品中的应用,以解决上述现有技术存在的问题,本发明提供的解木聚糖拟杆菌可以修复受损的肝脏组织,提高酒精肝肠道黏膜蛋白的表达,修复肠道屏障,从而来预防和治疗由酒精诱发的酒精性肝病。
7.为实现上述目的,本发明提供了如下方案:
8.本发明提供一株解木聚糖拟杆菌(bacteroides xylanisolvens)fcys01,保藏在中国典型培养物保藏中心,保藏编号为cctcc no:m 20211287,保藏日期为2021年10月18日,保藏地址为中国,武汉,武汉大学。
9.本发明还提供一种治疗或预防酒精性肝病的产品,所述产品的活性成分包括上述解木聚糖拟杆菌。
10.进一步地,所述产品为保健品或药品。
11.本发明还提供上述菌株在制备治疗或预防酒精性肝病产品中的应用。
12.进一步地,所述治疗或预防酒精性肝病产品的功能为(a1)至(a18)中的至少一项:
13.(a1)降低酒精肝患者血清中的谷丙转氨酶含量;
14.(a2)降低酒精肝患者血清中的谷草转氨酶含量;
15.(a3)降低酒精肝患者血清中的髓过氧化物酶含量;
16.(a4)降低酒精肝患者血清中的脂多糖含量;
17.(a5)降低酒精肝患者肝脏重量;
18.(a6)减少酒精肝患者肝脏肿大;
19.(a7)降低酒精肝患者肝脏中炎症因子白细胞介素1β含量;
20.(a8)升高酒精肝患者肝脏中抗炎症因子白细胞介素10含量;
21.(a9)降低酒精肝患者肝脏中炎症因子肿瘤坏死因子α含量;
22.(a10)降低酒精肝患者肝脏中炎症因子白细胞介素22含量;
23.(a11)降低酒精肝患者肝脏中甘油三脂含量;
24.(a12)降低酒精肝患者肝脏组织的空泡含量;
25.(a13)降低酒精肝患者肝脏组织的细胞浸润含量;
26.(a14)降低酒精肝患者肝脏脂肪含量;
27.(a15)恢复酒精肝患者肠道屏障;
28.(a16)升高酒精肝患者结肠上皮细胞中连接蛋白occludin蛋白含量;
29.(a17)升高酒精肝患者肠道有益菌丰度;
30.(a18)降低酒精肝患者肠道有害菌丰度。
31.本发明公开了以下技术效果:
32.本发明从健康男性人类的粪便内分离和筛选获得一株解木聚糖拟杆菌,该菌株通过降低血清中谷丙转氨酶、谷草转氨酶的表达,降低肝脏组织中促炎因子的表达,降低肝脏组织中甘油三酯的表达,减少脂质积累,降低肝脏中的炎症细胞浸润,修复受损的肝脏组织,提高肠道黏膜蛋白的表达,修复肠道屏障,从而来预防和治疗由酒精诱发的酒精性肝病,是一株在酒精性肝病预防和治疗领域具有潜在应用前景的益生菌新菌株。
附图说明
33.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
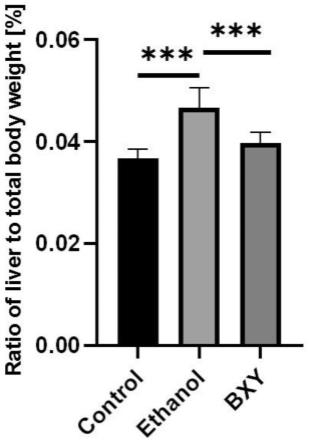
34.图1为小鼠的肝体比检测结果,其中control为空白组,ethanol为模型组,bxy为解木聚糖拟杆菌治疗组;
35.图2为小鼠肝脏组织he和油红o切片染色结果,其中control为空白组,ethanol为模型组,b.xylanisolvens为解木聚糖拟杆菌治疗组;
36.图3为小鼠结肠occludin蛋白检测结果,其中control为空白组,ethanol为模型组,b.xylanisolvens为解木聚糖拟杆菌治疗组;
37.图4为小鼠肠道内微生物门水平丰度检测结果,其中ctrl为空白组,etoh为模型组,bxy为解木聚糖拟杆菌治疗组;
38.图5为小鼠肠道内微生物属水平丰度检测结果,其中ctrl为空白组,etoh为模型组,bxy为解木聚糖拟杆菌治疗组。
具体实施方式
39.现详细说明本发明的多种示例性实施方式,该详细说明不应认为是对本发明的限制,而应理解为是对本发明的某些方面、特性和实施方案的更详细的描述。
40.应理解本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明。另外,对于本发明中的数值范围,应理解为还具体公开了该范围的上限和下限之间的每个中间值。在任何陈述值或陈述范围内的中间值以及任何其他陈述值或在所述范围内的中间值之间的每个较小的范围也包括在本发明内。这些较小范围的上限和下限可独立地包括或排除在范围内。
41.除非另有说明,否则本文使用的所有技术和科学术语具有本发明所述领域的常规技术人员通常理解的相同含义。虽然本发明仅描述了优选的方法和材料,但是在本发明的实施或测试中也可以使用与本文所述相似或等同的任何方法和材料。本说明书中提到的所有文献通过引用并入,用以公开和描述与所述文献相关的方法和/或材料。在与任何并入的文献冲突时,以本说明书的内容为准。
42.在不背离本发明的范围或精神的情况下,可对本发明说明书的具体实施方式做多种改进和变化,这对本领域技术人员而言是显而易见的。由本发明的说明书得到的其他实施方式对技术人员而言是显而易见得的。本发明说明书和实施例仅是示例性的。
43.关于本文中所使用的“包含”、“包括”、“具有”、“含有”等等,均为开放性的用语,即意指包含但不限于。
44.下述实施例中所用的试验材料,如无特殊说明,均为自常规生化试剂商店购买得到的。以下实施例中的定量试验,均设置三次重复实验,结果取平均值。
45.如无特殊说明,实施例中的pbs缓冲液均为ph7.0、0.1m的pbs缓冲液。
46.固体yhbhi培养基:37g/l脑心浸出液肉汤、5g/l酵母提取物、5mg/l血晶质、1g/l麦芽糖、1g/l纤维二糖和0.5g/l半胱氨酸,用双蒸水定容至1l,121℃,灭菌20min;液体yhbhi
培养基与固体yhbhi培养基的区别仅在于不加入琼脂。
47.固体m2gsc培养基:无菌瘤胃液30%(w/t),酪蛋白胨10g/l,酵母提取物2.5g/l,葡萄糖2g/l,纤维二糖2g/l,可溶性淀粉2g/l,半胱氨酸1g/l,碳酸氢钠4g/l,磷酸氢二钾0.45g/l,磷酸二氢钾0.45g/l,硫酸铵0.9g/l,氯化钠0.9g/l,七水合硫酸镁0.09g/l,氯化钙0.09g/l,刃天青1g/l,琼脂13g/l,用双蒸水定容至1l,ph调至6.6~6.8,115℃灭菌30min。液体m2gsc培养基与固体m2gsc培养基的区别仅在于不加入琼脂。
48.7-8周龄雄性spf级c57小鼠,体质量(20
±
2)g:华中农业大学动物中心,动物许可证号:hzaumo-2021-0007。
49.lieber-decarli基础对照液体饲料tp4030c(600ml40℃左右温水,218.80g主料,0.53g胆碱,2.50g维生素搅拌至均匀液体,定容至1000ml,混匀)和lieber-decarli酒精液体饲料tp4030d(600ml40℃左右温水,148g主料,0.53g胆碱,2.50g维生素搅拌至均匀液体,200ml40℃左右温水中加入50ml无水乙醇,定容至1000ml,混匀),灌胃用酒精溶液浓度为31.5%(v/v),灌胃用糊精溶液浓度为45%(w/v):南通特洛菲饲料科技有限公司。
50.采用南京建成谷丙转氨酶试剂盒(c009-2-1)检测血清中的谷丙转氨酶(alanine aminotransferase,alt/gpt)含量。采用南京建成谷草转氨酶试剂盒(c009-2-1)检测血清中的谷草转氨酶(aspartate aminotransferase,ast/gpt)含量。采用江苏酶免小鼠脂多糖酶联免疫试剂盒(mm-0634m1)检测血清中的脂多糖(lipopolysaccharide,lps)含量。采用南京建成总甘油三酯试剂盒(a110-1)检测肝脏中的总甘油三酯(triglyceride,tg)含量。采用江苏酶免小鼠白细胞介素-10酶联免疫试剂盒(mm-0176m1)检测肝脏中的白细胞介素-10(interleukin-10,il-10)含量。采用江苏酶免小鼠白细胞介素-1β酶联免疫试剂盒(mm-0040m1)检测肝脏中的白细胞介素-1β(interleukin-1β,il-1β)含量。采用江苏酶免小鼠白细胞介素-22酶联免疫试剂盒(mm-0892m1)检测肝脏中的白细胞介素-22(interleukin-22,il-22)含量。采用江苏酶免小鼠肿瘤坏死因子α酶联免疫试剂盒(mm-0132m1)检测肝脏中的肿瘤坏死因子α(tumornecrosis factor-α,tnf-α)含量。采用江苏酶免小鼠髓过氧化物酶酶联免疫试剂盒(mm-0338m1)检测肝脏中的小鼠髓过氧化物酶(myeloperoxidase,mpo)含量。
51.anti-occludin抗体(occludin抗体)、内参anti-beta actin(β-actin)、二抗goat anti-rabbit igg(hrp)为英国abcam公司。
52.实施例1菌株的分离、鉴定和保藏
53.一、菌株的分离
54.从湖北省武汉市华中农业大学进行样本取材,所取样本为健康人类男性新鲜粪便。
55.①
m2gsc培养基富集培养:将样品快速送入厌氧工作站进行稀释,稀释梯度为10-4
~10-6
,分别吸取每个梯度的稀释液200μl涂布固体m2gsc平板,每个梯度3个重复。涂布结束后,平板倒置在厌氧工作站37℃厌氧培养16h;
56.②
挑选m2gsc培养基平板上得到的菌落分别接种到yhbhi鉴定培养基中,37℃厌氧培养24h;
57.③
将培养的菌株接种至液体yhbhi培养基,然后加入20%甘油,-80℃冰箱保存。
58.二、菌株的鉴定
59.将分离得到的各个菌株进行形态鉴定、生理生化鉴定以及分子鉴定,其中菌株fcys01属于解木聚糖拟杆菌(bacteroides xylanisolvens)。
60.菌株fcys01的形态鉴定、生理生化鉴定结果:革兰氏阴性,菌体短杆状,两端钝圆,单个生长;具纤维素酶活性,发酵葡萄糖、木聚糖、木糖、半纤维素产酸。
61.菌株fcys01在液体yhbhi均匀浑浊生长,久置菌体呈白色沉淀。
62.菌株fcys01的最适生长温度为37~45℃,适宜ph为6.6~7.0。
63.菌株fcys01的16s rdna序列如seq id no.1所示:
64.seq id no.1:
65.tgcagtcgaggggcagcattttagtttgcttgcaaactaaagatggcgaccggcgcacgggtgagtaacacgtatccaacctgccgataactcggggatagcctttcgaaagaaagattaatatccgatagtatattaaaaccgcatggttttactattaaagaatttcggttatcgatggggatgcgttccattagtttgttggcggggtaacggcccaccaagactacgatggataggggttctgagaggaaggtcccccacattggaactgagacacggtccaaactcctacgggaggcagcagtgaggaatattggtcaatggacgagagtctgaaccagccaagtagcgtgaaggatgactgccctatgggttgtaaacttcttttatatgggaataaagtattccacgtgtgggattttgtatgtaccatatgaataaggatcggctaactccgtgccagcagccgcggtaatacggaggatccgagcgttatccggatttattgggtttaaagggagcgtaggtggattgttaagtcagttgtgaaagtttgcggctcaaccgtaaaattgcagttgaaactggcagtcttgagtacagtagaggtgggcggaattcgtggtgtagcggtgaaatgcttagatatcacgaagaactccgattgcgaaggcagctcactagactgcaactgacactgatgctcgaaagtgtgggtatcaaacaggattagataccctggtagtccacacagtaaacgatgaatactcgctgtttgcgatatacagtaagcggccaagcgaaagcattaagtattccacctggggagtacgccggcaacggtgaaactcaaaggaattgacgggggcccgcacaagcggaggaacatgtggtttaattcgatgatacgcgaggaaccttacccgggcttaaattgcatttgaataatctggaaacaggttagccgcaaggcaaatgtgaaggtgctgcatggttgtcgtcagctcgtgccgtgaggtgtcggcttaagtgccataacgagcgcaacccttatctttagttactaacaggttatgctgaggactctagagagactgccgtcgtaagatgtgaggaaggtggggatgacgtcaaatcagcacggcccttacgtccggggctacacacgtgttacaatggggggtacagaaggcagctacctggtgacaggatgctaatcccaaaaacctctctcagttcggatcgaagtctgcaacccgacttcgtgaagctggattcgctagtaatcgcgcatcagccatggcgcggtgaatacgttcccgggccttgtacacaccgcccgtcaagccatgaaagccgggggtacctgaagtacgtaaccgcaaggagcgtcc。
66.三、菌株的保藏
67.解木聚糖拟杆菌(bacteroides xylanisolvens)fcys01,已于2021年10月18日保藏于中国典型培养物保藏中心(简称cctcc,地址为:中国,武汉,武汉大学),保藏登记号为cctcc no:m 20211287。解木聚糖拟杆菌(bacteroides xylanisolvens)cctcc no:m 20211287,简称解木聚糖拟杆菌fcys01。
68.实施例2解木聚糖拟杆菌fcys01对治疗酒精性肝病小鼠的改善作用一、菌悬液的制备
69.菌悬液的制备方法:用pbs缓冲液悬浮供试菌,使菌浓度为1.0
×
109cfu/200μl。
70.供试菌为解木聚糖拟杆菌fcys01,得到的菌悬液命名为fcys01菌悬液。
71.二、分组处理方式
72.45只雄性c57小鼠,随机分成3组,每组15只,分组处理如下:
73.空白组:从试验开始至结束均采用lieber-decarli基础对照液体饲料饲喂;从试
验第8天开始至第15天,给予无菌pbs缓冲液(给予方式:灌胃,给予量:200μl/每只/每天);第16天,给予45%(w/v)糊精溶液(给予方式:灌胃,给予量:每只小鼠灌胃溶液的体积(μl)=体重(g)
×
20);
74.模型组:从试验开始至第4天采用lieber-decarli基础对照液体饲料饲喂,从第5天至结束均采用lieber-decarli酒精液体饲料饲喂;从试验第8天开始至第15天,给予无菌pbs缓冲液(给予方式:灌胃,给予量:200μl/每只/每天);第16天,给予31.5%(v/v)酒精溶液(给予方式:灌胃,给予量:每只小鼠灌胃溶液的体积(μl)=体重(g)
×
20);
75.解木聚糖拟杆菌fcys01组(简称fcys01组):从试验开始至第4天采用lieber-decarli基础对照液体饲料饲喂,从第5天至实验结束均采用lieber-decarli酒精液体饲料饲喂;从试验第8天开始至第15天,给予fcys01菌悬液(给予方式:灌胃,给予量:200μl/每只/每天);第16天,给予31.5%(v/v)酒精溶液(给予方式:灌胃,给予量:每只小鼠灌胃溶液的体积(μl)=体重(g)
×
20);
76.试验开始至结束为试验第1天至16天。
77.三、血清相关指标检测
78.实验第16天早上8点,实验组、模型组灌胃31.5%(v/v)酒精溶液,对照组灌胃45%(w/v)糊精溶液,灌胃9小时后从眼眶取血,血液4℃、3000r/min离心15min,收集血清。
79.检测血清中谷丙转氨酶(alt/gpt)、谷草转氨酶(ast/gpt)、脂多糖(lps)浓度,结果见表1。与空白组相比,模型组小鼠血清中alt、ast、lps水平均有显著升高,与模型组相比,fcys01组小鼠血清中alt、ast、lps水平显著降低,说明解木聚糖拟杆菌fcys01能明显改善酒精性肝病模型小鼠的血清中alt、ast、lps水平,预防肝病的发生。
80.表1
81.组别ast(u/g)alt(u/g)lps(ng/g)空白组0.17
±
0.050.11
±
0.021.42
±
0.32模型组0.33
±
0.1***0.55
±
0.28***2.68
±
0.46***fcys01组0.20
±
0.1##0.27
±
0.11##2.13
±
0.24##
82.注:与空白组相比,***p《0.001;与模型组相比,##p《0.01。
83.四、肝脏相关指标检测
84.实验第16天取完血清后,处死并解剖小鼠,收集肝脏。称取完整肝脏重量并记录计算小鼠的肝体比。
85.检测肝脏中总甘油三酯(tg)、白细胞介素1β(il-1β)、白细胞介素10(il-10)、白细胞介素22(il-22)、肿瘤坏死因子α(tnf-α)、髓过氧化物酶(mpo)的含量。
86.小鼠的肝体比检测结果见图1,control为空白组,ethanol为模型组,bxy为解木聚糖拟杆菌治疗组。与空白组相比,模型组小鼠的肝体比均有显著升高,与模型组相比,fcys01组小鼠的肝体比显著降低,说明解木聚糖拟杆菌fcys01能明显改善酒精性肝病模型小鼠的肝肿大,预防肝病的发生。
87.总甘油三酯(tg)、白细胞介素1β(il-1β)、白细胞介素10(il-10)、白细胞介素22(il-22)、肿瘤坏死因子α(tnf-α)、髓过氧化物酶(mpo)的检测结果见表2。与空白组相比,模型组小鼠的总甘油三酯(tg)、白细胞介素1β(il-1β)、白细胞介素22(il-22)、肿瘤坏死因子α(tnf-α)、髓过氧化物酶(mpo)均有显著升高,与模型组相比,fcys01组小鼠的肝体比总甘
油三酯(tg)、白细胞介素1β(il-1β)、白细胞介素22(il-22)、肿瘤坏死因子α(tnf-α)、髓过氧化物酶(mpo)显著降低。与空白组相比,模型组小鼠的白细胞介素10(il-10)显著降低,与模型组相比,fcys01组小鼠的白细胞介素10(il-10)显著升高。说明解木聚糖拟杆菌fcys01对酒精肝模型病理变化中il-1β、il-22、tnf-α等炎症因子产生抑制作用,对抗炎因子il-10有促进作用,对细胞因子tg有抑制作用,对细胞浸润因子髓过氧化物酶有抑制作用,从而抑制或减缓酒精性肝病的形成。
88.表2
[0089][0090]
注:与空白组相比,***p《0.001,**p《0.01,*p《0.05;与模型组相比,###p《0.001,##p《0.01,#p《0.05。
[0091]
五、组织形态学观察
[0092]
实验第16天取完血清后,处死并解剖小鼠,收集肝脏。将肝脏切片,进行苏木素-伊红(hematoxylin-eosin,he)染色和油红o(oil red o)染色,光学显微镜观察肝脏病变,400
×
显微照相。
[0093]
小鼠肝脏组织he和油红o切片染色结果见图2,其中control为空白组,ethanol为模型组,b.xylanisolvens为解木聚糖拟杆菌治疗组。空白组小鼠肝脏细胞形态正常,肝小叶结构完整,未见肝细胞变性、坏死或炎性细胞浸润,未见明显脂质沉积;模型组小鼠肝脏细胞变性,体积增大,胞浆内充满气球样的脂肪空泡,发生显著性的脂质沉积;fcys01组小鼠肝脏细胞形态趋于正常,与模型组相比脂质沉积明显改善。以上he和油红o切片染色结果提示,酒精饲料能够引起肝脏脂质累积,肝细胞变性,体积增大,胞浆出现脂肪空泡,产生炎性细胞浸润,最终导致酒精性肝病;解木聚糖拟杆菌fcys01可以减少脂肪空泡的形成,减少肝脏脂肪的沉积,缓解肝细胞变性,最终缓解小鼠酒精性肝病的进程。
[0094]
六、western blotting蛋白印记检测
[0095]
实验第16天取完血清后,处死并解剖小鼠,收集结肠,按照bca蛋白定量试剂盒说明书的方法提取总蛋白,采用western blot法检测结肠occludin蛋白的表达情况。
[0096]
western blot检测蛋白表达结果见图3,其中control为空白组,ethanol为模型组,b.xylanisolvens为解木聚糖拟杆菌治疗组。与空白组相比,模型组小鼠结肠中的occludin的表达量显著降低;与模型组相比,fcys01组小鼠结肠中的occludin的表达量显著升高,且与空白组中的表达量趋于一致。
[0097]
western blot检测结果表明:酒精饮食能够下调肠道连接蛋白occludin的表达;解木聚糖拟杆菌fcys01能够恢复酒精饮食引起的连接蛋白occludin的下调,说明解木聚糖拟杆菌fcys01可能通过修复肠道屏障,从而预防与治疗酒精引起的肝损伤。
[0098]
七、有益菌和有害菌丰度检测
[0099]
实验第16天取完血清后,处死并解剖小鼠,收集盲肠内容物,液氮速冻,dna提取及
高通量测序由北京诺禾致源生物信息科技有限公司进行。通过标准细菌16sv3-v4区域进行各组小鼠肠道内微生物多样性检测。
[0100]
16s微生物多样性检测结果见图4和图5。如图4所示,在门的水平上,与空白组相比,模型组小鼠盲肠内含物中的有益菌厚壁菌门(firmicutes)显著减少,有害菌变形菌门(proteobacteria)的含量显著升高;与模型组相比,实验组小鼠的盲肠内含物中的有益菌含量显著升高,恢复到和空白组相近的水平。
[0101]
如图5所示,在属的水平上,与空白组相比,模型组小鼠盲肠内容物中的有害菌escherichia-shigella的含量显著升高,有益菌akkermansia和lachnospiraceae的含量显著降低;与模型组相比,实验组小鼠盲肠内容物中的escherichia-shigella的含量显著降低,有益菌akkermansia和lachnospiraceae的含量显著升高,且与空白组中的表达量趋于一致。
[0102]
16s微生物多样性检测结果表明:酒精饮食能够上调肠道中有害菌的含量,下调有益菌的含量;解木聚糖拟杆菌fcys01能够恢复酒精饮食引起的有害菌含量的上调,有益菌的含量的下调,说明解木聚糖拟杆菌fcys01可能通过恢复肠道菌群,从而预防与治疗酒精引起的肝损伤。
[0103]
以上所述的实施例仅是对本发明的优选方式进行描述,并非对本发明的范围进行限定,在不脱离本发明设计精神的前提下,本领域普通技术人员对本发明的技术方案做出的各种变形和改进,均应落入本发明权利要求书确定的保护范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。