1.本发明属于医药领域,具体涉及一种新型抗肿瘤两性聚合物及其制备方法与应用。
背景技术:
2.肿瘤是一类严重危害人类生命健康的重大疾病之一。目前常规治疗肿瘤的方法有外科手术治疗、放射治疗、化学药物治疗和生物调节治疗等。其中,化疗作为全身性治疗手段,在恶性肿瘤治疗中具有手术、放疗不可替代的重要地位。近年来,新化疗药物的出现极大改善了肿瘤患者的预后,但化疗药物的毒性和肿瘤细胞对药物的耐药性正成为困扰化疗的两大难题。虽然报道的能够有效杀死肿瘤细胞的活性化合物很多,但大部分化合物仍存在溶解性差等问题;因此,研发一种能有效杀伤肿瘤细胞且毒性低、溶解度好的新型抗癌药物极为重要。
技术实现要素:
3.本发明的目的在于提供一种新型抗肿瘤两性聚合物,该两性聚合物抗肿瘤活性好,安全性高,溶解性好。
4.为实现上述目的,本发明采用如下技术方案:
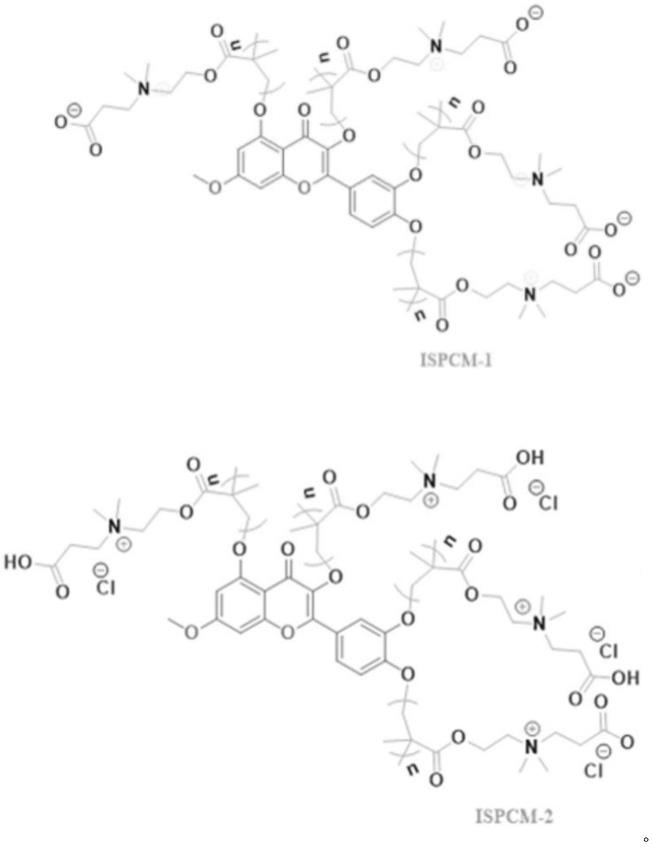
5.一种新型抗肿瘤两性聚合物,该两性聚合物为ispcm-1和ispcm-2,所述ispcm-1和ispcm-2的化学结构式如下:
6.[0007][0008]
本发明的另一目的在于提供一种新型抗肿瘤两性聚合物的制备方法,该方法包括以下步骤:
[0009]
步骤s1、将异鼠李素加入到反应器中,在反应器中加入etoh,搅拌使异鼠李素溶解在etoh中,加入氢氧化钾,在室温下搅拌;加入poly(carboxybetaine methacrylate),在室温下搅拌,反应过程中采用薄层色谱法监测反应过程,并在254nm和365nm的紫外灯下对反应结果进行分析,反应结束后,过滤,固体部分用乙醇反复洗涤,合并有机溶剂,浓缩,得化合物ispcm-1;
[0010]
步骤s2、将ispcm-1加入到反应器中,在反应器中加入etoh溶解,然后滴入1n的hcl调ph至4~6,得到ispcm-2。
[0011]
作为本发明的优选,步骤s1中poly(carboxybetaine methacrylate)的化学结构为:具体合成方法参照langmuir 2019,35,1846-1857公开的方法。
[0012]
作为本发明的进一步优选,异鼠李素加入量为1.0g,氢氧化钾加入量为0.7g,poly(carboxybetaine methacrylate)加入量2.5g。
[0013]
本发明提供的两性聚合物ispcm-1和ispcm-2在hct-116和hela中的活性分别为(53.27
±
1.17,68.51
±
4.55)和(55.11
±
5.87,67.62
±
6.28);因此,所述的两性聚合物ispcm-1和ispcm-2可以在制备抗肿瘤药物中的应用。
[0014]
作为本发明的优选,所述肿瘤包括结肠癌、宫颈癌。
[0015]
本发明提供的两性聚合物ispcm-1和ispcm-2在通过细胞成像实验以及细胞透射电镜观察发现,两性聚合物ispcm-1和ispcm-2具有显著的荧光特性,其与目标细胞具有很好的生物相容性,主要分布在细胞质、细胞核周围;因此,所述的两性聚合物ispcm-1和ispcm-2可以在制备用于特异性标记肿瘤细胞内的细胞质和细胞核的检测试剂和/或试剂
盒中的应用。
[0016]
本发明的优点和有益效果:
[0017]
(1)本技术提供的两性聚合物对肿瘤细胞的细胞质和细胞核具有靶向性,可直接进入肿瘤细胞的细胞质和细胞核内,其抗肿瘤活性好,与目标细胞具有很好的生物相容性,安全性高。
[0018]
(2)本技术提供的两性聚合物具有高分散和高聚集的特点,其溶解性好,可自发地组织或聚集为圆形或椭圆形结构,从而使药物进入到细胞系统中。
[0019]
(3)本技术提供的两性聚合物ispcm-1和ispcm-2具有明显的荧光特性,其与目标细胞具有很好的生物相容性,主要分布在细胞质、细胞核周围;该两性聚合物ispcm-1和ispcm-2可以在制备用于特异性标记肿瘤细胞内的细胞质和细胞核的检测试剂和/或试剂盒中的应用。
[0020]
(4)本技术提供的两性聚合物的制备方法简单,收率高。
附图说明
[0021]
图1是实施例1中ispcm-1的1h-nmr谱图;
[0022]
图2是实施例1中ispcm-1的红外谱图;
[0023]
图3实施例1的两性聚合物的紫外紫-可见光吸收光谱和荧光光谱;
[0024]
图4实施例1的两性聚合物的在ph=4、5和6下不同强酸下的荧光光谱;
[0025]
图5实施例1的ispcm系列两性聚合物的透射电镜图;
[0026]
图6不同细胞密度条件下实施例1的ispcm系列两性聚合物的成像图;
[0027]
图7实施例1的ispcm系列两性聚合物进入细胞内的透射电镜图。
具体实施方式
[0028]
下面结合附图和具体实施例来进一步说明本发明,但本发明的实施方式不限于此。对于未特别注明的工艺参数,可参照常规技术进行。除非特别说明,本发明采用的试剂、方法和设备为本技术领域常规试剂、方法和设备。
[0029]
实施例1新型抗肿瘤两性聚合物的制备
[0030]
一种新型抗肿瘤两性聚合物的制备方法,合成路线如下:
[0031][0032]
具体合成步骤为:
[0033]
步骤s1、化合物c的制备参照langmuir 2019,35,1846-1857公开的方法;
[0034]
步骤s2、将化合物d异鼠李素(1.0g,3.16mmol)加入到20ml圆底烧瓶中,在圆底烧瓶中加入etoh(5ml),搅拌使异鼠李素溶解在etoh中,加入氢氧化钾(0.7g,12.4mmol),在室温下搅拌30分钟;加入化合物c(2.5g),在室温下搅拌2h,反应过程中采用薄层色谱法(tlc)监测反应过程,并在254nm和365nm的紫外灯下对反应结果进行分析,反应结束后,过滤,固体部分用乙醇反复洗涤(2ml
×
3),合并有机溶剂,浓缩,得棕色凝胶(化合物ispcm-1),无需纯化,直接进行下一步,化合物ispcm-1的1h-nmr和红外谱图见图1和图2;
[0035]
步骤s3、将ispcm-1分别加入到五个5ml的圆底烧瓶中,在圆底烧瓶中加入etoh溶解,然后分别滴入hcl(1n)、h2so4(1n)、h3po4(1n)、ch3so3h(1n)和cf3so3h(1n)调ph至4~6,得到ispcm-2~6。
[0036]
本实施例采用bruker avanceii频谱分析仪(400mhz,meod)对化合物进行检测,通过1h-nmr记录产品的特性:化学位移以ppm表示,以四甲基硅烷(tms)作为内标,确定化合物ispcm-1~6的化学结构式如下:
[0037][0038]
实施例2紫外-可见光吸收光谱和荧光光谱分析
[0039]
本实施例为了观察新聚合物(实施例1提供的两性聚合物)的理化性质,在水中测定了该聚合物的紫外光谱和荧光光谱。如图3所示,在不同的浓度条件下,紫外吸收和荧光强度随着浓度的增加而增加,其作用范围为332~402nm。
[0040]
另外,本实施例为了考察所设计的两性聚合物在不同胃肠道酸性条件下的物理化学性质和光谱性质,观察其稳定性和浓度趋势的变化,本实施例在乙醇中制备样品的原液(5mm),稀释后在乙醇中制备适当浓度的溶液,然后选择不同的强酸(h2so4/hcl/h3po4/
ch3so3h/cf3so3h)来调节ph=4、5和6,观察两性酸离子聚合物在有机溶剂中的光谱性质,结果见图4。
[0041]
本实施例中荧光光谱采用岛津rf-5301pcs荧光光谱光度计进行光谱分析,荧光光谱记录波长为360~460nm,激发波长为400nm。
[0042]
从图4可以看出,对于硫酸,当ph=4时,发射强度随浓度的变化并不明显,而当ph=5和6时,发射强度为1.5倍,说明在这两种酸性条件下,发射强度随浓度的增加最为明显;在盐酸条件下,ph值为5和6时,发射强度增加2倍,比硫酸条件下增加0.5倍;磷酸和三氟甲基磺酸的荧光光谱呈现出相同的趋势变化,尽管ph=5时强度增加2倍,但ph=6时在强度250时变化几乎持平;在甲基磺酸的条件下,荧光光谱的变化非常显著,ph=4时的发射强度是其他酸性条件下的2到3倍,ph=5时的发射强度是其他酸性条件下的5到10倍;当ph=6时,发射强度有所下降,但仍是其他酸性的2.5倍左右。该结果可能是由于不同的离子容量和强酸的数量不同,导致两性聚合物的光谱特性不同。一般来说,不同强酸条件下的荧光光谱范围基本在400~405nm区域(见表1)。
[0043]
表-1不同ph条件下ispcm-2至ispcm-6的荧光光谱数据
[0044][0045]
实施例3 ispcm系列聚合物形态检测
[0046]
本实施例为了观察ispgm-1~6的形态,用zeiss ultra plus场发射扫描电子显微镜(电压15kev)逐一检测了ispgm-1~6的形态,具体方法为:将样品加入乙醇中,将悬浮沉淀加入硅片中,样品用导电胶粘在样品盘上,在1.0μm和5μm进行透射电镜成像,结果见图5。从图5可见,ispgm-1~6以水包油的形式牢固的封装起来,呈圆形或椭圆形均匀分布,证明本实施例提供的ispcm系列聚合物具有高分散和高聚集的特点,有利于药物动态自组装到细胞系统中,可大大提高药物的溶解性。另外,从图5可以看出,ispgm-1与ispgm-2~6的区别在于,ispgm-1主要是椭圆形,而ispgm-2~6几乎是圆形,这可能是由于不同酸离子的影响,使自组装的变化趋于规则的形状。
[0047]
实施例4体外细胞毒性活性的评价
[0048]
在生物活性方面,以isorhamnetin为阳性对照,采用mtt法测定了化合物ispcm1~6对人结肠癌细胞系(hct-116)、人宫颈癌细胞系(hela)和正常肝细胞系(l-02)的细胞毒性,具体方法为:将hct-116、hela和l02细胞置于含有10%胎牛血清和1%高糖的dmem培养基中,并在37℃、5%co2气氛中培养;将细胞培养基中的细胞以约每孔5.6
×
104个接种在96孔微孔板中(每孔的体积为100μl),将制备的化合物ispcm-1~6和对照isorhamnetin异鼠李素分别加入到孔中,使其最终浓度为0.2,0.4,0.8,1.0mg/ml,分别设置调零组和空白对照组,孵育24h后,加入10μl mtt溶液(1.0mg/ml),再孵育4h后,吸取培养液,加入100μldmso
溶解,在酶标仪上490nm处检测吸光度值(a)。
[0049]
细胞活性实验结果见表2,从表2可以看出,ispcm1和2的细胞毒性数据均与阳性对照相似,ispcm1和2的抗肿瘤活性略低于阳性对照,但差异不显著;对于ispcm3~6,几乎没有活性或超出有效评价的范围。
[0050]
表2为ispcm系列聚合物的活性数据
[0051][0052]a数据为三次重复实验的均值
±
sd。
[0053]
实施例5细胞成像实验
[0054]
本实施例在细胞成像中,测定了不同细胞密度条件下ispcm系列化合物的荧光形态。本实施例选择了不同的视野,并使用共聚焦显微镜测试了每种化合物(ispcm1~6)。结果在ispcm-1和2中均观察到显著的荧光特性,这表明ispcm-1和2与目标细胞具有很好的生物相容性,并产生明显的荧光特性,如图6所示。另外,从图6可以看出,细胞内产生的荧光主要分布在细胞质周围,很少分散在细胞核周围。证明本实施例提供的化合物对细胞质和细胞核有靶向性,尤其对于细胞质具有很好的靶向性。
[0055]
本实施例细胞成像实验的方法为:用胰蛋白酶处理处于对数生长阶段的hela细胞,将其接种于带有圆形帽的6孔板中,在37℃、5%co2气氛中培养24小时;用二甲亚砜制备聚合物储备溶液(10mg/ml),然后用二甲亚砜稀释到适当的浓度,每孔培养基中加入10μg/ml不同样品,处理24h后,丢弃培养基,用pbs洗涤2次,加入多聚甲醛固定溶液10min后,取出固定液,用pbs洗涤2次,dapi避光孵育10min。最后,丢弃染色液,再用pbs洗涤2次,用抗荧光猝灭剂处理后,在荧光显微镜下获得细胞的荧光图像。
[0056]
另外,本实施例为了进一步了解本技术提供的两性聚合物药物的细胞摄取情况,收集与该化合物孵育48h的hela细胞,并在透射电子显微镜下进行处理,以进行图像收集和分析。如图7所示,在细胞核(小箭头位置)和细胞器(小箭头位置)周围存在两性聚合物药物。与细胞成像结果相似,ispcm-1和2在体外对肿瘤细胞的抑制作用优于ispcm-3~6。这些结果表明,ispcm-1和2可作为新型抗肿瘤两性聚合物药物。此外,通过细胞透射电镜观察到,ispcm系列聚合物药物的溶解度有了很大的提高,这可以充分说明其与目标细胞的生物相容性。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。