1.本发明属于生物技术领域,涉及一种组合物及其在疾病检测中的用途,具体地涉及一种宫颈癌早期筛查检测试剂盒及其应用。
背景技术:
2.宫颈癌(cervical cancer)是女性最常见的生殖系统恶性肿瘤之一,在全球女性恶性肿瘤中居第二位,其发病率和死亡率仅次于乳腺癌,严重威胁女性身心健康。宫颈癌的发生几乎都是与高危型人乳头瘤病毒(hr-hpv)感染相关,发病年龄以40至50岁为最多,近年来发病有年轻化趋势。宫颈癌发生在子宫颈部位,多数为鳞癌,其次为腺癌、腺鳞癌,少见类型有小细胞癌、透明细胞癌等。宫颈癌早期一般没有任何症状,随着疾病的进展,才出现接触性出血、异常阴道流血等症状,需要主动筛查才会被发现。宫颈癌治疗效果与临床分期密切相关,早期癌宫颈癌通常有较好的预后,尽早发现宫颈癌可增加手术保留子宫的机会,提高总体生存率,早诊早治是提高治愈率的关键,同时宫颈癌有复发的可能性,因此预后监控亦要引起重视,如何尽早发现宫颈癌以及术后如何及时检测到宫颈癌的复发具有非常重要的临床意义。
3.目前宫颈癌的诊断技术有:1)宫颈刮片细胞学检查:易受到主观因素影响,有一定的假阴性率,容易漏诊;2)影像学技术:mri检查、b超检查、ct检查,但对较小的肿瘤不够灵敏,无法进行明确诊断;3)阴道镜检查:肉眼并不能观察出是否癌变,对有阴道狭窄、宫颈表面坏死、出血的患者亦不适用;4)宫颈活体组织检查:该方法属于有创性检查,操作较复杂,对需要长期跟踪观察的患者,会造成身体不适,且经济负担较重。因此有必要开发一种无创的可靠的新型宫颈癌标识物和检测技术,提高宫颈癌早癌检出率,改善宫颈癌治疗效果,降低宫颈癌死亡率。
4.随着分子生物学技术的发展,表观遗传学在近年来肿瘤研究上越来越受到重视,dna的甲基化、组蛋白修饰、染色质重塑以及非编码rna调控等表观遗传学改变都被认为与肿瘤的发生有着密切关系,其中dna的甲基化是最为常见的表观遗传学改变,其可调控细胞增殖、凋亡与分化,且水平与肿瘤的生物学特性密切相关。目前研究表明宫颈癌患者特定基因的dna甲基化改变(包括高甲基化和低甲基化)与已被证实的肿瘤特征有关,包括持续性增生信号的采集,抗细胞死亡,生长抑制的逃避,无限增生,炎症反应,能量代谢失调,诱导血管生成以及浸润激活。dna甲基化异常通常发生在癌症早期,并贯穿癌症的发生和发展过程,其甲基化状态一旦形成需要受到外界环境较长时间的持续刺激才会发生改变,因此dna甲基化指标的检测可以作为癌症诊断、早期筛查以及预后的重要生物指标。
5.针对dna甲基化检测方法大致可分为两类:全基因组甲基化分析和特异位点甲基化检测。全基因组甲基化分析检测成本较高,常作为一种高通量的筛选发现目标基因的手段;特异位点甲基化检测方法有联合亚硫酸氢钠的限制性内切酶分析法(cobra)、甲基化特异性pcr法(msp)、甲基化荧光定量法(methylight)、甲基化敏感性高分辨率熔解曲线分析法等,限制性内切酶分析法只能获得特殊酶切位点的甲基化情况,甲基化特异性pcr法基于
no.27所示的下游引物、如seq id no.28所示的荧光探针。
13.在本发明一实施例中,所述的宫颈癌基因甲基化检测的pcr引物探针组合,还包括括检测内参基因gapdh的pcr引物及探针,所述引物包括如seq id no.29所示的上游引物、如seq id no.30所示的下游引物,所述探针包括如seq id no.31所示的荧光探针。
14.在本发明一实施例中,所述荧光探针的5’端包含有荧光报告基团,包括fam、hex、ned、rox、tet、joe、tamra、cy3、cy5中的任意一种。
15.在本发明一实施例中,所述荧光探针的3’端包含有荧光淬灭基团,包括mgb、bhq-1、bhq-2、bhq-3中的任意一种。
16.在本发明一优选实施例中,所述荧光淬灭基团为mgb。
17.本发明第三方面提供宫颈癌早期筛查检测试剂盒,所述试剂盒包括如本发明第二方面所述的pcr引物探针组合,还包括阳性质控品以及阴性质控品。
18.在本发明一实施例中,所述阳性质控品为宫颈癌组织dna。
19.在本发明一实施例中,所述阴性质控品为白细胞dna。
20.在本发明一实施例中,所述宫颈癌早期筛查检测试剂盒反应体系的终浓度组成包括:0.1-1μm pcr引物、0.1-1μm探针。
21.在本发明一优选实施例中,所述宫颈癌早期筛查检测试剂盒反应体系的终浓度组成包括:0.1-0.5μm pcr引物、0.1-0.5μm探针。
22.在本发明一实施例中,所述宫颈癌早期筛查检测试剂盒的荧光定量pcr反应条件如下:
23.在本发明一实施例中,所述宫颈癌早期筛查检测试剂盒的荧光定量pcr反应条件如下:如下:
24.本发明第四方面提供宫颈癌基因甲基化检测的检测方法,包括以下步骤:
25.1)分离待测生物样品中目标基因的核酸;
26.2)将步骤1)所得核酸经亚硫酸氢盐转化处理,得到亚硫酸氢盐转化的dna(bis-dna);
27.3)采用甲基化荧光定量pcr技术检测步骤2)所得bis-dna的甲基化状态。
28.在本发明一实施例中,步骤1)所述生物样品包括组织、细胞中的一种。
29.在本发明一优选实施例中,步骤1)所述生物样品包括宫颈脱落细胞。
30.本发明第五方面提供如本发明第一方面所述的宫颈癌基因甲基化检测位点、如本发明第二方面所述的宫颈癌基因甲基化检测的pcr引物探针组合、如本发明第三方面所述的宫颈癌早期筛查检测试剂盒或如本发明第四方面所述的宫颈癌基因甲基化检测的检测方法在制备检测宫颈癌试剂盒中的应用。
31.本发明有益效果如下:
32.1)可作为宫颈癌的早期筛查、进程监测、预后评估的重要指标:本发明提供的宫颈癌早期筛查检测试剂盒以dna甲基化异常作为检测对象,dna甲基化异常通常发生在癌症早期,并贯穿癌症的发生和发展过程,其甲基化状态一旦形成需要受到外界环境较长时间的持续刺激才会发生改变,因此dna甲基化指标的检测可以作为宫颈癌的早期筛查、进程监测、预后评估的重要生物指标;
33.2)无创检测:本发明提供的宫颈癌早期筛查检测试剂盒可通过检测宫颈脱落细胞中宫颈癌相关基因甲基化状态来辅助诊断宫颈癌,实现无创检测;
34.3)单管多重基因甲基化检测:建立单管多重基因甲基化检测位点联检,减少试剂消耗,降低耗材成本,同时减少实验人员的操作步骤,减少劳动成本。
35.4)准确性高:本发明提供的宫颈癌早期筛查检测试剂盒通过多重数据分析筛选宫颈癌高甲基化候选基因,针对宫颈癌高甲基化候选基因上的多个甲基化检测位点设计特异性的基因甲基化检测引物和探针,覆盖10个以上甲基化cpg位点,采用多重pcr扩增技术扩增经亚硫酸氢盐修饰的待测dna样品,通过组合不同基因的甲基化情况进行联合检测或者通过检测单一基因的多个不同甲基化检测区域,同时为进一步提高检测灵敏度,本发明针对性地对单一基因的其中一个甲基化检测区域设计了两条上游引物或两条下游引物,通过多种途径提高试剂盒的灵敏度与特异性,实现宫颈癌早期筛查与诊断的准确检测。
附图说明
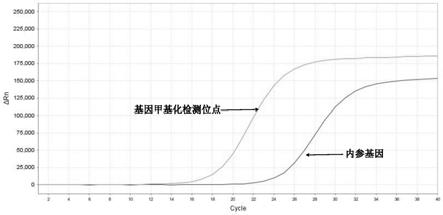
36.图1为本发明实施例提供的宫颈癌基因甲基化检测的典型检测结果阳性图,其中基因甲基化检测位点ct值≤25且小于内参基因ct值,判定检测结果为阳性;
37.图2为本发明实施例提供的宫颈癌基因甲基化检测的另一典型检测结果阳性图,其中基因甲基化检测位点ct值≤25且大于内参基因有扩增且ct值,
△
ct值≤5,判定结果为阳性;
38.图3为本发明实施例提供的宫颈癌基因甲基化检测的典型检测结果阴性图,其中基因甲基化检测位点ct值大于内参基因ct值且
△
ct值》5,判定结果为阴性。
具体实施方式
39.以下通过具体实施例对本发明进行详细描述,以使本领域技术人员能够容易地根据本说明书的公开内容实施本发明。以下所描述的实施例仅是本发明的一部分实施例,而
不是全部。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其它实施例,都属于本发明保护的范围。除非特别说明,本发明采用的试剂、方法和设备为本技术领域常规试剂、方法和设备,未注明具体条件的实验方法,通常按照常规条件,或制造厂商所建议条件实施。
40.本发明通过采用亚硫酸氢盐修饰法对待测宫颈癌核酸样品进行亚硫酸氢盐转化,结合荧光定量pcr技术,综合分析文献研究结果、tcga甲基化芯片数据库以及转录组测序表达谱,通过多重数据过滤分析,筛选宫颈癌高甲基化候选基因,并设计特异性的基因甲基化检测引物和探针,扩增经亚硫酸氢盐修饰的待测dna样品,根据pcr扩增结果来确定待测样品中目标基因的甲基化情况,实现宫颈癌的早期筛查与诊断。
41.本发明提供的宫颈癌早期筛查检测试剂盒的基因甲基化检测位点包括pax1、magi2、sox17中的一种或多种。
42.本发明提供的宫颈癌早期筛查检测试剂盒的pcr引物探针组合,包括以下1)-3)所示的核酸序列组合中的一种或多种:
43.1)pax1甲基化检测的pcr引物及探针,包括引物探针组合1、引物探针组合2、引物探针组合3中的一种或多种,其中所述引物探针组合1包括如seq id no.1所示的上游引物、如seq id no.2所示的下游引物、如seq id no.3所示的荧光探针,所述引物探针组合2包括如seq id no.4所示的上游引物、如seq id no.5与seq id no.6所示的下游引物、如seq id no.7所示的荧光探针,所述引物探针组合3包括如seq id no.8所示的上游引物、如seq id no.9所示的下游引物、如seq id no.10所示的荧光探针;
44.2)magi2甲基化检测的pcr引物及探针,包括引物探针组合4、引物探针组合5、引物探针组合6中的一种或多种,其中所述引物探针组合4包括如seq id no.11所示的上游引物、如seq id no.12所示的下游引物、如seq id no.13所示的荧光探针,所述引物探针组合5包括如seq id no.14所示的上游引物、如seq id no.15所示的下游引物、如seq id no.16所示的荧光探针,所述引物探针组合6包括如seq id no.17所示的上游引物、如seq id no.18所示的下游引物、如seq id no.19所示的荧光探针;
45.3)sox17甲基化检测的pcr引物及探针,包括引物探针组合7、引物探针组合8、引物探针组合9中的一种或多种,其中所述引物探针组合7包括如seq id no.20所示的上游引物、如seq id no.21所示的下游引物、如seq id no.22所示的荧光探针,所述引物探针组合8包括如seq id no.23所示的上游引物、如seq id no.24所示的下游引物、如seq id no.25所示的荧光探针,所述引物探针组合9包括如seq id no.26所示的上游引物、如seq id no.27所示的下游引物、如seq id no.28所示的荧光探针。
46.本发明提供的宫颈癌早期筛查检测试剂盒的pcr引物探针组合,还包括检测内参基因gapdh的pcr引物及探针,所述引物包括如seq id no.29所示的上游引物、如seq id no.30所示的下游引物,所述探针包括如seq id no.31所示的荧光探针。
47.优选地,所述荧光探针的5’端包含有荧光报告基团,包括fam、hex、ned、rox、tet、joe、tamra、cy3、cy5中的任意一种。
48.优选地,所述荧光探针的3’端包含有荧光淬灭基团,包括mgb、bhq-1、bhq-2、bhq-3中的任意一种。
49.进一步优选地,所述荧光淬灭基团为mgb。
50.本发明提供的宫颈癌早期筛查检测试剂盒检测样品包括组织、细胞中的一种。
51.本发明提供的宫颈癌早期筛查检测试剂盒检测结果判读包括:
52.1)阈值设定:可按仪器自动输出,也可根据仪器的使用说明手动调整基线,将阈值设定在荧光值对数图的线性部分,从软件中导出数据并读取ct值。
53.2)试剂盒有效性判定:
54.阴性质控品内参基因有扩增且ct值≤25,基因甲基化检测位点没扩增;阳性质控品内参基因与基因甲基化检测位点均有扩增且ct值≤25。
55.3)样品有效性判定:
56.a)内参基因有扩增且ct值≤25,则可继续分析;
57.b)内参基因ct值≥25或无扩增,但基因甲基化检测位点有扩增且ct值≤25,则可继续分析;
58.c)内参基因ct值》25或无扩增,基因甲基化检测位点无扩增或有扩增但ct值》25,则无法继续分析,需重复检测,若重复检测内参基因ct值》25或无扩增,则需要重新采样检测。
59.4)甲基化检测结果的判定(
△
ct值=基因甲基化检测位点ct值-内参基因ct值)
60.a)基因甲基化检测位点有扩增且ct值≤25,若基因甲基化检测位点ct值小于内参基因ct值或内参基因无扩增,判定结果为阳性;若基因甲基化检测位点ct值大于内参基因ct值,
△
ct值≤5,判定结果为阳性;
61.b)基因甲基化检测位点无扩增,或基因甲基化检测位点ct值大于内参基因ct值且
△
ct值》5,判定结果为阴性。
62.为更清楚展示本发明的技术方案,下面将结合具体实施例进一步阐述本发明。
63.实施例1:样品dna提取及亚硫酸氢盐转化
64.1、宫颈脱落细胞样本的处理及dna的提取
65.1)样品收集:
66.宫颈脱落细胞样品收集操作如下:医护人员先以窥阴器暴露宫颈,用棉拭子将宫颈口过多的分泌物擦去。将宫颈刷置于宫颈口,单方向旋转5圈以获得足量的上皮细胞样本,然后将宫颈刷头部放入装有细胞保存液的样本管中,沿刷柄折痕处将宫颈刷柄折断,将刷头留在样本管中,旋紧管盖,做好样本标识
67.2)dna提取:
68.通过使用安徽达健医学科技有限公司生产的核酸提取或纯化试剂(通用型)提取宫颈脱落细胞dna,具体步骤如下:
69.(a)将待测宫颈脱落细胞保存液样本4000rpm离心15min,用加样枪吸取废弃上清液,再加入500μl细胞保存液;
70.(b)取步骤a获得的细胞样本,每管加入500μl裂解液a,30μl蛋白酶k,70℃裂解40min;
71.(c)短暂离心,每管加入200μl异丙醇,充分混匀,短暂离心;
72.(d)将步骤c液体全部加入吸附柱中,全速离心30s;
73.(e)用600μl漂洗液i洗涤一次,全速离心30s;
74.(f)用600μl漂洗液ii漂洗一次,全速离心30s;
75.(g)再用600μl漂洗液ii漂洗一次,全速离心2min;
76.(h)离心柱在抽风柜内晾干3min,悬空加入70℃预热的洗脱液60μl,室温静置5min,13000rpm离心2min,收集dna到离心管中,-20℃保存。
77.2、亚硫酸氢盐转化:
78.通过使用安徽达健医学科技有限公司生产的核酸提取或纯化试剂(离心柱型)对步骤所得基因组dna进行亚硫酸氢盐转化,具步骤如下:
79.(a)取45μl待测dna样品于新的1.5ml离心管中并加入5μl转化缓冲液,置于金属浴37℃恒温孵育15min;
80.(b)孵育完成后,向每个样品中加入100μl预先制备的转化液,混匀并短暂离心,金属浴50℃避光孵育12~16小时;
81.(c)样品置于冰上(0~4℃)孵育10min;
82.(d)将吸附柱置于收集管中,向吸附柱中加入400μl结合液;
83.(e)将步骤c中的样品加入吸附柱中(含有结合液),盖紧管盖上下颠倒混匀数次,全速(14000rpm)离心30s,弃废液;
84.(f)向吸附柱中加入100μl漂洗液,全速离心30s,弃废液;
85.(g)向吸附柱中加入200μl脱磺液,室温(20℃~30℃)孵育20min,之后全速离心30s,弃废液;
86.(h)向吸附柱中加入200μl漂洗液,全速离心30s,重复加入200μl漂洗液,全速离心30s,弃废液及收集管;
87.(i)将吸附柱放入1.5ml无菌离心管中,向吸附膜的中间部位悬空滴加30μl洗脱液,洗脱转化dna,全速离心1min,收集bis-dna,-20℃保存。
88.实施例2:宫颈癌高甲基化候选基因及特异性引物、探针筛选
89.1、宫颈癌患者宫颈脱落细胞高甲基化候选基因的筛选
90.综合分析文献研究结果、tcga甲基化芯片数据库以及转录组测序表达谱,筛选具有显著差异的甲基化位点,通过多重数据过滤分析,最终筛选确定pax1、magi2、sox17为宫颈癌高甲基化候选基因。
91.2、宫颈癌甲基化检测的引物探针组合筛选
92.1)特异性引物、探针筛选:
93.根据上述pax1、magi2、sox17的核酸序列,在methyl primer express v1.0软件上进行甲基化引物和探针的设计,经申请人反复设计和推敲,筛选得到相关基因甲基化的pcr探针和引物,并将设计好的引物和探针送北京睿博兴科生物技术有限公司合成,具体序列见下表:
94.同时设置针对内参基因gapdh的特异性引物及探针,具体序列如下:名称序列(5’—3’)methy-gapdh-faagttaggttagtttggtagggaagtt(seq id no.29)methy-gapdh-raaccctaaaccacctcccc(seq id no.30)methy-gapdh-ptttgggtttttttgggggtaaggagatgt(seq id no.31)
95.其中上述探针序列的5’端修饰有荧光基团,选自fam、hex、ned、rox、tet、joe、tamra、cy3、cy5中的任一种,3’端标记有荧光淬灭基团,选自mgb、bhq-1、bhq-2、bhq-3中的
任一种。
96.实施例3:宫颈癌高甲基化候选基因的甲基化荧光定量pcr扩增检测
97.1、甲基化荧光定量pcr的反应体系如下:2
×
pcr反应预混液7.5μl,10μm的gapdh引物及探针各0.1μl,10μm上述引物探针组合中引物各0.5μl,探针各0.2μl,3μl bis-dna,补水至15μl。
98.2、甲基化荧光定量pcr的反应条件
99.3、甲基化荧光定量pcr的检测结果判读
100.1)阈值设定:可按仪器自动输出,也可根据仪器的使用说明手动调整基线,将阈值设定在荧光值对数图的线性部分,从软件中导出数据并读取ct值。
101.2)试剂盒有效性判定:
102.阴性质控品内参基因有扩增且ct值≤25,基因甲基化检测位点没扩增;阳性质控品内参基因与基因甲基化检测位点均有扩增且ct值≤25。
103.3)样品有效性判定:
104.a)内参基因有扩增且ct值≤25,则可继续分析;
105.b)内参基因ct值≥25或无扩增,但基因甲基化检测位点有扩增且ct值≤25,则可继续分析;
106.c)内参基因ct值》25或无扩增,基因甲基化检测位点无扩增或有扩增但ct值》25,则无法继续分析,需重复检测,若重复检测内参基因ct值》25或无扩增,则需要重新采样检测。
107.4)甲基化检测结果的判定(
△
ct值=基因甲基化检测位点ct值-内参基因ct值)
108.a)基因甲基化检测位点有扩增且ct值≤25,若基因甲基化检测位点ct值小于内参基因ct值或内参基因无扩增,判定结果为阳性;若基因甲基化检测位点ct值大于内参基因ct值,
△
ct值≤5,判定结果为阳性;
109.b)基因甲基化检测位点无扩增,或基因甲基化检测位点ct值大于内参基因ct值且
△
ct值》5,判定结果为阴性。
110.实施例4:临床样品检测验证试剂盒效果
111.1、宫颈脱落细胞样品检测
112.依据上述实施例1、2、3所述实验步骤对临床宫颈脱落细胞样品进行检测验证试剂盒效果,为验证宫颈癌基因甲基化检测的引物探针组合的检测效果,分别用上述实施例2中的引物探针组合对25例宫颈癌宫颈脱落细胞样品以及5例正常女性宫颈脱落细胞样品进行检测,其中编号1-25为宫颈癌宫颈脱落细胞样品,26-30为正常女性宫颈癌宫颈脱落细胞样
品,在阴性质控品、阳性质控品符合试剂盒有效性判定的情况下,典型的甲基化检测结果扩增图如图1、图2、图3所示,详细结果见下表,“ ”代表检测阳性,
“-”
代表检测阴性:代表检测阴性:
113.根据上述结果,统计分析如下:
114.从上述结果可得,本发明提供的宫颈癌早期筛查检测试剂盒中单重引物探针组合的检测灵敏度在72-88%之间,特异性在80-100%之间。
115.为进一步提高试剂盒的性能,通过对上述引物探针组合进行组合,期望以多重联检的方式提高试剂盒的检测效果,其中以下组合的检测灵敏度与特异性均在90%以上:检的方式提高试剂盒的检测效果,其中以下组合的检测灵敏度与特异性均在90%以上:
116.上述结果是基于宫颈癌单基因单检测位点的单管检测分析所得,此检测方式需要消耗较多的试剂同时增加实验人员的操作,实验成本较高,而单管多重基因甲基化检测位点联检可在较大程度减少试剂消耗,降低耗材成本,同时减少实验人员的操作,减少劳动成本。因此本发明建立单管多重基因甲基化检测位点联检进一步筛选宫颈癌早期筛查检测试剂盒的优选组合,以宫颈癌宫颈脱落细胞样品以及宫颈癌宫颈脱落细胞样品的dna样本为模板,测试单管多重基因甲基化检测位点联检的检测效果,结果如下:
117.结果显示部分单管多重基因甲基化检测位点联检的检测灵敏度与特异性出现一定幅度的下降,因此优选引物探针组合1、4、8,引物探针组合2、4、8,引物探针组合1、6、8以及引物探针组合2、6、8作进一步验证。
118.2、组织样品检测
119.通过用上述优选组合检测组织样品,检测其对组织样品的检测效果,结果如下:通过用上述优选组合检测组织样品,检测其对组织样品的检测效果,结果如下:
120.结果表明本发明提供的宫颈癌早期筛查检测试剂盒其检测灵敏度在93%-100%之间,特异性为100%,在检测宫颈癌组织样品基因甲基化时具备较高的检测灵敏度和检测特异性。
121.综上所述,本发明提供的宫颈癌早期筛查检测试剂盒有着较高的检测灵敏度和检测特异性,具备成为宫颈癌诊断、早期筛查的理想选择,助力宫颈癌的早诊早治。
122.上述说明示出并描述了发明的若干优选实施例,但如前所述,应当理解发明并非局限于本文所披露的形式,不应看作是对其他实施例的排除,而可用于各种其他组合、修改和环境,并能够在本文所述发明构想范围内,通过上述教导或相关领域的技术或知识进行改动。而本领域人员所进行的改动和变化不脱离发明的精神和范围,则都应在发明所附权利要求的保护范围内。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。