改进型as1411核酸适配体及利用其偶联的evs
技术领域
1.本技术属于肿瘤生物治疗技术领域,具体涉及一种改进型as1411核酸适配体及利用其偶联的evs专利申请。
背景技术:
2.核酸适配体是一段很短的单链dna或rna序列,通过在体内形成特定的三维空间结构进而与靶蛋白通过高亲和力结合来发挥一定生理功能。核酸适配体又被称为化学抗体,与常规的单克隆抗体相比,具有稳定性强、特异性强、亲和力强等特点。as1411是首个进入临床研究的as1411,能特异性的结合癌细胞表面的核仁蛋白,而核仁蛋白在多种癌细胞膜表面高表达,因此具有较好靶向作用。
3.细胞外囊泡(extracellular vesicles,evs)是一种尺寸在30~1000 nm之间的具有磷脂双分子层膜的球形小囊泡,普遍存在于各种细胞、细菌培养上清液和体液中。evs中包含有细胞来源的蛋白质、脂质、dna、mrna、mirna等,参与细胞的通讯、免疫调节等反应。当evs直径在30~150 nm时,可称之为外泌体(exosomes),而当evs直径在150~1000 nm时,可称之为微囊泡(microvesicles,mvs)。研究表明,细菌也会产生胞外囊泡。细菌分为革兰氏阳性细菌跟革兰氏阴性细菌两大类,革兰氏阳性细菌是单独的细胞壁结构,其胞外囊泡被称为evs;而革兰氏阴性细菌有两层膜,外膜跟内膜,研究发现,革兰氏阴性细菌的evs起源于外膜,因此也叫作(outer membrane vesicles,omvs)。
4.基于细胞外囊泡evs可以携带药物作用,现有技术中将其作为载体针对不同类型肿瘤细胞进行了较多研究。但由于细胞外囊泡evs缺乏一定靶向性,因此导致其实际应用效果较为有限。而结合核酸适配体的靶向性,如果能将其与细胞外囊泡evs进行结合,则可为提高细胞外囊泡evs的应用效果奠定一定技术基础。
技术实现要素:
5.基于现有as1411核酸适配体,本技术目的在于提供一种改进型的as1411核酸适配体,通过将其与evs的偶联,从而更好提高evs的靶向性,从而为相关疾病的治疗奠定一定技术基础。
6.本技术所采取的技术方案详述如下。
7.一种改进型as1411核酸适配体,其结构为:胆固醇-t碱基-as1411;所述t碱基为5~13个t碱基;所述as1411(28个碱基)核苷酸序列如seq id no.1所示,具体为:ttggtggtggtggttgtggtggtggtgg;也即,具体为:5t-as1411:胆固醇-ttttt-ttggtggtggtggttgtggtggtggtgg,6t-as1411:胆固醇-tttttt-ttggtggtggtggttgtggtggtggtgg,7t-as1411:胆固醇-ttttttt-ttggtggtggtggttgtggtggtggtgg,8t-as1411:胆固醇-tttttttt-ttggtggtggtggttgtggtggtggtgg,
9t-as1411:胆固醇-ttttttttt-ttggtggtggtggttgtggtggtggtgg,10t-as1411:胆固醇-tttttttttt-ttggtggtggtggttgtggtggtggtgg,11t-as1411:胆固醇-ttttttttttt-ttggtggtggtggttgtggtggtggtgg,12t-as1411:胆固醇-tttttttttttt-ttggtggtggtggttgtggtggtggtgg,13t-as1411:胆固醇-ttttttttttttt-ttggtggtggtggttgtggtggtggtgg。
8.利用所述改进型as1411核酸适配体偶联的evs,通过如下步骤制备获得:(一)提取evs备用按照现有技术,提取制备evs,所述evs为常规30~1000 nm的细胞外囊泡evs,或者为30~150 nm的外泌体exosomes,或者为omvs;以大肠杆菌omvs为例,具体提取制备方法如下:首先,将大肠杆菌菌液100000 g 离心30 min,弃沉淀,上清液再100000 g离心60 min;随后,用pbs溶液重悬沉淀物,再次100000 g离心60 min;最后,用pbs溶液重悬后,即为含有大肠杆菌外膜囊泡omvs溶液;所述大肠杆菌omvs,优选为携带有治疗用小分子(例如mir-126)的omvs;(二)孵育、偶联利用双蒸水调整改进型as1411核酸适配体浓度为10 μm,利用pbs调整omvs的浓度为100 μg/ml,然后按15 μl的核酸适配体,1 ml omv的比例,4℃振荡孵育过夜,即得到偶联有核酸适配体的大肠杆菌omvs;所述改进型as1411核酸适配体,优选采用5t-as1411、9t-as1411;利用所述改进型as1411核酸适配体偶联的evs在制备肿瘤药剂中的应用,通过改进型as1411核酸适配体靶向特定肿瘤细胞(例如乳腺癌细胞)后,利用evs所携带药物发挥抗肿瘤作用。
9.现有技术中,利用核酸适配体as1411靶向作用来改善携带装载药物的细胞外囊泡的靶向递送效果已进行了部分研究,并取得了一定肿瘤治疗效果。但现有技术中核酸适配体as1411在偶联细胞外囊泡时,主要采用“胆固醇-多肽-as1411”连接方式(也有使用生物素来替代多肽研究),但由于多肽及生物素类等物质的合成价格高昂,且操作较为复杂,以及靶向效率问题,因此发明人对于现有核酸适配体as1411做了进一步改进。总体上,本技术中通过对现有核酸适配体as1411的进一步改造、筛选,获得了可以与omvs进行较好偶联且具有较好靶向性的新的omvs,基于此,可为提高omvs的靶向性和提高其治疗应用效果奠定良好技术基础,也为其他类型囊泡的改进和应用提供了较好借鉴和参考。
附图说明
10.图1为纳米颗粒跟踪分析仪(nta)分析大肠杆菌omvs的粒径分布;图2 为投射电子显微镜(tem)观察大肠杆菌omvs的形态特征;图3 为改造后核酸适配体结构示意图以及与omvs偶联原理示意图;图4 为偶联后9t-as1411-omvs的粒径大小;图5为偶联后 9t-as1411-omvs的透射电镜;图6为流式细胞仪分析omvs与4t1细胞的结合效率;
图7为 激光共聚焦显微镜分析as1411-omvs与4t1细胞的结合效率;图8 为q-pcr分析孵育omvs、9t-s-as1411-omvs及9t-as1411-omvs 8小时后mda-mb-231细胞中mir-126的含量图9 为9t-as1411-omvs抑制细胞中靶蛋白的表达;图10为9t-as1411与现有as1411核酸适配体的比较图11为 动物水平分析9t-as1411-omvs-mir-126对肿瘤的抑制作用;其中上图为肿瘤生长曲线,中图为肿瘤大小,下图为肿瘤质量;图12为 免疫组化分析小鼠肿瘤组织中cxcr4的表达,其中上图为免疫组化染色结果,下图为免疫组化统计结果。
具体实施方式
11.下面结合附图和实施例对本技术做进一步的解释说明。在介绍具体实施例前,就下述实施例中所涉及部分生物材料、实验试剂、实验设备等部分实验背景简介如下。
12.生物材料:4t1细胞,中国科学院上海细胞库;balb/c小鼠(6周龄、雌性、spf级),购自北京维通利华有限公司,饲喂条件为:23~25℃,相对湿度55%~60%,每天照明时间维持在12小时(每天早晨8点照明,晚上八点关灯);胆固醇-13个t碱基-as1411:胆固醇-ttttttttttttt-ttggtggtggtggttgtggtggtggtgg),胆固醇-9个t碱基-as1411:胆固醇-ttttttttt-ttggtggtggtggttgtggtggtggtgg,胆固醇-9个t碱基-as1411 随机序列:胆固醇-ttttttttt-atcgatcgatcgatcgatcgatcgatcga,胆固醇-5个t碱基-as1411:胆固醇-ttttt-ttggtggtggtggttgtggtggtggtgg,均由苏州金唯智生物科技有限公司合成提供;实验试剂:氨苄青霉素、dna酶、胰蛋白酶、ager powder、bca蛋白浓度测定试剂盒、ripm-1640培养基,北京索莱宝公司产品;pvdf膜,美国immobilon公司产品;脱脂奶粉,北京鼎国公司产品;ripa裂解液、pmsf蛋白酶抑制剂,郑州贝贝生物公司产品;胎牛血清,美国gibco公司产品;dio细胞膜荧光探针,上海碧云天公司产品;兔β-actin单克隆抗体、山羊抗兔二抗,武汉三鹰生物技术有限公司产品;cxcr4抗体,英国abcam公司产品;实验设备:倒置荧光显微镜,日本奥林巴斯;透射电子显微镜,日本日立;
纳米颗粒跟踪分析仪,上海普迈;bd lsrfortessa流式细胞分析仪,美国bd;凝胶成像分析仪, 美国gene genius;荧光定量pcr仪,上海罗氏;多功能酶标仪,瑞士帝肯;部分实验溶液:as1411核酸适配体溶液:将装有适配体的ep管放置于离心机中,12000 rpm 离心1 min,根据适配体的浓度加入适量的双蒸水,配置成10 μm的水溶液,混匀后于4℃保存备用;dna酶(0.05 mg/ml):称取5 mg dna酶溶于100 ml pbs中,分装后-20℃保存备用;其他lb液体培养基、lb固体培养基、pbs(ph=7.4)、氨苄青霉素(100 mg/ml)、30%丙烯酰胺溶液、10% sds、10%过硫酸铵(10% ap)、1.5 m tris-hcl(ph=8.8)、0.5 m tris-hcl(ph=6.8)、10
×
蛋白电泳缓冲液(ph=8.3)、2
×
sds-page上样缓冲液、1
×
转膜液、1
×
pbst、蛋白封闭液(5
×
脱脂奶粉)、4%多聚甲醛固定液、1.5%戊巴比妥钠麻醉剂等参考现有技术常规配制即可。
13.实施例1在进一步介绍本技术具体技术方案前,本实施例中,发明人首先就本技术中所涉及的大肠杆菌外膜囊泡omvs(outer membrane vesicles)的提取方法简要介绍如下。
14.大肠杆菌外膜囊泡omvs的制备,具体采用如下操作提取获得:首先,将所保存的肠杆菌菌株划线接种于含有100 mg/ml氨苄青霉素的固体lb平板上,恒温培养箱里37℃倒置培养12 h;随后,挑取单克隆转接于含有100 mg/ml氨苄青霉素的5 ml 的lb液体培养基中, 37℃220 rpm震荡培养12 h;再吸取1 ml菌液转接于含有100 mg/ml氨苄青霉素的100 ml的lb液体培养基中,37℃、220 rpm震荡培养12 h;最后,取50 ml菌液,100000 g 离心30 min,弃沉淀,上清液再100000 g离心60 min;随后用10 ml的pbs溶液重悬沉淀物,再次100000 g离心60 min;最终用1 ml的pbs溶液重悬后,即为大肠杆菌外膜囊泡omvs溶液。
15.对所制备的大肠杆菌外膜囊泡omvs,采用纳米颗粒跟踪分析仪对其粒径进行分析,并采用透射电镜分析omvs的形态。结果如图1、图2所示。分析可以看出:所提取制备的大肠杆菌omvs的粒径主要分布在108.2 nm左右,同时其为具有双层膜的球形囊泡结构,结合这一形态特征和粒径大小,可以认定所提取获得的就是大肠杆菌omvs。
16.实施例2在实施例1所制备大肠杆菌omvs基础上,发明人进一步将胆固醇修饰的核酸适配体as1411(核酸适配体主要起靶向能力)与其进行了偶联,而为确定核酸适配体中的胆固醇与as1411之间碱基的长度对偶联omvs的靶向能力是否构成影响,发明人设计了三种碱基长度的as1411靶向系统:5个t的as1411(5t-as1411),9个t的as1411(9t-as141),13个t的as1411(13t-as1411),同时设计了一条9个t的随机序列as1411(9t-s-as1411)作为对照(随机序列的as1411不具有靶向能力),也即:5t-as1411:胆固醇-ttttt-ttggtggtggtggttgtggtggtggtgg,
9t-as141:胆固醇-ttttttttt-ttggtggtggtggttgtggtggtggtgg,9t-s-as1411:胆固醇-ttttttttt-atcgatcgatcgatcgatcgatcgatcga,13t-as1411:胆固醇-ttttttttttttt-ttggtggtggtggttgtggtggtggtgg),将上述核酸适配体与大肠杆菌omvs进行偶联制备as1411-omvs时,具体步骤如下:(1)利用双蒸水调整核酸适配体浓度为10 μm,然后将15 μl的10 μm的核酸适配体加入到1 ml浓度为100 μg/ml的大肠杆菌omvs溶液中,4℃振荡器上孵育过夜;(2)1000 rpm离心1 min,弃上清,使用dna酶进消化30 min后,再次1000 rpm离心1 min,弃上清,沉淀用pbs重悬后即为偶联有核酸适配体的大肠杆菌omvs,进一步地,通过分析as1411-omvs的膜电位,以验证核酸适配体与omvs是否成功偶联。
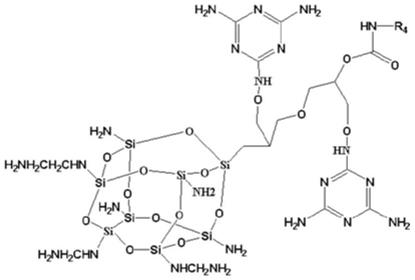
17.需要解释的是,这种偶联的技术原理为(如图3所示):核酸适配体as1411是一条单链dna,其本身带有负电荷;在将as1411与omvs孵育过夜时,as1411因其末端修饰的胆固醇的亲脂性从而可以与omvs进行偶联。
18.作为对照,发明人分别测量了未偶联as1411的omvs及偶联上as1411(以9t-as1411为例)的as1411-omvs的zeta电位;同时,将偶联上as1411的as1411-omvs使用dna酶消化处理后再次测量了其zeta电位。
19.另一方面,对偶联核酸适配体后的as1411-omvs,发明人对其粒径大小和形貌特征也进行了测定和分析。
20.zeta电位测定结果表明:未偶联的omvs膜电位为-9.61 mv,而偶联9t-as1411的omvs膜电位为-18.91 mv,在使用dna酶消化后,9t-as1411-omvs的膜电位又恢复到-9.26 mv。分析认为:由于9t-as1411内含有大量的脱氧核苷酸,本身带有负电荷,当9t-as141与omvs偶联后,会呈现出更低的膜电位,而在使用dna酶消化后,dna酶将omvs膜外偶联的9t-as1411消化掉,因此膜电位又得到恢复。也即,通过膜电位测定结果表明,本技术成功的将核酸适配体与omvs进行了偶联。
21.而利用纳米颗粒跟踪仪(nta)和透射电镜(tem)分别对偶和后的omvs(9t-as1411-omvs)的粒径测定和扫描图片结果分别如图4、图5所示。分析可以看出:9t-as1411-omvs的粒径大小在115.7 nm左右,其形态为典型的“球形”、“杯托状”结构,大小在110 nm左右。这一结果说明:偶联核酸适配体9t-as1411后,omvs的粒径和形态结构没有发生较大的变化,或者说核酸适配体 9t-as1411对omvs没有不良影响。
22.实施例3在实施例2所制备的偶联有核酸适配体as1411的omvs(5t-as1411-omvs、9t-as1411-omvs、9t-s-as1411-omvs、13t-as1411-omvs)基础上,基于细胞层面,以乳腺癌细胞(4t1细胞)为例,发明人对其靶向性进行了进一步实验,具体实验简介如下。
23.(一)利用流式细胞仪检测判定靶向能力已有研究认为,乳腺癌细胞膜表面的核仁素蛋白过量表达,因此发明人利用核酸适配体as1411对核仁蛋白高度亲和的特性,从而检测判定偶连有核酸适配体as1411的omvs(omvs作为治疗性载体应用)对乳腺癌细胞靶向能力,具体实验过程如下。
24.首先,将所保存的4t1细胞复苏培养后,进行扩增;具体而言:将4t1细胞复苏后,采用完全培养基、37℃恒温co2培养箱中培养1~2天,采用胰酶消化后,利用pbs进行离心清洗,最后利用pbs重悬细胞并调整计数。
25.随后,将4t1细胞以1
×
105/孔的量铺板6孔板;同时,对偶联核酸适配体as1411的omvs进行荧光标记,具体而言:取5 ml omvs于离心管中,加入50 μl细胞膜绿色荧光探针dio,37℃温育30 min,之后100000 g离心60 min,用5 ml的pbs溶液重悬沉淀物,再次100000 g离心60 min,弃去上清,使用1 ml 的pbs充分重悬,即得到荧光标记的omvs溶液(此过程应避光,以防止荧光染料淬灭);最后,分别将50 μg的5t-as1411-omvs-dio、 50 μg 的9t-as1411-omvs-dio、 50 μg 的9t-s-as1411-omvs-dio、 50 μg 的13t-as1411-omvs-dio加入到4t1细胞中,37℃孵育8 h,收集细胞于离心管中,进行流式分析。
26.偶联不同碱基长度核酸适配体后靶向能力测定结果如下表及图6所示。
27.偶联不同碱基长度核酸适配体后omvs的具体荧光值。
28.需要解释的是,具体测定分析时,使用flowjo7.6软件将细胞中的荧光强度换算成mean值,mean值的大小与细胞中的荧光强度成正比,mean值越高,代表细胞中的荧光强度越高;mean值越低,代表细胞中的荧光强度越低。
29.结合上表及图6结果,分析可以看出:(1)5t-as1411-omvs-dio、9t-as1411-omvs-dio、13t-as1411-omvs-dio组的细胞中均出现荧光,说明不论碱基长度大小,在偶联omvs后并不影响特定核酸适配体对4t1细胞的靶向作用,而且也表明omvs可以成功进入靶向4t1细胞内部;(2)未偶联核酸适配体的空白对照组omvs与偶联随机核苷酸序列的对照组(9t-s-as1411-omvs),其荧光强度相近,且均明显弱于实验组的荧光强度,这一结果说明虽然omvs可以成功进入靶向4t1细胞内部,但是由于没有靶向能力,进入靶向4t1细胞内部的omvs的量显然是小于实验组的;(3)就9t-as1411-omvs、5t-as1411-omvs、13t-as1411-omvs三个实验组别而言,其荧光强度值也有一定区别,而据此荧光强度也可以初步认定9t-as1411-omvs组的靶向效果最优,也因此,后续将主要对9t-as1411-omvs进行进一步研究。
30.(二)利用激光共聚焦显微镜观察偶联后omvs与4t1细胞结合的情况具体实验操作为:将4t1细胞以1
×
105孔的量铺板在激光共聚焦小皿中,随后分别将50 μg的 omvs-dio、50 μg 的9t-s-as1411-omvs-dio、50 μg 的9t-as1411-omvs-dio加入到4t1细胞中,37℃孵育8 h,利用激光共聚焦显微镜进行观察。
31.荧光照片结果如图7所示。分析可以看出:结果显示,omvs空白对照组和9t-s-as1411o-omvs对照组的细胞荧光强度相近,且都明显弱于9t-as1411-omvs实验组的细胞荧光强度,这进一步说明9t-as1411的靶向效果较好,能携带omvs更多、更快的进到4t1细胞中。
32.(三)利用q-pcr技术检测偶联后omvs在4t1细胞中的递送效率具体实验操作为:将4t1细胞以1
×
105/孔的量铺板6孔板,随后分别将50 μg的 omvs-mir-126、50 μg 的9t-s-as1411-omvs-mir-126、50 μg 的9t-as1411-omvs-mir-126加入到4t1细胞中,37℃孵育8 h,再使用rna提取试剂盒提取rna并进行加尾,然后进行反转录,最后进行荧光定量pcr检测分析。
33.需要解释的是,所述omvs
‑ꢀ
mir-126为内源性表达mir-126的omvs,其具体制备方法可参见《一种内源性高表达mirna的大肠杆菌胞外囊泡的制备方法》(专利申请号:cn201911054070.4)还需解释的是,荧光定量pcr分析时,采用的是mirna加尾法逆转录再qpcr,具体操作可参考如下。
34.(1)首先,提取omvs中的mirna并进行加尾,具体而言:收集大肠杆菌细胞并用pbs清洗,随后加入500 μl rl solution裂解细胞,之后加入40 μl 氯仿,充分混匀后12000 rpm 离心10 min;小心吸取上清200 μl于新的离心管中,加入400 μl 无水乙醇,充分混匀后转移至层析柱中,12000 rpm离心1 min,弃滤液;加入600 μl wash buffer后12000 rpm 离心1 min,弃滤液,重复此步骤一次;再在过滤柱膜中央加入40 μl 无rna酶水,静置2 min后12000 rpm 离心1 min即可得到mirna;参考如下反应体系将得到的mirna进行加尾:2
×
mirna rt solution mix,10 μl;mirna rt enzyme mix,2 μl;mirna,3 μl;rnase-free water,5 μl;混匀后,37℃恒温孵育30 min,即可得到加尾的mirna。
35.(2)随后,进行反转录:以步骤(1)中加尾后mirna作为模板,利用反转录引物126-r(aacatatgtgccgtggacggcgcatta)进行反转录,反应体系参考设计如下:rna,3 μl;引物,1 μl;dntp mix,1 μl;酶,2 μl;10
×
buffer,2 μl;rnase-free water,11 μl;反转录程序为:50℃、1 h,72℃、5 min;反转录产物4℃保存。
36.(3)最后,荧光定量pcr以步骤(2)反转录所得cdna作为模板,以16s rna为内参,进行荧光定量pcr;具体引物序列如下:f:ctcttgccatcggatgtgccca,
iiastiggifgssttqsgggg(上海淘普生物科技有限公司产品);所述nh2-as1411具体为:nh
2-ttggtggtggtggttgtggtggtggtgg(苏州金唯智生物科技公司产品)。
44.参考前述操作,将适配体与omvs偶联后,以50 μg的量加入到4t1细胞中,孵育8小时后,流式细胞仪检测分析。结果如图10所示。可以看出:本技术9t-as1411适配体组的荧光量是现有技术适配体组的2倍,这也说明,本技术所设计的核酸适配体在靶向效率方面是明显优于现有产品的。
45.实施例4在实施例3细胞实验基础上,发明人进一步构建了小鼠乳腺癌模型,同时利用9t-as1411-omvs-mir-126进行了动物实验,具体实验过程简介如下。
46.(一)构建balb/c小鼠乳腺癌模型将4t1细胞扩增培养后,调整浓度至4
×
107/ml,在小鼠的第四乳房垫附近注射100 ml细胞悬液进行荷瘤,一周左右小鼠即会成瘤,定期测量小鼠的肿瘤大小,进行记录并计算肿瘤体积。
47.(二)尾静脉给药待小鼠模型的肿瘤体积达到100-150 mm3(体积=0.5
×
长
×
宽
×
宽)时,进行分组(每组十只),分为:pbs组、9t-as1411-omvs-trna组(omvs-trna是构建omvs-mir-126时的支架,具体构建内容可参考现有技术《一种内源性高表达mirna的大肠杆菌胞外囊泡的制备方法》(专利申请号:cn201911054070.4》,在此是作为囊泡中没有载mirna的对照)、9t-as1411-omvs-mir-126组;先将omv的浓度调整为为500 μg/ml,每只小鼠取200 μl 进行尾静脉给药,pbs组使用等量的pbs进行尾静脉注射给药;每隔一天给药一次,共注射12次,24天给药完成之后,将小鼠麻醉脱颈处死,剥取小鼠肿瘤进行拍照并称重,同时对小鼠肿瘤组织进行免疫组化(ihc)分析(以检测特定cxcr4蛋白表达情况)。
48.小鼠肿瘤体积、大小及重量统计结果如图11所示。分析可以看出:实验组9t-as1411-omvs-mir-126组的小鼠肿瘤体积、大小及重量均明显小于对照组9t-as1411-omvs-trna组和空白对照组pbs组,这一结果说明9t-as1411-omvs-mir-126中的mir-126较好发挥了抗肿瘤效果。
49.免疫组化分析结果如图12所示(免疫组化过程中染色分析时,苏木素负染的细胞核呈现为蓝色,dab染色的阳性表达情况呈现棕黄色,以棕黄色为判断阳性的标准)。分析可以看出:实验组9t-as1411-omvs-mir-126中小鼠肿瘤组织中的cxcr4蛋白表达量明显降低。
50.综上实施例可以看出,本技术通过对核酸适配体的改进、筛选,确定了可以omvs偶联的最为高效的9t-as1411适配体,基于此适配体偶联的omvs具有较好靶向效率,在实际动物肿瘤治疗中也表现出较好应用效果,因此具有较好的科研推广和进一步开发应用价值。
再多了解一些
本文用于企业家、创业者技术爱好者查询,结果仅供参考。